3 - RISULTATI
3.1 - Profilo di binding di S33138 sui sottotipi recettoriali
dopaminergici D
2-like.
In una prima serie di esperimenti, l’interazione del composto S33138 sui recettori dopaminergici D2-like è stata vagliata in cellule CHO
stabilmente transfettate tramite binding competitivo con il composto antagonista [3H]spiperone (Fig. 13). In queste condizioni sperimentali, si dimostra che il S33138 è in grado di competere in ugual misura con i recettori D2Lh (isoforma lunga) e D2Sh (isoforma corta), se pur con
un’affinità di circa 25 volte più bassa rispetto a quella mostrata nei confronti del recettore D3h. Infine nei confronti dei recettori clonati D4h, il
composto S33138 presenta un’affinità così bassa da essere considerata trascurabile. Date queste osservazioni, non sono stati eseguiti ulteriori esperimenti su quest’ultimo sottotipo di recettore dopaminergico.
-10 -9 -8 -7 -6 -5 -4 -3 -25 0 25 50 75 100 D2Lh D2Sh D3h D4h B in d in g s p e c if ic o ( % ) log [S33138] (M)
Fig.13 - Isoterme competitive del binding dell’S33138 sui recettori D3h posti a confronto
In conclusione, come è facilmente osservabile in Tabella 1, i risultati di questi primi esperimenti dimostrano che il composto antipsicotico S33138 ha un’affinità prevalente per i recettori D3h e progressivamente sempre più bassa per i recettori D2h e D4h.
RECETTORE SPECIE TESSUTO RADIOLIGANDO (nM) pKi
D3 Umana Cellule CHO [3H]spiperone (0.5) 8.68±0.01
D2L Umana Cellule CHO [3H]spiperone (0.5) 7.13±0.03
D2S Umana Cellule CHO [3H]spiperone (0.5) 7.26±0.08
D4 Umana Cellule CHO [3H]spiperone (0.4) <5
Tab. 1 - Affinità dell’S33138 sui recettori dopaminergici D2-like
3.2 - Profilo di binding di S33138 e di altri agenti
antipsicotici sui recettori D
3h ,D
2Lh e D
2Sh.
In una serie successiva di esperimenti, l’affinità del S33138 è stata posta a confronto con quella di altri agenti antipsicotici sui recettori dopaminergici D3h, D2Lh e/o D2Sh, usando il [3H]spiperone come radioligando (Tabella 2). Gli antipsicotici che sono stati saggiati in questo studio sono: i neurolettici, aloperidolo, clorpromazina e pimozide; i derivati benzamidici, amisulpride, e raclopride; l’antipsicotico atipico, clozapina; gli antiosicotici di seconda generazione, olanzapina, quetiapina, risperidone, ziprasidone, sertindolo e zotepina, e gli agonisti parziali, aripiprazolo e bifeprunox .
I risultati dimostrano che, a differenza dell’S33138, nessuno degli altri agenti antipsicotici classici, così saggiati, dimostra di avere un’affinità così elevata per i recettori D3h rispetto a quella dimostrata nei confronti dei recettori D2Lh e/o D2Sh.
KI (nM)
FARMACO D3h D2Lh D2Sh
S33138 2.1±0.1 74.1±1.5 54.9±9.1 Aloperidolo 4.1±1.1 1.3±0.1 1.4±0.4
Clorpromazina 12.0±8.3 19.9±7.5 15.1±9.2 Pimozide 1.2±0.2 1.6±0.2 1.3±0.4 Amisulpride 4.9±1.3 10.5±0.3 5.7±0.5 Raclopride 2.9±0.6 5.8±0.7 2.8±0.8 Clozapina 562.3±16.5 177.8±4.0 166.0±13.4 Olanzapina 75.8±3.1 46.8±2.6 54.9±1.4 Quetiapina 1129±352 2511±117 1358±240 Risperidone 17.8±7.1 9.7±4.3 10.2±4.2 Ziprasidone 8.1±2.2 8.5±2.4 9.1±2.9 Sertindolo 7.6±2.3 2.1±0.7 ND Zotepina 17.6±3.0 33.20±11.4 14.4±5.8 Aripiprazolo 7.9±2.1 5.4±1.3 2.9±0.8 Bifeprunox 9.2±0.6 8.9±0.9 8.9±1.1
Tab. 2 - Interazione di S33138 sui recettori D3h, D2Lh e D2Sh in contrasto con altri
antipsicotici
3.3 - Proprietà antagoniste di S33138 sui recettori D
3h, D
2Lh
tramite saggio di binding con [
35S]-GTP S.
Numerosi studi (Newman-Tancredi,1999; Millan, 2000b, 2004a), hanno già dimostrato come la dopamina stimoli in modo dose-dipendente (approssimativamente due volte) il legame del [35S]-GTP S con i recettori D3h (DA, 1µM), D2Lh (DA, 10µM) e D2Sh (DA, 3µM), e che entrambe le interazioni possono essere bloccate dall’applicazione di aloperidolo con valori di pKB rispettivamente di 8.51±0.06 (D3h), di 9.49±0.16 (D2Lh) e di 8.90±0.16 (D2Sh) (Fig.14). -13 -12 -11 -10 -9 -8 -7 -6 -5 -4 -3 -25 0 25 50 75 100 D3h [ 3 5S ]-G T P γ S b in d in g (% d i D A , 1 µ M ) log [S33138] (M) + Dopamina [1 µM] log [S33138] (M)
A
-10 -9 -8 -7 -6 -5 -4 -3 0 25 50 75 100 D 2Lh [ 3 5 S ]-G T P γ S b in d in g (% D A , 1 0 µ M ) log [S33138] (M) + Dopamina [10 µM] log [S33138](M)
B
-12 -11 -10 -9 -8 -7 -6 -5 -4 -3 -25 0 25 50 75 100 D 2Sh [ 3 5 S ]-G T P γ S b in d in g (% d i D A , 3 µ M ) log [S33138] (M) + Dopamina [3µM] log [S33138] (M)C
Fig.14 - (A,B,C) Inibizione, concentrazione-dipendente, dell’S33138 sull’attività esercitatadalla dopamina sui recettori D3h, D2Lh, D2Sh.
Dalla Tabella 3 è facile evincere che il composto S33138 non modifica il legame con il [35S]-GTP S quando è usato da solo, mentre è in grado di sopprimere la stimolazione esercitata dalla dopamina sul legame del [35S]-GTP S verso i recettori D3h - con una pKB di 8.85±0.10. Questo
ultimo valore è in accordo con le affinità che il composto S33138 esercita sui recettori D3h (8.68). [3H]spiperone [35S]-GTP S ERK1/2 pKi pKB %MOI pKB %MOI D3h 8.68±0.01 8.85±0.10 97±3 9.08±0.02 104±4 [3H]spiperone [35S]-GTP S ERK1/2 pKi pKB %MOI pKB %MOI D2Lh 7.13±0.03 7.82±0.03 104±8 8.03±0.02 101±2
Tab.3 - Proprietà antagoniste del S33138 determinate dal blocco del binding stimolato dalla dopamina e dalla fosforilazione extracellulare regolata da chinasi. (MOI) inibizione
massimale osservata
Si può inoltre osservare che la curva che esprime il binding di [35 S]-GTP S sui recettori D3h ottenuta per dosi progressivamente crescenti di dopamina, risulta traslata parallelamente verso destra in presenza di concentrazioni crescenti di S33138 (3-100 nM), senza perdita dell’effetto massimale (Fig. 15). -11 -10 -9 -8 -7 -6 -5 -4 -3 -25 0 25 50 75 100 [ 3 5S ]-G T P γ S b in d in g (% d i D A , 1 µ M ) log [Dopamina] (M) S33138 0 nM 3 nM 10 nM 30 nM 100 nM
Fig.15 - Spostamento verso destra delle curve concentrazione-risposta della dopamina
sui recettori D3h in presenza di concentrazioni crescenti dell’S33138
[3H]spiperone [35S]-GTP S
pKi pKB %MOI
D2Sh
Computando gli stessi dati secondo il plot di Schild (Fig.16), è possibile dimostrare che l’S33138 è un antagonista nei confronti dei recettori D3h in quanto l’inclinazione della retta così ottenuta è prossima all’unità, essendo pari a 1.18, (r = 0.88) con un valore di pA2 (8.69) molto vicino ai suoi valori di pKB e pKi.
-9 -8 -7 0 1 2 3 lo g ( d o s e -1 ) log [S33138] (M) Plot di Schild pA 2=8.69
Fig.16 - Trasformazione di Schild dei dati ottenuti nella figura precedente
Queste osservazioni dimostrano che il composto S33138 si comporta come un antagonista competitivo e reversibile sui recettori D3h, inibendo il binding di [35S]-GTP S indotto da dopamina. Inoltre si comporta da antagonista sui recettori D2Lh e D2Sh, anche se in misura minore rispetto al D3h, come è indicato dai valori di pKB di 7.82±0.03 e 7.79±0.06 rispettivamente per questi recettori (vedi Figg. 14 B e C).
3.4 - Proprietà antagoniste di S33138 sui recettori D
3h e
D
2Lh: rilevazione della fosforilazione di MAP chinasi
tramite Western Blotting
Cussac (et al., 1999) e Millan (et al., 2004a) hanno recentemente dimostrato che la dopamina, attivando i recettori D3h o D2Lh trasfettati stabilmente in nelle cellule CHO, innesca una marcata fosforilazione, anche se transiente, di ERK1/2 (MAP-chinasi). A differenza della dopamina, il composto S33138, in quanto antagonista, non è in grado di
determinare un aumento della fosforilazione di ERK. Infatti, questo composto blocca in modo concentrazione-dipendente l’induzione esercitata dai recettori D3h con un valore di pKB di 9.08±0.02 su ERK 1/2 (Fig. 17-18).
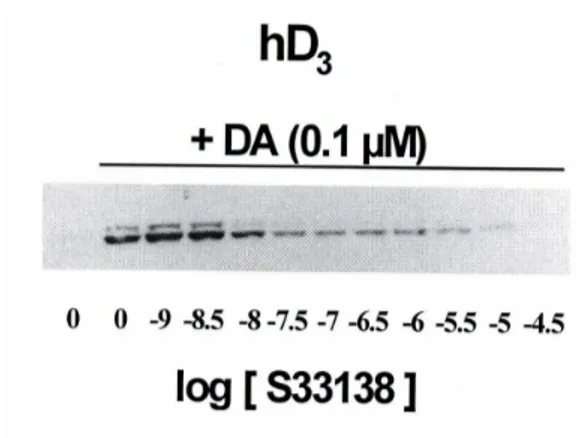
Fig. 17 - Proprietà antagoniste dell’S33138 sui recettori D3h verso la DA
-11 -10 -9 -8 -7 -6 -5 -4 -25 0 25 50 75 100 F o s fo ri la z io n e E R K 1 /2 (% d i D A , 0 ,1 µ M ) log [S33138] (M) + Dopamina [0,1 µM] log [S33138] (M)
Fig.18 - Proprietà antagoniste dell’S33138 sui recettori D3h valutate in modo
concentrazione-dipendente
SI può osservare inoltre che il composto S33138 è anche in grado di inibire la fosforilazione ERK 1/2 a seguito dell’induzione di dopamina sui recettori D2Lh con un pKB di 8.03±0.02, evidenziando così le sue proprietà antagoniste verso questi stessi siti recettoriali (Fig. 19-20).
Fig. 19 - Proprietà antagoniste dell’S33138 sui recettori D2Lh verso la DA -10 -9 -8 -7 -6 -5 -4 -25 0 25 50 75 100 F o s fo ri la z io n e E R K 1 /2 (% d i D A , 0 .1 µ M ) log [S33138] (M) + Dopamina [0,1 mM] log [S33138] (M)
Fig.20 - Proprietà antagoniste dell’S33138 sui recettori D2Lh valutate in modo
3.5 - Proprietà antagoniste di S33138 sui recettori D
3h e
D
2Lh, sui recettori co-transfettati D
3h e D
2Lh, e sui
recettori D
3i3(D2): studi enzimatici dell’attività dello
adenilato ciclasi
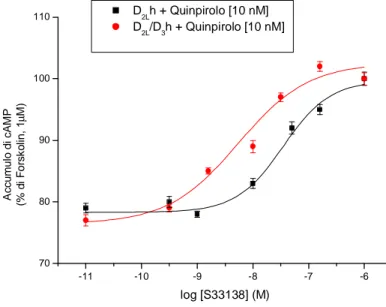
E’ noto che la somministrazione di forskolin, essendo un agonista diretto dell’adenilato ciclasi, determina un marcato aumento dell’accumulo intracellulare di cAMP in cellule COS-7 transfettate transientemente con un’adenilato ciclasi chimerica (AC-V/VI) e con i recettori D2Lh o D3h/D2Lh. D’altra parte, la contemporanea somministrazione di quinpirolo, agendo come agonista dopaminergico nei confronti dei recettori D2-like, provoca una riduzione nell’accumulo di cAMP. Partendo da una condizione di base definita dalle concentrazioni fisse di quest’ultimi composti, si può osservare che l’aggiunta di concentrazioni crescenti dell’antagonista S33138 determina un accumulo intracellulare di cAMP. Ciò è determinato dalla riduzione dell’influenza inibitoria del quinpirolo sia in cellule esprimenti i recettori D2Lh (pKB 7.57± 0.12) che più marcatamente in cellule co-transfettate con recettori D3h e D2Lh (pKB 8.69±0.14) (Fig 21).
-11 -10 -9 -8 -7 -6 70 80 90 100 110 A c c u m u lo d i c A M P (% d i F o rs k o lin , 1 µ M ) log [S33138] (M) D 2Lh + Quinpirolo [10 nM] D2L/D3h + Quinpirolo [10 nM]
Fig. 21 - Blocco dell’S33138 in modo concentrazione-dipendente dell’influenza inibitoria dell’agonista Quinpirolo nella formazione di cAMP stimolato da forskolin
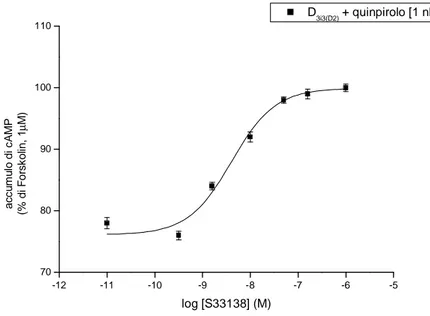
Il quinpirolo (EC50, 1.01 nM) riduce la formazione di cAMP anche in cellule COS-7 transfettate con AC-V/VI e con recettori chimerici D3i3(D2)h. Questi ultimi sono caratterizzati dalla sostituzione di una sequenza di 12 aminoacidi del terzo loop intracellulare con la corrispondente sequenza del recettore D2Lh per aumentarne l’affinità verso AC-V/VI. L’azione del quinpirolo è bloccata da S33138 con un valore di pKB di 8.71±0.16 (Fig. 22). -12 -11 -10 -9 -8 -7 -6 -5 70 80 90 100 110 a c c u m u lo d i c A M P (% d i F o rs k o lin , 1 µ M ) log [S33138] (M) D3i3(D2) + quinpirolo [1 nM]
Fig. 22 - Blocco dell’S33138 in modo concentrazione-dipendente dell’influenza inibitoria dell’agonista Quinpirolo nella formazione di cAMP stimolato da forskolin
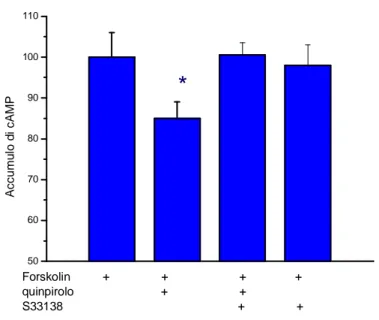
Contrariamente a quanto previsto dalla AC-V/VI, l’isoforma AC-V è sensibile ai recettori D3h, sebbene gli effetti degli agonisti siano meno marcati rispetto a quelli esercitati sui recettori D2Lh (Robinson e Caron, 1997; Maggio et al. 2003). Si osserva infatti che quinpirolo riduce in modo significativo l’influenza della forskolin sull’accumulo di cAMP in cellule co-transfettate con i recettori D3h e AC-V. L’effetto esercitato dal quinpirolo sull’accumulo intracellulare di cAMP è soppresso dalla simultanea somministrazione di S33138. Al contrario, nelle stesse condizioni di cultura, l’impiego di solo S33138 risulta del tutto inattivo nei confronti della attività basale della forskolin (Fig.23).
Fig. 23 - Blocco con una concentrazione fissa dell’S33138 dell’influenza inibitoria del quinpirolo sull’accumulo di cAMP stimolato da forskolin
50 60 70 80 90 100 110 Forskolin + + + + quinpirolo + + S33138 + + A c c u m u lo d i c A M P
![Fig. 19 - Proprietà antagoniste dell’S33138 sui recettori D 2L h verso la DA -10 -9 -8 -7 -6 -5 -4-250255075100Fosforilazione ERK 1/2(% di DA, 0.1µM) log [S33138] (M) + Dopamina [0,1 mM] log [S33138] (M)](https://thumb-eu.123doks.com/thumbv2/123dokorg/7307668.87957/8.892.318.614.159.380/fig-proprietà-antagoniste-recettori-verso-fosforilazione-erk-dopamina.webp)