Capitolo 4: Risultati e discussione
In questo capitolo verranno analizzati i risultati delle prove sperimentali descritte nel capitolo 3.
L’analisi del capitolo in esame è strutturata come segue: 1. swelling e perdita di peso;
2. stress-strain; 3. creep-relaxation;
4. deposizione con siringa attivata dalla pressione (PAM).
Di seguito si riporta la nomenclatura dei materiali utilizzati nella parte sperimentale.
Materiali utilizzati
Sigla Nomenclatura
G Gelatina non trattata
G_r.t. Gelatina reticolata termicamente
G/0.5GP_s Gelatina reticolata chimicamente con lo 0.5% (w/w) di genipina direttamente nella soluzione al 10% di gelatina in acqua
G/0.5GP_PBS Gelatina reticolata chimicamente con lo 0.5% (w/w) di genipina in PBS per 24 ore
CS_r.t. Chitosano reticolato termicamente
CS/0.5GP_s Chitosano reticolata chimicamente con lo 0.5% (w/w) di genipina direttamente nella soluzione all’1% di chitosano in acqua e acido acetico CS/G 40/60_r.t. Miscela di chitosano e gelatina di composizione in peso 40/60 reticolata
termicamente
CS/G 40/60_0.5GP_s Miscela di chitosano e gelatina di composizione in peso 40/60 reticolata chimicamente nella soluzione di preparazione della miscela con lo 0.5% (w/w) di genipina
CS/G 40/60_3GP_PBS Miscela di chitosano e gelatina di composizione in peso 40/60 reticolata chimicamente in PBS con il 3% (w/w) di genipina
CS/G 60/40_r.t. Miscela di chitosano e gelatina di composizione in peso 60/40 reticolata termicamente
CS/G 60/40_0.5GP_s Miscela di chitosano e gelatina di composizione in peso 60/40 reticolata chimicamente nella soluzione di preparazione della miscela con lo 0.5% (w/w) di genipina
CS/G 20/80_r.t. Miscela di chitosano e gelatina di composizione in peso 20/80 reticolata termicamente
CS/G 20/80_0.5GP_s Miscela di chitosano e gelatina di composizione in peso 20/80 reticolata chimicamente nella soluzione di preparazione della miscela con lo 0.5% (w/w) di genipina
PU Poliuretano GP Genipina
1. Swelling e perdita di peso
1.1 Miscele di chitosano e gelatina reticolate termicamente.
In Fig. 4.1 è mostrato il grafico della % SW in funzione del tempo per le miscele CS/G reticolate termicamente. 0 100 200 300 400 500 600 700 800 900 1 3 6 24 48 t (h) %SW CS/G 60/40_r.t. CS/G 40/60_r.t. CS/G 20/80_r.t. G_r.t.
Fig. 4.1 Andamento della percentuale di swelling in funzione del tempo delle miscele a base di chitosano e gelatina reticolati termicamente
I film di chitosano e gelatina presentano un elevato swelling iniziale che è più alto quanto più alta è la concentrazione di gelatina.
Le miscele di chitosano e gelatina inizialmente mostrano un andamento di swelling decrescente mentre per la miscela CS/G 40/60 tale andamento si manifesta per tempi maggiori alle 6 ore. Questo è dovuto alla presenza di gelatina che in contatto con l’acqua inizialmente rigonfia e con il passare del tempo tende a sciogliersi completamente.
In Fig. 4.2. è riportato l’ andamento della perdita di peso in funzione del tempo delle miscele CS/G reticolate termicamente
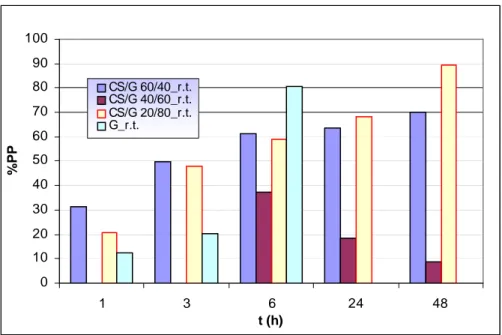
0 10 20 30 40 50 60 70 80 90 100 1 3 6 24 48 t (h) %PP CS/G 60/40_r.t. CS/G 40/60_r.t. CS/G 20/80_r.t. G_r.t.
Fig. 4.2 Andamento della percentuale di perdita di peso in funzione del tempo delle miscele a base di chitosano e gelatina reticolati termicamente
Per tutte le miscele, tranne che per la miscela CS/G 40/60, si nota che la percentuale di perdita di peso ha un andamento crescente con il tempo e si può notare che i valori di dissoluzione sono molto elevati. Per la miscela CS/G 40/60 non si ha dissoluzione prima delle 6 ore e si osserva che l’andamento della perdita di peso in funzione del tempo di tale miscela è decrescente.
Per la gelatina pura il massimo di dissoluzione rilevabile si ha dopo 6 ore di prova in quanto fino alle 48 ore si ha completa dissoluzione di questa.
1.2 Materiali reticolati chimicamente con genipina
I risultati presenti in questo paragrafo forniscono indicazioni sulla diversa efficacia dei metodi di reticolazione chimica, quella effettuata direttamente nella soluzione di preparazione delle miscele e quella in PBS, come descritto nel paragrafo 1.3 di questo capitolo.
In Fig. 4.3 è riportato l’andamento della percentuale di swelling (% SW) in funzione del tempo, dei materiali a base di gelatina.
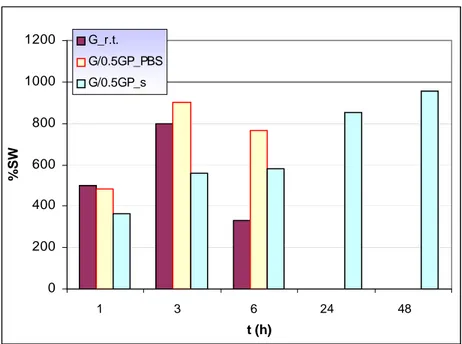
0 200 400 600 800 1000 1200 1 3 6 24 48 t (h) %SW G_r.t. G/0.5GP_PBS G/0.5GP_s
Fig. 4.3 Andamento della percentuale di swelling in funzione del tempo delle miscele a base di gelatina
In Fig. 4.4 è mostrato l’andamento della dissoluzione dei materiali a base di gelatina.
0 10 20 30 40 50 60 70 80 90 1 3 6 24 48 t (h) %P P G_r.t. G/0.5GP_PBS G/0.5GP_s
Fig. 4.4 Andamento della percentuale di perdita di peso in funzione del tempo delle miscele a base di gelatina
Dall’analisi dei due grafici si evince che:
1. per quanto riguarda lo swelling, la gelatina reticolata termicamente tende a rigonfiare rapidamente giungendo a valori di swelling di circa l’ 800%, dissolvendosi completamente dopo le 6 ore, ciò è confermato anche dal grafico della perdita di peso, che mostra una perdita di peso rapidissima giungendo all’ 80% in 6 ore.
2. La gelatina reticolata chimicamente in PBS mostra un andamento dello swelling simile a quello della gelatina reticolata termicamente, infatti si ha un rapido rigonfiamento con valori di percentuale di swelling vicino al 900% e la sua dissoluzione è molto elevata, con valori superiori all’80% , dopo 6 ore di esperimento.
3. La gelatina reticolata chimicamente in soluzione mostra un andamento dello swelling crescente. Per quanto riguarda la perdita di peso della gelatina reticolata chimicamente in soluzione, quest’ultima cresce nelle prime ore e poi raggiunge un valore costante pari circa al 15% del peso originario. Tali fatti indicano che la reticolazione chimica in soluzione rende il film di gelatina più stabile, ed è utile nel caso di utilizzo come substrati di coltura cellulare dove le strutture polimeriche devono resistere inalterate per un tempo pari all’adesione e alla proliferazione cellulare.
In Fig. 4.5 è riportato l’andamento dello swelling in funzione del tempo, dei materiali reticolati chimicamente, ordinati con la percentuale di gelatina crescente.
0 100 200 300 400 500 600 700 800 900 6 24 t (h) % S W CS/0,5GP_s CS/G 60/40_0,5GP_s CS/G 40/60_0,5GP_s CS/G 20/80_0,5GP_s G/0,5GP_s
Fig. 4.5 Andamento della percentuale di swelling in funzione del tempo delle miscele a base di chitosano e gelatina reticolati chimicamente in soluzione
Si può osservare, a 6 ore così come a 24, che la percentuale di swelling aumenta all’aumentare della percentuale di gelatina.
Confrontando la percentuale di swelling dei materiali a tempi diversi si può osservare come essa diminuisce per tutti i materiali analizzati, tranne che per la G/0.5GP_s che presenta un aumento della % SW all’aumentare del tempo. Tale fatto indica che la reticolazione chimica funziona perfettamente per le miscele e per il chitosano puro, mentre nel caso della gelatina bisognerebbe analizzare se un incremento della percentuale di reticolante incrementa il suo grado di reticolazione.
1.3 Influenza delle reticolazioni
Le principali caratteristiche meccaniche dei materiali dipendono, in gran parte, dalla struttura dei materiali e dai legami chimici che tengono uniti gli atomi costituenti. E’ importante rilevare che spesso le caratteristiche meccaniche di un dato materiale possono essere modificate per adattare il materiale ad esigenze particolari. Infatti è risaputo che nel caso dell’adesione e proliferazione cellulare, i materiali che presentano caratteristiche meccaniche diverse dal tessuto originario di partenza possono indurre alterazioni nelle cellule ed inficiare la rigenerazione tissutale. Quindi
è importante sviluppare dei metodi di lavorazione dei materiali che permettono di modificare le proprietà meccaniche in modo da rendere i materiali idonei al trattamento cellulare.
E’ proprio in questo ambito che si colloca il trattamento di reticolazione, il quale modifica le caratteristiche meccaniche dei biopolimeri in esame. In particolare il trattamento di seguito descritto serve ad aumentare la stabilità delle miscele in ambiente acquoso.
In questo lavoro si sono adottate due tipologie di reticolazioni:
1. reticolazione termica, consiste nella permanenza dei film polimerici in stufa da vuoto a 50°C per 90 minuti e per le successive 5 ore a 130°C. Il trattamento ha lo scopo di indurre la formazione di legami esterei tra i gruppi carbossilici nella gelatina e i gruppi amminici della gelatina e del chitosano, con conseguente eliminazione di acqua sotto forma di vapore. La caratterizzazione chimico-fisica dei materiali sottoposti a questo tipo di trattamento ha confermato l’avvenuta reticolazione [1].
2. reticolazione chimica mediante genipina.
E’ noto dalla letteratura che la genipina reagisce con composti contenenti gruppi amminici primari, come il chitosano ed altri peptidi e polipeptidi, per formare reticoli polimerici. Si pensa che la reticolazione sia dovuta a due reazioni che coinvolgono differenti siti sulla molecola di genipina. Le reazioni coinvolte sono:
a. attacco nucleofilo sull’atomo di carbonio C3 della genipina da parte dell’ammina primaria per formare un gruppo aldeidico intermedio. L’apertura dell’anello diidropiranoso è seguita dall’attacco del gruppo amminico secondario formatosi nel primo step di reazione;
b. transammidazione del gruppo estereo sulla genipina da parte di un gruppo amminico primario; questa reazione è la più lenta tra le due e avviene successivamente. La reazione è complicata dalla
omopolimerizzazione radicalica della genipina, indotta dall’ossigeno; questo causa la formazione di un gel che assume un colore blu [2]. Lo schema di reazione è riportato in Fig. 4.6
Reazione a: attacco nucleofilo
Reazione b: sostituzione nucleofila
Fig. 4.6 Meccanismo di reazione della genipina
Diversi agenti reticolanti, come la formaldeide, la glutaraldeide, carbodiimmidi, che sono stati utilizzati per modificare chimicamente i biopolimeri in esame, ma tutti questi composti possono comportare problemi di citotossicità [3]; è per superare questo problema che si è utilizzato un reticolante naturale come la genipina [4] .
Nella tab. 4.1 sono riportati i tempi di reticolazione delle miscele chitosano gelatina reticolate direttamente nella soluzione di preparazione delle miscele.
Materiale
Tempo di reticolazione (min)CS/G 60/40 330
CS/G 40/60 160
CS/G 20/80 77
Tab. 4.1: Tempi di reticolazione chimica in soluzione
Dalla precedente tabella si nota come il tempo di reticolazione diminuisca all’aumentare del contenuto di gelatina nella miscela. Questo è spiegabile in quanto aumentando la gelatina, vi è un maggior numero di gruppi amminici presenti nei suoi vari componenti amminoacidici e quindi aumentano i siti di reticolazione, aumentando la velocità di reticolazione e diminuendo di conseguenza il tempo di questa.
Nel seguente paragrafo si vuole illustrare l’influenza delle diverse metodologie di reticolazione sul comportamento allo swelling e alla dissoluzione. In particolare si sono analizzate le miscele di chitosano e gelatina 40/60 reticolate termicamente, chimicamente in soluzione e in PBS.
In Fig. 4.7 è riportato l’andamento della percentuale di swelling delle miscele suddette.
0 50 100 150 200 250 300 1 3 6 24 48 t (h) % S W CS/G 40/60_r.t. CS/G 40/60_0,5GP_s CS/G 40/60_3GP_PBS
Fig. 4.7 Andamento della percentuale di swelling in funzione del tempo delle miscele CS/G 40/60 reticolate con i diversi metodi illustrati
Si può osservare che l’andamento della percentuale di swelling (% SW) della miscela reticolata termicamente è crescente fino alle 6 ore e poi diventa decrescente.
Per la miscela reticolata chimicamente in soluzione si ha un andamento quasi costante fino alle 3 ore mentre poi si ha un andamento crescente fino alle 6 ore seguito da un andamento decrescente fino alle 48 ore , e si nota che le % SW a quei tempi hanno valori paragonabili a quelli della miscela reticolata termicamente.
Per la miscela reticolata chimicamente in PBS con il 3% di genipina si nota come i valori della % SW siano nettamente inferiori a quelli delle altre due miscele. Questo è dovuto al fatto che aumentando la percentuale di genipina, si ha un aumento del grado di reticolazione e una conseguente diminuzione del rigonfiamento e che tale rigonfiamento resti praticamente costante.
In Fig. 4.8 è riportato l’andamento della percentuale di perdita di peso della miscela chitosano e gelatina 40/60 reticolata termicamente e della miscela reticolata chimicamente in PBS.
0 5 10 15 20 25 30 35 40 6 24 48 t (h) % PP CS/G 40/60_r.t. CS/G 40/60_3GP_PBS
Fig.4.8 Andamento della percentuale di perdita di peso in funzione del tempo delle miscele CS/G 40/60 reticolate con i diversi metodi illustrati
Si osserva che la miscela reticolata termicamente presenta un andamento della percentuale di perdita di peso (% PP) decrescente all’aumentare del tempo, mentre la miscela reticolata chimicamente ha un andamento crescente.
Si nota che per tempi inferiori e uguali alle 24 ore i valori della % PP della miscela reticolata chimicamente sono nettamente inferiori a quelli della miscela reticolata termicamente, mentre alle 48 ore i valori tendono ad avvicinarsi. Questo conferma che la reticolazione chimica con elevate percentuali di genipina (3%) risulta essere molto più efficace di quella termica.
2. Stress-strain
2.1 Materiali reticolati termicamente
Sui campioni precedentemente analizzati è stata eseguita la caratterizzazione meccanica tramite l’uso del trasduttore isotonico già descritto nel paragrafo 2.4.4. L’intervallo di acquisizione dei dati del trasduttore è stato fissato in 1 secondo e l’intervallo di variazione del carico è stato fissato in 180 secondi.
La prova è stata effettuata variando il carico di volta in volta tramite l’ausilio di pesi aggiuntivi in piombo.
L’acquisizione è stata eseguita tramite un software appositamente sviluppato, ed i dati così ottenuti sono stati analizzati in modo da ricavare le curve
sforzo-deformazione dei materiali analizzati.
Nella Fig. 4.9 è possibile osservare l’andamento delle suddette curve per i materiali reticolati termicamente. 0 5 10 15 20 25 30 0 2 4 6 8 10 1 % strain stress (MPa) 2 CS/G 40/60_r.t. CS/G 60/40_r.t. CS/G 20/80_r.t. CS_r.t. G_r.t.
Fig. 4.9 Stress-strain dei materiali reticolati termicamente
Si nota che tutte le curve σ-ε presentano un andamento rettilineo che evidenzia che nel range di carico analizzato, i materiali analizzati hanno un comportamento elastico.
Le pendenze delle curve variano a seconda del materiale, e si nota che, benché il chitosano sia più rigido della gelatina, le pendenze delle curve σ-ε delle miscele aumentano all’aumentare della percentuale di gelatina (curve blu, fucsia e rossa). Questo vuol dire che si ha un irrigidimento del materiale aumentando la
concentrazione di gelatina e che tale irrigidimento non si può spiegare tramite una semplice legge additiva, ma tramite un modello di sistema chiuso basato sulla continuità di fase, che verrà spiegata nel paragrafo 2.5 di questo capitolo.
Dal grafico si nota una anomalia e cioè che la pendenza del chitosano puro e della miscela CS/G 20/80 sono simili, questo è spiegabile in quanto la percentuale di gruppi reattivi nella gelatina è superiore a quelli presenti nel chitosano, permettendo la formazione di un maggior grado di reticolazione e quindi un irrigidimento del materiale.
2.2 Materiali reticolati chimicamente
Le modalità di prova per i materiali reticolati chimicamente sono state eseguite in maniera identica a quelle dei materiali reticolati chimicamente.
La Fig. 4.10 mostra l’andamento delle curve σ-ε per i materiali reticolati con la genipina in soluzione. 0 2 4 6 8 10 12 14 16 18 0 1 2 3 4 5 % strain Stress (MPa) G_0,5GP_s CS_0,5GP_s CS/G 60/40_0,5GP_s CS/G 40/60_0,5GP_s CS/G 20/80_0,5GP_s
Il grafico evidenzia come:
1. gli andamenti delle curve σ-ε sono rettilinei e quindi che i materiali utilizzati hanno un comportamento elastico nel range di carico in cui essi sono stati studiati, come accadeva per quelli reticolati termicamente.
2. l’andamento meccanico del chitosano e della gelatina è molto simile tanto è che le due curve si sovrappongono quasi, mentre quello delle miscele mostra un andamento maggiore rispetto a quella dei componenti puri. Ciò fa capire che, poiché la reticolazione con genipina agisce semplicemente sui gruppi amminici del chitosano e della gelatina, i due componenti puri presentano lo stesso numero di tali siti reattivi e quindi l’andamento è simile per i componenti puri, mentre miscelando questi ultimi, si aumenta il numero dei siti reattivi e quindi aumentano i siti di reticolazione; ne consegue che il materiale si irrigidisce. Tuttavia tale irrigidimento non mostra un andamento proporzionale alla percentuale di uno dei due componenti.
2.3 Influenza delle reticolazioni
Con queste prove si è voluto analizzare la dipendenza dell’andamento stress-strain dai due tipi di reticolazione, termica e chimica, effettuati per lo stesso materiale. In Fig. 4.11 si analizza l’influenza delle reticolazioni sulla gelatina.
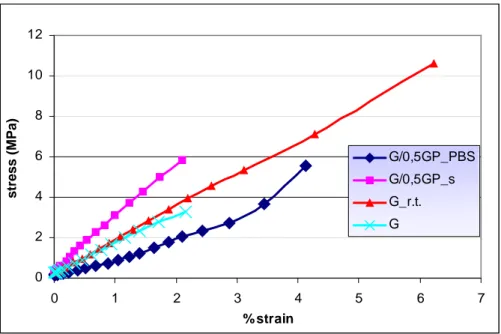
0 2 4 6 8 10 12 0 1 2 3 4 5 6 7 % strain stress (MPa) G/0,5GP_PBS G/0,5GP_s G_r.t. G
Fig. 4.11 Stress-strain dei materiali a base di gelatina
Si può osservare che l’andamento delle curve σ-ε della gelatina non trattata e della gelatina reticolata termicamente è simile, indice che il trattamento termico incide poco sulle caratteristiche di sforzo-deformazione del materiale.
Si nota invece che la reticolazione chimica apporta notevoli variazioni: la reticolazione con GP in soluzione fa aumentare la pendenza delle curve stress-strain, mentre la reticolazione in PBS fa diminuire tale pendenza sempre rispetto alla pendenza della curva stress-strain della gelatina non trattata.
In letteratura è stato visto che la gelatina reticolata con glutaraldeide ha un modulo di Young inferiore rispetto alla gelatina non trattata [5]. La reticolazione con glutaraldeide infatti causa la formazione di corti segmenti alifatici tra le catene di gelatina. E’ noto inoltre che quando una soluzione calda di gelatina viene sottoposta a raffreddamento, il materiale assume parzialmente una struttura a tripla elica responsabile di una reticolazione fisica della gelatina. Al crescere del contenuto di glutaraldeide il recupero della struttura a tripla elica si riduce e il materiale diventa più duttile. Dunque il bilancio tra la reticolazione fisica e la reticolazione chimica della gelatina influenza le prestazioni meccaniche del materiale.
Nel caso della genipina, si può ipotizzare che una reticolazione più pronunciata del materiale conduca ad un suo irrigidimento, a causa del maggior ingombro sterico
dell’agente reticolante rispetto al caso della glutaraldeide, per cui la reticolazione chimica influisce maggiormente sulla variazione delle proprietà meccaniche dei materiali rispetto alla reticolazione termica.
In Fig. 4.12 si analizza l’influenza delle reticolazioni su una miscela CS/G 40/60.
0 10 20 30 40 50 60 70 80 90 0 1 2 3 4 5 % strain stress (MPa) CS/G 40/60 CS/G 40/60_r.t. CS/G 40/60_0,5GP_s CS/G 40/60_3GP_PBS
Fig. 4.12 Stress-strain delle miscele CS/G 40/60 reticolate con i diversi metodi illustrati
In questo grafico si nota che tutti i tipi di reticolazioni apportano una diminuzione della pendenza rispetto alla miscela non trattata.
Si osserva che le curve della miscela reticolata termicamente e della miscela reticolata chimicamente con 0.5% di genipina si sovrappongono.
Inoltre risulta evidente che un ad un aumento della percentuale di genipina (dallo 0.5% al 3%) nella miscela corrisponde un aumento della pendenza della retta stress-strain (curva verde e curva celeste), cioè ad un irrigidimento del materiale, rispetto alla stessa reticolazione fatta a concentrazioni inferiori, ciò implica che vi sono ancora siti reattivi liberi, che non vengono impegnati con una concentrazione pari allo 0.5%.
2.4 Moduli di Young
Materiali reticolati termicamente
I moduli di Young dei materiali analizzati sono stati calcolati misurando la pendenza delle curve stress-strain.
In Fig. 4.13 è riportato l’andamento del modulo di Young delle miscele CS/G e dei componenti puri reticolati termicamente in funzione della percentuale di gelatina (N.B.: al CS corrisponde lo 0% di G). 0 100 200 300 400 500 600 0 40 60 80 100 %G E (MPa)
Fig. 4.13 Andamento del modulo di Young in funzione della percentuale di gelatina dei materiali reticolati termicamente
Si può notare come si ha una aumento lineare del modulo di Young delle miscele in funzione dell’aumento della percentuale di gelatina in miscela.
Questo comportamento risulta anomalo, in quanto ci si aspetterebbe una diminuzione del modulo di Young delle miscele all’aumentare della % di G, visto che il modulo di Young più grande, tra quello dei componenti puri, è quello del CS. Questo
comportamento dimostra la non additività di questa proprietà meccanica per le miscele reticolate termicamente.
Ultimo aspetto da notare è che i valori dei moduli di Young del CS e della miscela CS/G 20/80 sono all’incirca uguali, la spiegazione di questo andamento è gia stata
data al paragrafo 2.1 di questo capitolo. Inoltre si può notare come in realtà la presenza del chitosano irrigidisca il materiale a causa della formazione di legami i gruppi amminici del chitosano e i gruppi carbossilici della gelatina.
Materiali reticolati chimicamente
In Fig. 4.14 è riportato il modulo di Young delle miscele CS/G e dei componenti puri reticolati chimicamente con 0.5% G di genipina, espresso in funzione della
percentuale di gelatina (N.B.: al CS corrisponde lo 0% di G).
0 200 400 600 800 1000 0 40 60 80 100 %G E (MPa)
Fig. 4.14 Andamento del modulo di Young in funzione della percentuale di gelatina dei materiali reticolati chimicamente
Si può osservare che il modulo di Young del chitosano è maggiore rispetto a quello degli altri materiali, come nel caso dei materiali reticolati termicamente.
Altra caratteristica importante è che si ha un andamento crescente e lineare dei moduli di Young delle miscele CS/G, come nel caso precedente, fatto che conferma l’ipotesi esposta precedentemente.
In Fig. 4.15 si può fare un confronto tra i moduli di Young dei materiali reticolati chimicamente e quelli dei materiali reticolati termicamente.
0 200 400 600 800 1000 1200 0 40 60 80 100 %G E (MPa) reticolati termicamente reticolati chimicamente
Fig. 4.15 Andamento del modulo di Young in funzione della percentuale di gelatina dei materiali reticolati chimicamente e termicamente a confronto
Si nota che in tutti i casi i moduli di Young dei materiali reticolati chimicamente sono maggiori di quelli dei corrispondenti materiali reticolati termicamente.
Si osserva come per il CS reticolato chimicamente si sia avuto un incremento di quasi il 100% del valore del modulo di Young in confronto al CS reticolato termicamente. Tale fatto ci porta a concludere che la reticolazione chimica è più efficace di quella termica
2.5 Modello predittivo dei moduli di Young
Quando si realizzano miscele di polimeri è utile riuscire a predire alcune proprietà, come il modulo di Young, la permeabilità ai gas, ecc., dei materiali ottenuti, partendo dalle proprietà dei componenti della miscela. La predizione delle proprietà delle miscele polimeriche è utile, in quanto è possibile realizzare blends polimerici con le caratteristiche volute prima di intraprendere la sperimentazione.
Ci sono diversi modelli applicabili alle miscele polimeriche per quanto riguarda il calcolo del modulo di Young [6,7], ma nel nostro caso forniscono valori predittivi che si discostano molto dai risultati sperimentali.
Tra i vari modelli predittivi applicabili alle miscele polimeriche, quello sviluppato da Kolarik [8] è risultato il più adatto all’interpretazione dei dati sperimentali ottenuti. Lo schema è basato sulla combinazione di un modello a scatola chiusa a due parametri (schematizzato in Fig. 4.16) e sul concetto di continuità di fase.
F
v1s v2s v2p v1pF
Fig. 4.16 Equivalent Box Model per una miscela polimerica binaria
Il modello a due parametri è detto Equivalent Box Model (EBM), e si basa sull’accoppiamento in serie e in parallelo di blocchi che hanno proprietà meccaniche identiche a quelle dei componenti della miscela. Le dimensioni dei blocchi è data dalla frazione volumetrica di ogni costituente.
Tali frazioni volumetriche accoppiate in serie (con pedice s) e in parallelo (con pedice p) si possono calcolare per via analitica attraverso le seguenti formule:
vip = vi * Ci con i = 1,2 vis = vi * (1-Ci)
dove vi rappresentano le frazioni volumetriche della miscela e Ci rappresentano i parametri di continuità di fase.
Oppure si possono calcolare per via grafica [9], sempre conoscendo le frazioni volumetriche vi .
Il modello fornisce il valore del modulo di Young della miscela Eb. L’equazione che permette questo calcolo è la seguente:
E b
(
v 1p E 1⋅ + v 2p E 2⋅)
v s 2 v 1s E 1 v 2s E 2 +⎛
⎜
⎝
⎞
⎠
⎡
⎢
⎢
⎢
⎣
⎤
⎥
⎥
⎥
⎦
+ := (eq. 4.1) Dove si indicano con:Ei i moduli di Young dei componenti della miscela;
vs la frazione volumetrica della parte in serie che è pari a : vs = v1s + v2s .
Dai calcoli effettuati è risultato che i moduli di Young delle miscele di chitosano e gelatina reticolati termicamente ottenuti per via predittiva si avvicinano ai risultati ottenuti per via sperimentale, come rappresentato nel grafico di Fig. 4.17.
0 100 200 300 400 500 600 40 60 80 % G E (MPa) sperimentali predittivi
Fig 4.17 Andamento dei moduli di Young in funzione della percentuale di gelatina delle miscele reticolate termicamente ottenuti per via
sperimentale e per via predittiva
L’errore medio percentuale commesso nell’utilizzo di questo modello è dell’ordine del 7 %, ciò ci permette di affermare, come già più volte detto precedentemente, che la reticolazione di una miscele non induce un andamento additivo delle proprietà meccaniche dei singoli costituenti.
2.6 Caratterizzazione meccanica dei materiali reticolati termicamente
dopo immersione in mezzo di coltura
Al fine di caratterizzare il comportamento a umido dei materiali reticolati termicamente, questi sono stati immersi in un bagno in un terreno di coltura cellulare per 1 ora a 37°C, in modo da simulare il tipo di ambiente cellulare.
Tale processo serve a verificare possibili variazioni nelle proprietà meccaniche dei materiali dopo che gli scaffold vengono posti a contatto con soluzioni contenenti sali minerali, glucosio, proteine, amminoacidi, che sono i componenti base del terreno di coltura cellulare. Questa sperimentazione serve a verificare l’applicabilità degli scaffold nel settore dell’Ingegneria Tissutale.
Successivamente sono state effettuate le prove stress-strain e le prove di creep-relaxation, identiche a quelle sui materiali “secchi”.
Stress-strain e moduli di Young
In Fig. 4.18 sono riportate le curve sforzo-deformazione dei materiali reticolati termicamente dopo il bagno in mezzo di coltura.
0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 % strain stress (MPa) 6 CS_r.t. CS/G 40/60_r.t. CS/G 60/40_r.t. CS/G 20/80_r.t.
Fig. 4.18 Stress-strain dei materiali reticolati termicamente bagnati
Il primo aspetto che si osserva è la mancanza della curva relativa alla gelatina: ciò è dovuto al fatto che essa si è sciolta nel mezzo di coltura durante il bagno.
Il secondo aspetto da notare è che le curve non hanno un andamento rettilineo e che le pendenze diminuiscono drasticamente all’aumentare della percentuale di gelatina nelle miscele. Questo è dovuto alla presenza di gelatina nella miscela che tende a rigonfiare nel mezzo di coltura, e in parte a sciogliersi, plasticizzando il materiale. Inoltre si nota come al variare della concentrazione di gelatina, ad eccezione della miscela CS/G 60/40_r.t., il materiale diviene più rigido all’ aumentare di questa, cosa spiegabile con il fatto che la gelatina non reticolata tende a sciogliersi.
In Fig. 4.19 sono riportati i moduli di Young dei materiali umidi in funzione della percentuale di gelatina contenuta nelle miscele.
0 100 200 300 400 500 600 0 40 60 80 % G E (MPa)
Fig. 4.19 Andamento dei moduli di Young in funzione della percentuale di gelatina dei materiali reticolati termicamente bagnati
Si può notare che all’aumentare della percentuale di gelatina si ha un andamento fortemente decrescente dei valori dei moduli di Young, cosa che conferma quanto detto sopra.
I valori dei moduli di Young sono riportati nella tabella 4.2.
MATERIALE % G E (MPa) CS_r.t. 0 481 CS/G 60/40_r.t. 40 71,4 CS/G 40/60_r.t. 60 27,9 CS/G 20/80_r.t. 80 3,1 G_r.t. 100 sciolto
In Fig. 4.20 si è effettuato un confronto tra i materiali reticolati termicamente prima e dopo l’immersione in mezzo di coltura.
0 100 200 300 400 500 600 700 0 40 60 80 100 %G E (MPa) secchi bagnati
Fig. 4.20 Andamento dei moduli di Young in funzione delle percentuale di gelatina tra i materiali reticolati termicamente secchi e bagnati a confronto
In questo grafico si può notare che il chitosano subisce con il bagno una riduzione del modulo di Young pari al 20%.
Si osserva inoltre che l’andamento dei moduli di Young delle miscele secche e di quelle bagnate è opposto: crescente per i materiali secchi e decrescente per quelli bagnati in funzione del loro contenuto di gelatina.
Il bagno infatti riduce il modulo di Young delle miscele dell’ 80-99.5% rispetto ai campioni secchi. Ciò è spiegabile in quanto durante il bagno la gelatina si rigonfia e poi si degrada completamente.
3. Creep-relaxation
3.1 Materiali reticolati termicamente
Per meglio analizzare il comportamento viscoelastico dei materiali utilizzati sono state eseguite prove di creep-relaxation come specificato nel capitolo 3 paragrafo 2.4.3.
Tramite il trasduttore isotonico descritto nel capitolo 3 paragrafo 2.4.4, i film polimerici sono stati sottoposti a carico costante per la durata di un’ora, e dopo la rimozione del peso, si è avuto il rilassamento dei campioni. Il carico da applicare è stato calcolato tramite le curve stress-strain in corrispondenza dello 0.5% della deformazione.
Il grafico in Fig. 4.21 mostra l’andamento della percentuale di strain normalizzato dei materiali in funzione del tempo.
-1,4 -1,2 -1 -0,8 -0,6 -0,4 -0,2 0 0,2 0,4 0,6 0 20 40 60 80 100 120 t (min) % strain CS_r.t. CS/G 40/60_r.t. CS/G 60/40_r.t. CS/G 20/80_r.t. G_r.t.
Fig. 4.21 Andamento del creep dei materiali reticolati termicamente
Si nota che tutte le curve presentano lo stesso andamento qualitativo. Tale andamento è il classico andamento di un solido lineare standard a tre parametri che verrà descritto nel paragrafo 3.3 di questo capitolo.
Si può osservare come la parte iniziale (quella crescente) di ogni curva tende ad essere sovrapponibile per tutti i campioni con una percentuale di strain compresa tra lo 0 e 0,4 %, le principali differenze emergono nella seconda parte (quella decrescente) in quanto pur presentando lo stesso andamento qualitativo, mostrano percentuali di strain recuperato variabile in funzione della composizione, in un intervallo di strain compreso tra -1.2% e 0.
Si nota che il rilassamento delle miscele CS/G 40/60_r.t. e CS/G 60/40_r.t. è minore rispetto a quello dei componenti puri (curve fucsia, rossa) , mentre il rilassamento della miscela CS/G 20/80_r.t. è maggiore rispetto a quello dei componenti puri. Questo spiega notando che la miscela CS/G 20/80_r.t. presenta un marcato comportamento viscoelastico, infatti tale materiale si deforma di più rispetto agli altri nella fase di carico e dopo che il peso è stato rimosso, non riesce a recuperare la deformazione ottenuta, ma presenta un rilassamento più marcato, aspetto che non si è verificato per le altre due miscele. Questo è indice che il grado di reticolazione è più marcato per le altre due miscele che per quest’ultima.
3.2 Materiali reticolati chimicamente
In Fig. 4.22 sono riportati gli andamenti della percentuale di strain normalizzato dei materiali reticolati chimicamente con lo 0.5% di genipina in funzione del tempo. Le modalità di prova sono analoghe a quelle utilizzate per i materiali reticolati termicamente.
-0,6 -0,5 -0,4 -0,3 -0,2 -0,1 0 0,1 0,2 0,3 0,4 0 20 40 60 80 100 1 t (min) strain 20 CS/0,5GP_s CS/G 40/60_0,5GP_s CS/G 60/40_0,5GP_s CS/G 20/80_0,5GP_s G/0,5GP_s
Fig. 4.22 Andamento del creep dei materiali reticolati chimicamente
Si nota che nella prima parte della curva, gli andamenti sono molto simili (ad eccezione della gelatina) con il range della percentuale di strain compreso tra 0 e 0,2 %, come nel caso precedente.
Anche nella seconda parte della curva si ha sovrapposizione degli andamenti, fatta eccezione per la gelatina e per la miscela CS/G 20/80_0.5GP_s, in un range di rilassamento compreso tra 0 e -0,5 % ; la gelatina infatti presenta un range di rilassamento molto inferiore e la miscela CS/G 20/80_0.5GP_s ne presenta uno molto superiore, rispetto a quello delle altre miscele analizzate. Da tale andamento si evince, come nel caso precedente, che la reticolazione chimica, ma anche quella termica, laddove vi è un grande contenuto di gelatina, amplifica il comportamento viscoelastico della miscela.
3.3 Modello meccanico
Dopo un’attenta analisi degli andamenti delle curve di creep-relaxation, si può affermare che tutti i materiali hanno un comportamento paragonabile ad un solido lineare standard a tre parametri (Fig. 4.23), e come riportato in letteratura [10] .
Fig. 4.23 Rappresentazione del solido lineare standard a tre parametri
Tale modello è dato dalla combinazione di tre modelli elementari: 2 modelli lineari elastici (molle) e un elemento viscoso lineare (pistone). La loro combinazione è data da un parallelo tra una molla, di costante elastica K1 , e un pistone, con coefficiente di viscosità η, che a loro volta sono in serie con un’altra molla, di costante elastica K2. Il sottosistema molla-pistone in parallelo descrive il comportamento puramente
viscoelastico del materiale, mentre la molla con costante di elasticità K2 rappresenta il comportamento puramente elastico del materiale.
L’equazione matematica che descrive il modello suddetto è la seguente:
ε
ε
o 1
K2
K1 K2
+
⎛
⎜
⎝
⎞
⎠
e
K1 − ⋅K2⋅t η K⋅(
1 K2+)
⎡⎢
⎢⎣
⎤⎥
⎥⎦
⋅
−
⎡
⎢
⎢
⎢
⎣
⎤
⎥
⎥
⎥
⎦
⋅
:=
(eq. 4.2)Nel presente lavoro di tesi, partendo dall’equazione precedente e utilizzando l’andamento delle curve di creep-relaxation delle miscele, tramite il programma di interpolazione grafica Origin® 6.1, si sono calcolati i parametri K1, K2 e η che
schematizzano ogni materiale studiato inoltre si è calcolato il parametro τ che è pari: τ = η* (K1 + K2)/(K1* K2).
I risultati sono riportati nelle tabelle 4.3 e 4.4.
MATERIALE K1 (MPa) K2 (MPa) η (MPa*s) τ (s)
CS_r.t. 819 835,7 729224 0,49
CS/G 20/80_r.t. 3983 3996 2082508 0,29
CS/G 40/60_r.t. 4990 4650 3192276 0,47
CS/G 60/40_r.t. 6387 6860 4134483 0,34
G_r.t. 360 404,6 230750 0,34
Tab. 4.3: tabella parametri creep dei materiali reticolati termicamente
MATERIALE K1 (MPa) K2 (MPa) η (MPa*s) τ (s)
CS/0.5GP_s 360 498 223637 0,297
CS/G 20/80_0.5GP_s 360 498 223637 0,297
CS/G 40/60_0.5GP_s 290 352 168026 0,297
CS/G 60/40_0.5GP_s 229 291 136062 0,295
G/0.5GP_s 66 69,5 19745 0,162
Dall’analisi della Tab. 4.3 si può notare che la reticolazione termica influenza molto le caratteristiche di creep-relaxation dei materiali. In particolare i parametri K1, K2 e η per le miscele sono nettamente superiori rispetto a quelli dei materiali puri.
Dal confronto tra la Tab. 4.3 e la Tab. 4.4 si possono tracciare i grafici dei parametri del creep dei materiali reticolati termicamente e reticolati chimicamente in funzione della percentuale di gelatina.
In Fig. 4.24 si nota che per le miscele reticolate termicamente si ha un andamento di K1 decrescente all’aumentare della percentuale di gelatina, mentre per le miscele reticolate chimicamente l’andamento è leggermente crescente. Inoltre a parità di percentuale di gelatina, i valori di K1 delle miscele reticolate termicamente sono molto più elevati di quelli delle miscele reticolate chimicamente. Un andamento crescente di K1 indica che la componente elastica del materiale tende a dominare su quella viscosa.
Per i materiali puri, chitosano e gelatina, si osserva che essi hanno valori molto più bassi rispetto alle loro miscele e da un confronto tra materiali puri reticolati termicamente e quelli reticolati chimicamente, i primi risultano avere valori di K1 più elevati rispetto ai secondi.
0 1000 2000 3000 4000 5000 6000 7000 0 40 60 80 100 % G K1 (MPa) reticolati termicamente reticolati chimicamente
Fig. 4.24 Andamento di K1 in funzione della percentuale di gelatina dei materiali
In Fig. 4.25 si nota che per le miscele reticolate termicamente si ha un andamento di K2 decrescente all’aumentare della percentuale di gelatina, mentre per le miscele reticolate chimicamente l’andamento è crescente. Inoltre a parità di percentuale di gelatina, i valori di K2 delle miscele reticolate termicamente sono molto più elevati di quelli delle miscele reticolate chimicamente. Un andamento crescente di K2 è indice di un aumento del campo puramente elastico del materiale, cioè di un aumento della velocità di creep e di rilassamento.
Per i materiali puri, chitosano e gelatina, si osserva che essi hanno valori molto più bassi rispetto alle loro miscele e da un confronto tra materiali puri reticolati termicamente e quelli reticolati chimicamente, i primi risultano avere valori di K2 più elevati rispetto ai secondi.
0 1000 2000 3000 4000 5000 6000 7000 8000 0 40 60 80 100 % G K2 (MPa) reticolati termicamente reticolati chimicamente
Fig. 4.25 Andamento di K2 in funzione della percentuale di gelatina dei materiali
reticolati termicamente e chimicamente a confronto
In Fig. 4.26 si nota che per le miscele reticolate termicamente si ha un andamento di η decrescente all’aumentare della percentuale di gelatina, mentre per le miscele reticolate chimicamente l’andamento è crescente. Inoltre a parità di percentuale di
gelatina, i valori di η delle miscele reticolate termicamente sono molto più elevati di quelli delle miscele reticolate chimicamente.
Per i materiali puri, chitosano e gelatina, si osserva che essi hanno valori molto più bassi rispetto alle loro miscele e da un confronto tra materiali puri reticolati termicamente e quelli reticolati chimicamente, i primi risultano avere valori di η più elevati rispetto ai secondi.
Confronto eta 0,0E+00 5,0E+05 1,0E+06 1,5E+06 2,0E+06 2,5E+06 3,0E+06 3,5E+06 4,0E+06 4,5E+06 0 40 60 80 100 % G Eta (MPa*s) reticolati termicamente reticolati chimicamente
Fig. 4.26 Andamento di η in funzione della percentuale di gelatina dei materiali reticolati termicamente e chimicamente a confronto
Dall’analisi dei tre grafici si può affermare che la reticolazione termica accentui l’andamento viscoelastico del materiale, e che al crescere della percentuale di gelatina i valori di K1 , K2 , ed η diminuiscono rendendo il materiale plastico.
3.4 Creep-relaxation dei materiali reticolati termicamente dopo
immersione in mezzo di coltura
In Fig. 4.27 sono riportati gli andamenti di creep-relaxation relativi ai materiali reticolati termicamente che hanno subito un bagno in un mezzo di coltura.
-1,5 -1 -0,5 0 0,5 1 1,5 0 20 40 60 80 100 120 t (min) strain CS_r.t. CS/G 40/60_r.t. CS/G 60/40_r.t. CS/G 20/80_r.t.
Fig. 4.27 Andamento del creep dei materiali reticolati termicamente bagnati
Si può osservare come l’andamento qualitativo di tutte le curve , ad eccezione di quella del CS/G 20/80, è molto simile ed è paragonabile a quello di un solido lineare standard a tre parametri.
Per la miscela CS/G 20/80 l’andamento è diverso e il materiale inizia la fase di rilassamento molto tempo prima che venga rimosso il peso durante la prova; tuttavia analizzando il suo andamento si può far rientrare il suo comportamento in quello di un solido lineare standard.
Con la procedura spiegata nel paragrafo 3.3 di questo capitolo, si sono calcolati i parametri del modello meccanico che descrive il comportamento dei materiali studiati. Tali parametri sono riassunti nella tabella 4.5.
MATERIALE K1 (MPa) K2 (MPa) η (MPa*s) τ (s)
CS_r.t. 58,4 67,5 37350 0,3314
CS/G 20/80_r.t. 2,41 3,12 146 0,0298 CS/G 40/60_r.t. 491 492 263379 0,2977 CS/G 60/40_r.t. 25,5 30,3 25337 0,5085
Tab. 4.5: parametri creep dei materiali reticolati termicamente bagnati
Si può notare il notevole abbassamento dei valori di Ki e η di rispetto ai corrispondenti materiali secchi , particolarmente marcato per la miscela CS/G 20/80_r.t. Tale fatto è legato alla dissoluzione di gran parte della gelatina e che in soluzione porta a trasformare il materiale da viscoelastico a plastico.
4. Pressu re Activated Microsyringe
4.1 Caratterizzazione della macchina
I materiali finora utilizzati permettono di ottenere scaffold in forma di film, ma non di poter variare la loro topologia strutturale. Per studiare come geometrie diverse
influenzino le caratteristiche meccaniche, si è pensato di utilizzare un polimero che potesse essere lavorato tramite la tecnica PAM. Per utilizzare tale sistema il materiale deve essere solubile in un solvente altamente volatile, quale cloroformio. Per tale motivo si è scelto di usare un poliuretano a blocchi sintetizzato presso i laboratori del Dipartimento di Ingegneria Chimica.
Per prima cosa si sono effettuate prove preliminari di deposizione di una soluzione di PU in cloroformio all’8% (w/v), finalizzate ad individuare i parametri operativi ottimali.
Tali prove hanno riguardato la valutazione della larghezza delle piste sia in funzione della pressione di deposizione, a velocità di deposizione costante (pari a 2500 µm/s)
sia in funzione della velocità di deposizione a pressione di deposizione costante (pari a 30 cbar).
Nel grafico 4.28 è mostrato l’andamento della larghezza delle piste, a velocità di deposizione costante, in funzione della pressione di deposizione. Si nota che tale andamento è lineare crescente tra 50 e 200 µm e per pressioni comprese tra 5 e 70 cbar. 0 50 100 150 200 250 0 10 20 30 40 50 60 70 80 pressione (cBar) larghezza pista ( m)
Fig. 4.28 Larghezza delle piste in funzione della pressione di deposizione
In Fig. 4.29 è mostrato l’andamento della larghezza delle piste, a pressione di deposizione costante, in funzione della velocità di deposizione. Si nota che tale andamento è esponenziale decrescente tra 140 e 30 µm al crescere delle velocità di deposizione tra 2500 e 5000 µm/s. Ciò conferma il modello fisico-matematico sviluppato per la caratterizzazione del sistema PAM, dove la larghezza della pista cresce proporzionalmente all’aumentare della pressione e decresce in modo inversamente proporzionale alla velocità di avanzamento [11].
0 20 40 60 80 100 120 140 160 2000 2500 3000 3500 4000 4500 5000 5500 velocità (µm/s) larghezza pista ( µm)
Fig. 4.29 Larghezza delle piste in funzione della velocità di deposizione
Si sono scelti i parametri operativi che consentissero di ottenere piste larghe all’incirca 100-150 µm. Si è pertanto operato con i seguenti parametri:
pressione di deposizione: Pdep = 30 cbar ; velocità di deposizione: vdep = 2500 µm/s.
In seguito sono stati microfabbricati varie tipologie di scaffold utilizzando tre diverse geometrie della cella unitaria (quadrata, esagonale e ottagonale). Tali scaffold sono tridimensionali, in quanto costituiti dalla sovrapposizione di tre strati di deposizione tra i quali è stato depositato uno strato di polimero idrosolubile, che permette la formazione di una intercapedine in cui le cellule, una volta che il polimero idrosolubile è stato rimosso, possono penetrare ed inoltre che fa si che la struttura non collassi.
In Fig. 4.30 a,b,c sono riportate le immagini ottenute al microscopio elettronico delle tre diverse geometrie della cella unitaria degli scaffold ottenuti tramite deposizione con PAM.
Fig. 4.30a griglia quadrata Fig. 4.30b griglia esagonale
Fig. 4.30c griglia ottagonale
4.2 Stress-strain
Sono state eseguite le prove stress-strain sugli scaffold di PU ottenuti per deposizione con la tecnica PAM e sui film di PU ottenuti per casting.
Per prima cosa si è caratterizzato meccanicamente il poliuretano in forma di film ottenuto per casting.
In seguito si sono effettuate le medesime prove stress-strain sugli scaffold microdepositati.
Gli scaffold sono stati realizzati in tre diverse geometrie (quadrata, esagonale e ottagonale), per analizzare l’influenza della topologia sulle proprietà meccaniche. Inoltre questi scaffold sono stati confrontati con i film di PU per valutare la variazione delle proprietà meccaniche in funzione del diverso tipo di tecnica utilizzata per l’ottenimento di supporti per l’Ingegneria tissutale.
In Fig. 4.31 sono mostrati gli andamenti delle curve stress-strain del PU nelle diverse forme. 0 0,5 1 1,5 2 2,5 3 3,5 4 4,5 5 0 5 10 15 20 25 30 strain (%)
stress (MPa) griglia
esagoni ottagoni film
Fig. 4.31 Stress-strain delle diverse forme di PU
La curva σ-ε del film di PU presenta un tipico andamento lineare elastico, mentre per gli scaffold ottenuti tramite PAM le curve σ-ε hanno un andamento viscoelastico. La variazione delle proprietà meccaniche degli scaffold in PU sono da attribuire al fatto che i campioni ottenuti tramite PAM non sono provini a sezione piena, ma sono trame di tessuto che, sottoposte a trazione, subiscono un riarrangiamento che ne modifica la geometria.
A basse deformazioni le microstrutture mostrano un comportamento lineare elastico variabile con la geometria della cella unitaria. La pendenza delle curve nel loro tratto iniziale aumenta all’aumentare del numero dei lati della cella unitaria.
Ad alti valori della deformazione, gli scaffold presentano un comportamento plastico. In particolare si osserva che a parità di sforzo applicato è maggiore la deformabilità delle microstrutture con cella unitaria a minore numero di lati. Ciò lo si può spiegare considerando che aumentando il numero dei lati occorrono carichi maggiori per allineare tra loro le linee che compongono la cella.
Per caratterizzare la rigidità del materiale a bassa e ad alta percentuale di deformazione, sono state calcolate le pendenze delle curve σ-ε nel loro tratto iniziale elastico e nel successivo tratto plastico. Per valutare l’influenza della maglia sul materiale si è supposto di considerare la microstruttura come il parallelo del materiale e della maglia. Conoscendo dai dati sperimentali il valore del parallelo tra i due e conoscendo il modulo di Young del materiale puro, è stato possibile ricavare il modulo di Young della maglia.
Più precisamente, chiamando Ep1 la pendenza della curva σ-ε della fase I e Ep2 la pendenza della curva σ-ε della fase II e indicando con EPU il modulo di Young, calcolato sperimentalmente, del film di PU ottenuto per casting si sono ottenuti:
EI = (Ep1 * EPU) / (Ep1 + EPU) (eq. 4.3) EII = (Ep2 * EPU) / (Ep2 + EPU) (eq. 4.4)
Questo è stato fatto perché gli scaffold ottenuti tramite PAM hanno una struttura a maglia di tessuto. Nella definizione delle proprietà meccaniche delle maglie di tessuto c’è da dire che per le basse deformazioni è predominante l’influenza della geometria delle maglie. Per le alte deformazioni è predominante l’influenza del materiale in quanto la struttura a maglia di tessuto ha perso la sua conformazione originale, proprio a causa dell’elevata deformazione [12].
I moduli di Young EI ed EII per le differenti geometrie sono riportati rispettivamente nei grafici di Fig. 4.32 e di Fig. 4.33 a confronto con il modulo di Young del film ottenuto per casting.
0 50 100 150 200 250
griglia esagono ottagono film
E (MPa)
Fig. 4.32 Moduli di Young della fase I delle microstrutture in funzione della geometria della cella unitaria
0 50 100 150 200 250
griglia esagono ottagono film
E (MPa)
Fig. 4.33 Moduli di Young della fase II delle microstrutture in funzione della geometria della cella unitaria
I moduli di Young della fase I sono più elevati rispetto a quelli della fase II per ogni microstruttura analizzata. Inoltre il valore di EI cresce al crescere del numero dei lati della cella elementare, mentre EII si mantiene pressoché invariato con la geometria della cella elementare degli scaffold, ciò conferma che il valore di EII è una
Il comportamento meccanico del film di PU ottenuto per casting è stato analizzato anche dopo trattamento dello stesso in terreno di coltura per 1 ora a 37°C.
In Fig. 4.34 è mostrato il confronto tra gli andamenti delle curve σ-ε per il film di PU secco e per quello bagnato.
0 1 2 3 4 5 6 0 0,5 1 1,5 2 2,5 3 % strain stress (MPa) PU film secco PU film bagnato
Fig. 4.34 Stress-strain dei film di PU bagnato e secco a confronto
Si può osservare che l’andamento delle due curve σ-ε è rettilineo.
Si vede che la pendenza delle curve σ-ε del PU bagnato è nettamente inferiore a quella del PU secco, segno che il comportamento elastico del polimero è variato in conseguenza del bagno. Questo aspetto lo si può notare meglio confrontando i moduli di Young, che derivano dalle curve suddette, riportati nella Fig. 4.35. Ciò è spiegabile, tenendo conto che il poliuretano è un copolimero a blocchi, che esso presenta una componente idrofilia, la quale in presenza del terreno di coltura tende a legarsi all’acqua presente nel terreno e a rendere il materiale meno rigido.
0 50 100 150 200 250 secco bagnato tipo di film E (MPa)
Fig. 4.35 Moduli di Young dei film di PU secco e bagnato a confronto
4.3 Creep-relaxation
Sono state effettuate le prove di creep-relaxation, con le modalità già descritte nel paragrafo 2.4.3 del capitolo 3, su film di PU ottenuti per casting e sugli scaffold di PU ottenuti per deposizione con PAM.
Nella Fig. 4.36 sono messi a confronto gli andamenti del creep del film di PU secco e bagnato. -1,2 -1 -0,8 -0,6 -0,4 -0,2 0 0,2 0,4 0 20 40 60 80 100 1 t (min) % strain 20 film bagnato film secco
Si osserva un analogo andamento qualitativo delle curve creep-relaxation per i due tipi di film secco e bagnato. Focalizzando l’attenzione sulla prima parte della curva, si osserva una sovrapposizione degli andamenti per il film secco e per quello bagnato. Nella seconda parte si nota una forte differenza nella percentuale di recupero: il materiale secco ha un rilassamento circa 4 volte maggiore rispetto a quello del materiale bagnato.
Si può quindi dire che il bagno nel mezzo di coltura, per il PU, influenza maggiormente la proprietà di rilassamento del materiale.
E’ stata poi valutata l’influenza della geometria della cella unitaria degli scaffold sul comportamento viscoelastico.
In Fig. 4.37 sono mostrati gli andamenti delle curve creep-relaxation del film ottenuto per casting e degli scaffold di PU.
-1,5 -1 -0,5 0 0,5 1 1,5 0 20 40 60 80 100 120 tempo (min) strain (%) griglia esagono ottagono film
Fig. 4.37 Creep delle diverse forme di PU
Dal grafico precedente si nota che l’andamento è simile per tutti i campioni. Tale andamento indica che le diverse forme di PU hanno un comportamento paragonabile a quello di un solido lineare standard a tre parametri.
Con le modalità descritte nei paragrafi precedenti, è possibile calcolare i parametri del creep delle diverse forme di PU. Questi parametri sono riassunti nella tabella 4.6.
Forme di PU K1 (MPa) K2(MPa) η (MPa*s) τ (s)
griglia 32 33 11025 0,188
esagono 58 58 30900 0,295
ottagono 66 66 33796 0,284
film 16 246,5 4673 0,312
Tab. 4.6: parametri creep del PU film e delle diverse geometrie di PU ottenuto tramite PAM
Da questa tabella si può notare che il parametro K1 ha lo stesso ordine di grandezza per i diversi scaffold in PU ottenuti tramite PAM, e si vede che tale valore aumenta all’aumentare del numero di lati della cella unitaria. Il valore più basso si ha per il film di PU ottenuto per casting.
Si nota che i parametri K2 dei PU ottenuti per PAM hanno un ordine di grandezza inferiore rispetto a quello del film di PU e crescono al crescere del numero dei lati della cella unitaria. Analogamente η cresce al crescere del numero dei lati della cella unitaria mantenendosi comunque superiore al valore assunto dal film per casting. In base alle differenze di valore dei parametri dei campioni depositati e di quelli del film per casting, si può affermare che il parametro K1 è il più influenzato dal tipo di materiale, mentre i parametri K2 e η sono più influenzati dalla geometria, e che all’aumentare del numero dei lati della cella base, tali parametri aumentano proporzionalmente.
5. Confronto tra le proprietà meccaniche degli scaffold e dei
tessuti biologici
Dopo aver effettuato la caratterizzazione meccanica degli scaffold si sono confrontati i moduli di Young degli scaffold con quelli dei principali tessuti biologici, per vedere se era possibile utilizzare tali materiali come validi supporti per la ricrescita cellulare ed in particolare per valutare che tipo di tessuto è possibile rigenerare con tali biopolimeri.
E’ noto infatti che, se i moduli di Young dei tessuti da rigenerare si discostano molto da quelli del substrato polimerico, si può avere una concentrazione degli sforzi all’interfaccia tessuto/polimero, tale da generare una risposta infiammatoria dell’organismo, con formazione di una capsula fibrotica.
In tabella 4.7 sono riportati i moduli di Young di alcuni tessuti biologici [13].
Tipo di tessuto
Modulo di Young (MPa)
Vertebra toracica superiore 343Vertebra lombare 343 Tendine d’Achille 196.2 Tendine chordae 38.3 Valvola tricuspide 2.94 Nervo sciatico 6.57 Nervo femorale 6.57 Nervo mediano 6.57 Cornea 5.79 Sclera meridionale 3.77 Cartilagine tiroidea 26.2 Cartilagine costale 24.5
Tab. 4.7: Moduli di Young dei tessuti biologici di interesse
Confrontando le proprietà meccaniche, allo stato umido, degli scaffold studiati e i dati in tabella 4.7, si può dire che:
• le miscele di chitosano e gelatina possono rappresentare un valido biopolimeri nella rigenerazione sia del tessuto nervoso, sia di parte del sistema visivo (sclera e cornea), che della valvola tricuspide nonché della cartilagine.
• Il poliuretano in forma di film ottenuto per casting si adatta alla rigenerazione dei tendini, tuttavia variando la geometria della microstruttura è possibile modulare le proprietà meccaniche del polimero ed estendere il suo campo di applicazione anche alla rigenerazione del tessuto nervoso.
Bibliografia
[1] B. Angeli, Tesi di Laurea, Produzione e caratterizzazione di nuovi biomateriali e
loro utilizzo nella microfabbricazione di scaffolds per l’ingegneria tissutale , Anno
Accademico 2002-2003, pp. 18-19.
[2] M. F. Butler, Y.-F. Ng, P. D. A. Pudney, Mechanism and kinetics of the
crosslinking reaction between biololymers containing primary amine groups and genipin , Journal of Polymer Science: Part A: Polymer Chemistry, Vol. 41, pp.
3941-3953 (2003).
[3] W.-H. Chang, Y. Chang, P.-H. Lai, H.-W. Sung, A genipin-crosslinked gelatin
membrane as wound-dressing materials : in vitro and in vivo studies , Journal of
Biomaterials Science. Polymer Edition, Vol. 14, No. 5, pp. 481-495 (2003).
[4] F.-L. Mi, Y.-C. Tan, H.-C. Liang, R.-N. Huang, H.-W. Sung, In vitro evaluation
of chitosan membrane cross-linked with genipin , Journal of Biomaterials Science.
Polymer Edition, Vol. 12, No. 8, pp. 835-850 (2001).
[5] P. Calero, E. Jorge-Herrero, J. Turnay, N. Olmo, I. Lopez de Silanes, M.A. Lizarbe, M. Martin Maestro, B. Arenaz, J. L. Castillo-Olivares, Gelatines in soft
tissue biomateriali. Analysis of different crosslinking agents , Biomaterials 23 (2002),
pp. 3473-3478.
[6] I. S. Arvanitoyannis, A. Nakayama, S. Aiba, Chitosan and gelatin based edible
films : state diagrams, mechanical and permeation properties , Carbohydrate
Polymers 37 (1998), pp. 371-382.
[7] M. Cheng, J. Deng, F. Yang, Y. Gong, N. Zhao, X. Zhang, Study on physical
properties and nerve cell affinity of composite films from chitosan and gelatin solutions , Biomaterials 24 (2003), pp. 2871-2880.
[8] J. Kolarik, Simultaneous prediction of the modulus, tensile strength and gas
permeability of binary polymer blends , Eur. Polym. J. Vol. 34, No.5/6, pp. 585-590,
1998.
[9] J. Kolarik, A model for the yield strength of binary blends of thermoplastics , Polymer Vol. 35, No. 17, 1994, pp. 3631-3667.
[10] S.A. Berger, W. Goldsmith, E.R. Lewis, Introduction to Bioengineering , Oxford University Press, 1996, pp. 51-54.
[11] G. Vozzi, A. Previti, D. DE Rossi, A. Ahluwalia, Microsyringe-based deposition
of two-dimensional and three-dimensional polymer scaffolds with a well-defined geometry for application to Tissue Engineering , Tissue Engineering 2002 Dec. 8(6),
pp. 1089-1098.
[12] A. Marchetti, Appunti del corso di Proprietà fisiche e tecnologiche degli alti
polimeri , Università di Pisa, a.a. 2002/2003.
[13] H. Yamada, Strenght of biological materials , The Williams & Wilkins Company, Baltimore 1970.