III.
PAZIENTI,
MATERIALI
E METODI
1. I PAZIENTI
Sono stati analizzati i sieri di 3 pazienti (2 maschi e 1 femmina)
che presentano patologie renali croniche e sottoposti a trattamento
emodialitico. I prelievi sono stati fatti immediatamente prima del
trattamento di dialisi, i sieri sono stati aliquotati in volumi di 500μl, 100μl e 50μl e conservati a -20°C. Come riferimento (controllo) si è usato il siero di una persona non affetta da alcun tipo di patologia
renale.
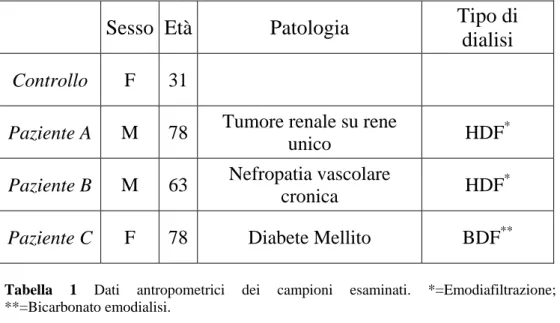
I dati antropometrici dei soggetti presi in considerazione sono
riportati in Tabella 1.
Sesso Età Patologia Tipo di
dialisi Controllo F 31
Paziente A M 78 Tumore renale su rene
unico HDF
*
Paziente B M 63 Nefropatia vascolare
cronica HDF
*
Paziente C F 78 Diabete Mellito BDF**
Tabella 1 Dati antropometrici dei campioni esaminati. *=Emodiafiltrazione;
**=Bicarbonato emodialisi.
2. MATERIALI
Tutti i prodotti chimici utilizzati in questo lavoro sono della
3. METODI
3.1 QUANTIFICAZIONE PROTEICA
La concentrazione proteica di ciascun campione è stata calcolata
utilizzando il reagente di Bradford [Bradford, 1976] e usando
ovoalbumina per la creazione della curva standard. Alternativamente
si è utilizzata la lettura a 280 nm dei campioni diluiti paragonando tra
loro i valori in modo proporzionale considerando, per semplicità,
ε280
mg/ml=1. Le quantità rilevate sono sempre espresse in mg/ml.
3.2 SDS-PAGE
Di ogni campione è stata fatta una corsa elettroforetica in
condizioni denaturanti secondo la procedura indicata da Laemmli
[Laemmli, 1970]. Il campione è stato opportunamente diluito con
l’SDS Reducing Buffer (0,5 M Tris-HCl, pH 6,8, 10% Glicerolo, 10%
SDS, 5% 2-β-mercapto-etanolo). In ogni lane di un gel avente lo spessore di 1mm sono state caricate uguali quantità di campione (15
μg). L’elettroforesi è stata effettuata utilizzando un apparecchiatura Mini-PROTEAN II (Bio-Rad Hercules, CA, USA) applicando un
3.3 ELETTROFORESI BIDIMENSIONALE
(3<pH<10)
La 2DE (Elettroforesi Bidimensionale) è stata effettuata secondo
Gorg e coautori [Gorg et al., 1988]. Un’aliquota, corrispondente a 80
μg di campione, è stata risospesa in 240μl di Rehidration Buffer (Urea 8M, CHAPS 2%, DTT 0,2%, IPG 0,8%, Pharmalyte pH 3-10 0,8% e
tracce di Blue di Bromofenolo). Il campione così preparato è stato
caricato su strip da 11cm (Immobiline DryStrip, pH 3-10 Amersham
Bioscience). L’IEF (Iso-Electro-Focusing) è stata effettuata per mezzo
di un apparecchio Multiphor (Amersham Biosciences) con 40000 V/h
a 15ºC.
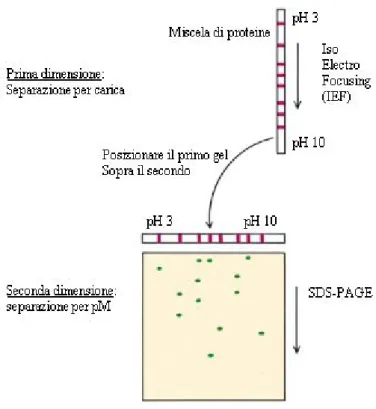
Fig. 6 Descrizione dei due tipi di separazione, per carica e per massa, che si susseguono
3.4 EQUILIBRATURA DELLE STRIP
Al termine dell’IEF, le strip sono state equilibrate per 8 minuti in
una soluzione 50 mM Tris-HCl, pH 8,8, Glicerolo 30%, Urea 6M,
SDS 4%, DTT 2% e per 12 minuti in una soluzione 50 mM Tris-HCl,
pH 6,8, Glicerolo 30% , Urea 6M, SDS 4%, Iodacetamide 2,5% e
tracce di Blue di Bromofenolo. La seconda dimensione è stata
effettuata in gel al 12%, o 15%, dello spessore di 1mm secondo il
protocollo di Laemmli [Laemmli, 1970].
3.5 COLORAZIONE DEI GEL
I gel sono stati colorati usando un protocollo Silver Stain
MALDI-TOF compatibile [Yan et al., 2000].
3.6 WESTERN BLOT
Ottanta μg di proteine separate attraverso 2DE sono state elettricamente trasferite su una membrana di poli-vinil-dien-fluoruro
(PVDF) (Hybond-P PVDF, Amersham Biosciences) attivata in
metanolo per 10 secondi, mediante l’utilizzo del Multiphor II
(Amersham Biosciences) applicando una corrente costante di 0,8
mA/cm2 di gel per la durata totale di un’ora.
L’equilibratura è stata effettuata con il metodo di Towbin: i fogli
Glicina 100mM e Metanolo al 5% (Cathodic Transfer Buffer), quelli
posti sull’anodo sono stati equilibrati in Tris 13mM, Glicina 100 mM
e Metanolo al 20% (Anodic Transfer Buffer). Il gel e la membrana
sono stati equilibrati in Tris 13 mM, Glicina 100 mM e Metanolo al
10% (Gel-PVDF Transfer Buffer).
3.7 IMMUNORIVELAZIONE
La membrana è stata saturata per un’ora in PBS (Tampone
Fosfato 5mM, NaCl 137mM, KCl 2,7mM) pH 7,5, Latte in polvere
scremato al 3%, Tween-20 allo 0,2%. In seguito la membrana di
PVDF è stata incubata tutta la notte a 4ºC con l’anticorpo primario
anti-HSA (DakoCytomation, Denmark). L’anticorpo è diluito 1000
volte in PBS pH 7,5, latte in polvere scremato al 3%, Tween-20 allo
0,2%.
Alla fine dell’incubazione sono stati effettuati quattro lavaggi
con PBS pH 7,5, latte in polvere scremato al 3%, Tween-20 allo 0,2%
ciascuno della durata di 10 minuti.
La membrana di PVDF è stata incubata per un’ora con anticorpo
secondario (Goat Anti-Rabbit IgG-HRP, Santa Cruz Biotechnology
Inc. California) diluito 1000 volte in PBS pH 7,5, latte in polvere
scremato al 3%, Tween-20 allo 0,2%. In seguito sono stati effettuati
PBS pH 7,5, latte in polvere scremato al 3%, Tween-20 allo 0,2% e
due lavaggi da 5 minuti ciascuno con PBS pH 7,5.
La reazione anticorpale è stata evidenziata trattando la
membrana con una Soluzione Cromogeno costituita da PBS pH 7,5,
4-cloro-1-naftolo 5M, Metanolo al 6% e Perossido di Idrogeno allo
0,025%.
3.8 ANALISI D’IMMAGINE
Le immagini dei gel e delle membrane di blotting sono state
acquisite attraverso l’uso di uno scanner piatto (Scanner Epson
Expression 1680 Pro). I dati acquisiti sono stati elaborati con l’ausilio
di opportuni software.
I gel delle elettroforesi monodimensionali sono stati elaborati
mediante il programma QuantityOne 4.2.3 (Bio-Rad Hercules, CA,
USA) che permette di avere una stima quantitativa dell’intensità di
ciascuna banda. Infatti la banda come appare sullo schermo del
computer è costituita da un insieme di pixel. Ciascun pixel ha una
coordinata X, una Y e un valore Z. Le coordinate X e Y indicano la
posizione in orizzontale e in verticale del pixel nell’immagine, e il
valore Z è l’intensità di segnale del pixel abbreviata come p.i. (Pixel
Intensity). L’intensità totale di una banda è data dalla somma delle
intensità di tutti i pixel che compongono la banda stessa. L’intensità
una sorgente di luce bianca l’unità dell’intensità del segnale
corrisponde alla Densità Ottica (O.D.). Nel linguaggio del software
tale densità ottica è definita come “intensità di volume”. Il volume è
dato dalla somma delle intensità dei singoli pixel moltiplicato per
l’area del pixel stesso e viene indicato, negli istogrammi riportati,
come Volume Percentuale.
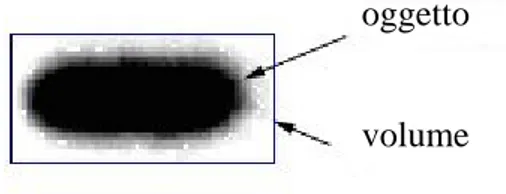
oggetto volume
Fig. 7 Illustrazione del volume considerato per il calcolo dell’intensità.
I gel delle elettroforesi bidimensionali sono stati elaborati
mediante il programma PD-Quest 6.2.1 (Bio-Rad Hercules, CA,
USA).
3.9 SPETTROMETRIA DI MASSA
Gli spot selezionati per l’identificazione sono stati analizzati
mediante Spettrometria di Massa MALDI-TOF presso il Laboratorio
di Proteomica Funzionale dell’Università di Siena.
Le fasi iniziali di questo processo consistono nella estrazione
dello spot dal gel, decolorazione, trattamento proteolitico (tripsina) ed
estrazione dei peptidi risultanti. Successivamente una aliquota di
della matrice e contemporanea ionizzazione degli analiti presenti nel
campione.
Gli ioni vengono accelerati da un campo magnetico all’interno di
un tubo dove viene fatto il vuoto. Il tempo che gli ioni impiegano per
attraversare questo tubo dipende dalla loro massa. Alla fine di tale
processo si ottiene una mappa delle masse dei peptidi triptici. I valori
delle masse ottenute dal campione sono paragonati con i valori delle
masse generate dalla digestione teorica della proteine presenti nel
database. In tal modo verrà fornita una lista delle proteine che hanno
una maggior percentuale di appaiamento col campione ignoto [Pierce