1
3.RISULTATI
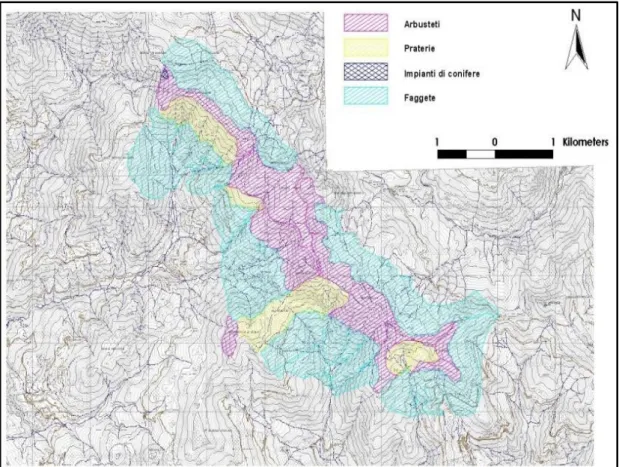
3.1 CARTA DELLA VEGETAZIONE
L’area che è stata rilevata va dal Passo della Focerella (1700 m) a nord, al Passo delle Forbici (1574 m) a sud.
La mappa (Fig. 3.1) che è stata realizzata indica la fisionomia vegetale dell’area del crinale e fornisce indicazioni utili all’individuazione delle zone maggiormente vocate alle specie ornitiche prese in considerazione.
2
Nella mappa sono individuate le 4 principali formazioni che costituiscono la
fisionomia del paesaggio vegetale del crinale appenninico:
Arbusteti
Praterie
Faggete
Impianti di conifer
Arbusteti
Formazioni tipiche delle zone poste al di sopra del limite superiore della faggeta
(1700 m). Sono caratterizzate dalla presenza di frutici (Ginepro nano) e suffrutici
(Mirtilli) che si elevano dal suolo per circa mezzo metro, formando densi
popolamenti che si diradano salendo verso la parti alte del crinale (Foto 1).
3
La composizione floristica comprende Calluna vulgaris, varie specie di Vaccinium
(V. gaultherioides e V. myrtillus) e Juniperus nana con la sua tipica forma prostrata
Negli arbusteti dell’area presa in esame è presente anche una stazione relitta di Rododendro (Rhododendron ferrugineum) (Foto 5) lungo il versante S-O del Monte
Vecchio.
FOTO 2: CALLUNA FOTO 3: MIRTILLO
FOTO 5: RODODENDRO FOTO 4: GINEPRO NANO
4 Praterie
Si sviluppano in maniere discontinua lungo il crinale, oltre il limite della faggeta, in
sostituzione degli arbusteti, ai quali si intercalano, sia per motivi naturali ma più
spesso, per motivi legati alle pratiche agro-pastorali .
Le praterie sono costituite da un tappeto piuttosto uniforme di specie erbacee per lo
più graminoidi (Foto 6) come Brachypodium genuense, Nardus stricta, Festuca
paniculata, oltre a specie di famiglie differenti come Alchemilla saxatilis e Luzula multiflora.
Foto 6: Prateria presso Bocca di Scala
5 Faggete
I boschi di faggio si estendono uniformemente fino a circa 1700 m di altitudine e
rappresentano le formazioni arboree più estese.
La faggeta in passato è stata intensamente interessata da interventi di ceduazione
anche se in anni recenti si è avviata la riconversione ad alto fusto.
Questo fatto è evidente salendo verso il crinale dove prima, si attraversano aree
goverante ad alto fusto (Foto 7), poi gradualmente altre governate a ceduo (Foto 8).
La faggeta forma popolamenti densi dove le altre entità floristiche sono rare o legate
ad impianti artificiali di conifere o latifoglie.
6 Impianti di conifere
L’impianto di conifere (Pinus mugo) si presenta come una formazione compatta e ben delimitata con alberi di altezza assai modesta e con le chiome dal portamento
tendenzialmente prostrato a seguire l’andamento del crinale (Foto 9).
7
Per comodità descrittiva l’area verrà suddivisa in quattro parti: 1) La Focerella- Monte Prado
2) Monte Prado – Monte Vecchio
3) Monte Vecchio – Monte Cella
4) Monte Cella – Passo le Forbici
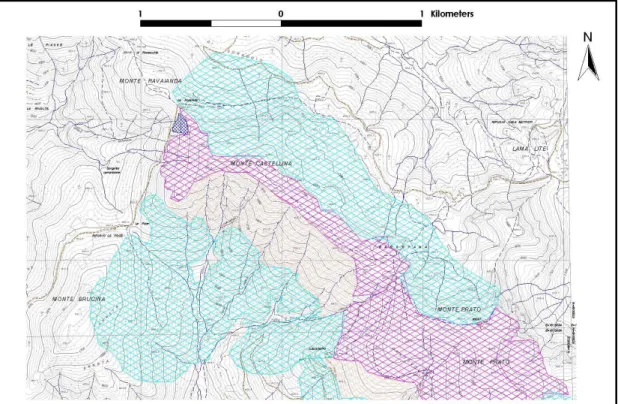
La Focerella – Monte Prado
Fig. 3.2: La Focerella - Monte Prado
La copertura vegetale rilevata (Fig. 3.2), rispecchia in modo sostanzialmente
invariato quella descritta nella carta di Tomei et al. (1990).
Le formazioni arbustive si allungano sul crinale sia dal lato emiliano che da quello
toscano e le praterie si estendono per un’area pressoché uguale a quella già
8
L’unica interessante differenza rilevata è la presenza, nelle vicinanze della Focerella, nel versante sud del Monte Castellino, di un’ ampia zona boscata a conifere di
impianto recente.
Questa formazione può assumere un notevole significato in funzione della fruizione
da parte della comunità ornitica, specialmente di quella componente più strettamente
legata ad ambienti arborei prima assenti.
9
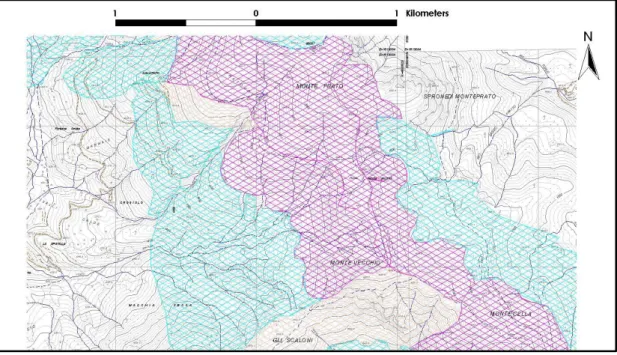
Monte Prado – Monte Vecchio
Fig. 3.3: Monte Prado - Monte Vecchio
Scendendo lungo il crinale verso sud (Fig. 3.3), dominano le formazioni arbustive
che, in corrispondenza del Monte Prado (versante toscano), si estendono verso il
basso fino al limite del faggio (circa 1700 m).
Attorno al rifugio Prado (1700 m ) è presente una zona a prateria, già rilevata nella
carta di Tomei et al. (1990), che sembra aver subito un ampliamento a seguito del
pascolo ovino che si attua in questa zona durante il periodo estivo.
Il tratto di crinale che arriva fino al Monte Vecchio presenta ancora le formazioni
10
11
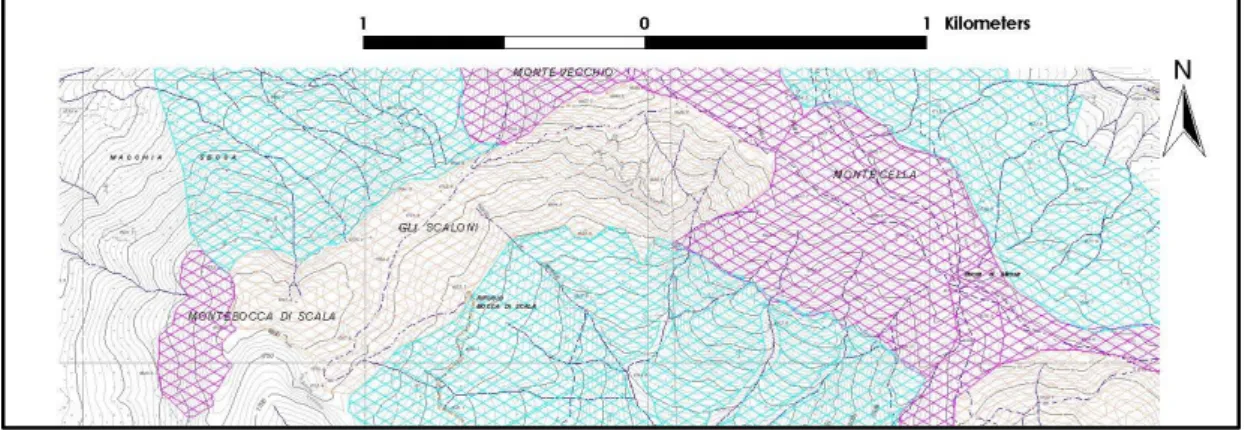
Monte Vecchio – Monte Cella
Fig. 3.4: Monte Vecchio – Monte Cella
Anche in questo tratto (Fig. 3.4) sono presenti gli arbusteti e un’ampia prateria a
graminacee che, rispetto alla carta del 1990, risulta maggiormente estesa fino ad
occupare il versante est del Monte Bocca di Scala (1846 m), tutto il versante
sud-est degli Scaloni fino al crinale in corrispondenza del Monte Cella (1946 m).
Questa maggiore estensione della prateria è dovuta agli interventi effettuati per il
Progetto LIFE, che ha ridotto gli arbusteti a favore delle praterie da pascolo le quali
però presentano evidenti segni di degradazione (testimoniata dalla presenza di specie
di scarso valore pabulare come Carlina acaulis).
Sul lato emiliano invece è presente, lungo i versanti nord-est, una distesa quasi
continua di arbusteti (con prevalenza di calluna e mirtilli) che vanno a terminare al
12
Foto 12: Versante sud-est Monte Cella
Foto 13::Carlina acaulis
13
Monte Cella – Le Forbici
Fig. 3.5: Monte Cella – Le Forbici
In questo tratto (Fig. 3.5) sono state rilevate marcate differenze rispetto alla carta
esistente.
Essa indica una presenza continua di arbusteti fino oltre le Forbici, che termina al
limite della faggeta.
14
Nel corso delle escursioni è stata invece rilevata un’ampia distesa di prateria a
graminacee nell’area attorno al rifugio Cella (1654 m) dovuta agli interventi effettuati nell’ambito del progetto LIFE che hanno ridisegnato la fisionomia vegetazionale dell’area.
Foto 16: Rifugio Cella
Verso le Forbici, il versante sud presenta ancora praterie che lasciano poi il posto agli
arbusti, che arrivano fino al limite della faggeta sia sul versante toscano che
15
Concludendo, le differenze maggiori tra la situazione constatata e la carta di Tomei
et al. (1990) si riscontrano in due zone, Monte Bocca di Scala e Monte Cella, che
sono state interessate dagli interventi del Progetto LIFE per la conservazione delle praterie montane dell’Appennino toscano (inizio anni 2000).
Monte Bocca di Scala
In questa zona la prateria presenta una maggiore estensione (Fig.3.6) rispetto alla
carta di Tomei (Fig. 3.7)
16
Fig.3.7: Monte Bocca di Scala, carta Tomei
17
Monte Cella
Questa è la zona dove sono state riscontrate le maggiori differenze rispetto alla carta
di Tomei et al..(1990)
Qui (Fig. 3.8) infatti è presente una estesa prateria che nella carta precedente (Fig.
3.9) non era stata cartografata
Fig. 3.8: Monte Cella
18
3.2 LA COMUNITA’ ORNITICA
3.2.1 Check list degli uccelli presenti nell’area di studio
Una volta individuati i tipi di habitat presenti nell’area di studio, il passo successivo è
stato quello di elencare le specie di avifauna che insistono in varia misura in essa; per
fare questo, è stato preso come riferimento l’ ”Atlante degli uccelli nidificanti e svernanti in Toscana” (Tellini et al., 1997) nonché notizie reperibili in Costa et al. (1998) riguardanti le comunità ornitiche presenti in Emilia Romagna.
La Tavola I presenta le specie che per loro modello di distribuzione durante la
nidificazione o lo svernamento sono risultate presenti nel territorio dell’aerea di
studio.
La tabella è organizzata nel modo seguente :
nella prima colonna vengono indicati l’Ordine e la Famiglia;
nella seconda il numero progressivo;
nella terza il Codice Euring;
nella quarta il nome comune
nella quinta il nome scientifico
nella sesta la fenologia, con cui si indica la possibile presenza sul territorio, delle varie specie di uccelli durante i diversi periodi dell’anno;
nella settima viene indicata la categoria SPEC;
nell’ottava le indicazioni sullo stato delle popolazioni secondo Birdlife International;
19 nella nona lo stato di minaccia in Italia secondo le categorie IUCN ricavate dal “Lista Rossa 2011degli Uccelli Nidificanti in Italia” (Peronace et al., 2012);
nella decima lo stato di minaccia a livello toscano secondo Sposimo e Tellini (1995).
I
TAVOLA I : CHECK LIST DEGLI UCCELLI PRESENTI NELL’AREA DI STUDIO (VEDI TESTO PER L’INDICAZIONE DELLE SIGLE)
Cod. Euring Nome comune Nome scientifico Fenologia SPEC Birdlife L.R.I. L.R.T.
1) Accipitriformes 1. Accipitridae
001 02310 Falco pecchiaiolo Pernis apivorus B,T Non SPECE Secure LC N
002 02690 Sparviere Accipiter nisus B,T,W Non SPEC Secure LC N
003 02870 Poiana Buteo buteo B,T,W Non SPEC Secure LC N
004 02960 Aquila reale Aquila chrysaetos B,W SPEC 3 Rare NT C
2) Falconiformes
2. Falconidae
005 03040 Gheppio Falco tinnunculus B,T,W SPEC 3 Declining LC B*
3) Galliformes
3.Phasianidae
006 03580 Pernice rossa Alectoris rufa B SPEC 2 Declining DD F
007 03670 Starna Perdix perdix B SPEC 3 Vulnerable LC F
008 03700 Quaglia Coturnix coturnix B,T SPEC 3 Depleted DD B*
009 03940 Fagiano comune Phasianus colchicus B Non SPEC Secure N
4) Columbiformes
4.Columbidae
010 06870 Tortora Streptopelia turtur B,T SPEC 3 Declining LC N
5) Cuculiformes
5.Cuculidae
II
6) Strigiformes
6.Tytonidae
012 07350 Barbagianni Tyto alba B SPEC 3 Declining LC N
7.Strigidae
013 07570 Civetta Athene noctua B SPEC 3 Declining LC N
014 07610 Allocco Strix aluco B Non SPECE Secure LC N
015 07670 Gufo comune Asio otus B,T Non SPEC Secure LC N
7)Caprimulgiformes 8. Caprimulgidae
016 07780 Succiacapre Caprimulgus europaeus B,T SPEC 2 Depleted LC N
8) Apodiformes
9.Apodidae
017 07950 Rondone Apus apus B,T Non SPEC Secure LC N
9) Coraciiformes
10.Upupidae
018 08460 Upupa Upupa epops B,T SPEC 3 Declining LC N
10) Piciformes
11.Picidae
019 08480 Torcicollo Jynx torquilla B,T SPEC 3 Declining EN N
020 08560 Picchio verde Picus viridis B,W SPEC 2 Depleted LC N
021 08760
Picchio rosso
maggiore Dendrocopos major B,W Non SPEC Secure LC N
11) Passeriformes
12.Alaudidae
III
023 09760 Allodola Alauda arvensis B,T SPEC 3 Depleted VU N
13.Hirundinidae
024 09910 Rondine montana Ptyonoprogne rupestris B,T Non SPEC Secure LC N
025 09920 Rondine Hirundo rustica B,T SPEC 3 Depleted NT N
026 10010 Balestruccio Delichon urbicum B,T SPEC 3 Declining NT N
14.Motacillidae
027 10050 Calandro Anthus campestris B,T SPEC 3 Declining LC B*
028 10090 Prispolone Anthus trivialis B,T Non SPEC Secure LC N
029 10110 Pispola Anthus pratensis T,W Non SPECE Secure NA
030 10140 Spioncello Anthus spinoletta B,T,W Non SPEC Secure LC N
031 10190 Ballerina gialla Motacilla cinerea B,T Non SPEC Secure LC N
032 10200 Ballerina bianca Motacilla alba B Non SPEC Secure LC N
15.Cinclidae
033 10500 Merlo acquaiolo Cinclus cinclus B Non SPEC Secure LC N
16.Troglodytidae
034 10660 Scricciolo Troglodytes troglodytes B Non SPEC Secure LC N
17.Prunellidae
035 10840 Passera scopaiola Prunella modularis B,T Non SPECE Secure LC N
036 10940 Sordone Prunella collaris B,T Non SPEC Secure LC C
18.Turdidae
037 10990 Pettirosso Erithacus rubecula B,T,W Non SPECE Secure LC N
038 11040 Usignolo Luscinia megarhynchos B,T Non SPECE Secure LC N
039 11210
Codirosso
spazzacamino Phoenicurus ochruros B,T,W Non SPEC Secure LC N
040 11220 Codirosso Phoenicurus phoenicurus B,T SPEC 2 Depleted LC N
041 11390 Saltimpalo Saxicola torquata B,W Non SPEC Secure VU N
042 11460 Culbianco Oenanthe oenanthe B,T SPEC 3 Declining NT B
IV
044 11870 Merlo Turdus merula B,W Non SPECE Secure LC N
045 11980 Cesena Turdus pilaris T,W Non SPECEw Secure NT
046 12000 Tordo bottaccio Turdus philomelos B,T Non SPECE Secure LC N
047 12010 Tordo sassello Turdus iliacus T,W Non SPECEw Secure NA
048 12020 Tordela Turdus viscivorus B,T,W Non SPECE Secure LC N
19.Sylviidae
049 12200 Usignolo di fiume Cettia cetti B Non SPEC Secure LC N
050 12670 Occhiocotto Sylvia melanocephala W Non SPECE Secure LC N
051 12760 Beccafico Sylvia borin B,T Non SPECE Secure LC N
052 12770 Capinera Sylvia atricapilla B,W Non SPECE Secure LC N
053 13070 Luì bianco Phylloscopus bonelli B,T SPEC 2 Declining LC N
054 13110 Luì piccolo Phylloscopus collybita B,T Non SPEC Secure LC N
055 13140 Regolo Regulus regulus T,W Non SPECE Secure NT N
056 13150 Fiorrancino Regulus ignicapillus B,T,W Non SPECE Secure LC N
20.Muscicapidae
057 13350 Pigliamosche Muscicapa striata B,T SPEC 3 Declining LC N
21.Aegithalidae
058 14370 Codibugnolo Aegithalos caudatus B,W Non SPEC Secure LC N
22.Paridae
059 14400 Cincia bigia Poecile palustris B,W SPEC 3 Declining LC N
060 14610 Cincia mora Periparus ater B,W Non SPEC Secure LC N
061 14620 Cinciarella Cyanistes caeruleus B,W Non SPECE Secure LC N
062 14640 Cinciallegra Parus major B,W Non SPEC Secure LC N
23.Sittidae
063 14790 Picchio muratore Sitta europaea B Non SPEC Secure LC N
V
24.Tichodromadidae
064 14820 Picchio muraiolo Tichodroma muraria B,W Non SPEC Secure LC C
25.Certhiidae
065 14870 Rampichino Certhia brachydactyla B Non SPECE Secure LC N
26.Oriolidae
066 15080 Rigogolo Oriolus oriolus B,T Non SPEC Secure LC N
27.Laniidae
067 15150 Averla piccola Lanius collurio B,T SPEC 3 Depleted VU N
28.Corvidae
068 15390 Ghiandaia Garrulus glandarius B,W Non SPEC Secure LC N
069 15600 Taccola Corvus monedula B,W Non SPECE Secure LC N
070 15670 Cornacchia grigia Corvus corone cornix B,W Non SPEC Secure LC N
29.Sturnidae
071 15820 Storno Sturnus vulgaris B,T SPEC 3 Declining LC N
30.Passeridae
072 15912 Passera d'Italia Passer italiae B,W VU N
073 15980 Passera mattugia Passer montanus B,W SPEC 3 Declining VU N
31.Fringillidae
074 16360 Fringuello Fringilla coelebs B,T,W Non SPECE Secure LC N
075 16380 Peppola Fringilla montifringilla T,W Non SPEC Secure LC
076 16400 Verzellino Serinus serinus B,T Non SPECE Secure LC N
077 16490 Verdone Carduelis chloris B,T,W Non SPECE Secure NT N
078 16530 Cardellino Carduelis carduelis B,T,W Non SPEC Secure NT N
079 16540 Lucarino Carduelis spinus T,W Non SPECE Secure LC E
080 16600 Fanello Carduelis cannabina B,T SPEC 2 Declining NT N
081 17100 Ciuffolotto Pyrrhula pyrrhula B,W Non SPEC Secure VU N
082 17170 Frosone
Coccothraustes
VI
32.Emberizidae
083 18570 Zigolo giallo Emberiza citrinella B,T Non SPECE Secure LC D
084 18580 Zigolo nero Emberiza cirlus B Non SPECE Secure LC N
085 18600 Zigolo muciatto Emberiza cia B SPEC 3 Depleted LC N
7
La comunità ornitica risulta pertanto composta da 86 specie, di cui 65 Passeriformi (76%) e 21 Non
Passeriformi (24%).
I Non Passeriformi, oggetto del presente lavoro, sono stati a loro volta ripartiti in diverse categorie
fenologiche attraverso le quali, si è potuto evidenziare il loro status all'interno del territorio di
studio, che è risultata la seguente (Fig. 3.10):
Nidificanti (B) : 28,6%
Nidificanti, Migratori (B, T) : 42,9%
Nidificanti, Migratori, Svernanti ( B, T, W) : 14,3 %
Nidificanti , Svernanti ( B, W) : 14,3% 28,6% 42,9% 14,3% 14,3% B B,T B,T,W B, W
Fig. 3.10: Composizione fenologica della comunità dei Non Passeriformi
Per quanto riguarda la categoria fenologica B, T, W c'è da dire che W ( wintering) sta ad indicare
individui la cui presenza non sembra assimilabile ad un vero e proprio svernamentoma
8
Su un totale di 21 specie presenti nella check list, le categorie SPEC sono cosi rappresentate ( Fig.
3.11) - SPEC 1 : nessuna - SPEC 2 : 14,3% - SPEC 3 : 42,9% - NON SPEC E : 9,5% - NON SPEC : 33,3%
Fig.3.11: Composizione categorie SPEC della comunità dei Non Passeriformi 14,3% 42,9% 9,5% 33,3% SPEC 2 SPEC 3 NON SPEC E NON SPEC
9
La figura 3.13 rappresenta invece il numero di specie, che in accordo in Birdlife International
(2004), possono rientrare nei differenti trend popolazionistici individuati:
- SECURE : 47,6% - DECLINING : 33,3% - DEPLETED : 9,5% - VULNERABLE : 4,8% - RARE : 4,8% 47,6% 33,3% 9,5% 4,8% 4,8% 0% 10% 20% 30% 40% 50% SECURE DECLINING DEPLETED VULNERABLE RARE
SECURE DECLINING DEPLETED VULNERABLE RARE
10
Lo stato di minaccia in Italia indicato secondo la Lista Rossa 2011 (Peronace et al., 2012), per
quello che riguarda i non passeriformi, è rappresentato nella fig 3.13
78,9% 10,5%
5,3% 5,3%
0% 20% 40% 60% 80% 100%
A Minor Preoccupazione (LC) Dati Insufficienti (DD) Quasi Minacciato (NT) In Pericolo (EN)
Fig 3.13:.Stato di minaccia dei non passeriformi in Italia
Lo stato di minaccia in Toscana ricavato dalla Lista Rossa Toscana di Sposimo e Tellini (1995) per
quello che riguarda i non passeriformi è rappresentato invece nella figura 3.14.
76,2% 9,5%
9,5% 4,8%
0% 10% 20% 30% 40% 50% 60% 70% 80%
Attualmente non minacciate (N)
Popolazioni autoctone minacciate da inquinamento genetico (F) Mediamente Vulnerabili (B*)
Rare ( C )
11
3.2.2 Schede descrittive delle specie legate agli ambienti montani
Qui di seguito vengono presentate una serie di schede relative ai caratteri distributivi, ecologici e
conservazionistici delle specie più caratteristicamente legate agli ambienti aperti montani, in
accordo con quanto riportato in Meschini e Frugis, (1993), Tellini et al., (1997), Lombardi et al.
(1998)., Brichetti e Fracasso, (2004), Birdlife International, (2004).
AQUILA REALE Aquila chrysaetos
Distribuzione e fenologia
Specie politipica a distribuzione oloartica.Nella Regione paleoartica occid: 2 sottospecie di cui
chrysaetos interessa l'Italia.Popolazione europea: 6600-12000 cp di cui 1000-5000 in Turchia
12
In Italia nidificano 300-400 coppie con una distribuzione continua sull'arco alpino, nell' Appennino
centrale e nella Sardegna orientale, piu localizzata nell' Appennino Tosco-Emiliano, in quello
meridionale e in Sicilia (Meschini e Frugis, 1993)
Nell'Appennino Tosco-Emiliano viene indicata la presenza di 8-14 coppie nidificanti, mentre pe la
Toscana Sposimo e Tellini, (1995) stimano 7-9 coppie di Aquila reale ( Lombardi et al., 1998)
Nell'Appennino Tosco-Emiliano il teritorio di ogni coppia è di circa 80 Km2, e i siti di nidificazione
sugli Appennini stanno tra loro in media 20 Km.
13
Esigenze ecologiche
Tipica specie di ambienti di altitudine, nidifica quasi esclusivamente su pareti rocciose, dove ogni
coppia ha a disposizione diversi nidi, piu o meno vicini tra loro, mentre necessita di estese paterie
per i territori di alimentazione.
Sulle Alpi i siti riproduttivi sono posti tra 800 e 2300 m di quota, sugli Appennini tra 300 e 1400 m
( Lombardi et al. , 1998)
L'Aquila caccia principalmente mammiferi di piccole e medie dimensioni (sull' Appennino
soprattutto la lepre), uccelli di medie e grossi dimensioni (fagiani, pernici, ecc.), rettili e anfibi
(Lombardi et al., 1998).
Movimenti e svernamento
Adulti normalmente sedentari, giovani e immaturi dispersivi, con movimenti abituali da fine
settembre-ottobre di qualche decine di chilometri nell'ambito dell'area riproduttiva ma anche verso
aree pedemontane e pianeggianti limitrofe, svernante localizzata (Lombardi et al., 1998)
Status e conservazione
A scala europea la specie è considerata rara e classificata come SPEC 3.
Attualmente in Italia la specie non sembra correre pericolo, ed il suo status è sicuramente
migliorato, specilamente sulle Alpi (Lombardi et al.,1998) e anche in Toscana negli ultimi hanni ha
fatto registrare un' espansione sia numerica che di areale anche se per l'esiguità della popolazioneè
stata inserita nella Lista Rossa fra le specie rare (Sposimo e Tellini, 1995).
Viene considerata nella L.R.I ( Peronace et al, 2012) una specie quasi minacciata (NT) , quindi
come specie prossima a qualificarsi per una categoria di minaccia.
14
Tra le minacce più comuni: trasformazioni ambientali, uccisioni illegali, avvelenamento indiretto,
aperture di strade nei siti riprodutivi, disturbo antropico sulle pareti di nidificazione (Bricchetti e
Fracasso, 2004)
Nell'area di indagine l'Aquila reale subisce il disturbo, con effetti negativi non quantificabili, delle
attività agricole e turistiche (nei territori di caccia) e dell'arrampicata sportiva (nei siti riproduttivi) (
Lombardi et al., 1998).
Fig.3.16:Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993)
15
Sull'Appennino la specie è presente con 3 coppie, due dei siti di nidificazione, utilizzati più o meno
con continuità, sono notissimi, e sembrano del tutto sicuri in quanto compresi in Riserve Statali ben
controllate.
Sull'Appennino si ha avuto negli ultimi anni un incremento di numero di coppie nidificanti, motivo
di questo incremento è da ricercare nella riduzione degli abbattimenti illegali, che peraltro ancora
sussistono, e l'incremento delle prede, nel caso dell'Appennino all'aumento della Marmotta
16
POIANA Buteo buteo
Distribuzione e fenologia
Specie politipica a distribuzione euroasiatica. Migratrice, sedentaria e dispersiva ( Brichetti e
Fracasso, 2004)
In Italia nidificano 2500-5000 coppie distribuite in modo pressocchè omogeneo su tutto il territorio
nazionale (Meschini e Frugis, 1993).
Anche in Toscana la specie è ben distribuita, con una popolazione stimata superiore alle 200 coppie,
17
Fig.3.17 Andamento della popolazione in Europa (Birdlife Int, 2004)
Esigenze ecologiche
Quasi ubiquitaria, risultando assente solo nelle zone piu intensamente antropizzate, la Poiana è piu
frequente in ambienti boscati alternati a zone aperte in media montagna, tra i 500 e i 1500 m di
altitudine, soprattuto in periodo riproduttivo.
Il nido viene costruito tra marzo e l'inizio di aprile per lo piu su alberi ad alto fusto.
Nella ricerca di cibo frequenta anche praterie d'alta quots, specialmente se prossime ad ambienti
boscati; si ciba di invertebrati, rettili, uccelli e mammiferi, ma anche di pesci e anfibi.
Movimenti e migrazioni
Migratrice regolare. Movimenti tra settembre-inzio novembre e marzo-maggio. Localmente erratica
in periodo invernale .
Svernante regolare. popolazione difficilmente stimabile in quanto compoata da individui sedentari e
da un numero sconosciuto di migratori.In toscana valutati 2000-5000 ind. svernanti.
Negli inverni miti lo svernamento appare regolare anche in zone montuose fino oltre 2000 m (
18
Status e conservazione
Specie classificata come Non SPEC , a scala europea è considerata sicura .
La specie non sembra in alcun modo minacciata , classificata secondo la Lista Rossa degli Uccelli
Nidificanti in Italia (Peronace et al.,2012) come specie a minor preoccupazione , anche nella Lista
rossa Toscana (Sposimo e Tellini,1995) risulta essere in nessun modo minacciata.
Fig. 31.8:.Presenza della specie in Italia come nidificante (Meschini e Frugis, 1993) Distribuzione sull’Appennino Tosco-Emiliano
La Poiana frequenta gli ambienti di altitudine solo per la ricerca del cibo, quindi in generale sembra
che a quote elevate le praterie siano scarsamente utilizzate , mentre al di sotto degli 800-1000 m la
specie appare comune e diffusa ( Lombardi et al., 1998).
Nell'Appennino , forse per il grande sviluppo lineare dell'ecotone boschi-praterie , che si ritrova a
19
SPERVIERE Accipiter nisus
Distribuzione e fenologia
Specie politipica a distribuzione oleopaleoartica. Popolazione europea 280000-380000 cp.
Migratrice, sedentaria e dispersiva. Sverna a sud dell'areale fino al nord Africa e Medio oriente .
In Italia è sedentaria e nidificante sulla penisola e in Sicilia, con presenze localizzate in Pianura
Padana ( Lombardi et al., 1998) .
Esigenze ecologiche
Nidifica in complessi boscosi diversificati, collinari e montani, prediligendo quelli fitti con alberi di
media grandezza, radurati e circondati da aree aperte, naturali o coltivate, utilizzate per cacciare. Piu
diffusa tra 550-1600 m, scarsa e localizzata in pianura. In migrazione e svernamento frequenta
anche zone urbane e suburbane,corsi fluviali, margini di zone umide, fondovalle e praterie montane
20
Fig.3.19 Andamento della popolazione in Europa (Birdlife Int., 2004)
Movimenti e migrazioni
Migratrice regolare. Movimenti tra settembre-ottobre con anticipi da agosto e ritardi fino a inizio
novembre e tra marzo e aprile, con ritardi fino a metà maggio.Giovani più tardivi degli adulti.
Svernante regolare. Popolazione difficilmente stimabile in quanto composta da individui sedentari e
da un numero sconosciuto di migratori ( Lombardi et al., 1998).
Status e conservazione
La specie é classificata come Non SPEC, ritenuta a livello europeo sicura ( Birdilife Int., 2004).
Inserita nella Lista Rossa Italiana (Peronace et al., 2012) come Specie a Minor Preoccupazione,
21
Fig.3.20. Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993)
Distribuzione in Appennino Tosco-Emiliano
La distribuzione della specie risulta verosimilmente sottostimata, forse per la non facile rilevabilità
della specie.
Pare anzi che lo Sparviero, con la Poiana e il Gheppio, sia il rapace diurno più diffuso in toscana. La
sua presenza è concentrata nei maggiori complessi forestali, tra cui Lunigiana, Garfagnana, Alpi
22
FALCO PECCHIAIOLO Pernis apivorus
Distribuzione e fenologia
Specie monotipica a distribuzione europea. Sverna principalmente nelle zone equatoriali dell'Africa
occidentale e centrale, secondariamente in quella orientale e meridionale. (Brichetti e Fracasso,
2004)
In Italia è migratrice nidificante (estiva). Piu comune e diffusa sulle Alpi, ancora ben rappresentata
sull'Appennino settentrionale, più scarsa o localizzta in quello centro-meridionale; rara e localizzata
nella Pianura Padana, Puglia e in alcune areedell'Appennino centro-meridionale.(Brichetti e
Fracasso, 2004)
Esigenze ecologiche
Nidifica in zone boscate diversificate, anche di scarsa estensione, di latifoglie e conifere pure o
23
Predilige castagneti e faggete, nidifica sugli alberi, a 10-20 m di altezza.( Brichetti e Fracasso,
2004)
I territori di alimentazione si estendono per circa 10 km2 e sono rappresentati da tutti gli ambienti
più o meno aperti posti in prossimità del sito riproduttivo (radure boschive, coltivi e pascoli, boschi
aperti e luminosi) nella tarda estate si spinge anche nelle praterie d'alta quota, fino a 1800 m
(Meschini e Frugis, 1993).
Nidificante tra 0-1500 m, con maggiore diffusione tra 400-1000 m. In migrazione frequenta anche
campagne alberate e zone suburbane.( Lombardi et al., 1998)
Fig.3.21 Andamento della popolazione in Europa (Birdlife Int., 2004)
Movimenti e migrazioni
Migratrice regolare. Movimenti tra metà gosto-ottobre e metà aprile-metà giugno; sporadici in
febbraio-marzo novembre. Giovani più tardivi degli adulti.
24
Status e conservazione
Considerata sicura a livello europeo classificata infatti come specie Non SPECE , specie con status
di conservazione europeo favorevole, concentrata in Europa
( Birdlife Int., 2004).
In Italia e in Toscana la specie non sembra attualmente minacciata, nonostante che tuttora persista ,
soprattuto in provincia di Reggio Calabria, l'usanza di abbattere individui della specie durante la
migrazione primaverile (Brichetti e Fracasso, 2004).
Tra le minaccie più comuni : distruzione e trasformazione di habitat di riproduzione e
alimentazione; uccisioni illegali durante la migrazione ( Lombardi et al., 1998)
Inserita nella Direttiva Uccelli allegato I.
Fig.3.22. Presenza della specie in Italia come nidificante (da Meschini e Fregi, 1993)
25
In Toscana la distribuzione del Pecchiaiolo interessa principalmente la dorsale appenninicadal
pistoiese all'aretino e i rilievi centro meridionali dalle Colline Metallifere alla zona amiatina (
26
GHEPPIO Falco tinnunculus
Distribuzione e fenologia
Specie politipica a distribuzione paleoartico-paleotropicale (Brichetti e Fracasso, 2004), Nella
regione paleoartica occidentale si hanno 6 sottospecie di cui tinnunculus interessa l'Italia.
Parzialmente migratrice e dispersiva; popolazioni meridionali e insulari sedentarie. Sverna in una
vasta area compresa tra l'Europa nord-occidentale e l'africa centrale; regolari le presenze in
Mediterraneo e Medio Oriente.
In Italia è sedentaria e nidificante in tutto il paese comprese piccole e grandi isole; migratrice nelle
aree montane. Non ugualmente distribuita. Più frequente nelle regioni centro-meridionali e insulari.
In Italia nidificano 5000-10000 coppie, distribuite su tutto il territorio nazionale eccetto la Pianura
Padana, a causa dei sistemi intensivi di coltivazione..
In toscana la consistenza della popolazione nidificante è stimata in 200-500 coppie distribuite in
tutta la regione con l'eccezione delle zone planiziali piu antropizzate e dei più estesi complessi
27
Esigenze ecologiche
Nidifica negli ambienti più disparati, da zone rupestri e forestali aperte, a quelle rurali e urbane.
Preferisce zone rocciose o alberate ricche di ampi spazi erbosi aperti (praterie, pascoli, steppe
cerealicole, incolti) utilizzati per cacciare.
Diffusa dal livello del mare fino a 2000 m .In svernamento risulta maggiormente legata ad ambienti
di media e bassa quota, con osservazioni più frequenti sotto i 1500-1600 m. ( Lombardi et al., 1998)
28
Movimenti e migrazioni
Migratrice regolare. Movimenti tra agosto-novembre e fine febbraio-inizio giugno.
popolazione italiana prevalentemente sedentaria, con movimenti di erratismo autunno-invernali in
senso verticale nelle aree montane ( Alpi in particolare) o nelle regioni settentrionaliin
concomitanza con condizioni metereologiche particolarmente sfavorevoli( persistente
innevamento).( Brichetti e Fracasso, 2004)
Svernante regolare . popolazione difficilmente stimabile in quanto composta da individui sedentari
e da un numero sconosciuto di migratori, ma verosimilmente superiore a 20000 individui, in
Toscana stimati 600-2000 ind.(Tellini et al., 1997)
Status e conservazione
A livello europeo è considerata una specie in diminuzione, DECLINING, specie le cui popolazioni
sono diminuite più del 10 %nel periodo 1990-2000 ( Birdlife Int., 2004), rientra pertanto nella
categoria SPEC 3, come specie con uno stato di conservazione sfavorevole.
A livello italiano la specie non sembra minacciata e rientra nella categoria a minor preoccupazione
nella Lista rossa 2011 ( Peronace et al.,2012).
A scala regionale invece la specie è ritenuta in declino ( Sposimo e Tellini, 1995), principalmente a
causa dell?alterazione e della scomparsa dell'habitat specifico in conseguenza dei cambiamenti in
atto nel paesaggio agropastorale (Lombardi et al., 1998). E' inserita nella Lista Rossa toscana nella
categoria B* Mediamente Vulnerabile, specie in cui le popolazioni in Toscana sono in diminuzione
in alcune aree; rischiano di subire contrazione di areale e di entrare nella categoria delle specie
29
Fig.3.24. Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993)
Distribuzione in Appennino Tosco-Emiliano
Sull'Appennino il Gheppio sembra avere una frequenza leggermente inferiore a quella delle
Apuane, forse per la minor disponibilità di idonei siti di nidificazione: gli ambienti rocciosi soo
assai piu ridotti in numero ed estensione .
le osservazioni ricadono sia nelle aree di alimentazione ( praterie e brughiere di altitudine, praterie
intrasilvatiche), che in alcuni dei probabili siti riproduttivi ( Porraie, Pania di Corfino).
Si può pertanto stimare che nell'area indagata siano presenti 10-15 coppie nidificanti. ( Lombardi et
30
STARNA Perdix perdix
Distribuzione e fenologia
Specie politipica a distribuzione euroasiatica; introdotta in America settentrionale.
Nella regione paleoartica occidentale 8 sottospecie, di cui italica , propria dell'Italia.
Popolazione europea : 2,6-5,1 milioni di coppie di cui 1-2 in Russia. Trend: contrazione di areale e
decremento numerico.
Sedentaria; popolazioni dell'Europa orientale parzialmente migratrici.
In Italia sedentaria e nidificante sull'Appennino settentrionale, più scarsa e localizzata sulle Alpi,
sull'appennino centrale , nelle regioni settentrionali e in Toscana.( Brichetti e Fracassi, 2004)
Storiacamente la specie occupava l'Italia peninsulare quasi senza soluzioni di continuità, se si
eccettuano i rilievi oltre i 1700 m e forse alcune delle zone più aride del Mezzogiorno, è sempre
stata assente dalla Sicilia, Sardegna ed isole minori ( Giglioli, 1907)
Perdix perdix italica è considerata estinta ed è stata sostituita progressivamente da sottospecie
31
Esigenze ecologiche
Nidifica in zone aperte erbose e cespugliose asciutte, preferibilmente ondulate e collinari, incolte o
coltivate a rotazione.
Diffusa fino a 2100 m sulle alpi occidentali, con massima frequenza tra 200-1000 m, in ianura è
generalmente molto scarsa tranne in alcune particolari situazioni ( Brichetti e Fracasso, 2004)
32
Movimenti e migrazioni
Sedentaria, compie erratismi di portata limitata, piu evidenti nel periodo autunno-invernale in
relazione alle disponibilità alimentari.
Gregaria nel periodo post-riproduttivo, quando ha luogo la formazione di gruppi di 5-15 individui,
con massimo di oltre 20-30. ( Brichetti e Fracasso, 2004)
Status e conservazione.
Specie classificata SPEC 3, considerata Vulnerabile a livello europeo con status di conservazione
sfavorevole. In Italia è presente con 2000-4000 coppie (Birdlife Int., 2004).
Nella Lista Rossa 2011 degli Uccelli Nidificanti in Italia ( Peronace et al., 2012) viene invece
inserita nella classe A Minor Preuccupazione.
A livello toscano rientra nelle popolazioni autoctone minacciate da inquinamento genetico,
categoria F, specie le cui popolazioni sono minacciate dalla presenza e/o dall'immissione di
individui non appartenenti a tali popolazioni ( Sposimo e Tellini, 1995)
Il suo declino, iniziato nei primi decenni del XX secol, si è accentuato a partire dagli anni '50. Tra le
minacce più cmuni la distruzione e trasformazione di habitat di riproduzione e alimentazione .
33
Fig.3.26. Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993)
Distribuzione in Appennino Tosco-Emiliano
Popolazioni autoctone autoriproducentesi sono scomparse da tempodall'area di studio, cosi come
dal resto d'Italia.In passato era presente e comune nelle nei coltivi delle apuane e dell'Appennino,
soprattutto a quote medio basse ( Lombardi et al., 1998)
Alcuni individui sono stati rilevati nel luglio 1995 in una stazione di prateria tra Foce del Termine e
il M. Prana, attorno a 900 m , senz'altro si trattava di individui derivanti da immissioni, effettuate
nella primavera 1995 dalla provincia di Lucca proprio nei pressi di M. Prana.La starna non è stata
34
QUAGLIA Coturnix coturnix
Distribuzione e fenologia
Specie politipica a distribuzione paleoartico-paleotropicale, introdotta in isole oceaniche.Nella
regione Paleartica occidntale 3 sottospecie cui cuturnix interessa l' Italia.
Migratrice, con popolazioni meridionali meno mobili. Sverna principalmente in Africa centrale
poco a sud del Sahara, più scarsamente nel bacino del Mediterraneo, raramente in Europa
centro-settentrionale (Brichetti e Fracasso, 2004)
In Italia è migratrice nidificante (estiva) diffusa in tutto il paese ma in modo frammentario,
soprattuto in Pianura Padana, nell'alto Tirreno, nelle regioni meridionali e in Sicilia; probabile
esistenza i una popolazione parzialmente sedentaria in Sardegna; nidificazione irregolare in isole
minori circum-siciliane, comprese le isole Maltesi.( Brichetti e Fracasso, 2004)
35
Nidifica in ambienti aperti erbosi diversificati, previlegiando quelli steppici con presenza molto
sparsa di cespugli o alberi; localmente su altopiani erbosi, in aree suburbane e coltivazioni intensive
di cereali e foraggere. In Sicilia e Sardegna rilevata una netta preferenza per coltivazioni omogenee
a grano; in varie regioni più frequente in aree montane. Diffusa tra 0-1800 mcon un massimo di
1850 sugli Appennini e di 2000 m sulle Alpi, con nidificazioni probabili fino a 2500 m. In periodo
invernale osservata in zone pianeggianti e collinari, anche suburbane, sotto i 500 m.(Brichetti e
Fracasso, 2004)
Fig.3.27 Andamento della popolazione in Europa (Birdlife Int., 2004)
Movimenti e migrazioni
Migratrice regolare; la popolazione sarda è ritenuta parzialmente sedentaria. Movimenti tra
agosto-novembre e metà marzo-giugno.
Una importante rotta di migrazione primaverile si sviluppa dalla Tunisia verso l' Europa
ord-orientale attraverso le coste laziali e medio adriatiche, mentre in autunno vengono utilizzate rotte
36
Migrazione numericamente fluttuante.Maschi adulti più precoci delle femmine e dei giovani in
primavera; i movimenti hanno luogo in coppie o piccoli gruppi fino a 20 individui.( Brichetti e
Fracasso, 2004)
Svernante localizzata, apparentemente regolare. popolazione difficile da valutare, ma probabilmente
superiore a 200 individui.
Casi di svernamento o presenze invernali in varie regioni, con più frequenza in quelle centrali e
meridionali. In Sardegna viene ipotizzata la presenza di individui sedentari, in parte già accoppiati e
possibilmente nidificanti, e di migratori svernanti (Brichetti e Fracasso, 2004)
Status e conservazione
La specie è considerata stabile a livello europeo, ma ha subito una significativa diminuzione nel
periodo 1970-1990 e non ha ancora raggiunto i precedenti livelli demografici, è inserita nella
categoria SPEC 3, quindi con uno stato di conservazione sfavorevole.
Nella Lista Rossa Italiana ( Peronace et al., 2012) non è classificata poichè i dati sono insufficienti ,
nel Libro Rosso degli Animali D'Italia ( Bulgarini et al., 1998) è classificata come specie a minor
rischio.
In Toscana è in diminuzione in alcune aree, rischiando di subire contrazione di areale e di entrare
nella categoria delle specie minacciate (Sposimo e Tellini, 1995).
37
Fig.3.27: Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993)
Distribuzione in Appennino Tosco-Emiliano
Trovata da Tellini sul crinale appenninico alla Paduletta ( attorno ai 1600 m), a ovest del M. Sillano,
la quaglia è una specie che dovrebbe localizzarsi solo al limite inferiore delle tipologie ambientali
38
PERNICE ROSSA Alectoris rufa
Distribuzione e fenologia
Specie politipica a corologia mediterranea, diffusa con tre sottospecie nelle zone idonee della
regione Paleartica sud-occidentale; nota anche come Pedrix rouge in Francia, Perdiz roja in
Spagna, Red-leggend partridge in Inghilterra, Rothuhn in Germania.
Le tre sottospecie comunemente accettate sono:
Alectoris r. rufa (Linnaeus, 1758): diffusa dalla Francia all'Italia nord-occidentale, presente all'Elba e in Corsica, introdotta con successo nelle Baleari ed in Gran Bretagna;
Alectoris r. hispanica ( Seoane, 1984): Penisola Iberica nord-occidentale, introdotta a Madera e nelle Azzorre;
Alectoris r. intercedens ( A.E: Brehm, 1858): diffusa dalla Spagna orientale e centro-meridionale, probabilmente introdotta nella Gran Canaria;
La Pernice rossa è tipica di habitat di media collina o montuosi, naturalmente presente in
39
Un tempo era diffusa anche nella Germania occidentale, in Svizzera, nella Francia nord-orientale e
sulle isole della Manica, zone che ha progressivamente abbandonato nel corso degli ultimi quattro
secoli, con lo spostamento verso Sud del suo areale di distribuzione, dovuto probabilmente a
cambiamenti climatici.
Fu introdotta in Gran Bretagna dalla Francia nel 1770 ed è attualmente stabile in quasi tutta
l'Inghilterra, in parti della Scozia e del Galles. Altri siti d'introduzione storica sono le Azzorre, la
Gran Canaria, Madera, l'Elba e Montecristo; è molto probabile che anche la presenza della specie
nelle Baleari e in Corsica sia dovuta all'uomo.
Recentemente sono state effettuate immissioni di Pernice rossa, con finalità venatorie, anche al di
fuori del normale areale di distribuzione, come ad esempio in .Irlanda; queste popolazioni sono però
per lo più incapaci di auto mantenersi.
La Pernice rossa è diffusa in Italia con una sola sottospecie, Alectoris r. rufa
Nel secolo scorso il centro di maggior diffusione della pernice rossa era localizzato nell'Appennino
settentrionale, dal Mar ligure alle Langhe e in tutta la media collina della Padania, terminando verso
est a livello delle provincie di Parma e Pistoia. Piccole popolazioni erano presenti in alcune vallate
alpine occidentali (Pellice, Susa), in Valtellina, sul Mottarone (Novara), nel Bassanese, nel
Veronese (ma la presenza in Veneto è dubbia); verso il centro la specie era presente nell'ascolano,
nel Pisano, sulle Alpi Apuane, all'Elba, a Pianosa, alla Capraia e a Castiglione della Pescaia (Spanò,
1992).
L'areale della specie in Italia negli ultimi decenni si è espanso verso Oriente (in Emilia-Romagna,
nelle provincie di Modena, Bologna e Forlì) in seguito ai massicci ripopolamenti a scopo venatorio,
che hanno dato origine a popolazioni stabili (almeno in ambiti protetti), che hanno colonizzato
habitat collinari un tempo occupati da Perdix perdix. Al contrario si è verificata una contrazione
dell'areale sul versante toscano delle provincie di Massa C., Lucca, Pistoia e Firenze e nella zona
40
Esigenze ecologiche
E' essenzialmente un uccello tipico degli spazi aperti, con clima mite e asciutto e vegetazione ricca
di cespugli e prati; è spesso associato a paesaggi coltivati con metodi non intensivi, costituiti da un
mosaico di appezzamenti diversi. In Italia e nella Penisola Iberica colonizza anche i versanti di
montagne con rocce affioranti, con alternanza di spazi aperti e di basse boscaglie, fino ai 2000 m.
Fig. 3.28 Andamento della popolazione in Europa (Birdlife Int, 2004)
Status e conservazione
L'intera popolazione europea di pernice Rossa si attesta intorno a 3,5 milioni di coppie, delle quali
2,5 milioni sono localizzate nella Penisola iberica e 0,5 in Francia.
L'espansione delle Alectoris nell'area mediterranea è in origine verosimilmente legata alla
trasformazione ambientale causata dal pascolo, nel senso di un habitat semiaperto, ottimale quando
poi è accoppiato ad un'agricoltura marginale variata, con piccoli appezzamenti di cereali (Spanò,
41
A partire dal 1960, le popolazioni selvatiche di questa specie hanno subito un declino che ha
interessato l'intero areale di distribuzione; in Francia si è scesi a valori sotto 1 coppia/Km2, in
Spagna e Portogallo esso è stato localizzato: notevole nelle piane costiere ma ridotto nella fascia
altitudinale compresa fra i 200 e i 1000 m s.l.m. In Gran Bretagna, si riscontra una maggior
diffusione della specie nell'Inghilterra orientale, tra l'Humber e il Tamigi. Le cause del declino
vanno ricercate nell'intensificazione dell'agricoltura (largo impiego di pesticidi, meccanizzazione,
irrigazione, scomparsa delle siepi) e nell'abbandono della pratica di coltivazione collinare -
montana. A ciò si aggiunge la forte pressione venatoria, esacerbata dal rilascio di soggetti di
allevamento, azione che incoraggia i cacciatori ad un prelievo a livelli che una popolazione
selvatica non potrebbe assolutamente sopportare.
Frequente immissione di soggetti ibridi di A.r. rufa x A. r. graeca e di A. r.rufa x A. r. chukar hanno
intaccato il patrimonio genetici dei ceppi selvatici, indebolendoli e accellerandone il declino
(Aebischer e Lucio, 1996)
Da una recente inchiesta, incompleta ma indicativa, è emerso per la pernice rossa, nel 1984, un
capitale italiano di brigate autunnali di circa 1400-1700 unità, cosi ripartite nelle ragioni di maggior
diffusione: Liguria 200-250, Piemonte 250-300, Lombardia 200, Emilia Romagna 600-700.
Contrazioni drastiche risultano essersi verificate in zone appenniniche abbandonate dall'agricoltura
e in regime di caccia libera. Le cause di diminuzione sono soprattutto da attribuire alle
modificazioni ambientali, all'abbandono dell'alta collina e della montagna, alla trasformazione degli
economi agro-silvo-pastorale ed al conseguente ritorno del bosco. Le cause di aumento locale sono
invece da ricercare nello spostamento dell'areale di distribuzione verso valle, nella scomparsa quasi
totale della competizione con la prima grande perdix, ecologicamente più esigente, nella presa di
coscienza dell'importanza di salvaguardare i ceppi rimasti (popolazioni sufficientemente poco
inquinate da immissioni incontrollate sono, infatti, reperibili nelle province di Imperia, Cuneo,
Piacenza e Livorno - Elba), nella conseguente limitazione del prelievo venatorio, nel controllo dei
42
pernice all'isola d'Elba è stata oggetto di una recente ricerca (Chiatante et al., 2013) che ha messo in
evidenza problemi di dimensione della popolazione, nonché d'inquinamento genetico della stessa,
per opera di passate immissioni non controllate. Questo problema è stato oggetto di ricerche
specifiche che hanno messo in evidenza le difficoltà gestionali legate ad un'effettiva possibilità di
recupero in stato di purezza della popolazione elbana in particolare (Baratti et al., 2004, Barbanera
et al., 2009, 2010, 2011 ).
Secondo visioni meno ottimistiche (De Franceschi, 1998), la tendenza generale delle popolazioni è
ad un decremento più o meno accentuato, ed inutili risultano le immissioni di soggetti appartenenti
a sottospecie alloctone, spesso anche in zone stranee all'areale. Nelle estreme zone alpine
occidentali (Alpi Marittime), dove l'areale si sovrappone a quello di Alectoris graeca, sono
conosciuti alcuni casi di ibridazione, infatti le due specie A. graeca e A. rufa sono in effetti delle "
semispecie" che con A. chukar formano una superspecie. Il loro isolamento riproduttivo non è
infatti ancora completo e nelle aree di contattodegli areali rispetti si formano ibridi naturali (fasce
ibride). Questo è indice di una derivazione filetica comune che secondo lo schema più accettato
(Blondel, 1986 ) vedrebbe A. graeca come entità più antica, risalente al Pleistocene medio e
contemporanea della A. barbara (Pernice sarda). Da graeca si sarebbe originata rufa e chukar
interno all'Olocene, con un processo di speciazione e quindi di separazione genetica non completato
43
Fig.3.29 Mappa della distribuzione delle tre specie di Alectoris con indicazione delle sottospecie e delle rispettive zone ibride (Blondel, 1986)
La specie ha uno status di conservazione sfavorevole in europa , rientra nella categoria SPEC 2:
vulnerabile. E' inserita nella Lista Rossa italiana come DD: dati insufficienti ( Peronace et al.,
2012). Lo status attuale della specie in Italia appare complessivamente favorevole. Infati pur
dovendosi segnalare la sua scomparsa in alcune vallate delle alpi occidentali, l' areale originario si è
espanso verso oriente nell'Appennino emiliano-romagnolo a seguita delle massicce
immissionieffettuate a fini venatori negli ultimi trent' anni. Per quanto appaia ababstanza rustica e
adattabile, essa trova unnfattore limitante nel mutare del paesaggio alto collinare e montano, dovuto
all'abbandono delle coltivazioni e alla conseguente espansione del bosco. L'eccessiva pressione
venatoria, peraltro non ispirata a corretti criteri di programmazione del prelievo, è un ulteriore
elemento negativo, che causa la diminuzione o comunque l'instabilità delle popolazioni. Un'
efficace azione di conservazione non può peraltro prescindere da una limitazione del
prelievovenatorio, che deve essere commisurato all'incremento annuo delle popolazioni.
La possibilità di costituire popolazioni di Pernice rossa attraverso azioni di reintroduzione in parti
dell'areale che hanno visto estinzioni locali, rappresenta uno dei maggiori problemi di carattere
44
Come accennato nel precedente paragrafolunghi perioriodi di prelievo venatorio non commisurato
al mantenimeto di popolazionivitali, ha portato o all'estinzione locale con conseguente
restringimento dell'areale riproduttivo ovvero alla costituzione di un complesso sistema
metapopolazionistico in cui a fronte di piccoli nuclei autosostenentesi, sopravvisuti in aree di
particolare valenza ecologica o soggette a protezione ( parchi, riserve naturali), si ritrovano altri con
popolamenti effimeri non autosostenentesi se non in seguito a ripopolamenti.
Gli stock disponibili per operazioni di ripopolamento a fine venatorio sono creati nella grande
maggioranza dei casi secondo criteri zootecnicidi produttività in situazioni di cattività spesso bel
lontane da quelle che ritroveranno gli individui rimmessi in natura.
da un punto di vista conservazionistico questo non è che tuttavia il problema minore; infati tali
criteri zootecnici hanno determinato la costituzione di assetti genetici di natura ibrida, sia
incrociando individui appartenenti a differenti sottospecie alla medesima specie, sia ricorrendo ad
individui appartenenti a specie (semispecie) diverse.
In questo modogli individui usati per i ripopolamenti non hanno niente a che vedere con le
popolazioni autoctone, costituendo essi stessi una via di ulteriore inquinamento delle popolazioni
sopravvissute, o nel caso dell'estinzione di queste, neopopolazioni del tutto estranee all'assetto
zoogeografico dei territori che le ospitano.
La possibilità di reperire materiale geneticamente idoneo per la ricostituzione di popolazioni
perdute è cosi legato alla effettiva disponibilità di individui compatibili biogeograficamente con i
territori in cui si intende operare.
Una concreta possibilità di poter operare con individui di tale tipo è oggi fonte di accesa discussione
a livello scientifico, eventualmente risolvibile con la conoscenza di profili genetici degli individui
45
Fig.3.30. Presenza della specie in Italia come nidificante (da Meschini e Frugis, 1993) Distribuzione in Appennino Tosco-Emiliano
Fino ai primi del '900 la Pernice rossa era presente, con popolazioni autoctone, nell'Appennino
settentrionale, dalla liguria alla media collina padana fino alle provincie di Parma e Pistoia, e nelle
Alpi Apuane sui M. Gabberi, M. Alto e M. Corchia ( Savi, 1827; Simi, 1859; Spanò,1992); gà alla
fine del secolo scorso era comunque quasi scomparsa dalla provincia di Lucca (Giglioli, 1907).
Sulle Apuane e sull'Appennino lucchese le segnalazioni più recenti sono assai scarse e
verosimilmente sono tutte riferibili ad animali provenienti da immissioni (Lombardi et al., 1998).
L'habitat riproduttivo della specie è rappresentato da macchia mediterranea, da pascoli cespugliati a
Erica sp. pl., Juniperus sp. pl., e più in generale da un mosaico ambientale in cui sono presenti
coltivi, boschi, zone erose o comunque nude e incolti, in media collina e in montagna ma per lo più
tra 300 e 800 m di quota ( Spanò, 1992). Tale habitat è ancora presente sulle Apuane e, in parte
sull'Appennino, ma è fortemente in rarefazione a quote medio basse soprattuto per quanto riguarda i
46
COTURNICE..Alectoris graeca
Nota: la specie non è riportata nell'atlante toscano ( Tellini et al., 1997) perchè estinta localmente. Tuttavia la specie è oggetto di continua e incontrollate immissioni ai fini venatori, per cui ne
riportiamo qui di seguito i caratteri generali in quanto isolati individui possono occasionalmente
ritrovarsi nel territorio di interesse di questa tesi.
Distribuzione e fenologia
Specie politipica a corologia europea. La sottospecie nominale è diffusa nella ex Jugoslavia sud-
orientale, Bulgaria meridionale e grecia, nonchè in Italia nell'Appennino centro-meridionale;
nell'arco alpino dalla Francia all'Austria, nella ex Jugoslavia occidentale e sud-occidentale è
presente la sottospecie saxatilis, mentre in Sicilia è presente A. g. whitakeri.Di recente è stata
formulata l'ipotesi che la popolazione appenninica sia da riferire a una nuova sottospecie diversa da
quella nominale, ovvero A. g. orlandoi . Tale ipotesi non è ancora stata confermata da specifiche
47
La popolazione europea è stimata 31000-59000 coppie, in gran parte concentrate in Italia e
Croazia.In Italia A. g. saxatilis è sedentaria e nidificante su Alpi e Appennini, A. g. whitakeri
(Coturnice siciliana) in Sicilia.
Esigenze ecologiche
Nidifica in ambienti montuosi, su pendii pietrosi aperti e soleggiayti, preferibilmente ripidi, con
copertura erbacea più o meno compatta e presenza di arbusti nani,cespugli sparsi e alberi isolati;
localmente ai margini di rimboschimenti. Piu diffusa tra 800-2200 m, con presenze quasi a livello
del mare in sicilia e massimo di 2600-2700 m sulle Alpi centrali e occidentali. In inverno frequenta,
soprattutto nelle vallate interne, versanti esposti a sud con innevamento scarso o assente (Brichetti e
Fracasso, 2004)
Fig 3.31: Andamento della popolazione in Europa (Birdlife Int, 2004)
Movimenti e migrazioni
Sedentaria, compie erratismi in senso verticale nel periodo autunno invernale, la cui portata sulle
autunno-48
invernali, anche fino a 35-40 individui, composti da uno o più gruppi familiari e da individui isolati
(Brichetti e Fracasso, 2004)
Status e conservazione
Dati preoccupanti riguardano le popolazioni stanziate in Francia, Austria,Svizzera, regione
balcanica, Bulgaria, ma solo in Francia ed in Bulgaria sono stati intrapresi studi mirati al
monitoraggio della specie nel medio-lungo periodo:
- per la Bulgaria, Dragoev (1974) sottolinea l'incidenza del prelievo, del regime climatico e
della fenologia delle piante alimentari, sulla produttività annuale delle popolazioni, ma non
ne qualifica gli effetti;
- in Francia le attuali popolazioni occupano una porzione limitata dell'areale originario,
situata al margine Sud-occidentale del Massiccio alpino francese, in continuità con quello
italo svizzero; è invece fortemente regredita al margine Nord-occidentale (Massiccio di
Vercons, Bauges, Bornes, Francigny, Chaublay) e in particolare sul versante settentrionale,
alta Savoia e regione Rodano-Alpi, dove i casi di scomparsi sono rispettivamente dell'ordine
del 75% e del 23-36%; stabili sono i nuclei stanziati nelle Alpi Marittime .
- in Austria, le popolazioni di coturnice sopravvivono nella Corinzia occidentale, a quote
comprese tra i 1400-2000m, mentre sono scomparsi dalla regione della Stiria e della restante
Austria superiore, parallelamente al declino delle attività agro-pastorali che ne avevano
favorito la diffusione.
- simili condizioni, aggravate da un uso massiccio di pesticidi, si ritrovano in Anatolia, mentre
in Tracia si conservano condizioni ambientali idonee alla specie .
La coturnice alpina si trova in declino notevole nella maggior parte dell'areale italiano.La densità
delle popolaioni è generalmente bassa in tutto l'arco alpino, dove la speciè ha subito una forte
contrazione a partire dagli anni '50.Tale contrazione si è estesa progressivamente da Est verso
49
molti siti alpini la popolazione residua è stimata all' 8-15% della popolazione iniziale.Da tempo la
coturnice è scomparsa dalla porzione più occidentale dell'appennino ligure-piemontese, dai rilievi
promissimi alla campagna romana (secolo scorso) e dalle isole d' Elba (fine 1700), Eolie,
Pantelleria (1900). Non esiste molta documentazione per quanto riguarda le consistenze attuali di
coturnice alpina in Italia.Densità di 2,1 coppie per 100 ha sono state riscontrate in provincia di
Trento (Meriggi et al.,1998).Dati riferiti al triennio 87-89 riguardani la Valle D'aosta, evidenziano,
concentrazioni di nidiate pari a 8,5 maschi territoriali per 100 ha (Bocca, 1990), decisamente
superiori alla media, che si attesta generalmente al di sotto delle tre coppie per 100 ha.
La speciè ha uno stato di conservazione sfavorevole in Europa, SPEC 2, rientra nello status di
Declining con popolazioni in diminuzione, .
Lo status attuale di conservazione sfavorevole della specie è riconducibile ad alcuni fattori negativi,
e segnatamente alle modificazioni ambientali dovute all'abbandono delle atività agricole e di quelle
pastorali nelle zone montane, all'eccessiva pressione venatoria e al braconaggio. Come nel caso
degli altri Galliformi di interesse venatorio, per far fronte al declino delle popolazioni si è ricorso al
ripopolamento. Fino ad un recente passato per tali immissioni sono stati piu spesso utilizzati ibridi
sia con la Pernice rossa che con la Coturnice orientale (Alectoris chukar), quando non addirittura
ibridi tra queste due ultime specie. Assai numerose sono state pure le immissioni di Coturnice
orientale. Fortunatamente non pare che tali ripopolamenti abbiano alterato l'individualità delle tre
sottospecie presenti in Italia. Un' efficace azione di conservazione non può prescindere da un lato
dalla limitazione della pressione venatoria con prelievi commisurati all'incremento annuo, dall'altro
dalla cessazione dei ripopolamenti indiscriminati. Interventi di reintroduzione tecnicamente corretti
potrebbero essere effettuati utilizando soggetti ottenuti in cattività da ceppi selezionatidelle distinte
50