4. RISULTATI
4.1 Costruzione delle librerie sottrattive
Nel nostro lavoro ci siamo avvalsi della tecnica dell’SSH. Questo metodo permette di ottenere banche di cDNA arricchite di trascritti differenzialmente espressi, presenti nei due campioni comparati. La caratteristica di questa tecnica è la particolare efficienza nell’isolare sequenze rare poco espresse. Per la costruzione della banca abbiamo utilizzato il PCR-Select cDNA Subtraction Kit (BD Biosciences).
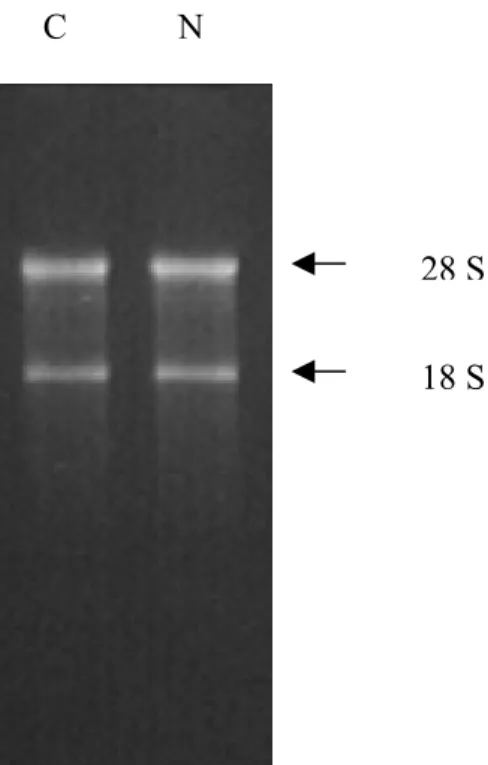
Dopo aver estratto l’RNA totale dai nostri campioni e valutato la sua qualità su gel denaturante (fig. 8).
C N
Fig. 8 : Analisi elettroforetica
su gel denaturante dell’RNA tot estratto dalle porzioni medio-temporali dei cervelli dei ratti condizionati (C) e dei ratti di controllo (N).
28 S 18 S
Dopo l’isolamentodell’mRNA poliA+ (vedere par. 3.4- Materiali e Metodi) abbiamo effettuato un controllo qualitativo e quantititativo dei nostri campioni, tramite RT-PCR, amplificando sia i geni ribosomali 5.8, 18 e 28 S (risultati non mostrati) che il gene G3PDH. Come stampo abbiamo utilizzato il cDNA ottenuto dalla retrotrascrizione sia dell’RNA totale che del poliA+.
Come si può vedere dalla fig. 9 la quantità dei nostri campioni è paragonabile e quindi si può procedere con la costruzione delle banche sottrattive.
C N
L 1 2 3 4 5 6 7 8
Fig.9: Controllo quantititativo del cDNA ottenuto tramite RT-PCR utilizzando i primer
della G3PDH e come stampo, il poliA+ del condizionato (C) e del controllo (N); lane 1-4
prodotto di amplificazione del campione condizionato;lane 5-8 prodotto di amplificazione del campione di controllo; lane 1-4 cicli 18; lane 2-5 cicli 22; Lane 3-7 cicli 26; Lane 4-8 cicli 30
Tramite l’SSH è stato quindi possibile ottenere due librerie sottrattive di cDNA: la libreria Forward, contenente i trascritti dei geni modulati positivamente dal condizionamento alla paura contestuale e la libreria
reverse, costituita invece dai trascritti dei geni modulati
negativamente.
Parallelamente alla costruzione delle due librerie sottrattive è stata effettuata una libreria sottrattiva di riferimento, utilizzando come
muscolo scheletrico digerito e da DNA di ΦX174 digerito con l’enzima HaeIII (forniti dal kit) .
Nella fig. 10 sono mostrati rispettivamente gli amplificati della libreria di controllo e delle due librerie sottrattive, forward e reverse. Come si può apprezzare, la sottrazione effettuata nei campioni di controllo è avvenuta in modo corretto in quanto la libreria in questione risulta costituita da bande discrete che coincidono con quelle del DNA di ΦX174 digerito con l’enzima HaeIII (marker IX).
1 2 3 4 5 6 7
Fig.10: Elettroforesi su gel di agarosio (2%) delle librerie e dei non sottratti ottenuti. Lane 1 libreria forward sottrata; Lane 2 libreria non sottrato forward; Lane 3 libreria di
controllo del muscolo scheletrico sottratto; Lane 4 libreria di controllo del muscolo scheletrico non sottrato; Lane 5 libreria riverse; Lane 6 libreria reverse non sottratto; Lane 7 marker IX.
Terminata la costruzione delle due librerie sottrattive è stata valutata l’efficienza della sottrazione, come suggerito dal protocollo adottato (vedere par. 3.7-Materiali e Metodi).
Abbiamo effettuato una PCR con i primer della G3PDH aumentando progressivamente il numero dei cicli, e utilizzando come stampo in un caso la libreria sottrattiva e nell’altro il corrispondente non sottratto. La sottrazione di entrambe le librerie è avvenuta correttamente visto
che i segnali del gene costitutivo sono sempre presenti nei campioni non sottratti mentre appaiono solo a cicli elevati nelle librerie; questo è indice di assenza o forte riduzione dello stampo rispetto al non sottratto. Nella figura 11 è riportata come esempio la prova di efficienza di sottrazione della libreria forward .
L 1 2 3 4 5 6 7 8 M
Fig.11: Valutazione della prova di efficienza di sottrazione per la libreria forward:
prodotti di PCR utilizzando come primer 5’G3PDH e 3’G3PDH forniti dal kit e come stampo la II PCR della libreria forward (lane 1,2,3,4)e la II PCR del non sottrato della libreria forward (lane 5,6,7,8);lane 1-5 18 cicli; lane 2-6 23 cicli; lane 3-7 28 cicli; lane 4-8 33 cicli;lane M marker
I cDNA della libreria forward sono stati clonati in un vettore di clonaggio T/A (TOPO TA Cloning® kit , Invitrogen; e trasferiti in
microtetraplates da 96 pozzetti; complessivamente sono stati raccolti
circa 600 cloni positivi.
La tecnica della SSH è un metodo molto efficiente per ottenere librerie sottrattive e garantisce un notevole arricchimento di trascritti differenzialmente espressi; anche se i campioni sottratti possono ancora contenere alcuni cDNA comuni al tester e al driver. Questo implica che alcuni cloni delle due librerie non siano differenzialmente espressi. Lo screening primario permette di eliminare questi falsi positivi.Questo studio riporta dati relativi allo screening primario di circa 400 cloni.
4.2 Risultati screening primario
Per verificare che la libreria in questione fosse rappresentativa i nostri inserti sono stati amplificati tramite una PCR da colonia, utilizzando
primers complementari alle regioni presenti ai due lati del sito di
clonaggio (vedi par. 3.7- Materiali e metodi). I prodotti sono stati analizzati su gel di agarosio (2%). Il risultato ottenuto, come può essere osservato dalla fig. 12, mostra che il clonaggio è avvenuto in modo corretto. Inoltre, dal momento che i frammenti amplificati presentano tutti pesi molecolari diversi possiamo affermare che la maggior parte dei cloni non è ridondante e che la libreria forward è altamente rappresentativa.
Lane 1 20 M Fig.12: Verifica della qualità dei cloni della libreria forward; lane 1-20
amplificazione con PCR da colonia dei cloni; lane M: marker IX (Roche).
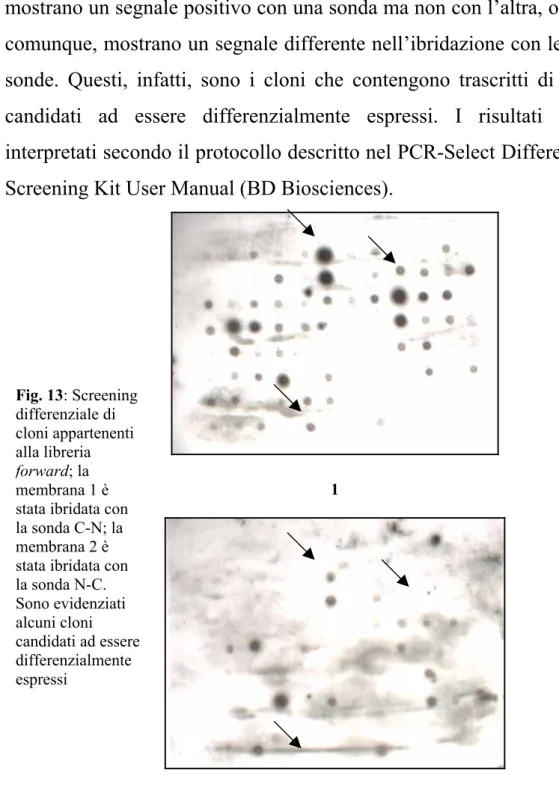
Per il momento sono stati selezionati solo i cloni che presentano un amplificato unico. Dopo denaturazione, 1 µl del prodotto di PCR è stato trasferito su due membrane Hybond N+. Le membrane sono state ibridate utilizzando come sonde i cDNA delle librerie sottrattive marcate non radioattivamente (vedere par. 3.8.3.- Materiali e metodi). Nella fig. 13 sono mostrati i risultati che abbiamo ottenuto dall’ibridazione di due membrane su cui era stato trasferito il prodotto della PCR di cloni della libreria forward. La membrana 1 è stata
ibridata con la sonda costituita dal cDNA della libreria forward (T-C), mentre la membrana 2 è stata ibridata con la sonda costituita dal cDNA della libreria reverse (C-T). Sono stati selezionati i cloni che mostrano un segnale positivo con una sonda ma non con l’altra, o che, comunque, mostrano un segnale differente nell’ibridazione con le due sonde. Questi, infatti, sono i cloni che contengono trascritti di geni candidati ad essere differenzialmente espressi. I risultati sono interpretati secondo il protocollo descritto nel PCR-Select Differential Screening Kit User Manual (BD Biosciences).
Fig. 13: Screening differenziale di cloni appartenenti alla libreria forward; la membrana 1 è stata ibridata con la sonda C-N; la membrana 2 è stata ibridata con la sonda N-C. Sono evidenziati alcuni cloni candidati ad essere differenzialmente espressi 1 .
4.3 Analisi delle sequenze
Nella tabella www sono mostrate alcune delle sequenze emerse dallo
screening primario, identificate mediante comparazione con le
sequenze depositate in banca dati (GenBank).
METABOLISMO MITOCONDRIALE
1VA6 ATP synthase subunit 6
1VE2 cytochrome oxidase subunit I
1VE9 NADH dehydrogenase subunit 5-6
1vF6 Rattus norvegicus gene for 12S
2VF2 cytochrome b mRNA,
2VG3 cytochrome c oxidase subunit I
TRASPORTO E RILASCIO DELLA VESCICOLE
1VH5 complexin 1
1VC1 coatomer protein complex, subunit beta 2
2VA6 amphiphysin (Amph)
2VB3 reg I binding protein I (Rbp1)
2VB10 ARP3 actin-related protein 3 homolog (Actr3)
2VC7 N-ethylmaleimide sensitive fusion protein attachment protein alpha
2VE11 GTP-binding protein SAR1b
TURNOVER PROTEICO
1VA11 tripartite motif protein 32 (Trim32) 2vH1 cullin 3
1VB12 proteasome maturation factor
TRASDUZIONE DEL SEGNALE INTRACELLULARE 1VB9 phosphoprotein enriched in astrocytes 15 (PEA-15)
1VC10 Type-Ia regulatory subunit of cAMP dependent protein kinase 1VB4 KIAA0974 protein
2VG1 tyrosine 3-monooxygenase/tryptophan
5-monooxygenase activation protein, zeta polypeptide
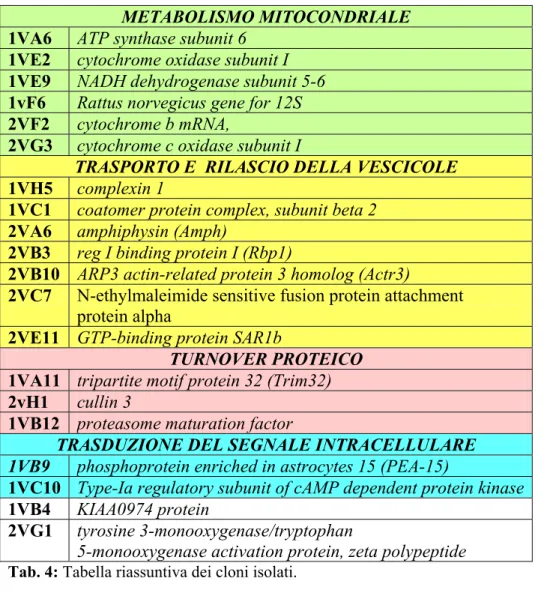
Tab. 4: Tabella riassuntiva dei cloni isolati.
I geni individuati sono stati suddivisi in base alle funzioni svolte dai loro prodotti. In questo studio in particolare sono stati analizzati i cloni 1VH5, 1VB9 e 1VA6.
4.3.1 Clone 1VH5
La sequenza del clone 1VH5 è:
5’….CTTGGGAAATGAGCAGTGGGTGCTTGGGGGCCCCAGCCCT TCCCTGAGTCCATTGCCCCTGTTTCTGGACTTGTTGGACCTGCTG GACCATTTGCTCTGTCTTCCTGTCTGTGAGCTACCACCCTAGTCT TCCCCAGCAGCCCTTGCATACTTTGTCCAGCTGTCTCCTTCTCTG TTGCTCTGCAAGGTTTGGCTTAAGAATTCCACAGCCAGAGGAA ACACAGCAATAGAGCTGGAGTGGGTGGGCTCGACACACTTGGA GTCCCTTGACGTGGTCTGTAATGCACTTTCCAGAGTCCCATCTT TCCCTGATCCCACCTGTCCCTGGTGGCCTCCTGTCCCCTTCATGG GGGCAGGCAGTCTCCTAGGGT….3’
Fig. 14: sequenza nucleotidica del clone 1VH5
La sequenza ottenuta è stata confrontata con le sequenze depositate in banca dati (GenBank), utilizzando programmi come FASTA e BLASTN. Di seguito sono riportati i dati ottenuti con BLASTN.
gi|62471461|gb|BC093605.1|Rattus norvegicus complexin 1 mRNA complete cds
gi|62990184|ref|NM_022864.2|Rattus norvegicus complexin 1(Cplx1)mRNA
La sequenza del clone in analisi mostra una similarità del 99% con le sequenze BC093605.1 e NM 022864.2. La sequenza con più alta similarità con il nostro campione è rappresentata da una porzione della
regione 3’-UTR dell’mRNA per la complessina 1 (CPLX I). La sequenza codificante del gene in questione è infatti compresa fra i nucleotidi 78 e 482. Di seguito è mostrato l’allineamento con una delle sequenze nucleotidiche:
gi|62990184|ref|NM_022864.2| Rattus norvegicus complexin 1 (Cplx1), mRNA Length=2105
Score = 728 bits (367), Expect = 0.0 Identities = 370/371 (99%), Gaps = 0/371 (0%) Strand=Plus/Plus 1VH5 1 CTTGGGAAATGAGCAGTGGGTGCTTGGGGGCCCCAGCCCTTCCCTGAGTCCATTGCCCCT 60 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 887 CTTGGGAAATGAGCAGTGGGTGCTTGGGGGCCCCAGCCCTTCCCTGAGTCCATTGCCCCT 946 1VH5 61 GTTTCTGGACTTGTTGGACCTGCTGGACCATTTGCTCTGTCTTCCTGTCTGTGAGCTACC 120 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 947 GTTTCTGGACTTGTTGGACCTGCTGGACCATTTGCTCTGTCTTCCTGTCTGTGAGCTACC 1006 1VH5 121 ACCCTAGTCTTCCCCAGCAGCCCTTGCATACTTTGTCCAGCTGTCTCCTTCTCTGTTGCT 180 ||||||||||||||||||||||||||||||||||||||||||||||| |||||||||||| Sbjct 1007 ACCCTAGTCTTCCCCAGCAGCCCTTGCATACTTTGTCCAGCTGTCTCTTTCTCTGTTGCT 1066 1VH5 181 CTGCAAGGTTTGGCTTAAGAATTCCACAGCCAGAGGAAACACAGCAATAGAGCTGGAGTG 240 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1067 CTGCAAGGTTTGGCTTAAGAATTCCACAGCCAGAGGAAACACAGCAATAGAGCTGGAGTG 1126 1VH5 241 GGTGGGCTCGACACACTTGGAGTCCCTTGACGTGGTCTGTAATGCACTTTCCAGAGTCCC 300 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1127 GGTGGGCTCGACACACTTGGAGTCCCTTGACGTGGTCTGTAATGCACTTTCCAGAGTCCC 1186 1VH5 301 ATCTTTCCCTGATCCCACCTGTCCCTGGTGGCCTCCTGTCCCCTTCATGGGGGCAGGCAG 360 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1187 ATCTTTCCCTGATCCCACCTGTCCCTGGTGGCCTCCTGTCCCCTTCATGGGGGCAGGCAG 1246 1VH5 361 TCTCCTAGGGT 371 ||||||||||| Sbjct 1247 TCTCCTAGGGT 1257
4.3.2 Clone 1VB9
La sequenza del clone 1VB9 è:
5’….GATGGATATCTGCAGAATTCGCCCTTAGCGTGGTCGCGGCCGAGG TAACAAACATTGCATTTACATTTGAGCTAAGAGACAATTTAGAGAAAG TTGAAGGTAGGAGCTTTTAGGATGTGGGAGCAAAACTTCACAGGGAAG GGAGGACCAGCTGTCAGAAGAGGGCTCTTGAAGCCAGACTGGCTAGA GCACCCTCACTTCCTAGCTGAGCCCAGTTTGCCCATCTCCTCTGGCCAC TGCTGCAGACACCTGCCTTAACACACACACCTCTAAGACTCCAGTTTTG CCTTAAAGGCCCTTCCTAAGTCTCCCTAGTCCTGCCTGGCATCTCCTTTG AGACAAGAAATCCTTGC….3’
Fig. 15: sequenza nucleotidica del clone 1VB9
La sequenza ottenuta è stata confrontata con le sequenze depositate in banca dati (GenBank), utilizzando programmi come FASTA e BLASTN. Di seguito sono riportati i dati ottenuti con BLASTN.
gi|61557369|ref|NM_001013231.1| Rattus norvegicus phosphoprotein enriched
in astrocytes 15 (Pea15), mRNA
gi|55249694|gb|BC085766.1| Rattus norvegicus phosphoprotein enriched in
astrocytes 15, mRNA (cDNA clone MGC:93673 IMAGE:7190459), complete cds
La sequenza del clone in analisi mostra una similarità del 99% sia con la sequenza NM_001013231.1 che con la sequenza BC085766.1 La sequenza con più alta similarità con il nostro campione è rappresentata da una porzione della regione 3’-UTR dell’mRNA per la
phosphoprotein enriched in astrocytes (PEA-15). La sequenza
e 481. Di seguito è mostrato l’allineamento con entrambe le sequenze nucleotidiche:
gi|61557369|ref|NM_001013231.1| Rattus norvegicus phosphoprotein enriched in astrocytes 15 (Pea15),
mRNA
gi|55249694|gb|BC085766.1| Rattus norvegicus phosphoprotein enriched in astrocytes 15, mRNA
(cDNA clone MGC:93673 IMAGE:7190459), complete cds Length=2355
Score = 599 bits (302), Expect = 2e-170 Identities = 305/306 (99%), Gaps = 0/306 (0%) Strand=Plus/Plus 1VB9 1 AACAAACATTGCATTTACATTTGAGCTAAGAGACAATTTAGAGAAAGTTGAAGGTAGGAG 60 |||||||||||||||||||||||||||||||||||||||||| ||||||||||||||||| Sbjct 1706 AACAAACATTGCATTTACATTTGAGCTAAGAGACAATTTAGAAAAAGTTGAAGGTAGGAG 1765 1VB9 61 CTTTTAGGATGTGGGAGCAAAACTTCACAGGGAAGGGAGGACCAGCTGTCAGAAGAGGGC 120 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1766 CTTTTAGGATGTGGGAGCAAAACTTCACAGGGAAGGGAGGACCAGCTGTCAGAAGAGGGC 1825 1VB9 121 TCTTGAAGCCAGACTGGCTAGAGCACCCTCACTTCCTAGCTGAGCCCAGTTTGCCCATCT 180 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1826 TCTTGAAGCCAGACTGGCTAGAGCACCCTCACTTCCTAGCTGAGCCCAGTTTGCCCATCT 1885 1VB9 181 CCTCTGGCCACTGCTGCAGACACCTGCCTTAACACACACACCTCTAAGACTCCAGTTTTG 240 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1886 CCTCTGGCCACTGCTGCAGACACCTGCCTTAACACACACACCTCTAAGACTCCAGTTTTG 1945 1VB9 241 CCTTAAAGGCCCTTCCTAAGTCTCCCTAGTCCTGCCTGGCATCTCCTTTGAGACAAGAAA 300 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1946 CCTTAAAGGCCCTTCCTAAGTCTCCCTAGTCCTGCCTGGCATCTCCTTTGAGACAAGAAA 2005 1VB9 301 TCCTTG 306 |||||| Sbjct 2006 TCCTTG 2011
4.3.3 Clone 1VA6
La sequenza del clone 1VA6 è:
5’…CTCTTTCATTACCCCCACAATAATAGGTCTACCAATTGTTGTAA CCATTATTATGTTCCCATCAATTCTATTCCCATCATCAAAACGCCTA ATCAGCAACCGACTACACTCATTTCAACACTGACTAATCAAACTTA TCATCAAACAAATAATGTTAATCCACACACCAAAAGGACGAACCT GAGCCCTAATAATTGTATCCCTAATTATATTTATTGGCTCAACCAA CCTTCTAGGGCTTCTTCCCCATACATTTACCCCTACCACTCAGCTAT CTATAAACCTAAGCATGGCCATCCCCCTATGAGCAGGAGCCGTAAT TCTAGGCTTCCGACACAAACTAAAAAATTCTTTAGCCCACTTCTTA CCGCAAGGAACCCCCATCTCACTAATTCCCATACTAATCATCATCG AAACTATCAGCCTATTTATTCAACCGATAGCACTAGCAGT …3’
Fig. 16 : sequenza nucleotidica del clone 1VA6
La sequenza ottenuta è stata confrontata con le sequenze depositate in banca dati (GenBank), utilizzando programmi come FASTA e BLASTN. Di seguito sono riportati i dati ottenuti con BLASTN.
gi|854269|emb|X14848.1|MIRNXX Rattus norvegicus mitochondrial menome
gi|20805882|gb|AF504920.1| Rattus norvegicus ATPase synthase subunit 6 mRNA, partial cds;
La sequenza del clone in analisi mostra una similarità del 98% sia con la sequenza X14848.1 che con la sequenza AF504920.1.La sequenza con più alta similarità con il nostro campione è rappresentata da una porzione della sequenza codificante dell’mRNA mitocondriale per la subunità 6 della ATPsintetasi (F6). La sequenza codificante del gene
in questione è infatti compresa fra i nucleotidi 7904 e 8584. Di seguito è mostrato l’allineamento con la sequenza X14848.1:
gi|854269|emb|X14848.1|MIRNXX Rattus norvegicus mitochondrial genome Length=16300
Score = 842 bits (425), Expect = 0.0 Identities = 446/453 (98%), Gaps = 0/453 (0%) Strand=Plus/Plus 1VA6 1 CTCTTTCATTACCCCCACAATAATAGGTCTACCAATTGTTGTAACCATTATTATGTTCCC 60 |||||||||||||||||||||||||||||||||||||||||| ||||||||||||||||| Sbjct 7924 CTCTTTCATTACCCCCACAATAATAGGTCTACCAATTGTTGTGACCATTATTATGTTCCC 7983 1VA6 61 ATCAATTCTATTCCCATCATCAAAACGCCTAATCAGCAACCGACTACACTCATTTCAACA 120 |||||||||||||||||||||| ||||||||||||||||||||||||||||||||||||| Sbjct 7984 ATCAATTCTATTCCCATCATCAGAACGCCTAATCAGCAACCGACTACACTCATTTCAACA 8043 1VA6 121 CTGACTAATCAAACTTATCATCAAACAAATAATGTTAATCCACACACCAAAAGGACGAAC 180 ||||||||||||||||||||||||||||||||||||||| |||||||||||||||||||| Sbjct 8044 CTGACTAATCAAACTTATCATCAAACAAATAATGTTAATTCACACACCAAAAGGACGAAC 8103 1VA6 181 CTGAGCCCTAATAATTGTATCCCTAATTATATTTATTGGCTCAACCAACCTTCTAGGGCT 240 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 8104 CTGAGCCCTAATAATTGTATCCCTAATTATATTTATTGGCTCAACCAACCTTCTAGGGCT 8163 1VA6 241 TCTTCCCCATACATTTACCCCTACCACTCAGCTATCTATAAACCTAAGCATGGCCATCCC 300 |||||||||||||||||||||||||||||||||||||||| |||||||||| |||||||| Sbjct 8164 TCTTCCCCATACATTTACCCCTACCACTCAGCTATCTATAGACCTAAGCATAGCCATCCC 8223 1VA6 301 CCTATGAGCAGGAGCCGTAATTCTAGGCTTCCGACACAAACTAAAAAATTCTTTAGCCCA 360 ||||||||||||||||||||||||||| |||||||||||||||||||||||||||||||| Sbjct 8224 CCTATGAGCAGGAGCCGTAATTCTAGGTTTCCGACACAAACTAAAAAATTCTTTAGCCCA 8283 1VA6 361 CTTCTTACCGCAAGGAACCCCCATCTCACTAATTCCCATACTAATCATCATCGAAACTAT 420 ||||| |||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 8284 CTTCTCACCGCAAGGAACCCCCATCTCACTAATTCCCATACTAATCATCATCGAAACTAT 8343 1VA6 421 CAGCCTATTTATTCAACCGATAGCACTAGCAGT 453 ||||||||||||||||||||||||||||||||| Sbjct 8344 CAGCCTATTTATTCAACCGATAGCACTAGCAGT 8376
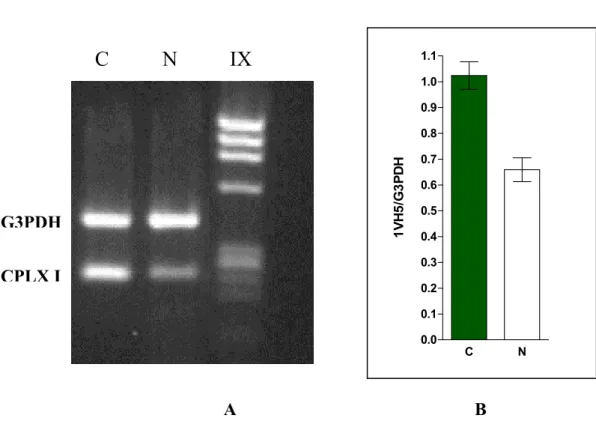
4.4 Risultati dell’analisi di espressione tramite RT-PCR relativa L’analisi di espressione dei cloni 1VH5, 1VB9 e 1VA6 è stata effettuata tramite la tecnica della RT-PCR relativa, utilizzando come controllo interno il gene costitutivo G3PDH (vedere par. 3.11 di Materiali e metodi). In particolare è emerso che il consolidamento del CFC è associato ad una modulazione positiva della trascrizione dei geni della CPLX I (fig, 17), della PEA-15 (fig. 18) e della F6 (fig. 19).
C N 0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 1.1 1V H 5 /G 3 P D C N IX H G3PDH CPLX I A B
Fig. 17 A) RT-PCR relativa e B) Livelli di espressione relativa del trascritto di CPLX 1; il gene costitutivo non ha mostrato differenze significative tra controllo e trattato; i segnali gene-specifico sono stati normalizzati con i segnali corrispondenti del gene costitutivo (T test, P< 0.05).
C N IX A B C N 0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 1V B 9 /G 3P D H G3PDH PEA-15
Fig. 18 A) RT-PCR relativa e B) Livelli di espressione relativa del trascritto di PEA15; il gene costitutivo non ha mostrato differenze significative tra controllo e trattato; i segnali gene-specifico sono stati normalizzati con i segnali corrispondenti del gene costitutivo. La differenza è significativa (T test, P< 0,05).
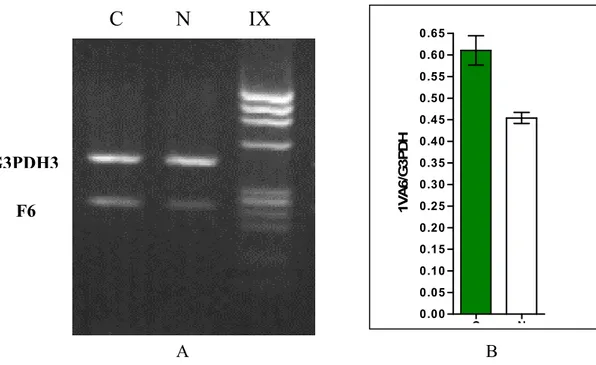
C N 0.00 0.05 0.10 0.15 0.20 0.25 0.30 0.35 0.40 0.45 0.50 0.55 0.60 0.65 1V A 6 /G 3 P D H C N IX F6 G3PDH3 A B
Fig. 19 A) RT-PCR relativa e B) Livelli di espressione relativa del trascritto di F6; il gene costitutivo non ha mostrato differenze significative tra controllo e trattato; i segnali gene-specifico sono stati normalizzati con i segnali corrispondenti del gene costitutivo. La differenza è significativa (Mann-Whitney, P< 0,05).