1. INTRODUZIONE
1.1 Proprietà nutrizionali dei vegetali
L’evoluzione delle attese dei consumatori denota una crescente attenzione verso aspetti della qualità dei prodotti alimentari connessi con le loro proprietà nutrizionali e salutistiche, dando sempre più importanza al concetto di qualità. Gli alimenti ad alto contenuto di composti salutistici hanno accolto sempre più attenzione da parte della comunità scientifica che ha coniato per essi il termine di
functional foods, definizione creata nel 1994 dall’Istitute of Medicine’s Food and
Nutrition Board per quei cibi che oltre alle normali funzioni nutrizionali apportino
benefici alla salute umana sia in termini di parametri fisiologici, sia come prevenzione delle malattie future, ritardando per esempio i processi di invecchiamento cellulare.
Infatti studi epidemiologici hanno messo in luce l’esistenza di una correlazione positiva tra il consumo di alimenti di origine vegetale e la riduzione del rischio di insorgenza delle malattie degenerative collegate con l’invecchiamento e più in generale con i danni causati dalle specie chimiche ossidanti (Reactive Oxygen
Species, ROS), fra cui i radicali liberi, la cui azione è spesso alla base di molte
patologie (Lasheras et al., 2002).
Gli alimenti di origine vegetale si inseriscono in questo contesto in quanto non solo contengono nutrienti essenziali quali proteine, carboidrati, lipidi e micronutrienti come vitamine e minerali, ma forniscono anche una elevata quantità di sostanze denominate composti nutraceutici con azione antiossidante nei confronti dei ROS come i carotenoidi, gli antociani, gli isoflavoni, i flavonoidi ed altri composti fenolici (Luthria et al., 2006). Con il termine composti nutraceutici si definiscono quelle sostanze che possiedono contemporaneamente proprietà nutrizionali e farmaceutiche, secondo la definizione coniata nel 1989 da Stephen De Felice, fondatore della Foundation for Innovation in Medicine, Cranford, NJ. Queste classi di composti sono sintetizzati ad opera del metabolismo secondario. Infatti, mentre il metabolismo primario è finalizzato alla crescita rifornendo l’organismo vegetale di composti quali zuccheri, proteine e lipidi, il metabolismo
secondario, che si realizza a spese di quello primario, sintetizza più o meno velocemente composti utilizzati dalla pianta per la difesa nei confronti di parassiti, erbivori, agenti tossici e, più generalmente, in condizioni di stress ossidativo La sintesi di questi composti fitochimici, essendo finalizzata ad un’azione protettiva, viene quindi modulata in maniera differente in funzione della presenza o meno di fattori di stress. Per esempio, qualora una specie venga coltivata in maniera da poter disporre di elementi nutritivi in abbondanza, in un ambiente caratterizzato da condizioni di luce né deficitarie né troppo elevate ed infine in assenza di una qualsiasi anche debole fonte di stress, questa tenderà ad accrescersi, privilegiando la produzione di una elevata biomassa a scapito del contenuto in metaboliti secondari.
Diversamente, qualora si riesca ad individuare il giusto compromesso tra le richieste nutritive della specie in questione e l’introduzione di una blanda fonte di stress controllato, il prodotto ottenuto, a fronte di una minima riduzione della biomassa, potrebbe essere caratterizzato da una notevole ricchezza in metaboliti secondari e quindi possedere una elevata qualità nutrizionale.
1.2 Specie ossigeno reattive (ROS)
Gli stress ambientali hanno sempre influenzato negativamente le produzioni agricole e le ricerche in questo campo sono sempre state ritenute necessarie dalla comunità scientifica; infatti le piante sono esposte nel loro ambiente ad una ampia gamma di stress, che possono insorgere per attività umane o per cause naturali, come la siccità o l’eccesso di acqua, la salinità, le variazioni di temperatura, le carenze o gli eccessi nutrizionali. Tutti questi fattori hanno un effetto diretto sulle reazioni in cui è coinvolto l’ossigeno, ed una caratteristica comune a tutti i tipi di stress è la capacità di aumentare in tali condizioni la produzione di specie reattive dell’ossigeno (ROS), quali l’anione radicale superossido (O2-.), il radicale idrossilico (OH.), il perossido di idrogeno (H2O2) e l’ossigeno singoletto (1O2), capaci di indurre la produzione a cascata di radicali liberi.
Infatti uno dei paradossi della vita aerobia risiede nel fatto che la molecola che sostiene la vita, l’ossigeno, non è solo essenziale per il metabolismo energetico della respirazione, ma è anche implicata in processi degradativi. L’ossigeno infatti
è una arma a doppio taglio, in quanto, sebbene renda possibile la vita sulla terra, diviene altamente tossico e potenzialmente letale nelle sue forme ridotte (ROS). La produzione delle ROS nelle cellule vegetali è un fenomeno che avviene naturalmente in conseguenza del metabolismo aerobio, come nel trasporto elettronico mitocondriale e cloroplastico, nei perossisomi, nei citocromi P-450, ma anche per cause esogene, quali stress di natura biotica o in presenza di stress ambientali, come la siccità, le variazioni di temperatura, l’incremento della pressione dell’ossigeno, la presenza di ossidanti, l’esposizione a radiazioni ionizzanti.
Le reazioni di formazione dei principali radicali sono:
1. Riduzione monovalente dell’ossigeno con produzione del radicale superossido: O2 + e- → O2 •−
2. Dismutazione del superossido con formazione di acqua ossigenata: 2 O2 •- + 2 H+ → H2O2 + O2
3. Riduzione dell’acqua ossigenata con formazione di radicali idrossilici: HOOH + D → • OH + OH- + D+
4. Degradazione di idroperossidi organici con generazione di radicali alcossilici: ROOH + Me2+ → RO• + OH- + Me3+
5. Produzione di radicali alchilici per estrazione di idrogeno da parte di radicali OH o per formazione di complessi fra metalli di transizione e l’ossigeno:
RH + •OH → R• + OH
-6. Addizione di ossigeno molecolare a questi radicali alchilici con formazione di radicali perossilici:
R• + O2 → ROO•
7. Formazione di nuovi radicali alchilici per reazioni a catena: R1H + ROO• → R1• + ROOH
8. In aggiunta a queste specie radicaliche e perossidiche l’ossigeno singoletto è un agente tossico di grande importanza. Può essere prodotto attraverso tre meccanismi di notevole rilevanza biologica:
a) attività fotosintetica: P* + O2 → 1O2 + P
b) reazione dell’acqua ossigenata con l’ipoclorito nel fagosoma di leucociti attivati:
H2O2 + OCl- → Cl- + 1O2 + H2O
c) per interazione bimolecolare fra radicali perossidici: ROO• + •OOR → ROOOOR→ 1O2 + 2RO•
Numerosi studi hanno indicato i radicali liberi come probabili determinanti di molte malattie legate a fenomeni di invecchiamento e degenerazione cellulare, essendo implicati in numerose reazioni di danno ossidativo a carico di proteine lipidi e DNA (Evangellia et al., 2008).
In alcuni studi è stato osservato come i radicali idrossilici (OH.) possano reagire con le basi nucleiche pirimidina e purina, così come con la cromatina, portando alla modificazione delle basi e all’instabilità genomica, conseguenze che determinano alterazioni dell’espressione genica che sono alla base del processo di carcinogenesi delle cellule umane (Rice-Evans et al., 1995).
In ulteriori studi è stato visto come l’accumulo di ROS sia accelerato nelle cellule tumorali; questo accumulo porta ad un danno diretto al DNA, con un incremento del ritmo di mutagenesi ed un mantenimento quindi del fenotipo oncogeno di tali cellule. I bersagli delle ROS comprendono anche i legami crociati DNA-proteine, la metilazione del DNA e la modificazione degli istoni, molecole che sono alla base della soppressione dei geni inibitori dei tumori e all’attivazione dei geni oncogeni (Ziech et al., 2011).
Per quanto riguarda i danni causati dalle ROS al DNA è stato osservato come il DNA mitocondriale venga danneggiato in maniera più considerevole rispetto al DNA nucleare; questo perché il mDNA manca di organizzazione nucleosomale, non possiede un sistema di autoriparazione e soprattutto è molto vicino alla catena
di ossidazione mitocondriale, luogo dove vengono primariamente prodotte le ROS. Il danno prodotto al mDNA gioca un ruolo importante nella patogenesi della degenerazione maculare legata all’avanzamento dell’età (Blasiak and Szaflik, 2011).
D’altro canto i radicali liberi, in quantità molto basse sono estremamente importanti in alcuni processi metabolici, quali per esempio il metabolismo dei lipidi (biosintesi delle prostaglandine e del leucotriene negli animali) e la biosintesi della lignina nelle pareti cellulari dei vegetali.
Anche nell’uomo è stato studiato come una bassa concentrazione di ROS abbia un ruolo importante nel pathway metabolico, mantenendo il normale stato redox ed avendo una funzione di conservazione dell’integrità vascolare; anche se un eccesso nella concentrazione di alcuni ROS, quali l’anione superossido ed un decremento nelle sintesi di ossido nitrico, che è il principale vasodilatatore, può portare alla vasocostrizione che è la causa principale dell’ipertensione nell’uomo (Rodrigo et al., 2011).
Una specifica fonte di stress, ovvero l’esposizione alle radiazioni ionizzanti è stata oggetto di numerosi studi, al fine di individuare una possibile correlazione tra la presenza delle radiazioni ionizzanti e l’aumento del potere antiossidante del frutto per contrastare la maggiore produzione delle ROS (Luthria et al., 2006).
Recenti ricerche su diverse specie ortofrutticole hanno evidenziato come il trattamento in post-harvest con radiazione UV-B incrementasse il contenuto di composti fenolici nell’uva (Cantos et al., 2000), di vitamina D nei funghi (Roberts et al., 2008) e di metaboliti ed enzimi antiossidanti in varie piante (Xu et al., 2008).
E’ stato inoltre osservato come quantitativi di radiazione UV-B pari a 20 o 40 KJ/m2 somministrati in post-harvest a frutti di pomodoro verdi promuovessero l’aumento di composti fenolici totali e di flavonoidi, e, quindi, del potere antiossidante totale, nei frutti giunti a maturazione completa (Liu et al., 2001).
1.3 Antiossidanti nei vegetali
Per far fronte alla inevitabile produzione di ROS, tutti gli organismi aerobici hanno sviluppato sofisticati sistemi di difesa essenziali per la loro sopravvivenza; infatti sintetizzano una serie di molecole antiossidanti nei vari organelli sede di produzione delle ROS e di possibile manifestazione del danno ossidativo.
Per antiossidanti si intendono quei composti in grado di prevenire l’insorgenza di danni cellulari connessi con lo stress ossidativo e causati dall’aumento dei radicali liberi. Antiossidanti sono le molecole presenti nei tessuti vegetali che, grazie soprattutto alla loro conformazione che li rende efficaci donatori di protoni (potenziale redox negativo), tendono facilmente ad ossidarsi e costituiscono per la loro instabilità un bersaglio ottimale per i radicali liberi, che quindi li ossidano preferenzialmente al posto di altre molecole essenziali. Una peculiarità di questi composti risiede nel fatto che una volta donati i protoni, si trasformano essi stessi in radicali, che però sono stabilizzati per risonanza e quindi poco reattivi; tali molecole antiossidanti agiscono pertanto da spazzini cellulari riuscendo a neutralizzare i radicali liberi prima che essi possano innescare una cascata di formazione di radicali e indurre danni all’organismo (Kaur and Kapoor, 2001). Gli antiossidanti si dividono in primari e secondari. Gli antiossidanti primari sono rappresentati da quei composti che donano direttamente un atomo di idrogeno, ossidandosi, e che quindi ritardano o interrompono la propagazione delle reazioni di autossidazione prevenendo la formazione dei radicali liberi. Esistono inoltre anche gli antiossidanti secondari che non agiscono direttamente sui radicali, ma sono in grado di ridurre gli antiossidanti primari, che sono stati ossidati, rendendoli nuovamente idonei a continuare la loro attività; questi ultimi possono chelare i metalli, restituire gli atomi di idrogeno agli antiossidanti primari e comportarsi da
oxygen scavenger.
La presenza di sostanze ad azione antiossidante nei prodotti di origine vegetale è una caratteristica estremamente positiva poiché consente, una volta che questi composti siano stati assunti con la dieta, di contrastare le ROS prodotte nell’organismo umano. In generale quindi i composti antiossidanti salvaguardano l’organismo dall’insorgenza di patologie ampiamente diffuse (cancro, cataratta, arteriosclerosi, diabete), grazie all’azione detossificante che hanno sui radicali
liberi. Tra le sostanze antiossidanti troviamo l’acido ascorbico (ASA), il glutatione ridotto (GSH), i carotenoidi quali luteina, licopene e β-carotene, l’α-tocoferolo, i composti fenolici con le relative sottoclassi che, grazie alla loro struttura molecolare e al loro potenziale redox sono capaci di ridurre le ROS, ossidandosi, e proteggendo così le altre macromolecole che altrimenti verrebbero irrimediabilmente danneggiate. Esistono inoltre una serie di enzimi antiossidanti come le superossido dismutasi (SOD), che catalizzano la dismutazione del superossido producendo perossido di idrogeno, quest’ultimo successivamente ridotto dalle catalasi, dall’ascorbico perossidasi o dalle perossidasi aspecifiche (Torres et al., 2006).
La presenza di antiossidanti in un alimento svolge un importante ruolo di prevenzione dell’ossidazione dei lipidi, prevenendo la formazione dei radicali liberi e dei composti secondari di ossidazione (Vanzani et al., 2011), e di protezione nei confronti dell’insorgenza di patologie quale l’arteriosclerosi (ossidazione delle LDL) e gli eventi tumorali (danni al DNA) (Pietta, 2000; Duthie and Crozier, 2000).
Nello specifico è stato evidenziato come l’assunzione di frutta e verdura sia alla base della riduzione di numerose patologie come l’osteoporosi e il miglioramento della struttura ossea nelle donne over 45 (Hamidi et al., 2011); tale funzione sembra essere legata alla specifica azione dei polifenoli, che influirebbero positivamente sul metabolismo delle cellule delle ossa (Trzeciakie et al., 2009). Naturalmente numerosi studi hanno focalizzato l’attenzione sulla connessione tra l’assunzione di frutta e vegetali e l’abbassamento dello stress ossidativo che porta ad una riduzione dell’insorgenza del rischio di cancro (Song et al., 2010).
Gli antiossidanti sono quindi oggi di primario interesse nel campo della ricerca scientifica in quanto molte di queste molecole hanno mostrato effetti protettivi nei confronti del danno cellulare determinato dai radicali liberi e quindi un effetto chemio-preventivo nei confronti del rischio associato a numerose patologie dell’uomo.
Sulla base di queste indicazioni è plausibile che gli effetti benefici determinati dal consumo di prodotti ortofrutticoli siano determinati dalla presenza di una miscela di composti antiossidanti, che svolgono una azione sinergica tra loro, conferendo
al prodotto una attività antiossidante maggiore rispetto alla semplice somma delle attività antiossidanti dei singoli composti. Infatti numerose ricerche hanno evidenziato come diete alimentari ricche sia in frutta che in verdura possano ridurre l’insorgenza di numerose patologie (Southon and Faulks, 2002; Wolfe et al., 2008).
Tra gli alimenti ricchi in composti antiossidanti, il pomodoro riveste un ruolo primario essendo un frutto che entra di diritto nella lista dei functional foods. Il pomodoro contiene infatti elevate concentrazioni di carotenoidi, tra i quali il licopene, che grazie alla sua struttura altamente insatura si è rivelato uno dei più potenti antiossidanti naturali, oltre ad essere coinvolto nei processi di comunicazione cellulare e di modulazione ormonale ed immunitaria (Rao et al., 2006). Inoltre il pomodoro è una ottima fonte di β-carotene (pro-vitamina A) e di luteina, importanti composti coinvolti nel buon funzionamento della vista, e contiene discrete quantità di acido ascorbico.
Ma il pomodoro è anche un buon accumulatore, soprattutto nella buccia, di flavonoidi, polifenoli che per la loro struttura chimica manifestano ottime proprietà antiossidanti (Pietta, 2000). Diversamente dai carotenoidi, i flavonoidi possono trovarsi in differenti compartimenti cellulari, liberi nel citoplasma, legati alla parete cellulare e glicosilati nei vacuoli. Tra i flavonoidi presenti nel pomodoro rivestono un ruolo importante, sia da un punto di vista qualitativo che quantitativo, la naringenina calcone, dotata di proprietà antiallergiche ed anti infiammatorie, la rutina, antimicrobica e anticarcinogena e la quercitina che somma alle proprietà della rutina anche quella anti infiammatoria (Nijveldt et al., 2001; Yamamoto et al., 2004; Hirai et al., 2007).
Il contenuto di questi composti all’interno del pomodoro varia per cause sia endogene che esogene. Per quanto riguarda le cause endogene numerosi studi hanno concluso come il contenuto di questi antiossidanti dipenda dalla componente varietale (Scalzo et al., 2005) e dallo stadio di maturazione a cui viene raccolto il frutto (Kotikova et al., 2011).
Anche le condizioni ambientali in cui sono allevate le piante possono influenzarne l’accumulo nei frutti (Crozier et al., 1997). Alcuni studi hanno infatti evidenziato come ci fosse una differenza significativa nel contenuto in polifenoli e nella
capacità antiossidante tra frutti ottenuti mediante agricoltura biologica o convenzionale (Faller et al., 2010).
Il contenuto di composti antiossidanti può variare anche a seguito di stress artificiali appositamente indotti dall’uomo. Recentemente l’attenzione dei ricercatori si è focalizzata sullo studio della relazione tra la radiazione UV-B presente nella luce solare e l’accumulo di tali composti, in condizioni di assenza o sovradosaggio di tale radiazione (Calvenzani et al., 2010, Giuntini et al., 2005; Liu et al. 2011).
Inoltre nel pomodoro sono presenti sali minerali che rivestono particolare importanza come il calcio, il potassio, il fosforo ed il ferro, spesso non presenti in quantità sufficienti in altri alimenti.. Proprio per un limitato apporto calorico unito all’elevato contenuto in minerali, vitamine ed antiossidanti, risulta un alimento ideale in linea con gli attuali indirizzi nutrizionali e può quindi essere inscritto nella lista dei cosiddetti functional foods.
1.4 Il frutto di pomodoro
1.4.1 Cenni storici sul pomodoro
Il pomodoro (Lycopersicum Esculentum) è originario dell’area sudamericana compresa tra Cile ed Equador, con successive aree di differenziazione in Centro-America. Inizialmente Linneo attribuì questa specie al genere Solanum; successivamente, Miller scisse il genere Solanum, formando il genere
Lycopersicum ed il sub-genere Eulycopersicum. (La Malfa, 2001). Quando i primi
conquistatori arrivarono in Centro America, una varietà di pomodoro (Lycopersicum Cerasiforme), veniva già coltivato dai nativi e si pensa che questa varietà sia l’antenato diretto delle nostre cultivars.
Poco dopo la conquista da parte di Cortez della citta atzeca di Tenochtitlan, dal 1521 chiamata Città del Messico, questo piccolo frutto compì la traversata dell’Oceano Atlantico. La prima menzione di questo frutto in Europa risale all’opera letteraria di Matthiolus, nel 1544. La coltivazione del pomodoro divenne diffusa in Spagna, Italia e Francia dove era apprezzato per il suo aspetto più che
per il suo sapore; addirittura gli vennero attribuite proprietà afrodisiache tanto da attribuirgli l’appellativo di pomme d’amour. In Nord America i conquistatori che giunsero in queste terre introdussero i pomodori solo per scopo ornamentale; una delle prime città che cominciò ad usarli per scopi culinari fu New Orleans (Smith, 2001).
Si dovette attendere la fine dell’ottocento perché i primi gastronomi rivalutassero il frutto; grazie ad incroci con varietà più produttive si passò progressivamente dalla coltura familiare alla produzione per fini industriali.
In Italia nel 1856 l’industriale Francesco Cirio cominciò una vasta produzione di conserve alimentari e nel 1875 aprì la prima fabbrica di conserva di pomodoro. Oggigiorno il pomodoro riveste una posizione di assoluta preminenza agronomica ed economica nel panorama dell’orticoltura italiana.
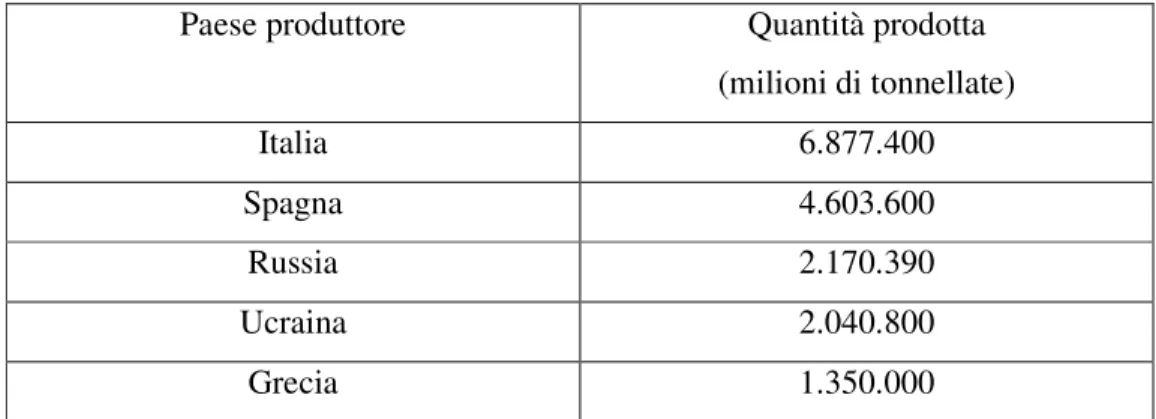
Infatti l’Italia risulta il maggiore produttore europeo di pomodori con circa 6.800.400 tonnellate di pomodori ottenuti dalla coltivazione nel 2009. Come mostra la tabella sottostante la Spagna è il secondo produttore e la Russia si attesta al terzo posto. Ucraina e Grecia sono risultate al quarto e quinto posto nella lista dei maggiori produttori europei.
Paese produttore Quantità prodotta (milioni di tonnellate) Italia 6.877.400 Spagna 4.603.600 Russia 2.170.390 Ucraina 2.040.800 Grecia 1.350.000
Tabella 1: Lista dei maggiori produttori europei e quantitativi di pomodori prodotti
1.4.2 Caratteristiche strutturali e morfologiche
Il pomodoro è una pianta dicotiledone erbacea, appartenente alla famiglia delle Solanacee; in relazione alle condizioni climatiche favorevoli ha tendenza perennante (può restare in coltivazione da 5 a 7 anni) e può avere durata e vigore differenti a seconda della varietà.
L’apparato radicale fibroso e ramificato può spingersi fino ad elevate profondità, sebbene la maggior parte delle radici rimanga nel primo strato di 30cm, e assuma conformazioni differenti in relazione all’origine della pianta. Se questa proviene da semina diretta in campo, la radice presenta infatti un robusto fittone centrale con numerose ramificazioni laterali, mentre nel caso in cui si effettui il trapianto, l’apparato radicale si sviluppa soprattutto lateralmente, interessando uno strato di terreno molto più superficiale di circa 30cm. Pertanto, in questo ultimo caso, il rifornimento idrico dovrà essere più costante, frequente e con quantità inferiori di acqua, mentre se la semina è stata effettuata direttamente in campo la pianta può esplorare il terreno anche in profondità, consentendo di essere meno soggetta a squilibri idrici e danni termici e consentendo quindi di crescere più vigorosa (La Malfa, 2001).
Il fusto è eretto nei primi stadi di sviluppo, poi diviene decombente e necessita di un tutore; è costituito da nodi ingrossati , dai quali si dipartono le foglie ed i getti ascellari, e da internodi più o meno lunghi dai quali nascono le infiorescenze. L’accrescimento è teoricamente illimitato, in quanto dopo ogni infiorescenza si ha la differenziazione di una nuova gemma apicale. Ciò non è del tutto corretto poiché vi sono tipi di accrescimento indefinito e definito; in questi ultimi l’apice vegetativo dello stelo e dei germogli, dopo aver dato luogo ad un certo numero di foglie e di infiorescenze, termina la crescita differenziando una infiorescenza, come accade in numerosi mutanti geneticamente modificati. Il fusto può raggiungere e superare altezze di 2m, con vigorose ramificazioni dicotomiche rigonfie nel punto di inserimento sul fusto principale (La Malfa,2001).
La disposizione delle foglie sugli steli è alterna esse sono imparipennate, picciolate, lunghe 20-30 cm e sono composte da 7-11 foglioline diseguali. Sono ricoperte di peli ghiandolari che secernono al contatto una sostanza dall’odore acre: la solanina. Si possono distinguere due forme di foglie, ossia quella normale
e quella a”patata”. Nel primo caso, il numero delle foglie è più elevato delle altre, il lembo è sottile, mentre il bordo è solitamente sinuato, inciso o dentato La foglia a patata è invece caratterizzata da un lembo fogliare più grande delle prime e con un margine generalmente intero.
La fioritura è scalare, con progressiva formazione delle infiorescenze in tempi ed in internodi successivi lungo il fusto principale e quelli secondari. I fiori sono ermafroditi con peduncoli articolati e riuniti in infiorescenze a racemo, portate lungo il fusto o sulle ramificazioni più grosse; il numero di fiori per infiorescenza è vario e nello stesso racemo la fioritura spesso non è contemporanea, infatti si possono avere nella stessa infiorescenza piccoli frutti, fiori aperti e fiori ancora chiusi.
Il fiore è dotato di un calice gamosepalo, costituito da 5 sepali verdi e persistenti; la corolla è rotata e con un numero di petali normalmente pari a 5 di colore giallo. Gli stami sono corti ed uniti fra loro a livello delle antere biloculari a formare una sorta di cono attorno al pistillo; l’ovario è supero e bicarpellare, ma si presenta plurisettato.
Lo stilo ha lunghezza variabile e si presenta slargato nella parte terminale a formare lo stigma, il quale può sporgere dal cono delle antere favorendo l’impollinazione incrociata (La Malfa, 2001).
1.4.3 Produzione, trasferimento e germinazione del polline
La microsporogenesi inizia già dopo la fioritura. La prima meiosi del polline delle cellule madri si verifica 9 giorni prima dell’antesi a 20 °C, quando l’antera è ancora ad un terzo della sua lunghezza finale. Il polline è formato da quattro tetradi e raggiunge la maturità in 4 giorni. Il numero potenziale di granuli pollinici è determinato geneticamente.
Da un singolo loculo di una antera possono maturare molti centinaia di granuli pollinici ad uno, due giorni dopo l’antesi. Le caratteristiche igroscopiche dell’endotecio possono provvedere alla forza meccanica richiesta per rompere la regione meno resistente dell’epidermide e l’assenza di spessore dell’endotecio ad alte temperature può essere causa del fallimento della deiscenza in alcune cultivar sensibili al calore. Le antere adiacenti sono collegate lateralmente da due filamenti
per formare un cono ed i granuli pollinici di tali antere vengono convogliati prima della dispersione in un canale comune nella zona di confine.
Il successivo trasferimento dei granuli pollinici allo stigma dipende dalla lunghezza dello stilo, e per avere una auto- impollinazione, lo stigma deve raggiungere la punta del cono dell’antera. La lunghezza dello stilo è determinato dalle condizioni genetiche e dalle condizioni di crescita. Infine i grani pollinici possono aderire allo stigma e dare luogo alla germinazione.
La germinazione del polline dipende dalla temperatura. Serve almeno un’ora a 25°C, 5 ore a 10°C o 20 ore a 5°C per fare germinare il polline. Il grado di germinazione si riduce a temperature al di fuori del range di 5-37°C. Il tasso di crescita del tubetto pollinico aumenta a temperature tra i 10 ed i 35°C, ma si riduce drasticamente al di fuori di questo range (Atherton and Rudich, 1986).
Le moderne cultivar di pomodoro sono auto- impollinatrici. Sebbene il polline maturo sia già pronto per essere trasferito durante l’apertura fiorale (antesi), lo stigma diventa pronto per riceverlo circa due giorni prima dell’antesi e rimane tale per 4 giorni o poco più. Una volta che il polline raggiunge lo stigma, i tubetti pollinici cominciano a crescere e possono raggiungere l’ovulo in 12 ore ad una temperatura di 25°C.
1.4.4 Anatomia del frutto
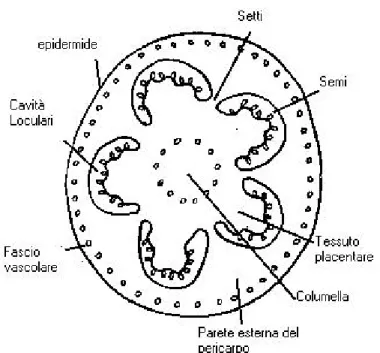
Il frutto di pomodoro è una bacca di grandezza e forma molto variabile, che si presenta così costituito:
-
Epicarpo o buccia
, formato da cellule poligonali molto appiattite che danno origine ad una pellicola che tende ad assottigliarsi man mano che il frutto si avvicina alla maturazione. La parete dell’epicarpo può essere divisa ulteriormente in una parete esterna, in pareti radiali che separano i loculi adiacenti (setti) ed in una parete interna (columella)- Mesocarpo o polpa,
formato dalle pareti delle logge costituite da uno strato più o meno spesso di cellule tondeggiante ed ovoidi, le cui sottili pareti sono costituite da cellulosa, emicellulosa e pectine.-
Endocarpo,
suddiviso in due o più logge delimitate da setti radiali, contenenti il tessuto placentare nel quale si trovano avvolti i semi in numero più o meno elevato.Figura 1 : Rappresentazione dell’anatomia del frutto di pomodoro in sezione trasversale.
1.4.5 Accrescimento del frutto e cambiamenti chimico- fisici
La crescita del frutto durante il suo sviluppo può essere descritta da una curva ad andamento sigmoide che può essere divisa in tre fasi:
- Una prima lenta crescita che dura 2-3 settimane e che porta il frutto a raggiungere circa il 10% del suo peso finale.
- Un secondo periodo più lungo che dura circa 3-5 settimane in cui si ha il picco di crescita in peso fresco ed in volume.
- Un ultimo periodo di crescita lenta in cui non c’è un alto incremento di peso ma avvengono importanti cambiamenti metabolici; per esempio il cambiamento di colore avviene 2-3 giorni dopo lo stadio mature green e progressivamente diventa da arancio a rosso.
La lenta crescita iniziale risulta dalla divisione e dalla successiva distensione cellulare, mentre la seguente rapida crescita è dovuta unicamente alla distensione cellulare; infine, l’ultima fase è caratterizzata più che dall’accrescimento, da profondi cambiamenti anatomici, fisiologici e metabolici che portano il frutto a maturare.
Uno dei principali cambiamenti fisici visibile ad occhio nudo è il cambiamento di colore, che avviene già 2-3 giorni dopo lo stadio mature green. Il passaggio dal colore verde chiaro dello stadio mature green al colore rosso è dovuto all’attività di degradazione della clorofilla combinata con l’intenso accumulo di β-carotene e licopene nella fase in cui si ha la trasformazione dei cloroplasti in cromoplasti (Archbold et al., 1982),
Dal momento che il colore della buccia è il principale indicatore dello stadio di maturazione della bacca, sono state sviluppate alcune scale di valutazione per classificare gli stadi maturativi del pomodoro in base alla colorazione della buccia (Tabella 2).
Stadio Descrizione
Verde Tutta la superficie del pomodoro appare verde
Breaker Prima apparizione di un colorito esterno roseo, rosso o giallo-tannino, che interessa non più del 10% della buccia
Invaiatura La colorazione rosea, rossa o giallo- tannino interessa un superficie che rientra tra il 10% ed il 30% della buccia Orange Più del 30%, ma meno del 60% della buccia appare rosa
o rossa
Pink Più del 60% ma meno del 90 % della buccia risulta rossa Red Ripe Più del 90 % della buccia risulta rossa. Questo è lo stadio di maturazione in cui il frutto è più adatto al consumo
Tabella 2. Classificazione degli stadi maturativi del frutto di pomodoro sulla base della
Nella prima settimana di sviluppo del frutto si verificano cambiamenti anatomici a carico delle cellule del pericarpo; due giorni dopo l’impollinazione i vacuoli presenti all’interno di ogni cellula si uniscono a formare un grosso vacuolo centrale e nel giro di un paio di settimane il citoplasma si riduce diventando un sottile strato delimitato alla periferia cellulare (Crooke and Grieson, 1983).
Oltre ai cambiamenti fisici rivestono molta importanza i cambiamenti chimici; uno dei quali è la variazione del contenuto in sostanza secca del pomodoro durante la maturazione; prima della fecondazione la sostanza secca costituisce il 17% del peso del frutto mentre si riduce al 5% a completa maturità (red ripe, RR). Gli elementi minerali più presenti, che rappresentano complessivamente il 90%, sono il potassio, l’azoto e il fosforo; tra questi il fosforo e l’azoto si riducono drasticamente durante la maturazione passando rispettivamente dal 3 allo 0,6% e dal 2 allo 0,4% mentre il contenuto di potassio rimane stabile .
Per quanto riguarda gli zuccheri, appena il frutto comincia a crescere, il contenuto di zuccheri riducenti passa dallo 0,2% presente nell’ovario al 2% dopo 2 settimane, per arrivare a rappresentare circa il 3% alla maturazione. Per quanto riguarda l’amido esso ha il massimo picco di accumulo 25-30 giorni dopo l’antesi ma poi durante la maturazione viene scisso per formare zuccheri riducenti. Esiste quindi una alta correlazione tra il contenuto di amido nei frutti allo stadio verde maturo (mature green, MG) e il contenuto totale di solidi solubili nei frutti RR (Dinar e Stevens, 1981). Il contenuto in acidi organici incrementa durante tutto lo sviluppo ed il pH di un frutto MG è di circa 4.0.
Tutti questi cambiamenti fisici e chimici portano quindi alla costituzione di un frutto complesso sia per quanto riguarda la struttura cellulare sia per quanto riguarda i sui costituenti nutraceutici.
In un frutto di pomodoro maturo si possono distinguere tre frazioni: polpa, buccia e semi, pari rispettivamente al 96-97%, 1,5-2,5% e 1,0-1,5% della sostanza secca. Un pomodoro maturo è costituito nella sua integrità per il 95% da acqua e per la rimanente parte da sostanze sospese e disciolte che rappresentano il residuo secco. Questo, alla maturazione completa, è formato da zuccheri (2-3,5%), acidi (0,25-0,50%), sostanze insolubili come pectine, cellulosa etc. (0,7-1.0%), amminoacidi e
proteine solubili (0,6-1,2%), elementi minerali (0,3-0,6%) e altri costituenti di cui fanno parte i composti antiossidanti come i carotenoidi, i polifenoli e le vitamine (0,15-0,20%).
Gli zuccheri sono rappresentati principalmente da glucosio e fruttosio che insieme rappresentano il 50% del residuo secco; gli acidi predominanti sono l’acido citrico e malico, che assieme costituiscono circa il 13% della sostanza secca. I composti insolubili sono costituiti da cellulosa, emicellulosa, pectine e lignina; questi composti sono responsabili della consistenza e compattezza del frutto. Gli amminoacidi rappresentano l’intera gamma di quelli considerati indispensabili dall’uomo. Altri composti quali fenoli, carotenoidi e vitamine hanno un ruolo primario come antiossidanti nei confronti delle specie ossigeno reattive causa di numerose patologie umane e sono quindi correttamente considerati composti essenziali, il cui contenuto è indice primario delle qualità salutistico-nutrizionali di un alimento (La Malfa, 2001).
1.4.6 Esigenze nutrizionali
Il pomodoro è una pianta con elevate esigenze termiche; è assai sensibile al gelo ed essendo originario delle zone tropicali, la sua stagione di crescita nei climi temperato-caldi corrisponde al periodo estivo. Negli altri periodi dell’anno deve invece essere coltivato in serra riscaldata.
I limiti termici per la germinazione del polline vanno da un massimo di 30°C ad un minimo di 10°C con un ottimo intorno ai 20-25°C. La temperatura ottimale per la fioritura è di 21°C mentre per la crescita della pianta passiamo da un minimo letale di 0°C ad un ottimo sui 22-26°C di giorno e 14-16°C di notte, con un massimo stimato a 30°C; infatti temperature superiori a tale valore provocano difetti di allegagione, difetti nella consistenza dei frutti e sulla colorazione delle bacche poiché a tali temperature il carotene continua a formarsi mentre si arresta la produzione di licopene facendo assumere alla bacca una colorazione giallo-arancio ed una consistenza molle.
Molto importanti per una ottimale crescita della pianta sono anche la disponibilità di luce e di CO2; infatti l’intensità e la qualità della luce possono influenzare
l’epoca della fioritura, l’allegagione e la colorazione delle bacche; inoltre sia la dimensione del frutto che il contenuto di solidi solubili sono fortemente influenzati dalla radiazione solare ricevuta. Quando la radiazione solare è più intensa, sia la materia secca che il contenuto di zuccheri raggiungono i loro livelli massimi. Gli effetti della luce sul metabolismo sono molteplici e spaziano dalla fissazione della CO2, alla sintesi proteica e dei pigmenti; un arricchimento di CO2 determina un aumento nella resa dei frutti, incrementandone il numero ed il peso. Estremamente importanti risultano essere le condizioni di pH del terreno e la disponibilità di minerali; il pomodoro si adatta a diversi tipi di terreno, ma predilige quelli ben drenati e ricchi di sostanza organica con un pH compreso tra 5.5 e 8.0. Per quello che riguarda la biodisponibilità dei minerali il pomodoro risulta essere una specie potassiofila cui seguono in ordine decrescente azoto, fosforo e calcio. Il potassio infatti influisce sulla qualità dei frutti migliorandoli per quel che concerne il contenuto di zuccheri, il residuo secco ed il colore, l’azoto stimola l’attività vegetativa; tuttavia, un eccesso di questo elemento potrebbe indurre un eccessivo rigoglio della vegetazione a danno dei frutti sia da un punto di vista quantitativo, poiché ci può essere un ritardo e una riduzione della fruttificazione, sia da un punto di vista qualitativo, con un peggioramento delle caratteristiche qualitative delle bacche. Infine il fosforo agisce sull’equilibrio tra fase vegetativa e riproduttiva, favorendo la formazione di tessuti più resistenti e la produzione di frutti e migliorando la consistenza delle bacche stesse. Anche il calcio ha un ruolo importante nella consistenza delle bacche in quanto una sua carenza porta al marciume apicale (La Malfa, 2001).
1.5 Antiossidanti nel pomodoro
1.5.1 I flavonoidi
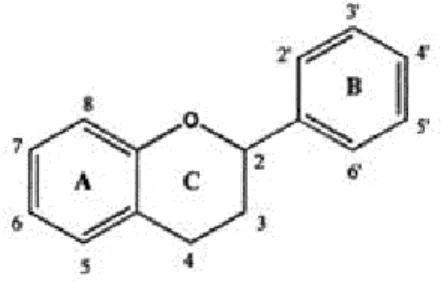
I flavonoidi sono composti pressoché ubiquitari e diffusi principalmente nelle piante superiori; allo stato attuale ne sono noti circa 4000. Da un punto di vista chimico sono composti che hanno in comune la struttura base del 2-fenil-α-benzopirone. Sono formati da due anelli aromatici tenuti insieme da un ponte a tre
atomi di carbonio (Figura 2) ed hanno come precursori per la loro sintesi il malonil-CoA ed il p-cumaril-CoA. Questi composti, prodotti dal metabolismo vegetale secondario, sono principalmente idrosolubili e solitamente presenti come glucosidi; nella stessa pianta un aglicone può essere combinato con zuccheri differenti.
Fig 2 : Struttura base di un flavonoide
Essi presentano molti gruppi ossidrilici su strutture ad anello, che conferiscono loro proprietà antiossidanti, infatti quali polifenoli vegetali, possono funzionare da agenti riducenti, da donatori di idrogeni, da chelanti di metalli e come quenchers (Herandez et al., 2009; Pietta, 2000). Complessando gli ioni ferro i flavonoidi interrompono la reazione di Fenton (Rice Evans et al., 1996).
La configurazione dei flavonoidi si basa su due anelli aromatici (A e B) legati da una catena a 3 atomi di carbonio (C6-C3-C6) che nella maggior parte dei casi è chiusa dall’ossigeno formando così un anello eterociclico; in alcune circostanze l’anello risulta aperto (calconi).
Le caratteristiche dei differenti gruppi di flavonoidi dipendono principalmente dalla configurazione dell’anello centrale che consente la seguente classificazione.
- Flavan-3-olo - Flavan-3,4-diolo - Flavanone - Flavanone-3-olo - Flavone - Isoflavone
- Flavone-3-olo - Calcone - Antocianidina
La famiglia dei flavonoidi include in maniera più generale sei sottogruppi principali: i calconi, i flavanoni, i flavonoli, i flavoni, le antocianine e gli isoflavoni.
I flavonoidi svolgono in natura funzioni di notevole importanza, come quella di impartire una colorazione ai fiori, frutti e foglie. Le colorazioni rosso, blu e violetto sono dovute alla presenza di antocianine, pigmenti derivati dai flavonoidi nei quali il nucleo γ-pironico è sostituito dallo ione pirossoinio carico positivamente. La tonalità gialla dipende dal numero di ossidrili legati all’anello benzilico del nucleo flavonico, l’intensità è tanto maggiore quanto più elevato è il numero di gruppi OH.
I flavonoidi agiscono inoltre come segnali chimici per alcune forme viventi come gli insetti; infatti è stato dimostrato come alcuni flavonoidi delle foglie abbiano una azione attrattiva o repulsiva sugli insetti e quindi siano in grado di condizionare questi ultimi nella scelta delle piante adatte alla deposizione delle uova oppure come fonte di nutrienti (Hartbone e Williams, 2000).
Oltre a determinare tali bellissime pigmentazioni, i flavonoidi hanno un ruolo chiave nel complesso sistema di segnali tra piante e microbi, nella fertilità maschile e come deterrenti per la predazione e la difesa da agenti indesiderati. Alcuni di questi flavonoidi infatti hanno lo scopo di inibire la germinazione delle spore fungine che si depositano sulla superficie delle foglie ed altri vengono sintetizzati in seguito all’infezione fungina e fungono come tossine in grado di ostacolare l’ulteriore estensione dell’invasione microbica e svolgendo il ruolo di fitoalessine (Hounsome et al., 2008).
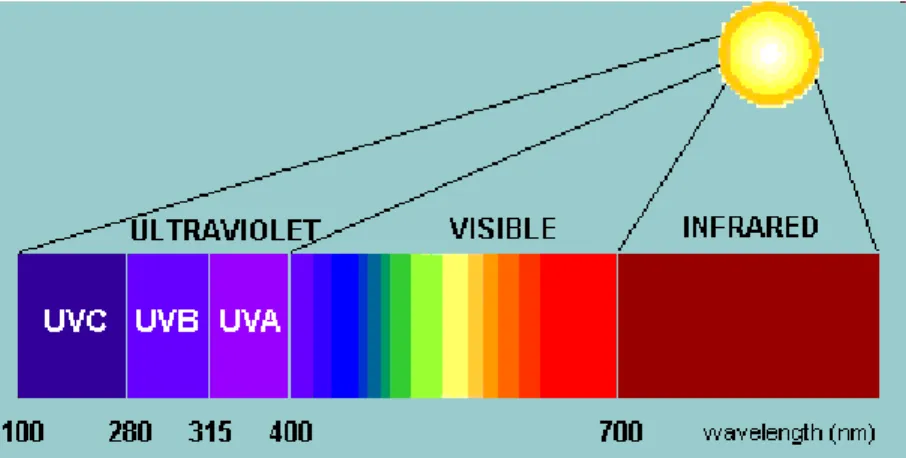
Non tutte le classi di flavonoidi assorbono la luce visibile, come accade per le antocianine che conferiscono pigmentazioni alle foglie ,fiori e frutti, ma è importante notare come i flavoni ed i flavonoli, pur non essendo colorati per l’occhio umano, assorbano molto fortemente nella regione UV dello spettro e possano essere quindi visti dagli insetti. Tale caratteristica può anche rappresentare
una protezione della pianta nei confronti della radiazione UV; infatti all’aumentare dell’altitudine, e quindi dell’irraggiamento UV, aumenta nella pianta la presenza di tali composti.
La caratteristica di alcuni flavonoidi di assorbire nell’ultravioletto è stata considerata un’evidenza del ruolo dei flavonoidi nella protezione da tali tipi di radiazioni (Sisa et al., 2010; Winkel e Shirley 2002; Agati e Tattini, 2006). Tale ipotesi è stata confermata mediante esperimenti con mutanti di Arabidopsis, che mostravano come alterazioni nella calcone sintasi (CSH) e nella calcone isomerasi (CHI) risultassero in fenotipi UV-ipersensibili; infatti la radiazione UV induce la sintesi di flavonoli con alti livelli di idrossilazione e, poiche l’idrossilazione non ha effetti sulle proprietà di assorbimento dell’UV, ma ha effetti sulla loro capacità antiossidante, questo ha suggerito che i flavonoli potessero giocare un ruolo nella risposta da stress a tali tipi di radiazioni ( Morales et al., 2010).
I flavonoli ed i flavanoni sono le principali sottoclassi dei flavonoidi presenti nei frutti; questi flavonoidi sono solitamente presenti come O-glucosidi, avendo uno zucchero coniugato, come il glucosio, il ramnosio, il rutinosio e l’arabinosio. La presenza di questi zuccheri incrementa la polarità dei flavonoidi così che,diventando più solubili, possano essere trasportati e immagazzinati all’interno dei vacuoli. I flavonoidi presenti principalmente nella frutta sono la quercitina ed il canferolo; nel frutto di pomodoro allo stadio di completa maturazione i principali flavonoidi presenti sono la rutina (quercitina-3-O-rutinoside), la naringenina-7-O-glucoside, la naringenina calcone ed il canferolo-3-rutinoside (Santangelo et al., 2007; Torres et al., 2005; Slimestad e Verheul, 2009).
Come componenti assunti con la dieta umana, i flavonoidi hanno svariate proprietà salutari e benefiche; innanzitutto esercitano un effetto protettivo sui vasi sanguigni in quanto riducono la permeabilità capillare ed aumentano la resistenza delle pareti vasali. Per spiegare l’azione vasoprotettiva possono essere invocati vari meccanismi di azione, tra cui ricordiamo l’azione stabilizzante delle membrane e quella di rigenerazione dell’acido ascorbico, capace a sua volta di rigenerare la vitamina E (Cossins et al., 1998).
L’azione positiva dei flavonoidi si estende anche al settore dei disturbi visivi; l’efficacia dei flavonoidi nelle retinopatie è ascrivibile in primo luogo ad un
aumento della resistenza delle pareti capillari e dei piccoli vasi e quindi ad un miglioramento della vascolarizzazione delle cellule coinvolte nei meccanismi della visione. Questo effetto è alla base del loro uso nei casi di miopia grave, di retinopatia e di degenerazione maculare dovuta ad arteriosclerosi (Majumdar e Srirangam, 2010; Hanneken et al., 2010).
L’azione di questi composti è anche motivata dal fatto che essi stimolano la trasformazione del trans-retinale in 11-cis retinale, ovvero favoriscono la rigenerazione della porpora retinica (rodopsina), con un effetto positivo sull’aumento del campo visivo ed il miglioramento della visione crepuscolare e notturna.
Tra le varie azioni dei flavonoidi, quella anti-infiammatoria riveste un ruolo estremamente importante e sembra essere dovuta principalmente all’inibizione dei radicali liberi dell’ossigeno ed al blocco degli enzimi coinvolti nel metabolismo dell’acido arachidonico; i flavonoidi interferiscono con tale metabolismo inibendo sia gli enzimi responsabili della sua liberazione dalle membrane (fosfolipasi) sia quelli coinvolti nel suo metabolismo (ciclossigenasi e lipossigenasi). In tal modo i flavonoidi sarebbero in grado di bloccare la sintesi di importanti mediatori chimici dell’infiammazione quali prostaglandine, tromboxani e leucotrieni. La capacità dei flavonoidi di inibire gli enzimi a cascata dell’acido arachidonico è legata alla loro azione di scavenger dei radicali liberi, a seguito della quale si interrompono i fenomeni di perossidazione lipidica che svolgono un ruolo importante nella regolazione dell’attività enzimatica delle ciclossigenasi (Hung et al., 2011).
In particolare è stato osservato come la quercitina inibisca diverse fosfolipasi, come il canferolo e la miricetina siano potenti inibitori delle lipossigenasi e come la rutina inibisca le ciclossigenasi (Pinto et al., 2011).
Tra le varie azioni benefiche è stata recentemente appurata anche una attività antivirale dei flavonoidi, soprattutto nei confronti del virus responsabile dell’immunodeficienza umana (HIV), responsabile dell’ AIDS: alcuni flavonoidi infatti sembrano svolgere una azione inibitoria diretta sull’attività del virus (Hartbone e Williams, 2000).
1.5.2 Biosintesi dei flavonoidi
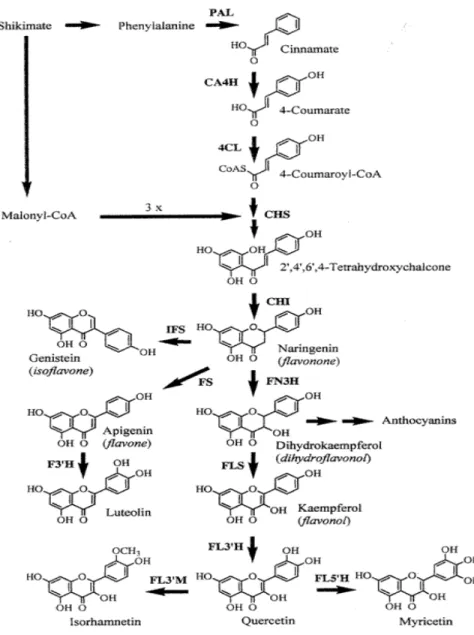
La figura 3. mostra il complesso pathway biosintetico dei flavonoidi. Il primo step è rappresentato dalla conversione dell’acetil-CoA in malonil-CoA, reazione catalizzata dall’enzima acetil-CoA carbossilasi. Poi tre molecole di malonil-CoA vengono condensate con una molecola di 4-cumaroil-CoA tramite la calcone sintasi (CHS).
Fig 3: Rappresentazione schematica delle ramificazioni più importanti nel percorso di
Non è noto se il meccanismo di ciclizzazione sia una reazione spontanea o sia invece catalizzata da una specifica ciclasi; tale reazione consta di una serie di riduzioni dei gruppi chetonici ad alcoli secondari.
L’enzima calcone isomerasi (CHI) catalizza la chiusura dell’anello eterociclico centrale, in particolare l’isomerizzazione del composto colorato in giallo 4,2’,4’,6’-tetraidrossicalcone nel composto incolore naringenina. Il flavanone naringenina viene convertito in diidrossicanferolo (DHK) grazie alla flavanone 3-idrossilasi (F3H). Il DHK funge da substrato per la sintesi dei flavonoli e delle antocianidine.
La flavonol sintasi (FLS) porta alla sintesi del flavonolo canferolo; le ossidrilazioni catalizzate dalla flavonoide 3’-idrossilasi (F3’H) e dalla flavonoide 3’-5’- idrossilasi (F3’5’H) rispettivamente portano alla diidroquercitina e alla diidromiricetina. La diidroquercitina viene trasformata in quercitina dalla FLS, e la diidromiricetina viene poi trasformata in miricetina dallo stesso enzima.
I diidroflavonoli sono incolori, e sono necessari altri tre enzimi per trasformarli in antocianidine ed antocianine colorate. Il primo enzima, la diidroflavonol 4-reduttasi (DFR), catalizza la riduzione dei diidroflavonoli in leucoantocianidine; l’antocianidina sintasi attua ulteriori processi di ossidazione, infine la glicosilazione delle leucoantocianidine avviene tramite l’enzima UDP glucosio:flavonoide 3-O-glucosiltrasferasi (3GT), per produrre le rispettive antocianine colorate.
L’enzima flavonoide metiltrasferasi opera un’esterificazione e successivamente avvengono glucosilazioni e metilazioni delle strutture formate, con l’ottenimento di ognuna delle sei classi di flavonoidi. E’ stato identificato un gene che regola tale via metabolica; tale gene è ANT1, ed è stato visto che la sua sovra-espressione causa la sovra-regolazione di geni che codificano per proteine sia nei primi stadi che negli ultimi della biosintesi di antocianidine, così come per geni coinvolti nella glicosilazione e nel trasporto di antocianine all’interno dei vacuoli. L’espressione di questo gene è normalmente bassa durante gli stadi di sviluppo e ristretta a tessuti specifici. Il gene ANT1 codifica per un fattore proteico MYB. Con l’incremento dell’espressione di ANT1 si ha la sovra-regolazione di un gene che
opera a valle e che codifica per la glutatione S-transferasi (GST). La sovra-espressione di ANT1 risulta in una alta regolazione dei geni che codificano per le proteine dei primi ed ultimi step della biosintesi delle antocianine, la calcone sintasi (CHS) e la diidroflavonolo riduttasi (DFR). Vengono sovra-regolati anche i geni che sembrano codificare per il 3-O-glucosiltransferasi e per il 5-O-glucosiltransferasi, così come per il tipo GST, una proteina che lega i flavonoidi, richiesta per il trasporto vacuolare; oltre a ciò, è stata notata la sovra-regolazione di altri tre geni: un gene simile alla calcone isomerasi (CHI-like), un omeodominio-GLABRA2 (HD-GL2) simile alla proteina HD-GL2 in Arabidopsis ed una permeasi simile alle proteine richieste per il trasporto vacuolare delle proantocianidine, come il gene TT12 in Arabidopsis (Mathews et al., 2003). In
Arabidopsis, il gene ICX1 è un regolatore negativo della biosintesi dei flavonoidi;
quindi il mutante icx1 porta ad un’elevata induzione del gene CHS e di altri geni legati a tale pathway (Wade et al., 2003).
1.5.3 Carotenoidi
I carotenoidi, sono pigmenti gialli liposolubili, situati all’interno delle membrane dei cloroplasti e dei cromoplasti, costituiti da otto unità isopreniche unite tra loro in modo tale che i gruppi metilici si trovino in posizione 1-6 ed i rimanenti gruppi non metilici siano in posizione 1-5. Possono essere sintetizzati ex novo in tutti gli organismi fotosintetici e anche in molti organismi non fotosintetici e conferiscono colorazione gialla, arancione o rossa a foglie fiori e frutti.
I carotenoidi si originano dalla via biosintetica dell’acido mevalonico, e l’acetil CoA rappresenta “il mattone” con il quale vengono costruiti.
Inizialmente si verifica la condensazione di due molecole di acetil CoA per formare l’acetoacetil CoA, azione catalizzata dall’enzima acetil CoA acetiltrasferasi; poi viene sintetizzato un composto a sei atomi di carbonio, il (3S)-3-idrossi-3-metilglutaril-CoA (HMG-CoA), tramite l’enzima HMG-CoA sintasi. L’HMG-CoA viene poi ridotto ad acido (3R)-mevalonico, in due tappe, con una reazione catalizzata dalla HMG-CoA reduttasi, che porta dapprima alla formazione
del tioemiacetale, poi questo per perdita del CoA porta alla formazione dell’acido mevaldico, e la seconda riduzione porta alla formazione dell’acido mevalonico. L’acido mevalonico viene trasformato in un composto a 5 atomi di carbonio, l’isopentenil pirofosfato, tramite la mevalonato chinasi e la fosfomevalonato chinasi.
La decarbossilazione del mevalonato-5-pirofosfato, che richiede ATP e metalli bivalenti, è catalizzata dalla pirofosfatomevalonato decarbossilasi. Si forma un’olefina, l’isopentenil pirofosfato (IPP), e viene persa una molecola di CO2 e una funzione ossidrilica.
L’IPP viene considerato l’elemento di base per la costruzione di tutti gli altri terpenoidi, infatti viene isomerizzato dalla IPP isomerasi, con la formazione del dimetilallil pirofosfato (DMAPP).
L’enzima isoprene sintasi catalizza l’eliminazione del gruppo difosfato del DMAPP per formare l’isoprene, un composto volatile.
Gli enzimi prenil-trasferasi catalizzano poi la condensazione di una molecola di isopentenil pirofosfato con un pirofosfato allilico, determinando quindi l’aggiunta di 5 atomi di carbonio alla molecola di origine. Per esempio, la preniltrasferasi GPP sintasi catalizza la condensazione dell’IPP con il DMAPP, per formare il geranil pirofosfato (GPP), una molecola a dieci atomi di carbonio,da cui hanno origine tutti i monoterpeni. La più importante trasformazione è rappresentata da una ciclizzazione dell’anello, catalizzata da enzimi definiti ciclasi, e che porta ad una gran varietà di molecole.
Dalla condensazione di una molecola di IPP con una di GPP, reazione catalizzata dalla farnesil pirofosfato sintasi, si ottiene una molecola di farnesil pirofosfato (FPP).
Anche l’FPP può andare incontro a reazioni di ciclizzazione; la condensazione di due molecole di FPP invece può portare alla formazione di una molecola a trenta atomi di carbonio, lo squalene, ad opera della squalene sintasi, enzima che può catalizzare anche l’eliminazione del residuo pirofosforico dal presqualene pirofosfato.
La condensazione di una molecola di FPP con una di IPP, che viene catalizzata dall’enzima GGPP sintasi, può dare luogo ad una molecola di GGPP (geranilgeranil pirofosfato).
Dalla condensazione di due molecole di GGPP si ottengono i tetraterpeni, composti formati da 8 unità isopreniche (40 atomi di carbonio).
L’enzima fitoene sintasi (PSY) catalizza la condensazione di due molecole di GGPP e porta alla formazione di prefitoene pirofosfato (PPPP) e successivamente di fitoene, per distacco del gruppo pirofosforico in C-1. Tale composto è incolore, e con successive desaturazioni può essere convertito in carotenoidi colorati, che presentano doppi legami coniugati.
Dopo 4 desaturazioni si forma il pigmento rosso licopene, mentre prima si formano fitofluene (incolore), ζ-carotene (giallo) e neurosporene (arancio).
Sul licopene, con la presenza del FAD, agisce la licopene ciclasi, portando alla formazione di β-carotene.
Le xantofille sono idrossi, epossi, furanossi e ossi derivati carotenoidici. Per ossidazione degli anelli iononici in posizione 3 e 3’ si formano le prime xantofille, tra cui la zeaxantina; un’ulteriore epossidazione nelle posizioni 5,6 e 5’,6’ porta alla formazione di xantofille quali la violaxantina. In questa ultima reazione, l’epossidazione può avvenire in presenza di luce e può portare alla interconversione della violaxantina nella zeaxantina, e viceversa.
Le xantofille, ma più precisamente tutti i carotenoidi, sono estremamente importanti in quanto mattoni fondamentali dei complessi antenna dei fotosistemi necessari per la cattura della luce. Infatti, in associazione con le clorofille e componenti proteiche definite CAB, i carotenoidi partecipano alla costituzione di complessi proteina-pigmento dei quali il più abbondante è l’LHCII, il complesso antenna del fotositema II (Maffei, 1998).
La funzione principale dei complessi antenna è di trasferire energia ai centri di reazione dei fotosistemi I e II e dato che l’energia viene ceduta per risonanza è indispensabile che alcuni pigmenti siano localizzati alla periferia del complesso. Oltre alle antenne maggiori (LHCI e LHCII) esistono complessi proteina pigmento denominati antenne minori, tra i quali i complessi CP23, CP26,CP29 (Cohen et al., 1995). Il ruolo di questi complessi è quello di mediare il trasferimento di energia
dai complessi LCHII ai centri di reazione, ma anche di calibrare le dimensioni dell’antenna in risposta alle condizioni di luce, dissociandosi o associandosi l’un l’altro e anche cambiando l’efficienza del trasferimento di energia attraverso l’azione del ciclo delle xantofille (Simpson e Knoetzel, 1996).
I carotenoidi, grazie alla loro struttura, oltre ad essere componenti fondamentali dei complessi antenna per la percezione della luce, esplicano funzioni protettive ed antiossidanti, bloccando la formazione delle ROS e specialmente dei radicali idrossilici e perossilici. Questa funzione è esercitata anche grazie al ciclo delle già citate xantofille deputato alla dissipazione dell’energia in eccesso sotto forma di calore. In particolare, quando la radiazione luminosa eccede la capacità dei fotosistemi di utilizzarla a fini fotosintetici, si realizza la de-epossidazione della violaxantina a zeaxantina, attraverso l’intermedio anteraxantina. La dissipazione di energia non radiante da parte della zeaxantina e, in misura minore, dell’anteraxantina, contribuisce a prevenire l’insorgenza dello stress foto-ossidativo dannoso per la pianta (Demmig Adams e Adams, 1996).
Oltre alla funzione antiossidante i carotenoidi possono agire come ormoni vegetali. Carote e pomodori, sono esempi eccellenti di fonti di carotenoidi importanti nella dieta umana come antiossidanti (Tonucci et al., 1995). I carotenoidi maggiormente presenti nel pomodoro sono il licopene, il β-carotene e la luteina.
Il licopene è un carotenoide insaturo a catena aperta ed è un isomero aciclico del β-carotene; è un efficace antiossidante e un ottimo radical quencher dell’ossigeno singoletto. Questo carotenoide inibisce l’ossidazione del DNA, delle proteine a bassa densità (LDL) e la perossidazione lipidica; a differenza del β-carotene, non viene trasformato in vitamina A, ma svolge la sua azione antiossidante indipendentemente. Nei frutti si ritrova prevalentemente sotto forma strutturale di isomero trans, ma l’assorbimento a livello intestinale è maggiore se la configurazione della molecola è cis. Dal momento che la cottura favorisce la trasformazione della forma trans a forma cis, il prodotto cotto ha una maggiore biodisponibilità di licopene ed una maggiore attività antiossidante ascrivibile a questo composto nutraceutico (Honest et al., 2011).
L’assorbimento del licopene, che è un composto lipofilo, è influenzato dalla presenza dei lipidi; infatti, una volta assorbito, esso si unisce alle micelle lipidiche
e attraversa la mucosa intestinale per trasporto passivo. La sua incorporazione nei chilomicroni, particelle lipopropteiche costituite da trigliceridi, fosfolipidi, colesterolo e proteine, consente il trasferimento al fegato dal quale tali complessi entrano nel torrente sanguigno per raggiungere i tessuti periferici ricchi in LDL quali prostata, surrene e testicoli.
Il ruolo fondamentale del licopene risiede nella capacità di inibire l’ossidazione delle LDL. Le LDL ossidate hanno una maggiore affinità per le pareti delle arterie, portando quindi più facilmente alla formazione di placche arteriosclerotiche. Il licopene svolge quindi un ruolo chiave nella patogenesi della arteriosclerosi, disordine che porta all’ischemia ed all’infarto (Riccioni, 2009).
Un’altra funzione del licopene risiede nella sua capacità di ridurre i livelli del colesterolo LDL, inibendo l’idrossi-metil-glutaril-CoA riduttasi, ovvero l’ultimo enzima della sintesi del colesterolo.
La caratteristica principale del licopene, ovvero la funzione antiossidante, è confermata dal fatto che è in grado di detossificare l’ossigeno singoletto due volte più velocemente del β-carotene e 10 volte più velocemente dell’α-tocoferolo. Altre importanti funzioni del licopene risiedono nella capacità di essere un potente inibitore della proliferazione delle cellule cancerogene, un antiinfiammatorio ed un anticoagulante; in particolare è stato visto come il licopene agisca specificatamente nel ridurre il rischi di cancro colon-rettale, della prostata e del pancreas (Singh et al., 2008).
Nel pathway biosintetico dei carotenoidi, a valle della sintesi del licopene, la licopene ciclasi porta alla formazione del β-carotene.
Il β-carotene oltre ad essere un composto nutraceutico fondamentale in virtù della sua azione antiossidante, riveste un ruolo importante per la salute umana poiché rappresenta il precursore della vitamina A. Infatti il β-carotene, una volta assorbito dalla mucosa intestinale e dal fegato, diviene il substrato di una diossigenasi che può portare alla formazione di tre molecole: il retinolo tutto trans (vitamina A), l’11-cis retinaldeide e l’acido retinoico. In particolare una β-carotene diossigenasi porta alla formazione di due molecole di retinale, che attraverso l’azione di una retinaldeide reduttasi formano due molecole di retinolo tutto trans.
Successivamente, attraverso l’azione di una isomerasi, si ha la formazione dell’11-cis-retinolo, che dal fegato passa nella retina.
Il retinolo tutto trans e l’11-cis retinaldeide sono estremamente importanti poiché entrano a far parte del ciclo visivo umano. Nella retina l’azione di una alcool deidrogenasi porta all’ossidazione dell’11-cis-retinolo con formazione dell’11-cis retinale. La conformazione di tale molecola in forma cis la rende capace di legarsi, attraverso la formazione di una base di Schiff (immina), al gruppo amminico di una proteina retinica chiamata opsina; tale combinazione, che avviene solamente in condizione di assenza di luce, porta alla formazione della rodopsina o porpora retinica, che è un pigmento retinico del fotorecettore, responsabile della visione notturna. L’unione di questi due composti avviene solamente in assenza di luce, poiché in presenza di luce l’energia dei fotoni che colpiscono la rodopsina ripristina la configurazione trans del doppio legame del retinale 11-cis, che si trasforma quindi in retinale tutto trans. La conformazione nello spazio di tale molecola non permette l’unione con la opsina e si ha quindi il distacco della opsina e del retinale tutto trans; tale molecola attraverso una retinene isomerasi viene trasformato in 11-cis retinale che in condizioni di assenza di luce può riprendere il ciclo visivo.
Da questa sintesi è possibile notare l’importanza dell’assunzione del β carotene, in quanto molecola fondamentale per il ciclo visivo ed il miglioramento della visione scotopica.
Non di minor importanza, per quanto riguarda l’azione antiossidante, risulta la xantofilla luteina. L’importanza della luteina risiede in primo luogo nella sua specifica azione antiossidante, ma anche nella proprietà di assorbire la radiazione ultravioletta e nella caratteristica di accumularsi in specifiche parti dell’occhio umano. Infatti la luteina e la zeaxantina sono gli unici carotenoidi che si ritrovano nella macula retinica, una piccola area della retina fondamentale per la visione, specialmente per quanto riguarda la nitidezza. Inoltre la luteina è l’unico carotenoide presente nel cristallino. Questa caratteristica, legata alla capacità di assorbire i raggi UV, fa sì che la luteina prevenga il rischio di degenerazione maculare e, in misura minore, di cataratta. E’ stato inoltre evidenziato come la
luteina sia in grado di prevenire il cancro al colon ed al polmone (Motohashi, 2006).
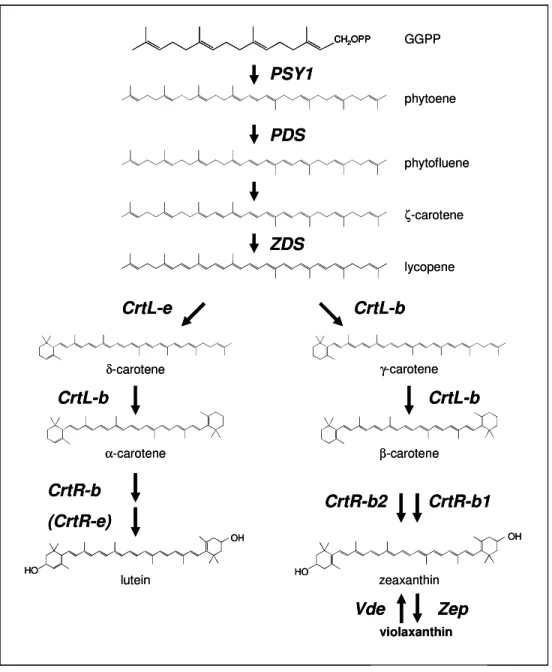
Fig. 4: Rappresentazione schematica della via biosintetica dei carotenoidi
GGPP phytoene phytofluene ζ-carotene lycopene CrtL-b δ-carotene CrtL-e CrtL-b α-carotene CrtR-b1 CrtR-b2 lutein Vde Zep violaxanthin CrtL-b β-carotene zeaxanthin γ-carotene CrtR-b (CrtR-e) PSY1 PDS ZDS CH2OPP CH2OPP OH HO OH HO GGPP phytoene phytofluene ζ-carotene lycopene CrtL-b δ-carotene CrtL-e CrtL-b α-carotene CrtR-b1 CrtR-b2 lutein Vde Zep violaxanthin CrtL-b β-carotene zeaxanthin γ-carotene CrtR-b (CrtR-e) PSY1 PDS ZDS CH2OPP CH2OPP OH HO OH HO OH HO OH HO
1.5.4 Vitamine
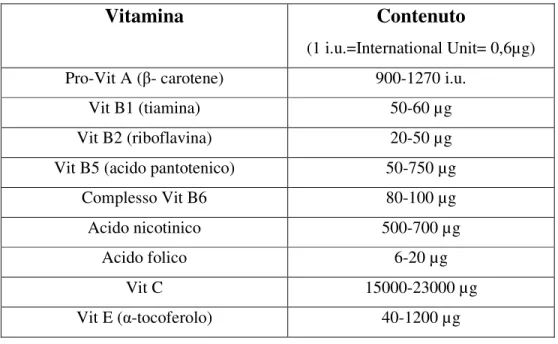
Il pomodoro oltre ad essere una ottima fonte di carotenoidi (tra cui il β-carotene o provitamina A), contiene numerose vitamine, quali la vitamina C (acido ascorbico), la vitamina E e l’acido nicotinico o VIT B5, come riportato nella tabella 3 sottostante.
Vitamina
Contenuto
(1 i.u.=International Unit= 0,6µg)
Pro-Vit A (β- carotene) 900-1270 i.u.
Vit B1 (tiamina) 50-60 µg
Vit B2 (riboflavina) 20-50 µg
Vit B5 (acido pantotenico) 50-750 µg
Complesso Vit B6 80-100 µg
Acido nicotinico 500-700 µg
Acido folico 6-20 µg
Vit C 15000-23000 µg
Vit E (α-tocoferolo) 40-1200 µg
Tabella 3: Contenuto vitaminico di un pomodoro maturo (da Davies e Hobson, 1981)
Vitamina C
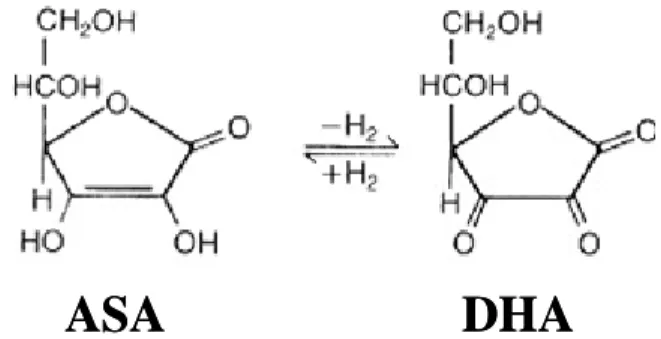
L’acido ascorbico è una molecola organica che si presenta sotto forma di cristalli dal sapore acidulo; è solubile in acqua e abbastanza solubile in etanolo all’80%. L’acido ascorbico ha elevato potere riducente, quindi si ossida facilmente all’aria, portando alla formazione di acido L-deidroascorbico. Nelle piante è piuttosto abbondante e si accumula in concentrazione intracellulare di 2-25 mM
.
L’acido ascorbico introdotto con gli alimenti è assorbito dal tratto gastro-intestinale in maniera molto simile al glucosio; l’assorbimento infatti avviene tramite diffusione passiva, se la concentrazione è rilevante, o mediante trasporto attivo nel caso di piccole dosi. La forma ossidata (acido L-deidroascorbico), in relazione alla sua maggiore lipofilia, è assorbita più facilmente della forma ridotta,
che a pH fisiologici si trova in forma anionica. Nell’intestino si realizza l’ossidazione dell’ASA a DHA che è trasportato più velocemente attraverso le membrane cellulari. All’interno delle cellule la vitamina C viene quindi ripristinata in forma ridotta, in grado di agire come antiossidante e come scavenger dei radicali liberi.
Oltre a questa importantissima funzione l’acido ascorbico svolge una azione fondamentale nella sintesi del collagene, una proteina del tessuto connettivo costituita da fibre insolubili in acqua e che possiedono una elevata resistenza alla tensione. Il collagene rappresenta il principale elemento fibroso della pelle, delle ossa, della cartilagine e dei denti. La sua struttura primaria mette in evidenza, oltre a numerosi residui di glicina, anche due aminoacidi quali la 4-idrossiprolina e la 5-idrossilisina, che si formano per idrossilazione rispettivamente della prolina e della lisina. Gli enzimi coinvolti in questa reazione (prolil e lisil idrossilasi) contengono nel loro sito attivo un atomo di ferro; affinchè l’enzima possa esercitare la propria funzione è necessario che l’atomo di ferro sia nella forma Fe2+. In assenza di acido ascorbico, che mantiene il ferro allo stato ridotto, si forma un collagene povero di questi due aminoacidi, con perdita delle proprietà funzionali proprie del collagene idrossilato. La mancata formazione delle fibrille di collagene di consistenza adeguata determina lo scorbuto, caratterizzato da lesioni della pelle, affaticamento muscolare, gengive gonfie e molli, fragilità dei vasi sanguigni, osteoporosi e anemia (Paoletti, 1998).
Oltre ad essere importante per la sintesi del collagene, l’acido ascorbico è fondamentale per la biosintesi della carnitina, una molecola essenziale per il trasporto degli acidi grassi a lunga catena nei mitocondri, organelli sede della β-ossidazione. Pertanto, nel caso di carenza di acido ascorbico, si può verificare una significativa alterazione del metabolismo dei lipidi.
La VIT C interviene attivamente nelle reazioni di idrossilazione microsomiale che l’organismo attua per facilitare l’escrezione di composti xenobiotici tossici, come ad esempio gli idrocarburi policiclici aromatici (IPA).
L’acido ascorbico interviene anche a livello del sistema nervoso centrale e nelle ghiandole surrenali, nella formazione delle catecolamine, rappresentate dalla noradrenalina, adrenalina e dopamina, che si ottengono per idrossilazione della