1
1. INTRODUZIONE
1.1 L’uva
L’uva è la materia prima dell’industria enologica; a livello botanico è una bacca classificata nel gruppo della frutta carnosa con semi, che deriva dall’infiorescenza della Vitis vinifera.
Avvenuta la fecondazione del fiore, l’ovario si trasforma in un piccolo acino (allegazione), che aumenta progressivamente di volume e di peso, diventando un frutto dal nome botanico di bacca.
La bacca è legata al raspo mediante un pedicello, che serve a condurre le sostanze nutritive, attraverso la linfa ascendente, dal terreno fino alla bacca ossia all’acino.
L’infruttescenza della vite si presenta sotto forma di grappolo, costituito da un supporto erbaceo detto raspo o graspo, con un asse centrale detto rafide, suddiviso in numerose ramificazioni, dette racimoli, che terminano con i pedicelli portanti l’acino. Quest’ultimo presenta forma, peso e colore diversi principalmente in base alla varietà o cultivar di appartenenza, ma anche a seconda della tecnica di allevamento delle piante, non disgiunta dalle condizioni pedo-climatiche.
La forma più frequente dell’acino delle uve da vino è la forma sferica, talvolta più o meno allungata. Per quanto riguarda il colore, le uve possono essere bianche, rosse o nere. L’acino incomincia ad assumere la sua colorazione, abbandonando l’originario color verde, all’invaiatura e soltanto a maturazione completa appare nella sua colorazione definitiva.
L’intensità del colore può variare considerevolmente da un’annata all’altra, in quanto la sintesi di sostanze colorate (antociani) da parte della vite è influenzata sensibilmente dalle condizioni climatiche, che costituiscono un parametro variabile e incontrollabile della produzione enologica.
2
L’acino, in continuo aumento dalla fase di allegagione, raggiunge il suo peso definitivo a maturazione; in questa fase, il peso varia da 1 a 5 g a seconda della varietà, della tecnica di allevamento e delle condizioni pedo-climatiche.
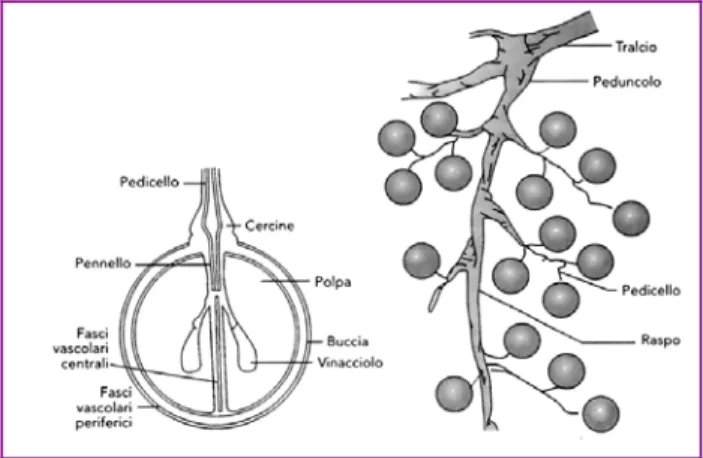
Gli acini sono generalmente piccoli nelle uve da vino, e il loro peso varia anche in relazione al numero e alla grandezza dei vinaccioli (Figura 1).
Figura 1: Frutto della vite, a sinistra l’acino d’uva a maturità, a destra la struttura del grappolo (Ribereau – Gayon et al., 2006)
L’acino contiene normalmente quattro vinaccioli, che derivano dai quattro ovuli fecondati dell’ovario; spesso, però , i vinaccioli sono tre o due o uno solo a causa dell’aborto di uno o più ovuli.
Talvolta l’acino è apirene, cioè senza vinaccioli, oppure contiene vinaccioli molto piccoli e vuoti all’interno a causa di una difettosa fecondazione. In questo caso l’acino ha una crescita ridotta, resta piccolo e presenta un maggior contenuto zuccherino; questi acini sono detti acinellati (acinellatura).
L’assenza di vinaccioli (apirenia) negli acini è una caratteristica della varietà, particolarmente apprezzata per le uve da tavola e per le uve destinate alla preparazione di uve passite.
Allo stato fresco, i vinaccioli costituiscono il 4-6% del peso delle uve e la loro composizione percentuale è riportata nella Tabella 1.
Dal punto di vista morfologico, ciascun vinacciolo è formato da una mandorla grassa (albume) avvolta da un guscio legnoso, che a sua volta è racchiuso da una cuticola.
3
Caratteristica fondamentale del vinacciolo, dal punto di vista enotecnico, è il suo elevato contenuto in sostanze tanniche, che migrano nei vini soprattutto durante la macerazione nella vinificazione in rosso.
La maturazione fisiologica del vinacciolo, corrispondente al momento in cui il vinacciolo è in grado di riprodurre una nuova pianta, avviene nella maggior parte dei casi alla maturazione industriale della polpa, cioè quando l’uva ha raggiunto il più elevato contenuto in zuccheri. Non sempre, però, questo avviene; nelle varietà tardive, ad esempio, la maturazione fisiologica dei vinaccioli si verifica prima della vendemmia, mentre nelle uve precoci, come quelle da tavola, il vinacciolo acquista la capacità di germinare dopo la maturazione industriale, durante la fase di sovramaturazione, nella quale l’apporto al vinacciolo di sostanze necessarie al suo completo sviluppo è ancora in atto.
Allo stato secco, i vinaccioli contengono in media il 13% di sostanza grassa; per questo motivo, i vinaccioli vengono utilizzati per l’estrazione dell’olio, che, dopo rettifica, viene normalmente usato per l’alimentazione umana.
Acqua 30 – 40 Sostanze grasse 9 – 18 Sostanze tanniche 4 – 6 Sostanze glucidiche 32 – 36 Sostanze azotate 4 – 6 Sostanze minerali 1 -4
Tabella 1: Composizione percentuale dei vinaccioli (Sciancalepore, 1998)
La polpa è la parte più importante dell’acino in quanto il contenuto vacuolare delle sue cellule fornisce il mosto, e rappresenta, a maturazione, dal 75 al 95% dell’intero acino.
I suoi principali costituenti sono: acqua, zuccheri, acidi organici, sostanze minerali, azotate, pectiche e odorose.
4
Gli zuccheri sono rappresentati essenzialmente da glucosio e fruttosio anche se sono stati identificati altri tipi, quali saccarosio, arabinosio, xilosio, maltosio ecc. Il contenuto in zuccheri delle uve varia, in genere, da 150 a 250 g/l. Tuttavia, in casi eccezionali e per cultivar particolari (cv. Moscato) le uve possono presentare un tenore in zuccheri sensibilmente più elevato.
Gli acidi organici variano sensibilmente sia da un punto di vista qualitativo sia quantitativo in base alla varietà e al clima dell’annata. Gli acidi più rappresentati sono il tartarico, il malico e il citrico; questi si trovano anche in tutti gli altri tessuti vegetali della vite. Sia pur in quantità estremamente modeste, sono stati identificati altri acidi quali l’ascorbico, il d-chetoglutarico, il fumarico ecc.
La polpa risulta particolarmente ricca in elementi minerali; il potassio è certamente l’elemento principale, seguito dal calcio, dal magnesio e dal sodio. L’acido fosforico è l’anione più rappresentativo.
Le sostanze azotate sono presenti in forma ammoniacale e in forma organica; quest’ultima è costituita da amminoacidi, polipeptidi e proteine, che, insieme, costituiscono il miglior alimento azotato dei lieviti.
Le sostanze pectiche che si ritrovano nella polpa sono rappresentate dalla pectina solubile, che si differenzia dalla pectina insolubile o protopectina che si ritrova fissata alla parte solida dell’uva.
Le sostanze odorose, responsabili dell’aroma caratteristico del vino e principalmente presenti nella buccia, si ritrovano presenti in piccole quantità nella polpa. La composizione delle sostanze odorose è molto complessa; le tecniche analitiche oggi disponibili hanno identificato oltre 500 costituenti, per lo più volatili.
I componenti della polpa non sono distribuiti uniformemente in modo da formare un sistema omogeneo; in una sezione trasversale della polpa, infatti, si possono distinguere tre zone:
- una zona interna, cioè attorno ai vinaccioli, con il più basso contenuto in zuccheri e il più alto contenuto in acidi;
- una zona mediana con il più elevato contenuto in zuccheri e con bassi contenuti in sostanze polifenoliche;
5
- una zona esterna, a contatto con la buccia, ricca di sostanze polifenoliche e povera di acidi e sostanze zuccherine.
L’involucro della polpa è costituito dalla buccia (Tabella 2); questa è formata da uno strato di cellule epidermiche che, insieme, rappresentano l’epidermide o buccia dell’acino. Lo spessore della buccia è diverso a seconda della varietà o cultivar dell’uva e varia da 1,5 a 3,8 µm nelle varietà di Vitis vinifera.
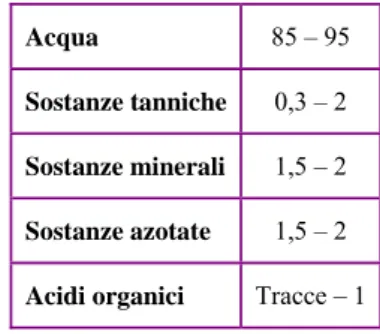
Acqua 85 – 95
Sostanze tanniche 0,3 – 2
Sostanze minerali 1,5 – 2 Sostanze azotate 1,5 – 2 Acidi organici Tracce – 1
Tabella 2: Composizione percentuale della buccia (Sciancalepore, 1998)
La buccia è rivestita da una cuticola, che a sua volta è coperta di pruina, una sostanza cerosa che conferisce l’aspetto vellutato all’acino. La pruina è costituita essenzialmente da un estere dell’acido palmitico (C15H31COOH),
con alcol triossilico [C26H39(OH)3]; per saponificazione fornisce altri composti
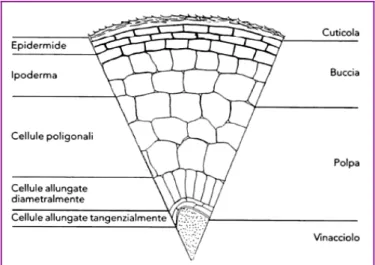
quali alcoli, esteri, acidi grassi, aldeidi. La pruina rende la buccia non bagnabile, ma soprattutto serve a trattenere i lieviti (o microrganismi in genere), apportati dal vento, dalla polvere e dagli insetti, necessari ad assicurare la fermentazione del mosto (Figura 2).
Il tenore in zuccheri delle cellule della buccia è molto basso. A parità di peso, la buccia è ricca in acidi come la polpa, ma è soprattutto l'acido citrico che predomina. L'acido malico, che è presente in notevole quantità nella buccia dell'acino acerbo, viene in seguito attivamente metabolizzato nel corso della maturazione. L'acido tartarico è per la maggior pane esterificato dagli acidi fenolici (acido caffeico, acido cumarico). Poiché una quantità rilevante di cationi salifica questi acidi, il pH del contenuto di queste cellule della buccia è sempre più elevato di quello della polpa.
6
La buccia è caratterizzata, soprattutto, da quantità rilevanti di prodotti secondari di importanza enologica fondamentale (composti fenolici e sostanze aromatiche), che si accumulano durante la maturazione.
I composti fenolici presenti nella buccia dell’uva a maturità sono acidi benzoici e cinnamici, flavonoli e tannini: essi si ripartiscono nelle cellule dell'epidermide e nei primi strati sottoepidermici sia nelle uve bianche sia nelle uve rosse.
La buccia dell'uva rossa contiene, inoltre, antociani essenzialmente localizzati negli strati cellulari dell'ipoderma.
Le cellule adiacenti alla polpa possono essere eccezionalmente colorate in alcune annate, anche la polpa stessa è colorata nelle varietà “teinturiers” ed in alcune varietà americane o ibridi produttori diretti. La composizione in antociani varia da una varieta all'altra; essa dipende dai sostituenti delle antocianidine e dalla loro natura eterosidica
La buccia dell'uva matura contiene importanti quantità di sostanze aromatiche e di precursori d'aroma.
Figura 2: Morfologia schematica dei diversi tessuti dell'acino d'uva a maturità (Ribereau – Gayon et al., 2006)
7
Gli acini dell’uva sono portati dal raspo che ha il compito di collegare l’acino al tralcio della vite con la sua linfa ascendente.
Il raspo raggiunge le sue dimensioni definitive prima della completa maturazione dell’acino; rappresenta il 2,5 – 7% del peso del grappolo alla maturazione dell’uva.
La composizione chimica del raspo (Tabella 3) assomiglia a quella delle foglie: è povero in zuccheri ed ha una ricchezza media in acidi (180-200 meq/kg), che sono salificati a causa della presenza di cationi in quantità rilevante.
I raspi sono ricchi di composti fenolici e possono contenere sino al 20% dei composti fenolici totali del grappolo; si tratta di molecole più o meno polimerizzate a forte sapore astringente.
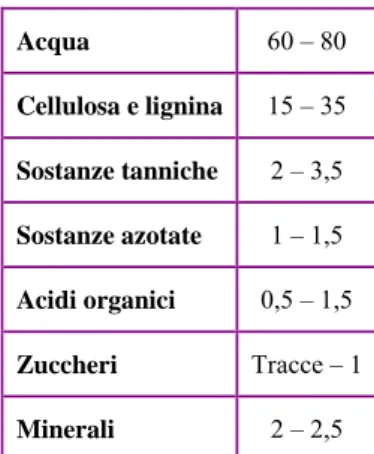
Non subiscono variazioni notevoli durante il periodo di maturazione, ad esclusione del contenuto in acqua che diminuisce progressivamente durante la maturazione in relazione al progredire della lignificazione dei tessuti vegetali del raspo. Acqua 60 – 80 Cellulosa e lignina 15 – 35 Sostanze tanniche 2 – 3,5 Sostanze azotate 1 – 1,5 Acidi organici 0,5 – 1,5 Zuccheri Tracce – 1 Minerali 2 – 2,5
Tabella 3: Composizione percentuale del raspo (Sciancalepore, 1998)
In definitiva, costituenti dell’uva sono racchiusi tutti nel grappolo, che rappresenta la materia prima avviata in cantina per la vinificazione.
Il grappolo si presenta, a maturazione, in forme diverse (alato, sferico, a fittone, a forma di cono) e di peso variabile da 150 – 200 g (nelle uve da vino) fino a 3 Kg e oltre (nelle uve da tavola); le parti che lo costituiscono sono il
8
succo d’uva (mosto), i raspi, le bucce e i vinaccioli, nelle proporzioni riportate in Tabella 4.
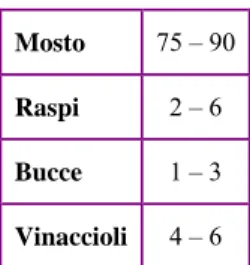
Mosto 75 – 90
Raspi 2 – 6 Bucce 1 – 3 Vinaccioli 4 – 6
Tabella 4: Composizione percentuale del grappolo (Sciancalepore, 1998)
1.1.1 La maturazione dell’uva
Avvenuta la fecondazione, l’ovario si trasforma in un piccolo acino (allegagione), che aumenta progressivamente di peso e di volume, diventando sede di profonde trasformazioni anatomiche, fisiche e chimiche fino a raggiungere prima lo stato di maturazione fisiologica, in cui i vinaccioli risultano germinabili e quindi in grado di riprodurre la pianta, e poi lo stato di maturazione industriale durante la quale viene effettuata la vendemmia.
Nel ciclo evolutivo dell’acino si possono distinguere i seguenti stadi di sviluppo (Figura 3):
- periodo erbaceo; - invaiatura; - maturazione;
- la sovramaturazione (quando l’uva non viene raccolta).
Nella fase erbacea l’acino funziona come organo verde, accumula la clorofilla al di sotto dell’epidermide, aumenta di volume e di peso fino a raggiungere la forma definitiva e il suo peso massimo, accumulando notevoli quantità di acidi organici e piccole quantità di zuccheri rappresentati essenzialmente da glucosio. Questa fase dura da 45 a 65 giorni, a seconda della varietà e delle condizioni ambientali.
9
La successiva fase dell’invaiatura si manifesta con il cambio del colore dell’acino. Inizialmente questa fase interessa soltanto alcuni acini del grappolo, successivamente si estende a tutti gli altri. L’invaiatura, dunque, è caratterizzata dalla scomparsa della clorofilla (ne rimangono solo tracce) e dal cambiamento di colore, che dal verde passa al giallo nelle uve bianche e al rosso, rosso violaceo nelle uve nere; nell’uno e nell’altro caso, l’acino perde di consistenza. In questa fase, inoltre, si verifica un progressivo aumento del contenuto di zuccheri mentre, contemporaneamente, diminuisce l’acidità libera, sia per parziale salificazione sia per distruzione degli acidi, consumati in parte per la respirazione cellulare. In un appezzamento di vigneto, questa fase può durare dagli 8 ai 15 giorni e più se la fioritura è stata molto lunga.
Figura 3: Fasi di sviluppo dell’uva (Ribereau – Gayon et al., 2006)
Nella fase di maturazione industriale che, a differenza della maturazione fisiologica, riveste maggior interesse per l’enologo, l’acino si arricchisce in zuccheri più o meno rapidamente a seconda delle condizioni pedo-climatiche; anche le sostanze azotate aumentano, unitamente ai minerali che vanno a salificare gli acidi organici. Questo periodo dura da 35 a 55 giorni.
Dopo la fase di maturazione industriale, l’uva va incontro a numerose trasformazioni e modifiche chimico-fisiche che determinano la fase della sovramaturazione. In questa fase il raspo lignifica, riducendo sensibilmente l’apporto di sostanze nutritive al frutto, gli acini perdono acqua per
10
evaporazione, gli zuccheri e gli acidi organici diminuiscono a causa di fenomeni respiratori. Il tutto determina una diminuzione della resa in mosto e una diminuzione del contenuto in zuccheri. Da qui la necessità per il vinificatore del controllo della maturazione dell’uva.
Gli aspetti più importanti della maturazione dell’uva, che interessano l’enologo sono:
a) crescita e sviluppo dell’acino; b) aumento degli zuccheri; c) diminuzione degli acidi;
d) evoluzione delle sostanze azotate; e) evoluzione delle sostanze minerali; f) sintesi dei composti fenolici;
g) evoluzione delle sostanze aromatiche.
a) Crescita e sviluppo dell’acino
Come già ricordato, l’acino aumenta continuamente di volume e di peso dall’allegagione alla maturazione. In questa fase l’acino assume la sua forma definitiva, mentre il massimo peso viene raggiunto alcuni giorni (da 5 a 10) prima della maturazione; in tale periodo, infatti, avviene una leggera perdita di peso dell’acino, dovuta a perdita d’acqua.
In generale la dimensione di un acino a maturazione dipende dalla piovosità che si verifica dopo l’allegagione; infatti l’acino ottenuto nelle annate piovose presenta dimensioni maggiori rispetto a quello prodotto in annate secche.
Anche una produzione scarsa del vitigno favorisce l’aumento di volume e di peso dell’acino, indipendentemente dalle caratteristiche varietali.
Un altro fattore che influenza il peso dell’acino è costituito dal numero di vinaccioli; l’acino, infatti, pesa di più se contiene vinaccioli; a un aumento del numero di vinaccioli diminuisce il tenore zuccherino e aumenta il grado di acidità.
11
b) Aumento degli zuccheri
Subito dopo l’invaiatura, il tenore zuccherino dell’acino varia bruscamente passando, in pochi giorni dall’ 1 – 2% nella fase dell’invaiatura al 18 – 20% (e oltre, a seconda della varietà) nella fase della maturazione.
Sin dall'inizio le infiorescenze, a causa del loro tenore in ormoni della crescita, costituiscono un potente centro di richiamo per i prodotti della fotosintesi. Tuttavia, per tutta la fase di crescita erbacea, il tenore in zuccheri dell'uva acerba non supera i 10-20 g/kg di peso fresco (dell'ordine di quello delle foglie). Gli zuccheri importati giornalmente sono metabolizzati con forte intensità per lo sviluppo del frutto, ma soprattutto per la crescita e la maturazione dei vinaccioli. I1 richiamo di sostanze nutritive verso il frutto è ancora più rilevante nei giorni che precedono l'invaiatura.
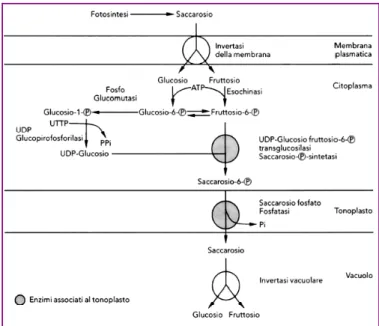
La scomparsa degli ormoni della crescita, in particolare delle auxine, e l'aumento del tenore in acido abscissico, vanno a corrispondere all'attivazione delle principali attività enzimatiche coinvolte nell'accumulo degli zuccheri nei vacuoli delle cellule della polpa. È il caso della saccarosio-fosfatosintetasi, della saccarosiosintetasi e dell'esochinasi (Figura 4).
Questo accumulo si verifica contro il gradiente di diffusione e questo trasporto necessita di energia per contrastare la pressione osmotica che cresce con l'aumentare del tenore in zuccheri; questa può raggiungere i 30 bar alla fine della maturazione. Un complesso enzimatico associato al tonoplasto delle cellule del pericarpo assicura questo trasporto.
Durante l’invaiatura, gli zuccheri migrano nell’acino essenzialmente dalle riserve glucidiche delle radici, del tronco e dei tralci; durante il periodo della maturazione, gli zuccheri presenti nell’acino provengono quasi esclusivamente dalle foglie. La foglia della vite, infatti, contiene sempre glucosio, fruttosio, saccarosio e amido, che si formano per fotosintesi clorofilliana.
Gli zuccheri, sintetizzati nelle foglie, migrano verso il grappolo attraverso il floema, esclusivamente sotto forma di saccarosio.
12
Figura 4: Meccanismo biochimico della penetrazione e dell'accumulo degli zuccheri nei vacuoli delle cellule della polpa dell'uva (Ribereau – Gayon et al., 2006)
La quantità di zuccheri che si accumula negli acini è direttamente proporzionale alla durata dell’insolazione, come è dimostrato dall’alto contenuto zuccherino delle uve prodotte dalle zone a clima più caldo e a maggior insolazione. Oltre alle condizioni climatiche, l’accumulo di zuccheri nell’acino durante la maturazione è influenzato dalla varietà e dal sistema di allevamento della vite.
Profonde modificazioni delle vie metaboliche si verificano già all'invaiatura, facilitando così il non utilizzo degli zuccheri traslocati. Lo studio dell'evoluzione della respirazione nel corso dello sviluppo dell'uva fornisce informazioni su questi cambiamenti.
L’intensità respiratoria aumenta proporzionalmente alla moltiplicazione cellulare nel corso della prima fase di crescita, poi resta relativamente stabile sino a maturità .
Prima dell'invaiatura, la polpa e soprattutto i vinaccioli, sono responsabili della maggior parte della respirazione mentre nel corso della maturazione, è soprattutto a livello della buccia che l’attività respiratoria è rilevante.
13
All'invaiatura, il quoziente respiratorio (rapporto tra anidride carbonica liberata e ossigeno consumato) si modifica, indicando un cambiamento del substrato respiratorio.
Durante tutta la fase di crescita erbacea, il quoziente respiratorio resta vicino ad 1. In realtà, il quoziente respiratorio del pericarpo dell'uva acerba è leggermente superiore ad 1, mentre quello dei vinaccioli è vicino a 0,7.
È probabile che la respirazione dei vinaccioli si compia a spese degli acidi grassi di cui sono ricchi, visto che nel pericarpo questo quoziente è il risultato in primo luogo della combustione degli zuccheri e secondariamente degli acidi organici.
Dopo l'invaiatura, il valore del quoziente respiratorio aumenta per arrivare a 1,5 alla fine della maturazione. Si può logicamente pensare che l'acino d'uva, nella sua globalità, utilizzi essenzialmente acidi organici come substrato respiratorio durante la maturazione.
Un'ulteriore informazione sulle modifiche delle vie metaboliche è fornita dall'evoluzione del rapporto glucosio/fruttosio nel corso dello sviluppo dell'uva. Siccome il saccarosio è la forma principale di trasporto dei prodotti della fotosintesi, questo rapporto dovrebbe essere vicino ad 1 nell'uva in cui avviene l'accumulo di questi prodotti.
Nell'uva acerba, all'inizio dello sviluppo, il glucosio predomina e rappresenta circa 1'85% degli zuccheri riduttori dell'acino. Questo rapporto, vicino a 5, diminuisce per arrivare a 2 in prossimità dell'invaiatura, e poi ad 1 all'inizio della maturazione; esso resta poi relativamente costante sino a maturità (tra 1 e 0,9).
Se il glucosio è più sensibile alla respirazione cellulare rispetto al fruttosio, quest'ultimo interviene preferenzialmente nelle reazioni di sintesi cellulare. È questo il fenomeno che spiega l'elevato rapporto glucosio/fruttosio nel corso dello sviluppo erbaceo dell'uva e la sua diminuzione dopo l'invaiatura, in relazione con un rallentamento dell'attività biosintetica.
Oltre al glucosio e al fruttosio, nell’uva è presente il saccarosio (0,5 – 2%), che subisce immediatamente il fenomeno dell’inversione nel mosto, formando parti uguali dei due zuccheri principali.
14
Nell’uva e nel mosto sono stati identificati altri zuccheri semplici (pentosi) e polisaccaridi complessi; tra i primi, i più rappresentati sono l’arabinosio e lo xilosio, tra i secondi, il più comune è il ramnosio.
c) Diminuzione degli acidi
L’acidità dell’uva è composta principalmente da tre acidi organici: tartarico, malico e citrico. Ciascuno di questi acidi ha un suo proprio comportamento nel corso della maturazione dell’uva; da questo diverso comportamento dipenderà la costituzione futura del vino.
Al momento dell’invaiatura dell’acino, il succo raggiunge la massima acidità titolabile che, espressa come acido tartarico, raggiunge e supera, in particolari uve e annate, i 30 g/l.
Nel corso della maturazione, questa acidità diminuisce fino all’epoca della vendemmia attestandosi intorno al valore di 10 g/l, anche se sono frequenti i casi in cui alla raccolta delle uve i valori di acidità titolabile siano inferiori (5 g/l).
Cause della diminuzione di questa acidità sono tre:
1. la diminuzione della concentrazione dei costituenti la polpa; ciò è dovuto all’accrescimento degli acini durante la fase di maturazione; 2. la migrazione delle basi che vanno a neutralizzare gli acidi;
3. la combustione degli acidi per attività respiratoria delle cellule vegetali.
La biosintesi di questi tre acidi avviene attraverso un meccanismo di formazione diverso per ogni singolo acido, partendo dagli zuccheri; inoltre, la sintesi di ciascun acido è localizzata di preferenza in particolari tessuti della pianta.
Dei tre acidi, l’acido tartarico, che costituisce l’acido caratteristico dell’uva, tanto che anticamente veniva designato col nome di acido uvico, è sintetizzato
15
esclusivamente negli organi verdi in via di accrescimento, in particolare nelle foglie, a partire dal glucosio.
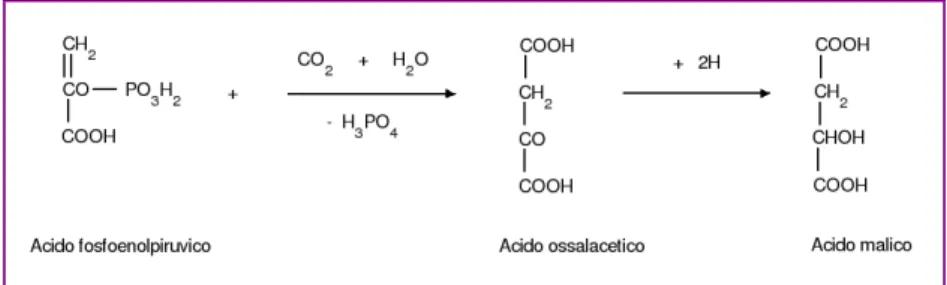
L’acido malico è sintetizzato nelle foglie giovani e adulte, attraverso il meccanismo della β-carbossilazione dell’acido fosfoenolpiruvico (Figura 5).
Figura 5: β-carbossilazione dell’acido fosfoenolpiruvico (Sciancalepore, 1998)
L’acido citrico è sintetizzato nelle radici, quasi esclusivamente a partire dal saccarosio; successivamente migra negli organi verdi della pianta.
Nel corso della maturazione, i tre acidi non presentano la medesima evoluzione; tutti e tre gli acidi diminuiscono dall’invaiatura, ma l’andamento di questa diminuzione si presenta diverso a seconda degli acidi.
L’acido citrico, il meno rappresentato dei tre, non subisce apprezzabili variazioni, dimostrandosi particolarmente resistente alla salificazione e in particolare all’ossidazione respiratoria.
La diminuzione dell’acido tartarico è in stretta relazione all’andamento stagionale; infatti, diminuisce rapidamente con la siccità e con temperature esterne alte, mentre aumenta in conseguenza delle piogge.
La diminuzione dell’acido tartarico è anche apparente perché in relazione all’aumento del volume dell’acino.
La diminuzione dell’acido malico dipende essenzialmente dall’attività respiratoria. Per questo motivo, in annate calde, con l’aumentare dell’attività respiratoria delle cellule vegetali dell’acino, il contenuto in acido malico subisce un rapido decremento. Inoltre, la sua diminuzione è dovuta all’utilizzo dell’acido malico nella sintesi glucidica, nella fase finale della maturazione dell’uva.
16
Pertanto, la diminuzione dell’acido malico è reale ed effettiva in quanto consumato dall’attività respiratoria e utilizzato anche per la sintesi dei glucidi.
Tali acidi sono presenti nell’uva in parte come acidi liberi e in parte salificati; le forme salificate sono rappresentate in particolare dal tartrato acido di potassio COOH – (CHOH)2 – COOH e dal malato acido di potassio
COOH – CH2 – CHOH – COOH.
L’acido tartarico all’inizio dell’invaiatura si trova essenzialmente allo stato libero e solo una modesta quantità (1% circa) è presenta sotto forma di sale; alla vendemmia la forma libera si riduce drasticamente e aumenta considerevolmente la quantità di acido tartarico totalmente salificato.
Anche il notevole contenuto di acido malico allo stato libero (70% circa) all’inizio dell’invaiatura si riduce enormemente alla vendemmia a favore della forma salificata (65% circa).
Le percentuali delle frazioni libere e salificate degli acidi determinano la concentrazione idrogenionica del mosto misurata con il valore di pH. Questo valore passa da 2,8 all’invaiatura a 3,5 all’epoca della vendemmia.
Le percentuali delle forme libere e parzialmente e/o totalmente salificate degli acidi tartarico, malico e citrico sono in relazione diretta col valore della costante di dissociazione di ciascuna funzione acida.
Oltre ai tre acidi citati, nell’uva sono presenti numerosi altri acidi in quantità decisamente modeste; alcuni provengono dal ciclo dell’acido citrico (piruvico, fumarico, cis-aconitico, α-chetoglutarico, succinico e ossalacetico), altri sono da mettere in relazione alla varietà dell’uva, all’andamento stagionale e allo stato di maturazione dell’uva.
d) Evoluzione delle sostanze azotate
Durante la maturazione dell’uva il contenuto dell’azoto aumenta considerevolmente. Secondo Peynaud, il tenore in azoto delle uve mature è 5 volte più alto di quello all’epoca dell’invaiatura. Alla maturazione, l’azoto è compreso tra 0,1 e 1,2 g/l di mosto.
17
Questo azoto è presente principalmente sotto forma di composti organici rappresentati da amminoacidi, polipeptidi e proteine; una parte modesta (10 – 15% circa) si trova sotto forma di ammoniaca, nitrati e nitriti.
Tra tutte le forme azotate, l’azoto ammoniacale e l’azoto amminico sono di particolare interesse per la vinificazione, in quanto costituiscono il principale alimento dei lieviti e dei batteri per il loro accrescimento. Infatti queste due forme azotate si riducono drasticamente, quasi a scomparire nei primi 2 – 3 giorni della fermentazione, contemporaneamente allo sviluppo dei lieviti.
L’azoto polipeptidico e quello proteico aumentano nel corso della maturazione per un processo di proteosintesi, che porta alla formazione di composti sempre più complessi.
Il contenuto di azoto totale (in media 300 mg/l) e le percentuali delle varie forme sono influenzati dalle condizione pedo-climatiche, in particolare dalla piovosità, dallo stato di maturazione e sanità delle uve e dal fattore varietà o cultivar.
Importante è anche la composizione aminoacidica del succo d’uva, non solo perché costituisce l’alimento principale dei lieviti della fermentazione, ma anche per l’alto valore biologico e nutritivo che riveste nell’alimentazione umana.
Nel succo d’uva sono stati dosati molti aminoacidi allo stato libero; di questi, risultano sempre presenti, in tutti gli stadi di maturazione, l’acido aspartico, l’arginina, la glutammina, la fenilalanina, la prolina e l’istidina; altri aminoacidi quali la tirosina e il triptofano pur presenti in quasi tutte le cultivar di uve mature, non sono stati trovati nei primi stadi della maturazione delle stesse uve. Tutti gli aminoacidi sono sintetizzati nelle foglie da dove migrano poi nell’acino.
La maggior parte dell’azoto proteico è rappresentato dagli enzimi; l’enzima più studiato e conosciuto è la polifenolossidasi che riveste un ruolo di particolare importanza non solo per la qualità di un vino, ma anche per la sua stabilità nel tempo.
18
Oltre alla polifenolossidasi, sono stati identificati altri enzimi del gruppo delle ossidoreduttasi, quali le perossidasi, la tirosinasi ecc., enzimi del gruppo delle idrolasi (saccarasi, proteasi, ecc.) ed enzimi pectolitici.
e) Evoluzione delle sostanze minerali
Nel corso della maturazione dell’uva, il contenuto in sostanze minerali del succo d’uva aumenta fino a raggiungere i 4 – 5 g/l. l’aumento più consistente avviene allo stadio iniziale della maturazione; l’aumento è tanto più intenso quanto più frequenti sono in questo periodo le precipitazioni oppure le irrigazioni; in tali condizioni, l’acino accumula grandi quantità di cationi e anioni assorbiti dal terreno attraverso le radici.
Fra i cationi viene prevalentemente assorbito il potassio che costituisce dal 40 al 60% dell’insieme degli ioni minerali del mosto.
In termini quantitativi, il contenuto di potassio varia da 1 a 2,5 g/l di mosto, seguono magnesio (0,1 – 0,3) calcio e sodio oltre allo ione ammonio, quest’ultimo in stretta relazione alla concimazione azotata del terreno.
Tra gli anioni vengono assorbiti lo ione fosforico, il più rappresentato con contenuto medio (espresso come PO43-) di 0,4 g/l di mosto, lo ione fosforico e
lo ione cloridrico.
L’aumento delle sostanze minerali è più evidente nelle parti solide dell’acino rispetto alla polpa; il contenuto in sostanze minerali si triplica nella buccia dall’inizio dell’invaiatura alla maturazione dell’acino.
La presenza dei minerali nella polpa dell’acino e quindi nel mosto riveste particolare importanza per la crescita dei lieviti, tanto che il mosto che ne è privo non fermenta.
19
f) Sintesi dei composti fenolici
Una della caratteristiche più importanti della maturazione è il rapido accumulo di composti fenolici che contribuiscono in maniera importante all’aroma e al colore delle uve e dei vini.
I composti fenolici delle uve includono acidi idrossicinnamici, acidi idrossibenzoici, flavoni, flavonoli, flavononi, flavan – 3 – oli, antocianidine e proantocianidine (tannini) e stilbeni. Si tratta di prodotti secondari del catabolismo degli zuccheri, di cui le vie di biosintesi sono presenti ed in parte attive dall'inizio dello sviluppo del frutto, la concentrazione di fenoli totali di conseguenza aumenta continuamente nel corso di questo periodo.
Per quanto riguarda i tannini, il loro brusco aumento all'inizio dello sviluppo è seguito da una fase di accumulo più lento nel corso della maturazione, ciò fa supporre che la biosintesi sia meno attiva dell'aumento di volume degli acini.
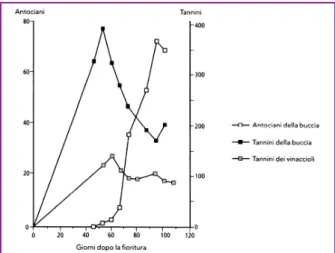
Il contenuto di tannini nei vinaccioli raggiunge il picco massimo prima dell'invaiatura, per poi diminuire fortemente sino ad un valore più basso e relativamente stabile quando i vinaccioli sono maturi. Il tenore in tannini della buccia, al momento dell’invaiatura è già elevato e corrisponde, a volte, a più della metà del tenore a maturità.
Figura 6: Evoluzione dei composti fenolici, espressi in mg/g di sostanza secca (Ribereau – Gayon et al., 2006)
20
Nelle uve bianche la quantità in acidi fenolici, esterificati dall'acido tartarico in flavan-3-oli e in proantocianidine oligomere, è elevata all'inizio dello sviluppo e diminuisce in seguito sino ad arrivare a concentrazioni minime a maturità.
Nelle uve a bacca colorata, gli antociani cominciano ad accumularsi nella buccia all'incirca due settimane prima che il colore diventi visibile.
Il loro tenore aumenta in seguito nel corso della maturazione ma, come per i tannini, passa da un massimo e poi diminuisce generalmente a maturità.
La comparsa degli antociani è legata all'accumulo degli zuccheri nell'uva, tuttavia non è stato possibile stabilire nessuna relazione diretta tra i due fenomeni; inoltre, diversi fattori, come la luce, permettono di aumentare la velocità di accumulo degli antociani, senza modificare il tenore in zuccheri della buccia.
g) Evoluzione sostanze aromatiche
Parecchie centinaia di sostanze chimiche diverse partecipano all'aroma varietale delle diverse uve. In questa miscela complessa si possono distinguere idrocarburi, alcoli, esteri, aldeidi e altri composti carbonilici.
Quasi tutti i composti sin qui identificati si ritrovano in numerose varietà che non possiedono un aroma varietale particolarmente tipico.
Tuttavia, per certe varietà è ormai accertato che l'aroma caratteristico è dovuto ad un numero limitato di composti specifici, presenti in debole quantità (da ng a µg/l).
Si deve tener presente che il potenziale aromatico dell'uva è costituito come segue:
- sostanze aromatiche, libere e volatili;
- precursori non volatili e non aromatici (glicosidi, derivati della cisteina, acidi fenolici, acidi grassi);
21
- composti volatili, aromatici o no, che per la loro instabilità si autotrasformano in altri composti aromatici (terpenoli, dioli terpenici, norisoprenoidi a C13...).
L'uva contiene numerosi composti di origine terpenica.
I monoterpeni si trovano sia allo stato libero che in forma legata, sotto forma di eterosidi; i più rappresentati in forma libera sono: linalolo, geraniolo, nerolo, citronellolo, α–terpineolo.
I1 contenuto in alcoli terpenici, sia liberi che legati, aumenta nel corso dello sviluppo dell'acino; gli eterosidi terpenici sono abbondanti già dall'inizio dello sviluppo dell'acino, quando è verde (da 250 a 500 µg/kg di peso fresco), mentre gli alcoli terpenici liberi sono in minima quantità (da 30 a 90 µg/kg di peso fresco).
La frazione legata rimane sempre più elevata di quella libera per tutta la durata della maturazione, ed aumenta anche dopo la maturazione, mentre l'incremento della frazione libera si attenua e la sua quantità può anche diminuire.
Certi alcoli terpenici liberi, come il linalolo e l'α-terpineolo diminuiscono durante la fase di sovramaturazione. Questa evoluzione sembra dimostrare che lo stoccaggio degli alcoli terpenici avviene per la maggior parte in forma legata.
Altri composti precursori dell’aroma, i carotenoidi, sono attualmente ben conosciuti: essi hanno la stessa origine degli alcoli terpenici, ma hanno un peso molecolare più elevato. Il tenore in carotenoidi dell'acino d'uva è compreso in un range da 15 a 2.500 µg/kg di peso fresco.
I più importanti, in ordine decrescente, sono: la luteina, il β-carotene, la neoxantina e la 5,6-epossi-luteina. Queste molecole, generalmente contenute nei plastidi cellulari, sono essenzialmente localizzate nelle parti solide dell'acino: la buccia è 2-3 volte più ricca in carotenoidi della polpa.
A seconda della loro struttura i carotenoidi sono presenti in percentuali
22
Durante la maturazione si osserva una diminuzione del tenore in carotenoidi ed un aumento di certe molecole da essi derivate, come i norisoprenoidi .
I norisoprenoidi a 13 atomi di carbonio sono frutto di una rottura ossidativa della molecola del carotenoide al livello del legame tra il C9 e il C10. Sebbene siano presenti in natura norisoprenoidi da 9 a 20 atomi di carbonio, per le uve ed i vini sono importanti solo quelli formati da 13C.
In maniera paragonabile ai monoterpeni, anche i norisoprenoidi sono presenti in forma glicosilata, soprattutto come monoglucosidi.
1.1.2 Indice di maturazione delle uve
Il termine “indice di maturazione” è riferito alla maturazione industriale, che corrisponde al momento in cui la polpa ha raggiunto il più alto contenuto zuccherino e il grappolo ha raggiunto il massimo del peso.
Dal punto di vista enotecnico, per poter stabilire l’epoca più conveniente per la raccolta delle uve da avviare alla vinificazione, sono state proposte diverse formule per i calcolo degli indici di maturazione.
Diversi autori si sono interessati negli anni alla individuazione di questa epoca, proponendo diverse formule, i cui termini sono rappresentati dal contenuto glucidico, dall’acidità titolabile, dal contenuto in acidi tartarico e malico, dall’alcalinità delle ceneri, dal pH.
Tutte queste formule si basavano sul principio che, durante la maturazione, mentre l’acidità diminuisce, gli zuccheri e le sostanze minerali aumentano.
Nessuno degli indici proposti da questi autori ha trovato pratica applicazione in quanto le variazioni quantitative cui sono soggetti i diversi costituenti riportati nelle formule sono in relazione a fenomeni tra loro indipendenti.
Infatti il contenuto zuccherino è in relazione con l’intensità e la densità delle radiazioni luminose, il tenore in acido malico con la temperatura, la quantità di acidi liberi e combinati con il regime delle piogge ecc.
Successivamente sono stati proposti due indici, uno basato sul rapporto glucosio/fruttosio, che nelle uve mature è pressoché uguale a 1, e un altro
23
basato sul rapporto fra la quantità di zucchero presente nel mosto d’uva e la misura della deviazione saccarimetrica dello stesso mosto. Quest’ ultimo indice viene utilizzato in Francia, come è noto, per differenziare i vini liquorosi dolci naturali da quelli ottenuti da vino addizionato di mosto concentrato.
Anche questi ultimi due indici non hanno trovato pratica applicazione per l’inconveniente di subire variazioni troppo esigue per gradi di maturazione sensibilmente diversi.
Tra tutti gli indici proposti per la determinazione dell’epoca più opportuna per la vendemmia, forse quello di Carino – Canina, che prende in esame il rapporto zuccheri/acidità totale, ha una certa applicabilità soprattutto per la semplicità di esecuzione non disgiunta da una certa attendibilità del metodo soprattutto se esteso per diversi anni, per un numero elevato di campioni e per uno stesso vitigno elevato in una determinata zona.
Per le nostre uve ad esempio, l’indice di maturazione calcolato dalla formula zuccheri per 100 ml / acidità totale per litro è compreso tra 3 e 5.
In pratica nelle ultime settimane della fase di maturazione dell’uva, ogni 3 – 4 giorni si dovrà prelevare un campione medio, costituito da 10 – 12 grappoli; questi saranno spremuti nel modo più completo possibile con un torchietto da laboratorio; nel risultante mosto, previa filtrazione su tela, verrà determinato sia il contenuto zuccherino con un mostimetro sia l’acidità titolabile; i valori ottenuti consentiranno di stabilire la data della raccolta o vendemmia, che sarà effettuata quando la concentrazione zuccherina del mosto tenderà a rimanere costante. Ovviamente questo modo di operare dovrà tener conto:
- delle condizioni climatiche, in particolare dell’umidità eccessiva e delle piogge, che specialmente negli ultimi giorni della maturazione delle uve insidiano la sanità del prodotto, e
- del programma di lavoro dello stabilimento enologico, in regime di sovra-carico durante la vendemmia.
24
1.1.3 Fattori determinanti la produzione quali-quantitativa
La qualità e la quantità dell’uva dipendono da diversi fattori permanenti, variabili, modificabili, accidentali.I principali fattori permanenti sono costituiti dal vitigno, dal portainnesto e dall’età del vigneto; l’azione di questi fattori è costante da un’annata all’altra.
I fattori variabili sono rappresentati essenzialmente dal clima, nel suo insieme, che durante il ciclo vegetativo e quello successivo della produzione e maturazione dell’uva può variare da un’annata all’altra a seconda delle variazioni di temperatura, della durata di insolazione e dell’intensità delle piogge.
I fattori modificabili riguardano le condizioni colturali a cominciare dalla potatura, per finire alle concimazioni invernali e primaverili; a modificare queste condizioni interviene l’opera del viticoltore.
I fattori accidentali sono costituiti da attacchi di parassiti vegetali e animali e da eventi metereologici eccezionali. Indubbiamente tra tutti i fattori che hanno una notevole influenza sulla produzione quali-quantitativa dell’uva è importante la varietà dei vitigni; questi si differenziano per il loro portamento, per la forma dei diversi organi (foglie, tralci, grappoli) e per le caratteristiche fisiologiche che si traducono in una produzione enologica diversa per quantità e qualità
Un fattore che influenza notevolmente la produzione quali-quantitativa dell’uva è il clima. La vite è coltivata tra il 35° e il 50° grado di latitudine; essa si adatta a climi caldi e freddi; nelle zone a clima freddo la pianta ha un portamento modesto e produce uve con scarso tenore in zuccheri e con elevata acidità, mentre in zone calde la vite ha un portamento vigoroso e la sua produzione di uva è caratterizzata da un alto contenuto zuccherino e un basso contenuto in acidi organici.
Oltre all’aspetto caldo – freddo del clima, un altro fattore climatico che interviene sulla qualità delle uve e dei futuri vini è rappresentato dall’umidità, o meglio dalla disponibilità di acqua; questo fattore in certe annate domina le caratteristiche del vitigno fino a vanificarle.
25
Altrettanto importante è il fattore costituito dalle caratteristiche chimico-fisiche-pedologiche del terreno, che dovrebbe permettere il drenaggio delle acque e nello stesso tempo immagazzinare acqua da fornire alla pianta soprattutto nel periodo di accrescimento.
Durante la fase di maturazione, le abbondanti precipitazioni sono sfavorevoli alla qualità dell’uva; in questi casi, infatti, la vite produce uva con basso contenuto glucidico e scarsa resistenza alle malattie crittogamiche. La peronospora, l’oidio e la muffa verde (Penicillium glaucum) sono le malattie più frequenti che interessano sia le foglie sia i grappoli. Oltre a queste malattie, nelle annate piovose è frequente la muffa grigia dovuta allo sviluppo della Botrytis cinerea.
Gli acini dell’uva colpita da questo ifomicete si presentano coperti da un feltro di ife color grigio, che distrugge la buccia e penetra nella polpa, determinando un’evaporazione dell’acqua e una composizione anomala dei costituenti la polpa in particolare decomponendo gli acidi, gli zuccheri, le sostanze polifenoliche e azotate.
I vini che si ottengono da queste uve, oltre ad avere una composizione anomala, sono soggetti ad alterazioni di colore, in quanto la muffa secerne un’ossidasi che attacca i polifenoli.
Una particolare attenzione merita l’attacco della Botrytis nella forma larvata, la cosiddetta muffa nobile, cioè senza che la muffa formi le fruttificazioni dalla caratteristica forma di cono. Questo tipo di muffa si sviluppa in zone a clima moderatamente caldo, dove l’umidità non troppo elevata, si alterna a periodi di insolazione con il risultato di una produzione di uve abbastanza zuccherine, di normale acidità e con un aroma molto delicato e gradevole, particolarmente adatte alla produzione di vini speciali.
Anche se la vite presenta un particolare adattamento a diversi tipi di terreno in virtù dei numerosi vitigni, in genere i terreni granitici danno vini molto profumati e ricchi di potassio; i terreni calcarei favoriscono l’accumulo di zucchero nella polpa, dando vini abbastanza alcolici; i terreni ben dotati di sostanza organica, consentendo una rigogliosa vegetazione e un’abbondante produzione di uve danno vini caratterizzati da un modesto grado alcolico e una
26
limitata serbevolezza per l’alto contenuto di sostanze azotate (Sciancalepore, 1998; Ribereau – Gayon et al., 2006).
1.1.4 Il ruolo dell’etilene nella maturazione dell’uva
L’uva è considerata ad oggi un frutto non-climaterico (Coombe e Hale, 1973); tuttavia, alcuni studi recenti hanno mostrato che l’etilene è capace di influire nei processi fisiologici della maturazione delle bacche d’uva (Chervin et al., 2004).
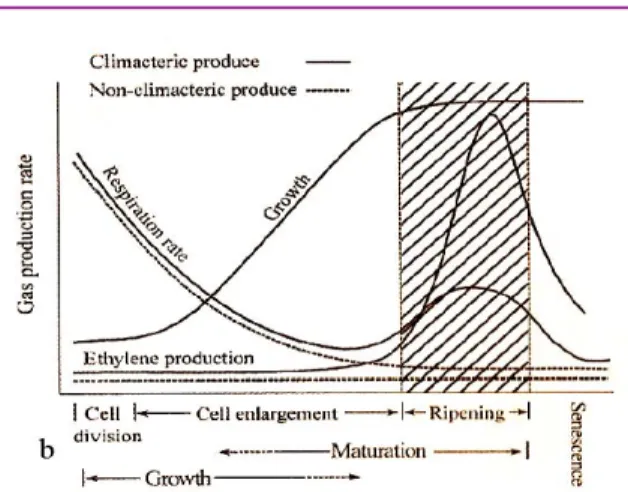
La differenza tra frutti climaterici e non climaterici dipende dalla presenza o meno di un picco nella respirazione e nella produzione di etilene durante la maturazione (Figura 7).
Figura 7: Andamento del tasso respiratorio in relazione alla produzione di etilene e alla crescita di frutti climaterici e non climaterici
Il momento corrispondente al picco della produzione dell’etilene nei frutti climaterici viene considerato come l’inizio dei cambiamenti che riguardano il colore, l’aroma, la consistenza ed altri attributi biochimici e fisiologici tipici della fase di ripening; al contrario, la maturazione dei frutti non-climaterici è considerata essere indipendente dall’etilene e l’intensità respiratoria si mantiene stabile durante tutto il periodo.
27
Tuttavia, Chervin et al. (2004), hanno mostrato che anche nell’uva si verifica un improvviso incremento della produzione di etilene endogeno all’inizio della fase di maturazione e che i tessuti delle bacche d’uva hanno vie metaboliche completamente funzionali per la sintesi dell’etilene che si attivano solo prima dell’invaiatura, quando le bacche iniziano ad accumulare zuccheri, e, nelle cultivar di uve rosse, ad accumulare anche antocianidine.
Tre fatti hanno indotto a considerare l'influenza dell'etilene endogeno e dei suoi recettori nello sviluppo e nella maturazione delle bacche d'uva:
1. osservazioni iniziali evidenziano che la maturazione delle uve può essere sia inibita che promossa da etilene esogeno, in funzione del tempo di applicazione sul periodo di sviluppo della bacca;
2. l'osservazione di un picco di produzione dell'etilene intorno all'invaiatura; 3. la disponibilità dell'1-metilciclopropene, uno specifico inibitore dei
recettori dell'etilene.
La classificazione dell'uva come frutto non climaterico avvenuta negli anni Settanta fu principalmente dovuta ad una serie di dati che mostravano solo leggeri cambiamenti nei livelli di etilene endogeno vicino all'invaiatura (Coombe e Hale, 1973).
Infatti, tali studi mostrarono che la quantità di etilene endogeno prodotto dall'uva era piuttosto bassa se espressa come una concentrazione rispetto al volume di gas interno (meno di 0,5 µl/l), ma se espressa come concentrazione per peso di tessuto, può essere chiaramente osservata un'esplosione di etilene attorno all'invaiatura (Alleweldt et al., 1977).
Recentemente è stato mostrato che la percezione dell’etilene è critica per alcuni cambiamenti della bacca associati alla maturazione; la percezione dell'etilene è richiesta per l'incremento del diametro della bacca, il decremento dell'acidità e l'accumulo delle antocianine nelle bacche in maturazione (Chervin et al., 2004).
Tesniere et al. (2004), inoltre, riportano che la segnalazione dell’etilene è implicata anche nella regolazione dell’espressione dell’enzima alcol
28
deidrogenasi nelle uve; e altri reports mostrano il ruolo dell’etilene anche in altri frutti non climaterici come fragole (Trainotti et al. 2005) e agrumi (Katz et al. 2004).
Questi risultati non implicano necessariamente che l'uva debba essere considerata facente parte dei frutti climaterici, ma l'impiego di nuove tecniche e nuovi strumenti induce cambiamenti nel modo di categorizzare la maturazione dei frutti.
1.1.5 Sostanze nutraceutiche presenti nelle uve
Nel loro naturale sviluppo, le piante devono contrastare gli effetti provocati da una serie di fattori di stress per mantenere il loro stato di salute. Per le piante, le condizioni di stress includono siccità, salinità, carenze nutrizionali, intensa insolazione, condizioni climatiche avverse, inquinanti, patogeni e insetti.
A causa del loro stato sessile, le piante devono la loro capacità di sopravvivere a condizioni sfavorevoli alla loro plasticità genomica e alla capacità di stimolare l’attivazione di sistemi di difesa fra i quali la sintesi di numerosi fitochimici.
La maggior parte delle sostanze bioattive delle piante sono metaboliti secondari, non direttamente implicati nello sviluppo, crescita e riproduzione, ma implicate nella difesa e nell’adattamento della pianta all’ambiente in cui si sviluppa.
I prodotti naturali della pianta possono essere sinteticamente ascritti a tre classi principali di composti: fenilpropanoidi, isoprenoidi e alcaloidi, ampiamente distribuiti nei prodotti di origine vegetale e nelle erbe medicinali.
Preziose fonti di fitochimici con funzioni nutraceutiche per l’uomo sono rappresentate dall’uva e dal vino.
Agli inizi degli anni Novanta fu data importanza al “paradosso Francese” che sottolineò i benefici alla salute apportati da un consumo regolare e moderato di vino. Studi mostravano una bassa incidenza nella popolazione francese di malattie cardiovascolari, malgrado una dieta ricca in grassi, soprattutto saturi, favorita da un consumo giornaliero di vino rosso (Renaud e de Longeril, 1992).
29
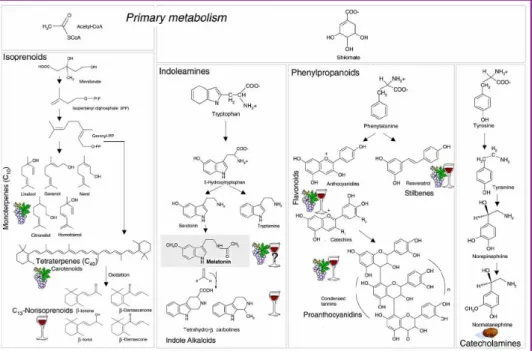
I farmaconutrienti dell’uva, presenti maggiormente nella buccia e nei semi, derivano da differenti vie metaboliche (Figura 8).
Figura 8: Fitochimici dell’uva (Irti e Faoro, 2006)
La via metabolica dei fenilpropanoidi, che prende il nome dal precursore acido scichimico, produce fenoli semplici o acidi fenolici, flavonoidi, stilbeni e proantocianidine.
I fenoli semplici che si trovano nell’uva includono gli acidi idrossibenzoici e idrossicinnamici.
I flavonoidi sono divisi in flavonoli, flavanoli e antocianine. Il gruppo dei flavanoli contiene le catechine e le epicatechine, le unità monomeriche delle proantociandine, mentre le antocianine sono responsabili del colore dei vini.
Il resveratrolo è il più importante degli stilbeni, a cui si aggiungono i non comuni piceidi, pterostilbeni e viniferine, che rispettivamente sono glucosidi del resveratrolo, derivati dimetilati del resveratrolo e suoi oligomeri.
Infine, le proantocianidine, anche conosciute come tannini condensati, sono caratterizzate da un grado di polimerizzazione che va principalmente da 3 a 11, fino a 17 e più.
Commento [CS1]: Controlla
30
Le proprietà biologiche degli alimenti e delle bevande funzionali ricche in fenilpropanoidi sono molteplici: antipertensive, cardioprotettive, antinfiammatorie e antimutagene.
Le tetraidro – β – carboline sono alcaloidi indolici, derivati dal triptofano, presenti in piccole quantità, che contribuiscono al potere antiossidante delle uve. Queste molecole hanno un ampio spettro di proprietà; ad esempio effetti psicofarmacologici, in quanto intervengono sul re-uptake della serotonina, e un’azione anticancerogena, per la loro capacità di indurre apoptosi cellulare.
Anche la melatonina (N – acetil – 5 – metossitriptamina) è stata recentemente trovata nell’uva; i suoi livelli circolanti nell’organismo sono implicati nel controllo del sonno, del tono vascolare, nell’omeostasi del calcio, nello sviluppo sessuale, del sistema immunitario e del cancro. Inoltre, la melatonina è in grado di ridurre le specie radicaliche e migliorare l’attività degli enzimi “detossificanti” come la superossido dismutasi, la glutatione perossidasi e la glutatione reduttasi.
Il contenuto di melatonina nell’uva varia a seconda della cultivar, risultando più alto nei vinaccioli, con la possibilità di essere aumentato dai trattamenti agrochimici.
In conclusione, le proprietà farmaconutrizionali dell’uva sono il risultato dell’attività sinergica di tutta una serie di fitochimici contenuti nei tessuti del frutto, che grazie ad un loro consumo regolare contribuiscono ad ottenere effetti benefici per la salute (Iriti e Faoro, 2006).
31
1.2 La produzione di metaboliti secondari nelle piante
Le piante sono organismi sessili ed in quanto tali non possono sfuggire ai loro predatori. Per questo motivo i vegetali, durante milioni di anni di evoluzione, hanno sviluppato sistemi metabolici che sintetizzano un’enorme quantità di sostanze chimiche che agiscono sia da deterrenti nei riguardi di erbivori e di patogeni, sia da difesa nei confronti di stress abiotici.
Il fatto stesso che le piante siano resistite ai continui attacchi dei fitofagi è una dimostrazione dell’efficienza del loro sistema chimico di difesa.
I metaboliti secondari agiscono in vario modo nei confronti dei fitofagi: essi sono in grado di fungere da deterrenti, ma anche da attrattanti, con lo scopo della perpetrazione della specie.
Molte volte la capacità di una molecola di svolgere l’uno o l’altro effetto sul fitofago è legata alla concentrazione con cui questa molecola viene sintetizzata.
Queste sostanze, normalmente denominate metaboliti secondari, sintetizzate dal metabolismo secondario delle piante, sono importanti per l’effetto che hanno su organismi benefici come gli impollinatori e i simbionti.
Ma l’importanza dei metaboliti secondari delle piante si estende anche all’uomo, sono infatti i principali responsabili del gusto, del colore e del profumo dei nostri cibi. Inoltre rappresentano una ricca fonte di materie prime per l’industria farmaceutica, in dipendenza delle loro funzioni antiossidanti e farmacologiche.
1.2.1 I composti fenolici
I composti fenolici sono la classe più studiata del metabolismo secondario. La variabilità molecolare e l’ampia distribuzione nel regno vegetale dei composti fenolici fa di queste molecole un argomento di studio estremamente interessante sia per quanto riguarda il loro ruolo nei processi fisiologici e biochimici, sia per la loro partecipazione ai meccanismi di difesa chimica dai predatori e dai fattori ambientali.
32
1.2.2 La via dell’acido scichimico e degli aminoacidi aromatici
La via dell’acido scichimico è comunemente denominata la via degli aminoacidi aromatici, anche se non tutti gli aminoacidi aromatici vengono sintetizzati tramite questo processo.La via dell’acido scichimico è presente nei batteri, nei funghi e nelle piante, ma è assente negli animali monogastrici per i quali è necessario introdurre tramite la dieta gli aminoacidi aromatici essenziali quali la fenilalanina e triptofano. La tirosina viene invece direttamente sintetizzata a partire dalla fenilalanina.
Nelle piante gli aminoacidi aromatici sintetizzati non sono utilizzati solo per la sintesi proteica ma anche come substrati per una grande quantità di metaboliti secondari.
La funzione dei derivati della via dell’acido scichimico è molteplice e va dalla protezione dagli agenti atmosferici, come le radiazioni UV, ai composti chimici di difesa contro erbivori e patogeni. Comunque il maggiore impiego riguarda la sintesi della lignina.
In generale la via prende il nome da un intermedio metabolico che si forma per unione del fosfoenolpiruvato (PEP) e dell’eritroso-4-fosfato (E4P).
Si può considerare la biosintesi degli aminoacidi aromatici suddividendola in due parti:
1. la via dell’acido scichimico, che partendo dall’E4P e dal PEP porta all’acido corismico;
2. la trasformazione dell’acido corismico nei tre aminoacidi aroamtici Phe, Tyr e Trp.
La figura 9 illustra i sette passaggi fondamentali di questa via. La prima reazione riguarda la condensazione di una molecola dell’intermedio della glicolisi PEP con un intermedio della via dei pentosi fosfati E4P per formare il composto eterociclico 3-idrossi-D-arabino-eptulosonico-7-fosfato (DAHP), che possiamo considerare derivato del 2-deossi-D-glucosio-6-fosfato. Questo primo passaggio è catalizzato dalla DAHP sintasi.
33
Il secondo passaggio consiste nella trasformazione dell’eterociclo contenente ossigeno del DAHP, nel cicloesano variamente sostituito rappresentato dall’acido 3-deidrochinico. Questa reazione è resa possibile dall’intervento della 3-deidrochinato sintasi, un enzima per la cui attività sono richiesti NAD+ e un catione divalente.
Figura 9: Via dell’acido scichimico (Maffei, 1998)
Nelle piante il terzo e il quarto passaggio della via dell’acido scichimico sono catalizzati da un enzima bifunzionale costituito da un singolo polipeptide in cui vengono svolte le attività sia della 3-deidrochinato deidratasi, che trasforma l’acido 3-deidrochinico in acido 3-deidroscichimico, che della scichimato deidrogenasi che converte l’acido 3- deidroscichimico in acido scichimico.
Il quinto enzima coinvolto nella via biosintetica è la 5-enolpiruvilscichimato 3-fosfato sintasi (EPSP sintasi) che causa la formazione reversibile del
34
composto da cui prende il nome e di fosfato inorganico, a partire dallo scichimato 3-fosfato e dal PEP.
L’ultimo passaggio nella via dell’acido scichimico riguarda la formazione dell’acido corismico tramite l’eliminazione del fosfato dall’EPSP operata dall’enzima corismato sintasi.
Il termine “corismico” deriva dal greco e significa “forca” o biforcazione. In effetti esiste un bivio metabolico che divide il pool di acido corismico in due vie: una verso la sintesi di Phe e tyr e l’altra verso quella del Trp.
Il primo enzima che agisce nella via di produzione della Phe e della Tyr è la corismato mutasi, che trasforma l’acido corismico in acido prefenico (Figura 10).
Figura 10: Via biosintetica dall’acido corismico agli aminoacidi aromatici fenilalanina e tirosina (Maffei, 1998)
L’acido prefenico viene quindi transaminato dalla prefenato amminotransferasi, per formare acido arogenico.
A questo punto non si è ancora formato l’anello aromatico e occorrono una decarbossilazione e la perdita di una molecola d’acqua, operata dalla arogenato deidratasi, per formare la Phe e una decarbossilazione ed una riduzione, operate dalla arogenato deidrogenasi, per formare la Tyr.
35
L’attività della arogenato deidratasi è competitivamente inibita dalla Phe ed è stimolata dalla Tyr, mentre l’arogenato deidrogenasi sembra essere inibita dalla Tyr.
La via di biosintesi del Trp è più complessa in quanto prevede la formazione dell’anello indolico (Figura 11).
Il primo enzima coinvolto è l’antranilato sintasi, che utilizza un donatore di amminogruppi (di solito glutammina) per trasformare l’acido corismico nell’acido aromatico acido antranilico.
Figura 11: Via biosintetica che dall’acido corismico porta al triptofano
(Maffei, 1998)
La antranilato fosforibosil transferasi catalizza il trasferimento di un frammento fosforibosilico del fosforibosilfosfato sull’antranilato.
36
Nel passaggio seguente, che è essenzialmente irreversibile, la fosforibosil antranilato isomerasi porta al riarrangiamento della struttura furanica del ribosio e trasforma il fosforibosil antranilato nel composto 1-(O-carbossifenilammino)-1-deossiribulosio-5-fosfato (CdRP).
Questa molecola è il substrato della reazione successsiva che, tramite l’azione della indol-3-glicerofosfato sintasi, porta alla formazione dell’anello indolico della molecola denominata indol-3-glicerofosfato.
Il complesso della triptofano sintasi catalizza gli ultimi due passaggi nella via che porta al Trp. La triptofano sintasi α catalizza la conversione dell’indol-3-glicerofosfato in indolo, mentre la subunità β porta alla definitiva formazione dell’aminoacido a partire dall’indolo e dalla serina.
1.2.3 La biosintesi dei fenoli semplici
Il termine fenolico viene comunemente utilizzato per descrivere tutti quei composti organici che possiedono uno o più gruppi sostituenti ossidrilici (OH) legati ad un anello aromatico.
Una caratteristica importante di questi composti è la loro acidità, dovuta alla facilità di rottura del legame tra l’ossigeno e l’idrogeno che forma il corrispondente ione negativo detto fenossido.
Le proprietà più importanti dei fenoli comprendono:
- la capacità dello ione fenossido di delocalizzare la carica negativa e di formare anioni emichinonici in cui la carica risulta sul carbonio anziché sull’ossigeno;
- la possibilità dello ione di perdere un altro elettrone e di formare il radicale corrispondente;
- l’abilità dei fenoli di formare ponti idrogeno con altre molecole.
La Phe prodotta durante le reazioni appena descritte viene utilizzata, oltre che per la sintesi di proteine, anche attraverso la sua deaminazione, per la
37
produzione di acido trans-cinnammico. Tale reazione è catalizzata dall’enzima fenilalanina ammonio liasi (PAL).
In alcuni casi, soprattutto in alcune graminacee, l’enzima può agire anche utilizzando la Tyr come substrato, in questo caso si forma acido trans-p-cumarico e l’enzima viene definito tirosina ammonio liasi (TAL) (Figura 12).
L’acido cinnammico va incontro a diverse sostituzioni dell’anello aromatico, che tramite idrossilazioni e metilazioni portano alla sintesi dei cosiddetti acidi cinnammici p-idrossilati.
Numerosi composti derivano dall’acido cinnammico: alcoli, esteri e ammidi cinnamiliche, cumarine, ma anche molecole più complesse come flavonoidi e xantoni, come anche molecole molto più semplici come acidi benzoici e fenoli semplici.
Figura 12: Formazione degli acidi traans-p-cumarico e trans-cinnammico a partire rispettivamente dalla Tirosina e dalla Fenilalanina (Maffei, 1998)
1.2.4 La biosintesi dei fenoli complessi: i flavonoidi
I flavonoidi, prodotti naturali ampiamente distribuiti nelle piante, sono formati da due anelli aromatici tenuti insieme da un ponte a tre atomi di carbonio. Sono composti polifenolici, principalmente idrosolubili, di solito presenti nella pianta come glucosidi, che hanno come precursori per la sintesi il malonil-CoA ed il p-cumaril-CoA.
38
Il loro nome deriva da flavus (= giallo) riferendosi al ruolo che giocano come pigmenti vegetali. I flavonoidi infatti, sono essenziali per la riproduzione delle piante in quanto sono in grado di attrarre gli insetti impollinatori e propagatori di semi. Tuttavia la colorazione che donano ai tessuti vegetali varia in funzione del pH. I pigmenti blu si formano per chelazione con certi ioni metallici (ad esempio Fe(III) o Al(III) ) mentre un gruppo specifico di flavonoidi, le antocianine, è responsabile per i colori rosso, blu e violetto.
Oltre alle loro importanti funzioni legate alle strategie riproduttive, i flavonoidi sono particolarmente utili all’uomo sia per i loro impieghi in medicina sia per i loro effetti sull’ecosistema agricolo (esercitano un effetto sulle associazioni simbiontiche sia micorriziche che azoto-fissatrici che agiscono direttamente sulla nutrizione fosforica e azotata della pianta).
I flavonoidi assorbono fortemente la radiazione ultravioletta e il loro accumulo nell’epidermide delle foglie ne suggerisce una funzione specifica di protezione del danno che questo tipo di radiazioni causano al DNA delle cellule.
I flavonoidi giocano un ruolo essenziale anche nello sviluppo del polline, in quanto in grado di generare un gradiente di concentrazione nel pistillo capace di guidare il tubetto pollinico verso l’ovario.
Esistono sei classi principali di flavonoidi: i calconi, i flavanoni, i flavoni, i
flavonoli, le antocianidine e gli isoflavoni.
Il primo step della biosintesi dei flavonoidi consiste nella conversione dell’acetil-CoA in malonil-CoA, reazione catalizzata dall’enzima acetil-CoA carbossilasi. Tre molecole di malonil-CoA vengono condensate con una molecola di 4-cumaril-CoA tramite la calcone sintasi (CHS) (Figura 13).
Per quanto riguarda il meccanismo di ciclizzazione non si è ancora stabilito se si tratti di una reazione spontanea o se sia catalizzata da una ciclasi specifica; la reazione comunque prevede una serie di riduzioni dei gruppi chetonici ad alcoli secondari.
La chiusura dell’anello eterociclico centrale prevede una serie di reazioni tra cui la più conosciuta è catalizzata dall’ enzima calcone isomerasi (CHI), la quale
39
promuove in particolare l’isomerizzazione del composto colorato in giallo 4,2’,4’,6’-tetraidrossicalcone nel composto incolore naringenina (flavanone).
Figura 13: Via di biosintesi dei flavonoidi
La naringenina formatasi viene convertita in diidrossicanferolo (DHK) grazie alla flavanone 3-idrossilasi (F3H). Il DHK funge da substrato per la sintesi dei flavonoli e delle antocianidine.
40
La riduzione del DHK, operata dalla flavonol sintasi (FLS) porta alla sintesi del flavonolo canferolo, mentre le ossidrilazioni catalizzate dalla flavonoide 3’-idrossilasi (F3’H) e dalla flavonoide 3’-5’- 3’-idrossilasi (F3’5’H) portano rispettivamente alla diidroquercitina (che verrà trasformata dalla FLS nel flavonolo quercetina) e alla diidromiricetina, che tramite la catalisi della FLS porta ad un altro flavonolo, la miricetina.
Occorrono almeno tre altri enzimi per trasformare i diidroflavonoli incolori in antocianidine ed antocianine colorate.
Il primo enzima, la diidroflavonol 4-reduttasi (DFR), catalizza la riduzione dei diidroflavonoli in leucoantocianidine; ulteriori processi di ossidazione sono catalizzati dalla antocianidina sintasi.
Infine la glicosilazione delle leucoantocianidine, operata dall’enzima UDP glucosio: flavonoide 3-O-glucosiltrasferasi (3GT), produce le rispettive antocianine colorate.
L’esterificazione operata dalle flavonoide metiltrasferasi e le successive glucosilazioni e metilazioni delle strutture così formate, portano poi alla sintesi di innumerevoli composti per ogni classe di flavonoidi.
1.2.4.1 I tannini
I tannini, presenti nelle piante superiori, sono delle molecole fenoliche ad alto peso molecolare in grado di complessare sia con gli zuccheri che con le proteine.
Nelle piante superiori i tannini sono rappresentati da due gruppi di polimeri: i
tannini condensati ed i tannini idrolizzabili.
Come indica il termine i tannini idrolizzabili possono essere separati per azione di acidi, basi ed in alcuni casi da enzimi idrolitici (come la tannasi) in zuccheri (di solito glucosio) o polioli e un acido fenolico.
Quando l’acido fenolico è rappresentato dall’acido gallico si parla di
41
esaidrossidifenolo. Quando il gruppo esaidrossidifenolico viene staccato dalla molecola, lattonizza immediatamente a formare l’acido ellagico.
Sia i gallotannini che gli ellagitannini derivano dalla via dell’acido scichimico. In natura sono molto più frequenti gli ellagitannini dei gallotannini.
I tannini condensati, o proantocianidine, sono oligomeri e polimeri prodotti dalla via biosintetica dei flavonoidi. Essi si trovano nei frutti, nella corteccia, nelle foglie e nei semi di molte piante, dove svolgono una funzione di protezione da patogeni microbici, insetti ed erbivori.
Allo stesso tempo danno gusto e astringenza a molte bevande, tra cui vini, succhi di frutta e tè, dimostrando anche numerosi effetti benefici per la salute umana, quali attività antiossidante, antibiotica, anti-ipertensiva, anti-allergica e di inibizione di alcuni enzimi e recettori.
I tannini condensati sono costituiti da catene di due o più unità monomere di
flavan-3-oli (catechine) e/o di flavan-3,4-oli (leucoantocianidine), formando
polimeri di massa molecolare fino a 3500 Da. (Figura 15).
Figura 14: Strutture dei flavan-3-oli che costituiscono le proantocianidine
Figura 15: Struttura dei flavan-3,4-dioli
Le unità strutturali monomeriche non possono essere considerate come tannini in quanto la loro massa molecolare è troppo bassa e la loro reattività nei confronti delle proteine molto ridotta. Bisogna arrivare ai dimeri per avere una massa molecolare sufficiente per permettere la formazione di legami con le
42
proteine. Tuttavia quando i polimeri di tannini diventano troppo ingombranti rischiano di non potersi avvicinare ai siti attivi delle proteine impedendo alla reazione di avvenire.
Le catechine possiedono due cicli benzenici legati da un ciclo ossigenato saturo; questa struttura presenta due carboni asimmetrici (C2 e C3) che sono all’origine di quattro isomeri; la (+)-catechina e la (-)-epicatechina corrispondono alle forme più stabili.
Le proantocianidine oligomere possono essere divise in due gruppi principali: le procianidine, formate da catene di catechine e/o epicatechine, e le
prodelfinidine formate invece da catene di gallocatechine e/o epigallocatechine.
Le procianidine dimere a loro volta possono essere divise in due categorie principali:
• le procianidine B, che risultano dalla condensazione di due unità di flavan-3-oli legati tra loro per mezzo di un legame C4-C8 (da B1 a B4) o C4-C6 (da B5 a B8) (Figura 16);
• le procianidine A, che possiedono, oltre al legame interflavanico C4-C8 o C4-C6, un legame di tipo etereo tra i carboni C5 o C7 dell’unità inferiore e il carbonio C2 dell’unità superiore (Figura 17).
Similmente le procianidine trimere possono essere divise in:
• procianidine C, i cui legami interflavanici corrispondono al tipo B dei dimeri;
• le procianidine D, in cui un legame interflavanico è del tipo B e l’altro del tipo A.
43
Figura 17. Procianidine A (Dixon R. A. et al., 2005)
La via di biosintesi delle proantocianidine condivide alcuni passaggi con la via di biosintesi dei flavonoidi, portando alla produzione di flavan-3,4-dioli (leucocianidine); questi composti sono precursori della sintesi delle antocianine ma contribuiscono anche alla formazione delle unità monomeriche necessarie per l’estensione dei polimeri.
La sintesi dei polimeri di proantocianidine si ritiene sia il risultato dell’addizione di una serie di intermedi derivata da flavan-3,4-dioli ad un’unità terminale di flavan-3-olo (catechina o epicatechina) (Figura 18) (Bogs et al., 2005).
Figura 18: Schema della via biosintetica che conduce alla formazione di antocianine e proantocianidine (Bogs et al., 2005)
La biosintesi dei flavan-3-oli può essere considerata come il prodotto dell’attività enzimatica della leucoantocianidina riduttasi (LAR), la quale