Introduzione
alla
38
L’osteoartrite (OA) è la principale causa del dolore alle articolazioni in
pazienti anziani e di mezza età. Essa è caratterizzata dalla perdita progressiva
della cartilagine articolare che conduce alla denudazione della superficie
articolare. I fattori di rischio (età, lavoro, ecc.) sono strettamente collegati ad un
sovraccarico di tipo meccanico delle articolazioni e si presume che gran parte
delle osteoartiti siano indotte proprio da accumuli di stress meccanico.12
Inoltre, la perdita di cartilagine osservata nell’OA e nell’Artrite
Reumatoide è il risultato di un complesso processo che comporta il degrado di
vari componenti della matrice cartilaginea, in seguito all’aumentata attività delle
proteasi liberate eccessivamente dai condrociti articolari e dalle cellule sinoviali.
In particolare, la degradazione del collagene di tipo II della cartilagine è un processo chiave che porta alla perdita dell’integrità strutturale e funzionale
della cartilagine stessa. Il collagene di tipo II è una proteina con struttura a tripla
elica, resistente alla maggior parte delle proteasi; solo alcuni membri della
famiglia enzimatica delle MMPs (le collagenasi MMP-1, MMP-8 e MMP-13 e la
metalloproteasi di membrana MT1-MMP) sono in grado di idrolizzare questo
substrato. Una volta che le molecole di collagene sono sfaldate, la struttura ad
elica viene svolta a temperatura corporea e si denatura in gelatina, la quale viene
poi degradata in piccoli peptidi dalle gelatinasi (MMP-2 e MMP-9).12
Nella famiglia delle MMPs, la MMP-13, conosciuta come collagenasi-3, è
considerata il principale target nella OA, a causa della sua preferenza nella
degradazione del collagene di tipo II rispetto al tipo I e III.
La MMP-13 è particolarmente espressa nella cartilagine dei pazienti affetti
39
Sono stati messi a punto modelli sperimentali di topi osteoartritici ai quali
è stata indotta, mediante tecniche di microchirurgia, l’instabilità all’articolazione
del ginocchio; questi modelli sperimentali di OA hanno mostrato cambiamenti cellulari e molecolari simili a quelli visti nell’OA sull’uomo. In particolare, la via
di espressione della MMP-13 è stata correlata con la presenza di condrociti
patologici che subiscono una differenziazione ipertrofica nel primo stadio di
sviluppo di questa malattia. Inoltre, l’immunocolorazione della MMP-13 è
maggiormente evidente nei condrociti localizzati in zone mediali e superficiali
della cartilagine osteoartritica, i quali esprimono anche collagene di tipo X, un
marker dei condrociti ipertrofici.12
Ciò quindi suggerisce che la copresenza di MMP-13 e collagene di tipo X nell’area adiacente alla lesione conferma la stretta relazione tra la differenziazione
ipertrofica dei condrociti e la loro produzione di MMP-13.
Inoltre, questo legame è stato confermato da studi effettuati sull’attivatore
trascrizionale Runx2 responsabile della regolazione positiva sia della MMP-13 sia
dei condrociti ipertrofici. Un modello sperimentale di OA usando topi mancanti
del fattore Runx2 ha rivelato una riduzione della distruzione cartilaginea e della
formazione degli osteofiti, accompagnata da una ridotta espressione di collagene
di tipo X e di MMP-13, rispetto a topi wild-type in cui è stata indotta l’instabilità
al ginocchio.
Questi esperimenti quindi convalidano la teoria che la MMP-13 è un valido target per lo sviluppo di farmaci contro l’osteoartrite. Pertanto le attuali
strategie di sviluppo dei medicinali per il trattamento dell’osteoartrite sono
40
degli inibitori noti della MMP-13 è stato utilizzato con successo come agente
terapeutico a causa della mancanza di selettività per un isozima specifico, che
determina elevati dosaggi ed effetti collaterali muscolo scheletrici dipendenti dalla
durata del trattamento. Tuttavia il problema rimane nella ricerca della selettività,
poiché la maggior parte delle MMPs conservano caratteristiche comuni, come la
presenza di uno ione zinco e molte uguaglianze nelle sequenze amminoacidiche
del sito di legame. Nonostante questo, le principali differenze strutturali osservate tra le MMPs sono la dimensione e la forma del sito S1’ situato in prossimità del
catione catalitico.13
Questo lavoro di tesi si basa su uno studio di “virtual screening” svolto presso l’Università di Napoli alla ricerca di nuove strutture quali inibitori chelanti
lo zinco della MMP-13. Inizialmente è stato eseguito uno screening del database “Life Chemicals” mediante un docking computazionale effettuato con il
programma Autodock (AD4). In seguito è stata applicata una serie di filtri basati
su criteri razionali e chimico-fisici, al fine di ottenere solo composti dotati di una
potenza inibitoria e altamente selettivi verso MMP-13. Esempi di questi filtri sono
la scelta e applicazione di uno specifico valore di energia libera di legame (-10.5
kcal/mol), lo scarto di molecole per le quali non sono state predette coordinazioni con lo ione zinco catalitico, la valutazione dell’occupazione della tasca S1’ per
aumentare la selettività d’azione per MMP-13 e la valutazione della possibilità di
ottimizzare chimicamente le molecole.
Soltanto un totale di venti composti, ottenuto dalle precedenti selezioni, è
stato acquistato e saggiato per l’attività inibitoria su MMP-13 mediante tecniche
41
mostrato un’attività considerevole ad una concentrazione di 100 µM diventando,
così, cinque nuovi lead. I rimanenti composti non sono stati approfonditi.13
Dalla Tabella 6 possiamo osservare che i cinque inibitori sono
strutturalmente diversi gli uni dagli altri e che tutti i composti attivi, ad eccezione
di 25, possiedono una funzione carbossilica come gruppo chelante lo zinco
(ZBG).
Come già sottolineato nella parte introduttiva della tesi, tra i possibili
ZBGs, il gruppo idrossammico è sicuramente il più performante. Molecole
contenenti questo gruppo chelante si sono rivelate gli inibitori più potenti.
Tuttavia la presenza di questo gruppo determina generalmente una bassa stabilità del composto in vivo ed un’apprezzabile tossicità dovuta alla degradazione
metabolica a idrossilammina. Anche se meno potenti rispetto agli inibitori portanti
il gruppo idrossammico, i carbossilati rappresentano una valida alternativa, poiché
conservano una buona attività chelante, associata a riduzione dei numerosi effetti
collaterali legati al metabolismo. Infatti, recentemente i ricercatori di Novartis
hanno dimostrato che inibitori portanti un gruppo carbossilico, come il composto
26 (Figura 16), risultano equipotenti ai corrispondenti derivati idrossammici in
modelli in vivo. A causa di questa analogia strutturale, alcune proprietà chimico-
fisiche fondamentali, calcolate in silico, dei cinque lead sono state confrontate con
42
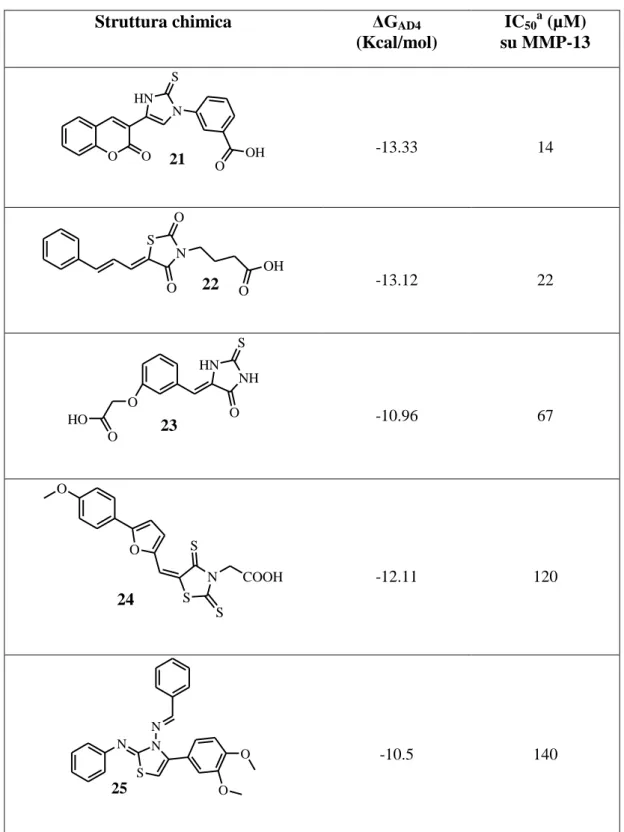
Tabella 6. Struttura chimica, energia di legame, IC50.13
Struttura chimica ΔGAD4 (Kcal/mol) IC50a (µM) su MMP-13 O O N HN OH O S 21 -13.33 14 N S OH O O O 22 -13.12 22 O HO NH HN O S O 23 -10.96 67 O S N COOH S S O 24 -12.11 120 N S N N O O 25 -10.5 140 a
Il valore di IC50 rappresenta la concentrazione richiesta per produrre il 50% dell’inibizione dell’enzima.
43 HO O H N S S OEt N O O O O
Figura 16. Struttura del composto 26.
Come mostrato nella Tabella 7, tutti gli inibitori, con l’eccezione di 25,
possiedono valori molto simili a quelli di 26. Per questo motivo tali composti
rappresentano dei lead ideali.
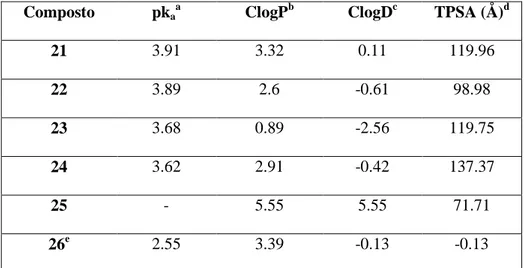
Tabella 7. Predizione delle proprietà chimico fisiche dei composti 21-25 e 26.13
Composto pka a
ClogPb ClogDc TPSA (Å)d
21 3.91 3.32 0.11 119.96 22 3.89 2.6 -0.61 98.98 23 3.68 0.89 -2.56 119.75 24 3.62 2.91 -0.42 137.37 25 - 5.55 5.55 71.71 26e 2.55 3.39 -0.13 -0.13 a pk
a predizioni riferite a ZBG. b Coefficiente di partizione calcolato n-ottanolo/acqua. c
Coefficiente di distribuzione calcolato a pH=7.4. dArea di superficie polare topologica. eAttività orale dei derivati acidi carbossilici inibitori della MMP-13 usati per confronto.13
44
L’attività inibitoria dei cinque lead è stata valutata sugli isoenzimi
MMP-1, MMP-2, MMP-3, MMP-13, MMP-14 (Tabella 8) dal gruppo di ricerca del
Prof. A. Rossello, mediante tecniche di spettroscopia in fluorescenza.
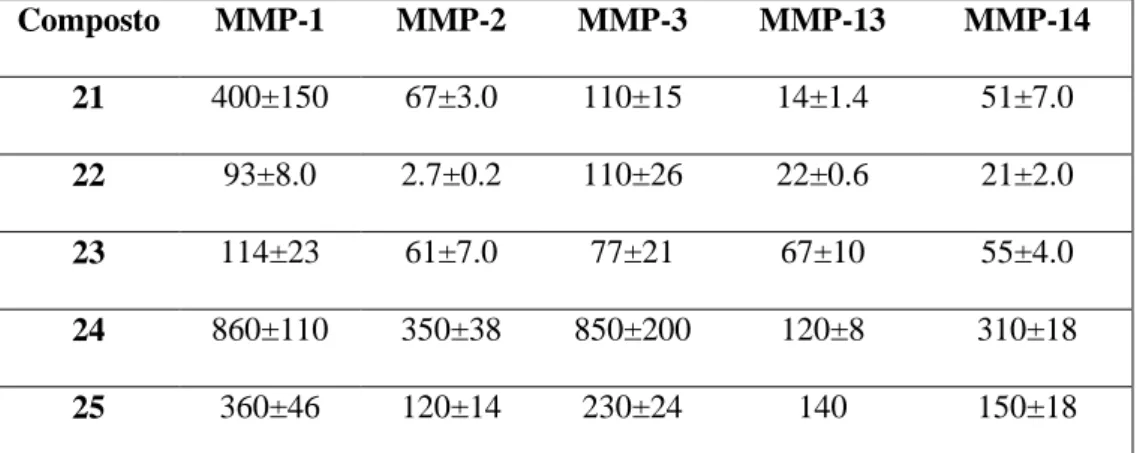
Tabella 8. Attività in Vitro a(valori di IC50µM) dei nuovi inibitori MMP-13 saggiati su alcune MMPs.13 Composto MMP-1 MMP-2 MMP-3 MMP-13 MMP-14 21 400±150 67±3.0 110±15 14±1.4 51±7.0 22 93±8.0 2.7±0.2 110±26 22±0.6 21±2.0 23 114±23 61±7.0 77±21 67±10 55±4.0 24 860±110 350±38 850±200 120±8 310±18 25 360±46 120±14 230±24 140 150±18 a
I saggi sono stati eseguiti tre volte. I valori finali mostrati sono il risultato medio dei tre esperimenti indipendenti (±SD).
I composti che presentano una funzione carbossilica come ZBG (21, 22, 23,
24) presentano anche delle profonde diversità nella loro struttura chimica: in 21 la porzione carbossilica è direttamente collegata all’anello benzenico; in 22 tale
porzione è collegata a un nucleo rodaninico mediante un link propilico; infine, 23 e
24 legano il gruppo carbossilico all’anello benzenico e tiossotiazolidindionico
mediante, rispettivamente, un ponte ossimetilenico e metilenico. Nonostante le
diversità strutturali tutti i composti presentano un piccolo numero di legami rotabili
(range da 0 a 4). La rigidità di 21 consente il corretto orientamento del ZBG per
chelare lo ione Zn++ catalitico e del gruppo P1’ nella tasca S1’, mentre l’anello imidazoltionico si trova in una posizione idonea per stabilire un’interazione π-π con
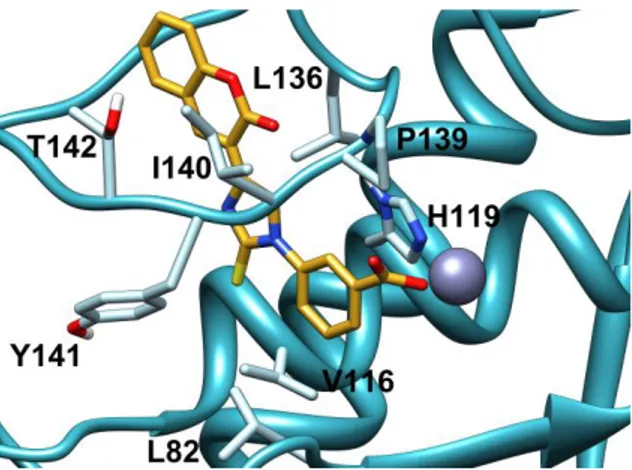
la catena laterale di His119. Infine il nucleo del cromenone si inserisce nella tasca S1’ conferendo alta selettività per MMP-13 (Figura 17).13
45
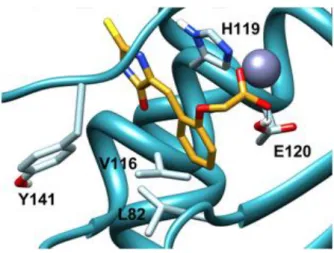
Figura 17. Docking di 21 (giallo) nel sito catalitico di MMP-13.13
Il composto 22 presenta una IC50 del tutto simile per le isoforme MMP-13
e MMP-14, ciò è dovuto alla presenza di una catena cinnamilidenica la quale non è in grado di occupare totalmente la tasca S1’ dell’enzima (Figura 18).13
Figura 18. Docking di 22 (giallo) nel sito catalitico di MMP-13.13
A differenza dell’inibitore 22, il composto 23 possiede un gruppo P1’
piccolo e polare, e questo comporta una minore attività e selettività rispetto a 21 e
22. Tuttavia, in 23 (Figura 19), l’anello tioidantoinico può essere sostituito con
46
l’interazione con il tunnel S1’ peculiare nella MMP-13. Per questo motivo,
l’estensione del gruppo P1’ in questo lead è prioritaria.13
Figura 19. Docking di 23 (giallo) nel sito catalitico di MMP-13.13
Anche per il composto 24 lo studio di docking ha confermato come ZBG il
gruppo carbossilico (Figura 20).13
Figura 20. Docking di 24 (giallo) nel sito catalitico di MMP-13.13
L’inibitore 25 è il più debole inibitore in tutte le MMPs su cui è stato
saggiato. Nonostante ciò, è l’unico il cui gruppo P1’ è in grado di stabilire alcuni
47
un’interazione di tipo π con His119. L’anello tiazolidinico crea dei contatti
lipofilici con i residui Leu81 e Leu82 del piano della tasca S1’, mentre il gruppo
N-benzilico si proietta verso i carboni β di Tyr141 e Ile140. La bassa attività che
presenta questo composto è attribuibile alla presenza di uno ZBG molto debole
(dimetossibenzene) (Figura 21).13
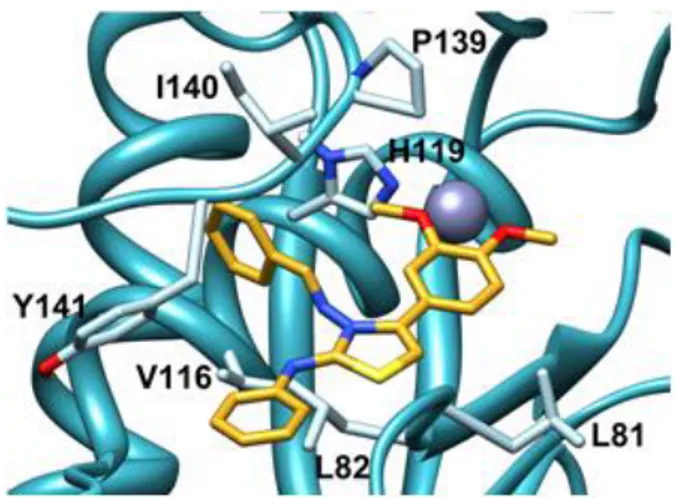
Figura 21. Docking di 25 (giallo) nel sito catalitico di MMP-13.13
In conclusione, nessuno di questi composti ha un gruppo P1’ grande
abbastanza per occupare tutto il tunnel S1’ della MMP-13, né sufficientemente
ottimizzato per interagire con la tasca stessa, per tale motivo l’IC50 di questi
48
Derivati Cumarinici
In questo lavoro di tesi, sulla base del derivato 21 sono state sintetizzate
due piccole librerie di composti (54-60 e 61-68) portanti sostituenti diversi nelle varie posizioni dell’anello benzo-fuso del nucleo cromenonico e/o dell’anello
fenilico pendente. I derivati 54-60 sono stati sintetizzati con lo scopo di validare il
modello di docking; i derivati 61-68 sono stati sviluppati con lo scopo di
migliorare la potenza e la selettività per la MMP-13, in un processo di
lead-optimization del composto 21.14
O O N HN OH O S 21 Derivati 54-60 Derivati 61-68 O O N N X R R1 O O N HN S COOH Y J Z W R= H, COOH, COOEt R1= H, CH3 X= O, S Y= H, Br W= H, OCH3, OH Z= H, OCH3, Cl, CH2=CHCH2 J= H, OCH3
Intermedi chiave per la sintesi dei composti 54-68 sono i derivati
49
La 3-acetilcumarina 27 è un prodotto commerciale.
O O CH3 O
27
La preparazione dei derivati cumarinici non commerciali (28-34) è stata
effettuata utilizzando una procedura riportata in letteratura per la sintesi di
analoghi derivati (Schema 1).15 L’opportuna salicilaldeide e l’etilacetoacetato
vengono fatti reagire in EtOH a 20°C per 5h, utilizzando piperidina come base.
Un campione analitico è stato cristallizzato da EtOH. La struttura di tutti i derivati
di nuova sintesi 28-34 è stata confermata da dati analitici e spettroscopici (Tabella
9). Schema 1 CHO OH W O O O O O O Piperidina EtOH t.a. Z Z W 28-34 J J W= H, OCH3, OH Z= H, OCH3, Cl, CH2=CHCH2 J= H, OCH3
I derivati 27-34 vengono poi trasformati nei corrispondenti α-bromo
50 Schema 2 O O O O O O Br Z Z CuBr2 CHCl3, AcOEt W W 35-42 27-34 J J W= H, OCH3, OH Z= H, OCH3, Cl, CH2=CHCH2 J= H, OCH3
La sintesi di questi derivati prevede di preparare inizialmente una
sospensione di bromuro di rame (II) in AcOEt. Alla miscela di reazione in agitazione a riflusso viene aggiunto l’appropriato derivato 27-34 sciolto in
cloroformio a caldo. In queste condizioni la reazione procede rapidamente con lo
sviluppo di HBr e la conversione del bromuro di rame (II) in bromuro di rame (I).
La reazione è terminata quando non si ha più sviluppo di HBr, il solido nero di
CuBr(II) scompare e la soluzione vira dal verde al giallo ambra. Un campione
analitico viene ottenuto per cristallizzazione da EtOH. La struttura dei composti di
nuova sintesi 35-42 viene confermata con dati analitici e spettroscopici (Tabella
10).
I derivati 43-53 sono ottenuti per reazione dell’opportuno α-bromo chetone
35-42 con l’opportuna arilammina in EtOH a riflusso per circa 2h (Schema 3).17
Al termine, il solido formatosi viene raccolto per filtrazione a p.r. I prodotti 43-53
così ottenuti sono sufficientemente puri da essere utilizzati come tali nelle reazioni
successive senza bisogno di ulteriore purificazione. Le costanti chimico-fisiche e
51 Schema 3 O O O Br W Y H2N NaHCO3 EtOH O H N O O W R R Y Z Z 43-53 35-42 J J R= H, COOH, COOEt Y= H, Br W= H, OCH3, OH Z= H, OCH3, Cl, CH2=CHCH2 J= H, OCH3
I derivati 43, 45-53 vengono poi fatti reagire con tiocianato d’ammonio in
acido acetico glaciale, a riflusso per 1.5 h (Schema 4).18 Al termine, il prodotto
insolubile viene raccolto per filtrazione a pressione ridotta, lavato con H2O e
successivamente con CH3CN a caldo per fornire i derivati 54, 57, 61-68 che
vengono purificati mediante lavaggio con Et2O. La struttura dei derivati 54, 57,
61-68 è stata confermata con dati analitici e spettroscopici (Tabella 12).
Schema 4 O O N HN S Z W Y R O O Z W O H N R NH4SCN 54, 57, 61-68 43, 45-53 Y CH3COOH J J R= H, COOH, COOEt Y= H, Br W= H, OCH3, OH Z= H, OCH3, Cl, CH2=CHCH2 J= H, OCH3
I derivati 54 e 57 vengono poi trasformati nei corrispondenti analoghi
N-metilati 55 e 58 (Schema 5). La sintesi prevede di preparare inizialmente una
52
porzioni idruro di sodio, in atmosfera di azoto, mantenendo la miscela di reazione
in agitazione a temperatura ambiente finché non è terminato lo sviluppo di H2. Si
aggiunge poi rapidamente a 0°C un eccesso di ioduro di metile e si lascia in
agitazione a temperatura ambiente per 12 h controllandone l’andamento mediante
TLC. Al termine, le acque madri vengono versate lentamente in ghiaccio:
precipita un solido costituito dai derivati 55 e 58, che viene filtrato a p.r. ed
essiccato su P2O5. La struttura dei composti 55 e 58 viene confermata con dati
analitici e spettroscopici (Tabella 12).
Schema 5 O O N N S H3C CH3I, NaH DMF anidra 54, 57 55, 58 0°C R O O N HN S R R= H, COOEt
Il derivato 58 viene sottoposto a idrolisi per fornire il composto 56. Una
soluzione del derivato 58 in una miscela MeOH/H2O viene raffreddata in un
bagno di ghiaccio, si aggiunge LiOH·H2O e si lascia in agitazione a 80°C per tutta
la notte. Al termine le acque madri vengono acidificate con HCl 10%. Si ottiene
un precipitato (56) che viene filtrato a p.r. La struttura del composto 56 viene
53 Schema 6 1) MeOH/H2O 0°C 2) LiOH . H 2O 80°C 3) HCl 10% O O N N S COOCH2CH3 H3C O O N N S COOH H3C 58 56
I derivati 59-60 vengono ottenuti per reazione dei derivati 43 e 44 con
cianato di potassio in acido acetico glaciale per circa 1h.18 Al termine della
reazione, vengono aggiunti 10 ml di H2O. Si ottiene un prodotto insolubile, che
viene filtrato a pressione ridotta e lavato con MeOH a caldo, costituito dai derivati
59-60 che vengono purificati mediante lavaggio con Et2O (Schema 7). La struttura
dei composti 59-60 viene confermata con dati analitici e spettroscopici (Tabella
13). Schema 7 KOCN CH3COOH 60-65°C O O N HN O O H N O O R 43-44 59-60 R R= H, COOH