PARTE SECONDA
TUMORE DEL TESTICOLO A
CELLULE DI LEYDIG E PRESENTE
STUDIO CLINICO
1. CELLULE DI LEYDIG
Un testicolo di un uomo di 20 anni contiene circa 700 milioni di cellule di Leydig, che da sole rappresentano il 5-12% del volume testicolare.
1.1 Differenziazione nella vita embrionale e adulta
Durante l’ottava settimana di vita intrauterina, le cellule di Leydig originano dal mesenchima della cresta urogenitale posteriore, localizzata tra le corde sessuali primitive delle gonadi maschili.
Tra la quattordicesima e la diciottesima settimana, metà del volume testicolare è rappresentato dalle cellule di Leydig. Rapidamente si produce un’involuzione progressiva di queste cellule fino a che, durante i primi anni di vita post-natale, esse spariscono, per poi generarsi nuovamente durante l’infanzia.[25,26]
Dopo la pubertà il numero di cellula di Leydig decresce progressivamente e nell’uomo adulto la loro divisione è un evento eccezionale.[26] Fino alla quinta decade di vita, la produzione di testosterone è mantenuta su parametri normali ed è dovuta al numero fisiologico di cellule di Leydig necessarie per la normale funzione testicolare; invece nell’uomo di età maggiore di 60 anni il numero di cellule di Leydig decresce, fino a dimezzarsi, rispetto ad un giovane. [27,28,29]
Il processo di differenziazione delle cellule di Leydig dai precursori cellulari è influenzato dai fattori paracrini del testicolo, dall’LH ipofisario e probabilmente dall’IGF-1 (fattore di crescita insulino-simile di tipo 1). [30] Le cellule di Leydig
sono elementi costituenti dello stroma del testicolo, di probabile origine mesenchimale, alle quali è stata riconosciuta attività endocrina: sono indicate con il nome di cellule interstiziali (di Leydig) e nel loro insieme costituiscono la ghiandola
interstiziale del testicolo.
Sono abbastanza voluminose (diametro fino a 20-25 µm) e possono trovarsi isolate o in piccoli gruppi; nel primo caso hanno forma sferoidale, mentre nel secondo assumono forma poliedrica per gli intimi rapporti che contraggono reciprocamente. Il nucleo, sovente eccentrico, è abbastanza grande e presenta la cromatina dispersa; contiene uno o più nucleoli.
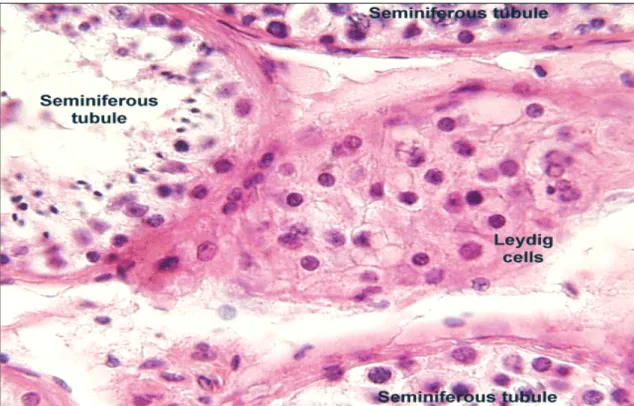
Il citoplasma, nei comuni preparati istologici, appare vacuolizzato, con metodiche idonee risulta ricco di goccioline lipidiche. Vengono inoltre rilevati visibili granuli di pigmento giallo-brunastro e formazioni cristalline (cristalli di Reinke) di dimensioni anche notevoli (Figura 5).
Figura 5. Aspetto istologico delle Cellule interstiziali di Leydig
(ematossilina-eosina, ingrandimento 20x).
1.2 Fisiologia
La cellula di Leydig è responsabile della quantità di steroidi circolanti prodotta. Il testosterone, sintetizzato a partire dal colesterolo, è il principale steroide prodotto dai testicoli. Non è chiaro se la quantità di colesterolo utilizzato per la biosintesi del testosterone derivi dal plasma sanguigno o da una biosintesi ex-novo. In entrambi i casi, il colesterolo deve essere trasportato dal gruppo di cellule metabolicamente attive nei mitocondri, dove l’enzima della scissione della catena laterale del colesterolo lo converte i pregnenolone e nel frammento isocaproaldeide C-6. Il pregnenolone viene poi trasportato fuori dalla membrana mitocondriale nel reticolo endoplasmatico liscio, dove è convertito in testosterone; in seguito il testosterone
diffonde attraverso la membrana cellulare e rimane intrappolato nel fluido extracellulare e nel plasma sanguigno per mezzo delle macromolecole che legano gli steroidi.
La regolazione della produzione di testosterone dipende dall’LH. Il trasporto dell’LH alle cellule di Leydig sembra essere mediato dalle cellule endoteliali con un meccanismo recettoriale. Una volta penetrato nelle cellule di Leydig, l’LH consente il trasporto del colesterolo nei mitocondri e il suo legame agli enzimi di clivaggio della catena laterale.
Oltre all’LH, altre molecole sono in grado di modificare la steroidogenesi delle cellule di Leydig: tra i peptidi ipofisari FSH e prolattina; tra i fattori non-ipofisari LH-RH, inibina e attivina, EGF, IGF-1, TGF-β e la stimolazione adrenergica; infine è possibile una inibizione diretta della steroidogenesi da parte di estrogeni e androgeni.
Le concentrazioni di testosterone nella circolazione periferica cambiano drasticamente durante il ciclo vitale:
- aumento nel feto tra dodicesima e diciottesima settimana di gestazione; - ulteriore rialzo a circa 2 mesi di vita;
- picco massimo durante la seconda o terza decade di vita; successivo plateau e poi diminuzione.
Questi aumenti corrispondono ai seguenti fenomeni:
- organizzazione neonatale o “imprinting” dei tessuti bersaglio androgeno-dipendenti, che garantisce l’adeguata risposta nella pubertà e nell’età adulta; - mascolinizzazione dell’uomo durante la pubertà;
- preservazione della crescita e della funzione degli organi riproduttivi negli adulti. [30]
1.3 Localizzazioni ectopiche
Normalmente le cellule di Leydig sono presenti nell’interstizio testicolare, formando gruppi di più di 10 cellule (Fig. 13A e 13B). Alcune di queste sono strettamente in rapporto con lo strato miofibroblastico della lamina propria dei tubuli seminiferi; tali cellule vengono denominate “cellule di Leydig peritubulari”: nel testicolo normale queste cellule peritubulari non sono osservabili.
Sono state descritte localizzazioni ectopiche delle cellule di Leydig, sia all’interno del parenchima testicolare che all’esterno.
Per quanto concerne il primo caso, sono state evidenziate cellule di Leydig nei tubuli seminiferi ialini dei testicoli di uomini con criptorchidismo o con ipogonadismo ipogonadotropo.
Le localizzazioni extraparenchimali possono creare equivoci per il patologo che non ricorda tale evenienza; secondo alcuni studi, le cellule di Leydig sono state ritrovate al di fuori del parenchima testicolare in 12 su 16 (75%) orchiectomie: [25]
nel 50% dei casi sono state ritrovate nella tonaca testicolare; - nel 14.4% dei casi sono state ritrovate nel cordone spermatico;
- nel 25% dei casi avevano sede intra o perineurale. [31]
Nistal e Paniagua hanno supposto che queste cellule si sviluppassero da precursori ritrovati accanto o all’interno dei piccoli nervi esterni al testicolo [32]. Mignon e collaboratori hanno dimostrato che le cellule di Leydig intraparenchiamli e quelle extraparenchimali hanno identico immunofenotipo, ad eccezione dell’immunocolorazione al testosterone. [33]
Il numero di cellule ectopiche è variabile tra 30 e 40, meno frequentemente più di 150. Quando queste sono molto numerose possono propagarsi lungo la corda sessuale testicolare, oppure possono essere confuse con una neoplasia metastatica, con il rischio di errata diagnosi; recentemente è stato descritto un caso di un uomo di 39 anni con tumore a cellule di Leydig extratesticolare nell’epididimo e nel cordone spermatico .[34] Le caratteristiche morfologiche di benignità, la scarsità di atipie e l’assenza di reazione stromale hanno stabilito la natura innocua di questi riscontri.
1.4 Anomalie morfologiche
Le cellule di Leydig nell’uomo adulto possono mostrare vacuoli intracitoplasmatici, pleomorfismo cellulare e multi-enucleazione.
I vacuoli sono il risultato dell’accumulo di colesterolo e trigliceridi, secondario ad una interruzione nella sintesi del testosterone. Inoltre è possibile che la degradazione di queste molecole, precursori del testosterone, non venga adeguatamente effettuata. Questo dato concorda con il calo delle cellule che reagiscono all’immunofluorescenza con testosterone, che si osserva negli uomini anziani.
Le cellule di Leydig pleomorfe sono caratterizzate da grossa dimensione cellulare, volume citoplasmatico esteso e nuclei ipercromici, che si associano ad una significativa diminuzione dell’immunocolorazione al testosterone.[35]
Le cellule di Leydig multi-nucleate possono essere normalmente riscontrate in pazienti criptorchidi [36,37] e nell’uomo molto anziano[38].