Classificazione:
Non aromatici
Aromatici
PENTATOMICI
ESATOMICI
BENZOCONDENSATI
POLICICLICI
N
H
O
S
ETEROCICLI AROMATICI
PENTATOMICI con 1 ETEROATOMO
N
H
O
N
H
FURANO- PIRROLO-TIOFENE
AROMATICITA’: viene rispettata la regola di
Huckel per n=1
n.b.: i MO sono 5 e non sono perfettamente degeneri (non
N
H
K
B
= 10
-14
Basicità del pirrolo e della pirrolodina
N
H
COMPOSTO
E di risonanza
(Kcal/mol)
Benzene
36
Piridina
28
Furano
16
Pirrolo
22
Tiofene
29
Ciclopentadiene
3
IL BENZENE ha ENERGIA di
RISONANZA SUPERIORE ad ALTRI
DERIVATI ETEROCICLI
FURANO- PIRROLO-TIOFENE
REATTIVITA’:
Danno reazioni si SelAr molto più velocemente delbenzene a causa della maggiore densità elettronica presente sull’anello benzenico.
Infatti, non solo abbiamo 6 elettroni p su 5 centri ma si possono scrivere strutture del tipo:
N H N H N H N H N H
Tali strutture rendono conto della esaltata reattività nucleofila di tali sistemi e della scala di reattività
pirrolo > furano > tiofene > benzene
FURANO- PIRROLO-TIOFENE
ORIENTAMENTO:
N H H NO 2 N H H NO 2 N H H NO2 + NO2 N H N H H NO 2 N H H NO2 + NO2 N H Attacco in 2: Attacco in 3:E’ preferita la sostituzione in 2 perché l’addotto s
corrispondente è stabilizzato da un maggior numero di strutture di risonanza
Reazioni di sostituzione elettrofila
aromatica
imidazolo
ossazolo
tiazolo
S
1 2 4 5H
N
1 2 4 5O
1 2 4 5N
3N
3N
31,3-diazolo
1,3-ossazolo
1,3-tiazolo
ETEROCICLICI 5 TERMINI con 2
ETEROATOMI: 1,3-
ETEROCICLI a 6 TERMINI
N N N N N AROMATICITA’N
REAZIONI ACIDO-BASE CATALISI NUCLEOFILA
REATTIVITA’ DELLA PIRIDINA
1) Reattività del doppietto elettronico solitario dell’azoto
2) Reattività dell’anello aromatico
K
b= 10
-9N
Sostituzione elettrofila aromatica
Sostituzione nucleofila aromatica
Basicità della Piridina
REATTIVITA’ DELLA PIRIDINA
SOSTITUZIONE ELETTROFILA AROMATICA
In considerazione delle strutture a separazione di
carica precedentemente viste, la piridina è molto meno
reattiva del benzene.
Ha una reattività simile a quella del nitrobenzene e
quindi non dà acilazione di Friedel-Kraft mentre le
rimanenti quattro reazioni richiedono condizioni
estremamente drastiche
Reazioni di sostituzione elettrofila
aromatica
+ + N + N N H H H NO 2 NO 2 NO 2 NO 2+ N
la carica positiva è sistemat a sull'azoto che possiede solt anto
un sestetto di elettroni + + + H N N N H H NO 2 NO 2 NO 2 NO 2 + N
quest a st rut t ura è simile a quella che deriva
dall' at t acco in 2 + + N + N N H H H NO 2 NO 2 NO 2 NO 2 + N SOSTITUZIONE in 2
ORIENTAMENTO
Le sostituzioni elettrofile avvengono alla posizione 3:
SOSTITUZIONE in 4
REATTIVITA’ DELLA PIRIDINA
SOSTITUZIONE NUCLEOFILA AROMATICA
Reazione di Chichibabin
N N
N
struttura particolarmente stabile.La carica negativa è sull'azoto che è più elettronegativo del carbonio
2 NH H 2 NH H 2 NH H I stadio: attacco nucleofilo dello ione ammiduro al C-2 della piridina
II Stadio: Stabilizzazione dell’intermedio anionico per allontanamento di uno ione idruro
N N NH2 + H 2 NH H C5H5N + NaNH2
III stadio: Stabilizzazione dello ione idruro per reazione acido-base + N NH H 2 H N N H H N NH
IV stadio: Riprotonazione dell’anione della 2-amminopiridina per azione dell’ acqua
N NH2
+ + H O2
N NH
ETEROCICLI PRESENTI negli
ACIDI NUCLEICI
Composizione chimica di un acido
nucleico
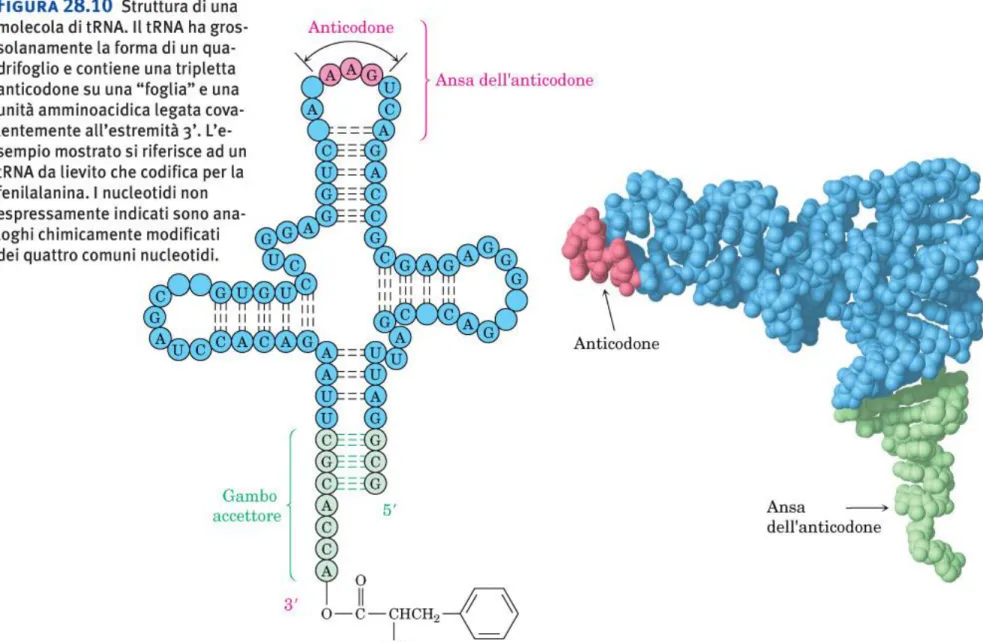
Figura 28.10 Struttura di una molecola di tRNA. Il tRNA ha grossolanamente la forma di un quadrifoglio e contiene una tripletta anticodone su una “foglia” e una unità amminoacidica legata covalentemente all’estremità 3’. L’esempio mostrato si riferisce ad un tRNA da lievito che codifica per la fenilalanina. I nucleotidi non espressamente indicati sono analoghi chimicamente modificati dei quattro comuni nucleotidi.
ETEROCICLI BENZOCONDENSATI
N
H
REATTIVITA’
L’indolo da con gli elettrofili reazioni di sostituzione che avvengono sull’anello pirrolico (più reattivo)
ORIENTAMENTO:
La reazione avviene preferenzialmente, nella posizione 3
1 N 3 2 5 4 6 7 8 N 1 3 2 5 4 6 7 8
ETEROCICLI BENZOCONDENSATI
REATTIVITA’Le chinoline e isochinoline danno con gli elettrofili reazioni di
sostituzione che avvengono sull’anello benzenico (non disattivato) ORIENTAMENTO:
La reazione avviene preferenzialmente, sia per la chinolina che per l’isochinolina alle posizioni 5 e 8
N NO 2 N 5-nitrochinolina + 0 °C , 3 HNO H 2 S O 4 N NO 2 8-nitrochinolina
La Morfina da Papaver somniferum
NH
DERIVATI SINTETICI della MORFINA
Alcaloidi contenenti Indolo o anelli indolici ridotti
N O O N H H H H H N CH2 N CH3 CH3 HGramina
Stricnina Strychnos nuxvomicaLa morte è provocata dalla paralisi dei muscoli respiratori
Piccolissime dosi stimolano i muscoli respiratori, dosi più alte li paralizzano.