UNIVERSITA’ DI PISA
Scuola di Specializzazione in Cardiologia
Dipartimento Cardio-Toracico e Vascolare
Tesi di Specializzazione
“RUOLO DELLO STRESS OSSIDATIVO E DELLA
DISFUNZIONE MITOCONDRIALE NELLA
REGOLAZIONE METABOLICA DEL FLUSSO
CORONARICO: NUOVO MECCANISMO DI ISCHEMIA
MIOCARDICA?”
Relatore: Candidato:
Chi.mo Prof. Alberto Balbarini Dott.ssa Giacinta Guarini
Le scoperte consistono nel vedere ciò che
tutti hanno visto e pensare ciò che nessuno ha
pensato.
Albert Szent-Gyorgyi
ABSTRACT
Recenti studi sperimentali ed osservazioni cliniche hanno evidenziato la concomitante
presenza di stress ossidativo e disfunzione mitocondriale in molte patologie cardiovascolari e in condizioni cliniche ad esse associate, tra le quali l’ipertensione arteriosa, la cardiomiopatia ischemica e diabetica, la sindrome metabolica e l'obesità’. Nessuno studio ha tuttavia definito se la disfunzione mitocondriale sia la causa o la conseguenza dell’ischemia miocardica. Poiché i mitocondri sono coinvolti in quasi tutti gli aspetti della vita cellulare sintetizzando ATP e altre sostanze vasoattive tra le quali le
specie reattive dell’ossigeno (ROS), ipotizziamo che l’incremento dello stress ossidativo
ed il danno mitocondriale siano la causa di una corrotta comunicazione tra cardiomiociti
e microcircolo coronarico, tale per cui la regolazione metabolica del flusso coronarico sia alterata con conseguente sviluppo di ischemia miocardica. Scopo del seguente studio e’ quello di dimostrare che l’alterazione della regolazione metabolica del flusso miocardico indotta dalla disfunzione mitocondriale, sia di per se’ in grado di generare insufficienza coronarica e conseguente danno ischemico tissutale. Nel presente studio verranno
discussi pertanto la regolazione metabolica del flusso coronarico in condizioni
fisiologiche e in modelli animali di sindrome metabolica e diabete mellito; mediante l’utilizzo di tali modelli animali, verrà inoltre dimostrata l’esistenza di un meccanismo aggiuntivo di ischemia miocardica, quella indotta dalla disfunzione mitocondriale.
Key Words
coronary microcirculation, mitochondrial dysfunction, oxidative stress, diabetic
INTRODUZIONE
Studi sperimentali su modelli animali ed osservazioni cliniche hanno evidenziato un
substrato fisiopatologico comune alle diverse patologie cardiovascolari: la presenza di
aumentato stress ossidativo e di disfunzione mitocondriale. Lo stress ossidativo sembra
infatti mediare molte delle condizioni e delle complicanze associate al diabete mellito, all’ipertensione arteriosa, alla dislipidemia, alla sindrome metabolica e all'obesità in particolare l’alterata/ridotta perfusione miocardica tipica di queste condizioni. 1-8
La maggior parte delle specie reattive dell’ossigeno (ROS) prodotte, tra le quali figurano l’anione superiossido (O2-), il perossido di idrogeno (H2O2) ed il radicale ossidrile (OH-),
sono di derivazione mitocondriale. In condizioni fisiologiche infatti, alcuni elettroni
vengono persi dai complessi I e III della catena di trasporto degli elettroni (ETC) durante
il processo di fosforilazione ossidativa (Figura 1). Gli elettroni spaiati e persi da tali
complessi mitocondriali interagiscono con le molecole di ossigeno presenti localmente
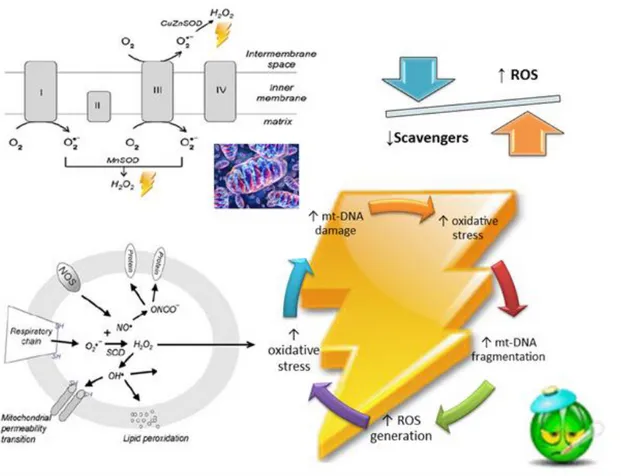
Figura : Rappresentazione schematica della catena fosforilativa mitocondriale. In condizioni fisiologiche,
durante il processo di ossidazione dei vari substrati, protoni vengono pompati dai complessi mitocondriali I, II, III e IV attraverso la membrana interna mitocondriale, generando un gradiente che verrà’ utilizzato per la sintesi di ATP ad opera dell’ ATPase synthase (complesso V) a partire dall’ADP. Tuttavia questo processo di trasferimento di elettroni non e’ un meccanismo perfetto poiché’ anche in condizioni fisiologiche alcuni elettroni vengono persi, in particolare a livello dei complessi I e III, generando una quantità’ minima di ROS.
In condizioni di pH fisiologico il O2- reagisce con i protoni presenti nell’ambiente
mitocondriale e viene efficientemente convertito in una molecola meno reattiva quale l’H2O2, o spontaneamente o mediante l’intervento di enzimi scavenger quali la
manganese superossido dismutase (MnSOD) (reazione 1). Sebbene l’H2O2 non sia
altamente reattivo di per se’, il potenziale distruttivo di questa molecola deriva dalla capacita’ di reagire con metalli riduttivi tra cui il ferro ed il rame, con successiva formazione di una più tossica specie reattiva dell’O2, il OH- in una serie di steps di
seguito riportati (reazioni 2 e 3):
1) 2 O2- + 2H+ → O2 +H2O2 oppure
2) O2- + Fe3+ → O2 + Fe2+O2- + H2O2 + H+ → O2 + H2O + •OH 3)
Fe2+ + H2O2 → Fe3+ + •OH + OH-
Per tale motivo le cellule ed in particolare i mitocondri sono dotati di enzimi scavenger
quali la Catalasi (CAT) ed la Glutatione Peroxidase (GPX), che metabolizzato e neutralizzano l’H2O2 in H2O e O2 .
In condizioni patologiche invece, la quantità di ROS generata supera le capacita’ difensive mitocondriali e cellulari; pertanto, tali specie reattive dell’O2 interagiscono con
proteine, lipidi e soprattutto il DNA mitocondriale (mtDNA) che viene a trovarsi a stretto
contatto con elevate concentrazioni di ROS, alterandone conseguentemente la funzione e l’espressione. Tutte queste evidenze di un ruolo critico dello stress ossidativo nello sviluppo della disfunzione mitocondriale e viceversa, sono confermate di fatto dal
frammentazione del mt-DNA, sia in pazienti con patologie quali diabete mellito tipo 2 ed
insulino resistenza che in modelli animali di obesità e sindrome metabolica.9-12
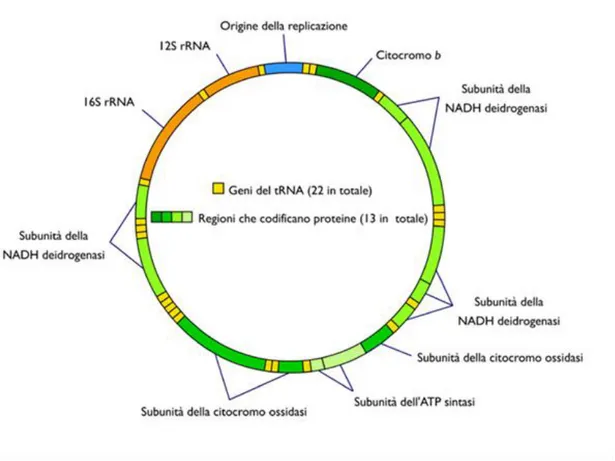
L’importanza di tali osservazioni risiede nel fatto che i mitocondri contengono numerose molecole di mt-DNA (Figura 2), dalle quali dipende la sintesi di molte delle proteine
coinvolte nel processo di respirazione cellulare (Complessi I, III, IV, V). Le molecole di
mt-DNA risultano da 6 a 7 volte più interessate da mutazioni perché maggiormente
affette dai danni dello stress ossidativo, in quanto tali molecole sono situate nei
mitocondri dove vengono generati in elevate quantità i ROS, e perché le molecole di
mt-DNA non sono protette da proteine istoniche a differenza di quelle del mt-DNA nucleare.
Mancano inoltre nei mitocondri gli enzimi di riparazione del mt-DNA. Si comprende
pertanto come qualsiasi situazione di danno al DNA mitocondriale, di fatto alteri l’intero funzionamento del processo di fosforilazione ossidativa cellulare. D’altra parte, se la catena di trasporto degli elettroni non funziona in maniera adeguata, e’ verosimile che il consumo di ossigeno si associ ad una maggiore produzione di ROS e ad una ridotta
sintesi di ATP e fosfati ad alto contenuto energetico, con successiva alterazione di tutti i
Figura 2: Rappresentazione schematica del DNA mitocondriale. L’importanza del mt-DNA risiede nel fatto
che in tali molecole di DNA sono codificati i geni responsabili per la sintesi delle proteine che costituiscono la catena di trasporto degli elettroni. Il DNA mitocondriale e’ infatti composto tra l’altro da 13 geni che codificano per i Complessi respiratori I,III, IV e per l’ATP sintasi. Lo stress ossidativo mediante danni al mt-DNA e’ in grado di interferire direttamente con la capacita’ della cellula di generare ATP.
L’aumentato stress ossidativo si associa quindi invariabilmente alla disfunzione mitocondriale, generando un circolo vizioso nel quale lo stress ossidativo sostiene ed
Figura 3: Rappresentazione schematica del danno cellulare da stress ossidativo. L’aumentata produzione di
ROS determina un circolo vizioso nel quale lo stress ossidativo sostiene e mantiene altro stress ossidativo mediante l’induzione di danno al DNA mitocondriale, preposto alla sintesi delle proteine che compongono la catena di trasporto degli elettroni mitocondriali. I ROS sono particolarmente importanti a livello mitocondriale e cellulare dove possono interagire con proteine, lipidi e DNA (mt-DNA) alterandone struttura e funzione. L’incremento dello stress ossidativo da un lato favorisce la produzione di altri ROS e dall’altro riduce l’efficacia dei sistemi di protezione cellulare.
L’importanza dei mitocondri non e’ da limitarsi al ruolo svolto nel metabolismo energetico cellulare e alla produzione di sostanze tossiche quali i ROS; infatti, e’ ormai dimostrato chiaramente che alcune delle specie reattive dell’ossigeno ed in particolare l’H2O2, fungono anche da molecole messaggeri intercellulari. E’ di rilievo notare che
proprio nell’ambito cardiovascolare, ed in particolare nella regolazione metabolica del flusso coronarico, che l’H2O2 perde i connotati di superflua e dannosa molecola
acquisendo importanti funzioni di signalling. In uno studio pubblicato nel 2006, Chilian e
altri investigatori hanno proposto un meccanismo alternativo di regolazione metabolica
del flusso coronarico. Tali ricercatori hanno dimostrato che il processo di regolazione del
flusso sanguigno miocardico durante incremento del lavoro cardiaco, dipende dalla
produzione di un metabolita attivo rilasciato dalle cellule miocardiche in maniera
direttamente proporzionale al lavoro compiuto e non come precedentemente proposto, da un meccanismo a feedback negativo nel quale l’adenosina o altri metaboliti attivi venivano prodotti in risposta ad un segnale/errore tra ossigeno apportato e consumato.13
Tale regolazione metabolica sarebbe quindi governata da sistemi di controllo a tipo
feed-forward, per cui ad un aumento del lavoro cardiaco corrisponderebbe un incremento
proporzionale del flusso miocardico, mediato dal rilascio in quantità crescenti di una
sostanza vasoattiva, coinvolta direttamente nella dilatazione coronarica, identificata nell’H2O2. Chilian ha infatti dimostrato mediante studi sia in vitro che in vivo che i
cardiomiociti metabolicamente attivi producono H2O2 in quantità direttamente
proporzionali al lavoro svolto, che la quantità di H2O2 prodotta correla in maniera lineare
e direttamente proporzionale con il flusso miocardico sanguigno, che l’H2O2 induce
in parte attraverso l’attivazione di canali del potassio voltaggio dipendenti, noti come Kv channels o canali sensori dell’O2, a livello delle cellule muscolari vascolari lisce
(SMVCs). 13-16
Sembra inoltre che lo stress ossidativo sia coinvolto in un altro importante meccanismo
quale la formazione di circoli collaterali nella circolazione coronarica. Rocic e altri
investigatori hanno infatti dimostrato che una “critica” quantità di ROS e’ necessaria ad
avviare tutti quei meccanismi di trasduzione del segnale che, in ultima analisi, conducono
alla formazione di nuovi vasi coronarici.17 Alcuni investigatori hanno infatti proposto “the redox hypothesis window”, dimostrando che un’elevata concentrazione di ROS o un eccessivo stato di riduzione cellulare impatta in maniera negativa sia la regolazione
metabolica del flusso coronarico che la formazione di circoli collaterali in corso di
ischemia miocardica.16, 18
Partendo quindi da queste osservazioni cliniche e da studi sperimentali che documentano l’estrema criticità dei mitocondri e dei metaboliti attivi da essi prodotti sia in condizioni fisiologiche che in stati patologici, che nasce il presente studio volto a chiarire il ruolo dei mitocondri nella regolazione metabolica del flusso coronarico e l’eventuale coinvolgimento degli stessi nello sviluppo di ischemia miocardica. Nel seguente studio,
utilizzando modelli animali di disfunzione mitocondriale, ipotizziamo e dimostriamo che la disfunzione mitocondriale e’ di per se’ un meccanismo sufficiente ad indurre ischemia miocardica, indipendentemente dalla presenza di altre comorbidita’.
PROTOCOLLO, MATERIALI & METODI
Il presente studio e’ suddiviso in due sezioni; la prima parte si svolge in vivo e prevede l’utilizzo di animali geneticamente modificati e trattamenti farmacologici volti specificamente o ad indurre disfunzione mitocondriale o ad attenuare lo stress ossidativo e l’aumentata produzione di radicali liberi. In questa sezione verranno valutate la funzione contrattile ventricolare sinistra sia a riposo che durante stress, che la
vasodilatazione coronarica in corso di aumentato lavoro cardiaco (nota come regolazione
metabolica del flusso coronarico). Verrà inoltre analizzata la funzione mitocondriale, sia
vascolare-aortica che miocardica-ventricolare sinistra, nei 4 gruppi di studio e l’impatto che tale disfunzione assume nell’indurre ischemia miocardica.
Nella seconda parte, sezione II, si procederà ad una successiva verifica in vitro dei dati
ottenuti in vivo, e ad ulteriori indagini volte a chiarire i meccanismi fisiopatologici
A. Studi in vivo
I. Induzione di disfunzione mitocondriale: frammentazione del mt-DNA
II. Riparazione dei danni da stress ossidativo al mt-DNA
III. Valutazione della funzione cardiaca a riposo e durante stress con Norepinefrina
IV. Quantificazione del flusso sanguigno miocardico (MBF, ml/min/g)
V. Emodinamica in vivo
VI. Isolamento di arteriole mesenteriche e valutazione della risposta dilatatoria
endotelio-dipendente ed -indipendente
VII. Valutazione dell’efficienza della catena di trasporto degli elettroni a livello vascolare aortico
VIII. Isolamento di mitocondri miocardici e valutazione dell’efficienza respiratoria IX. Staining tissutale di regioni ipossiche miocardiche
Tutti gli animali partecipanti nel presente studio, i ratti Zucker Lean (ZL) e i Zucker Fatty
Obese (ZOF), sono stati acquistati da i Laboratori Harlan (USA). I ratti sono stati ospitati
nella nostra Struttura per animali (Animal Facility, NEOUCOM) e mantenuti con un ciclo
luce-buio di 12 ore, aventi libero accesso ad acqua e cibo ad libitum. L’Istituto e la Commissione per l’utilizzo e la cura degli Animali dell’Northeastern Ohio Universities College of Medicine (NEOUCOM, Ohio-USA) ha approvato tutti i protocolli e le
procedure sperimentali, in conformità con le Linee Guida per la cura e l'uso di animali da Laboratorio dell’Istituto Nazionale per la Salute (NIH pubblicazione no. 85-23, riveduta nel 1996).
Quando necessario, i ratti sono stati anestetizzati con isoflurano al 4% tramite una
camera di induzione e il mantenimento è stato ottenuto mediante isoflurano al 2-3% e
INDUZIONE DI DISFUNZIONE MITOCONDRIALE: FRAMMENTAZIONE DEL mt-DNA
In breve, la disfunzione mitocondriale è stata indotta in ratti magri (ZL) altrimenti non
presentanti alcuna patologia cardiovascolare, mediante la somministrazione endovenosa
di una proteina ricombinante capace di penetrare nelle cellule, contenente l’enzima di taglio e riparazione del DNA, l’esonuclease III, e di agire selettivamente a livello del DNA mitocondriale (mt-DNA) grazie alla presenza di una sequenza di localizzazione
mitocondriale (mt-tat-ExoIII). Il trattamento con mt-tat-ExoIII frammenta il mt-DNA,
compromette la produzione di energia ed induce un aumento dei ROS di derivazione
mitocondriale. I ZL (n = 8 in ogni gruppo) sono stati sottoposti ad incannulamento
cronico della vena giugulare destra sotto anestesia con isoflurano e sono stati trattati nei 3
giorni successivi o con 80 µg/ die di mt-tat-ExoIII ( gruppo ZL + Exo III) o con soluzione
RIPARAZIONE DEI DANNI DA STRESS OSSIDATIVO AL mt-DNA
In questo gruppo sono stati utilizzati i ratti Zucker Fatty Obese (ZOF) che nel complesso
costituiscono un modello genetico animale di obesità e diabete mellito non insulino
dipendente. Questi ratti presentano una mutazione autosomica recessiva sul cromosoma 5
a carico del gene fa, che induce una disfunzione del recettore per la leptina, manifestando
leptino-resistenza e conseguente obesità, iperlipidemia, ipercolesterolemia, iperfagia, un
grado variabile di iperglicemia, insulino-resistenza, atrofia muscolare, elevati livelli di
stress ossidativo e frammentazione del mt-DNA. In questo modello di aumentato stress
ossidativo e frammentazione del mt-DNA, la riparazione del mt-DNA è stata indotta dalla
somministrazione endovenosa di una proteina ricombinante in grado di penetrare nelle cellule, composta dall’enzima di riparazione del DNA, l’endonucleasi III, e da una sequenza di localizzazione mitocondriale che ne indirizza specificatamente le sede di
azione (mt-tat-EndoIII). A seguito del trattamento con mt-tat-EndoIII si osserva un
miglioramento nella sintesi di energia (ATP) e diminuisce la produzione mitocondriale di
ROS. I ZOF (n = 8 in ogni gruppo) sono stati sottoposti a cateterizzazione cronica della
vena giugulare destra, sotto anestesia con isoflurano, seguita da 3 giorni di trattamento o
con 1 μg/g di peso corporeo al giorno di mt-tat-EndoIII (gruppo ZOF + Endo III), o con
VALUTAZIONE DELLA FUNZIONE CARDIACA A RIPOSO E DURANTE STRESS CON NOREPINEFRINA
Tutti gli animali nei 4 gruppi di studio (ZL, ZL + Exo III, ZOF, ZOF + Endo III) sono
stati sottoposti a ecocardiografia al termine dei 3 giorni di trattamento, in condizioni
basali/di riposo. I ratti sono stati anestetizzati con isoflurano come descritto sopra. A tale scopo e’ stato utilizzato un ecocardiografo progettato selettivamente per studi in animali di piccola taglia, (Vevo 770, Visual Sonic, Canada ed il trasduttore lineare da 12-38
MHz, RMV710B). La funzione sistolica e diastolica del ventricolo sinistro è stata
valutata secondo le linee guida della Società Americana di Ecocardiografia.19
Gli spessori sisto-diastolici delle pareti anteriore e posteriore del ventricolo sinistro sono
stati registrati con immagini M-mode, utilizzando la media di misurazioni effettuate in
circa 5-10 cicli cardiaci consecutivi nelle proiezioni parasternale asse corto, a livello dei
muscoli papillari. Per la valutazione della funzione sistolica ventricolare sinistra i
seguenti parametri sono stati calcolati: frazione di eiezione (EF%), frazione di
accorciamento (FS%), portata cardiaca indicizzata (CI ml/min/g). La funzione diastolica
ventricolare sinistra è stata valutata mediante analisi con il Doppler pulsato. Il picco
precoce (E-wave) e tardivo (A-wave), il tempo di decelerazione dell’onda E (E dec) ed il
tempo di rilassamento isovolumetrico (IVRT) ed il rapporto E/A sono stati ottenuti dalla proiezione apicale quattro camere. In aggiunta a questi parametri e’ stata calcolata la massa ventricolare sinistra utilizzando la formula Troy per cui la massa ventricolare
sinistra (LV mass) =1.055*[(AWd+EDD+PWd)3-EDD3], dove 1,055 è il peso specifico del miocardio, AWd e’ lo spessore della parete anteriore; PWd corrisponde allo spessore
della parete posteriore, e EDD e’ il diametro telediastolico ventricolare sinistro.20 E’ stato
inoltre ottenuto l’indice di massa ventricolare sinistra (LVMI) espresso in mg/g di peso corporeo, per correggere per le differenze biometriche tra animali obesi e non.
In un sottogruppo di animali (n=4) nei 4 bracci di trattamento, e’ stata inoltre calcolata la
portata cardiaca indicizzata (CI ml/min/g di peso corporeo) durante stress con
Norepinefrina (NE) a dosi crescenti (NE 2.5 - 5.0 - 7.5 - 10 ug/kg/min) per valutare la
QUANTIFICAZIONE DEL FLUSSO SANGUIGNO MIOCARDICO (MBF, ml/min/g)
Per la quantificazione assoluta del flusso miocardico (MBF, ml/min/g) e’ stata impiegata l'ecocardiografia di contrasto in tempo reale (RT-MCE). A questo scopo è stata utilizzata
una sonda lineare (7 MHz) ed il sistema ecografico Acuson Sequoia C512 (Siemens,
Mountain View, Calif) utilizzando un basso indice meccanico (MI < 0.20) e le sequenze
Contrast Pulse Sequences Myocardial Contrast Echocardiography (CPS MCE). I gains
sono stati adeguati per ottenere immagini senza segnale spontaneo dal miocardio, prima
che il contrasto fosse somministrato, e sono stati poi mantenuti costanti nel corso dell’esame. Microbolle lipidiche contenenti gas di perflutreno (Definity, Lantheus Medical Imaging) sono state diluite ad una concentrazione di 1/10 in soluzione salina sterile e il mezzo di contrasto cosi’ ottenuto è stato poi infuso per via endovenosa ad una velocità costante di circa 30 microlitri/min negli animali magri e doppia nei gruppi con
ZOF. Le immagini di perfusione sono state acquisite in tempo reale (frame rate utilizzato
30 Hz), dopo una sequenza distruttiva di 5 frames ad alta energia (MI di 1.9). Il tempo di acquisizione per la curva di riempimento utilizzato e’ stato di circa 7 secondi. Le immagini sono state ottenute nelle proiezioni parasternale asse lungo o corto a livello dei
muscoli papillari. Dopo aver ottenuto le immagini in condizioni basali/di riposo, è stata
infusa per via endovenosa continua Norepinefrina a dosi crescenti (NE
2.5-5.0-7.5-10μg/kg/min) in modo da incrementare il lavoro cardiaco. Durante ogni steps, solo dopo
che la risposta alla dose somministrata di NE ha indotto un plateau della pressione
sono state ottenute le curve di riempimento per il calcolo del MBF. Per ogni dosi di NE, da 5 a 7 curve di riempimento sono state registrate. L’analisi delle curve cosi’ ottenuta mediante MCE è stata effettuata utilizzando il programma iMCE (software iMCE, non
disponibile in commercio, gentile concessione di Jonathan R. Lindner e collaboratori,
University of Portland, Oregon-USA). Da 3 a 5 regioni di interesse (ROIs), a seconda
della qualità delle immagini ottenute, sono state posizionate all'interno delle pareti del
ventricolo sinistro nella proiezione parasternale asse lungo o asse corto. Una ulteriore ROI e’ stata posizionata all'interno della cavità ventricolare sinistra (LV) per ottenere l’intensità del segnale nella cavità. L’intensità media del segnale all'interno di ogni singola regione di interesse è stata misurata automaticamente in ogni fotogramma. La
curva di riempimento di intensità del segnale nel tempo (Figura 4), dopo la distruzione
delle microbolle, è stata ottenuta per ciascuna regione di interesse utilizzando una
funzione esponenziale: y = A (1-e-βt), dove y è l'intensità del segnale in un dato
momento, β è la pendenza iniziale della curva e A è l'intensità plateau. Il MBF è stato poi
stimato utilizzando il modello volumetrico proposto da Vogel et altri.21 Da tre a cinque
curve di riempimento miocardico sono state in media ottenute per ogni animale in ogni
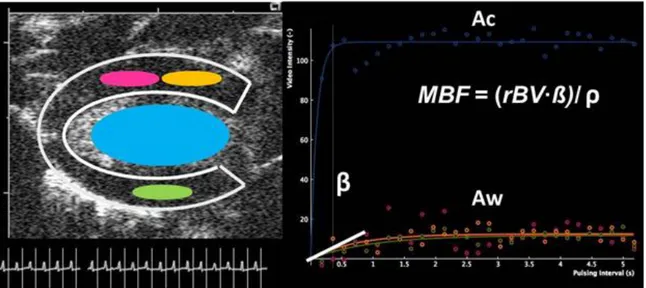
Figura 4: Esempio di analisi delle immagini di ecocontrasto per il calcolo del MBF (ml/min/g). Da 3 a 5
ROIs sono posizionate in diversi punti delle pareti ventricolari e una a livello della cavita’ventricolare sinistra per ottenere le curve esponenziali di riempimento miocardico con le microbolle. Dall’analisi delle curve i seguenti parametri W, C e β sono dedotti. A rappresenta il plateau dell'intensità’ acustica nota anche come l’area di sezione capillare nel distretto esplorato. β rappresenta la percentuale di aumento del segnale acustico, ed e’ interpretata come la velocità’ di scorrimento dei globuli rossi. Il MBF è stato stimato utilizzando il modello volumetrico proposto da Vogel dove MBF = (rBV · ß)/ρ, dove ρ è uguale alla densità del tessuto miocardico (1.05); rBV e’ il volume sanguigno miocardico relativo, pari a rBV = Aw/Ac.
EMODINAMICA in vivo
Dopo il trattamento di 3 giorni (sia con mt-tat-ExoIII per i ratti ZL o mt-tat-EndoIII nel
gruppo ZOF o la soluzione eparinata come controllo interno per ogni gruppo), tutti gli
animali (n=8 per ogni gruppo) sono stati sottoposti ad eco-cardio-contrastografia da
stress, con dosi crescenti di NE (NE 2.5-5.0-7.5-10μg/kg/min), durante anestesia con
isoflurano, e dopo l'iniezione del bloccante ganglionico esametonio (1g/kg di peso
corporeo) al fine di prevenire i riflessi neuro-cardiovascolari e di aumentare al massimo il
consumo miocardio di ossigeno. I ratti anestetizzati sono stati instrumentati con un
catetere da 0.8 Fr dotato di un microtrasduttore in punta ad alta fedeltà (SPR-1000),
collegato ad un sistema di acquisizione dati (PowerLab ML820, ADInstrument, Colorado Springs) attraverso un’unità di interfaccia (strumento Millar, bilanciamento del trasduttore, TCB 600) progettato per misurare invasivamente la pressione arteriosa
sistolica, diastolica e media (MAP) e la frequenza cardiaca (HR). Il catetere è stato fatto avanzare dall’arteria femorale sinistra in aorta addominale per le misurazioni emodinamiche. Da tali parametri e’ stato poi calcolato il doppio prodotto (DP), ossia il prodotto della MAP e della HR, utilizzato per stimare il lavoro cardiaco (CW) come
surrogato del consumo miocardico di ossigeno. Tutte le variabili sono state misurate in
continuo, registrate ed archiviate su un computer iMac collegato al sistema PowerLab
(ADInstruments, Castle Hill, Australia). I dati emodinamici sono stati raccolti e analizzati
ISOLAMENTO DI ARTERIOLE MESENTERICHE E VALUTAZIONE DELLA RISPOSTA DILATATORIA ENDOTELIODIPENDENTE ED -INDIPENDENTE
Una sezione di intestino è stata prelevata dall’animale al termine dell’eco-stress e posta in soluzione fisiologica salina tamponata (PSS) a 4°C contenente (in mM) 145 NaCl, 4.7
KCl, 2 CaCl2, 1.17 MgSO4, 1.2 NaH2PO4, 5 glucosio, 2 piruvato, 0.02 EDTA, e 3 acido
propanesulfonico 3-N-morpholino (MOPS), allo scopo di isolare arteriole mesenteriche. Questa soluzione e’ composta per l’1% da acidi grassi, non contiene albumina di siero bovino ed è stata tamponata a pH 7,4 a 36.5°C. I microvasi sono stati isolati in ambiente
a temperatura controllata (4°C). Arteriole con un diametro esterno < 200 micron sono
state identificate, sezionate con cura e pulite del tessuto adiposo aderente. I microvasi mesenterici cosi’ isolati, sono stati incannulati con micropipette e collegati a reservoirs pieni con soluzioni PSS, senza BSA. L’altezza dei reservoirs è stato impostata per ottenere una pressione intraluminale di 60 cmH2O. Le arteriole che non erano in grado di
mantenere costante la pressione endoluminale, in assenza di trattamento, sono state
escluse dall'analisi. Il diametro interno è stato misurato con un sistema di
video-calibrazione collegato ad un sistema composto da un microscopio ed una videocamera.
Le arteriole sono state lentamente riscaldate a 37°C e valutate per lo sviluppo del tono
spontaneo. Tutti i farmaci sono stati aggiunti alla soluzione tampone precedentemente
descritta (bath). I dosaggi dei farmaci aggiunti sono espressi come la concentrazione
cumulativa finale in moli nella soluzione tampone, assumendo come non significativo il
spontaneamente per un tempo compreso tra i 30 ed i 45 minuti dalla dissezione, poi il
bath è stato sostituito. Dopo 15 minuti circa, i vasi sono stati costretti con Endotelina (10
-9
M), e nuovamente è stato sostituito il bath. A seguire concentrazioni crescenti di VIP
(VIP: 10-8, 10-7, 10-5, 5x10-5 M) sono state aggiunte alla soluzione tampone, al fine di
valutare la risposta agonista-mediata, dilatazione endotelio-dipendente. E’ stata inoltre
valutata la risposta vasodilatatoria a dosi crescenti di Acetilcolina (Ach, dal 10-8M a 10-5
M) e la dilatazione endotelio-indipendente mediante risposta al nitroderivato di sodio
(5X10-5 M). La vasodilatazione percentuale è stata calcolata come variazione nel
diametro del vaso indotta da un intervento farmacologico, rispetto al totale di tono attivo
VALUTAZIONE DELL’EFFICIENZA DELLA CATENA DI TRASPORTO DEGLI ELETTRONI A LIVELLO VASCOLARE AORTICO
Preparazione di tessuto omogenato di Aorta l’aorta toracica di ratti nei 4 gruppi di studio e’ stata prelevata, gentilmente pulita, rimosso il grasso peri-adventiziale ed il tessuto connettivo circostante. L'aorta e’ stata poi tagliata in piccoli pezzi, ed ulteriormente sminuzzata nel buffer SHE (250 mM sucrose, 10 mM HEPES, 1 mM
EDTA, pH7.2), successivamente digerita con Collagene tipo II (2 mg/ml, 278 unita/mg, Worthington Biochemical Co. Lakewood, NJ). L’omogenato cosi’ ottenuto e’ stato poi centrifugato a 2,000 g per 20 min a 4 C. Il supernatante sottoposto alla determinazione
proteica con il metodi di Lowry e l'assay per determinare l'attività degli enzimi della
catena fosforilativa.
Assay per valutare l'attività’enzimatica della catena mitocondriale di trasporto degli elettroni (ETC) La catena di trasporto degli elettroni e’ stata valutata come descritto in studi già’pubblicati e validati, con alcune modifiche.22,23,24
Aliquote appropriate di tessuto omogenato di aorta sono state prelevate e sottoposte all’analisi per valutare l'attività’ enzimatica (ETA) usando uno spettrofotometro UV/VIS (Shimadzu, model UV2401PC). Brevemente, il Complesso I è stato testato attraverso il monitoraggio del consumo di NADH a 340 nM mediante l’aggiunta a 25 mg/ml di proteine mitocondriali di 5.0 µM di antimicina A, 60 µM di ubichinone I e 75 mM di
NADH. 25-27 L'attività’ del Complesso II e’ stato stimato mediante la riduzione di
dichlorophenol indophenol DCPIP stimolata da TTFA (theonyl trifluroacetone)
riduzione del ferricytochrome c stimolato dall' ubiquinol-2 (Q2H2), e verificato
all’inibizione con Antimycin A come gia’ dimostrato in precedenza.28
L’attivita’ del complesso IV e’ stata valutata mediante misurazione dell’ossidazione del ferrocytochrome c e ulteriormente confermata mediante inibizione con KCN. 27, 29 L’attivita’ del super complesso SCR (complex II + complex III) e’ stato analizzato mediante la riduzione del ferricytochrome c stimolato dal succinato. 27, 30
ISOLAMENTO DI MITOCONDRI MIOCARDICI E VALUTAZIONE DELL’EFFICIENZA RESPIRATORIA
I mitocondri sono stati isolati da porzioni di ventricolo sinistro come riportato in altri
studi e protocolli approvati precedentemente.31 Il tessuto miocardico e’ stato
omogeneizzato in 180 mM KCl, 5.0 mM Mops, 2.0 mM EGTA, pH 7.25 (20 ml/g
tessuto) con un omogeneizzatore Polytron (impostazione bassa, 3s). Il processo di respirazione mitocondriale e’ stato valutato come descritto in studi gia’ pubblicati e validati, mediante centrifugazione differenziale con alcune modifiche. 22
I mitocondri sono stati precipitati per centrifugazione a 16.000 x g per 10 minuti e al
termine risospesi in un medium che conteneva 230 mM manitol, 70 mM sucrose, 1 mM
EDTA, e 5 mM Trizma/HCl buffer, pH 7.4 (M-buffer), inibitore protease/phosphtase (1
compressa di complete/phosSTOP in 10 ml, Roche Applied Science, Indinapolis, IN)
prima della misura del consumo di ossigeno. La respirazione mitocondriale è stata
misurata con il metodo polarografico utilizzando un elettrodo di ossigeno di Clark
(Hansatech Oxytherm Unità Electron, Norfolk, UK). Preparazioni mitocondriali sono
stati aggiunti ad una concentrazione dei media di 0.5 mg/ml, ed il consumo di ossigeno è stato indotto dall’aggiunta di malato (5 mM) e glutammato (140 mM). ADP (0.2 mM) e’ stata successivamente aggiunta ed i seguenti parametri misurati: Stato 2, consumo di O2 prima dell’aggiunta di ADP; Stato 3, consumo di ossigeno stimolato dall'ADP; Stato 4, consumo di ossigeno dopo l’aggiunta di oligomicina (2 µg/ml) seguito da ADP; Uncoupling oxygen consumption (consumo di ossigeno durante disaccoppiamento della catena fosforilativa), indotto da FCCP (2.5 µM) seguito dall’aggiunta di oligomicina.
L’elettrodo per la misurazione dell’O2 e’ stato calibrato assumendo che la concentrazione
STAINING TISSUTALE DI REGIONI IPOSSICHE MIOCARDICHE
Al fine di valutare la presenza di ischemia miocardiche nei 4 gruppi di trattamento, ai ratti e’ stato somministrato per via endovenosa il cloridrato di pimonidazole, un sostanza nota commercialmente come Hypoxyprobe (HPI Inc, Burlington, MA,USA) utilizzato
quale marcatore di ipossia. L' Hypoxyprobe si lega ad aree di tessuto con pO2 inferiore a
10 mmHg (valori di pO2 normali, in aree non ischemiche miocardiche superiori a 15
mmHg). Hypoxyprobe (60 mg/kg di peso corporeo) è stato somministrato per via
endovenosa, durante infusione di Norepinefrina ad alte dosi (NE 10 ug/Kg/min) per 20
minuti, allo scadere dei quali i ratti sono stati poi sacrificati.
Aree di tessuto del ventricolo sinistro dello spessore circa di 3 mm, nelle porzioni peri-papillari, sono state sezionate con un apposito microtomo. I tessuti cosi’ prelevati sono stati immediatamente fissati e montati. Almeno 30 sezioni di circa 10 µm sono state
acquisite per ogni animale. Di queste almeno 10 sezioni per ogni animale sono state
selezionate in modo casuale per scopi di immunostaining. Ogni sezione è stata bloccata
con siero, seguita dal trattamento con anticorpi anti-pimonidazole (anticorpi primari) e
successivamente con anticorpi secondari colorati (di asino diretti anti-topo 595 nm).
Dopo il legame, le sezioni sono state lavate e le immagini di fluorescenza sono state
acquisite utilizzando un microscopio epifluorescente. Almeno 10 campi, scelti a caso tra
le sezione colorate con gli anticorpi suddetti, sono stati acquisiti, confrontati ed
B. Studi in vitro
In questa sezione verranno discussi i seguenti metodi:
X. Isolamento di arteriole coronariche
XI. Isolamento dei cardiomiociti e stimolazione elettrica
XII. Valutazione della risposta dilatatoria al conditioned buffer di miociti cardiaci
isolati
XIII. Misurazione dell’H2O2 nel conditioned buffer di miociti cardiaci isolati
XIV. Misurazione delle purine nel conditioned buffer di miociti cardiaci isolati
Tutti gli animali (ZL e ZOF) da cui sono state isolate arteriole coronariche e cardiomiociti
per questa sessione di studi in vitro (n=8 in ogni gruppo), sono stati trattati per 3 giorni
consecutivi con mt-tat-Exo III o con mt-tat-Endo III o con soluzione eparinata nei
ISOLAMENTO DI ARTERIOLE CORONARICHE
Per l’isolamento di arteriole coronariche, i ratti (n=4 in ogni gruppo) sono stati successivamente anestetizzati con pentobarbital sodico (alla dose di 50 mg/Kg
somministrata per via intra peritoneale) e una sternotomia mediana è stata eseguita. Il
cuore è stato asportato e messo in soluzione fisiologica salina tamponata (PSS) a 4°C. Il buffer utilizzato per la dissezione dei microvasi coronarici e’ composto da (in mmol/L): 145 NaCl, 4.7 KCl, 2 CaCl2, 1.17 MgSO4, 1.2 NaH2PO4, 5 glucosio, 2 piruvato, 0.02
EDTA, 3.0 acido propanesulfonico 3-N-morpholino (MOPS) e 1% di albumina sierica
bovina (1 gm/100 ml). La soluzione è stata tamponata a pH di 7.4 a 4°C. Il PSS (bath)
utilizzato per perfondere i vasi coronarici durante lo studio delle risposte dilatatorie ha la
stessa composizione di cui sopra, ma è stata tamponata a pH di 7.4 e portato alla
temperatura di 37°C. Singole arteriole sono state sezionate dal ventricolo sinistro di ratti
ZL e ZOF secondo protocolli precedentemente descritti ed approvati in altri studi.32, 33
Una porzione del ventricolo sinistro comprendente arteriole di dimensioni adeguate è
stata selezionata, asportata e posizionata sotto un microscopio da dissezione. Ogni
arteriola liberata dal tessuto muscolare circostante è stata isolata e trasferita in un nuovo
piano da dissezione a temperatura controllata (4°C) contenente soluzione fisiologica
tamponata (PSS). I rami laterali sono stati legati ed esclusi con suture 11-O. I microvasi
sono stati quindi trasferiti in una camera di lucite, incannulati e legati alle due estremità
con micropipette. La preparazione è stata poi trasferita sotto un microscopio di fase
invertito. Le perdite sono state valutate misurando la pressione intraluminale a portata
adeguatamente ottenute e non ci sono leaks da rami laterali o nelle estremità. Tutte le
preparazioni nei quali i microvasi non erano in grado di mantenere costante la pressione
endoluminale, in assenza di trattamento, sono stati esclusi dallo studio. Tutti gli agenti
(conditioned buffer e Catalasi) sono stati aggiunti alla soluzione tampone (bath)
ISOLAMENTO DI MIOCELLULE CARDIACHE E STIMOLAZIONE ELETTRICA
Miociti cardiaci sono stati enzimaticamente isolati da cuori di ratti ZL e ZOF (n=4, in
ogni gruppo). Dopo l'asportazione del cuore, l'aorta è stata incannulata, e la preparazione
è stata sospesa in un apparato di perfusione. Il cuore è stato inizialmente perfuso per via
retrograda dall'aorta a 37°C con soluzione tampone ossigenata-HEPES
(4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid ) non contenete calcio (pH 7,45 [titolato
con 5 M NaOH]) per risciacquare il sangue ed eliminare la contrazione residua. La
soluzione utilizzata per perfondere inizialmente il cuore e’ cosi’ composta in mM: 10
HEPES, 30 taurina, 113 NaCl, 4.7 KCl, 0.6 KH2PO4, 0.6 Na2HPO4, 1.2 MgSO4, 0.032
rosso fenolo, 12 NaHCO3 e 10 KHCO3. Dopo la cessazione dell’attività contrattile, la
perfusione è stata mantenuta con un buffer contente tutte le sostanze suddette e in
aggiunta 0.25 mg/ml di collagenase (liberase blendzyme I, Roche), 0.14 mg/ml di tripsina
e 12.5 µM di CaCl2. Dopo aver mantenuto la perfusione del cuore per ulteriori 10-12
minuti con questa nuova soluzione, si e’ proceduti all'identificazione dei miociti isolati nel perfusato dal cuore cosi’ ottenuto. I cuori sono quindi stati staccati dall'apparecchio di perfusione e posti in una soluzione "stop" che contiene il buffer di perfusione con il 10%
di BSA e 12.5 mM Ca2 +. Il cuore è stato ulteriormente ripartito in piccoli pezzi che sono
stati resi ancora più piccoli posizionandoli nel buffer di stop. Dopo la conferma microscopica della presenza di miociti, il buffer e’ stato filtrato e le cellule isolate sono state posizionate in una provetta da 50 ml. Successivamente, CaCl2 è stato aggiunto in
state lasciate sedimentare creando un pellet, mediante centrifugazione per 5 minuti a
1500 rpm, e il buffer separato e scartato. Le cellule sono state risospese nello stop buffer
contenete calcio, e poi piccole aliquote sono state utilizzate per la conta delle cellule,
utilizzando un emocitometro, per consentire la diluizione/concentrazione (tramite
centrifugazione) finale di 100.000 cellule per ml. La vitalità del miociti è stata determinata mediante test di esclusione al trypan blu e configurazione a “barra”. In media oltre il 70% delle cellule mostrava come configurazione tipo quella a “barra”.
I cardiomiociti cosi’ isolati, sono stati stimolati elettricamente a 200 e 400 ipm, ed il
conditioned buffer rilasciato in coltura (sia dopo stimolazione che a riposo) utilizzato non
solo per valutare la produzione di specifiche sostanze vasoattive rilasciate dai
cardiomiociti, quali H2O2 ed eventuali purine, ma anche per stabilire gli effetti vasoattivi
in arteriole coronariche isolate sia da ratti ZL che ZOF. Oltre a questi protocolli, abbiamo
trattato il conditioned buffer con catalasi (da 500 a 1000 U/mL), enzima scavenger dell’H2O2, per determinare se il catabolismo dell’H2O2 modificasse in maniera
sostanziale la vasodilatazione arteriolare indotta dal conditioned buffer prodotto dai
cardiomiociti stimolati e a riposo. Inoltre, nel gruppo ZL, il conditioned buffer e' stato
trattato con Catalasi e con 8-pSPT, inibitore del recettore purinergico A1 per determinare
VALUTAZIONE DELLA RISPOSTA DILATATORIA AL CONDITIONED BUFFER DI MIOCITI CARDIACI ISOLATI
Per dimostrare che i livelli di H2O2 e altri metaboliti rilasciati dai cardiomiociti
metabolicamente attivi sono in grado di produrre vasodilatazione, aliquote del
conditioned buffer sono state rimosse dalla sospensione dei miociti e somministrate ad
arteriole coronariche isolate. Il conditioned buffer da ZL-CM e ZOF-CM e’ stato
aggiunto al bath di arteriole isolate da entrambi gli strain (ZOF e ZL), per verificare la
risposta vasodilatatoria ed per chiarire se una diversa risposta fosse eventualmente da
attribuire alla produzione di differenti molecole vasoattive da ZL-CM o ZOF-CM o ad un’alterata risposta arteriolare (ZOF vs. ZL).
MISURAZIONE DI H2O2 NEL CONDITIONED BUFFER DI MIOCITI CARDIACI ISOLATI
La produzione di perossido di idrogeno (H2O2) e’ stata misurata elettrochimicamente
mediante il sistema APOLLO 4000 (World Precison Instruments, Europe). Questo
strumento è un analizzatore ottico multicanale di radicali liberi, progettato per il
rilevamento di una serie di specie reattive dell’ossigeno (in particolare NO, H2O2). Il
sistema Apollo 4000 che consente di stimare anche quantità’ infinitesimali di perossido di idrogeno (H2O2 rilevata <10 nM a 100 mM), utilizza un sensore di 2,0 millimetri
prodotto in acciaio inox (ISO-HPO-2, specificatamente progettato per l'impiego in colture
cellulari e applicazioni simili), rivestito da una membrana sostituibile (# 600012) e
contenente una soluzione elettrolitica interna ricaricabile (# 100042). Il sensore è stato
posizionato in campioni, aliquote di 50 l, del conditioned buffer derivato dalla sospensione dei cardiomiociti isolati da ZL-CM e ZOF-CM. I campioni di conditioned
buffer sono stati ottenuti da miociti non stimolati e durante la stimolazione mantenuta per
circa 20 minuti a 200 o 400 ipm. Ogni elettrodo e’ stato calibrato usando diluizioni seriate
di H2O2, e le correnti registrate dal campione di conditioned buffer sono state calcolate
QUANTIZZAZIONE DELLE PURINE (AMP, ADP, ATP E ADENOSINA) RILASCIATE NEL CONDITIONED BUFFER DI MIOCITI CARDIACI ISOLATI
Il dosaggio delle purine è stato condotto con cromatografia a coppia ionica mediante
HPLC Beccando, costituito da un sistema a due pompe (Beckman System Gold
Programmable Solvent Module 125) con iniettore da 20 μl (injector loop Rheodyne
7725i) e da un rivelatore spettrofotometrico UV (Beckman System Gold Detector 166) ad una lunghezza d’onda di 254 nm, collegato ad un computer SuntaQ 386, provvisto di software per la registrazione, l’identificazione e la calibrazione (Beckman System Gold V3.10). Per la separazione delle sostanze è stata utilizzata una colonna C-18 (Beckman
C-18 Analytical P/N 243533, Ultrasphere ODS 4.6 mm-25 cm) munita di precolonna C-
18. Il metodo cromatografico impiegato ha permesso la separazione e la determinazione
quantitativa di AMP, ADP, ATP e adenosina. I picchi cromatografici delle sostanze presenti nelle soluzioni campione sono stati analizzati con l’ausilio di una curva di taratura (0,1-75 μM) per la determinazione delle purine nel campione. Il campione e’
costituito dal conditioned buffer ottenuto da cardiomiociti isolati di ZL e ZOF, indicati
rispettivamente come ZL-CM e ZOF-CM, non stimolati e stimolati elettricamente a 200 e
ANALISI STATISTICA DEI DATI
L’analisi statistica è stata effettuata utilizzando il software di statistica GraphPad Prism 4. I risultati sono espressi come media ± SEM, salvo diversamente indicato. Il test two-way
ANOVA, per misure ripetute seguito dal Bonfferoni post-test o l’analisi della varianza
(one-way ANOVA) sono stati utilizzati quando necessari per l'analisi statistica. Un valore
RISULTATI
VARIABILI BIOMETRICHE:
In condizioni di riposo non si sono osservate variazioni significative nei 4 gruppi per quel
che riguarda i principali parametri emodinamici: pressione arteriosa sistolica (PAS,
mmHg), diastolica (PAD, mmHg) e media (MAP, mmHg) e frequenza cardiaca (HR). Nei
sottogruppi obesi (ZOF vs. ZOF + Endo III) e magri (ZL vs. ZL + Exo III) il peso corporeo (BW, g) e’ risultato paragonabile. (Tabella I)
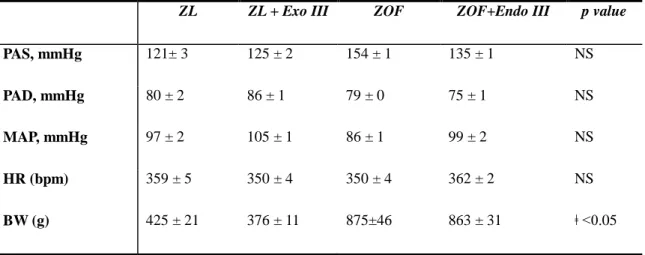
Tabella I : Riassunto delle principali variabili biometriche nei 4 gruppi di studio
ZL ZL + Exo III ZOF ZOF+Endo III p value
PAS, mmHg 121± 3 125 ± 2 154 ± 1 135 ± 1 NS
PAD, mmHg 80 ± 2 86 ± 1 79 ± 0 75 ± 1 NS
MAP, mmHg 97 ± 2 105 ± 1 86 ± 1 99 ± 2 NS
HR (bpm) 359 ± 5 350 ± 4 350 ± 4 362 ± 2 NS
BW (g) 425 ± 21 376 ± 11 875±46 863 ± 31 ǂ <0.05
Sezione I: studi in vivo
VALUTAZIONE DELLA FUNZIONE CARDIACA SISTOLICA E
DIASTOLICA A RIPOSO
Nella Tabella II sono riportati per brevità solo i principali parametri utilizzati per valutare
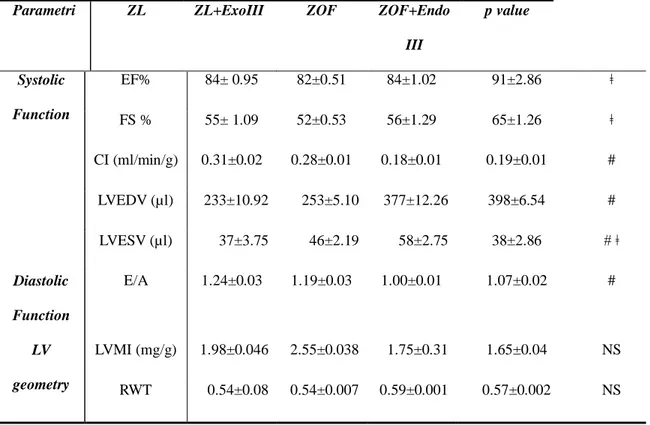
la funzione sisto-diastolica nei 4 gruppi di trattamento. E’ importante sottolineare che la funzione contrattile e’ apparentemente conservata nel gruppo ZOF, con valori di EF% e FS% indicativi di funzione sistolica globale ventricolare sinistra conservata, rispetto ai
valori di normalità per questo strain di ratto (ZL EF% 84± 0.95 e FS% 55± 1.09 vs. ZOF
EF% 84±1.02 e FS% 56±1.29; p=NS). Tuttavia ad una più attenta analisi risulta evidente
che il sottogruppo degli obesi presenta un indice cardiaco (CI ml/min/g) a riposo
significativamente ridotto rispetto al gruppo magri (CI ml/min/g, ZL 0.31±0.02 vs. ZOF
0.18±0.01; p<0.001) e solo parzialmente migliorato dopo il trattamento con
mt-tat-EndoIII (CI ml/min/g: ZOF 0.18±0.01 vs. ZOF+mt-tat-EndoIII 0.19±0.01; p=NS). Il trattamento
con mt-tat-Exo III nel gruppo ZL ha determinato una riduzione non significativa della
funzione contrattile come dimostrato da valori solo lievemente ridotti di EF%, FS% e
indice cardiaco (EF% ZL 84 ± 0.95 vs. ZL+ExoIII 82 ± 0.51; FS% ZL 55 ± 1.09 vs.
ZL+ExoIII 52 ± 0.53; CI ml/min/g ZL 0.31 ± 0.02 vs. ZL+ExoIII 0.28 ± 0.01; p=NS). Al
trattamento con mt-tat-EndoIII ha fatto seguito un incremento significativo del volume
telediastolico ventricolare sinistro ed una riduzione del volume telesistolico rispetto al
58±2.75 vs. ZOF+EndoIII 38±2.86 µl; p<0.05) con una riduzione consensuale dell’indice
di massa ventricolare sinistra (LVMI, mg/g) e del relative wall thickness (RWT), senza pero’ raggiungere la significatività statistica. Si segnala riduzione significativa del rapporto E/A nel gruppo degli obesi verso gruppo magri (E/A ZL 1.24±0.03 vs. ZOF
1.00±0.01; p< 0.05).
Tabella II: Valutazione ecografica della funzione sisto-diastolica nei 4 gruppi di trattamento
Parametri ZL ZL+ExoIII ZOF ZOF+Endo
III p value Systolic Function EF% 84± 0.95 82±0.51 84±1.02 91±2.86 ǂ FS % 55± 1.09 52±0.53 56±1.29 65±1.26 ǂ CI (ml/min/g) 0.31±0.02 0.28±0.01 0.18±0.01 0.19±0.01 # LVEDV (µl) 233±10.92 253±5.10 377±12.26 398±6.54 # LVESV (µl) 37±3.75 46±2.19 58±2.75 38±2.86 # ǂ Diastolic Function E/A 1.24±0.03 1.19±0.03 1.00±0.01 1.07±0.02 # LV geometry LVMI (mg/g) 1.98±0.046 2.55±0.038 1.75±0.31 1.65±0.04 NS RWT 0.54±0.08 0.54±0.007 0.59±0.001 0.57±0.002 NS
VALUTAZIONE DELLA PERFORMANCE CONTRATTILE DURANTE STRESS CON NOREPINEFRINA: STIMA DEL LAVORO CARDIACO E DELL’INDICE CARDIACO
L’infusione di NE a dosi crescenti ha determinato nei 4 gruppi un paragonabile incremento del lavoro cardiaco (p= NS), calcolato come il doppio prodotto (DP) della
frequenza cardiaca per la pressione arteriosa media. Tuttavia la situazione e’
completamente differente se anziché considerare parametri emodinamici quali MAP e HR per valutare la performance cardiaca si utilizza l’indice cardiaco, ovvero la portata cardiaca corretta per il peso corporeo dell’animale. Tale correzione per il peso corporeo si
rende necessaria, per tener conto delle differenze biometriche tra ZOF e ZL,
indipendentemente dal tipo di trattamento ricevuto. Il grafico in Figura 5 rappresenta il
DP raggiunto per ogni dose infusa di NE (da 2.5 a 10 µg/Kg/min) nei 4 gruppi di studio,
mentre nella Figura 6 sono riportati per ogni gruppo ed in ogni condizione, i valori di
Indice Cardiaco (CI ml/min/g di peso corporeo), dopo somministrazione del bloccante
ganglionico esametonio (riportato come “baseline”). Come si può vedere il trattamento
con mt-tat-Exo III non determina variazioni significative nel DP raggiunto (p=NS vs. ZL per ogni condizione esplorata), con una riduzione lieve invece dell’indice cardiaco, che raggiunge la significatività statistica solo alla dose di NE 5.0 µg/Kg/min.
I ratti ZOF presentano valori di DP raggiunto per ogni step di NE sovrapponibili a quello
dei ZL e degli altri 2 gruppi di trattamento (ZOF+Endo III e ZL+Exo III), mentre la
portata cardiaca durante stress con NE non aumenta in maniera sostanziale come nel
frammentazione del mt-DNA induce nel rispettivo gruppo di trattamento (ZOF+Endo
III), nei ratti obesi, un miglioramento sostanziale della performance cardiaca (ZOF vs.
ZOF +Endo III, p<0.05) con valori di DP e di CI paragonabili a quelli dei ZL alle dosi di
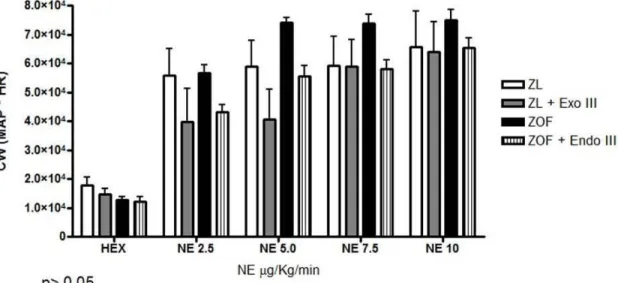
Figura 5: In questo grafico sono riportati i valori di DP (MAP*HR) raggiunti nei 4 gruppi di studio durante
stress con NE a dosi crescenti (NE 2.5-10 µg/Kg/min). Il lavoro cardiaco cosi’ stimato e’ risultato paragonabile in tutti i gruppi ed in tutte le condizioni esplorate (p>0.05).
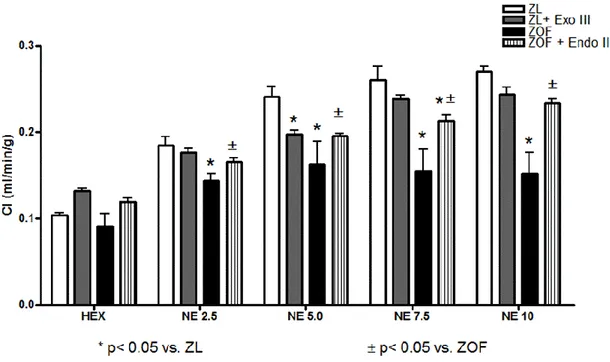
Figura 6: in questo grafico sono riportati i valori di indice cardiaco nei 4 gruppi ed in tutte le condizioni di
studio. Non ci sono differenze statisticamente significative per i valori di CI basali (in condizioni di riposo, dopo somministrazione di esametonio). L’induzione di disfunzione mitocondriale nei ratti magri (ZL + Exo III), determina solo una lieve riduzione della portata cardiaca durante stress che raggiunge la significatività statistica solo alla dose di 5 µg/kg/min(ZL + Exo III vs. ZL, p<0.05). Come si può vedere i ratti ZOF presentano valori persistentemente ridotti di CI (ml/min/g) rispetto al gruppo ZL, per tutte le dosi di di NE somministrata. La riparazione del mt-DNA a seguito del trattamento con mt-tat-Endo III nel gruppo ZOF, induce un miglioramento della performance cardiaca durante stress (p< 0.05 ZOF vs. ZOF+ Endo III, da NE 2.5 a 10 µg/Kg/min), con valori di CI paragonabili nei due gruppi alle dosi di NE rispettivamente di 2.5-5.0-10µg/Kg/min (ZL vs. ZOF+Endo III, p=NS).
VASODILATAZIONE CORONARICA METABOLICA
In tutti e 4 i gruppi di studio il valore di flusso sanguigno miocardico (MBF) in condizioni basali, dopo somministrazione del bloccante ganglionico esametonio, e’ risultato paragonabile (MBF ml/min/g: ZL 8.2±0.9 vs. ZL+ExoIII 7.2±0.3 vs. ZOF 7.0
±0.4 vs. ZOF+Endo III 6.9 ±0.5, p=NS). Come atteso, i ratti ZOF hanno mostrato
compromissione della regolazione metabolica del flusso miocardico, esibendo scarso
incremento del MBF durante stress con Norepinefrina (NE 2.5µg/Kg/min: ZL 12.4±0.1
vs. ZOF 8.4±0.3ml/min/g; NE 5.0µg/Kg/min: ZL 15.4±0.5 vs. ZOF 9.4±1.1 ml/min/g;
NE 7.5µg/Kg/min: ZL 16.1±0.6 vs. ZOF 10.0±0.6 ml/min/g; NE 10 µg/Kg/min: ZL 19.8±0.3 vs. ZOF 10.7±1.0 ml/min/g). L’induzione di disfunzione mitocondriale mediante somministrazione per 3 giorni della proteina ricombinate mt-tat-Exo III ha
attenuato, nel gruppo ZL+Exo III, la vasodilatazione coronarica durante stress cardiaco
(NE 2.5µg/Kg/min: ZL 12.4±0.1 vs. ZL+Exo III 9.1±0.5 ml/min/g; NE 5.0µg/Kg/min:
ZL 15.4±0.5 vs. ZL+Exo III 9.1±0.9 ml/min/g; NE 7.5µg/Kg/min: ZL 16.1±0.6 vs.
ZL+Exo III 10.9±2.3 ml/min/g; NE 10 µg/Kg/min: ZL 19.8±0.3 vs. ZL+Exo III 10.6±2.3
ml/min/g). Inoltre, in accordo con la nostra ipotesi, i ratti obesi in cui lo stress ossidativo
e la frammentazione del mt-DNA erano stati prevenuti ed attenuati in seguito al
trattamento con mt-tat-Endo III, hanno esibito una capacita’ maggiore rispetto ai ZOF di incrementare il flusso sanguigno miocardico per far fronte alle necessita’ metaboliche del tessuto cardiaco (NE 2.5µg/Kg/min: ZOF+Endo III 9.5±0.7 vs. ZOF 8.4±0.3ml/min/g;
NE 5.0µg/Kg/min: ZOF+Endo III 12.6±0.8 vs. ZOF 9.4±1.1 ml/min/g; NE
ZOF+Endo III 15.2±0.9 vs. ZOF 10.7±1.0 ml/min/g). Complessivamente questi dati
(Figura 7) dimostrano che la capacita’ di incrementare il flusso miocardico durante aumento del lavoro cardiaco e’ attenuata dalla presenza di disfunzione mitocondriale (vedi ZOF e ZL+Exo III), il cui trattamento risulta efficace per restaurare un’appropriata
0 1.0×104 2.0×104 3.0×104 4.0×104 5.0×104 6.0×104 7.0×104 8.0×104 9.0×104 0.0 2.5 5.0 7.5 10.0 12.5 15.0 17.5 20.0 22.5 ZL ZL+Endo III ZOF ZOF+Endo III CW (MAP*HR) M B F ( m l/ m in/ g )
Figura 7: Relazione lavoro cardiaco-flusso miocardico (ml/min/g) per tutti e 4 i gruppi di studio, in
condizioni basali (dopo somministrazione del bloccante ganglionico esametonio) e durante stress con NE (2.5-5.0-7.5-10 µg/Kg/min). Il valore di MBF in condizioni basali e’ risultato paragonabile nei 4 gruppi di confronto. Il gruppo dei ZL (quadrati bianchi) mostra la migliore relazione lavoro cardiaco/flusso miocardico, mentre la vasodilatazione coronarica metabolica risulta significativamente depressa nel gruppo ZOF (rombi neri). L’induzione di danno al mt-DNA nel gruppo ZL ha determinato una compromissione significativa della regolazione coronarica del flusso miocardico durante incremento del lavoro cardiaco (p<0.05 ZL vs. ZL+ExoIII e p=NS ZL+Exo III vs. ZOF). I ratti obesi trattati con mt-tat-Endo III hanno esibito migliore accoppiamento lavoro cardiaco/MBF durante stress con NE (ZOF+Endo III vs. ZL p=NS, ZOF+Endo III vs. ZOF p<0.05) se confrontati con ZOF.
VASODILATAZIONE ENDOTELIO-MEDIATA ED ENDOTELIO-INDIPENDENTE IN ARTERIOLE MESENTERICHE ISOLATE
Un quadro di disfunzione endoteliale (Figura 8), come dimostrato dalla compromissione
della vasodilatazione di arteriole mesenteriche isolate in risposta alla somministrazione di
VIP a dosi crescenti, è stata evidenziato nei gruppi con danno mitocondriale preesistente
o indotto (ZOF e ZL+Exo III). La dilatazione Ach-mediata inoltre, è risultata
compromessa solo nei ratti ZOF e completamente normalizzata dopo trattamento con
mt-tat-Endo III. La vasodilatazione endotelio dipendente è stata restaurata nel gruppo
ZOF+Endo III. Tutti e 4 i gruppi di trattamento hanno presentato normale dilatazione
arteriolare mesenterica in risposta alla somministrazione di sodio nitroprussiato (SNP)
Figura 8: Vasodilatazione endotelio-dipendente in arteriole mesenteriche isolate, in risposta a dosi
crescenti di VIP e Ach nei 4 gruppi di studio. La risposta al VIP e’ risultata significativamente depressa nei ratti con danno ossidativo mitocondriale (ZOF e ZL+Exo III vs. ZL p< 0.05). Il trattamento con mt-tat-Endo III e’ risultato solo parzialmente efficace nel restaurare tale risposta. La vasodilatazione a dosi crescenti di Ach e’ risultata compromessa nel gruppo ZOF ma completamente normalizzata nel gruppo ZOF+Endo III e ZL+Exo III (p<0.05 vs. ZL). Non si sono registrate alterazioni della vasodilatazione endotelio-indipendente (dati non mostrati), con dilatazione SNP-mediata paragonabile nei 4 gruppi di studio (p=NS).
VALUTAZIONE DELLA RESPIRAZIONE MITOCONDRIALE IN MITOCONDRI ISOLATI DA TESSUTO CARDIACO
Nel grafico in Figura 9 sono riportati i dati relativi allo studio della respirazione
mitocondriale, utilizzando i substrati del Complesso I, in mitocondri isolati da tessuto
cardiaco nei 4 gruppi di trattamento. Alterazioni dello Stato 3 (ADP-dipendente) e del
consumo di O2 in condizioni di disaccoppiamento della catena fosforilativa (uncoupling
oxygen consumption) sono state identificati nel gruppo dei ratti obesi, anomalie che
persistono nel gruppo ZOF+Endo III, seppur di grado inferiore (p<0.05 vs. ZL). Il
trattamento con mt-tat-Exo III ha ridotto le capacita’ bioenergetiche massime mitocondriali nei ratti ZL (p<0.05 vs .ZL), senza pero’ indurre sostanziali modifiche nella capacita’ di sintetizzare ATP a partire dall’ADP durante lo Stato 3 della respirazione mitocondriale.
Sta te 3 Sta te 4 RC R Sta te 2 con sump tion 2 Un coup ling O 0 5 10 ZL ZL+Exo III ZOF
ZOF + Endo III
* p <0.05 vs ZL * * * * * 50 150 250 350 450 * n m o l O2 /m in /g p ro t.
Figura 9: Valutazione della respirazione mitocondriale (NADH-dipendente) in mitocondri isolati da cuori
di ratti. La presenza di disfunzione mitocondriale si manifesta in ratti ZOF e ZOF+Endo III con ridotta sintesi di ATP durante lo Stato 3 della respirazione cellulare e mediante alterazione delle proprietà bioenergetiche massimali
In Figura 10 sono rappresentati i dati relativi alla respirazione mitocondriale utilizzando i
substrati del Complesso mitocondriale II (FADH2-dipendente), in mitocondri isolati da
cuori di ratti ZOF e ZOF+Endo III. Come si può osservare, in questo caso e’ stata riscontrata una differenza significativa per il consumo di O2 in condizioni di
disaccoppiamento della catena fosforilativa, con in particolare migliori condizioni
State 3 State 4 RCR State 2 cons umption 2 Uncou pling O 0.0 2.5 5.0 ZOF ZOF+EndoIII * p< 0.05 vs. ZOF * 50 150 250 350 450 n m o l O2 /m in /m g p ro t.
Figura 10: Valutazione della respirazione mitocondriale attraverso il Complesso II (FADH2-dipendente) in
mitocondri isolati da cuori di ratti obesi (ZOF e ZOF+EndoIII). A seguito del trattamento con mt-tat-EndoIII si osserva un maggior consumo di O2 in condizioni di disaccoppiamento della catena fosforilativa,
VALUTAZIONE DELL’EFFICIENZA DELLA CATENA DI TRASPORTO DEGLI ELETTRONI VASCOLARE AORTICA
In Figura 11 sono riportati i risultati relativi allo studio del sistema di trasporto degli
elettroni (ETC activity), da tessuto vascolare aortico prelevato nei 4 gruppi. Differenze
significative sono state riscontrate per quel che riguarda l'attivita' di tutti e 4 i Complessi mitocondriali nei ratti obesi (p<0.05 ZL vs. ZOF). In particolare e’ risultata significativamente alterata la funzione dei complessi III e IV, importanti perché coinvolti
rispettivamente nella generazione di H2O2 e nella sintesi di ATP. La riparazione dei danni
da stress ossidativo al mt-DNA mediante la somministrazione della proteina ricombinante
mt-tat-Endo III negli animali obesi, ha migliorato significativamente l'attività di tutti i
Complessi di trasporto mitocondriali (p<0.05 ZOF vs. ZOF+Endo III; p=NS ZOF+Endo III vs. ZL). L’induzione di frammentazione del mt-DNA ha ridotto, seppur non in maniera statisticamente significativa, l'attività del sistema di trasporto degli elettroni nei
Complex I ZL ZL+E xoIII ZO F ZOF+ End oIII 0 5 10 15 20 25 30 35 40 45 ZL ZL+ExoIII ZOF ZOF+EndoIII * * p < 0.05 vs. ZL ± p < 0.05 vs. ZOF ± n m o l o x id a ti o n /m in /m g p ro t. Complex III ZL ZL+Ex oIII ZOF ZOF +End oIII 0 25 50 75 100 125 150 175 ZL ZL+ExoIII ZOF ZOF+EndoIII * * p< 0.05 vs ZL ± p< 0.05 vs ZOF ± n m o l C y t c r e d u c e d /m in /m g p ro t. Complex II ZL ZL+ ExoI II ZOF ZO F+End oIII 0 10 20 30 ZL ZL+ExoIII ZOF ZOF+EndoIII * p< 0.05 vs. ZL * n m o l s u c c in a te o x id a ti o n /m in / m g p ro t. Complex IV ZL ZL+E xoIII ZOF ZOF +End oIII 0 25 50 75 100 125 150 175 ZL ZL+ExoIII ZOF ZOF+EndoIII * p < 0.05 vs ZL ± p< 0.05 vs ZOF ± n m o l f e rr o c y t c o x id a tio n /m in /m g p ro t.
Figura 11: Rappresentazione schematica dell'attività della catena di trasporto degli elettroni (Complessi
mitocondriali I-IV), di tessuto vascolare aortico isolato in tutti e 4 i gruppi. Si sono osservate differenze significative per quel che riguarda l'attività dei Complessi I-IV nei ZOF (p<0.05 vs. ZL). Il trattamento con mt-tat-Endo III ha significativamente migliorato l'attività mitocondriale nei ratti obesi (p<0.05 ZOF vs. ZOF+Endo III, p=NS ZOF+Endo III vs. ZL). L’induzione di frammentazione del mt-DNA mediante somministrazione di mt-tat-Exo III non ha influenzato in maniera significativa il trasporto degli elettroni e l'attività dei complessi mitocondriali I-IV nei ratti magri (p=NS ZL vs. ZL+ExoIII).
IMMUNOSTAINING DI AREE DI IPOPERFUSIONE MIOCARDICA DURANTE STRESS CARDIACO CON NOREPINEFRINA
In Figura 12 sono riportati immagini ottenute con un microscopio a fluorescenza di
sezioni di tessuto cardiaco, dopo staining tissutale con il marcatore di ipossia
(pimonidazole, Hypoxyprobe), ottenute in tutti e 4 i gruppi di trattamento durante stress
con Norepinefrina (NE 10 µg/Kg/min per 20 minuti). Come si può vedere nel pannello in
alto a sinistra, sezione di cuore di ZL, non si osserva un chiaro segnale ipossico. Il
trattamento con mt-tat-Exo III (pannello B) e l’induzione di frammentazione
mitocondriale e' sufficiente nel generare aree ipossiche durante stress cardiaco. I ratti
obesi (pannello C), manifestano numerose regioni ipossiche, localizzate prevalentemente
in regioni subsarcolemmali, mentre la somministrazione della proteina ricombinante
mt-tat-Endo III attenua il segnale di fluorescenza nelle sezioni di cuore di ratti ZOF
Figura 12: Sezioni rappresentative di regioni miocardiche marcate con hypoxyprobe, dopo stress cardiaco
con NE ad alte dosi, nei 4 gruppi di trattamento. Si osservi la presenza di aree di ipoperfusione (evidenziate con le frecce bianche) nei gruppi ZL+Exo III e ZOF (pannelli B e C). Il trattamento della frammentazione mitocondriale previene in parte ed attenua lo sviluppo di regioni ipossiche nel gruppo ZOF+Endo III (pannello D). I ratti ZL (pannello A) non presentano un chiaro segnale ipossico, come evidenziato dall’assenza di segnale fluorescente.
Sezione II: studi in vitro
RISPOSTA ARTERIOLARE AL CONDITIONED BUFFER DI MIOCITI CARDIACI ISOLATI
In Figura 13 e’ riportato il grafico relativo alla risposta ottenuta dall’aggiunta di aliquote
di conditioned buffer (200 e 500 µl) rilasciato da miociti cardiaci stimolati a 400 bpm,
isolati da ZL (ZL/CB) e da ratti ZOF (ZOF/CB), quando aggiunto al bath di arteriole
coronariche isolate da cuori di entrambi gli strains (ZL/Art e ZOF/Art). Il ZL/CB ha
indotto vasodilatazione massima di entità pari a circa il 42±6% se aggiunto ad arteriole
isolate da cuori di ZL e del 39±5% se sono state utilizzate arteriole di ZOF. La vasodilatazione indotta e’ risultata significativamente compromessa in risposta al CB prodotto da ZOF quando sono state utilizzate le arteriole isolate da ZOF (vasodilatazione
massima raggiunta compresa tra 11±2%, p<0.05 ZOF/CB→ZOF/Art vs. 42±6%
ZL/CB→ZL/Art; p<0.05 28±3% ZOF/CB→ZL/Art vs. 39±5% ZL/CB→ZOF/Art), e
significativamente depressa quando il ZOF/CB e’ stato aggiunto al bath di ZL/Art,
ottenendo vasodilatazione massima indotta pari a circa 28±3% (28±3%
ZOF/CB→ZL/Art vs. 11±2% ZOF/CB→ZOF/Art, p<0.05; 28±3% ZOF/CB→ZL/Art
vs. 42±6% ZL/CB→ZL/Art p<0.05; 28±3% ZOF/CB→ZL/Art vs. 39±5%
Figura 13: grafico relativo alla risposta vasodilatatoria indotto da aliquote di conditioned buffer rilasciato
da cardiomiociti stimolati a 400 bmp, isolati da cuori di ratti ZL e ZOF, quando aggiunto al bath di arteriole coronariche di entrambi gli strains. Il conditioned buffer di ZOF e’ risultato molto meno efficace nell’indurre vasodilatazione quando aggiunto ad arteriole ZL o ZOF. Il conditioned buffer di ZL ha indotto vasodilatazione massima in arteriole ZL e di entità minore in arteriole ZOF.