Chimica Nucleare
X
A Z
numero di massa
numero atomico Simbolo dell’elemento
Numero atomico (Z) = numero di protoni nel nucleo
Numero di massa (A) = numero di protoni + numero of neutroni
= numero atomico (Z) + numero di neutroni
A Z 1p 1 or 11 H protone 1n 0 neutrone 0e -1 or -1 0β elettrone 0e +1 or +1 0β positrone 4He 2 or 42 α particella α 1 1 1 0 0 -1 0 +1 4 2
Bilanciare le equazioni nucleari
1. Conserva il numero di massa (A).
La somma di protoni più neutroni nei prodotti deve uguagliare la somma di protoni più neutroni nei reagenti.
1n 0 U 235 92 + 138 55 Cs + 96 37 Rb + 2 10 n 235 + 1 = 138 + 96 + 2x1
2. Conserva il numero atomico (Z) o carica nucleare.
La somma delle cariche nucleari nei prodotti deve uguagliare la somma delle cariche nucleari nei reagenti.
1n 0 U 235 92 + 138 55 Cs + 96 37 Rb + 2 10 n 92 + 0 = 55 + 37 + 2x0
212Po decade attraverso emissione α. Scrivi
l’equazione nucleare bilanciata del decadimento di
212Po. 4He 2 or 42 α particella α - 212Po 4He + AX 84 2 Z 212 = 4 + A A = 208 84 = 2 + Z Z = 82 212Po 4He + 208Pb 84 2 82
Stabilità nucleare e decadimento radioattivo
Decadimento Beta 14C 14N + 0β + ν 6 7 -1 40K 40Ca + 0β + ν 19 20 -1 1n 1p + 0β + ν 0 1 -1 Diminuzione # neutroni di 1 Aumento # protoni di 1 Perdita di un positrone 11C 11B + 0β + ν 6 5 +1 38K 38Ar + 0β + ν 19 18 +1 1p 1n + 0β + ν 1 0 +1 ν e ν hanno A = 0 e Z = 0 Diminuzione # neutroni di 1 Aumento # protoni di 1Cattura elettronica 37Ar + 0e 37Cl + ν 18 -1 17 55Fe + 0e 55Mn + ν 26 -1 25 1p + 0e 1n + ν 1 -1 0 Decadimento α 212Po 4He + 208Pb 84 2 82 Fissione spontanea 252Cf 2125In + 21n 98 49 0
Stabilità nucleare e decadimento radioattivo
Diminuzione # protoni di 1 Aumento # neutroni di 1
Diminuzione # protoni di 2 Diminuzione # neutroni di 2
n/p troppo alto
decadimento beta
X
n/p troppo basso
emissione di positrone o cattura elettronica
Stabilità nucleare
• Alcuni numeri of neutroni e protoni sono extra stabili • n or p = 2, 8, 20, 50, 82 e 126
• come sono stabili i numero di elettroni associati ai gas nobili (e- = 2, 10, 18, 36, 54 e 86)
• I nuclei con un numero pari di protoni e neutroni sono generalmente più stabili rispetto a quelli con un numero dispari di protoni o neutroni.
• Tutti gli isotopi degli elementi con numero atomico maggiore di 83 sono radioattivi.
L’energia di legame nucleare (BE) l’energia richiesta per
scindere un nucleo nei suoi componenti, cioè neutroni e protoni. BE + 19F 91p + 101n
9 1 0
BE = 9 x (massa p) + 10 x (massa n) – massa19F
E = mc2
BE (uma) = 9 x 1.007825 + 10 x 1.008665 – 18.9984 BE = 0.1587 uma 1 uma = 1.49 x 10-10 J
BE = 2.37 x 10-11J
energia di legame
nucleare per nucleone = energia di legame numero di nucleoni
= 2.37 x 10-11 J
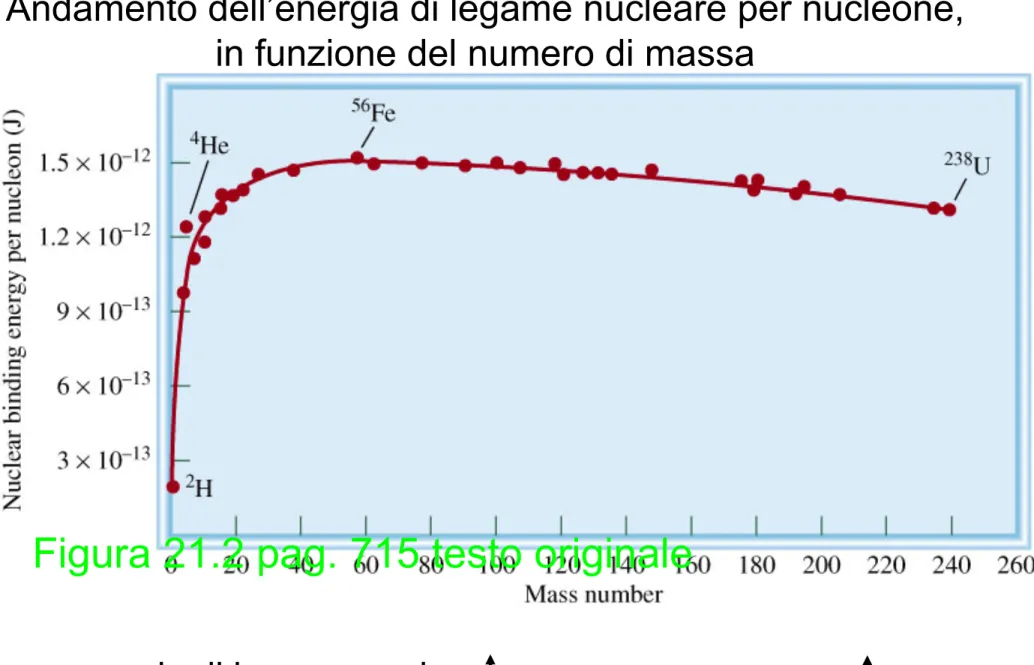
Andamento dell’energia di legame nucleare per nucleone, in funzione del numero di massa
stabilità nucleare energia di legame nucleare
nucleoni
Cinetica del decadimento radioattivo N figlio velocità = - ΔN Δt velocità = λN ΔN Δt = λN - N = N0exp(-λt) lnN = lnN0 - λt N = numero di atomi presenti al tempo t N0 = numero di atomi presenti al tempo t = 0
λ = la costante cinetica di decadimento
ln2 =
t½
Cinetica del decadimento radioattivo
[N] = [N]0exp(-λt) ln[N] = ln[N]0 - λt
[N]
Datazione con il radiocarbonio
14N + 1n 14C + 1H
7 0 6 1
14C 14N + 0β + ν
6 7 -1 t½ = 5730 anni
Datazione utilizzando l’isotopo uranio-238
238U 206Pb + 8 4α + 6 0β