CAPITOLO 4
DIFFUSIONE, SOLUBILITA’, FENOMENI
DI INTRAPPOLAMENTO E PERMEABILITA’
4. 1GeneralitàIn questo capitolo è trattata l’analisi teorica di quei fenomeni i cui parametri fondamentali, per ciò che concerne l’acciaio F82H , sono l’oggetto della tesi svolta, ovvero diffusione solida, cioè all’interno di strutture di natura solida , solubilità e fenomeni di intrappolamento dell’idrogeno. Questi parametri regolano completamente il movimento d’idrogeno all’interno della struttura cristallina dell’acciaio, e la permanenza di esso all’interno del metallo in trappole, o in siti previsti dalla regolare disposizione degli atomi nei piani cristallini della struttura ospitante.
Da una loro analisi è possibile studiare fenomeni di infragilimento o rotture avvenenti nei manufatti in acciaio.
4. 2Diffusione solida
La diffusione può essere definita come il meccanismo con cui la materia si muove attraverso la materia, ovvero quantifica la mobilità di atomi, di qualsiasi natura, ospiti o appartenenti alla struttura ospitante, all’interno di una matrice cristallina. Essa è funzione della temperatura, della natura del reticolo cristallino, che accoglie le specie, e del carattere delle specie stesse, generalmente gassose, ospiti.
Dalla temperatura, ovviamente, dipende il contenuto energetico della specie ospite che, quindi, al crescere della temperatura vede aumentare la sua disponibilità energetica per il movimento all’interno del materiale. All’aumentare della temperatura, inoltre, cresce anche la mobilità degli atomi del metallo ospitante e, quindi, il numero di vacanze, ovvero di posizioni reticolari non occupate. Da analisi sperimentali è emersa la seguente dipendenza, di tipo Ahrrenius, della diffusione dal fattore termico:
) ( 0 RT Q
e
D
D
=
⋅
− (4. 1)con D0, coefficiente preesponenziale(in m2/sec), Q, energie di attivazione per le specie che diffondono(in J/mole), fattori dipendenti fondamentalmente dall’affinità della specie diffondente con la struttura ospitante. R è la costante universale dei gas(in J/(mole*K))
La natura della struttura ospitante si concretizza, soprattutto, nel tipo di reticolo cristallino, da cui dipende il fattore di compattazione della matrice metallica, e dagli spazi interatomici concessi alle specie ospiti. Altri fattori condizionati sono il numero e tipologie di siti interstiziali, ovvero cavità presenti naturalmente nelle strutture metalliche, e il numero e tipologie di trappole.
Il carattere della specie, invece, riguarda la dimensione della stessa e la possibilità per essa di incunearsi tra gli atomi del reticolo metallico.
Esistono due tipi principali di meccanismi di diffusione solida: ● Meccanismo di diffusione per vacanza o sostituzionale ● Meccanismo di diffusione interstiziale
4. 2. 1 Meccanismo di diffusione per vacanza o sostituzionale
Gli atomi possono muoversi nel reticolo cristallino da un sito atomico all’altro se le vibrazioni termiche consentono di superare l’energia di attivazione, Q, e se ci sono vacanze altri difetti cristallini nella matrice, trappole. Le vacanze nei metalli e nelle leghe sono difetti di equilibrio e, pertanto, ne sono presenti in gran quantità, consentendo, così, che avvenga la diffusione sostituzionale degli atomi. All’aumentare della temperatura, poi, cresce il numero delle vacanze ed è disponibile molta energia termica, come abbiamo detto, decretando velocità di diffusione più alte, soprattutto a elevate temperature. La velocità di diffusione è condizionata, inoltre, dalle differenze di dimensioni atomiche e dalle differenze di energie di legame delle varie matrici metalliche ospitanti.
Il legame tra atomi è anche legato al punto di fusione del metallo, in particolare cresce con esso; questa correlazione è legata al fatto che tanto maggiore è questo valore di temperatura, altrettanto più grosse sono le energie di legame che tengono cucito il reticolo cristallino.
4. 2. 2 Meccanismo di diffusione interstiziale
La diffusione interstiziale avviene quando gli atomi si muovono da un sito interstiziale ad un altro, senza spostare permanentemente nessuno degli atomi del reticolo cristallino della matrice. Affinché il meccanismo sia efficace, la dimensione delle specie diffondenti deve essere relativamente più piccola rispetto a quella degli atomi della struttura ospitante. Atomi piccoli come ossigeno,
idrogeno, azoto e carbonio possono diffondere in tale maniera all’interno del ferro-α, caratterizzato
da una struttura cubica a corpo centrato(CCC), e del ferro-γ, organizzato in una struttura cubica a facce centrate(CFC).
4. 2. 3 Leggi di Fick a)Prima Legge di Fick
Le relazioni di Fick regolano il flusso diffusivo di una specie attraverso una superficie ed in mezzi isotropi e non, in funzione del gradiente di concentrazione della specie stessa, del tempo e dello spazio. la relazione valida nel caso in cui la struttura, che accoglie il flusso sia isotropa, è[18]:
)
(C
div
D
J
=
−
⋅
(4. 4) PRIMA LEGGE DI FICK Che si specializza nella forma:X
C
D
J
∂
∂
⋅
−
=
(4. 5)Nel caso in cui è studiata la diffusione lungo una specifica direzione, come nel caso di lastre piane e sottili. J è il flusso per unità di superficie, D è il coefficiente di diffusione, C la concentrazione della sostanza che diffonde, e X è la coordinata spaziale monodimensionale. In alcuni casi il coefficiente di diffusione è indipendente dalla concentrazione della specie diffondente, in altri casi, invece, esso dipende significativamente dalla concentrazione, come nel caso di diffusione in alti polimeri. Si ricorda, invece, sempre a proposito di D, la stretta dipendenza esponenziale dalla temperatura e dall’energia di legame, come precisato sopra.
Il segno negativo della relazione trova giustificazione nel fatto che il flusso è in direzione opposta rispetto alla crescita del valore di concentrazione all’interno del mezzo di diffusione.
E’ bene rimarcare il fatto che la relazione, appena esposta, è valida, in generale, solo in mezzi isotropi, dove i valori di diffusione e le proprietà strutturali del mezzo di diffusione sono uguali in ogni direzione. In altri casi il coefficiente di diffusione può assumere valori diversi a seconda della direzione lungo la quale esso è misurato.
Si vuole, ora, ricavare l’espressione della prima legge di Fick valida nel caso in cui la geometria del mezzo, in cui avviene la diffusione, sia cilindrica. Occorre, allora, passare ad un sistema di coordinate cilindriche, r, θ, z. Applicando la(4. 4) otteniamo:
)
(
Z
C
C
r
C
D
J
∂
∂
+
∂
∂
+
∂
∂
⋅
−
=
θ
(4. 6)Considerando un cilindro di lunghezza notevolmente superiore alle dimensioni della sezione, e per effetto della simmetria del flusso rispetto alla coordinata θ(sempre nel caso di mezzo isotropo), si ottiene l’utile semplificazione:
r
C
D
J
∂
∂
⋅
−
=
(4. 7)Che tornerà molto utile nella risoluzione del sistema di equazioni differenziali nello studio del desorbimento termico.
b)Seconda legge di Fick
La prima legge di Fick non e' sufficiente per risolvere completamente tutti i problemi di diffusione. Infatti basta notare che il flusso diffusionale puo' modificare il gradiente di concentrazione che spesso e', conseguentemente, funzione del tempo. Dalla combinazione della relazione di sopra e dell’equazione di continuità:
divJ
t
C =
∂
∂
(4. 8)si ottiene la legge cercata:
)
(
2 2 2 2 2 2Z
C
Y
C
X
C
D
t
C
∂
∂
+
∂
∂
+
∂
∂
⋅
=
∂
∂
(4. 9)SECONDA LEGGE DI FICK
che, nel caso di diffusione lungo una direzione specifica, come prima, si specializza nella:
2 2
X
C
D
t
C
∂
∂
⋅
=
∂
∂
(4. 10)4. 3Solubilità
La solubilità quantifica la presenza di una specie all’interno di una struttura cristallina che la ospita. Tale valore è in relazione con l’organizzazione reticolare della specie ospitante, ed, ovviamente, con la natura della sostanza ospite.
Si prenda come riferimento la presenza di idorgeno all’interno di un reticolo cristallino di acciai. Gli atomi della struttura reticolare dell’acciaio possono essere organizzate essenzialmente in 4 forme allotropiche, a seconda del campo di temperature in cui viene a trovarsi la lega[19]:
● Ferro-α, fino alla temperatura di 768°C e con struttura CCC, detta anche Ferrite
● Ferro-β, dalla temperatura di 758°C fino a 906°C e con struttura CCC, anch’essa nota come Ferrite
● Ferro-γ, dalla temperatura di 912°C alla temperatura di 1401°C con struttura CFC, conosciuta anche come Austenite
● Ferro-δ, dalla temperatura di 1401°C fino ai 1530°C e con struttura CCC
L’idrogeno tende a soggiornare in siti reticolari, non occupati dagli atomi costituenti il reticolo ospitante, determinati dalla disposizione reciproca di quest’ultimi. Tali siti, detti anche siti interstiziali, sono di due tipi, per ciò che concerne le due strutture allotropiche del ferro: ● Siti ottaedrici
● Siti tetraedrici
La ubicazioni di queste allocazioni sono differenti a seconda delle strutture CCC o CFC:
Figura 4. 2Siti ottaedrici e tetraedrici in CFC
La struttura CFC prevede un maggiore impacchettamento, ovvero un miglior tasso di occupazione volume, pari al 74% dello spazio a disposizione, della struttura CCC che, invece, si limita al 68%. Ciò nonostante, i valori di solubilità per l’idrogeno sono decisamente superiori per la più”occupata” struttura CFC austenitica, il 4,17ppm contro l’2,62 ppm della ferrite, valore raggiunto ai 900°C[32]. I massimi valori per la solubilità, poi, sono raggiunti allorché l’acciaio passo allo stato liquido, ovvero ai 1540°C, con tenori di idrogeno raggiunti pari allo 0, 13%. Questo fenomeno, tra l’altro, ci induce a porre molta attenzione all’atto del raffreddamento di un manufatto di acciaio, da condurre lentamente per favorire il più possibile la fuoriuscita di idrogeno, che, altrimenti, può essere causa di rotture più o meno, severe, da blistering o fish eye, a drastiche fratture[20].
4. 4Fenomeni di intrappolamento
Le trappole sono siti di allocazione preferenziale per le specie diffondenti, in particolar modo per l’idrogeno. Esse, non previste dal regolare ordinamento cristallino, sono spesso ubicate in corrispondenza di imperfezioni strutturali, come difetti, dislocazioni, inclusioni, bordi di grano, dislocazioni, segregazioni, microvuoti e interfacce cementite-struttura reticolare.
I siti di intrappolamento esercitano azione attrattiva sugli atomi delle sostanze che diffondono nella struttura; questo perchè un atomo d’idrogeno, che vi si trova ubicato, è ad un livello di energia potenziale decisamente più basso rispetto a quello di un ordinario sito interstiziale; altrettanta energia sarà, poi, necessaria alla liberazione delle specie intrappolate.
Si definiscono, ora, alcuni parametri utili alla comprensione dell’intrappolamento:
● El, barriera di energia potenziale necessaria ad una specie per passare da un sito interstiziale ad un altro
● E’, supplemento di energia ad EL necessaria ad una specie per entrare in un sito di intrappolamento.
● La somma di E’+EL è pari a Et, ovvero all’energia complessiva necessaria all’ingresso in una trappola
● Ed, contenuto energetico minimo alla liberazione di una specie da una trappola ● La differenza tra Ed e Et, ovvero ∆E, costituisce l’energia di legame di una trappola
figura4. 3Parametri legati all’intrappolamento
L’energia di legame è un parametro molto identificativo per una trappola. A seconda, infatti, dei valori di ∆E trovati dalle analisi di un campione è possibile stabilire il carattere della trappola, ovvero profonda o reversibile, e la natura, cioè se essa è costituita da un vuoto, inclusioni, segregazioni e così via. Si ricorda, poi, che maggiore è l’energia di legame, maggiore è la popolazione di atomi di idrogeno in una trappola[24].
● Se
∆E>-30 kJ/mole e β<<1→→TRAPPOLA REVERSIBILE
● Se ∆E<-50 kJ/mole e β>>1→→TRAPPOLA PROFONDA(o
irreversibile)[20]
β=C
HּK/N
CH è la concentrazione di idrogeno che diffonde all’interno del reticolo, K è una costante legata all’intrappolamento, N è il numero di siti interstiziali
Questa è una classificazione adottata da alcuni studiosi[24], più in generale si può dire che i concetti di reversibilità e irreversibilità di una trappola sono strettamente legati alla maggiore o minore probabilità di rilascio di idrogeno, allorquando esso si trovi all’interno di uno di tali siti.
Un’altra annotazione da aggiungere riguarda il valore di E’ che, data la sua difficile valutazione, viene spesso posto uguale a zero, senza conseguenze sui risultati ricavati, eventualmente, da prove sperimentali.
E’ riportata, ora, la natura delle varie trappole a seconda dei valori di energia di legame, secondo quanto riportato in[21, 23]:
NATURA DELLE TRAPPOLE
∆E=-29 kJ/mole
MICROVUOTI
∆E=-8. 8, -9. 6 kJ/mole
BORDI DI GRANO
∆E=-26. 5 kJ/mole
DISLOCAZIONI
∆E=-9. 7 kJ/mole
INTERFACCE Fe-FeO
xE
t=72, 2 kJ/mole
INTERFACCE Fe-MnS
∆E=-28. 1 kJ/mole
INTERFACCE Fe-TiC
Alle alte temperature, tipicamente sopra i 300°C, tutte le trappole possono essere considerate reversibili, dato che il contenuto termico delle specie popolanti codeste allocazioni, comincia a consentirne una certa mobilità, diversamente da quanto accade al di sotto di tali campi di temperature. Da qui discende l’enorme importanza di condurre lenti raffreddamenti per pezzi che sono stati riscaldati ad alte temperature in ambienti contenenti idrogeno, per favorirne un più efficace e ingente smaltimento.
I materiali a fusione nucleare, infatti, sono a rischio da infragilimento e rotture da idrogeno all’atto dello spegnimento, ovvero proprio quando subiscono forti raffreddamenti.
La diffusione è fortemente condizionata dalla presenza di trappole, in quanto esse influenzano negativamente sulla mobilità delle specie gassose attraverso un’azione di natura attrattiva nei loro confronti, come dicevamo anche prima.
Il fenomeno dell’intrappolamento incide anche sui fenomeni di infragilimento e rottura da idrogeno con effetti contrastanti:
L’idrogeno intrappolato è ovviamente strappato a quello che diffonde, in una struttura, responsabile dell’infragilimento, rigonfiamenti, occhi di pesce; l’effetto, però, può ritenersi positivo sull’acciaio se la trappola di destinazione è di tipo benefico, ovvero quando la deposizione di idrogeno non genera conseguenze sulla struttura. In altri casi l’idrogeno, che si raccoglie all’interno della trappola, si combina con altre specie (ad esempio il C)o con altro idrogeno, generando, quindi, specie più ingombranti che esercitano forti pressioni generando l’insorgere di cricche, o addirittura, in alcuni casi, rotture improvvise, determinate anche dal calore di reazione sviluppato dalle reazioni con il carbonio o dalla ricombinazione degli idrogeni. Le dislocazioni giocano un ruolo fondamentale in questa situazione, esse, infatti possono drenare l’idrogeno, durante il loro moto da trappole reversibili verso tipologie di trappole dannose[25].
Una seconda caratterizzazione per le trappole è quella che le distingue in fisiche e attrattive.
Le prime sono costituite semplicemente da discontinuità della matrice metallica, le altre invece interagiscono con l’idrogeno con forze di varia natura, ad esempio di natura elettronica, meccanica, termica o con un gradiente di potenziale chimico. Il flusso diffusivo, infatti, è proporzionale al gradiente di potenziale chimico, come si evince dalla legge di Fick, ed allo stesso modo dipendente dalla temperatura, secondo il coefficiente di diffusione. Le sollecitazioni meccaniche, invece, finiscono per condizionare i gradienti di potenziali chimici, causando, a volte anche indipendentemente da quest’ultimi, flussi di idrogeno. La distinzione principale tra le due classi, con riferimento alla figura sottoriportata, è che nella prima l’atomo A è ugualmente attratto sia da siti ordinari C che d’intrappolamentoB, mentre invece nella seconda così non accade, e l’idrogeno tende a migrare verso la posizione B di trappola, per poi continuare il suo moto fino al sito caratterizzato dalla più bassa energia potenziale.
figura 4. 4trappole fisiche, attrattive e miste
Le imperfezioni strutturali, ad esempio singolarità del cristallo o precipitati, artefici delle trappole fisiche, generano campi di forze a componenti idrostatiche di trazione o compressione, che determinano variazione del potenziale chimico, e, quindi, flussi di natura diffusiva di natura attrattiva o repulsiva, ovvero le trappole possono richiamare o respingere specie diffusive[17]. Quest’ultima considerazione è eloquente del fatto che spesso è difficile categorizzare i siti di intrappolamento, e che, spesso, essi possono definirsi di natura mista tra le due sopra dette, la cui rappresentazione è posta in basso nella figura 4. 4.
4. 5Permeabilità
Un altro fattore importante ai fini dello studio dell’acciaio F82H , per usi futuri come materiale strutturale in reattori a fusione nucleare , è la permeabilità, ovvero la quantità di idrogeno che riesce ad entrare nella struttura metallica dell’acciaio, alla base di successivi fenomeni di infragilimento e rotture da idrogeno. E’l’idrogeno permeato durante lo svolgimento delle reazioni nucleari la causa di possibili rotture o degradazioni delle strutture in acciaio a bassa attivazione all’atto dello spegnimento, come segnalavamo anche precedentemente.
L’idrogeno presente normalmente sottoforma di idrogeno molecolare H2, nell’ambiente esterno, deve subire una scissione in 2 atomi di idrogeno monoatomico prima di fare il suo ingresso nel metallo:
H2(gas)=2H(disciolto) (4. 2)
la quantità di specie che, poi, effettivamente entra è regolata dalla legge di Sieverts:
CH=Ksּ(PH2)1/2(4. 3)
Che evidenzia una dipendenza lineare tra concentrazione di idrogeno monoatomico permeato e radice quadrata della pressione di idrogeno molecolare a contatto con la superficie del metallo esposto[17]. La costante Ks è legata a fenomeni di impedenza che si possono verificare sulla superficie del metallo destinatario della corrente di idrogeno; la formazione di ossidi superficiali è il più classico tra tali fenomeni. Nelle prove designate alla misura di questo parametro, infatti, si provvede ad un rivestimento superficiale dell’acciaio di prova con Palladio, proprio per evitare l’insorgere di ossidi.
4. 6Modelli per lo studio della diffusione e intrappolamento dell’idrogeno
Sono analizzate, ora, tutte quelle teorie sulla diffusione e intrappolamento, necessarie allo studio, e alla valutazione, dei parametri oggetto della tesi.
MODELLO DI ORIANI[22]
La teoria di Oriani prevede due soli possibili siti di allocazioni per l’idrogeno all’interno di una struttura cristallina di un metallo, ovvero i siti interstiziali, quelli regolari previsti dalla regolare disposizione degli atomi del metallo nei piani reticolari, e i siti di intrappolamento. Secondo lo studioso americano c’è equilibrio tra l’idrogeno che abbandona e fa il suo ingresso nelle trappole. La teoria si basa, inoltre, sull’ipotesi della bassa occupazione di trappole da parte dell’idrogeno. Lo studioso americano, inoltre, afferma che le allocazioni di intrappolamento principali sono costituite da interfacce(tra 2 fasi diverse, tra fasi e precipitati)e microvuoti. [23]
Le considerazioni di Oriani sono sicuramente accettabili in condizioni di alte temperature, ovvero al di sopra dei 300°C, quando, come abbiamo detto, le specie gassose dispongono di una certa libertà di movimento, ed infatti saranno alla base della valutazione sperimentale e teorica di alcune grandezze studiate nella presente tesi; successivamente, infatti, da tali ipotesi e con le correlazioni di Fick sarò in grado di sviluppare un modello matematico per lo studio della diffusione e dell’intrappolamento, durante lo svolgimento delle prove sperimentali del mio lavoro
La teoria va in difficoltà alle basse temperature dove la presenza di trappole irreversibili non si concilia molto bene con l’equilibrio locale, dato che tali siti attraggono, ma non rilasciano idrogeno.
MODELLO DI LEE AND LEE[24]
Il modello sviluppato dalla coppia di omonimi è sicuramente tra i più semplici, e per questo uno dei più utilizzati per determinare i parametri fondamentali del fenomeno di intrappolamento. l’approccio al problema può dirsi semiempirico, in quanto la valutazioni delle grandezze d’interesse è condotta per via teorica, ma supportata da analisi sperimentali.
In particolare lo studio è incentrato sulla determinazione della Ed, ovvero l’energia di detrappolamento.
Definiamo la quantità di idrogeno, che fugge dalle trappole, come: ) (
)
1
(
RT Ede
X
A
dt
dX
−⋅
−
⋅
=
(4. 4)dove X=1-(N/N0), con N e N0, rispettivamente il numero di trappole occupate ad un istante t generico e numero di trappole occupate all’inizio; A è , invece, semplicemente una costante. Il termine 1-X, invece, diventa misura della quantità di idrogeno intrappolato in uno specifico tipo di trappola.
La parte sperimentale dell’approccio consiste nella valutazione delle temperature di picco, Tp, di rilascio di flussi di idrogeno, da parte di un provino preventivamente caricato di idrogeno, in esperienze condotte, ad esempio in uno spettrometro di massa, a varie velocità di riscaldamento, Φ. Riportando su di un grafico i valori di ln(Φ/Tp2) e i valori di 1/Tp, ricaviamo una retta la cui pendenza è pari al valore - Ed/R da cui prontamente si ricava il valore oggetto del nostro interesse. All’aumentare di Φ, cresce la quantità di idrogeno rilasciato e la temperatura di picco.
L’incremento del flusso riflette la crescita del parametro diffusione alle alte temperature, mentre a basse Φ, il flusso diventa più omogeneo su tutto il campo di temperature attraversato, ovvero il desorbimento avviene più gradualmente, e, quindi, meno intensamente al momento del picco. L’incremento della temperatura di picco al crescere della velocità di riscaldamento è da ascriversi ai tempi di diffusione e di liberazione delle specie gassose intrappolate.
L’approccio è tanto semplice quanto attraente ed utilizzato, sfortunatamente viene trascurato il fenomeno diffusivo, per ciò che concerne, in particolare, la possibilità di spostamento di idrogeno da una trappola ad un’altra, ovvero si trascura il fenomeno del ritrappolamento.
Le rette utilizzate per la valutazione delle energie di attivazione sono riportate nel prosieguo del capitolo(pag. 14)
MODELLO DI Mc-NABB AND FOSTER[21]
Il tipo di approccio, previsto da questa teoria, considera la diffusione condizionata sia dall’intrappolamento che dalla liberazione dai siti di intrappolamento, il modello precedente non considerava questo primo fattore. I due fattori, inoltre, possono considerarsi indipendenti tra di loro, senza, ad esempio, la relazione di equilibrio che li lega nello studio di Oriani.
Lo studio converge sulla stesura di una relazione che correla la quantità di idrogeno catturata dalle trappole, n, la concentrazione di idrogeno che diffonde nel reticolo cristallino, Cl, e le frequenze di uscita e di ingresso nelle trappole, p e k, nel seguente modo:
dt
dn
=kּC
lּ(1-n)-pּn
(4. 5) ) ( 0 0 RT E lC
e
C
=
⋅
− conE
0,
pari al calore di soluzione (4. 6) ) ( 0 RT Ese
k
=
ν
⋅
− (4. 7) ) ( RT E l de
p
=
ν
⋅
− (4. 8)con ν0 e νl, rispettivamente frequenze degli atomi di idrogeno in siti interstiziali e trappole.
L’utilizzo di questa relazione, assieme alle ipotesi di Oriani, che ne semplificano la forma, ci permetterà di ricavare il sistema di equazioni differenziali per l’analisi teorico-pratica del desorbimento termico(vedi Capitoli successivi).
MODELLI CON LA DIFFUSIONE[24]
Si distinguono in 2 classi, ovvero quelli che considerano una bassa occupazione delle trappole e quelli che, invece, ne considerano una ingente occupazione.
1)MODELLI A BASSA OCCUPAZIONE DI TRAPPOLE a)MODELLO DI YOSHINARI
Esso è basato sulla seguente relazione:
∞
∂
∂
M
M
t=∑
4
2r
D
ּexp(-Sּα
n2)
(4. 9) (la sommatoria è estesa da n=1 a n=∞)Dove Mt e M∞ sono rispettivamente la quantità di idrogeno liberata dal provino al tempo t ed il contenuto di idrogeno iniziale nel provino, cilindrico di raggio a, D è il coefficiente di diffusione effettivo, αn sono, invece, le radici positive della funzione di Bessel:S, poi, è definito come segue:
∫
⋅
=
tD
dt
S
0
(4. 10)
La concentrazione dell’idrogeno è considerata uniforme all’interno del provino all’istante iniziale(t=0), mentre invece la concentrazione sulla superficie esterna dopo lunghi tempi(t=∞)è valutata nulla.
Data l’ipotesi di bassa occupazione delle trappole, il modello funziona bene con lo studio di trappole a bassa energia di legame.
b)ALTRI ESEMPI
Gli altri modelli sono delle varianti sul tema, i cui risultati, però, non sono altrettanto soddisfacenti dal punto di vista della corrispondenza con dati sperimentali. CHORKENDORF utilizza una D dipendente dalla temperatura, secondo la solita relazione di tipoAhrrenius, ed una distribuzione Gaussiana, per ciò che concerne la distribuzione della concentrazione all’interno del provino all’istante iniziale; ONO AND MESHI adottano, ugualmente, un coefficiente di diffusione effettivo e stabiliscono che la concentrazione di idrogeno all’interno del reticolo raggiunge, per lunghi tempi, un equilibrio termico con la pressione dell’ambiente che circonda il provino.
2)MODELLI AD ALTA OCCUPAZIONE DI TRAPPOLE a)MODELLO DI WILSON AND BASKES
Il modello in esame correla in maniera rigorosa diffusione e caduta nelle trappole, anche se per un solo tipo specifico di trappola.
Il caricamento del provino si fa con Deuterio, la cui distribuzione è esplicitata in una funzione G(x). I metalli per le prove sono AISI 316(acciai inossidabili austenitici).
Le equazioni del modello, ovvero di conservazione della massa sono:
)
(
2 2x
G
t
C
X
C
D
t
C
T+
∂
∂
−
∂
∂
⋅
=
∂
∂
(4. 11)
) ( 0 2 RT E T e T
e
C
C
C
D
t
C
−⋅
⋅
+
⋅
⋅
=
∂
∂
ν
λ
(4. 12)C
eT=C
0T-C
T (4. 13)Con C, pari alla concentrazione di deuterio libero, CT quello intrappolato, C0T , la concentrazione di trappole(per unità di volume), CeT, le trappole non occupate, D è la solita funzione esponenziale della temperatura, ET, pari all’energia di intrappolamento, λ, la distanza tra una trappola e l’altra, detto anche cammino libero medio.
Nonostante la scarsa aderenza con analisi sperimentali nello stretto confronto di risultati, il modello sembra, invece, seguire qualitativamente le tendenze delle prove, ovvero le funzioni hanno un andamento accostabile a quelle valutate direttamente dalle prove.
b)ALTRI ESEMPI
Altri modelli sviluppati non portano neanche ad una corrispondenza qualitativa tra realtà sperimentale e analisi teorica; come nel caso di ABRAMOV, che parte dagli studi di Mc-NABB AND FOSTER e ORIANI, per quanto riguarda siti interstiziali e trappole, e risolve le equazioni di Fick per valutare il profilo iniziale dell’idrogeno impiantato nel provino.
LINO, invece, sviluppa un modello che includerebbe due diversi tipi di trappole ad alta occupazione, il problema è, però, che dall’analisi delle equazioni ricavate da questi studi emerge l’ipotesi di bassa occupazione di trappole, contravvenendo alle ipotesi iniziali di ingente presenza di idrogeno ai siti di intrappolamento.
4. 6. 1Relazione tra picchi e variabili di processo[24]
L’intensità e la posizione del picco sull’asse delle temperature sono controllate dalle condizioni operative utilizzate durante la conduzione delle prove di desorbimento termico, effetuate in uno spettrometro di massa, i cui dettagli processuali sono esplicitati più dettagliatamente nel seguito della tesi.
a)Dipendenza dalla concentrazione iniziale di idrogeno
La concentrazione iniziale d’idrogeno è, ovviamente, quella legata al caricamento del provino, che si effettua prima dell’analisi allo spettrometro. L’incremento di tale parametro porta ad un abbassamento della temperatura di picco e ad un incremento del flusso d’idrogeno liberato. Tuttavia la prima variazione è relativa se rapportata ad altre variabili, anche non dipendenti dalle condizioni operative, come ad esempio il numero di trappole del materiale.
Se l’incremento del flusso è semplicemente spiegato da una maggiore occupazione delle trappole, dato che aumenta la quantità di idrogeno che popola la struttura del metallo, non altrettanto chiaro è il motivo dell’abbassamento della temperatura di picco; essa potrebbe essere dovuta ad una minore probabilità di rioccupazione delle trappole, fenomeno chiaramente osteggiato da un aumento dell’occupazione stessa dei siti di intrappolamento, così, quindi, da aumentare il valore di diffusione all’interno del reticolo metallico.
Le prove sono condotte a 10 K/min e con un provino di raggio cilindrico pari a 8mm(anche per quanto riguarda i grafici successivi, laddove non è specificato diversamente).
I grafici sono ottenuti dall’applicazione del modello matematico per l’analisi del desorbimento termico, la cui esplicitazione è rimandata ai capitoli successivi.
Figura 4. 5Dipendenza dalla concentrazione di caricamento
b)Dipendenza dalla velocità di riscaldamento
La velocità di riscaldamento, detta anche rampa di temperatura, innalza flusso e temperatura di picco.
Il primo effetto è legato ai tempi minimi necessari alla diffusione ed alla fuoriuscita di idrogeno dalle trappole, che non possono essere ristretti oltremodo dagli effetti legati alle temperature.
Il secondo effetto è un’ulteriore riprova dell’alto valore del coefficiente di diffusione alle alte temperature, come abbiamo anche accennato poc’anzi.
A tal proposito è bene osservare che è meglio operare a velocità di riscaldamento non troppo eccessive, per avere picchi e temperature più contenute ed amministrabili. Nel presente lavoro non andremo oltre i 10°C/min.
Figura 4. 6Dipendenza dalla rampa di temperature
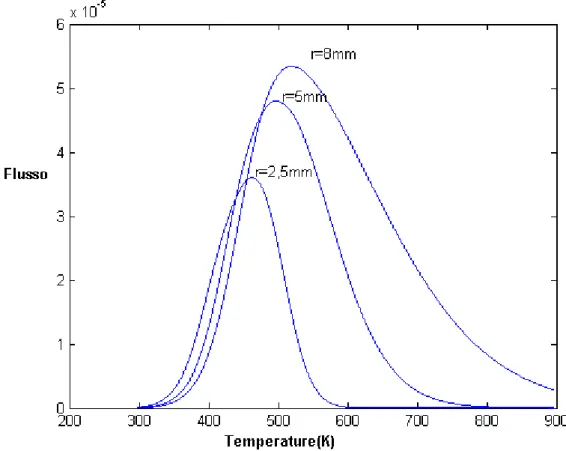
c)Dipendenza dallo spessore del provino
L’utilizzo di provini a spessori maggiori comporta temperature, picchi e ampiezza degli stessi, decisamente superiori. Ciò e di immediata comprensione:Più grande e lo spessore, maggiore è la capienza di idrogeni, nonché il tempo a loro necessario per fuggire dall’acciaio e raggiungere il sensore. E’ ovviamente analoga la dipendenza, nel caso si utilizzi un provino di geometria cilindrica, dei parametri sopra citati dal raggio del campione.
Figura 4. 7Dipendenza dal raggio dello spessore
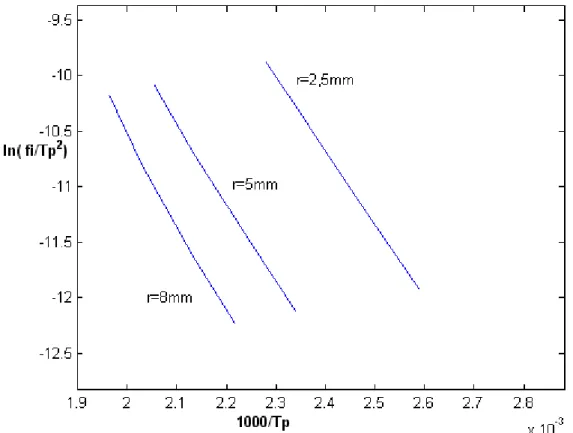
Sono riportate, inoltre, le rette che legano il logaritmo naturale del parametro Ф/Tp2 in funzione del reciproco della temperatura di picco stessa, 1/Tp, parametrizzate rispetto al raggio del provino cilindrico:
Figura 4. 8Rette di dipendenza logaritmica Per l’analisi di Lee and Lee
4. 6. 2Relazione tra picchi e parametri legati all’intrappolamento
Anche i parametri indipendenti dalle condizioni di prova incidono sull’emissione e sulla temperatura del picco. Questi fattori, che ora saranno indicati, sono strettamente legati alla natura del materiale testato.
a)Effetto delle costanti legate all’intrappolamento
I fattori k e p, citati precedentemente ed espressione della frequenza di intrappolamento e detrappolamento, non sembrano incidere significativamente sulle grandezze prese in esame. Da qui discende anche la difficoltà nella loro individuazione dal “fit” con i dati sperimentali delle prove di desorbimento termico.
b)Dipendenza dalla densità di trappole
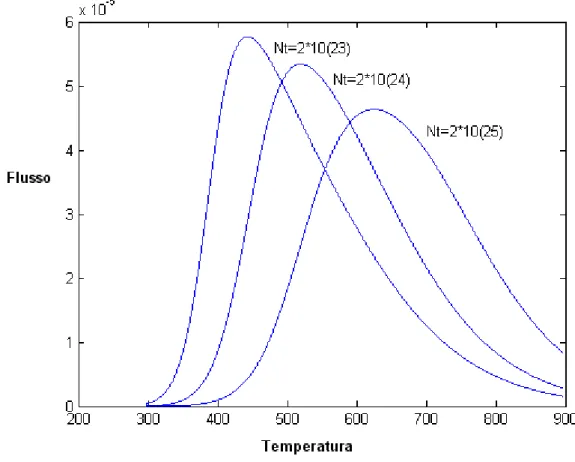
La densità di trappole incide sull’intensità, area e temperatura di picco; per valori troppo modesti di tale parametro, poi, non è rilevabile nemmeno una concreta presenza di picco. Ben diversa è la situazione con numero di trappole crescenti, in cui picchi e temperature sembrano essere molto sensibili.
Il picco diminuisce di entità, contrariamente a quanto ci si attenda, in quanto il modello contempla solo le trappole ad alte temperature, e non considera l’idrogeno diffusibile liberato durante la prima fase del desorbimento.
La temperatura di picco sono, invece, in crescita all’aumentare della densità di trappole; ciò è sintomo della maggiore difficoltà di rilascio di idrogeni quando aumentano, in concreto, le possibilità sia di intrappolamento che di ritrappolamento nei siti.
Figura 4. 9Dipendenza dal numero di trappole
c)Dipendenza dai parametri variabili di intrappolamento, Ed, Et, ∆E
I parametri vanno analizzati congiuntamente, in quanto tali entità sono vincolate tra loro.
Diminuendo l’energia di legame, ∆E, ovvero incrementando l’energia per la liberazione dalle trappole, Ed, e mantenendo fisso l’energia di intrappolamento, Et, si osserva un innalzamento del posizionamento del picco sull’asse delle temperature, ma scarse variazioni per ciò che concerne l’intensità di quest’ultimo. Il primo fenomeno trova le sue ragioni nell’incremento dell’energia termica che un individuo deve trovare per la sua liberazione, ovvero una maggiore temperatura, il secondo effetto è da ascriversi, invece, al fatto che la popolazione di idrogeno nella matrice metallica, a parità di concentrazione e numero di trappole, non ha subito variazioni derivanti da diversi valori delle energie legate all’intrappolamento.
Figura 4. 10Dipendenza dall’energia di legame
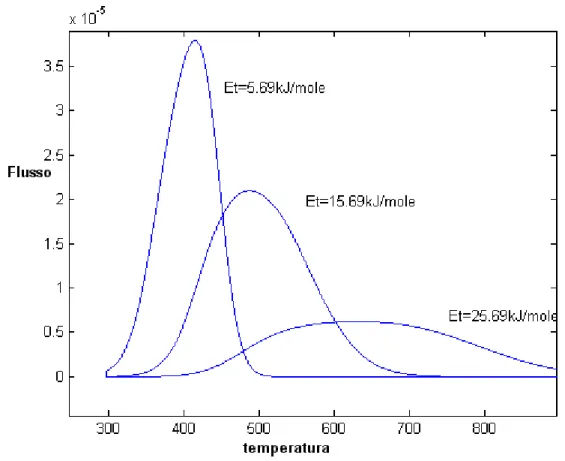
Questo è invece l’effetto derivante dalla variazione dell’energia per la caduta nelle trappole, mantenendo costante l’energia di legame, e determinando anche, perciò, la variazione l’energia di detrappolamento. Si ricorda, a tal proposito, che l’energia di intrappolamento è posta pari all’energia per la diffusione reticolare interstiziale, El.
Figura 4. 11 Dipendenza dall’energia d’intrappolamento
La temperatura di picco in crescita è condizionata dal concomitante incremento dell’energia per la liberazione dalle trappole
4. 7Infragilimento e rotture da idrogeno
Lo studio dei fenomeni di diffusione, intrappolamento e solubilità di idrogeno si propone, tra gli altri scopi, la prevenzione di rotture e danneggiamenti in acciai soggetti all’interazione con idrogeno. Il problema è particolarmente avvertito per acciai ferritici e metalli, che possono dare origine a idruri stabili. Gli infragilimenti che occorrono alle strutture ferritiche sono a controllo di diffusione[26].
Il contatto idrogeno-metallo è responsabile dei seguenti accadimenti[19]:
● Decarburazione alle alte temperature(sopra i 200°C), detto anche attacco da idrogeno
● Ricombinazione molecolare di idrogeno atomico con possibili blistering o rotture improvvise
● Frattura differita
Un altro tipo di danneggiamento causato dalla presenza di idrogeno è il fenomeno della SCC. Questo tipo di problema affligge maggiormente gli acciai inossidabili, ed il ruolo dell’idrogeno, sviluppato dalla semireazione catodica di corrosione, è quello di addensarsi all’apice della cricca,
zona densa di dislocazioni e, quindi, di forte richiamo, ed impedirne l’arrotondamento che consentirebbe, invece, la plasticizzazione del materiale.
Gli effetti, appena elencati, sono di tipo irreversibile, ma ci sono anche forme reversibili di danneggiamento. L’idrogeno, che diffonde all’interno di una struttura in forma monoatomica, provoca distorsioni del reticolo e blocca il moto di dislocazioni, condizionando, così, la possibilità, per il materiale colpito, di deformarsi plasticamente. Questo tipo di effetto svanisce non appena l’idrogeno è allontanato dal materiale, ed è per questo detto reversibile[26].
Le fonti di idrogeno, responsabili di tali fenomeni, possono essere:
● Corrosione, in particolare i semi processi catodici che accompagnano il fenomeno corrosivo ● Deposizioni elettrolitiche, cadmiature, cromature, etc. . Tali rivestimenti impediscono l’uscita di idrogeno, una volta che esso abbia fatto il suo ingresso nella struttura
● Pretrattamenti di materiali, decapaggi chimici o elettrochimici, acidi o basici
● Saldatura, la potenza termica necessaria, infatti, potrebbe decomporre l’acqua in idrogeno e ossigeno.
Allo stato fuso, inoltre, l’acciaio è maggiormente aggredibile, in quanto in tali condizioni esso è dotato di una maggiore solubilità verso H, come detto anche in precedenza, e tende a dissociare, date le alte temperature raggiunte, il vapore a contatto in idrogeno e ossigeno. Questa causa è attualmente ben controllata, andando ad agire sull’atmosfera a contatto con il pezzo, e conducendo raffreddamenti sotto vuoto o estremamente lenti, evitando, così, l’insorgere di fiocchi bianchi superficiali al termine del raffreddamento del fuso stesso, in particolare durante la transizione austenite-ferrite.
Per infragilire completamente gli acciai ad elevata resistenza(R≥1500 MPa), caso in cui non rientra propriamente l’F82H(vedi fig 3. 1, capitolo 4, siamo su valoriintorno ai 500 MPa), sono sufficienti tenori di idrogeno disciolto inferiori a 1ppm, mentre per acciai con resistenze comprese tra i 500 e i 1000 MPa, occorrono quantità fino ai 5-10ppm.
Un rimedio sicuro da problemi insorti da saldature o deposizioni elettrolitiche è quello di effettuare un riscaldamento successivo all’intervento sull’acciaio per favorirne il più possibile, compatibilmente con le condizioni superficiali del pezzo, l’espulsione. Nel caso l’idrogeno non abbia ancora prodotto effetti reversibili, infatti, è possibile portare l’acciaio a 150°C-200°C, per periodi di tempo solitamente proporzionali al quadrato dello spessore, e recuperare, quindi, le caratteristiche meccaniche iniziali del pezzo. Nel caso in cui le dimensioni dell’acciaio assumano grosse proporzioni, o che vi sia presenza di rivestimenti superciali, bisognerà ricorrere a temperature o tempi maggiori.
La quantità di idrogeno, che entra nel reticolo metallico della struttura, e non si ricombina per poi ridisperdersi nell’ambiente, è regolata dalla legge di Sievert, precedentemente chiarita.
figura4. 12Esempio di manufatto colpito da rottura da idrogeno
4. 7. 1Problemi di blistering
L’idrogeno raccolto dal manufatto in acciaio potrebbe legarsi ad altri suo simili e costituire molecole di H2 all’interno del reticolo stesso. La specie molecolare generata è, sicuramente, più ingombrante di quella monoatomica e per questo possibile cause di cricche, in casi peggiori, poi, il calore di reazione di ricombinazione potrebbe assumere proporzioni tali da portare a fusione locale la zona coinvolta, con immaginabili conseguenze disastrose sul materiale colpito. La formazione di cricche è originata dall’incompatibilità di deformazione plastica tra matrice ed il difetto all’atto dell’azione di pressione esercitata dalla formazione stessa di idrogeno molecolare.
Il fenomeno del rigonfiamento è legato a concentrazioni limite di idrogeno monoatomico contenute nella matrice metallica dell’acciaio:
● Se CH<CH, crit rischio di frattura differita(vedi dopo) ● Se CH>CH, crit possibileformazione di blister
Il processo di ricombinazione è favorito in difetti fisici o chimici della struttura, ovvero in dislocazioni o vacanze, in particolare la presenza di quest’ultime incrementa la probabilità di accadimento per tali fenomeni. I difetti chimici che, invece, propiziano le dette reazioni tra idrogeni, sono costituite essenzialmente da impurezze reticolari, tra queste prevalgono inclusioni di MnS o ossidi; la sede designata, invece, è l’interfaccia reticolo metallico-impurezze.
Per evitare tali problemi insorti dalla presenza dei solfuri di manganese, occorre limitare la quantità di zolfo nella composizione degli acciai fino allo 0, 001%, oppure disperdere alcuni elementi nella struttura, come Ce e Ca, che determinano una modifica geometrica delle particelle di solfuro in forma sferica; il procedimento, tra l’altro, migliora anche la tenacità del manufatto metallico. Si previene, anche, questo tipo di problemi utilizzando acciai non calmati, di sicura migliore resistenza a tali situazioni[26].
4. 7. 2Frattura differita
Il fenomeno della frattura differita o “fatica statica”, come spesso viene chiamato, è un aspetto della fragilizzazione da idrogeno che interessa particolarmente gli acciai ad altissima resistenza, specie quelli rivestiti elettroliticamente con Cd o Zn. Apprezzabili quantità di idrogeno vengono infatti introdotte nell’acciaio durante il processo di elettrodeposizione del rivestimento, il quale, d’altra parte, ne ostacola fortemente la successiva fuoriuscita. Al contrario degli altri casi di infragilimento, quello causato dall’idrogeno raggiunge la massima severità in condizioni di carico statico, dando luogo a quei casi di frattura differita sotto sollecitazioni assai inferiori al carico nominale di rottura[27].
L’acciaio coinvolto, inoltre, risulta meno tenace, in particolare per ciò che concerne l’allungamento percentuale a rottura, carico necessario alla rottura per strizione, e rottura a fatica(parametro KIC), con possibili successivi collassi strutturali il cui tempo, prima dell’avvenuta, è ovvia funzione del tenore di idrogeno disciolto e dell’intensità dello sforzo applicato.
Per ogni valore di concentrazione di idrogeno, esiste un limite di carico al di sotto del quale la rottura differita non accade; il limite è funzione del carico di snervamento, della microstruttura, del grado di deformazione, della temperatura di lavoro.
figura 4. 14Curve di rottura differita per l’acciaio AISI 4340 per diverse concentrazioni di idrogeno ottenute riscaldando l’acciaio, sovrasaturo di idrogeno, a 150°C per tempi diversi
E’interessante notare, infine, come questo tipo di frattura avviene in condizioni diametralmente opposte a quelle più convenzionali, ovvero ad alte temperature e basse velocità di deformazione[26].
4. 7. 3Prevenzione[26]
Il primo metodo è, ovviamente, per prevenire tutte le forme di danneggiamento da idrogeno, quello di evitare la formazione e la permanenza di idrogeno atomico sulla superficie dei materiali metallici.
Nel caso l’idrogeno provenga da reazioni elettrochimiche è bene impedire o, comunque, limitare la scarica dell’idrogeno, accelerando i processi di ricombinazione. Quando si effettua un decapaggio, ad esempio, si cerca di realizzare ambo le cose dette sopra:utilizzo, infatti, inibitori per ridurre la produzione di idrogeno, e controllo che nella soluzione decapante non vi sia tracce di veleni di ricombinazione, come solfuri e cianuri.
L’infragilimento da saldatura è, invece, scongiurato ricorrendo a materiali di apporto privi di idrogeno ed effettuando tali operazioni in ambienti anidri, non umidi, in quanto il vapore d’acqua è una dei maggiori fornitori di idrogeno alle alte temperature.
Un secondo metodo può essere quello di adottare materiali o rivestimenti per materiali, laddove le applicazioni ce lo consentono, poco permeabili all’idrogeno, come ad esempio acciai austenitici o nichel, o anche materiali non metallici come la gomma.
Per quanto riguarda gli acciai ferritici, aggiunte di nichel e molibdeno migliorano la resistenza all’infragilimento, mentre quelle di cromo e molibdeno ne incrementano quella all’attacco, come abbiamo sottolineato anche in precedenza. La suscettibilità di tali acciai all’idrogeno cresce all’aumentare della resistenza meccanica, e ciò condiziona pesantemente la scelta del tipo di trattamento termico da effettuarsi; pertanto in ambienti a rischio di tali fenomeni è bene accontentarsi di acciai a più bassa resistenza.