Capitolo 1:
1.1 Premesse
La riparazione dei difetti di lunghezza dell’uretere si pone come obiettivo quello di preservare la funzione renale e di assicurare la continuità dell’apparato urinario. Ciò viene ottenuto mediante principi fondamentali di chirurgia ricostruttiva quali: un ottimo afflusso di sangue alla regione anatomica sede dell’anastomosi, un efficiente drenaggio delle urine, la completa escissione dell’area patologica e la presenza di una anastomosi “tension-free”.
I difetti di lunghezza ureterale derivanti da traumatismo esterno sono piuttosto rari, mentre la causa di gran lunga più frequente risulta essere il traumatismo iatrogeno. Altri motivi di danno ureterale includono l’asportazione chirurgica per neoplasia, infezioni ed infiammazioni esitanti in stenosi con compromissione funzionale dell’organo.
Il danno ureterale non rappresenta una problematica di frequente riscontro in urologia, tuttavia la preservazione della continuità dell' epitelio transizionale rappresenta la soluzione teoricamente ottimale per la conservazione di una efficiente funzione renale.
1.2 Cenni di anatomia dell’apparato urinario
1.2.1 L’uretere
L’uretere rappresenta l’estensione tubulare del sistema collettore renale che decorre verso il basso e medialmente mettendo in comunicazione il rene con la vescica urinaria. Nell’adulto, l’uretere è lungo generalmente da 24 a 30 cm, anche se esiste una certa variabilità interindividuale; generalmente si riconoscono una porzione lombare, iliaca, pelvica, iuxtavescicale ed intramurale.
Gli ureteri ed il sistema collettore che si estende fino alle papille renali sono tappezzati da cellule epiteliali di tipo transizionale, identiche a quelle che tappezzano le pareti della vescica e di parte dell’uretra.
Al di sotto dell’epitelio vi è uno strato di tessuto connettivo detto lamina propria, che insieme all’epitelio costituisce la mucosa. Quando non distesa dall’urina, la mucosa ureterale forma delle pieghe longitudinali. (Fig. 3).
Fig. 3 Uretere in sezione trasversale. Dall’interno all’esterno si possono individuare l’epitelio di transizione, la Fig. 2 Posizione e rapporti anatomici dell’uretere nella donna
I calici renali, la pelvi e l’uretere sono dotati di capacità contrattile garantita da uno strato di muscolatura liscia che ne costituisce parte della parete. Negli ureteri, questo muscolo può generalmente esser suddiviso in uno strato interno di fibre muscolari a decorso longitudinale ed in uno strato esterno a decorso obliquo e circolare. In condizioni normali, l’urina prodotta dal rene non viene trasportata passivamente, ma viene veicolata attivamente dalla pelvi renale alla vescica dall’azione peristaltica ureterale. All’esterno della muscolare propria dell’uretere è presente uno strato avventiziale che contiene un plesso di sottili vasi sanguigni che decorrono longitudinalmente assieme ad esso ed originano nel suo decorso retroperitoneale dall’arteria renale, dall’arteria gonadica, dall’aorta addominale e dall’iliaca comune, dall’iliaca interna e dai suoi rami. In vicinanza dell’uretere, i rami arteriosi decorrono longitudinalmente nell’avventizia periureterale formando un esteso plesso anastomotico che consente di mobilizzare lunghi tratti ureterali dal tessuto retroperitoneale circostante senza compromettere la vitalità dell’organo a patto di preservare il più possibile l’integrità dell’avventizia e dei vasi in esso contenuti.
Nel suo decorso retroperitoneale, l’uretere è in rapporto posteriormente con il muscolo psoas, incrocia poi anteriormente i vasi
iliaci ed entra nella pelvi all’altezza della biforcazione dell’arteria iliaca comune. Anteriormente l’uretere destro è in rapporto con la porzione terminale dell’ileo, il cieco, l’appendice, il colon ascendente, mentre il sinistro con il colon discendente ed il sigma.
L’intimo rapporto tra uretere ed organi circostanti, le sue dimensioni e mobilità fanno sì che l’uretere possa essere facilmente mobilizzato contestualmente agli organi circostanti in corso di interventi chirurgici, rendendolo particolarmente suscettibile al traumatismo iatrogeno. Nella pelvi femminile, gli ureteri sono in stretto rapporto con la cervice uterina e sono incrociati anteriormente dalle arterie uterine.
L’uretere non ha calibro uniforme, ma presenta, nel suo decorso, tre distinti restringimenti naturali: il primo situato a livello della giunzione pieloureterale, il secondo all’incrocio con i vasi iliaci ed il terzo alla giunzione uretero-vescicale nella pelvi essendo quest’ultima quella di calibro minore.
1.2.2 La vescica
È un organo cavo e mediano con funzioni di serbatoio urinario, situata nella piccola pelvi. Nell’adulto, la vescica in fase di deplezione è interamente situata all’interno della pelvi, mentre in fase di replezione risale ben al di sopra della sinfisi e può essere apprezzata durante l’esame obiettivo. La vescica vuota ha un apice, una superficie superiore, due superfici laterali o anterolaterali, una base o superficie posteriore e un collo. L’apice supera di poco il pube e termina in un cordone fibroso residuo dell’uraco, deputato nella vita embrionale alla
connessione tra vescica e cavità allantoidea. Questo cordone fibroso decorre dall’apice della vescica all’ombelico tra il peritoneo e la fascia trasversale, creando una salienza del peritoneo parietale anteriore detta legamento ombelicale mediano. La superficie superiore o cupola è l’unica ricoperta dal peritoneo, sebbene nel maschio anche una piccola porzione della base ne sia ricoperta. La faccia superiore della vescica è in rapporto con l’utero e l’ileo nella donna, con l’ileo e la porzione del colon che si trova nella cavità pelvica nel maschio. La base della vescica guarda posteriormente e nel maschio è separata dal retto dai vasi deferenti, dalle vescicole seminali e dagli ureteri, nella femmina dall’utero e dalla vagina. Le superfici anterolaterali della vescica sono in rapporto bilateralmente con il pube, con il muscolo elevatore dell’ano e con il muscolo otturatorio.
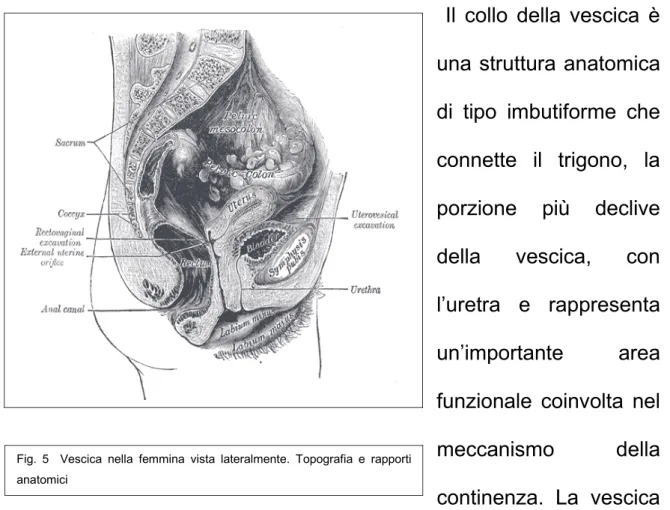
Il collo della vescica è una struttura anatomica di tipo imbutiforme che connette il trigono, la porzione più declive della vescica, con l’uretra e rappresenta
un’importante area
funzionale coinvolta nel
meccanismo della
continenza. La vescica è un organo cavo capace di distendere le proprie pareti ed accogliere un’ elevata quantità di urina. In fase di replezione infatti, il collo rimane nella sua sede naturale, ma la cupola risale nella cavità pelvica e nella porzione più caudale dell’addome, dove entra in contatto con la faccia posteriore della parte inferiore della parete addominale anteriore e la sua superficie ricoperta dal peritoneo è a contatto con il contenuto addominale.
L’interno della vescica è completamente coperto da numerosi strati di epitelio di tipo transizionale; il connettivo lasso sottostante consente una considerevole distensione della mucosa. Proprio per la proprietà
Fig. 5 Vescica nella femmina vista lateralmente. Topografia e rapporti anatomici
della vescica di variare la sua capacità, la mucosa vescicale in fase di deplezione risulta esuberante facendo assumere alla vescica un aspetto “rugoso”, rugosità che scompare a vescica piena quando la parete muscolare e la mucosa contestualmente si distendono.
Solo in corrispondenza dell’area trigonale la mucosa è fermamente aderente alla muscolatura sottostante del trigono superficiale e per tale motivo il trigono è sempre liscio, indipendentemente dallo stato di replezione. Il muscolo detrusore, che costituisce la muscolatura propria della parete vescicale, viene comunemente descritto come suddiviso in tre distinti strati muscolari, longitudinale interno, circolare intermedio e longitudinale esterno. Tuttavia sembra che una netta suddivisione in strati sia presente solo al livello del collo vescicale. La muscolatura vescicale infatti è organizzata in fasci muscolari piuttosto grossolani, variamente intrecciati che non formano delle lamine vere e proprie.
L’irrorazione arteriosa è fornita dall’arteria vescicale superiore, media e inferiore rami della branca anteriore dell’arteria ipogastrica. Alla vescica arrivano anche piccoli rami delle arterie otturatoria e glutea inferiore; nella donna, le arterie uterina e vaginale mandano alcuni rami alla base della vescica. Dal punto di vista venoso la vescica è avvolta da un ricco plesso venoso generalmente situato tra la parete
vescicale propriamente detta e lo strato avventiziale che la ricopre, che sbocca nelle vene ipogastriche. Il plesso venoso comunica anche con il plesso venoso retro pubico o plesso di Santorini che drena il pene ed altri organi perineali.
1.2.3 Anatomia della giunzione uretero-vescicale
La giunzione ureterovescicale viene comunemente descritta come una struttura valvolare in grado di consentire il passaggio unidirezionale di urina dall’uretere alla vescica prevenendo così il reflusso vescicoureterale. Anatomicamente è costituita dalla porzione terminale dell’uretere, dal trigono e dalla parete vescicale adiacente (Fig. 6). Gli studi di Tanaghoe Collaboratori(1) hanno individuato una
continuità anatomica a questo livello tra trigono e uretere a costituire una entità strutturale unica ureterotrigonale il cui tono muscolare è responsabile della proprietà antireflusso della giunzione.
Quando il bolo urinoso, veicolato dall’onda peristaltica ureterale, si approssima alla porzione intramurale la giunzione si apre consentendo all’urina di giungere in vescica.
Inoltre, quando la vescica si riempie e progressivamente si distende, il
trigono viene progressivamente stirato consentendo un allungamento consensuale della porzione intramurale dell’uretere con conseguente aumento della capacità di tenuta.
Durante la minzione, quando si verificano la contrazione attiva del detrusore ed il conseguente aumento della pressione endovescicale, si ha contemporaneamente le contrazione del trigono che serra completamente la porzione intramurale impedendo sia il reflusso che l’afflusso di urina.
Alla fine della minzione la resistenza diminuisce bruscamente mentre riprende il passaggio di urina dall’uretere alla vescica.
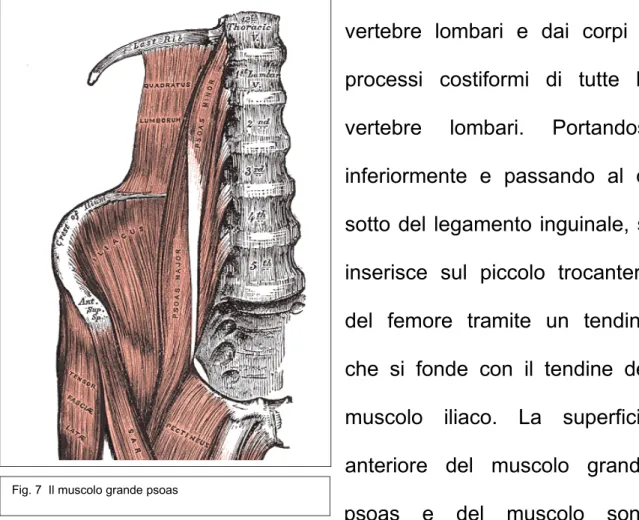
1.2.4 Il muscolo grande psoas
Il muscolo grande psoas è un muscolo fusiforme, che insieme al muscolo iliaco costituisce il muscolo ileo psoas (Fig. 7). Origina dal corpo della dodicesima vertebra toracica, dai corpi delle prime quattro vertebre lombari e dai corpi e processi costiformi di tutte le vertebre lombari. Portandosi inferiormente e passando al di sotto del legamento inguinale, si inserisce sul piccolo trocantere del femore tramite un tendine che si fonde con il tendine del muscolo iliaco. La superficie anteriore del muscolo grande psoas e del muscolo sono ricoperte da una guaina connettivale di consistenza piuttosto fine nella porzione più craniale, ma che tende lungo il basso ad ispessirsi
costituendo un rivestimento fibroso piuttosto resistente. Sulla superficie anteriore del muscolo grande psoas si può trovare anche se frequentemente assente il muscolo piccolo psoas che origina a livello della porzione più craniale del grande psoas e vi decorre anteriormente confluendo poi in un tendine che si inserisce in basso sulla linea pettinea.
1.3 Il reimpianto ureterale con psoas hitch
1.3.1 Introduzione
Il reimpianto ureterale con psoas hitch è stato descritto per la prima
volta da Zimmerman(2) nel 1960, ma reso popolare successivamente
da Turner-Warwick e Worth(3) nel 1969; questa tecnica viene utilizzata
per riparare i difetti di lunghezza del terzo distale dell’uretere e consiste nella mobilizzazione e sospensione della vescica verso l’alto e lateralmente, riducendo la distanza tra vescica e rene rendendo così possibile anastomizzare direttamente la vescica con un uretere più corto del normale (Fig.8).
La tecnica originale prevedeva l’esecuzione di una anastomosi uretero-vescicale senza tecnica antireflusso; Harrow(4) nel 1968
modificò lievemente tale tecnica proponendo l’esecuzione di un tunnel sottomucoso antireflusso (tecnica di Politano-Leadbetter(5)) nel quale
Fig. 8 (A e B) Reimpianto ureterale con “bladder psoas-hitch”
indovare l’uretere distale al momento della anastomosi. Alternativamente una anastomosi antireflusso può essere ottenuta ripiegando l'uretere terminale a polsino di camicia (metodica “split-cuff”) (Fig. 9).
Da allora, è stata enfatizzata la necessità di un’anastomosi ureterovescicale non refluente. Il vantaggio di tale metodica sarebbe quello di una minore incidenza di pielonefrite ed insufficienza renale da reflusso cronico ed infezione. Sebbene ciò rappresenti un aspetto di primaria importanza nel paziente pediatrico, la sua importanza nell’adulto non è chiara.
Il vantaggio di una anastomosi refluente consiste nella semplicità di esecuzione, minori tempi operatori, minore rischio di stenosi ureterale e la possibilità di coprire un gap ureterale di 2-3 cm maggiore rispetto alla anastomosi non refluente.
Fig. 9 Reimpianto ureterale con metodica “split- cuff”
Sin dalla sua introduzione nell’armamentario chirurgico urologico, diversi studi(6,7) hanno dimostrato la sua efficacia a lungo termine e la
sua superiorità rispetto ad altre procedure.
Infatti, il reimpianto ureterale con psoas hitch offre il vantaggio di conservare la continuità dell’epitelio transizionale e consente di mantenere intatta l’integrità dell’alta via urinaria controlaterale riducendo così il rischio di infezioni croniche del tratto urinario ed anormalità elettrolitiche che sono frequenti rispettivamente dopo transureteroureterostomia (TUU) e sostituzione di uretere con un segmento ileale. La tecnica psoas hitch tuttavia può essere raramente utilizzata in concomitanza con transureteroureterostomia nei casi più complicati di chirurgia ricostruttiva ureterale per difetti ureterali bilaterali.
Può essere ulteriormente utilizzata effettuando una mobilizzazione del rene e nefropessi inferiore, particolarmente a sinistra, consentendo così di abbreviare ulteriormente la distanza fra la pelvi renale e la vescica.
1.3.2 Indicazioni e controindicazioni
Indicazioni alla psoas hitch includono: il traumatismo dell’uretere distale, le fistole ureterali secondarie a chirurgia pelvica, la resezione ureterale distale per neoplasia uroteliale, le stenosi dell’uretere distale ed il fallimento di un precedente reimpianto ureterale.
Tuttavia, difetti di lunghezza dell’uretere distale estesi cranialmente al tratto pelvico possono richiedere soluzioni ricostruttive più complesse. Una vescica contratta o di scarse dimensioni generalmente rappresenta una controindicazione data la insufficiente mobilità e capacità vescicale, condizioni essenziali per l’esecuzione della psoas-hitch.
Una valutazione uro dinamica preoperatoria può fornire importanti informazioni sulla capacità contrattile detrusoriale e sulla compliance vescicale.
Preoperativamente i difetti dell’uretere dovrebbero essere studiati con una urografia o uro-TC o una pielografia anterograda (tramite nefrostomia) o una pielografia ascendente.
1.3.3. Descrizione della tecnica chirurgica
Si procede ad incisione cutanea tipo Pfannestiel o mediana longitudinale ombelico-pubica; posizionato il catetere vescicale si riempie la vescica con circa 200 ml di soluzione fisiologica sterile in maniera da agevolare l’identificazione del margine vescicale.
Si accede allo spazio prevescicale di Retzius e si procede alla mobilizzazione della vescica mediante sezione del deferente, del legamento rotondo e del legamento ombelicale mono o bilateralmente. Una sufficiente mobilità vescicale si raggiunge se la cupola vescicale in corso di trazione raggiunge i vasi iliaci. In caso di insufficiente mobilità, può essere necessaria la sezione del peduncolo vescicale superiore controlaterale.
Una volta identificato l’uretere a livello dell’incrocio con i vasi iliaci esso viene sezionato al di sopra del tratto patologico; si posiziona un punto di repere sull’estremità prossimale e si procede ad una sua mobilizzazione.
Si procede quindi alla mobilizzazione verso l’alto e lateralmente della cupola vescicale; questa manovra può essere ulteriormente facilitata dalla cistotomia anteriore che viene generalmente eseguita longitudinalmente od obliquamente, ma può essere eseguita
orizzontalmente e chiusa verticalmente secondo la tecnica descritta da Heineke-Mikulicz.
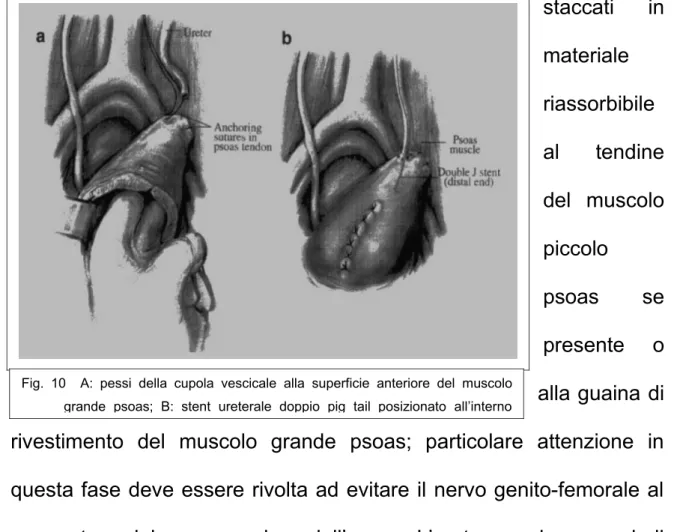
La cupola della vescica viene quindi solidarizzata mediante due punti staccati in materiale riassorbibile al tendine del muscolo piccolo psoas se presente o alla guaina di rivestimento del muscolo grande psoas; particolare attenzione in questa fase deve essere rivolta ad evitare il nervo genito-femorale al momento del passaggio dell’ago. L’uretere viene quindi anastomizzato, con o senza tecnica antireflusso, alla porzione supero laterale della cupola vescicale; prima della chiusura della cistotomia anteriore, viene posizionato un catetere ureterale “pigtail” per il drenaggio delle urine ed il mantenimento di una anastomosi “asciutta” (Fig. 10 A,B). Generalmente la psoas hitch riesce a coprire un “gap” ureterale tra i 5 ed i 15 cm rispetto al solo reimpianto ureterale.
Fig. 10 A: pessi della cupola vescicale alla superficie anteriore del muscolo grande psoas; B: stent ureterale doppio pig tail posizionato all’interno
Le percentuali di successo del reimpianto ureterale con psoas hitch si aggirano intorno al 85% negli adulti e bambini. Le complicanze più comuni sono rappresentate dalla fistola urinaria e dalla stenosi ureterale sul segmento anastomotico.
1.4 Le alternative alla psoas hitch
1.4.1 Resezione ureterale ed anastomosi
In caso di difetto ureterale sufficientemente breve, è possibile eseguire una ureteroureterostomia; questa deve essere eseguita mediante tecnica “tension free” previo spatolamento
delle due estremità
dell’uretere. La sutura viene eseguita in punti staccati di materiale riassorbibile; tali punti non devono essere troppo vicini tra di loro per il rischio di ischemia e conseguente stenosi (Fig. 11). Viene quindi posizionato un catetere ureterale per 2-6 settimane.
Fig. 11 Ureteroureterostomia: spatolamento ureterale e sutura in punti staccati
1.4.2 Tecnica con lembo vescicale di Boari
La tecnica di sostituzione parziale dell'uretere distale con un lembo vescicale peduncolizzato, descritta inizialmente da Boari(8) alla fine del
secolo scorso, trova oggi indicazione per il trattamento dei difetti ureterali di una certa entità del tratto ureterale medio e inferiore. Quando il tratto patologico è troppo lungo o la mobilità ureterale è troppo limitata per eseguire una ureteroureterostomia, il flap di Boari rappresenta una valida alternativa.
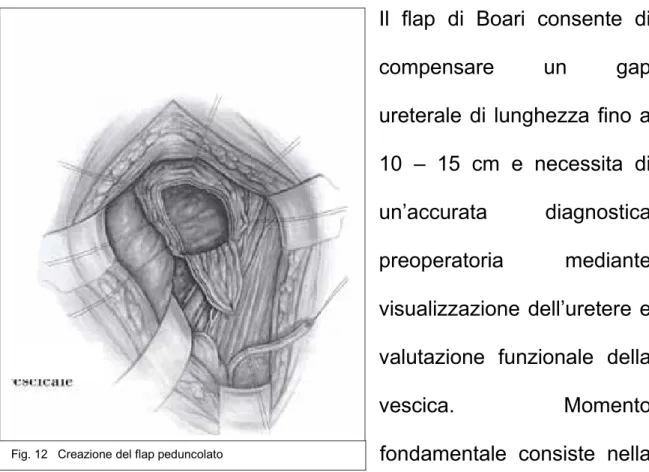
Il flap di Boari consente di compensare un gap ureterale di lunghezza fino a 10 – 15 cm e necessita di
un’accurata diagnostica
preoperatoria mediante
visualizzazione dell’uretere e valutazione funzionale della
vescica. Momento
fondamentale consiste nella individuazione della arteria vescicale superiore o di uno dei suoi rami omolateralmente alla lesione; viene poi creato un flap di parete
vescicale a sede postero-laterale, di almeno 4 cm di larghezza il cui apporto vascolare è garantito dal vaso precedentemente individuato. Si procede infine a chiusura anteriore del flap e della breccia vescicale e completamento dell’anastomosi (Fig. 12,13,14).
1.4.3 Transureteroureterostomia
Questa tecnica fu descritta per la prima volta da Sharpe(9) nel 1906 e Fig. 13 Anastomosi tra uretere e flap peduncolato
vescicale
Fig. 14 Completamento dell’anastomosi e chiusura della breccia
ureterali. Consiste sostanzialmente nella trasposizione controlaterale dell’uretere patologico e nella anastomosi ureteroureterale termino-laterale su uretere controtermino-laterale sano. Dati della letteratura mostrano un tasso di complicanze a lungo termine accettabile (2.4%)(10).
Per il buon esito dell’intervento è necessario disporre di una lunghezza ureterale sufficiente ad attraversare la linea mediana per realizzare un’anastomosi “tension-free” sul lato opposto; è importante inoltre evitare inginocchiamenti e torsioni durante il tragitto ureterale (Fig. 15). Maggiore è il segmento ureterale patologico, meno acuta è l’angolazione dell’anastomosi e maggiore sarà la possibilità di ostruzione meccanica.
Il punto migliore per attraversare la linea mediana è a livello della biforcazione aortica dove gli ureteri decorrono più vicini l’uno all’altro. Sebbene questo tipo di soluzione abbia mostrato una certa efficacia e sicurezza, il suo utilizzo rimane sicuramente limitato a difetti ureterali coinvolgenti l’uretere prossimale laddove la ureteroneocistostomia non è possibile.
1.4.4 Uretere ileale
L’utilizzo di un segmento ileale viene generalmente riservato ai casi in cui, per lunghezza e posizione del tratto ureterale coinvolto, è preclusa l’esecuzione di una ureteroureterostomia, flap di Boari o psoas-hitch (Fig. 16).
La tecnica è stata per la prima volta descritta da Shoemaker(11) nel
1906 poi resa più
popolare da
Goodwin(12) nel 1959.
Da allora tale procedura è stata utilizzata con risultati
non del tutto
soddisfacenti dovuti
alla progressiva
dilatazione ed
allungamento del tratto ileale, al reflusso, infezioni, acidosi metabolica ed eccessiva secrezione mucosa. Inoltre mentre per l'uretere sinistro la sostituzione avviene con un'ansa a pieno canale in direzione peristaltica, a destra la sostituzione avviene
Fig. 16 Sostituzione ureterale con tratto ileale
in senso contrario alla peristalsi. Con lo scopo di ovviare alle suddette problematiche è stata proposta la sostituzione di uretere ileale con la tecnica di Yang-Monti(13,14), la quale prevede l’isolamento
di un tratto ileale di 2-3 cm di lunghezza che viene sezionato sul suo versante antimesenterico e riconfigurato sul suo asse longitudinale. Isolando tre segmenti ileali vengono di solito coperti gap ureterali estesi sino a 18 cm. L’incisione a carico della porzione prossimale dell’anello prossimale e quella distale del distale è stata eseguita in sede paramesenterica (Fig. 17,18). Ciò consente di eseguire prossimalmente una anastomosi spatolata termino-terminale ed una anastomosi ileo-vescicale con meccanismo antireflusso secondo Lich-Grégoir(15,16).
1.4.5 Autotrapianto renale
L'auto-trapianto di rene è una procedura chirurgica che prevede l'asportazione di un rene dalla sua sede naturale per riposizionarlo dopo eventuale “chirurgia da banco”, nello scavo pelvico.
L'autotrapianto di rene viene effettuato in situazioni in cui patologie o lesioni di varia natura, comportano un danno a carico dei vasi, dell'uretere o del parenchima renale tali da non essere trattabili in situ in modo conservativo, per cui soprattutto in presenza di rene unico
funzionante, si rende indispensabile il mantenimento della funzionalità del rene interessato(17,18,19).
L'intervento viene generalmente eseguito in regime di elezione. Dal punto di vista tecnico, la procedura consiste nel prelievo dell'organo, nel suo eventuale trattamento al di fuori dell'organismo e infine nell'impianto, che di solito viene fatto in fossa iliaca, praticando una anastomosi dei vasi renali (arteria e vena) sui vasi iliaci del paziente mentre l'uretere viene reimpiantato in vescica mediante plastica antireflusso extravescicale secondo Lich-Grégoir (Fig. 19).
Capitolo 2
:
2.1 Pazienti
Tra il Novembre 2000 ed il Maggio 2010, sono stati sottoposti a resezione di uretere distale e reimpianto ureterale con psoas hitch presso l’Unità Operativa di Urologia Universitaria della Azienda Ospedaliero-Universitaria Pisana, 22 pazienti di cui 7 maschi e 15 femmine, di età media 54,6 anni (range 24 e 74). (Tab. I)
2.2 Diagnostica
La diagnostica di cui ci siamo avvalsi per diagnosticare stenosi o neoplasie dell’uretere terminale comprendeva indagini ecografiche, radiologiche ed endoscopiche. L’ecografia è stata eseguita in tutti i
Tab. I Pazienti inclusi nello studio
Caratteristiche dei pazienti inclusi nello studio
Età media al momento dell’intervento (aa) 54,6 (range 24 - 74)
Sesso 15 F7 M
pazienti data la scarsa invasività della metodica ed i bassi costi, evidenziando una situazione di idroureteronefrosi più o meno marcata secondo l’entità ed il tempo di insorgenza della stenosi. L’ecografia rimane comunque un’indagine di primo livello che assieme alla clinica consente di evocare il sospetto clinico confermato poi da esami di tipo radiologico quali urografia endovenosa, uro-TC, pielografia ascendente e discendente. L’urografia endovenosa e la uro-TC rappresentano esami fondamentali per la diagnostica della stenosi ureterale; la uro-TC consente tuttavia, mediante la ricostruzione multi planare una migliore localizzazione topografica del tratto stenotico. Talvolta, per quantificare esattamente l’entità del tratto stenotico si è resa necessaria l’esecuzione di una pielografia ascendente, procedura mediante la quale, per via endoscopica, si provvede ad incannulamento dell’uretere ed opacizzazione dell’uretere dal basso verso l’alto. Nei casi in cui il paziente era portatore di nefrostomia percutanea (2 casi nella nostra serie) posizionata per urosepsi o algia lombare è stata eseguita una pielografia discendente, la quale mediante il tramite nefrostomico consente di opacizzare la via escretrice dall’alto verso il basso. In caso di incertezza diagnostica è stata eseguita ureteroscopia diagnostica.
2.3 Tecnica chirurgica
La tecnica che abbiamo utilizzato per il reimpianto ureterale con psoas hitch si conforma a quella descritta originariamente da Zimmerman.
Essa prevede un accesso tramite un’incisione sovraombelicopubica. L’apertura della parete muscolare. L’isolamento, legatura e sezione dell’arteria ombelicale, indi l’isolamento dell’uretere nel tratto interessato e la sua preparazione fino alla vescica. Si prepara poi la cupola vescicale e si effettua la sua extraperitoneizzazione. Si esegue una cistotomia longitudinale sulla cupola. Si esegue ureterectomia distale “en bloc” con pastiglia vescicale in caso di neoplasia transizionale dell'uretere terminale, e si effettua chiusura in doppio strato della breccia vescicale perimeatale. Si prepara il muscolo psoas e vi si ancora il corno vescicale con due punti “DEXON” 2.0. Si procede al reimpianto ureterale nel corno vescicale con la tecnica antireflusso più adeguata alla lunghezza e al calibro dell'uretere disponibile posizionando uno stent ureterale tipo ”pigtail” di adeguata lunghezza. Si effettua chiusura in doppio strato della cistotomia longitudinale. Si procede al posizionamento di punti di detensione dell’anastomosi uretero-vescicale ed emostasi. Si procede poi a
lavaggio per la verifica della tenuta delle cistorrafie. Si inserisce Foley vescicale 18 CH. Si effettua poi la chiusura delle brecce peritoneali e quindi la chiusura della parete per strati. Nei casi di resezione ureterale per carcinoma transizionale è opportuno eseguire una linfoadenectomia loco-regionale contestualmente alla resezione del segmento ureterale sede della lesione.
In quattordicesima giornata postoperatoria viene eseguita una cistografia trans catetere vescicale con mdc allo scopo di verificare l'assenza di stravaso delle suture vescicali ed ureterali. (Fig. 20)
Fig. 20 Cistografia eseguita in paziente che presentava recidiva pelvica di etp sigma inglobante l'uretere terminale trattato con asportazione della stessa e reimpianto ureterale con “bladder
psoas-Il tutore ureterale posizionato in sede intraoperatoria al momento del confezionamento della anastomosi ureterovescicale viene solitamente rimosso dopo due settimane.
Di seguito si espongono le fasi della tecnica operatoria con l’ausilio di immagini:
Isolamento e sospensione dell'uretere con fettuccia
Sondaggio del lume
Tutela dell'uretere con cateterino tipo Bracci
Mobilizzazione della vescica ed esecuzione di cistotomia mediana
Sollevamento della vescica aperta fino all’uretere resecato, e fissaggio della stessa al muscolo psoas
Incisione della parete vescicale a tutto spessore a livello del lembo fissato allo psoas per creare un tramite attraverso il quale viene fatto passare l’uretere
Creazione di un tunnel sottomucoso all’interno del quale transita l’uretere per qualche centimetro
”
2.3 Raccolta dei dati e follow-up
La raccolta retrospettiva dei dati è avvenuta mediante analisi delle cartelle cliniche e dei registri operatori. Oltre alle caratteristiche demografiche dei pazienti sono state raccolte notizie inerenti l’anamnesi patologica dei pazienti, l’intervento chirurgico, il decorso e
punti staccati in materiale riassorbibile lungo tutta la circonferenza e nuovamente tutelato con catere ureterale tipo “pigtail
Aspetto dell'uretere reimpiantato nel corno vescicale, fissato allo psoas, mediante tecnica antireflusso con tunnel sottomucoso e tutelato da catetere “pigtail”
Il follow-up a lungo termine è stato eseguito mediante intervista telefonica comprendente domande volte alla valutazione delle complicanze a lungo termine legate alla procedura.
In particolare sono stati valutati i risultati funzionali mediante esame delle urografie o uro-TC postoperatorie e delle successive ecografie di controllo. Come misura della funzionalità renale sono stati presi in considerazione i valori della creatinina sierica.
Capitolo 3:
3.1 Indicazioni alla procedura e dettagli intraoperatori
L’intervento di resezione e reimpianto ureterale con psoas hitch si è reso necessario in 6 casi (27%) di pazienti precedentemente sottoposte a chirurgia pelvica ginecologica. (Tab. II)
Di queste, 4 pazienti erano stato sottoposte a isterectomia per via addominale, una ad isterectomia per via endovaginale ed una a plastica transvaginale per prolasso uterino e cistocele.
Dati intraoperatori
Lunghezza del segmento ureterale patologico (cm) 4,5 (range 2,5 – 9)
Tipo di anastomosi ureterovescicale eseguita Split-cuff 18 Politano-Laedbetter 2
Diretta 2
Indicazioni al reimpianto
Esiti di chirurgia ginecologica 6 Etp uretere terminale 5 Esiti di urolitiasi 5 Endometriosi 3 Esiti di radioterapia esterna 1 Stenosi di reimpianto ureterale 1 Recidiva neoplastica pelvica 1
Durata dell’intervento - media e range – (min) 170 (130 - 210)
Perdita stimata di sangue - media e range – (ml) 350 (150 - 600)
In 5 casi (23%) la presenza di un carcinoma transizionale a carico dell’uretere terminale ha richiesto la resezione e reimpianto.
In ulteriori 5 casi (23%) la flogosi cronica esito di storia di urolitiasi, ha esitato in stenosi e compromissione funzionale.
In 3 pazienti (15%) l’intervento è stato indicato per endometriosi estrinseca o intrinseca e conseguente stenosi ureterale.
In un caso (4%) il restringimento dell’uretere è insorto dopo radioterapia pelvica esterna; in un caso (4%) si è dovuti ricorrere a reimpianto dopo stenosi su pregressa ureterocistoneostomia eseguita per reflusso vescico-ureterale; in un caso (4%) l'uretere terminale era compresso da recidiva pelvica di K sigma asportata contestualmente. Per quanto riguarda la tecnica anastomotica ureterovescicale, in 18 dei 22 casi (82%) è stata eseguita tecnica antireflusso “split-cuff”, in 2 pazienti (9%) è stata eseguita la tecnica con tragitto sottomucoso se-condo “Politano-Laedbetter” ed in ulteriori 2 casi (9%) una anastomosi diretta con spatolamento ureterale; in tutti i casi è stata utilizzata una sutura riassorbibile in punti staccati di monocryl 4-0.
La lunghezza media del segmento ureterale patologico asportata è stata di 4,5 cm con range compreso tra 2,5 – 9 cm; la durata dell’intervento è stata mediamente di 170 minuti (range 130 - 210) e la perdita di sangue media di 350 ml (range 150 - 600).
3.2 Complicanze a breve termine
Non si sono verificate complicanze intraoperatorie nei pazienti inclusi in questa serie. In un paziente (4%), a distanza di tempo di due settimane dall’intervento, dopo la rimozione del tutore ureterale si è verificato un episodio urosettico trattato con successo mediante terapia antibiotica per via parenterale; tale paziente era stato sottoposto a reimpianto con tecnica refluente per stenosi ureterale da urolitiasi.
3.3. Complicanze a lungo termine
Il follow-up medio dei pazienti è risultato di 50,9 mesi con un range compreso tra 4 e 118. Mediante intervista telefonica sono stati raccolti dati inerenti le condizioni generali dei pazienti, la creatinina sierica ed eventuali esami di diagnostica per immagini eseguiti (Tab. III). Due pazienti risultavano deceduti per cause non inerenti alla procedura eseguita: un paziente maschio deceduto per etp del sigma dopo 10 mesi ed una paziente femmina per diffusione metastatica da carcinoma dell’utero dopo 6 mesi; in questi casi le informazioni di
interesse del presente studio sono state comunque raccolte mediante intervista di familiari.
Al follow-up telefonico, 3 pazienti (13,6%) hanno riferito la presenza di algia lombare cronica; in due di essi il dolore era localizzato omolateralmente alla sede della lesione, mentre un altro paziente riferiva dolenzia lombare bilaterale. L’entità del dolore è stata riferita come lieve-moderata e comunque nessuno dei 3 pazienti ha necessitato di terapia antidolorifica.
In nessuno dei pazienti della nostra serie si sono verificati episodi di pielonefrite, mentre 5 su 22 pazienti (22,7%) hanno riferito episodi di
Tab. III Complicanze a lungo termine
Complicanze a lungo termine
Algia lombare cronica 3/22 (13,6%)
Pielonefrite 0/22
Episodi di infezioni delle vie urinarie 5/22 (22,7%)
Imaging alta via escretrice Nei limiti della norma 20/22 (91%)
Patologico 2/22 (9%)
Reinterventi 0/22
Funzione renale (creatininemia)
Lieve IRC 1/22 (4%) Nei limiti 21/22 (96%)
infezioni delle vie urinarie, tuttavia nessuno dei pazienti riferiva più di 2 episodi l’anno.
L’indagine ecografica dell’alta via escretrice risultava nella norma in 20/22 pazienti (91%), mentre in 2 (9%) pazienti il rene omolaterale alla sede della lesione ureterale è risultato di dimensioni inferiori al controlaterale.
La funzione renale è stata valutata esclusivamente mediante il valore della creatininemia sierica. Una paziente, monorene, su 22 (4%), presentava una insufficienza renale di grado lieve (creatininemia sierica di 1,9 mg/dl); tale paziente tra l’altro riferiva alcuni episodi infettivi del basso tratto urinario in assenza di segni di pielonefrite ed in presenza di un esame che documentava un’apparato urinario nei limiti della norma; in questa paziente era stata utilizzata tecnica anastomotica ureterovescicale tipo “split-cuff”. Negli altri 21 pazienti il valore della creatinina risultava nei limiti della norma. Nessuno dei pazienti è stato sottoposto a reintervento eseguito per complicanza o fallimento dell’intervento di resezione e reimpianto ureterale con tecnica psoas-hitch.
Capitolo 4:
4.1 Discussione
La mobilizzazione della vescica verso l’alto per compensare un difetto di lunghezza ureterale è stata descritta per la prima volta nel 1933. Zimmerman e Collaboratori(2) descrissero per la prima volta la tecnica
che solidarizzava la vescica al tendine dello psoas, mentre Harrow(4)
modificò leggermente la tecnica aggiungendo l’esecuzione di un tunnel sottomucoso per l’uretere in modo da prevenire il reflusso.
Da allora la necessità di eseguire un’anastomosi con meccanismo antireflusso è stata sempre più enfatizzata anche nel paziente pediatrico in maniera tale da ridurre il rischio di pielonefrite ed insufficienza renale cronica secondaria a reflusso ed infezione. Tuttavia l’importanza del meccanismo antireflusso, soprattutto nel paziente adulto risulta poco chiara. I vantaggi di un’anastomosi di tipo refluente sono, la maggiore semplicità della tecnica di esecuzione, tempi chirurgici minori, ridotto rischio di stenosi anastomotica e la possibilità di risparmiare 2 – 3 cm di lunghezza rispetto all’anastomosi antireflusso con il tunnel sottomucoso. Nel presente studio abbiamo utilizzato più frequentemente un’anastomosi tipo “split-cuff”, che consente di utilizzare un segmento breve di uretere e si adatta anche ad ureteri dilatati, con risultati più che soddisfacenti data la scarsità di
complicanze tardive e la presenza di insufficienza renale cronica lieve in una sola paziente su 22 trattati.
La versatilità del reimpianto della psoas hitch è stata negli anni dimostrata da diversi Autori i quali con i loro studi hanno analizzato la funzionalità e la validità della tecnica. (Tab. IV)
Autore Rivista e anno Numero di Casi Media Follow up Risultati e criteri di valutazione Riedmiller Staehler Matthews El-Khader Ahn Eur Urol 1984 Urol Int 1984 J Uro 1997 Acta Urol Belg 1998
Urology 2001 181 111 20 18 24 N.D. N.D. 6 anni 5,7 anni 2,7 anni 96,7 % di successi 72% eccellente/buono 85% non reinterventi 72,4 % successi 100 % successo (nessun reintervento) Totale 354 Media 4,8 anni Media Successi 85,22 %
Matthews e Marshall(5) hanno esaminato in retrospettiva 20 pazienti
sottoposti a reimpianto ureterale con psoas hitch onde determinare l’efficacia a lungo termine della procedura. La durata del follow-up è stata in media di 6 anni con risultati oltremodo positivi. Difatti 17 pazienti (85%) non hanno avuto necessità di reintervento ed hanno mantenuto un’ottima funzione renale. In 2 pazienti sottoposti a reimpianto per etp dell’uretere è stato necessario effettuare un Tabella IV: Principali serie di reimpianto ureterale con tecnica “Bladder Psoas-Hitch”
intervento ricostruttivo mediante condotto ileale ed un solo paziente ha riscontrato dolore persistente al fianco.
Ahn e Loughlin(20) hanno analizzato 24 pazienti sottoposti a reimpianto
ureterale con psoas hitch con un follow up medio di 32,75 mesi. In un solo caso si è avuta un’ urosepsi postoperatoria. Negli altri pazienti non si sono riscontrati casi di dolore cronico ai fianchi, pielonefrite ricorrente, idronefrosi persistente o funzionalità renale compromessa, inoltre nessun paziente ha avuto necessità di reintervento per complicanze a breve o lungo termine.
El-Khader et al(21) hanno effettuato un’analisi su 18 pazienti sottoposti
a questo tipo di procedura con un follow-up medio di 5,7 anni. L’analisi ha riscontrato la validità della tecnica con 17 successi ed un solo decesso.
Riedmiller et al(22) hanno riportato la loro esperienza con questa
procedura effettuata su 181 pazienti con un 96,7 % di successi.
Staehler et al(23) hanno analizzato i dati raccolto da 111 reimpianti
eseguiti con la tecnica psoas hitch in dodici anni di lavoro. I risultati degli interventi sono stati classificati come eccellenti nel 72 % dei casi e si sono verificati fallimenti solo nel 16 %.
Patil et al(24) riportano un’esperienza istituzionale e
assistito da robot “Da Vinci”, su 12 pazienti con un follow up medio di 15,5 mesi. L’analisi dei dati evidenzia una riuscita dell’intervento su tutti i pazienti i quali non mostrano più alcun segno della patologia iniziale.
Le alternative possibili per il reimpianto ureterale sono meno desiderabili.
_La transureteroureterostomia espone a rischio di infezione e stenosi la via escretrice ricevente ed ha numerose controindicazioni tra cui: lunghezza inadeguata per realizzare un’anastomosi senza tensioni, precedenti dissezioni o mobilizzazioni dell’uretere, pregressi traumi o terapia radiante, tubercolosi renale o ureterale, litiasi recidivante mono o bilaterale, neoplasie uroteliali, fibrosi retroperitoneli, pielonefrite cronica di entrambi i reni o reflusso dell’uretere nel distretto ricevente. _Il flap secondo Boari presenta un elevato rischio di necrosi del lembo vescicale per inadeguata vascolarizzazione con conseguente fibrosi e stenosi dell’anastomosi. Questa tecnica è controindicata nei casi di ridotta capacità vescicale, in caso di vescica neurogena o di carcinoma a cellule transizionali.
_La superiorità della tecnica “psoas-hitch” rispetto alla sostituzione con ileo a pieno a canale consiste nella possibilità di mantenere la continuità uroteliale; inoltre evita anormalità elettrolitiche dovute al
riassorbimento di urina dal segmento ileale interposto, evita la produzione di muco che può portare ad una stenosi del segmento stesso e, al contrario della sostituzione ileale, può essere effettuata anche in urgenza. Oltre a questo la sostituzione ileale ha numerose controindicazioni non presenti nella psoas hitch che includono: livelli sierici di creatinina > 2 mg/dl, la presenza di una vescica neurogena, malattie infiammatorie intestinali, enteriti post RT e disfunzioni epatiche.
Per tali considerazioni attualmente, per perdite di sostanza ureterali estese ed alte, le vie escretrici vengono ricostruite mediante ansa ileale ridotta di calibro con la tecnica di Yang-Monti che riduce notevolmente la superficie della mucosa intestinale in contatto con le urine.
_L’autotrapianto renale rappresenta una procedura chirurgica piuttosto complessa suscettibile di complicanze di natura vascolare (es. trombosi, stenosi), più frequenti in reni infetti, ematuria generalmente in sede di impianto dell'uretere, raccolte urinose in sede di intervento in caso di fistola ureterale o renale ed ostruzione della via escretrice.
4.2 Conclusioni
In conclusione, alla luce della letteratura internazionale e della presente esperienza, il reimpianto ureterale con tecnica “bladder psoas-hitch” rappresenta una tecnica sicura ed affidabile per ricostruire i difetti dell’uretere terminale dovuti a patologia multipla, adattandosi anche a situazioni cliniche complesse come i reinterventi. Un’anastomosi ureterovescicale antireflusso con tecnica “split-cuff” può essere ragionevolmente impiegata nell’adulto senza eccessivi rischi e complicanze(25).
Bibliografia
1. Tanagho, E A, Meyers, F H, and Smith, D E: The trigone: Anatomical and physiological considerations. 1. In relation to the ureterovescical junction. J. Urol., 100:623, 1968.
2. Zimmerman IJ, Precourt WE, and Thompson CC: Direct uretero-cysto-neostomy with the short ureter in the cure of ureterovaginal fistula. J Urol 83: 113, 1960.
3. Turner-Warwick R, Worth PHL: The psoas bladder-hitch procedure for the replacement of the lower third of the ureter. Br J Urol 41: 701,1969
4. Harrow BR: A neglected maneuver for ureterovescical reimplantation following injury at gynaecologic operations. J Urol 100: 280, 1968.
5. Politano VA, Leadbetter WF: An operative technique for the correction of vesicoureteral reflux. J. Urol 79:932, 1958.
6. Matthews R, Marshall FF: Versatility of the adult psoas hitch ureteral
reimplantation. J Uro 158: 2078, 1997.
7. Riedmiller H, Becht E, Hertle L, et al: Psoas-hitch ureteroneocystostomy: experience with 181 cases. Eur Urol 10: 145, 1984.
8. Casati E, Boari A: Contributo sperimentale alla plastica dell' uretere. Atti Accad Scient Med Nat 14: 149, 1894.
9. Sharpe, N W: Transuretero-ureteral anastomosis. Ann. Surg. 44:687, 1906.
10. Noble IG, Lee KT, Mundy AR: Transuretero-ureterostomy: a review of 253 cases. Br J Urol. Jan 79:20-3, 1997.
11. Shoemaker J: Discussie op voordracht van J. M. van Damn over interabdominale plastiken. Ned Tijdschr Geneesk. 836, 1911.
12. Goodwin, W E, Winter, CC and Turner, R D: Replacement of the ureter by small intestine: clinical application and results of the “ileal ureter” . J Urol, 81:406,1959.
13. Yang WH: Yang needle tunneling technique in creating antireflux and continent mechanisms. J Urol 150: 830, 1993.
14. Monti PR, Lara RC, Dutra MA, de Carvalho JR: New techniques for construction of efferent conduits based on the Mitrofanoff principle. Urology 49: 112, 1997.
15. Lich R Jr, Howerton LW, Davis LA: Recurrent urosepsis in children. J Urol 86: 554, 1961.
16. Grégoir W, Van Regmorter G: Le reflux vésico-uréteral congenital. Urol Int 18:127, 1964.
17. Hardy JD. High ureteral injuries: management by autotransplantation of the kidney. JAMA 184:97, 1964.
18. Novick AC, Stewart BH, Straffon RA: Extracorporeal renal surgery and autotransplantation: indications, techniques, and results. J Urol 123:806, 1980.
20. Ahn M, Loughlin KR: Psoas hitch ureteral reimplantation in adults-analysis of a modified technique and timing of repair. Urology 58:184, 2001. 21. El Khader k, Guille F, Patard JJ, Mhidia A, Ziade J, Manunta A, Lobel B: Ureteral reimplantation on psoas bladder: long term results. Acta Urol Belg. 66:15, 1998.
22. Riedmiller H, Becht E, Hertle L, Jacobi G, Hohenfellner R: Psoas-hitch ureteroneocystostomy: experience with 181 cases. Eur Urol. 10:145, 1984. 23. Staehler G, Schmeller N, Wieland W: Ureteral reimplantation using the psoas bladder-hitch. Experience based on 111 operations in 100 patients. Urol Int. 39:143, 1984.
24. Patil NN, Mottrie A, Sundaram B, Patel VR: Robotic-assisted laparoscopic ureteral reimplantation with psoas hitch: a multi-institutional, multinational evaluation. Urology ; 72:47, 2008.
25. Sagalowsky Al: Early results with split-cuff nipple ureteral reimplants in urinary diversion. J Urol.; 154:2028, 1995.