Parte Generale
1.4 Recenti sviluppi nella ricerca di antagonisti A
2Aselettivi
Numerosi ligandi sono stati sintetizzati e saggiati per la loro affinità ai recettori adenosinici. Per i sottotipi A1 e A2A sono state definite delle SAR abbastanza dettagliate che hanno costituito la comprensione del dominio di legame dei recettori, illustrando le caratteristiche necessarie per un’alta affinità e selettività verso un sottotipo. Queste SAR sono state usate per lo sviluppo di un farmacoforo che descrivesse le caratteristiche di legame dei vari ligandi. Con la scoperta del recettore A3 le SAR sono diventate più complesse da interpretare e molti ligandi già noti sono stati testati anche per questo sottotipo per definire il loro completo profilo di legame. Il recettore A2B non è stato ancora ben caratterizzato per quanto riguarda le SAR. A differenza degli agonisti, gli antagonisti del recettore dell’adenosina sono strutturalmente diversi dall’adenosina. Paragonando le varie classi di composti si osserva che, sebbene essi abbiano strutture diverse, mostrano alcune caratteristiche comuni.
In generale sono strutture: - Planari;
- Aromatiche o ricche di elettroni Π; - Eterocicliche contenenti atomi si azoto. [1]
Gli etero cicli sono per la maggior parte bicicli fusi 6:5 o sistemi triciclici fusi 6:6:5, portanti sostituenti idrofobici. Inoltre gli antagonisti non presentano il residuo di ribosio che è invece essenziale per l’attività agonista.Negli ultimi anni , gli antagonisti A2A si sono dimostrati un importante strumento farmacologico considerando la loro funzione neuro protettiva. In particolare sono collocati nello striato e sono coespressi con i recettori D2 della dopamina. E’ stato abbondantemente riportato che il blocco dei recettori A2A contrasta la catalessi indotta dai recettori della dopamina o dalla deplezione da dopamina, suggerendo che gli antagonisti di tale recettore possano rappresentare un approccio alternativo per il trattamento del Parkinson. In più tali antagonisti sembrano proteggere dalla morte cellulare indotta da ischemia. Così, su questa linea, sono stati studiati
Parte Generale
numerosi composti eterociclici che potrebbero essere classificati come: derivati xantinici e derivati polieterociclici azotati.[29]
1.4.1 Derivati xantinici
I primi antagonisti dell’adenosina riportati in letteratura sono state le xantine naturali: caffeina e teofillina[1], che però mostrano una scarsa affinità e selettività. In seguito sono stati sintetizzati numerosi derivati xantinici, alcuni dei quali si sono dimostrati antagonisti selettivi per i sottotipi A1 e A2A. Il primo derivato xantinico considerato antagonista A2A è stato la 3,7-dimetil-1-propargilxantina, ma era poco attivo. In un programma focalizzato sulle xantine 1, 3 e 8 sostituite, è stata scoperta una famiglia di 8-stiril xantine , che rappresentano il primo esempio di antagonisti selettivi per l’A2A. In particolare la 1,3 dipropil-7-metil-8-(3,4-dimetossi stiril)xantina, (KF17837,3), che era molto potente sul recettore A2A. Altri studi identificarono la 3-clorostirilcaffeina (CSC, 4), che era meno potente della 3 per l’A2A, ma molto selettiva per l’A1. Comunque, problemi come la scarsa solubilità in acqua delle xantine e il fatto che questi composti fotoisomerizzano se esposti alla normale luce in soluzione diluita, ne hanno limitato l’uso farmacologico. Per esempio, il 3, dopo foto isomerizzazione, diventa una miscela stabile del 18% di 3 e 82% di 15. Per superare il problema dell’isomerizzazione, sono stati sintetizzati derivati in cui il gruppo etenil è stato rimpiazzato con gruppi come 1-naftil o ciclopropil, ma il risultato è stato una perdita di potenza e selettività. Due approcci sono stati proposti per aumentare la solubilità in acqua delle xantine: introduzione di gruppi polari sull’anello fenilico, o preparazione di pro farmaci “fosfati”. L’introduzione di un gruppo solfonico in posizione para (10) o meta (11)ha condotto a derivati solubili ma con potenza minore di 20-30 volte. Risultati più interessanti sono stati ottenuti con la preparazione di pro farmaci “fosfato”, come per esempio il profarmaco molto solubile (12) che dopo il taglio da parte delle fosfatasi produce il derivato MSX-2 (13), con alta affinità e selettività per l’ A2A. Questi studi hanno rivalutato le stirilxantine come antagonisti A2A, infatti il composto 14 è stato selezionato per studi clinici di fase 3 per il trattamento del Parkinson. Questo composto mostra un equilibrio stabile E/Z di 19:81 con effetto anti catalettico nei modelli studiati con aloperidolo.
Parte Generale
Sfortunatamente è stato recentemente visto che la foto isomerizzazione si può avere anche allo stato solido, non solo in soluzione diluita, formando la struttura
16. [29]Figura 1.4.1. N N N N O O CH3 CH3 DMPX,1 N N H N H N O H3C0 2 N N N H N O O OCH3 OCH3 (E)-KF17837, 3 N N N N O O H3C CH3 CH3 Cl CSC, 4 N N N N O O CH3 CH3 Br BS-DMPX, 5 N N N N O O CH3 CH3 Cl CS-DMPX,6 N N N H N O O S DMPTX, 7 N N N N O O CH3 CH3 8 N N N N O O CH3 CH3 9 N N N N O O CH3 CH3 SO3K pSS-DMPX, 10 N N N N O O CH3 CH3 SO3K mSS-DMPX, 11 N N N N O O CH3 CH3 OCH3 O P NaO ONa O FOSFATASI N N N N O O CH3 CH3 OCH3 OH Profarmaco, 12 MSX-2, 13 N N N N O O OCH3 OCH3 KW-6002, 14 CH3
Parte Generale N N N N O O CH3 OCH3 OCH3 LUCE N N N N O O CH3 OCH3 OCH3 3, 18% 15, 82% Figura 1.4.2. Isomerizzazione.
1.4.2 DERIVATI AZOTATI
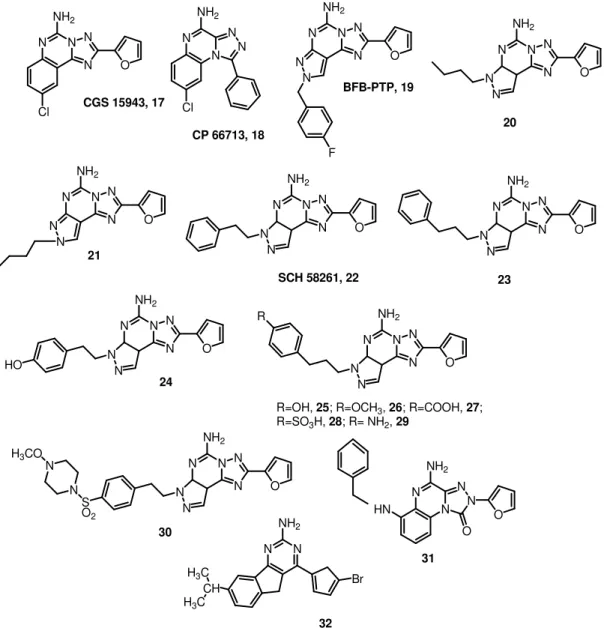
I grandi problemi dei derivati xantinici hanno stimolato gli scienziati a ricercare strutture eterocicliche alternative come “lead compounds”. Sono state studiate molte strutture, come ad esempio i composti CGS 15943 (17) e CP 66,713 (18). Questi derivati, sebbene non selettivi, sono stati il punto da partenza per lo sviluppo di derivati non xantinici quali 8FB-PTP (19) in cui il fenile è sostituito con un pirazolo, che ha mostrato buona affinità per l’A2A sebbene senza selettività. Un importante studio fatto sul nucleo pirazolo-triazolo-pirimidinico ha permesso la determinazione delle importanti caratteristiche strutturali cruciali per una elevata selettività e potenza sull’A2A, come la presenza di un amino gruppo in posizione 5, del furano in posizione 7 e l’influenza dei sostituenti sull’anello pirazolico. La sostituzione del pirazolo con un triazolo permette il mantenimento dell’affinità ma produce perdita completa della selettività. Un’ottimizzazione della
N N N N O O CH3 N N N N O O H3C OCH3 0CH3 OCH3 OCH3 16
Parte Generale
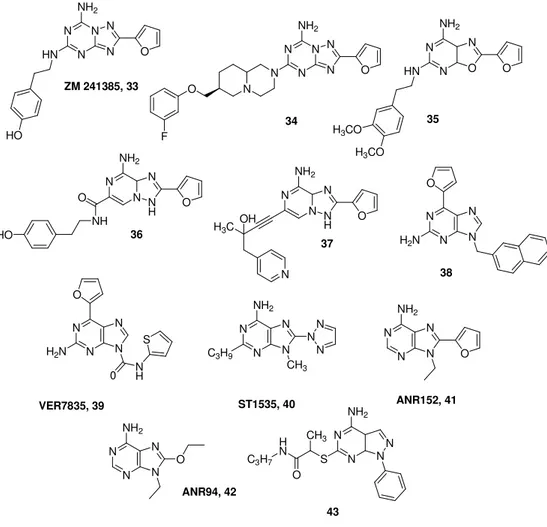
sostituzione sull’N7 ha portato alla scoperta di due composti (22) e (23), che si sono dimostrati i più potenti antagonisti selettivi per l’A2A. La loro scarsa solubilità e biodisponibilità ne ha però limitato l’uso. Sono state quindi apportate varie modifiche del composto 23 nel tentativo di aumentarne la idrofilicità ottenendo quindi i derivati 24 (OH fenolico in para al fenile) e 25 che sono più idrofili e più selettivi e affini. Eccezionalmente, la sostituzione del fenolo con un metossi porta a diminuzione dell’idrofilicità ma comunque consente di conservare la potenza e l’affinità per l’A2A. Visto che l’introduzione di gruppi ossigenati sull’anello fenilico non era sufficiente per conferire adeguata solubilità, sono stati introdotti altri gruppi polari come carbossilici e solfonici (27 e 28), ma con effetto negativo sulla potenza e la selettività. Un gruppo aminico in para aumenta affinità, selettività ma poco la solubilità (29). Un buon equilibrio tra affinità, selettività e solubilità si ha con un gruppo solfonamidico (30) se usato sotto forma di cloridrato. Negli ultimi anni solo due classi di composti triciclici hanno dato risultati interessanti: le trazolo-chinoxaline e le indeno pirimidine. Nella prima classe solo il composto 31 presenta un profilo di legame promettente. Ogni modificazione sul tale nucleo dà riduzione dell’affinità. Contrariamente, le indeno-pirimidine sono una classe molto promettente: in particolare il 32 mostra buona affinità per l’A2A. Comunque le strutture tricicliche presentano numerosi problemi come la scarsa solubilità in acqua e la difficile preparazione. Per superare tali problemi, la ricerca si è orientata su strutture bicicliche. Il primo risultato in tale campo è stato ottenuto col composto denominato ZM 241585 (33), uno dei più potenti antagonisti A2A mai sperimentati, con buona solubilità in acqua. Sono state apportate varie modifiche sulla struttura triazolo-triazinica come quella in posizione 5 e la sintesi dei deaza analoghi triazolo-pirimidine. In particolare il derivato 34 ha mostrato grande potenza e selettività per l’A2A. Altri composti sono le ossazolo pirimidine (35) e le triazolo-pirazine (36), tutti composti che si legano in maniera buona al recettore. Infine, semplici derivati dell’adenina si mostrano promettenti per il legame all’A2A, come i composti ANR152 (41) e ANR94 (42). In questa serie di composti si deve sottolineare che mentre ANR152 era più potente per l’A2A con poca selettività per l’A1, la sostituzione dell’anello furanico con una funzione etossi (42) ha portato a
Parte Generale
diminuzione dell’affinità ma ad aumento della selettività. Entrambi questi composti sono capaci di migliorare i deficit motori della malattia di Parkinson nei modelli di ratto.[29] N N N N Cl NH2 O CGS 15943, 17 N N N N NH2 Cl N N N N NH2 O N N F BFB-PTP, 19 CP 66713, 18 N N N N NH2 O N N 20 N N N N NH2 O N N 21 N N N N NH2 O N N SCH 58261, 22 N N N N NH2 O N N 23 N N N N NH2 O N N HO 24 N N N N NH2 O N N R
R=OH, 25; R=OCH3, 26; R=COOH, 27;
R=SO3H, 28; R= NH2, 29 N N N N NH2 O N N S O2 N N H3CO 30 N N N N O O NH2 HN 31 N N NH2 CH H3C H3C Br 32
Parte Generale N N N N N NH2 HN O HO N N N N N NH2 O N N O F 34 N N O N NH2 O 35 HN H3CO H3CO N N N H N NH2 O O NH HO 36 N N N H N NH2 O H3C OH N 37 N N N N H2N O 38 N N N N N H H2N O 0 S N N N N NH2 CH3 N N N C3H9 N N N N NH2 O N N N N NH2 O ANR94, 42 N N N N S CH3 O H N C3H7 43 ZM 241385, 33 VER7835, 39 ST1535, 40 ANR152, 41 NH2
Figura 1.4.4. Derivati biciclici.
Per quanto riguarda l’applicazione terapeutica degli antagonisti A2A nel trattamento del morbo di Parkinson, il composto più promettente di questa serie di molecole è rappresentato da KW6002 (Istradefillina, 14). Questo composto è ora in studi clinici di fase III. Altri composti attualmente in fase di studio sono V2006, e vari analoghi di SCH58261 (22), che sono invece in fase II. Potremmo dire che attualmente KW6002 sia il candidato più vantaggioso come agente anti Parkinson, ma se alcuni composti emergenti potessero essere utili in monoterapia e non in combinazione con la dopamina (come KW6002), dovrebbero in questo senso aprirsi nuove frontiere. In più è stato dimostrato che gli effetti neuro protettivi degli antagonisti A2A non sono ristretti ai neuroni dopaminergici. Infatti tali antagonisti producano effetti benefici sui neuroni di ratto in termini di
Parte Generale
sopravvivenza cellulare, in particolare nella corteccia cerebrale, anche se il meccanismo implicato è poco chiaro. Comunque, se la strategia della sintesi dei derivati non xantinici sembri risolvere problemi relativi all’affinità e alla selettività recettoriale, ancora lavoro è necessario per ottenere composti con struttura più semplice e con proprietà chimico-fisiche drug like come la solubilità in acqua. [29 ]
N
N
N
N
O
O
OCH
3OCH
3CH
3 KW6002 (14): ISTRADEFILLINA1.4.3 Requisiti di legame degli antagonisti
Come è stato dimostrato, il legame degli antagonisti A2A con il recettore consiste essenzialmente in interazioni idrofobiche. E’ stato usato come modello il composto CGS15943 (17), potente e non selettivo antagonista.
N
N
N
N
Cl
NH
2O
CGS 15943, 17
Parte Generale
Secondo gli studi di molecular modeling, l’interazione col ligando avviene a livello di larghe tasche idrofobiche che consistono soprattutto nei domini trans membrana (TMs) 3, 6, e 7. Gli aminoacidi idrofobici che partecipano a questa interazione col ligando sono Leu85, Ile135, Leu167, Phe 168, Phe 182, Val 186, Trp 246 e Leu 249 vicino all’anello chinazolinico e l’Ile 80,Val 84 e Ile 274 in prossimità dell’anello furanico. Un’importante interazione idrofila è invece il legame a idrogeno formato tra l’amino gruppo esociclico in posizione 5 e Asp 253 (TMS 6). Un addizionale legame a idrogeno debole tra la catena laterale di Asn 181 e N6 del CGS15943 aumenta la stabilità del complesso. Un altro modello interessante risulta dallo studio dell’interazione tra il recettore e una serie di composti pirazolo-triazolo-pirimidinici. In particolare, l’aggiunta del gruppo 4-amminofenilpropilico in posizione N7 del nucleo ha dato vita ad un antagonista molto selettivo per l’A2A (Ki= 0,22nM), che non interagisce significativamente con l’A2B i l’A3. Le SAR derivate da questo composto indicano che risultano essenziali per la selettività e l’affinità per l’A2A:
La struttura triciclica pirazolotriazolopirimidinica; - La presenza dell’anello furanico;
- Il 5 amino gruppo esociclico;
- Il sostituente arilalchilico sull’azoto in 7.
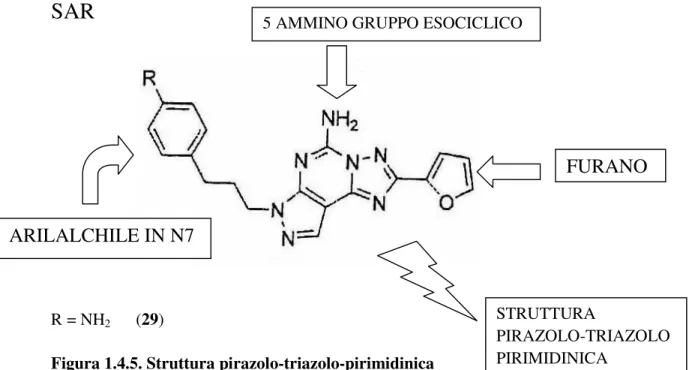
Altre interazioni idrofobiche tra la parte 4-aminofenilpropilica e le tasche idrofobiche TM4 e TM5 e il legame a idrogeno tra l’amino gruppo in 4 e l’Asn 145 potrebbero contribuire ad aumentare l’affinità per l’A2A. La sequenza di allineamento del recettore ha indicato che la maggior parte degli aminoacidi nel presunto sito di legame con l’antagonista 29 è conservata tra i vari recettori adenosinici. Anche se gli aminoacidi collocati vicino alle posizioni N5, N7, N8 della triazolo pirimidina può variare. In particolare gli aminoacidi idrofili come Leu167 e His 250 (Gln167 e Ser 247 nel sottotipo A3). Dall’altro lato le ingombranti e idrofobiche catene delle Leu 167 e His 250 sembrano accomodare un 5 amino gruppo non sostituito. I requisiti di legame della struttura pirazolotriazolopirimidinica sono schematizzati in Figura 1.4.5.
Parte Generale
SAR
R = NH2 (29)
Figura 1.4.5. Struttura pirazolo-triazolo-pirimidinica
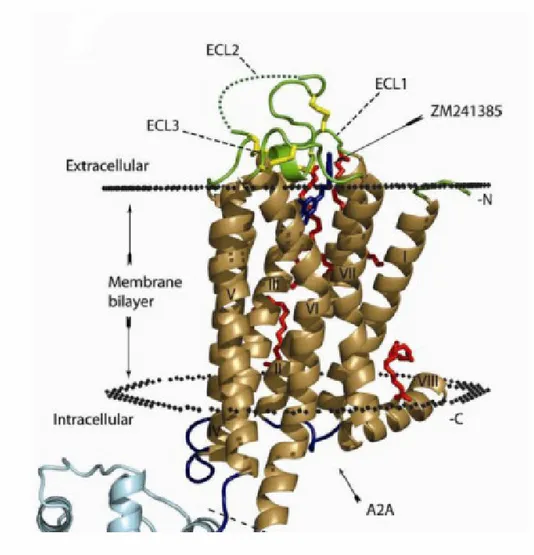
E’ stato recentemente descritto lo studio cristallografico del recettore dell’adenosina A2A umano complessato con un antagonista altamente selettivo, ZM241385 (33), ad una risoluzione di 2.6 Å. Le eliche transmembrana del recettore che interagiscono con la molecola sono ECL2 e 3. L’antagonista si posiziona co-linearmente rispetto alle eliche transmembrana V, VI e VII, e la cavità di legame risulta allungata all’ECL3 e i terminali ad elica dei TMVI e VII. La Phe 268 dell’ECL2 forma varie interazioni idrofobiche con la struttura biciclica dello ZM241385. Il Trp 246 che stabilizza il legame con l’antagonista si trova a distanza di circa 3 Å dall’anello furanico. Inoltre vi sono un’interazione idrofobica con Ile 274 e un legame a idrogeno con Asn 253. Adiacente alla Phe 168 abbiamo un residuo polare (GLu 169) che interagisce con il gruppo aminco esociclico (N15). Il sito di legame include anche quattro molecole di acqua.[30] Lo studio cristallografico del recettore A2A dell’adenosina è rappresentato in Figura 1.4.6.
FURANO
5 AMMINO GRUPPO ESOCICLICO
ARILALCHILE IN N7
STRUTTURA
PIRAZOLO-TRIAZOLO PIRIMIDINICA
Parte Generale
Figura 1.4.6. Struttura cristallografica del recettore A2A dell’adenosina