Introduzione alla
Parte
24 Negli ultimi anni il gruppo di ricerca presso il quale è stato svolto questo lavoro di tesi ha intrapreso lo studio di ligandi alla Proteina Traslocatrice (TSPO).
Come abbiamo già ampiamente descritto nella parte generale il TSPO, grazie alla sua prima localizzazione mitocondriale, riveste un ruolo importante sia nella regolazione della proliferazione cellulare e dell’apoptosi , che nella biosintesi degli steroidi. Il TSPO risulta quindi essere un target promettente per lo sviluppo di nuovi strumenti terapeutici per il trattamento clinico di numerosi disordini quali tumori, malattie neurodegenerative , autoimmuni ed infettive, tutte patologie correlate ad un alterato equilibrio dei processi vita/morte cellulari . In particolare , un incremento della morte cellulare caratterizza patologie acute quali l’infarto, AIDS, disturbi epatici, così come le patologie neurodegenerative . Al contrario, una ridotta capacità delle cellule di andare incontro ad apoptosi può portare all’accumulo di cellule anomale , caratteristico sia dei tumori che delle malattie autoimmuni.
Per quanto riguarda invece l’azione stereoidogenica , le evidenze di una iperespressione del TSPO e delle proteine stereoidogeniche associate in seguito ad un danno traumatico nel cervello e nel midollo spinale, insieme ad un aumento locale del livello di steroidi, suggerisce che tale recettore possa giocare un ruolo neuroprotettivo mediato dalla neurosteroidogenesi. Tra le patologie che implicano una alterazione dei livelli di alcuni specifici neurosteroidi possiamo ricordare i disturbi correlati allo stress , la depressione e le malattie neurodegenerative.
Di conseguenza, l’identificazione di nuovi specifici ligandi per il TSPO risulta di grande importanza al fine di caratterizzare i potenziali ruoli farmacologici e terapeutici di tale recettore.
L’espressione basale di questo recettore risulta infatti alterata in vari disturbi : una down-regulation si osserva in condizioni di stress cronico o ripetuto ed in molti disturbi psichiatrici. Al contrario il TSPO è up-regolato in una serie di neuropatologie che includono i gliomi, i disturbi neurodegenerativi , quali l’Alzheimer, così come in varie forme di danno celebrale e di infiammazione . Una densità particolarmente elevata di tale recettore si osserva nei tessuti neoplastici. Il TSPO potrebbe così rappresentare un marker sensibile e specifico di alterazioni patologiche , oltre che un mezzo diagnostico dello stato e progressione della patologia, incoraggiando le ricerche verso lo sviluppo di nuovi ligandi del TSPO quali strumenti adatti per tecniche di imaging molecolare.
Riferendoci al modello farmacoforico ipotizzato per tale proteina recettoriale, abbiamo studiato l’interazione di nuovi ligandi con la tasca lipofila L1, introducendo infatti sull’indolo in posizione in 2, sia un gruppo eterociclico aromatico quale il tiofene (V) , che gruppi più ingombranti di tipo bifenilico (III) e naftilico (IV) come indicato in Figura 8.
La progettazione di tali ligandi è stata realizzata sulla base della struttura delle N,N-2-fenilindol-3-gliossilamidi
I
una nuova classe di ligandi per il TSPO descritti recentemente da questo gruppo di ricerca .[7,8]26
I
Come abbiamo già descritto precedentemente, il legame dei derivati 2-fenilindolgliossilamidici
I
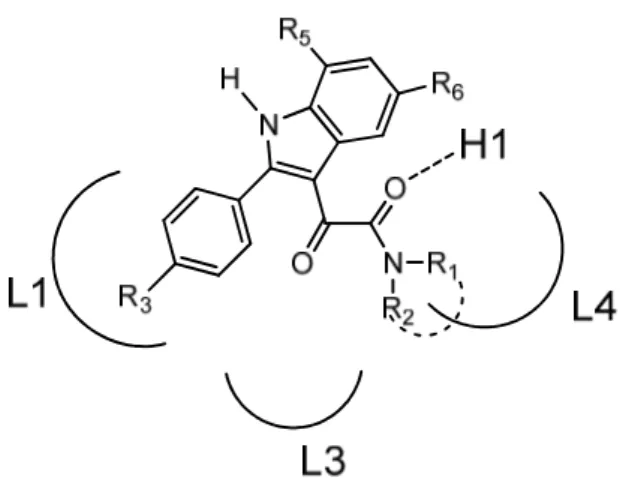
con il recettore dovrebbe avvenire mediante quattro interazioni fondamentali :(i) il fenile in posizione 2 che occupa l’area lipofila L1 ;
(ii) i sostituenti alchilici R1 e R2 che interagiscono rispettivamente
con le aree lipofile L4 e L3 ;
(iii) il carbonile amidico che funziona da accettore nella formazione di un legame ad idrogeno con il sito H1. [7] (
Figura 7
)
Figura 7. Interazione dei derivati 2-fenilindolgliossilamidici con il
Inoltre per meglio valutare l’affinità di legame dei ligandi 2-arilindolgliossilamidici con le tasche L3 ed L4 del recettore, abbiamo sostituito R1 ed R2 con catene alifatiche simmetrichee
asimmetriche. N O O N R1 R2 H S V III I IV
Figura 8. Interazione dei gruppi più ingombranti con la tasca L1 La procedura generale di sintesi utilizzata nella preparazione delle
N,N-dialchil-2-naftilindol-3-ilgliossilamidi 25-32 e N,N-dialchil- 2-bifenilindol-3-ilgliossilamidi 33-36 è mostrato nello SCHEMA 1.
SCHEMA 1
Ar = Naftile (21),Bifenile (22) R1 = CH3, CH2CH3, (CH2)2CH3,(CH2)3CH3 ,(CH2)5CH3
R2 =(CH2)2CH3, (CH2)3CH3, (CH2)4CH3, (CH2)5CH3 , CH2C6H5
I composti commercialmente disponibili naftilindolo 21 e 2-bifenilindolo 22, vengono acetilati con cloruro di ossalile in etere dietilico anidro, a temperatura ambiente per ottenere i cloruri indolgliossalilici corrispondenti 23-24, successivamente condensati con le appropiate ammine, in presenza di trietilammina , in toluene anidro, per ottenere derivati 25-36. Le rese di reazione, le costanti chimico-fisiche e le caratteristiche spettroscopiche dei composti 25-36 sono
indicati nella Tabella 2. Per meglio valutare l’affinità di legame
di derivati di nuova sintesi per il TSPO abbiamo inoltre introdotto in posizione 2 un anello tiofenico.
Nel caso dei derivati tiofenidolilici la sintesi è rappresentata nello SCHEMA 2 .
SCHEMA 2
R1=R2 (CH2)2CH3 ; (CH2)3CH3
La procedura generale di sintesi utilizzata nella preparazione dei derivati N,N-dialchil-2-tienilindol-3ilgliossilamidici prevede la formazione dell’indolo (37), attraverso la reazione di Fischer tra fenilidrazina cloridrato e acetiltiofene. La successiva acetilazione a 0°C con cloruro di ossalile in Et2O anidro porta alla
formazione del cloruro acilico corrispondente 38 . Infine il derivato 38 viene condensato in presenza di NEt 3 con l’ammina
dipropilica e dibutilica ottenendo i corrispondenti derivati 39-40.
29