Capitolo 1
Tomografia Ottica
1.1 Proprietà ottiche dei tessuti
In tomografia ottica (OT), le immagini delle proprietà ottiche del mezzo sono ricostruite a partire da misure della luce infrarossa che incide sul contorno dell’oggetto.
Assorbimento e scattering sono i due fenomeni fisici che influiscono sulla propagazione della luce nei tessuti biologici; benché entrambi siano importanti, lo scattering è il meccanismo dominante [Cheong 1990]. Anche per sezioni sub-millimetriche di tessuto, i fotoni iniettati vengono scatterati molte volte prima di raggiungere il bordo. Come conseguenza, un fascio laser collimato e coerente in ingresso sarà in effetti incoerente ed isotropico dopo aver attraversato pochi millimetri di tessuto. L’assorbimento, e in più piccola misura anche lo scattering, dipendono dalla lunghezza d’onda. In più, la concentrazione di alcuni cromofori varia nel tempo, riflettendo le variazioni fisiologiche nel tessuto. Ancor più importante, il profilo di assorbimento dipende dallo stato di ossigenazione dell’emoglobina. L’indice di rifrazione varia molto poco su scala macroscopica ed è tipicamente intorno a 1.40 per molte tipologie di tessuto [Bolin 1989]. Gli indici di rifrazione dei singoli costituenti varia da 1.33 per l’acqua a circa 1.55 per il grasso e una soluzione concentrata di proteine [Bennett 1951].
Assorbimento: Il coefficiente di assorbimento,
µ
a(in mm-1), può essere ricavato dalla seguente equazionedove dI è la variazione differenziale di intensità I del fascio di luce collimata che attraversa una traiettoria infinitesima dx in un mezzo omogeneo con coefficiente di assorbimento
µ
a. L’integrazione su uno spessore x fornisce: 0ax
I
=
I e
−µIl coefficiente di assorbimento può anche essere espresso in termini di densità delle particelle ρ e sezione trasversale di assorbimento
σ
a comeµ
a=
ρσ
aDa cui si ottiene la legge di Lambert-Beer 0
ax
I
=
I e
−ρσIl rapporto 1/
µ
a è chiamato lunghezza della traiettoria di assorbimento ed è uguale alla media della traiettoria libera che un fotone percorre tra eventi consecutivi di assorbimento. La trasmissione T è definita come il rapporto tra intensità trasmessa e intensità incidente0
I
T
I
=
e l’attenuazione, o densità ottica (OD) di un mezzo attenuante è data da
10 10 0
1
log (
)
log
I
OD
T
I
=
= −
o ancheOD
=
log ( )
10e
⋅
µ
ax
=
α
cx
Scattering : Lo scattering è un fenomeno in cui la direzione della radiazione varia
all’interno del mezzo. La nuova direzione della radiazione dipende dalle proprietà dello scatteratore e dalla direzione iniziale della radiazione. Come per l’assorbimento, si può definire un coefficiente di scattering
µ
s (espresso in mm-1) per una sorgente collimata, ricavandolo dalla seguente equazione 0sx
I
=
I e
−µdove I è la componente non scatterata della luce dopo aver attraversato un campione non-assorbente di spessore x. Il coefficiente di scattering in termini di densità delle particelle ρ e di sezione trasversale di scattering
σ
sèµ
s=
ρσ
sLa lunghezza della traiettoria di scattering ,1/
µ
s, è la distanza media che un fotone percorre tra due eventi di scattering consecutivi e la quantitàµ
sx è lo spessoreottico(adimensionale) di un campione espresso in termini di lunghezza della traiettoria di
scattering.
Quando un fotone, incidente lungo una direzione descritta dal vettore unitario e subisce s
un evento di scattering, la probabilità angolare di essere scatterato nella direzione es' è data
dalla funzione di fase normalizzata f e e( ,s s'). Per i tessuti molli si può assumere che la distribuzione di probabilità è solo una funzione dell’angolo tra il fotone incidente e quello scatterato, e non dipende dall’angolo di incidenza relativo allo scatter. Quindi la funzione di fase può essere convenientemente espressa come una funzione del coseno dell’angolo di scattering
f e e
(
s⋅
s')
=
f
cos( )
θ
Una teoria sviluppata da [Mie 1908] permette di derivare le soluzioni analitiche della funzione di fase per lo scattering di un’onda elettromagnetica piana formata da particelle sferiche di ogni dimensione. Si noti che nel limite dove la dimensione dello scatter è minore della lunghezza d’onda del fotone incidente, la teoria di Mie può essere approssimata dalla teoria di Rayleigh dello scattering [Rayleigh 1871].
L’anisotropia può essere caratterizzata in termini di coseno medio dell’angolo di scattering, chiamato fattore di anisotropia g:
1
1
cos
(cos ) cos
g
θ
f
θ
d
θ
−
=
∫
I casi limite sono g =0 per scattering perfettamente isotropico, e g =1 per scattering in avanti completo dell’onda incidente. I tessuti biologici nel range di lunghezza d’onda del vicino infrarosso sono fortemente scatterati, con fattori di anisotropia tipicamente nel range 0.69≤ ≤g 0.99 [Cheong 1990]. Il coefficiente di scattering di trasporto (o ridotto),
'
s
µ , è definito come
µ
s'=
µ
s(1
−
g
)
Questa quantità può essere interpretata come rappresentante il coefficiente di scattering isotropico equivalente ed è un parametro fondamentale nella teoria della diffusione della propagazione della luce attraverso mezzi casuali. La traiettoria media percorsa da un fascio collimato di luce prima che esso diventi effettivamente isotropico è data da 1/ '
s
Combinando assorbimento e scattering, si può definire un coefficiente di attenuazione
totale
µ µ µ
t=
s+
aDove 1/µt è solitamente riferito alla traiettoria media libera tra un evento di scattering o un evento di assorbimento.
Per analogia, il coefficiente di attenuazione di trasporto, µtr, è definito come
µ
tr=
µ
a+
µ
s(1
−
g
)
=
µ
a+
µ
s'Una terza quantità che influisce sulla propagazione della luce all’interno del mezzo è l’indice di rifrazione nin che corrisponde al rapporto tra la velocità della luce nel vuoto e
nel mezzo.Variazioni nell’indice di rifrazione tra materiali diversi può causare effetti di riflessione e rifrazione a livello delle interfacce tra i materiali. Nella maggior parte delle applicazioni di tomografia ottica, l’indice di rifrazione viene assunto costante all’interno del mezzo.
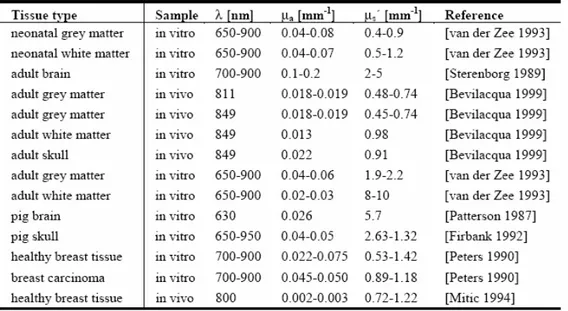
Nella maggior parte dei tessuti, la propagazione della luce è dominata dallo scattering. Come risultato di questa proprietà, dopo aver attraversato pochi millimetri, la propagazione della luce nei tessuti può essere descritta come un processo diffusivo. Diverse tipologie di tessuto hanno diverse proprietà di scattering e di assorbimento, come mostrato in tabella 1.1.
Benché per i materiali biologici il coefficiente di scattering sia generalmente più grande del coefficiente di assorbimento, la maggior parte delle informazioni di interesse per la tomografia ottica sono riferite all’assorbimento. I maggiori costituenti del tessuto biologico che contribuiscono all’assorbimento nel vicino infrarosso sono acqua, lipidi ed emoglobina. Mentre i primi due rimangono circa costanti su brevi scale temporali, le concentrazioni di ossi e deossiemoglobina variano insieme alla funzione e al metabolismo del tessuto. Cioè le variazioni corrispondenti nell’assorbimento possono fornire utili informazioni cliniche fisiologiche.
Tab. 1.1 Proprietà ottiche di varie tipologie di tessuti
1. 2 Tecniche sperimentali
I dispositivi sperimentali utilizzati in tomografia ottica possono essere divisi in tre classi: sistemi che lavorano ad onda continua (Continuous wave), i sistemi che lavorano nel dominio della frequenza (Frequency domain) e quelli che lavorano nel dominio del tempo (Time domain). In tutti questi sistemi, l’idea base per l’acquisizione dei dati è la stessa. Il design del dispositivo comprende un set di sorgenti di luce e un set di rivelatori collocati intorno all’oggettoΩ . Un’illustrazione bidimensionale di una tipica situazione di misura OT è mostrata in fig.1.1, dove m sorgenti sono posizionate in εi, j=1,...,m ed m rivelatori sono
posizionati in ςk,k=1,...,m. Dapprima la luce proveniente da una sorgente laser ad infrarossi è guidata all’interno dell’oggetto usando una delle sorgenti in εi, e la luce trasmessa viene misurata utilizzando rivelatori sensibili alla luce in ςk,k =1,...,m. Quindi il processo di misura viene ripetuto per tutte le posizioni m delle sorgenti.
Fig. 1.1 Design di un dispositivo OT. Le sorgenti ed i ricevitori sono posizioni sul bordo dell’oggetto [Tarvainen 2006].
SISTEMI CONTINUOUS WAVE
Gli strumenti che lavorano ad onda continua utilizzano sorgenti di luce di intensità costante e misurano l’intensità (Γ =ω 0)della luce trasmessa in corrispondenza dei siti di misura, in corrente continua. Molti sistemi continuous wave sono stati sviluppati per la tomografia ottica [ Colak 1999, Piao 2005, Schmitz 2005]. Nonostante ciò, si conoscono alcuni svantaggi relativi all’imaging continuous wave. In primo luogo, le misure di intensità risultano essere sensibili alle proprietà ottiche dei tessuti vicino alla superficie e agli effetti di accoppiamento sulla superficie piuttosto che alle proprietà ottiche più profonde all’interno del tessuto [Gibson 2005].
Secondariamente, gli effetti di assorbimento e scattering non possono essere distinti solo sulla base di misure di intensità [Arridge 1998]. Perciò, le misure continuous wave sono utilizzate di solito per l’imaging differenziale, dove la ricostruzione viene ottenuta utilizzando la differenza tra i dati misurati e i dati relativi a misure di riferimento. Il punto di forza dei dispositivi di imaging continuous wave è la velocità nell’acquisizione dei dati che permette una risoluzione temporale veloce per l’imaging [Schmitz 2002, Piao 2005]. In seguito sono discussi gli altri due sistemi di misura, i sistemi che lavorano nel dominio della frequenza ed i sistemi che lavorano nel dominio del tempo. Entrambi questi sistemi di misura sono in grado di produrre un maggior numero di informazioni rispetto al sistema
continuous wave, perciò le distribuzioni di assorbimento e di scattering possono essere
SISTEMI NEL DOMINIO DELLA FREQUENZA
Nei sistemi che lavorano nel dominio della frequenza, viene utilizzata una sorgente, modulata in ampiezza ad alta frequenza (qualche centinaia di MHz) e vengono misurati l’attenuazione dell’ampiezza e la variazione di fase della luce trasmessa. Un diagramma del comportamento temporale della luce trasmessa ( )Γ ω durante una misura nel dominio della frequenza è illustrato in fig.1.2. La figura mostra un segnale in ingresso modulato in intensità nell’immagine di sinistra, e un segnale misurato che risulta attenuato e variato in fase nell’immagine di destra. Sono stati sviluppati ed apprezzati diversi sistemi che lavorano nel dominio della frequenza [Franceschini 1997, Everdell 2005, McBride 2001, Nissilä 2005, Pogue 1997]. I dispositivi che lavorano nel dominio della frequenza sono relativamente economici, facili da sviluppare e da utilizzare, e possono fornire un campionamento temporale relativamente veloce.
Le tipologie di dati che si ottengono da una misura nel dominio del tempo sono: l’ampiezza Γ( )
ω
e la variazione di fase arg(
Γ( )
ω
)
di una misura complessa Γ( )ω . In molti casi, la ricostruzione viene implementata utilizzando il logaritmo dell’ampiezza logΓ( )ω
e i dati relativi alla variazione di fase. In alternativa, possono anche venire utilizzate la parti reale ed immaginaria della misura, rispettivamente Re( ( ))Γω eIm( ( ))Γω .
SISTEMI NEL DOMINIO DEL TEMPO
Nei sistemi che lavorano nel dominio del tempo (time-resolved), viene fornito come ingresso un impulso di luce di breve durata ( qualche picosecondo), e viene misurata la distribuzione temporale Γ( )t dei fotoni trasmessi [Schmidt 2000, Hebden and Harridge 1997]. Questa distribuzione temporale è conosciuta come la temporal point spread
function (TPSF) [Delpy 1988, Patterson 1989]. Un diagramma dell’andamento temporale
del segnale di luce trasmessa ( )Γ t durante una misura nel dominio del tempo è illustrato nella riga finale della fig.1.2. La figura mostra la pulsazione di luce in ingresso nell’immagine di sinistra e la TPSF trasmessa nell’immagine di destra. Diversi sistemi che lavorano nel dominio del tempo sono stati sviluppati e apprezzati [ Eda 1999, Grosenick 1999, Hebden 1991, Pifferi 2003, Schmidt 2000]. Nei sistemi nel dominio del tempo, i tempi di misura sono solitamente più lunghi rispetto ai sistemi nel dominio della
frequenza. Per contro, i sistemi nel dominio del tempo offrono misure altamente sensibili, anche attraverso grandi spessori di tessuto.
Fig.1.2 Diagramma dell’andamento temporale della luce trasmessa durante una misura di tomografia ottica. In
alto ci sono i segnali in ingresso (immagine di sinistra) e in uscita (immagine di destra) della misura nel dominio della frequenza, mentre in basso ci sono i segnali in ingresso (immagine di sinistra) e in uscita (immagine di
destra) della misura nel dominio del tempo[Tarvainen 2006].
Benché la TPSF possa essere usata direttamente per la ricostruzione, solitamente vengono derivate poche tipologie di dati da ( )Γ t . Alcuni esempi di queste tipologie di dati sono [Schweiger 1997]:
intensità integrata : 0
( )
E
= Γ
∫
∞t dt
(1.1) intensità time-gated : 0( )
T( )
E T
= Γ
∫
t dt
(1.2)momento temporale n-esimo : 1
0
( )
n n
momento centrale n-esimo : 1
0
(
)
( )
n n
c
=
E
−∫
t
−
t
Γ
t dt
(1.4)trasformata di Laplace normalizzata : 1
0
( )
st( )
L s
=
E
−∫
∞e
−Γ
t dt
(1.5) trasformata di Mellin-Laplace : 1 0( )
n st( )
nML s
=
E
−∫
∞t e
−Γ
t dt
(1.6)CONFRONTO TRA GLI APPROCCI
Sono valide alcune relazioni tra i dati misurati con le diverse modalità. La relazione più importante è tra le misure nel dominio del tempo e le misure nel dominio della frequenza, che sono correlate attraverso la trasformata di Fourier
0
( )
ω
∞( )
t e
−i tωdt
Γ
= Γ
∫
(1.7)Infatti, in alcuni casi, il sistema che lavora nel dominio del tempo è utilizzato per ottenere le misure, mentre i dati nel dominio del tempo a diverse frequenze, ottenute dai dati nel tempo con la trasformata di Fourier, sono utilizzati per la ricostruzione. Si noti, inoltre, che l’intensità DC misurata corrisponde all’intensità integrata definita nell’equazione (1.1), cioè (Γ = =ω 0) E. I parametri nel dominio del tempo e nel dominio della frequenza e la loro dipendenza sono discussi in maniera più dettagliata in [Arridge 1992 ].
E’ tuttora in studio la questione della sensibilità dei diversi schemi di misura e la scelta dei dati di misura più adatti per la ricostruzione delle immagini, anche se le performance dei diversi sistemi di misura sono state sondate solo in studi recenti [Nissilä 2007]. In [Nissilä 2007], le performance dei dispositivi nel dominio del tempo e nel dominio della frequenza sono state studiate mettendo a confronto sia la qualità dei dati relativi all’ampiezza e alla fase, sia i risultati ottenuti con la ricostruzione delle immagini. In più, viene proposto un protocollo per la valutazione delle performance degli strumenti di migrazione dei fotoni e vengono apprezzati, in particolare, otto sistemi che lavorano nel dominio del tempo e in continuous wave, proprio in accordo con questo protocollo [Pifferi 2005].
1.3 Applicazioni
Durante gli ultimi dieci anni, la tomografia ottica si è sviluppata molto velocemente da tecniche sperimentali di laboratorio in una modalità di imaging che è testata per una varietà di applicazioni. Allo stato attuale, la tomografia ottica è in costante sviluppo e nuove tecniche sperimentali, così come nuovi approcci modellistici, sono costantemente elaborati e riconosciuti.
Ci sono molte ragioni che favoriscono la tomografia ottica come modalità di imaging. In primo luogo, i metodi ottici sono in grado di produrre informazioni sull’ossigenazione e sul volume del sangue nei tessuti, in modo che si possano differenziare tra loro i tessuti molli. In più, è possibile fornire informazioni addizionali circa il tessuto bersaglio con la tomografia ottica. In secondo luogo, la procedura di misura è non invasiva e la radiazione è non ionizzante, perciò la tecnica è sicura per il paziente. In terzo luogo, la strumentazione è relativamente poco costosa e facilmente trasportabile; ciò rende possibile usare questa tecnica per diagnosi in ambulatorio e monitoraggio continuo del paziente. Un fattore limitante nella tomografia ottica è la veloce attenuazione della luce nel mezzo.
1.3.1 Imaging del seno
Negli ultimi anni la diagnostica ottica del tumore al seno ha attratto l’interesse di numerosi gruppi di ricerca per le caratteristiche non invasive e la possibilità di ottenere informazioni funzionali, complementari a quelle radiografiche. I principali componenti del tessuto mammario, quali il sangue, i lipidi e l’acqua, presentano un diverso assorbimento della luce nell’intervallo spettrale da 600 nm a 1000 nm (visibile e vicino infrarosso) ed è quindi possibile, in linea di principio, evidenziare strutture del seno con diversa composizione sulla base delle loro differenti proprietà di assorbimento della luce. Lo svantaggio della tomografia ottica è che la sua risoluzione spaziale è relativamente povera se messa a confronto con la mammografia a raggi X, che è, ad oggi, il metodo più comune per l’imaging del seno. Nonostante ciò, la tomografia ottica presenta alcuni vantaggi rispetto alla tomografia a raggi X: la radiazione è non ionizzante, perciò il paziente non è sottoposto ad alcuna radiazione nociva; inoltre, la tomografia ottica non richiede la
compressione del seno che risulta fastidiosa e, in molti casi, dolorosa per la paziente. In più, a differenza della tomografia a raggi X, la sensibilità della tomografia ottica per le donne più giovani è buona come per le donne più anziane.
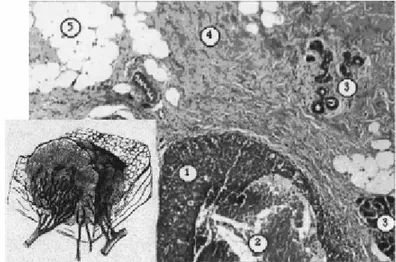
Fig. 1.3 Sezione di un carcinoma al seno, che mette in risalto l’alta eterogeneità del tessuto. Le cellule maligne
sono confinate ai canali (1). Si nota una regione di cellule necrotiche (2). Sono mostrati i lobuli normali (3), lo stroma fibroso (4) e le regioni adipose (5). Nel riquadro sulla sinistra viene mostrata la vascolarizzazione delle
zone cancerose; queste regioni risultano altamente assorbenti [Colak 1999].
In tomografia ottica, sono stati sperimentati un certo numero di approcci per l’imaging del seno. Molti studi clinici sono stati realizzati usando strumenti che comprimono il seno [Durduran 2002, Franceschini 1997]. Questo approccio riduce l’attenuazione della luce trasmessa ed assicura che la geometria in esame sia nota. Lo svantaggio della tecnica di compressione è che, benché la compressione sia più delicata che nella mammografia a raggi X, causa variazioni nelle proprietà ottiche del tessuto del seno. La geometria del seno compresso è stato utilizzato per studiare le proprietà ottiche della composizione del tessuto del seno. La stessa geometria è stata utilizzata anche per scannerizzare il seno in modo da produrre immagini delle proiezioni e da determinare le proprietà ottiche del tumore [Fantini 1998, Grosenick 2004, Spinelli 2005].
Una tecnica ideale per generare immagini tridimensionali del seno è circondare il seno con sorgenti e rivelatori [McBride 2001, Pogue 1997, Schmitz 2005, Yates 2005]. Lo svantaggio di questo approccio è che la distanza che la luce deve percorrere è più lunga e le intensità rivelate della luce sono più basse rispetto alla geometria
composizione del tessuto mammario. Inoltre, sono state ottenute ricostruzioni complete tridimensionali delle proprietà ottiche del seno di pazienti affette dal tumore al seno [Pogue 2004, Yates 2005]. Misure sul seno sono state inoltre ottenute con una tanica emisferica riempita di un fluido simile al tessuto con le sorgenti e i rivelatori localizzati sui bordi della tanica [Colak 1999, Yates 2005]. Tale tanica, riempita con il fluido, ha alcuni benefici rispetto agli altri approcci, per esempio le coppe possono alloggiare un gran numero di taglie di seno, l’accoppiamento delle sorgenti e dei rivelatori è costante e indipendente dal soggetto, e la geometria esterna del volume soggetto ad imaging è nota esattamente.
Fig. 1.4 Sulla sinistra, il prototipo del sistema mammografico a coppa. La freccia indica l’alloggiamento della
coppa, mostrata sulla destra. Si possono vedere le estremità di alcune fibre di sorgenti e ricevitori all’interno della coppa. La luce rossa divergente proviene da una delle fibre sorgenti che emettono a circa 670 nm
[Colak 1999].
Occorre tenere conto, tuttavia, che la struttura dei tessuti causa una forte diffusione della luce ed una semplice misura dell’attenuazione è influenzata sia dall’assorbimento che dalla diffusione e non è quindi possibile discriminare l’effetto dei due eventi. Per misurare simultaneamente i coefficienti di assorbimento e diffusione è stata sviluppata una tecnica innovativa di trasmittanza risolta nel tempo. Essa si basa sulla misura della distribuzione temporale dei fotoni trasmessi dal tessuto in seguito all’immissione di un impulso laser di breve durata. La forma della distribuzione temporale della luce trasmessa dipende dalle proprietà ottiche (assorbimento e diffusione) del mezzo attraversato, alle quali si può quindi risalire.
L’assorbimento fornisce poi informazioni sulla composizione del tessuto e la diffusione sugli aspetti strutturali. La diagnostica clinica si basa dunque sulla possibilità i evidenziare un tumore a fronte di differenti proprietà ottiche del tessuto neoplastico rispetto a quello sano. Utilizzando questa metodica operante nel dominio del tempo sono stati sviluppati, a Milano e a Berlino (Physikalisch-Technische Bundesanstalt), i due primi prototipi clinici. Questi strumenti sono attualmente in fase di sperimentazione clinica all’interno di un trial multicentrico, nell’ambito del progetto europeo OPTIMAMM. Lo strumento di Milano (MAMMOT; MAMMOgraph for Optical Tomography) è stato realizzato nell’ambito di una consolidata collaborazione tra il personale della Sezione Politecnico di Milano dell’Istituto di Fotonica e Nanotecnologie del CNR e quello del Dipartimento di Fisica del Politecnico di Milano. La mammella è debolmente compressa tra due piatti di Plexiglass e l’immagine mammografia viene ottenuta con due fibre ottiche coassiali (una di iniezione e l’altra di raccolta) che compiono una scansione bidimensionale da parti opposte della mammella. Al fine di ottenere informazioni più mirate sulle diverse componenti del tessuto, nella fibra di iniezione vengono lanciati quattro impulsi laser della durata di 200-400 ps rispettivamente a 685, 785, 915 e 975 nm. Con un campionamento ogni millimetro, attraverso una strumentazione di rivelazione con elevata risoluzione temporale e sensibilità al singolo fotone, vengono quindi acquisite quattro forme d’onda, che processate opportunamente forniscono le immagini ottiche, cioè le mappe di assorbimento e diffusione alle quattro lunghezze d’onda. Nel trial clinico attualmente in corso presso la clinica “S. Pio X” di Milano, sono stati analizzati fino ad ora più di 130 pazienti, con patologie sia benigne che maligne. Insieme ai dati di Berlino, questa rappresenta la più ampia casistica attualmente disponibile a livello internazionale. I risultati sono molto incoraggianti ed è stato possibile discriminare i differenti tipi di lesione ed iniziare a strutturare una banca dati con le proprietà ottiche delle diverse patologie.
Fig. 1.5 Mammografie X (sinistra) ed immagini ottiche di assorbimento (centro) e diffusione (destra) di una
paziente con un carcinoma (SX) ed due cisti (DX), ottenute con MAMMOT.
Il tumore è caratterizzato da intenso assorbimento, dovuto all’elevata vascolarizzazione, mentre la ciste, essendo liquida, ha minor coefficiente di diffusione rispetto al tessuto adiposo circostante.
1.3.2 Imaging funzionale cerebrale
Le metodologie ottiche sono state ampiamente studiate nell’imaging funzionale delle attività cerebrali sia con adulti che con neonati. L’imaging ottico della funzione cerebrale è basato sul fatto che le proprietà di scattering e di assorbimento per la luce nel vicino infrarosso forniscono informazioni sull’attività cerebrale. Benché la tomografia ottica soffra della bassa risoluzione spaziale, ha alcuni vantaggi rispetto alle altre tecniche di imaging cerebrale, tra le quali la più usata è la risonanza magnetica funzionale. In primo luogo, la tomografia ottica può essere utilizzata per distinguere tra ossi-emoglobina e deossi-emoglobina. In secondo luogo, è in grado di acquisire immagini molto rapidamente, e quindi ha un’eccellente risoluzione temporale. Terzo, un dispositivo per la tomografia ottica è facilmente trasportabile, e perciò può essere usato in un ambiente naturale, rilassato. Sono stati pubblicati pochi articoli sull’imaging ottico cerebrale, tra cui [Boas 2004, Hoshi 2003, Strangman 2002].
La maggior parte delle immagini ottiche della funzione cerebrale sono state ottenute facendo assunzioni semplificative sulla geometria del tessuto e sulle sue proprietà ottiche. Ma, in anni recenti, sempre un numero sempre maggiore di studi è stato realizzato utilizzando l’approccio topografico, in cui il trasporto della luce nei tessuti è completamente modellato. La tomografia ottica è stata utilizzata per determinare le proprietà ottiche del cervello adulto [Choi 2004] e per il monitoraggio del cervello del neonato prematuro [Hintz 2001]. Per di più, il metodo
DX
SX
tumour cysts tumour
è stato largamente studiato con piccoli animali [Siegel 2003] e per produrre immagini tridimensionali, che sono state utilizzate per monitorare l’emodinamica del cervello umano e per ricostruire immagini dell’attivazione della corteccia motoria [Fantini 1997, Gibson 2006].
Recentemente, le tecniche di stima dello stato sono state applicate al problema della ricostruzione tempo-variante della tomografia ottica [Diamond 2006, Prince 2003]. Il metodo fornisce una risoluzione temporale più alta per la ricostruzione, e migliora le stime dell’emodinamica funzionale. In più, sono stati studiati approcci multi-modalità che combinano l’imaging di risonanza magnetica funzionale con la tomografia ottica applicata al cervello [Boas 2005, Zhang 2005].
1.3.3 Imaging cerebrale neonatale
Il danno ipossico-ischemico cerebrale neonatale è la causa più frequente di handicap infantile. Tale danno è dovuto alla riduzione dell’ossigenazione cerebrale, determinata dalla diminuzione della concentrazione dell’ossigeno presente nel sangue o del flusso ematico cerebrale. Il neonato in terapia intensiva, soprattutto se pretermine o di basso peso alla nascita, è, per la sua condizione di prematurità e/o di patologia associata e/o di manovre assistenziali necessarie, a notevole rischio di subire episodi di ipossigenazione cerebrale, potenzialmente in grado di determinare danni neurologici. La possibilità di poter valutare l’ossigenazione cerebrale dei neonati a rischio, sia come quantità d’ossigeno presente nel parenchima cerebrale sia come apporto di sangue in termini di flusso e volume ematico cerebrale, permetterebbe di attuare manovre in grado di prevenire il verificarsi del danno ipossico-ischemico.
L’applicazione della tomografia ottica al neonato è risultata di grande valore potenziale nel poter fornire informazioni sull’ossigenazione, sul volume ematico e sul flusso ematico cerebrale. La spettroscopia nel vicino infrarosso è, infatti, l’unica metodica attualmente disponibile, anche se non ancora utilizzata nella pratica clinica, in grado di misurare in modo non invasivo ed al letto del paziente l’ossigenazione ed i parametri emodinamici cerebrali del neonato [Gibson 2005]. Al momento attuale, i danni cerebrali neonatali sono diagnosticati clinicamente per mezzo degli ultrasuoni, che forniscono solo informazioni anatomiche, e per mezzo dell’imaging di risonanza magnetica.
(strumento utilizzato nel neonato per misurare la SaO2 e la frequenza cardiaca mediante una sonda che viene posta alla mano o al piede), non riflettere l’effettiva ossigenazione cerebrale, come per esempio in neonati pretermine e/o patologici, in cui il sistema d’autoregolazione cerebrale può non funzionare adeguatamente, risultandone uno squilibrio tra offerta (ridotta) e richiesta d’ossigeno (normale o aumentata) da parte del tessuto cerebrale. La principale utilità della pulsiossimetria, nel neonato sottoposto ad ossigenoterapia, è di prevenire l’ipossia, non l’iperossia; la curva di dissociazione dell’emoglobina, infatti, è piatta al di sopra di un valore di SaO2 di 95%, quindi la pulsiossimetria non è sicura nel proteggere dai danni da iperossia. Inoltre, a basse saturazioni (sotto 80%) i pulsiossimetri sono meno affidabili in quanto le misure sperimentali sono eticamente difficili da condurre.
Parametri come la saturazione di ossigeno dell’emoglobina (SaO2) e la pressione parziale d’ossigeno del sangue arterioso (PaO2) non sono in grado di indicarci l’adeguatezza dell’offerta rispetto alla richiesta d’ossigeno da parte dei tessuti. La misura “sistemica” di tali parametri fornisce, infatti, una misura dell’offerta
d’ossigeno ai tessuti, ma non
dell’equilibrio tra offerta e richiesta d’ossigeno. Un valore di SaO2 ritenuto normale può risultare insufficiente rispetto ad una transitoria maggior richiesta d’O2 da parte di un determinato tessuto, con conseguente ipossia relativa, aumento del metabolismo cellulare anaerobio, acidosi e disfunzione cellulare. La misura dell’ossigenazione tissutale “regionale” (StO2) fornita dalla NIRS deriva da tutti e 3 i compartimenti (venoso, capillare ed arterioso) vascolari, e principalmente dalla rete capillare locale. Una SaO2 “locale” più bassa della “sistemica” è di solito interpretata come aumento del consumo d’O2 locale. Recentemente è stato dimostrato come la NIRS sia in grado di misurare contemporaneamente, oltre alla StO2, anche la SaO2 (sangue arterioso, = misura dell’offerta d’O2) e la SvO2 (sangue venoso, parametro direttamente collegato al flusso ematico e consumo d’ossigeno) regionali, separatamente, rendendo
possibile una misura dell’adeguatezza dell’offerta d’O2 rispetto alla richiesta d’O2. Il monitoraggio continuo della StO2, SaO2 e SvO2 a livello cerebrale (“cerebral status”) del neonato permetterebbe la diagnosi precoce della compromissione di tale equilibrio, prima dell’instaurarsi del danno irreversibile da ischemia, ipossia o iperossia.
![Fig. 1.1 Design di un dispositivo OT. Le sorgenti ed i ricevitori sono posizioni sul bordo dell’oggetto [Tarvainen 2006]](https://thumb-eu.123doks.com/thumbv2/123dokorg/7269901.83184/6.892.271.595.124.378/design-dispositivo-sorgenti-ricevitori-posizioni-bordo-oggetto-tarvainen.webp)