75
5. Il gruppo della tobermorite
Il gruppo della tobermorite (tab. 5.1)comprende una serie di inosilicati caratterizzati dalla presenza di catene tipo wollastonite legate a strati di poliedri Ca a coordinazione VII. Il particolare interesse riposto in queste fasi è da ricercarsi nelle strette relazioni strutturali con le fasi C-S-H
che si formano durante il processo di idratazione del cemento, oltre che nelle loro proprietà di scambio cationico già evidenziate nel capitolo introduttivo.
La fase eponima di questo gruppo è la tobermorite, descritta da Heddle (1880) su campioni provenienti da Tobermory, Isle of Mull, Scozia. Claringbull & Hey (1952) mostrarono la corrispondenza fra il diffrattogramma di polveri della tobermorite e quello del composto C-S-H (I) sintetizzato da Taylor (1950), avviando così le intense ricerche cristallochimiche e strutturali su questo minerale. Parallelamente alle ricerche condotte sulle fasi naturali, i chimici dei cementi osservarono l’esistenza di tre differenti stati di idratazione dei composti C-S-H (I) che furono chiamati tobermorite 14 Å, tobermorite 11 Å e tobermorite 9 Å, dalla periodicità del caratteristico riflesso basale a 14.0, 11.3 e 9.3 Å. Seguendo la proposta di nomenclatura suggerita da McConnell (1954) queste fasi sono indicate rispettivamente con i nomi mineralogici di plombièrite, tobermorite e riversideite. Oltre alla tobermorite, caratterizzata da una cella ortorombica per la struttura di famiglia, Henmi & Kusachi (1992) hanno descritto, nella località giapponese di Fuka, una fase con cella monoclina per la struttura di famiglia, denominandola clinotobermorite; questa fase è dimorfa rispetto alla tobermorite.
Alcuni autori inseriscono nel gruppo informale della tobermorite anche altri silicati idrati di calcio, naturali o sintetici, caratterizzati da distanze basali di 12.6 Å e 10.2 Å. Esse vengono associate alle specie mineralogiche tacharanite ed oyelite. La struttura di entrambe è tuttavia ancora irrisolta e pertanto la correlazione con le fasi del gruppo della tobermorite è ipotetica.
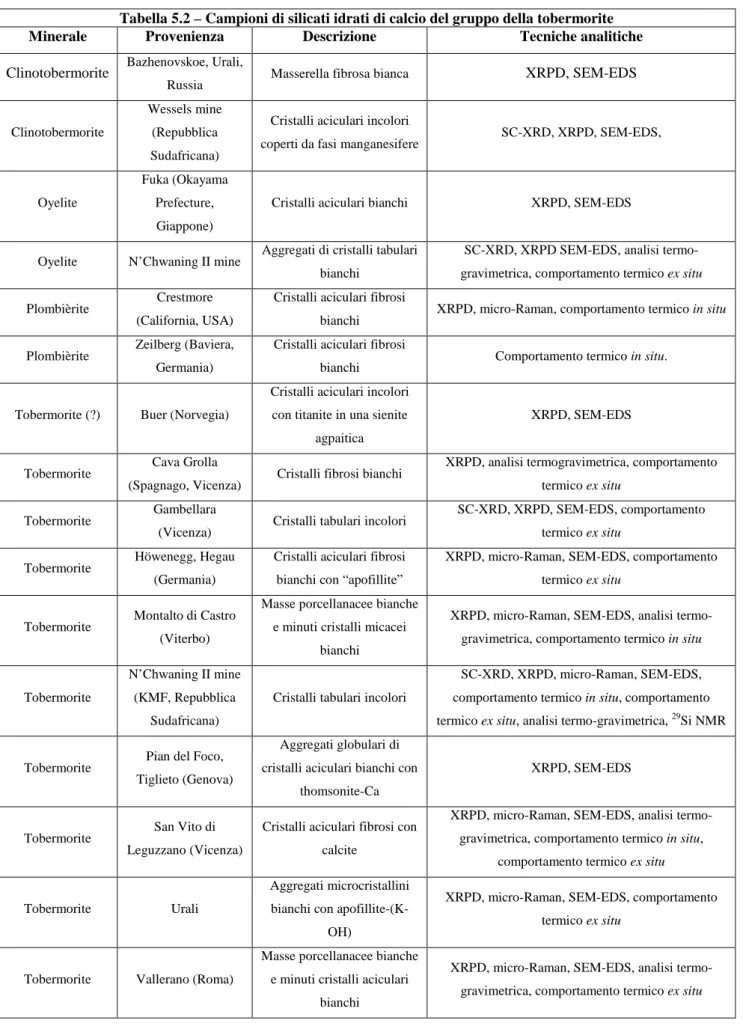
Durante lo svolgimento di questa tesi di dottorato sono stati esaminati numerosi esemplari di minerali appartenenti al gruppo della tobermorite. Essi vengono riportati in tabella 5.2, con una breve descrizione delle caratteristiche morfologiche e degli studi condotti su di essi. Alcuni campioni pervenutici come tobermoriti sono risultati altre fasi (es. tacharanite o thaumasite).
Tabella 5.1 – Minerali del gruppo della tobermorite
Nome Formula chimica Ca/Si d002
Clinotobermorite Ca5[Si6(O,OH)18]·5H2O 0.83 11.3 Å Oyelite Ca5BSi4O14(OH)·6H2O 1.25 10.2Å Plombièrite Ca5Si6O16(OH)2·7H2O 0.83 14.0 Å Riversideite Ca5Si6O16(OH)2 0.83 9.3 Å Tacharanite Ca12Al2Si18O51·18H2O 0.67 12.6 Å Tobermorite Ca4-5Si6O15(O,OH)2·5H2O 0.67 – 0.83 11.3 Å
76
Tabella 5.2 – Campioni di silicati idrati di calcio del gruppo della tobermorite Minerale Provenienza Descrizione Tecniche analitiche
Clinotobermorite Bazhenovskoe, Urali,
Russia Masserella fibrosa bianca XRPD, SEM-EDS
Clinotobermorite
Wessels mine (Repubblica Sudafricana)
Cristalli aciculari incolori
coperti da fasi manganesifere SC-XRD, XRPD, SEM-EDS,
Oyelite
Fuka (Okayama Prefecture, Giappone)
Cristalli aciculari bianchi XRPD, SEM-EDS
Oyelite N’Chwaning II mine Aggregati di cristalli tabulari bianchi
SC-XRD, XRPD SEM-EDS, analisi termo-gravimetrica, comportamento termico ex situ Plombièrite Crestmore
(California, USA)
Cristalli aciculari fibrosi
bianchi XRPD, micro-Raman, comportamento termico in situ Plombièrite Zeilberg (Baviera,
Germania)
Cristalli aciculari fibrosi
bianchi Comportamento termico in situ.
Tobermorite (?) Buer (Norvegia)
Cristalli aciculari incolori con titanite in una sienite
agpaitica
XRPD, SEM-EDS
Tobermorite Cava Grolla
(Spagnago, Vicenza) Cristalli fibrosi bianchi
XRPD, analisi termogravimetrica, comportamento termico ex situ
Tobermorite Gambellara
(Vicenza) Cristalli tabulari incolori
SC-XRD, XRPD, SEM-EDS, comportamento termico ex situ
Tobermorite Höwenegg, Hegau (Germania)
Cristalli aciculari fibrosi bianchi con “apofillite”
XRPD, micro-Raman, SEM-EDS, comportamento termico ex situ
Tobermorite Montalto di Castro (Viterbo)
Masse porcellanacee bianche e minuti cristalli micacei
bianchi
XRPD, micro-Raman, SEM-EDS, analisi termo-gravimetrica, comportamento termico in situ
Tobermorite
N’Chwaning II mine (KMF, Repubblica
Sudafricana)
Cristalli tabulari incolori
SC-XRD, XRPD, micro-Raman, SEM-EDS, comportamento termico in situ, comportamento termico ex situ, analisi termo-gravimetrica, 29Si NMR
Tobermorite Pian del Foco, Tiglieto (Genova)
Aggregati globulari di cristalli aciculari bianchi con
thomsonite-Ca
XRPD, SEM-EDS
Tobermorite San Vito di Leguzzano (Vicenza)
Cristalli aciculari fibrosi con calcite
XRPD, micro-Raman, SEM-EDS, analisi termo-gravimetrica, comportamento termico in situ,
comportamento termico ex situ
Tobermorite Urali
Aggregati microcristallini bianchi con
apofillite-(K-OH)
XRPD, micro-Raman, SEM-EDS, comportamento termico ex situ
Tobermorite Vallerano (Roma)
Masse porcellanacee bianche e minuti cristalli aciculari
bianchi
XRPD, micro-Raman, SEM-EDS, analisi termo-gravimetrica, comportamento termico ex situ
77
5.1 Assetto strutturale dei minerali del gruppo della tobermorite
Lo studio dei minerali del gruppo della tobermorite riveste un particolare interesse per la comprensione delle interessanti proprietà tecnologiche mostrate da questi composti. Fra le varie specie appartenenti a questo gruppo, la più frequente è la tobermorite s.s. (tobermorite 11 Å) e su di essa sono stati condotti i maggiori sforzi volti alla comprensione del suo assetto strutturale. La tobermorite compare spesso in campioni microcristallini o policristallini, non utilizzabili per studi strutturali con tecniche di cristallo singolo. Inoltre anche gli esemplari dotati di migliore cristallinità mostrano costantemente evidenze di disordine strutturale, come streaks diffusi nei diffrattogrammi di raggi X o di elettroni. Questo rende ragione delle notevoli difficoltà incontrate nello studio di questa fase.
La determinazione della struttura dei minerali del gruppo della tobermorite è un processo iniziato con lo studio cristallografico, termico e chimico di McConnell (1954) condotto su campioni provenienti da Ballycraigy (County Antrim, Irlanda) e proseguito con il primo modello strutturale di tobermorite proposto da Megaw & Kelsey (1956). Queste studiose, utilizzando i medesimi campioni di McConnell, descrissero la struttura della tobermorite in termini di strati di poliedri Ca e catene tipo wollastonite, senza tuttavia fornire coordinate e distanze atomiche. Gli studi degli autori citati evidenziarono la compresenza, nei diffrattogrammi di cristallo singolo, di riflessi netti ed intensi (riflessi di famiglia) e riflessi deboli e diffusi (riflessi caratteristici). I fotogrammi di cristallo singolo indicavano una cella pseudo-ortorombica con parametri a 11.3, b 7.3, c 22.6 Å; prendendo in considerazione soltanto i riflessi netti ed intensi, aventi indici h e k pari, può essere definita una sotto-cella con parametri a’ = a/2 e b’ = b/2, e gruppo spaziale I centrato. La risoluzione della struttura media della tobermorite fu effettuata da Hamid (1981) su campioni provenienti da Zeilberg (Baviera, Germania); questo autore confermò la presenza di strati di poliedri Ca e di catene tipo wollastonite. La risoluzione della struttura media portava ad individuare due catene con occupanza dimezzata, traslate l’una rispetto all’altra di b/2. Hamid (1981) risolse la struttura di famiglia nel gruppo spaziale Imm2 e ritenne che le catene della tobermorite fossero singole. Hoffmann & Armbruster (1997) risolsero invece la struttura media della clinotobermorite su campioni provenienti dalla Wessels mine (Kalahari Manganese Field, Repubblica Sudafricana). Anch’essi misero in luce l’esistenza di un disordine strutturale lungo [001], evidenziato nei diffrattogrammi di cristallo singolo dalla presenza di streaks continui lungo c*. Benché non fossero in grado, sulla base dei dati ottenuti, di poter inequivocabilmente dimostrare il grado di polimerizzazione delle catene silicatiche, Hoffmann & Armbruster (1997) ipotizzarono l’esistenza di doppie catene sulla base della distanza del legame Si-OH (Nyfeler & Armbruster, 1998; si veda anche § 3.2.2).
78
Applicando i principi della teoria OD ai minerali del gruppo della tobermorite ed utilizzando cristalli di eccezionale qualità provenienti dalle miniere del Kalahari Manganese Field (Repubblica Sudafricana), Merlino et al. (1999; 2000; 2001) riuscirono a risolvere la struttura reale di tobermorite e clinotobermorite, evidenziando la presenza di doppie catene silicatiche.
Le fasi del gruppo della tobermorite sono chiaramente distinte dagli altri silicati idrati di calcio trattati in questa tesi per la presenza di una unità strutturale comune a tutti i membri e definita da Bonaccorsi & Merlino (2005) come “modulo complesso” (fig. 5.1). Tale unità è costituita da uno strato di poliedri Ca (strato tipo tobermorite), parallelo a (001), al quale sono unite, su ambo i lati, catene tipo wollastonite. Il modulo complesso è C-centrato, con parametri a 11.2, b 7.3 e c0 11.2 Å.
I poliedri di coordinazione dei cationi Ca2+ nello strato tobermoritico possono essere descritti come prismi trigonali monocappati o, seguendo la descrizione di Hoffmann & Armbruster (1997), come formati da una parte piramidale e da una domatica. I poliedri, aventi coordinazione VII, sono connessi fra loro mediante condivisione di spigoli e formano colonne lungo [010]. Lungo tale direzione si alternano due tipi di poliedri: uno ha il sito apicale occupato da una molecola di H2O,
l’altro da O2- o da OH-; il corrispondente legame Ca-O è significativamente spostato rispetto alla posizione normale (fig. 5.1). Le colonne di poliedri Ca sono unite fra loro ancora per condivisioni di spigoli, formando uno strato bidimensionalmente infinito. Colonne adiacenti presentano i siti apicali su lati opposti dello strato tobermoritico.
Fig. 5.1 – Struttura dei minerali del gruppo della tobermorite.
In alto, a sinistra: esempio di modulo complesso, con lo strato tobermoritico (in blu) legato alle catene tipo wollastonite (in giallo). In basso, a sinistra, ed in alto, a destra: il modulo complesso visto rispettivamento lungo [010] e [100]. Si può apprezzare la forma del poliedro di coordinazione del Ca e la morfologia delle catene tipo wollastonite, composte da gruppi disilicato e tetraedri ponte. Il disegno si riferisce a fasi con cella di famiglia ortorombica.
79
Le catene tipo wollastonite (dreierketten) corrono lungo [010] su ambo i lati dello strato tobermoritico. Le singole catene possono essere descritte come formate da gruppi disilicato (paired
tetrahedra nella terminologia dei chimici dei cementi) uniti fra loro da bridging tetrahedra. Le
catene silicatiche sono legate allo strato tobermoritico mediante condivisione di uno spigolo (lo spigolo più corto del poliedro Ca) con i paired tetrahedra e mediante condivisione di un vertice del tetraedro ponte con un sito apicale dei poliedri Ca, sito corrispondente a O2- o OH
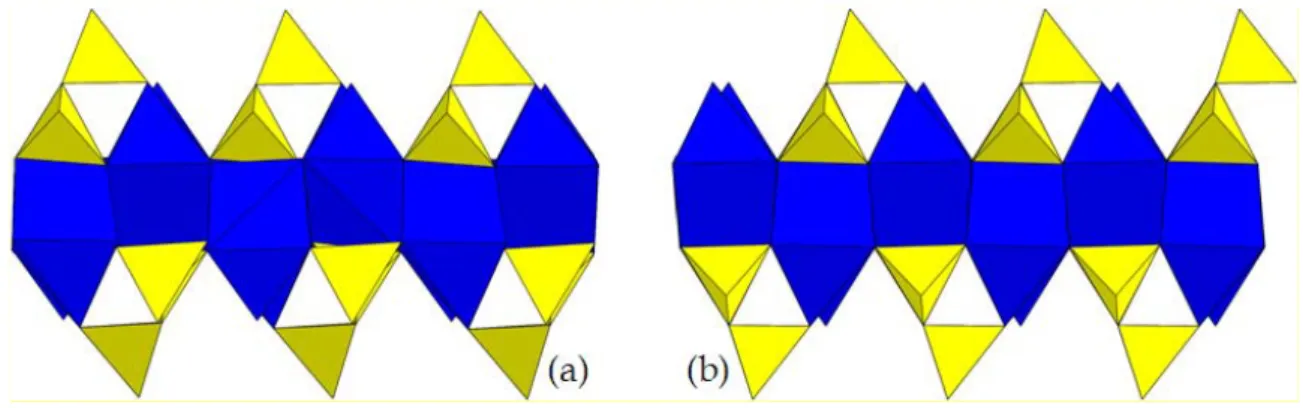
-Esistono due differenti disposizioni delle catene wollastonitiche sui due lati dello strato tobermoritico, disposizioni che danno origine a due differenti tipi di modulo complesso (fig. 5.2); in un caso, i tetraedri ponte sono posti a destra su un lato e a sinistra sull’altro (o viceversa) rispetto ai
paired tetrahedra, originando così il modulo complesso di tipo A; nell’altro caso i tetraedri ponte
sono posti sempre a destra (o a sinistra) rispetto ai paired tetrahedra su entrambi i lati dello strato tobermoritico (modulo complesso di tipo B).
. Quest’ultimo dato rende ragione dello spostamento del legame Ca-O rispetto alla posizione normale.
Il succedersi di moduli complessi di tipo A origina fasi con sottocella monoclina; le fasi con sottocella ortorombica mostrano invece moduli complessi di tipo B.
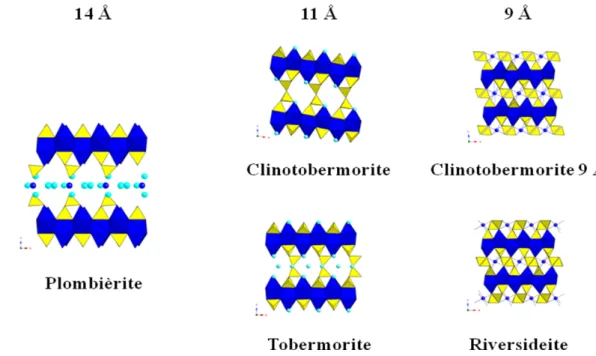
L’origine della differente distanza basale 002 fra le varie specie del gruppo della tobermorite è invece da ricercarsi nel loro diverso grado di idratazione; si distinguono così la plombièrite (tobermorite 14 Å), contenente 7 molecole H2O, la tobermorite e la clinotobermorite (tobermorite e
clinotobermorite 11 Å), contenenti 5 molecole H2O, e, infine, la riversideite (tobermorite 9 Å),
priva di molecole di H2O (fig. 5.3).
80
Fig. 5.3 – Assetti strutturali delle fasi a 14, 11 e 9 Å del gruppo della tobermorite.
Si osservi che mentre la plombièrite può essere descritta come un interstratificato, per la presenza di uno strato contentente Ca e molecole di H2O intercalato fra i moduli complessi, soltanto le fasi a 11
Å presentano una struttura microporosa s.s., con la presenza di cavità strutturali occupate da molecole di H2O e/o cationi Ca2+
Come già detto, gli effetti di diffrazione ottenuti dai cristalli dei minerali appartenenti al gruppo della tobermorite mostrano la compresenza di riflessi netti ed intensi e di riflessi deboli e diffusi, assenze sistematiche non di gruppo spaziale ed evidenze di geminazioni; ciò suggerisce la natura OD di queste fasi. Applicando i principi di tale teoria ai minerali del gruppo della tobermorite, Merlino et al. (1999, 2000. 2001) hanno ricavato i possibili politipi (tab. 5.3).
. Le fasi a 9 Å, infine, non hanno un carattere microporoso.
Tabella 5.3 – Politipi MDO nel gruppo della tobermorite
G.S. a (Å) b (Å) c (Å) α (°) β (°) γ (°)
Plombiérite Cella di famiglia I2mm 5.63 3.71 27.99
MDO1 F2dd 11.2 7.3 56.0 90 90 90
MDO2 B11b 6.735 7.425 27.987 90 90 123.25
Clinotobermorite Cella di famiglia A2/m 5.638 3.671 22.642 97.3
MDO1 Cc 11.276 7.343 22.642 97.28
MDO2 C1 11.274 7.344 11.468 99.18 97.19 90.02
Tobermorite Cella di famiglia I2mm 5.632 3.692 22.487 MDO1 F2dd 11.265 7.386 44.97
MDO2 B11m 6.735 7.385 22.487 123.25
81
MDO1 C2/c 11.161 7.303 18.771 92.91
MDO2 C1 11.156 7.303 9.566 101.08 92.83 89.98 Riversideite Cella di famiglia Pnmm 5.58 3.65 18.78
MDO1 Fd2d 11.16 7.32 37.40
MDO2 P1121/a 6.7 7.32 18.70 123.5
La natura OD delle varie fasi del gruppo della tobermorite e l’esistenza di differenti politipi sono legate alle relazioni metriche fra la periodicità lungo b delle catene silicatiche, pari a 7.3 Å, e la periodicità degli strati a poliedri Ca, uguale a 3.65 Å, esattamente la metà di quella delle catene tipo wollastonite. Pertanto queste ultime possono connettersi agli strati di poliedri Ca in due posizioni distinte, traslate l’una rispetto all’altra, lungo l’asse b, di 3.65 Å (fig. 5.4).
Fig. 5.4 – Possibili modalità di connessione fra catene tipo wollastonite e strato tobermoritico.
Utilizzando i principi della teoria OD, Merlino & Bonaccorsi (2008) hanno derivato altri possibili politipi finora non osservati in natura (tab. 5.4). Merita di essere notato come questi ipotetici politipi della clinotobermorite derivino dall’impilamento di moduli complessi di tipo B (caratteristici dei campioni con cella di famiglia ortorombica noti in natura) e viceversa gli ipotetici politipi della tobermorite siano costituiti da moduli complessi di tipo A.
Tabella 5.4 – Ipotetici politipi MDO in clinotobermorite e tobermorite
G.S. a (Å) b (Å) c (Å) α (°) β (°) γ (°)
Clinotobermorite Cella di famiglia Pnmn 5.638 3.671 22.460 MDO1 Fd2d 11.276 7.342 44.920
MDO2 C1121/d 11.276 7.342 22.460 90
Tobermorite Cella di famiglia Pnmm 5.633 3.693 22.487 MDO1 F2/d11 11.27 7.38 44.97 90
82
5.1.1 La versatilità dello strato tobermoritico
‹‹La natura non opera con l’intervento di molte cose quel che si può fare col mezo di poche.›› Così scriveva Galileo Galilei nel suo Dialogo sui massimi sistemi (Firenze, 1632). La determinazione e la conoscenza di un sempre maggior numero di strutture di composti sia naturali che sintetici consente di osservare come l’affermazione del grande scienziato seicentesco trovi riscontro anche alla scala atomica, con la presenza di moduli ricorrenti in vari tipi di fasi cristalline.
Lo strato tobermoritico, come abbiamo sopra denominato lo strato formato da poliedri con calcio a coordinazione VII, è stato ad esempio riscontrato in altre fasi silicatiche, mostrando quindi la sua versatilità di adattamento ad altri tipi di strutture.
La tabella 5.5 riporta le specie mineralogiche nelle quali è stata accertata la presenza di strati tipo tobermorite. Esse sono riconducibili a tre tipi strutturali differenti, esemplificati dalle strutture della rinkite, della roumaite e della fukalite.
La rinkite fa parte di un gruppo di disilicati comprendente anche mosandrite e nacareniobsite-(Ce); si tratta di specie mineralogiche tipiche di rocce magmatiche alcaline. La struttura di queste tre fasi è stata risolta rispettivamente da Galli & Alberti (1971), Bellezza et al. (2009) e Sokolova & Hawthorne (2008). Esse presentano gruppi disilicato, strati “ottaedrici” tipo rosenbuschite e strati tipo tobermorite (fig. 5.5).
La roumaite (Biagioni et al., 2010), scoperta nelle cavità delle sieniti a nefelina delle Iles de Los (Guinea), è strettamente correlata alle fasi del gruppo della rinkite presentando le
Tab. 5.5 – Fasi naturali con strato tipo tobermorite
Specie Formula chimica a (Å) b (Å) c (Å) α(°) β(°) γ(°) S.G.
rinkite (Na,Ca)3(Ca,Ce)4Ti(Si2O7)2OF3 7.437(2) 5.664(2) 18.843(3) 90 101.38(1) 90 P21/c
mosandrite (,Ca,Na)3(Ca,Ce)4Ti(Si2O7)2(H2O,O,F)4·H2O 7.398(1) 5.595(1) 18.662(2) 90 101.37(1) 90 P21/c
nacareniobsite-(Ce) (Na,Ca)3(Ca,Ce)4Nb(Si2O7)2OF3 7.468(2) 5.689(1) 18.891(4) 90 101.37(3) 90 P21/c
dovyrenite Ca6Zr(Si2O7)2(OH)4 5.666(16) 18.844(5) 3.728(11) 90 90 90 Pnnm
roumaite (Ca,Na,)3(Ca,REE,Na)4(Nb,Ti)(Si2O7)2(OH)F3 7.473(2) 11.294(2) 18.778(4) 90 101.60(2) 90 Cc
fukalite Ca4Si2O6CO3(OH)2 7.573(3) 23.364(5) 11.544(4) 90 109.15(1) 90 P21/c
Fig. 5.5 – Struttura dei minerali del gruppo della rinkite. In
verde, lo strato tipo rosenbuschite; in azzurro, lo strato tobermoritico; in giallo, i gruppi disilicato.
83
stesse unità modulari. La differenza risiede nella disposizione dei gruppi disilicato, all’origine di una cella primitiva nelle fasi del gruppo della rinkite e di una cella C centrata nella roumaite. La forte somiglianza strutturale fra i due gruppi è rivelata anche dalla presenza di domini di tipo rinkitico all’interno dei cristalli di roumaite.
Isomorfa con la roumaite, la dovyrenite è stata rinvenuta in xenoliti carbonatici termometamorfosati nel massiccio di Yoko-Dovyren (Russia) da Gałuskin et al. (2007). Lo studio strutturale di questa nuova specie è stato ostacolato dall’esteso disordine strutturale e dalle piccole dimensioni dei cristalli. Pertanto Kadiyski et al. (2008) hanno risolto la struttura media della dovyrenite nel gruppo spaziale Pnnm, ipotizzando una possibile struttura ordinata analoga a quella successivamente riscontrata nella roumaite.
Le fasi qui discusse (rinkite, mosandrite, nacareniobsite-(Ce), roumaite e dovyrenite) presentano una sottocella corrispondente a quella della tobermorite 9 Å. Aspetto comune è lo strato a poliedri di calcio (strato tobermoritico), decorato su entrambi i lati da gruppi disilicato: nella tobermorite 9 Å la connessione fra strati successivi avviene mediante i tetraedri ponte delle catene wollastonitiche, nelle altre fasi è uno strato tipo rosenbuschite ad assicurare la connessione fra due strati tobermoritici. La fig. 5.6 mostra come i tetraedri ponte della tobermorite 9 Å siano sostituiti, nelle fasi tipo rinkite e tipo roumaite, da un ottaedro occupato da Nb o Ti.
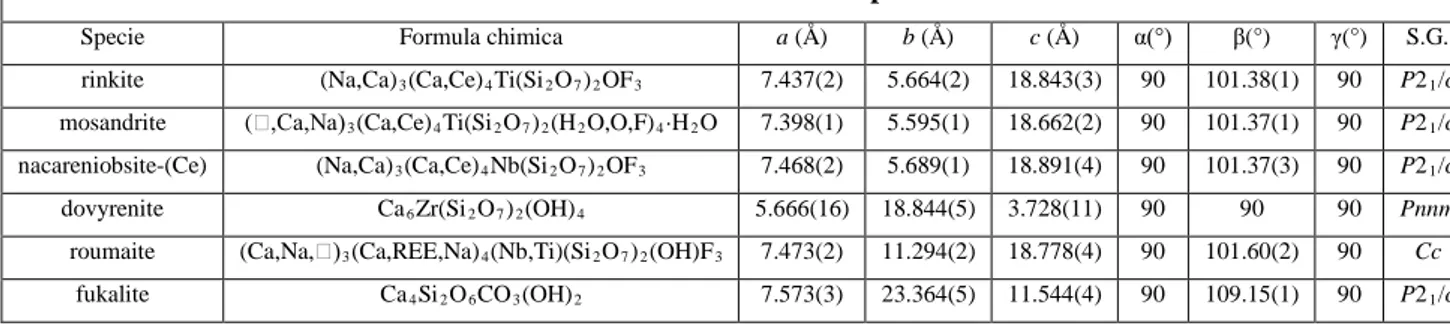
84 La fukalite è un silico-carbonato presente in rocce skarnoidi quale prodotto di alterazione idrotermale tardiva. Si tratta di un esempio di disordine bidimensionale, trattato da Merlino et al. (2009) attraverso l’uso della teoria OD. Tali autori hanno anche risolto la struttura reale della fukalite. Essa mostra la presenza di differenti unità strutturali: strati tipo tobermorite, strati tipo tilleyite, catene silicatiche, aventi periodicità pari a 4 tetraedri, e gruppi carbonato (fig. 5.7).
I poliedri Ca presentano caratteristiche geometriche analoghe a quelle riscontrate nei minerali del gruppo della tobermorite. In tabella 5.6 è riportato l’intervallo di variazione ed il valore medio delle distanze di legame nei poliedri dello strato tipo tobermorite nelle fasi considerate.
I siti dello strato tobermoritico di rinkite, mosandrite e nacareniobsite-(Ce) sono occupati da Ca e REE; Sokolova & Hawthorne (2008) inseriscono anche Na nel sito AP
Tab. 5.6 – Distanze medie e variabilità delle distanze di legame negli strati tipo tobermorite
della nacareniobsite-(Ce). Analogamente, Biagioni et al. (2010) ipotizzano la presenza di Ca, REE e Na nei siti M5-M8 dello strato tobermoritico; questo in accordo con quanto riportato da Ferreira et al. (2003) e Zanardi et al.
sito d media (Å) range sito d media (Å) range
rinkite M4 2.45 2.36-2.72 mosandrite M4 2.419 2.327-2.643
M5 2.47 2.33-2.66 M5 2.457 2.390-2.609
nacareniobsite-(Ce) MH 2.46 2.36-2.707 dovyrenite Ca1 2.475 2.411-2.700
AP 2.49 2.335-2.688
roumaite M5 2.44 2.32-2.563 fukalite Ca1 2.444 2.308-2.531
M6 2.49 2.37-2.83 Ca1A 2.440 2.327-2.556
M7 2.44 2.367-2.541 Ca4 2.437 2.317-2.554
M8 2.49 2.34-2.74 Ca4A 2.445 2.289-2.527
Fig. 5.7 – Struttura della fukalite, vista lungo [100]. In
verde: strati tipo tilleyite; in azzurro: strati tipo tobermorite; in giallo: gruppi disilicato; in nero: gruppi carbonato.
85
(2006) i quali hanno osservato la sostituzione 2Ca2+ = M+ + M3+ in silicati sintetici isostrutturali con la tobermorite 11 Å. Pertanto, strutture con moduli di tipo tobermoritico possono accomodare anche altri cationi, oltre al Ca2+, aprendo la via alla possibilità di sintesi di una ricca serie di composti con strutture tipo tobermorite.
5.2 Problematiche nomenclaturali nel gruppo della tobermorite
Bonaccorsi & Merlino (2005) hanno evidenziato come, ad eccezione della clinotobermorite, nessuna specie mineralogica appartenente al gruppo della tobermorite sia stata ufficialmente approvata dalla Commission on New Minerals, Nomenclature and Classification (CNMNC) dell’International Mineralogical Association. Prendendo in esame la IMA/CNMNC List of Mineral
Names, aggiornata a novembre 2009, si può verificare come plombièrite, riversideite e tobermorite
abbiano lo stato di grandfathered, ossia di specie mineralogiche pre-IMA.
Partendo dalla constatazione di Taylor (1953b) relativa all’esistenza di tre differenti stati di idratazione nel gruppo di composti sintetici C-S-H (I), McConnell (1954) attribuì i nomi plombièrite, tobermorite e riversideite alle fasi con riflessi basali rispettivamente a 14, 11.3 e 9.3 Å. Nel caso della fase a 14 Å McConnell non fece tuttavia differenza fra le fasi cristalline ed i gel C-S-H. Anche per questa ragione, Taylor (1964) evidenziò l’esistenza di problemi nomenclaturali legati soprattutto alla natura poco definita di alcune fasi.
I progressi nella conoscenza strutturale di questi composti ottenuti nell’ultimo decennio consentono di poter comprendere ed illustrare la variabilità chimica presentata da alcune di queste specie, sia alla luce dei differenti rapporti Ca:Si sia del variabile contenuto in H2O, e quindi di poter ipotizzare
una revisione nomenclaturale di questo gruppo di inosilicati.
5.2.1 Plombièrite
Il termine plombièrite è stato usato per la prima volta da Daubrée (1858) per indicare un gel silicatico formatosi, assieme a zeoliti (“apofillite” e “cabasite”) ed opale, a causa dell’azione di acque calde su materiali cementizi che i Romani avevano messo in opera in prossimità delle scaturigini termali a Plombières (Vosgi, Francia). Daubrée scriveva:
‹‹Dans des cavités situées à la partie inférieure de la couche de maçonnerie, et à proximité de
points qui reçoivent un jet direct d’eau thermale, il se produit assez abondamment des dépots gélatineaux, trasparents et incolores. En se desséchant à l’air libre, la substance devient, au bout de quelques heures, opaque et d’un blanc de neige. […] Selon les conditions de temperature dans lesquelles on la place succéssivement, elle perd ou elle gagne de l’eau […]. L’analyse a montré que
86
cette substance est un silicate de chaux hydrate, sans alcali, qui, après une dessication a 100 degrés, a eté trouvé compose de:
Silice ……….. 40,6
Chaux ……… 34,1
Alumine ………. 1,3
Eau avec traces d’acide carbonique 23,2 99,2
[…] Il constitue très-probablement une espèce nouvelle dont on pourrait peut-étre rappeler
l’origine par le nome de plombièrite››.
Come già detto, McConnell (1954) ha proposto uno schema nomenclaturale basato sui differenti gradi di idratazione delle fasi del gruppo della tobermorite; il termine plombièrite fu pertanto applicato alle fasi a maggior grado di idratazione, caratterizzate da una periodicità basale di 14 Å. Occorre tuttavia osservare che il nome plombièrite è stato applicato a fasi con differenti gradi di cristallinità; McConnell (1954) lo ha applicato, ad esempio, ad un gel silicatico proveniente da Ballycraigy (County Antrim, Irlanda), probabilmente analogo ai prodotti sintetici del gruppo del C-S-H (I). Questo autore riporta il diffrattogramma di polveri della plombièrite di Ballycraigy; va subito rimarcata l’assenza del riflesso basale a 14 Å e lo scarso numero di riflessi osservati, la cui intensità risulta peraltro generalmente debole. Tutto ciò, assieme alla larghezza dei riflessi (indicati con la lettera b, broad), è indizio della natura scarsamente cristallina del prodotto studiato. L’assenza del riflesso basale a 14 Å potrebbe essere spiegabile ricordando che nelle tobermoriti scarsamente cristalline, con assenza di ordine a lungo raggio, i riflessi presenti appartengono generalmente alla classe hk0 (Taylor, 1964). Il riflesso a 5.48 Å riportato da McConnell (1954) può comunque essere indicizzato, utilizzando la cella di famiglia della plombièrite, con gli indici 101; la debolezza e l’allargamento di tale riflesso sono tuttavia una evidenza del forte disordine strutturale presente nella direzione di c*
McConnell (1954; 1955) riporta a sostegno della tesi dell’identità fra il gel C-S-H da lui studiato e la plombièrite di Daubrée (1858) anche tre analisi chimiche. Come detto sopra, McConnell non distingue fra fasi cristalline e scarsamente cristalline, indicandole tutte come plombièrite; secondo Taylor (1964) tale nome dovrebbe essere applicato soltanto alle fasi scarsamente cristalline, in ottemperanza alla priorità di utilizzo di tale nome da parte di Daubrée ad indicare un gel silicatico ricco di Ca. Per la fase cristallina a 14 Å sarebbe pertanto necessario un nome differente.
87
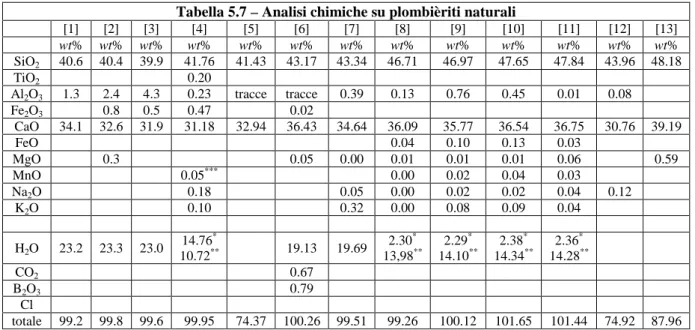
Vari autori hanno prodotto altre analisi chimiche di plombièrite (tobermorite 14 Å), spesso unite a dati diffrattometrici che inequivocabilmente mostravano la presenza del riflesso basale a 14 Å; la tabella 5.7 riporta le analisi chimiche note in letteratura.
Le analisi [1-4] sono state condotte per via umida; è interessante notare come Daubrée (1858) sottolinei che il suo campione sia stato analizzato previo riscaldamento a 100°C. È noto che la plombièrite perde molecole di H2
Le analisi [5-13] sono state invece eseguite mediante microsonda elettronica; in alcuni casi il contenuto di H
O già a 55°C (Farmer et al., 1966), trasformandosi nella fase a 11 Å; tuttavia il campione francese mostra ancora un alto contenuto di volatili.
2
La risoluzione della struttura della fase naturale a 14 Å da parte di Bonaccorsi et al. (2005), condotta su campioni provenienti da Crestmore, fornisce certamente un importante contributo per la O è stato ricalcolato sulla base del bilancio di carica e della formula teorica. Questo è ad esempio il caso della plombièrite di Cornet Hill (Apuseni Mountains, Romania) descritta da Marincea et al. (2001). In questa località la plombièrite deriva dall’alterazione idrotermale della scawtite ed è stata identificata sulla base di diffrattogrammi di polvere raccolti su campioni di scawtite, che hanno evidenziato la presenza del riflesso basale a 14 Å. Questi autori descrivono la scomparsa di tale riflesso su campioni riscaldati a 800°C; l’idratazione del materiale riscaldato sembra tuttavia ricomporre la plombièrite. Marincea et al. (2001) riportano analisi chimiche in microsonda elettronica dei campioni di plombièrite rumena.
Tabella 5.7 – Analisi chimiche su plombièriti naturali
[1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] wt% wt% wt% wt% wt% wt% wt% wt% wt% wt% wt% wt% wt% SiO2 40.6 40.4 39.9 41.76 41.43 43.17 43.34 46.71 46.97 47.65 47.84 43.96 48.18 TiO2 0.20 Al2O3 1.3 2.4 4.3 0.23 tracce tracce 0.39 0.13 0.76 0.45 0.01 0.08 Fe2O3 0.8 0.5 0.47 0.02 CaO 34.1 32.6 31.9 31.18 32.94 36.43 34.64 36.09 35.77 36.54 36.75 30.76 39.19 FeO 0.04 0.10 0.13 0.03 MgO 0.3 0.05 0.00 0.01 0.01 0.01 0.06 0.59 MnO 0.05*** 0.00 0.02 0.04 0.03 Na2O 0.18 0.05 0.00 0.02 0.02 0.04 0.12 K2O 0.10 0.32 0.00 0.08 0.09 0.04 H2O 23.2 23.3 23.0 14.76* 10.72** 19.13 19.69 2.30* 13,98** 2.29* 14.10** 2.38* 14.34** 2.36* 14.28** CO2 0.67 B2O3 0.79 Cl totale 99.2 99.8 99.6 99.95 74.37 100.26 99.51 99.26 100.12 101.65 101.44 74.92 87.96 [1] Plombières, Vosgi, Francia (Daubrée, 1858); [2] Ballycraigy, Co. Antrim, Irlanda (McConnell, 1954); [3] Ballycraigy, Co. Antrim, Irlanda (McConnell, 1955); [4] Scawt Hill, Co. Antrim, Irlanda (McConnell, 1955); [5] Hatrurim Formation (Gross, 1977); [6] Crestmore, California (Mitsuda & Taylor, 1978); [7] Fuka, Giappone (Henmi & Kusachi, 1992); [8-11] Cornet Hill, Romania (Marincea et al., 2001); [12-13] Gumeshevsk, Urali, Russia (Grabhezev et al., 2007). *(H2O)+; **(H2O)-; ***Mn espresso come Mn2O3.
88
corretta definizione di questa specie. La formula della plombièrite può essere espressa come Ca5Si6O16(OH)2·7H2
La tabella 5.8 mostra il ricalcolo delle analisi di tabella 5.6 effettuato assumendo una completa occupanza dei siti tetraedrici, ponendo (Si+Al+Fe
O.
3+
) = 6 apfu. La presenza di B2O3 e CO2
nell’analisi [6] è stata attribuita rispettivamente ad oyelite e calcite; pertanto nel ricalcolo sono state sottratte al totale delle moli di CaO, SiO2 e H2O quelle dovute al contributo dei due minerali citati.
Nei siti tetraedrici, Si4+ può essere parzialmente vicariato da Al3+
Il numero di atomi di Ca per unità formula è solitamente vicino al valore teorico di 5 apfu; in alcuni casi si ha un eccesso di Ca che potrebbe anche essere legato alla presenza di altre fasi nel campione analizzato (es. calcite). Raramente si hanno invece plombièriti significativamente povere in Ca, con valori minimi di ~4.5 apfu.
; il contenuto massimo di Al è di 0.67 apfu, ma generalmente è inferiore a 0.20 apfu.
La differenza più significativa fra i dati chimici e la formula strutturale di Bonaccorsi et al. (2005) riguarda il numero di molecole d’acqua. Laddove misurate sperimentalmente, le molecole di H2O
risultano sempre maggiori di 8 pfu. Nei campioni [8-11] il valore di 6 molecole di H2O pfu è un
artificio introdotto dagli autori. Va tuttavia sottolineata la difficoltà nell’ottenere dati quantitativi accurati per quanto riguarda il contenuto in H2O di queste fasi. Pertanto sulla base delle
considerazioni sin qui svolte, riteniamo che la formula della plombièrite possa essere scritta come
Tabella 5.8 – Formule chimiche di plombièriti naturali
[1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13]
apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu
Si4+ 5.78 5.53 5.28 5.91 6.00 6.00 5.94 5.98 5.89 5.93 6.00 5.99 6.00 Ti4+ 0.02 Al3+ 0.22 0.39 0.67 0.04 0.00 0.00 0.06 0.02 0.11 0.07 0.00 0.01 Fe3+ 0.08 0.05 0.05 0.00 Ca2+ 5.20 4.78 4.52 4.73 5.11 4.98 5.09 4.95 4.80 4.87 4.94 4.49 5.23 Fe2+ 0.00 0.01 0.01 0.00 Mg2+ 0.06 0.01 0.00 0.00 0.00 0.00 0.01 0.11 Mn2+ 0.00* 0.00 0.00 0.00 0.00 Na+ 0.05 0.01 0.00 0.00 0.00 0.01 0.03 K+ 0.02 0.06 0.00 0.01 0.01 0.01 O2- 16.18 15.21 14.32 15.52 15.78 15.98 16.06 15.88 15.52 15.70 15.96 15.00 16.34 OH- 1.82 2.79 3.68 2.48 2.22 2.02 1.94 2.12 2.48 2.30 2.04 3.00 1.66 H2O 10.1 9.25 8.3 10.8 8.4 8.1 5.9 5.6 5.8 5.9
[1] Plombières, Vosgi, Francia (Daubrée, 1858); [2] Ballycraigy, Co. Antrim, Irlanda (McConnell, 1954); [3] Ballycraigy, Co. Antrim, Irlanda (McConnell, 1955); [4] Scawt Hill, Co. Antrim, Irlanda (McConnell, 1955); [5] Hatrurim Formation (Gross, 1977); [6] Crestmore, California (Mitsuda & Taylor, 1978); [7] Fuka, Giappone (Henmi & Kusachi, 1992); [8-11] Cornet Hill, Romania (Marincea et al., 2001); [12-14] Gumeshevsk, Urali, Russia (Grabhezev et al., 2007).
89
Ca5-x(AlySi6-y)O15-2x-y(OH)2+2x+y·7H2O, con 0<x<0.5 e 0<y<0.7.
Lo studio di Bonaccorsi et al. (2005), caratterizzando strutturalmente la fase a 14 Å del gruppo della tobermorite, consente pertanto di poter distinguere la fase cristallina da quella serie di composti scarsamente cristallini attribuiti genericamente alla plombièrite. Rimane tuttavia da comprendere se i gel silicatici, così come descritti in letteratura, siano vere e proprie fasi amorfe o piuttosto fasi a 14 Å con elevato grado di disordine strutturale. In quest’ultimo caso, trattandosi comunque di fasi cristalline, potrebbero tutte essere descritte con il medesimo nome mineralogico. La plombièrite potrebbe pertanto essere ridefinita come specie mineralogica utilizzando come neotipo il campione studiato da Bonaccorsi et al. (2005) e proveniente da Crestmore (California, USA), mantenendo tale nome visto il suo consolidato utilizzo nella letteratura mineralogica. Naturalmente sarebbero auspicabili studi diffrattometrici sul materiale proveniente da Plombières, ammesso che possa ancora essere reperito e che sia analogo a quello studiato nel XIX secolo da Daubrée.
5.2.2 Tobermorite e clinotobermorite
Il termine tobermorite è stato utilizzato per la prima volta da Heddle (1880) per indicare un nuovo silicato idrato di calcio scoperto a Tobermory (Isle of Mull, Scozia). Claringbull & Hey (1952) riportano il diffrattogramma di uno dei campioni di tobermorite studiati da Heddle, evidenziando la presenza del riflesso basale a 11.3 Å. Pertanto, McConnell (1954) ha attribuito il nome tobermorite alle fasi appartenenti al gruppo omonimo e caratterizzate da periodicità basali di 11 Å.
Nel 1992 Henmi & Kusachi hanno descritto, dal deposito giapponese di Fuka (Okayama Prefecture, Giappone), il dimorfo con sottocella monoclina della tobermorite e lo hanno denominato clinotobermorite.
Gli studi strutturali di Merlino et al. (1999, 2000, 2001) hanno consentito di comprendere la cristallochimica di queste due fasi. Inoltre lo studio di questi autori ha permesso di interpretare il differente comportamento termico mostrato dai campioni di tobermorite alla luce del contenuto di Ca all’interno delle cavità strutturali.
Le tabelle 5.9 - 5.11 riportano i dati chimici relativi ai ritrovamenti di tobermoriti e clinotobermoriti naturali descritti in letteratura; le analisi sono state condotte sia con metodi tradizionali per via umida sia attraverso microsonda elettronica. Quest’ultimo tipo di indagine non consente tuttavia un’accurata determinazione del contenuto in volatili e, nella fattispecie, di H2O. Pertanto nasce il
problema di quale procedura seguire per il ricalcolo delle formule cristallochimiche. Esistono due possibili soluzioni.
90
1) Ricalcolo sulla base del numero di anioni. Tale ricalcolo tuttavia risente della scarsa accuratezza nella determinazione del contenuto in H2O. Anche assumendo la presenza di 5 H2O pfu, rimarrebbe
comunque l’incertezza sul rapporto O2-:OH
-2) Ricalcolo sulla base di un numero fissato di cationi. Questa soluzione ovvierebbe alla poco accurata conoscenza del numero di anioni sul quale effettuare il ricalcolo ma risente in misura importante della variabilità chimica delle tobermoriti legata alla introduzione di cationi “zeolitici”. Pertanto non è possibile effettuare il ricalcolo sul numero di atomi di Ca pfu, visto che essi possono variare fra 4 e 5 apfu. Anche l’eventuale somma fra Ca e cationi tetraedrici non avrebbe una base di ricalcolo sicura sulla quale impostare i successivi calcoli. Alcune evidenze strutturali indicano inoltre che persino il numero di cationi tetraedrici potrebbe essere variabile, con la possibilità di omissione dei tetraedri di bridging. Tuttavia i campioni naturali hanno solitamente un buon grado di cristallinità e possiamo in prima approssimazione trascurare le eventuali interruzioni delle catene silicatiche, ricalcolando la formula strutturale sulla base di 6 cationi tetraedrici, assumendo che Si
, funzione della composizione cationica del campione studiato. Riteniamo pertanto sconsigliabile effettuare il ricalcolo su base anionica.
4+
possa essere vicariato da Al3+ o, raramente, da Fe3+
La tabella 5.9 riporta analisi chimiche di campioni naturali di tobermorite, condotte sia per via umida (analisi [1-6]) sia attraverso tecniche più moderne. In particolare, l’analisi [7] è stata condotta con spettrometria di assorbimento atomico ed analisi termo-gravimetrica per la determinazione del contenuto in H
.
2O mentre le restanti analisi sono state condotte con microsonda elettronica. Le
analisi chimiche sono state ricalcolate sulla base di 6 (Si+Al+Fe3+) apfu; gli anioni sono stati ricalcolati in modo da bilanciare elettrostaticamente la formula del campione in esame. Si evidenzia come l’analisi di McConnell (1954) (analisi [4]) porti al ricalcolo di un numero negativo di OH -come conseguenza di un eccesso di cariche positive (Ca > 5 apfu).
Tabella 5.9 – Analisi chimiche su tobermoriti naturali
[1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% SiO2 46.508 46.62 46.17 44.86 45.39 45.45 49.6 45.24 45.12 48.95 34.40 48.30 46.7 TiO2 0.10 0.0 Al2O3 2.402 3.895 4.26 6.35 5.63 3.81 3.31 2.70 3.56 2.32 2.2 Fe2O3 1.139 0.664 - 0.13 0.50 0.07 0.23 tracce 0.0 CaO 33.404 33.978 35.15 36.02 24.53 33.30 37.4 34.64 35.24 33.69 25.85 27.59 37.3 FeO 1.853 1.080 0.15 MgO 0.474 tracce 4.38 0.50 0.02 0.04 0.04 0.50 4.90 0.0 MnO 0.0 Na2O 0.356 0.891 0.56 0.05 1.25 0.22 0.44 0.24 0.55 0.72 0.24 0.1 K2O 1.445 0.572 0.25 0.05 0.71 0.27 0.12 0.23 0.07 0.27 0.19 0.1 H2O 12.606 12.109 13.47 11.10 8.32 * 16.88 ** 1.06 * 12.69 ** 1.81 * 13 ** 14.15 15.52 13.85 9.90 16.85 13.2 CO2 1.42 totale 100.187 99.81 100.01 100.40 100.78 100.37 100 99.91 99.93 99.85 75.20 100.39 99.6
91
apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu
Si4+ 5.56 5.41 5.42 6.00 5.14 5.20 6.00 5.45 5.50 5.63 5.34 5.68 5.68 Ti4+ 0.01 0.00 Al3+ 0.34 0.53 0.59 0.85 0.76 0.54 0.48 0.37 0.66 0.32 0.32 Fe3+ 0.10 0.06 0.01 0.04 0.01 0.02 0.00 0.00 Ca2+ 4.28 4.22 4.42 5.16 2.98 4.08 4.85 4.24 4.60 4.15 4.30 3.48 4.86 Fe2+ 0.19 0.10 0.01 Mg2+ 0.08 0.74 0.09 0.00 0.01 0.01 0.12 0.86 0.00 Mn2+ 0.00 Na+ 0.08 0.20 0.13 0.01 0.27 0.05 0.10 0.06 0.12 0.22 0.05 0.02 K+ 0.22 0.08 0.04 0.01 0.10 0.10 0.02 0.04 0.01 0.05 0.03 0.02 O2- 15.96 15.33 15.44 17.34 13.99 14.69 16.70 15.05 15.82 15.08 15.45 15.44 16.44 OH- 1.04 1.67 1.56 -0.34 3.01 2.31 0.30 1.95 1.8 1.92 1.55 1.56 0.56 H2O 4.5 3.85 4.5 5.12 4.86 3.67 5.1 4.7 5.72 4.35 4.35 5.84 5.07
[1] Pier of Tobermory, Island of Mull, Scozia (Heddle, 1880); [2] Bloody Bay, Island of Mull, Scozia (Heddle, 1880); [3] Loch Eynort, Skye, Scozia (Claringbull & Hey, 1952); [4] Ballycraigy (McConnell, 1954); [5] Prà da la Stua, Trento (Gottardi & Passaglia, 1966); [6] Monte Biaena (Gottardi & Passaglia, 1967); [7] Castle Hill, Ayrshire (Webb, 1971); [8] Heguri, Giappone (Mitsuda, 1973); [9] Fuka, Giappone (Mitsuda & Taylor, 1978); [10] Portree, Scozia (Mitsuda & Taylor, 1978); [11] Hatrurim Formation, Israele (Gross, 1977); [12] Gruppo di Voltri, Liguria (Lucchetti & Penco, 1978); [13] Fuka, Giappone (Kusachi et al., 1980). *H2O
(+)
; **H2O (-)
.
L’analisi [5], invece, mostra un significativo deficit di Ca (2.98 apfu) con un importante contenuto in Mg (0.74 apfu). Secondo Mitsuda (1973) il Mg non entrerebbe in quantità significative nella struttura della tobermorite e pertanto i risultati riportati da Gottardi & Passaglia (1966) potrebbero riferirsi ad un campione contenente, oltre alla tobermorite, anche un silicato di Mg. Analoghi bassi valori di Ca ed alti contenuti in Mg sono stati riportati da Lucchetti & Penco (1978) su tobermoriti del Gruppo di Voltri (Liguria; analisi [12]). Il ricalcolo dell’analisi [8] è stato eseguito attribuendo la CO2
La tabella 5.10 riporta analisi condotte in microsonda elettronica e con l’ICP-AES (analisi [19]). Le analisi [19-24] mostrano un totale di Ca pfu inferiore a 4 apfu; la causa potrebbe essere da ricercarsi nella qualità delle analisi chimiche (eventuale non omogeneità dei campioni analizzati).
alla presenza di calcite e quindi sottraendo dalle moli di CaO quelle legate al contributo del carbonato di calcio.
Tabella 5.10 – Analisi chimiche su tobermoriti naturali
[14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% SiO2 43.87 48.08 46.88 46.33 48.98 44.17 50.45 51.46 49.52 50.41 51.50 47.68 51.25 TiO2 0.03 0.02 0.01 0.06 0.09 0.05 0.17 Al2O3 4.58 3.96 4.04 4.20 1.03 5.70 3.16 3.72 3.87 3.59 4.38 6.07 0.04 B2O3 0.03 Fe2O3 0.03 CaO 33.88 35.24 34.60 35.03 37.90 27.00 32.01 32.09 30.67 32.82 30.62 36.00 37.40 FeO 0.01 0.01 0.02 0.92 0.85 1.27 1.29 1.34 0.02 0.04 MgO 0.03 0.03 0.03 0.04 0.00 0.49 0.50 0.74 0.74 0.85 0.27 0.02 MnO 1.70 0.03 0.02 0.03 0.03 0.01 0.03 0.04 0.03 0.00 SrO 0.45 Na2O 0.52 0.03 0.02 0.04 0.01 1.40 0.49 0.55 0.69 0.45 0.74 0.00 0.06 K2O 0.03 0.03 0.02 0.02 1.04 0.24 0.32 0.41 0.38 0.39 0.18 0.01 H2O 12.17 * 11.46 20.65 13.12 11.27 13.99 11.53 11.31 11.10 8.51
92 3.68**
F 0.00 0.31 0.00
totale 100.85 87.38 85.61 85.65 99.56 100.02 100.92 100.85 101.26 101.29 101.34 101.66 97.33
apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu
Si4+ 5.34 5.47 5.45 5.42 5.85 5.21 5.59 5.53 5.49 5.54 5.45 5.22 5.99 Ti4+ 0.00 0.00 0.00 0.00 0.01 0.00 0.01 Al3+ 0.66 0.53 0.55 0.58 0.14 0.79 0.41 0.47 0.51 0.46 0.55 0.78 0.01 B3+ 0.01 Fe3+ 0.00 Ca2+ 4.42 4.30 4.31 4.39 4.85 3.41 3.80 3.69 3.65 3.86 3.47 4.22 4.69 Fe2+ 0.00 0.00 0.00 0.09 0.08 0.12 0.12 0.12 0.04 0.00 Mg2+ 0.01 0.01 0.01 0.01 0.00 0.08 0.08 0.12 0.12 0.12 0.00 0.00 Mn2+ 0.08 0.00 0.00 0.00 0.00 0.00 0.00 0.00 0.00 0.00 Sr2+ 0.11 Na+ 0.08 0.00 0.00 0.01 0.00 0.32 0.11 0.11 0.15 0.10 0.15 0.00 0.01 K+ 0.00 0.00 0.00 0.00 0.16 0.03 0.04 0.06 0.05 0.05 0.03 0.00 O2- 15.53 15.09 15.09 15.23 16.57 13.51 14.67 14.38 14.52 14.89 14.11 14.77 16.38 OH- 1.47 1.91 1.91 1.77 0.43 3.49 2.33 2.62 2.48 2.11 2.89 2.12 0.62 H2O 4.2 4.34 6.4 3.67 2.75 3.93 3.18 2.55 3 3.02 F 0.00 0.11
[14] Heguri, Giappone (Kato et al., 1984); [15-17] Skye, Scozia (Livingstone, 1988); [18] Fuka, Giappone (Henmi & Kusachi, 1992); [19-25] Puyuhapi, Cile (Aguirre et al., 1998); [26] Cornet Hill, Romania (Marincea et al., 2001). *H
2O(+); **H2O(-).
A fianco dei dati di letteratura, sono state prodotte analisi chimiche su campioni di tobermoriti naturali studiati nel corso di questa tesi di dottorato. Le analisi sono state condotte sia con il sistema EDS che WDS; nel primo caso le analisi chimiche sono state effettuate presso il Dipartimento di Scienze della Terra dell’Università di Pisa, nel secondo presso l’Università degli Studi di Modena e Reggio Emilia.
Tabella 5.11 – Analisi chimiche su tobermoriti naturali
[27] [28] [29]c [30]c [31] [32] [33] [34] [35] [36] [37] [38] [39] [40] wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% wt.% SiO2 53.03 52.65 46.55 47.44 61.61 47.73 49.59 56.83 52.85 57.54 57.46 60.34 54.67 47.97 TiO2 0.01 Al2O3 0.20 0.05 0.36 8.68 7.56 6.51 2.94 3.50 3.96 8.00 B2O3 0.00 0.23 Fe2O3 0.01 CaO 36.70 35.31 39.04 36.53 38.39 42.60 39.91 43.17 37.46 39.52 39.04 39.66 41.37 44.03 FeO 0.10 0.02 MgO 0.08 0.09 0.11 MnO 0.08 0.01 0.06 SrO Na2O 0.00 0.08 0.02 K2O 0.01 0.12 0.10 0.99 2.94 3.18 H2O 9.44 9.65 13.75 CO2 F 0.00 0.00 0.18 totale 99.72 97.98 100.34 83.97 100 100 100 100 100 100 100 100 100 100
apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu apfu
Si4+ 5.97 5.99 5.90 6.00 6.00 4.94 5.09 6.00 5.24 5.66 5.60 6.00 5.53 5.01
Ti4+ 0.00
Al3+ 0.03 0.01 0.05 1.06 0.91 0.76 0.34 0.40 0.47 0.99
93
[27-28] Cornet Hill, Romania (Marincea et al., 2001); [29] Fuka, Giappone (Henmi & Kusachi, 1992); [30] Wessels mine, Repubblica Sudafricana (Hoffmann & Armbruster, 1997); [31] N’Chwaning II mine, Repubblica Sudafricana (questo studio); [32] Vallerano, Roma (questo studio); [33] Höwenegg, Germania (questo studio); [34] Wessels mine, Repubblica Sudafricana (questo studio); [35] Urali, Russia (questo studio); [36] Gambellara, Vicenza (questo studio); [37] San Vito di Leguzzano, Vicenza (questo studio); [38] Bazhenovskoe, Russia (questo studio); [39] cava Grolla, Vicenza (questo studio); [40] Montalto di Castro, Viterbo (questo studio). c = clinotobermorite.
Le analisi chimiche EDS sono normalizzate a 100 e sono state condotte sia su campioni opportunamente lucidati sia su frammenti non lucidati. I risultati sono generalmente di buona qualità, con rapporti Ca/Si all’interno degli intervalli di variazione attesi. Inoltre, per quelle fasi di cui era già nota la chimica, i dati EDS presentano un buon accordo. Le analisi condotte in WDS mostrano invece una serie di problematiche che meritano di essere qui brevemente commentate. Il caso più tipico è rappresentato da totali molto bassi; attraverso gli studi termo-gravimetrici è possibile ammettere contenuti in H2
L’esame delle 40 analisi chimiche mostra un ampio intervallo di variazione nel contenuto di Ca. La determinazione dell’assetto strutturale della tobermorite pone dei vincoli sulla possibile composizione presentata da questa fase. Generalmente il contenuto di Ca pfu è compreso fra 4 e 5
apfu. Fra le analisi riportate, il 77.5% cade in questo intervallo composizionale. La restante parte
vede valori più bassi in 9 analisi (valori compresi fra 2.98 apfu e 3.98 apfu) o più alti in 2 analisi, con un valore massimo di 5.30 apfu misurato sulla clinotobermorite della località tipo da Henmi & Kusachi (1992). I bassi valori di Ca potrebbero essere dovuti all’analisi di campioni non omogenei e contenenti fasi con un basso valore del rapporto Ca:Si (es. smectiti, come nel caso della tobermorite del Gruppo di Voltri; Lucchetti & Penco, 1978); tuttavia potrebbero anche essere giustificati alla luce di possibili sostituzioni all’interno dello strato tobermoritico. In § 5.1.1 è stata descritta la possibilità di sostituzioni 2Ca
O pari a 13-15 wt.% con conseguenti totali nell’ordine di 85-87
wt.%. Tuttavia, non è stato infrequente il caso di totali molto più bassi. Le ragioni potrebbero essere
sostanzialmente tre: 1) scarsa qualità della superficie lucidata; 2) presenza di elementi non analizzati; 3) instabilità sotto il fascio elettronico. Pertanto al momento in tabella 5.11 saranno utilizzate le analisi chimiche ottenute in modalità EDS (analisi [31-40]).
2+
= Na+ + M3+ Fe
in tale unità strutturale. Generalmente il catione 3+ Ca2+ 4.43 4.30 5.30 4.95 4.00 4.73 4.39 4.88 3.98 4.17 4.08 4.22 4.48 4.93 Fe2+ 0.01 0.00 Mg2+ 0.01 0.02 0.02 Mn2+ 0.01 0.00 0.01 Sr2+ Na+ 0.00 0.01 0.00 K+ 0.00 0.02 0.02 0.13 0.38 0.40 O2- 15.89 15.66 17.58 16.9 15.00 15.53 15.25 16.76 14.62 15.00 14.76 15.44 15.49 15.87 OH- 1.11 1.34 -0.58 0.10 2.00 1.47 1.75 0.24 2.38 2.00 2.24 1.56 1.51 1.13 H2O 2.98 2.99 ~5.8 F 0.07
94
trivalente è rappresentato da REE3+ o Y3+; le analisi qui riportate non consentono di sostenere tale ipotesi a meno di non ammettere una parziale introduzione di Al3+
Nelle catene silicatiche delle tobermoriti naturali la sostituzione Si
in coordinazione ottaedrica nello strato tobermoritico. Tuttavia, numerosi studi spettroscopici volti a determinare il ruolo di tale elemento nelle fasi C-S-H tendono a mostrare come esso vada ad occupare generalmente i siti tetraedrici (Diamond, 1964; Komarneni et al., 1985; Richardson et al., 1993; Faucon et al., 1999; Andersen et al., 2003) o, in alcuni casi, le cavità strutturali assumendo in tal caso una coordinazione V (Andersen et al., 2003). I valori di Ca pfu più alti di 5 apfu possono invece essere legati alla presenza di calcite o altre fasi con più elevato rapporto Ca/Si (es. xonotlite) nei campioni studiati. Non è infatti infrequente osservare la stretta associazione di tobermorite con queste fasi.
4+
/Al3+
La formula generale di tobermorite e clinotobermorite può dunque essere scritta come
è piuttosto frequente; infatti sono piuttosto rare le tobermoriti naturali prive di Al, fra le quali è degna di menzione la tobermorite della N’Chwaning II mine (Kalahari Manganese Field, Repubblica Sudafricana). Il contenuto massimo di Al misurato nelle tobermoriti è ~ 1 apfu, in accordo con la regola di Loewenstein per la quale non possono esistere tetraedri di Al uniti fra loro; poiché è generalmente accettato che l’Al sostituisca il Si nei tetraedri di bridging delle doppie catene silicatiche, il valore massimo del rapporto Al/(Al+Si) è appunto uguale a 1/6.
Ca4+x(AlySi6-y)O15+2x-y(OH)2-2x+y·5H2
Mentre l’intervallo composizionale delle tobermoriti naturali vede il passaggio da termini con 4 Ca
pfu fino a termini con 5 Ca pfu, i campioni di clinotobermorite fino ad oggi descritti hanno sempre 5
Ca pfu (analisi [29-30]); potrebbero rappresentare una eccezione i campioni provenienti dalle vulcaniti terziarie del Vicentino descritti in § 7.2.
O, con 0<x<1 e 0<y<1.
La fig. 5.8 mostra la variabilità composizionale del contenuto in cationi “zeolitici” delle tobermoriti e clinotobermoriti le cui analisi sono riportate nelle tabelle 5.9 - 5.11; sono state tralasciate le analisi che presentavano contenuti di Ca inferiori a 4 apfu. Si osserva una soluzione solida pressocché completa fra un termine che presenta la posizione all’interno delle cavità strutturali completamente occupata da Ca2+ ed un termine le cui cavità sono completamente vacanti. Il contenuto in alcali (Na+K)+ è variabile; l’unica analisi che porterebbe a ricalcolare una predominanza di alcali nelle cavità strutturali è l’analisi di Heddle (1880). Tuttavia quest’ultima è stata condotta per via umida su un quantitativo di materiale tale da non poter garantire l’omogeneità del campione e quindi la reale composizione della tobermorite studiata. Il campione più ricco in alcali fino ad oggi studiato sembra pertanto essere quello di Höwenegg (Hegau, Germania), con un rapporto Ca/K molto vicino a 1.
95
Utilizzando le regole nomenclaturali per le soluzioni solide (Nickel, 1992) e considerando la natura “zeolitica” di tali cationi, è possibile applicare i suffissi di Levinson come nel caso delle zeoliti. Pertanto con il termine tobermorite si indicano almeno due specie mineralogiche distinte: tobermorite- e tobermorite-Ca. Tale distinzione si riflette anche sul differente comportamento termico mostrato in seguito al riscaldamento a 300°C di queste due fasi. Come detto, alcune tobermoriti naturali presentano importanti contenuti di cationi alcalini nelle cavità strutturali. Di conseguenza, ulteriori studi potrebbero portare alla definizione di un’altra specie di tobermorite a cui attribuire il nome di tobermorite-K.
5.2.3 Riversideite
Il termine riversideite comparve per la prima volta nella letteratura mineralogica ad opera di Eakle (1917) il quale descrisse due nuovi minerali provenienti dal deposito di Crestmore (Riverside County, California, USA): la crestmoreite e, appunto, la riversideite. Quest’ultima differiva dalla crestmoreite soltanto per il minor contenuto di H2O. Flint et al. (1938), studiando campioni di
crestmoreite e riversideite, conclusero che si trattava della medesima fase e proposero di discreditare il nome riversideite. Taylor (1953a) riesaminò alcuni campioni indicati come
Fig. 5.8 – Composizione chimica, espressa come % in atomi per unità formula, delle cavità dei campioni di
96
riversideite e formati da soffici aggregati fibrosi bianchi. I diffrattogrammi di polveri indicarono la presenza dei riflessi basali a 14.0 e 11.2 Å caratteristici di plombièrite e tobermorite ma non il riflesso basale a 9.3 Å che dovrebbe caratterizzare la riversideite. Taylor (1953a) osservò invece ulteriori riflessi attribuiti alla wilkeite (nome “discreditato” che indica una ellestadite-(F), minerale appartenente al gruppo delle apatiti; Rouse & Dunn, 1982; Pasero et al., 2010). I dati diffrattometrici riportati da Taylor (1953a) sono in accordo con quelli della crestmoreite di Flint et
al. (1938) e quelli di Clark & Bunn (1940). Pertanto riversideite e crestmoreite sono delle
intercrescite di tobermorite ed ellestadite-(F). Come già detto, nel 1954 McConnell propose uno schema nomenclaturale per i minerali appartenenti al gruppo della tobermorite; egli assunse che le fasi aventi periodicità basali di 11 e 9 Å potessero subire una rapida idratazione con conseguente aumento di tale periodicità a meno di una adeguata conservazione. McConnell (1954) ipotizzò pertanto che i campioni di Eakle studiati da Flint et al. (1938) e Taylor (1953a) fossero in realtà dei campioni di riversideite (tobermorite 9 Å) i quali, in seguito ad una impropria conservazione, si erano idratati passando alla fase a 11 Å (McConnell, 1954)
La tobermorite 9 Å è stata ottenuta frequentemente quale prodotto di riscaldamento di tobermoriti “normali”. Non sono invece note segnalazioni naturali sicure di questa fase. Gross (1977) descrive succintamente la presenza di riversideite nella Hatrurim Formation (Israele), in stretta associazione con le altre fasi del gruppo della tobermorite. Marincea et al. (2001), descrivendo le paragenesi idrotermali derivanti dall’alterazione di skarn a spurrite, tilleyite e gehlenite di Cornet Hill (Apuseni Mountains, Romania), riportano la presenza di una fase a 9 Å; essa forma fibre lunghe fino a 50 μm, strettamente associate a plombièrite. La presenza di fasi cr iptocristalline e la stretta associazione con la plombièrite rendono molto difficoltosa l’analisi chimica. Marincea et al. (2001) riportano un’unica analisi chimica, condotta in microsonda elettronica, sulla riversideite rumena; essi hanno ricalcolato il contenuto in H2O sulla base della formula Ca5Si6O16(OH)2·2H2O
(Mandarino, 1999). Bonaccorsi & Merlino (2005) riportano invece la formula Ca5Si6O16(OH)2. La
risoluzione da parte di Merlino et al. (2001) della struttura della “clinotobermorite-9 Å” ottenuta disidratando un campione di clinotobermorite a 300°C ha mostrato la totale perdita di molecole di H2
I dati presenti in letteratura non consentono di poter affermare con certezza l’esistenza in natura di una tobermorite 9 Å; pertanto riteniamo che la riversideite meriti lo status di specie questionabile Q in attesa di future ricerche sui campioni naturali caratterizzati da periodicità basali di 9 Å.
O e la presenza di gruppi OH. Molto probabilmente la stessa composizione è mostrata dalla fase a 9 Å con simmetria di famiglia ortorombica.
97
5.3 Riconoscimento delle fasi del gruppo della tobermorite da
diffrattogrammi di polvere
La natura microcristallina presentata sovente dai campioni di minerali appartenenti al gruppo della tobermorite ne preclude lo studio con tecniche di cristallo singolo e pertanto per la loro corretta caratterizzazione si deve ricorrere alla diffrattometria di polveri.
La distinzione fra le fasi a 14, 11 e 9 Å risulta agevole, per la presenza del caratteristico riflesso basale 002 a 14.0, 11.3 e 9.3 Å rispettivamente. Necessita invece maggiore attenzione la distinzione fra fasi con simmetria di famiglia monoclina ed ortorombica e soprattutto fra gli eventuali politipi presenti nel campione. Generalmente i diffrattogrammi di polveri raccolti utilizzando radiazioni convenzionali mostrano i soli riflessi di famiglia, consentendo quindi una distinzioni fra fasi con simmetria di famiglia monoclina ed ortorombica ma di fatto rendendo impossibile l’eventuale ulteriore distinzione dei politipi presenti. Quest’ultima è possibile utilizzando radiazioni molto brillanti (luce di sincrotrone) e/o nel caso di cristalli di
eccezionale qualità, come ad esempio avviene nel caso dei campioni di tobermorite provenienti dalla N’Chwaning II mine (Kalahari Manganese Field, Repubblica Sudafricana).
Nel corso di questa tesi di dottorato abbiamo affrontato la problematica legata alla distinzione, con tecniche di polveri, di campioni di tobermorite da campioni di clinotobermorite.
Come è noto, il diffrattogramma di polveri contiene informazioni geometriche e strutturali relative al campione studiato: la posizione dei picchi è infatti funzione delle costanti reticolari del minerale mentre l’intensità della diffrazione è legata al fattore di struttura Fhkl del riflesso hkl e quindi alla
distribuzione della densità elettronica all’interno della cella unitaria. La risoluzione della struttura dei minerali del gruppo della tobermorite da parte di Merlino et al. (1999, 2000, 2001) e di Bonaccorsi et al. (2005) consente pertanto di poter ottenere dei diffrattogrammi di polveri calcolati da comparare con quelli osservati.
Fig. 5.9 – Differenze nel diffrattogramma di polveri di
clinotobermorite (in rosso) e tobermorite (in nero). La clinotobermorite mostra due riflessi a 5.59 e 5.28 Å mentre la tobermorite ne presenta uno a 5.45 Å. Sull’asse delle ascisse i valori angolari, in 2θ, sono riferiti alla radiazione CuKα.
98
Le differenze fra le celle di famiglia di tobermorite e clinotobermorite portano a differenti posizioni di alcuni riflessi. Se consideriamo ad esempio la regione compresa fra 5 e 6 Å (fig. 5.9), nel diffrattogramma di polveri della tobermorite osserveremo un riflesso a ~ 5.45 Å, corrispondente al riflesso 101 (indicizzato sulla base della sottocella); nei diffrattogrammi della clinotobermorite, invece, in tale posizione non compare alcun riflesso ma sono presenti due riflessi a ~5.59 e ~5.28 Å, corrispondenti rispettivamente agli indici 100 e 102 nella sottocella della clinotobermorite. Un’altra regione del diffrattogramma di polveri in grado di consentire il riconoscimento è compresa fra 2.95 e 3.10 Å. La tobermorite presenta due riflessi di intensità simile a valori dhkl pari a 3.088 e 2.978 Å;
la clinotobermorite presenta invece due riflessi a valori di dhkl
Il riconoscimento dei vari politipi attraverso diffrattogrammi di polvere, benché possibile, è tuttavia legato ad un’ottima qualità dei dati (alto rapporto segnale/fondo) e ad una buona cristallinità del campione studiato. La necessità di un elevato rapporto segnale/fondo deriva dalla usuale debolezza dei riflessi di superstruttura mentre la buona cristallinità tende a prevenire l’eccessivo allargamento ed indebolimento di tali riflessi.
pari a 3.07 e 3.01 Å, con il secondo riflesso più intenso del primo. Un ulteriore elemento distintivo è il riflesso 215 della clinotobermorite, che cade a 1.92 Å. Tuttavia, l’utilizzo di quest’ultimo riflesso come elemento diagnostico deve prevedere la verifica dell’assenza di calcite. Quest’ultima fase è spesso intimamente associata a campioni microcristallini di tobermorite/clinotobermorite e presenta un riflesso proprio attorno a 1.92 Å.
5.4 Studi spettroscopici sui minerali del gruppo della tobermorite
5.4.1 Spettroscopia NMR
La natura microcristallina e spesso disordinata delle fasi del gruppo della tobermorite, siano esse naturali o sintetiche, ha visto il fiorire, negli ultimi trent’anni, di una serie di studi spettroscopici volti alla comprensione della struttura locale di queste fasi minerali. Nel corso di questo lavoro di dottorato abbiamo utilizzato, in particolare, le spettroscopie 29
Il primo lavoro dedicato alla spettroscopia NMR sulle fasi del gruppo della tobermorite si deve a Wieker et al. (1982). Questi autori utilizzarono i risultati dello studio di Lippmaa et al. (1980) i quali mostrarono la dipendenza fra il chemical shift ed il grado di polimerizzazione dei tetraedri silicatici. L’intervallo degli “spostamenti chimici” del
Si NMR e micro-Raman.
29
Si (fig. 5.9A, 5.9B) è stato suddiviso in intervalli dipendenti dal numero di ossigeni condivisi dai tetraedri silicatici: Q0, Q1, Q2, Q3 e Q4 (Engelhardt et al., 1973). Nelle fig. 5.9C e 5.9D sono indicati gli intervalli relativi a Q4(nAl) e
99
Fig. 5.10 – Intervalli dello spostamento chimico per silicati con differenti gradi di polimerizzazione (da
Kirkpatrick et al., 1985).
Q3(nAl). Questi intervalli sono poi stati a loro volta suddivisi in funzione del numero di tetraedri primi vicini contenenti Al3+ in sostituzione di Si4+.
Gli studi hanno consentito di ottenere informazioni sul grado di polimerizzazione delle catene silicatiche di tobermoriti naturali e sintetiche. Wieker et al. (1982) evidenziarono la presenza di catene singole nelle fasi a 14 Å, 9 Å e nelle fasi a 11 Å ottenute per disidratazione di tobermoriti 14 Å; le tobermoriti 11 Å ottenute attraverso la sintesi idrotermale mostravano invece catene doppie. Successivamente vari autori hanno ottenuto dati spettroscopici su campioni di silicati idrati di calcio e, in particolare, su esemplari di tobermoriti (Young, 1988; Grutzeck et al., 1989; Okada et al., 1994; Cong & Kirkpatrick, 1996b; Brunet et al., 2004). Oltre ad utilizzare l’isotopo 29Si, alcuni autori hanno riportato dati anche riguardo agli isotopi 17O (Cong & Kirkpatrick, 1996a; Cong & Kirkpatrick, 1996c) e 27Al (Andersen et al., 2003).
5.4.2 Spettroscopia micro-Raman
L’uso della spettroscopia micro-Raman nella caratterizzazione di vari materiali cementizi è cominciata oltre 30 anni fa (Bensted, 1976). Uno dei principali vantaggi è rappresentato dalla possibilità di effettuare studi in situ, senza dover affrontare alcuna preparazione del campione. In tal
100
modo è stato possibile studiare le reazioni di idratazione, carbonatazione e degradazione dei cementi, oltre a poter identificare anche piccolissimi quantitativi di materiale (Potgieter-Vermaak et
al., 2006).
La spettroscopia Raman rileva le variazioni nella frequenza di un laser causate dalle interazioni con i modi vibrazionali in un cristallo o in una molecola. Si tratta di una tecnica spettroscopica sensibile alla struttura locale e che quindi non richiede una periodicità a lungo raggio, richiesta invece negli esperimenti di diffrazione. Recenti studi sui silicati idrati di calcio effettuati con tale tecnica sono stati condotti da Kirkpatrick et al. (1997) e da Garbev et al. (2007).
A causa della bassa elettronegatività del calcio, è possibile assumere che le interazioni fra le vibrazioni che coinvolgono gli atomi di Ca e quelle derivanti dalla parte silicatica siano trascurabili; in tal modo è possibile identificare le vibrazioni degli anioni [SiO4]4-. L’interpretazione degli spettri
è di tipo empirico ed è basata sul confronto con le frequenze osservate da altri autori (Kirkpatrick et
al., 1997; Garbev et al., 2007). In tabella 5.12 sono riportati gli intervalli di frequenza osservati nei
silicati idrati di calcio e le relative interpretazioni.
Tab. 5.12 – Intervalli di frequenza e assegnazione delle bande osservate negli spettri Raman delle fasi C-S-H (da Kirkpatrick et al., 1997).
Frequenza o intervallo di frequenza Interpretazione
1077 Stretching simmetrico (SS) del legame C-O nei gruppi
carbonato
800 – 1080 SS dei tetraedri Si-O
1080 SS dei tetraedri Q3
950-1010 SS dei tetraedri Q2
870-900 SS dei tetraedri Q1
740 Bending simmetrico (SB) nel piano O-C-O nei gruppi
carbonato
600-700 SB dei legami Si-O-Si. Può esservi il contributo dato
dalle deformazioni dei poliedri Ca-O
650-680 SB dei tetraedri Q2
600-630 SB dei tetraedri Q3
430-540 Deformazioni interne dei tetraedri Si-O (bending dei
legami O-Si-O)
300-350 Vibrazioni dei poliedri Ca-O
<280 Vibrazioni complesse, fino ad oggi non comprese.
101
5.5 Comportamento termico dei minerali del gruppo della tobermorite
Come più volte rimarcato, le fasi a 14, 11 e 9 Å appartenenti al gruppo della tobermorite differiscono fra loro per il differente grado di idratazione. Molto interessante risulta anche il comportamento termico di queste fasi, legato alla loro progressiva disidratazione.
La tobermorite 14 Å passa ad una fase a 11 Å a temperature di 80-100°C, per poi trasformarsi nella fase a 9 Å a circa 300°C. La tobermorite 11 Å presenta invece un comportamento molto complesso, divisibile in almeno due differenti tipi: comportamento “normale”, nel quale la tobermorite 11 Å si trasforma nella fase a 9 Å a circa 300°C, e comportamento “anomalo”, nel quale la fase a 11 Å persiste come tale anche oltre i 300°C. Campioni aventi un comportamento “normale” sono stati descritti a Crestmore (California, USA; Taylor, 1953b; Farmer et al., 1966), Ballycraigy (Irlanda del Nord; McConnell, 1954), Fuka (Giappone; Mitsuda et al., 1972), Urali (Russia; Merlino et al., 2001) e Montalto di Castro (Viterbo; Merlino et al., 2008). Al contrario tobermoriti provenienti da Loch Eynort (Scozia; Gard & Taylor, 1957), Heguri (Giappone; Mitsuda, 1973), San Vito di Leguzzano (Vicenza; Merlino et al., 2008) e dal Kalahari Manganese Field (Repubblica Sudafricana; Merlino et al., 2000) hanno mostrato il cosiddetto comportamento “anomalo”.
Mitsuda & Taylor (1978) hanno studiato tredici campioni naturali di tobermorite i quali mostravano differenti comportamenti; fra essi hanno individuato un terzo tipo di comportamento, definito “misto”. Si tratta di un comportamento termico intermedio fra quello “normale” ed “anomalo”; a 300°C permane il riflesso basale a 11 Å ma compare anche quello a 9.3 Å. Alcuni campioni studiati da Mitsuda & Taylor (1978) mostravano un comportamento ancora più complesso; ad esempio la tobermorite 14 Å proveniente da Crestmore (California, USA) passava alla fase a 11 Å a 90°C e a quella a 9 Å a 300°C. Tuttavia, a 900°C, quest’ultima si trasformava in una nuova fase con periodicità basale di circa 10 Å. Analogamente, un campione di tobermorite 14 Å proveniente da Bingham (Utah, USA) mostrava un comportamento “normale” ma, a 700°C, si trasformava in una fase a 10 Å. Merlino et al. (2008) hanno osservato come la tobermorite sudafricana presentasse un comportamento “anomalo” ma, sorprendentemente, al di sopra di 420°C, si trasformasse in una tobermorite 10 Å. Da questi pochi esempi risulta evidente quanto sia complesso il comportamento termico dei minerali del gruppo della tobermorite. Merlino et al. (1999) hanno ipotizzato che la differenza fra comportamento “normale” ed “anomalo” mostrato dai campioni di tobermorite 11 Å sia legato alla concentrazione di cationi Ca2+ all’interno delle cavità strutturali. Questi cationi sono legati a molecole di H2O zeolitica e la disidratazione dei campioni porta ad una coordinazione
incompleta dei cationi Ca2+, con il successivo riarrangiamento strutturale atto a ricreare una adeguata coordinazione attorno al Ca, con la decondensazione delle catene e la comparsa della fase a 9 Å (comportamento “normale”). Al contrario, l’assenza di Ca non richiede sostanziali modifiche




![Fig. 5.7 – Struttura della fukalite, vista lungo [100]. In verde: strati tipo tilleyite; in azzurro: strati tipo tobermorite; in giallo: gruppi disilicato; in nero: gruppi carbonato](https://thumb-eu.123doks.com/thumbv2/123dokorg/7531243.107078/10.892.120.778.716.1016/struttura-fukalite-strati-tilleyite-azzurro-tobermorite-disilicato-carbonato.webp)