Le Complicazioni delle Fratture
Le complicazioni che si possono presentare in un soggetto fratturato sono molteplici; possono essere immediate, precoci o tardive a seconda che si verifichino contemporaneamente alla frattura, nei primi due-tre giorni, oppure nelle prime settimane o dopo alcuni mesi dalla data del trauma (Mancini & Morlacchi, 2002). Alcune di queste sono spesso sottostimate nei nostri animali per le difficoltà diagnostiche ed interpretative soprattutto a lunga distanza.
In un soggetto traumatizzato si possono avere compromissioni generali e
locali (Schemitsch & Bhandari, 2001; Mancini & Morlacchi, 2002).
4.1 COMPLICAZIONI GENERALI
• Shock: complicazione immediata, che spesso accompagna le più gravi fratture diafisarie degli arti, le fratture di bacino e di colonna, ecc..
• Embolia adiposa: complicazione precoce, rara, di fratture multiple, soprattutto se localizzate alle ossa lunghe provviste di abbondante midollo (femore, ecc.).
• Tromboembolia: altra complicazione precoce che spesso rappresenta l’evoluzione di processi flebotrombotici o tromboflebitici.
In tutti questi casi è necessario effettuare una diagnosi e un trattamento tempestivo in quanto esitano rapidamente nella morte del soggetto (Schemitsch & Bhandari, 2001; Mancini & Morlacchi, 2002).
Tra le complicazioni generali tardive, alle quali sono particolarmente esposti i soggetti anziani, sono da ricordare:
• Broncopolmoniti: per ipoventilazione polmonare.
• Piaghe da decubito: dovute a iperflessione delle sporgenze ossee sulla cute distrofica (Schemitsch & Bhandari, 2001; Mancini & Morlacchi, 2002).
4.2 COMPLICAZIONI LOCALI 4.2.a Complicazioni locali immediate
Le complicazioni locali immediate possono essere cutanee, articolari, viscerali, vascolari e nervose (Schemitsch & Bhandari, 2001; Mancini & Morlacchi, 2002).
• Cutanee: l’esposizione della frattura rappresenta una delle più temibili complicazioni locali. L’eventuale inquinamento del focolaio da parte di germi penetrati dall’esterno dà facilmente origine a osteomielite.
• Articolari: l’associazione della frattura alla lussazione del capo articolare di uno dei due frammenti (“frattura-lussazione”) aggrava la prognosi.
• Viscerali: sono tipiche quelle della pleura o dei polmoni nelle fratture costali scomposte e lo pneumotorace in seguito a fratture di omero e di scapola; anche se non frequente, si può riscontrare rottura della vescica o dell’uretra a causa di fratture pelviche.
• Vascolari: consistono generalmente nella contusione di vasi contigui al focolaio di frattura, con conseguente vasospasmo e trombosi. La lacerazione delle paresi vasali è invece più rara.
• Nervose: comprendono le lesioni midollari e quelle radicolari (che complicano le fratture vertebrali) oltre alle lesioni dei tronchi nervosi che contraggono stretti rapporti anatomici con i segmenti scheletrici sedi di frattura. I tronchi nervosi più facilmente interessati sono: il n. radiale in caso di fratture della diafisi omerale, il n. mediano e il n. radiale nelle fratture sovracondiloidee dell’omero, il n. sciatico spesso coinvolto nelle fratture-lussazioni dell’acetabolo e il n. peroneo nelle fratture della fibula.
4.2.b Complicazioni locali precoci
Tra le complicazioni locali precoci si possono ricordare (Schemitsch & Bhandari, 2001; Mancini & Morlacchi, 2002):
• La sindrome di Volkmann: è una sindrome ischemica che determina sclerosi avascolare di tutti i tessuti molli dell’avambraccio e della mano con successiva retrazione dei flessori; causa forte contrattura in flessione sia il carpo che le dita ed è pressoché esclusivo delle fratture sovracondiloidee dell’omero.
• L’infezione del focolaio di frattura: rappresenta l’evoluzione sfavorevole di una frattura esposta, trattata inadeguatamente o non tempestivamente. Può derivarne osteomielite e quindi anche un disturbo di consolidazione.
4.2.c Complicazioni tardive
Le complicazioni tardive più comuni includono la “malattia da frattura”, disturbi di consolidazione, malunioni, disturbi dell’accrescimento ed osteomieliti (Denny, 1998; Jackson & Pacchiana, 2004).
Malattia da frattura
Il termine “malattia da frattura” è stato utilizzato da Muller (1963) per descrivere la sindrome da esaurimento muscolare, rigidità articolare ed osteoporosi che derivano dall’immobilizzazione prolungata dell’arto durante la guarigione della frattura (Denny, 1998).
La malattia da frattura rappresenta una reale complicanza del trattamento delle fratture; è caratterizzata da atrofia dei tessuti molli, delle unghie e della cute, in associazione agli effetti sulle articolazioni, quali alterazioni della cartilagine e della capsula articolare (Herron, 2001).
Questi effetti sono più comunemente collegati ad immobilizzazioni esterne per mezzo di ingessature, ma possono conseguire anche ad altri metodi di fissazione esterna o interna (Herron, 2001).
Le cause che provocano questa patologia non sono state ben determinate, ma sembrano essere multiple; non esiste alcun trattamento soddisfacente per questa condizione, per cui è importante compiere ogni tentativo per prevenirla (Herron, 2001).
Il carico funzionale dell’arto, per esempio, sembra avere un effetto preventivo sull’insorgenza di questa affezione, per cui si dovrebbe impiegare una fissazione stabile della frattura che consenta all’arto il ritorno più precoce possibile al normale carico funzionale (Herron, 2001).
L’effettuazione di una fissazione interna rigida della frattura, mediante placca da osteosintesi, permette in genere di mobilizzare precocemente e senza dolore l’arto ed evitare quindi questa complicazione (Denny, 1998).
Disturbi di consolidazione
Per disturbo di consolidazione si intende ogni alterazione del normale processo riparativo di una frattura: la frattura consolida ugualmente ma in un tempo più lungo (ritardo di consolidazione), oppure non consolida affatto (pseudoartrosi) (Mancini & Morlacchi, 2002).
Queste due patologie rappresentano essenzialmente fasi e gradi di gravità diverse dello stesso evento patologico (Hoefle, 2001).
I fattori (Mancini & Morlacchi, 2002) che predispongono all’instaurarsi di un disturbo di consolidazione sono:
• la sede della frattura; • il tipo di frattura;
• la plurifocalità delle fratture in uno stesso arto.
Per quanto riguarda il primo fattore appaiono maggiormente esposte ai disturbi di consolidazione le fratture diafisarie rispetto a quelle metafisarie;
questo è la conseguenza di una maggior vascolarizzazione della metafisi, più ricca di osso spongioso, rispetto alla diafisi (Mancini & Morlacchi, 2002). Analogamente, tra due fratture diafisarie appartenenti a segmenti scheletrici diversi, andrà meno facilmente incontro ad un disturbo di consolidazione il focolaio contornato da più abbondanti masse muscolari; le ossa dell’avambraccio sono coperte da pochi tessuti molli e per questo sono più soggette a questo tipo di complicazioni (Mancini & Morlacchi, 2002).
Per quanto riguarda il tipo di frattura, tendono a riparare più facilmente quelle che presentano una maggior superficie di contatto tra i frammenti; le fratture spiroidi, ad esempio, consolidano più facilmente rispetto alle trasverse (Mancini & Morlacchi, 2002).
Nei casi nei quali si hanno due focolai di frattura nello stesso segmento scheletrico o nello stesso arto, uno solo tende a consolidare entro i normali tempi previsti: i poteri riparativi sembrano “polarizzarsi” su un focolaio ed indirizzarsi secondariamente sull’altro solo quando il primo è ormai pressoché consolidato; in questo caso si può parlare di interferenze di consolidazione (Mancini & Morlacchi, 2002).
Ritardi di consolidamento e pseudoartrosi riconoscono le stesse cause (Denny, 1998; Mancini & Morlacchi, 2002):
1) il movimento reciproco dei frammenti;
2) la diastasi, cioè l’allontanamento reciproco delle superfici di frattura, dovuto a:
a. interposizione di tessuti molli
b. cattivo allineamento dei frammenti
c. distrazione dei frammenti per trazione od uso improprio dei mezzi di fissazione interna
4) la compromissione dell’apporto vascolare endostale, periostale o parostale per:
a. danno ai vasi nutritizi dell’osso
b. eccessivo scollamento o danneggiamento periostale
c. grave comminuzione
5) i fattori generali che rallentano la guarigione delle fratture.
Ognuno di questi fattori può determinare da solo sia un ritardo di consolidazione che una pseudoartrosi. L’evoluzione verso l’una o l’altra forma dipende dalla durata e gravità del danno prodotto sul tessuto interframmentario (Mancini & Morlacchi, 2002).
Ritardo di consolidamento
:
Si parla di unioni ritardate quando una frattura non ha consolidato nel tempo previsto per quel tipo di frattura, in quella sede, in un paziente di quell’età, pur essendo evidente una certa attività ossea (Mancini & Morlacchi, 2002; Brunetti & Petruzzi, 2005).
La causa più comune è l’immobilizzazione inadeguata dei monconi ossei; la guarigione della frattura evolverà quindi in presenza di un certo grado di tensione; la presenza di un discreto grado di flessione è tollerata, mentre la torsione e la rotazione impediscono la guarigione in quanto determinano uno stiramento della rete fibroblastica del callo osseo (Denny, 1998; Jackson & Pacchiana, 2004).
Clinicamente, nonostante il tempo intercorso, persiste algia in sede di frattura; l’animale presenta zoppia, atrofia muscolare, ridotto range del movimento delle articolazioni prossimale e distale alla frattura e si può riscontrare una motilità preternaturale (Mancini & Morlacchi, 2002; Millis & Jackson, 2005). Le fratture del terzo distale di radio ed ulna rappresentano il sito più comune di unione ritardata (DeAngelis, 1975).
Radiograficamente, l’immagine del callo endostale è scarsa, per cui la rima di frattura resta visibile. A differenza di quanto si riscontra nella pseudoartrosi, tuttavia, il callo periostale non appare interrotto a livello della rima di frattura, i canali midollari non sono obliterati e i margini della frattura non presentano note di sclerosi (Mancini & Morlacchi, 2002).
Nelle immagini radiografiche riprese nel tempo, è possibile rilevare i segni di un’attività ossea progressiva, ossia di un aumento della radiopacità a livello delle linee di frattura (Johnson & Hulse, 2004a).
Pseudoartrosi
Si intende comunemente per pseudoatrosi postraumatica o non unione la frattura non consolidata e non consolidabile se non con l’ausilio di adeguati provvedimenti chirurgici, quali toilette del focolaio, apposizione di un trapianto, ecc. (Mancini & Morlacchi, 2002).
La pseudoartrosi (figura 4.2.c1) è l’espressione tipica del vero e proprio fallimento biologico dell’intero processo di callogenesi (Einhorn, 1998) in cui il processo osteogenetico si blocca nella fase di callo fibroso (Marchetti, 1988).
Generalmente la causa è da ricercare in un’errata scelta d’intervento e in errori tecnici del chirurgo, piuttosto che in cedimenti biologici imputabili al paziente (Johnson & Hulse, 2004a).
Il termine pseudoartrosi, dal greco “falsa articolazione”, può indurre a ritenere che questo disturbo sia costantemente caratterizzato da grossolana mobilità interframmentaria (Mancini & Morlacchi, 2002); in realtà le manifestazioni cliniche di mancata unione possono essere assai variabili.
Figura 4.2.c1: Schema del processo di formazione del
callo osseo normale e di non unione in una frattura diafisaria (Brunetti & Petruzzi, 2005).
Weber e Cech (1976) hanno classificato le pseudoartrosi in due ampi gruppi: 1) pseudoartrosi biologicamente attive o vitali;
2) pseudoartrosi biologicamente inattive o non-vitali.
Il gruppo delle biologicamente attive è caratterizzato da scarsa o irrilevante motilità preternaturale (pseudoartrosi serrate) per la formazione di un manicotto di callo fibrocartilagineo che, pur non saldando tra loro i capi ossei, li mantiene vicini e in qualche modo solidali. L’assenza di dolore ai tentativi di mobilizzazione interframmentaria è il risultato della natura cronica del processo. Coesistono spesso turbe trofiche a carico della cute, ipotrofia muscolare e deficit funzionale dell’arto (Marchetti, 1988; Mancini & Morlacchi, 2002).
Le pseudoartrosi vitali si distinguono a loro volta in tre tipi (Denny, 1998; Jackson & Pacchiana, 2004; Millis & Jackson, 2005):
I. Tipo ipertrofico: si forma tipicamente un callo a forma di “zampa d’elefante”, ben vascolarizzato, che non copre la distanza tra i monconi; nella lacuna tra i capi della frattura sono presenti
cartilagine e tessuto fibroso. È presente inoltre sclerosi dei monconi ossei e, in seguito, la cavità midollare tende ad occludersi. Possono derivare da inchiodamenti centromidollari delle fratture della diafisi omerale e femorale che permettono la rotazione sul focolaio di frattura. La pseudoartrosi ipertrofica può essere anche conseguenza di cerchiaggi lenti e/o di sequestri (frammenti ossei necrotici) sul sito di frattura.
II. Tipo debolmente ipertrofico: in questo tipo di non-unione vi è minima formazione di callo ed è moderatamente instabile; è causata da instabilità a seguito della fissazione con placca. Questo tipo di non unione viene a volte definita “a zoccolo di cavallo”.
III. Tipo oligotrofico: in questo caso non vi è formazione di callo ed i frammenti sono in genere ampiamente separati e connessi solamente da tessuto fibroso. Il fallimento nel trattamento di una frattura da avulsione con la fissazione interna conduce in genere ad una pseudoartrosi oligotrofica.
Le pseudoatrosi biologicamente non attive si distinguono per: motilità preternaturale (per questo vengono anche definite pseudoartrosi lasse), assenza di dolore, impotenza funzionale ai movimenti attivi e al carico (Mancini & Morlacchi, 2002).
Radiograficamente non si rilevano segni di reazione ossea a livello del focolaio di frattura ed i capi ossei appaiono diastasati e sclerotici; la rima di frattura è colma di tessuto fibroso e le cavità midollari sono chiuse da osso corticale (Johnson & Hulse, 2004a).
Si classificano in quattro tipi (Denny, 1998; Jackson & Pacchiana, 2004; Millis & Jackson, 2005):
I. Tipo distrofico: si presenta come complicazione di fratture comminute dove uno o più frammenti scarsamente vascolarizzati ne
impediscono la guarigione. I frammenti non vitali, infatti, non sono in grado di formare un ponte tra gli altri frammenti. Questo tipo di non unione è più comune nei soggetti geriatrici.
II. Tipo necrotico: consegue a fratture comminute o infette in cui frammenti non vitali rimangono vicino al focolaio di frattura come fossero dei sequestri; in questo modo impediscono il normale consolidamento.
III. Tipo da perdita di sostanza: il difetto è, di solito, un risultato del trauma originale, ma può anche essere dovuto ad un sequestro, ad un riassorbimento o ad una rimozione dei frammenti al momento dell’intervento chirurgico; se la perdita di sostanza è troppo ampia non può essere ricolmata dal processo di guarigione.
IV. Tipo atrofico: rappresenta il risultato finale degli altri tre tipi; generalmente si presenta come complicazione delle fratture di radio e ulna nei cani di piccola taglia ed in particolare nei barboncini toy. Sul sito di frattura è presente instabilità, con perdita dell’attività osteogenica, osteoporosi ed eventualmente anche osteolisi.
Malconsolidamento
Si definiscono consolidamenti errati o malunioni le fratture guarite in cui non si è ottenuto o mantenuto durante la guarigione un corretto allineamento anatomico (Johnson & Hulse, 2004a).
Le cause sono da ricercarsi in difetti di terapia: un’impropria riduzione e/o immobilizzazione (Mancini & Morlacchi, 2002).
In rapporto allo spostamento residuo dei frammenti di frattura i consolidamenti errati si distinguono in (Mancini & Morlacchi, 2002):
• angolari: con deformità in valgismo, in varismo, in recurvato e in procurvato;
• con decalage o rotazione di un frammento rispetto all’altro.
La consolidazione avvenuta con incompleto ripristino della morfologia scheletrica può decorrere senza alcun disturbo. Oltrepassati però certi limiti intervengono alterazioni funzionali della deambulazione per le quali si rende necessaria la correzione chirurgica della deformità (Mancini & Morlacchi, 2002).
Le deformazioni angolari sono caratterizzate dalla perdita del corretto parallelismo fra le articolazioni situate prossimalmente e distalmente all’osso che, se gravi, possono avere effetti deleteri sulla funzionalità dell’arto e indurre osteoartrite delle articolazioni adiacenti (Johnson & Hulse, 2004a). Per quanto riguarda i consolidamenti errati con accorciamento, se la riduzione della lunghezza interessa un sistema osseo singolo, come nel caso del femore, dell’omero, è possibile un certo grado di compensazione con l’estensione delle articolazioni adiacenti; se invece viene coinvolto un segmento osseo normalmente appaiato ad un altro (radio/ulna, tibia/fibula) si ha una perdita di congruenza e di allineamento delle articolazioni adiacenti (Johnson & Hulse, 2004a).
Le deformazioni rotazionali sono quelle meno tollerate e nella maggior parte dei casi si hanno a carico delle fratture femorali non adeguatamente stabilizzate e possono influire negativamente sulla funzionalità dell’anca e del ginocchio (Johnson & Hulse, 2004a).
Per la correzione della deformità in genere è necessaria un’osteotomia e in seguito l’applicazione di un’adeguata fissazione fino a quando la guarigione sia completata (Hoefle, 2001).
Disturbi dell’accrescimento
Le fratture fisarie costituiscono approssimativamente il 30% della totalità delle soluzioni di continuo dell’osso negli animali che non hanno ancora raggiunto la maturità scheletrica; un trauma ad una cartilagine di accrescimento, con o senza frattura, può determinare una chiusura precoce della cartilagine stessa ed esitare in un accorciamento o in deformità angolare dell’arto (Johnson & Hulse, 2004a; Jackson & Pacchiana, 2004).
La fisi è tradizionalmente divisa in quattro zone (Boudrieau, 2005):
1. Zona di riserva: immediatamente vicina all’epifisi; è qui che avviene la divisione cellulare casuale dei condrociti e la produzione della matrice. 2. Zona di proliferazione: la divisione dei condrociti avviene in maniera
lineare; le vere cellule germinali della fisi sono quelle più vicine all’epifisi, alla base di ogni colonna cellulare. La divisione cellulare di questi condrociti si verifica nelle colonne che si estendono lontano dall’epifisi e contemporaneamente si modifica la loro forma che da rotonda o ovale diventa appiattita. Questa è, inoltre, un’area di forte produzione della matrice.
3. Zona ipertrofica: i condrociti appiattiti si estendono gradualmente da un terminale all’altro di questa zona ed assumono forma cuboidale aumentando molto il loro volume. La matrice si riduce notevolmente e subisce dei cambiamenti biochimici che la preparano alla seguente calcificazione.
4. Zona di calcificazione provvisoria: in questa zona avviene la disseminazione della matrice con fosfato di calcio amorfo, che porta alla formazione dei cristalli di idrossiapatite e alla seguente calcificazione dei setti longitudinali della matrice.
La fisi risulta più debole dell’osso e dei legamenti circostanti ed in particolare la zona ipertrofica, perché formata da cellule relativamente grandi rispetto alla quantità di matrice presente (Johnson & Hulse, 2004a).
Le forze di avulsione o di taglio possono causare attraverso questa zona delle fratture che guariscono rapidamente grazie alla continua crescita della cartilagine fisaria e alla formazione del callo metafisario. Una volta colmati gli spazi di frattura, la normale ossificazione encondrale riprende e la fisi mantiene la sua funzione. Tuttavia se il danno interessa le cellule in accrescimento (cioè della zona di riserva e di proliferazione, la crescita della cartilagine fisaria non avviene; procede, al contrario, l’ossificazione encondrale con formazione dell’osso negli spazi di frattura che esita nella chiusura prematura della fisi (Johnson & Hulse, 2004a).
Il malallineamento della fisi fratturata, in cui l’osso epifisario e metafisario vengono a contatto, permette la guarigione dell’osso trabecolare e la formazione di un ponte fisario che può impedire la normale funzione della fisi (Johnson & Hulse, 2004a).
La sede anatomica che presenta questo tipo di complicazione con maggior frequenza è l’avambraccio, in seguito a lesioni traumatiche di radio od ulna (Jackson & Pacchiana, 2004).
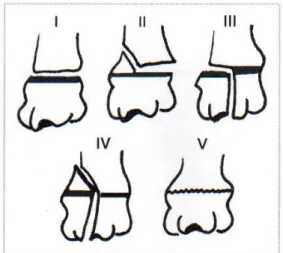
Per le fratture che interessano le epifisi e le fisi di accrescimento viene adottata generalmente la classificazione di Salter-Harris, che le suddivide in 5 tipi (Brunetti & Petruzzi, 2005), rappresentata nella figura 4.2.c2.
Figura 4.2.c2: Classificazione delle fratture
delle fisi di accrescimento, secondo lo scheda di Salter-Harris (Brunetti & Petruzzi, 2005).
Osteomielite
L’osteomielite è un processo infiammatorio che colpisce tutti i componenti anatomici dell’osso: midollo osseo, corticale e, a volte, periostio; può essere acuta o cronica (Johnson & Hulse, 2004b).
Gli agenti eziologici possono infettare l’osso per via ematogena o esogena; in caso di traumi o fratture i germi penetrano per via esogena (Jackson, Pacchiana, 2004).
I fattori responsabili di questa complicazione sono una combinazione della contaminazione batterica locale, deficit di vascolarizzazione ossea locale e instabilità del focolaio di frattura (Toal & Mitchell, 2002).
L’osteomielite post-traumatica è generalmente secondaria a fratture esposte nelle quali vi è comunicazione tra il focolaio di frattura ed una ferita cutanea (Jackson, Pacchiana, 2004).
Il periostio, che in condizioni normali fornisce un’adeguata difesa contro l’invasione da parte di organismi estranei, è danneggiato, per cui perde questa funzione protettiva e diviene estremamente suscettibile alle infezioni (Denny, 1998).
La contaminazione ossea avviene per contiguità attraverso la breccia cutanea; una comune fonte di inoculazione batterica è costituita, inoltre, dalla contaminazione del campo operatorio durante la riduzione a cielo aperto delle fratture (Johnson & Hulse, 2004b; Jackson, Pacchiana, 2004).
I microrganismi isolati più frequentemente dalle ossa infette nel cane includono vari tipi di Stafilococchi (in particolare S. aureus), Streptococchi, Pasteurella, Pseudomonas, Proteus, Klebsiella e coliformi (Vaughan, 1975) con una prevalenza (71%) dei gram positivi (Braden, 1991); le infezioni monomicrobiche sono più frequenti rispetto alle polimicrobiche (Jackson & Pacchiana, 2004).
Anche i batteri anaerobi possono essere coinvolti nelle infezioni ossee e si ritrovano di solito associati ad altri organismi; in particolare sono stati isolati:
Actinomyces spp., Clostridium spp., Peptostreptococcus spp., Bacteroides spp. e Fusobacterium spp. (Johnson & Hulse, 2004b).
Le infezioni possono essere suppurative o non suppurative ma le prime rappresentano l’incidenza maggiore (Jackson & Pacchiana, 2004).
Sebbene il tipo e la quantità di batteri inoculati siano fattori importanti nello sviluppo delle infezioni ossee, i batteri da soli non necessariamente causano osteomielite. Esistono, infatti, numerosi altri fattori (Johnson & Hulse, 2004b; Jackson & Pacchiana, 2004) coinvolti nella patogenesi dell’osteomielite post-traumatica, quali:
-
l’estensione delle lesioni dei tessuti molli e le alterazioni dell’apporto ematico;-
la formazione di un film biologico (glicocalice);-
la stabilità della riduzione della frattura.Il danno tissutale può essere provocato dal trauma oppure può verificarsi durante la procedura chirurgica; i tessuti traumatizzati e l’osso devitalizzato costituiscono un eccellente terreno di coltura per i batteri (Johnson & Hulse, 2004b).
Inoltre, la presenza di materiale estraneo quale mezzi di sintesi, fili da sutura, ecc., rappresenta un fattore favorevole addizionale alla proliferazione batterica (Tsukayama, 1999; Schemitsch, Bhandari, 2001).
Il glicocalice è un insieme di matrice batterica, detriti cellulari dell’ospite, proteine sieriche, ioni, carboidrati e fibronectina che avvolge le colonie e facilita l’adesione batterica; i batteri gram-positivi, infatti, possiedono recettori per la fibronectina, mentre i gram-negativi e gli anaerobi si legano alla matrice e alle proteine cellulari. Il film biologico inoltre protegge i batteri dalla fagocitosi, dagli anticorpi dell’ospite e dall’effetto degli antibiotici (Johnson & Hulse, 2004b; Jackson & Pacchiana, 2004).
L’osteomielite viene aggravata dall’instabilità della frattura: il movimento continuo ostacola la rivascolarizzazione degli spazi compresi tra le estremità ossee fratturate e ciò previene il raggiungimento dell’area da parte dei meccanismi di difesa dell’ospite (Johnson & Hulse, 2004b).
La contaminazione batterica primaria si realizza solo in un terzo delle fratture esposte; l’infezione batterica secondaria della ferita si sviluppa dopo 6-8 ore (Muller et al., 1970) e questo condiziona la scelta dei tempi d’intervento e del tipo di trattamento da effettuare.
Rispetto alla forma ematogena, l’osteomielite post-traumatica insorge in maniera meno brusca e denota, fin dall’inizio, un andamento torpido con tendenza alla fistolizzazione e cronicizzazione (Mancini & Morlacchi, 2002). Quando il focolaio di infezione è all’interno della cavità midollare, la diffusione all’interno di essa è rapida, il pus penetra nella corticale, scorre sotto il periostio, lo rompe e raggiunge l’esterno fuoriuscendo attraverso le fistolizzazioni cutanee. Alcune aree di osso corticale possono perdere l’apporto sanguigno e necrotizzarsi; si arriva alla formazione di sequestri demarcati da tessuto fibroso e da un’area di osso nuovo e denso, definita
cassa da morto (Denny, 1998).
I caratteri clinici dell’osteomielite variano a seconda dello stadio della malattia. La risposta iniziale dell’osso all’infezione è costituita dall’infiammazione: i tessuti molli della parte divengono caldi, iperemici, tumefatti e dolenti. L’animale spesso è piretico, depresso e parzialmente o completamente anoressico (Johnson & Hulse, 2004b).
I segni radiografici specifici variano a seconda dello stadio della malattia, della sede dell’infezione e della patogenicità degli organismi infettivi (Johnson & Hulse, 2004b).
Il primo segno di osteomielite acuta, costituito dalla tumefazione dei tessuti molli, può essere osservato già 24 ore dopo l’infezione. Le modificazioni ossee radiografiche non sono invece visibili, in genere, prima di due settimane
dall’infezione quando si possono rilevare aree di rarefazione ossea a livello delle metafisi o attorno agli impianti metallici (chiodi, viti o placche) utilizzate per stabilizzare la frattura. In seguito si può osservare un’ombra periostale con deposizione di nuovo osso lamellare orientato perpendicolarmente all’asse maggiore dell’osso (Johnson & Hulse, 2004b). una reazione periostale irregolare si può già notare a 7-10 giorni dall’inizio dell’infezione (Toal & Mitchell, 2002).
Col progredire dell’infezione diviene evidente la lisi del cavo midollare; possono svilupparsi dei sequestri, che si presentano più radiodensi rispetto all’osso circostante, e con la formazione dell’involucro (nuovo osso che circonda il sequestro), aree di sclerosi e lisi si alternano a livello dell’osso corticale e midollare delle sede di infezione (Johnson & Hulse, 2004b).