2. Materiali e metodi
2.1 Studio in vivo
Gli esperimenti sono stati realizzati su cavie di sesso maschile tipo Dunkin-Hartley (300-500 g) in osservanza della direttiva 86/609/CEE sulla sperimentazione animale, recepita in Italia con il D.L. 116/92.
Nella prima fase del disegno sperimentale si è proceduto alla realizzazione del modello di desensibilizzazione omologa in vivo mediante l’impianto sottocutaneo di minipompe osmotiche riempite con salbutamolo, realizzando un’esposizione continuativa e
prolungata al β2 agonista. Su questo modello è stata valutata la
responsività al carbacolo e al salbutamolo.
Dopo la realizzazione del modello di desensibilizzazione omologa, le seconda fase della sperimentazione prevedeva lo studio degli effetti prodotti dalla somministrazione cronica di montelukast in animali desensibilizzati mediante la valutazione della responsività al carbacolo e della risposta rilasciante al salbutamolo.
2.1.1 Modello di desensibilizzazione omologa
Sulla base del lavoro di Finney et al. (2000), il modello di
desensibilizzazione omologa è stato realizzato mediante
somministrazione cronica di salbutamolo ottenuta mediante l’impianto
sottocutaneo di micropompe osmotiche (Alzet).
L’intervento di impianto prevedeva l’anestesia dell’animale con una
dose di 25-30 mg/Kg di pentobarbitale sodico per via intraperitoneale. Di seguito, veniva effettuata un’incisione di 1,5 cm nella zona
interscapolare, lo scollamento del tessuto connettivo per mezzo di una pinza emostatica, l’inserimento della micropompa e la sutura della
ferita.
Nel gruppo di controllo le micropompe erano riempite con il veicolo (tampone fosfato sterile, pH 7), mentre nel gruppo di desensibilizzati le pompe contenevano una soluzione di salbutamolo di concentrazione tale da consentire il rilascio di 40 µg/Kg/h.
2.1.2 Studio funzionale
Le cavie venivano anestetizzate con una dose di 100 mg/Kg di pentobarbitale sodico e sacrificate mediante dissanguamento ascellare. Questa procedura risulta più utile della dislocazione cervicale nel conservare la funzionalità dell’organo in vitro.
L’albero tracheobronchiale veniva posto in una soluzione di
Krebs-Henseleit riscaldata a 37º e ossigenata con carbogeno. Di seguito, si procedeva velocemente alla pulizia dell’organo (toilettatura) allo
scopo di rimuovere i depositi adiposi e isolare il tessuto.
La trachea veniva divisa a metà e allestita utilizzando la tecnica del “preparato a zig zag aperto”. Questo metodo prevede il taglio
longitudinale della parte anteriore della trachea, così da risparmiare la muscolatura liscia localizzata nella parte posteriore dell’albero
tracheobronchiale. Con il bisturi venivano poi effettuati dei tagli laterali in maniera alternata per tutta la lunghezza del tessuto.
Da ciascun organo si ottenevano due porzioni, le cui estremità venivano legate con un filo ognuna ad un supporto fisso. I preparati venivano disposti in un bagno per organi isolati da 20 ml contenente la soluzione di Krebs termostatata a 37ºC e ossigenata con carbogeno.
L’altra estremità veniva legata con un filo ad una leva isometrica
unita ad un trasduttore (Grass mod.FTO3D), che registrava la tensione applicata dall’organo durante le risposte contrattili e inviava l’impulso
ad un amplificatore (Buxco Elettronics Inc.) e al poligrafo. Il preparato veniva sottoposto ad una tensione di 0,50 g per 45-50 min., per consentirne la stabilizzazione nelle nuove condizioni di sopravvivenza.
Per la valutazione della risposta rilasciante al salbutamolo, il preparato veniva contratto con carbacolo (Sigma-Aldrich, St.Louis, MO, USA) alla concentrazione sub-massimale di 3×10-4 M.
Al raggiungimento del plateau veniva valutato l’effetto rilasciante del salbutamolo nell’intervallo di concentrazioni compreso tra 3×10-9
e 3×10-4 M.
Per la valutazione della risposta al contratturante, dopo la stabilizzazione il preparato veniva trattato con concentrazioni di carbacolo comprese tra 3×10-9 e 3×10-4 M.
Successivamente, il preparato veniva lavato con una soluzione di Krebs termostatata a 37ºC, allo scopo di allontanare l’agonista dai
recettori, e lasciato stabilizzare per circa 45 min. Infine, veniva provocata la contrazione con KCl 40 mM per ottenere un riferimento sulla capacità di contrazione del tessuto e valutare eventuali differenze nella risposta tra controlli desensibilizzati, e desensibilizzati trattati con montelukast.
2.2
Trattamenti
farmacologici
con
montelukast
Dopo la realizzazione del modello di desensibilizzazione omologa, la seconda parte dello studio era finalizzata a valutare gli effetti della somministrazione cronica di montelukast (Merck, NJ, USA) in cavie precedentemente trattate con salbutamolo, per stabilire la capacità del farmaco di modificare i parametri caratteristici del modello sperimentale di desensibilizzazione.
Il montelukast veniva somministrato per iniezione intraperitoneale una volta al giorno per 6 giorni consecutivi alla dose di 1 mg/Kg e 5 mg/Kg.
Tabella 1. Caratteristiche chimiche e farmacologiche del montelukast
Principio attivo Montelukast
Nome Chimico 2-[1-[[(1R)-1-[3-[2-(clorichinolin-2- il)etenil]fenil]-3-[2-(2-idrossipropan-2- il)fenil]propil]sulfanilmetil]
ciclopropil]acetato
Attività Inibitore dei cisteinil-leucotrieni
2.3 Studio in vitro
2.3.1 Colture cellulari e desensibilizzazione
omologa in vitro
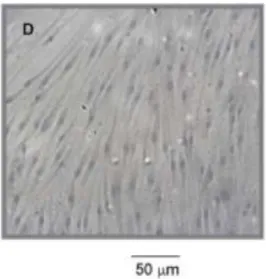
Per lo studio in vitro sono state impiegate cellule muscolari lischie bronchiali umane (LONZA, CC-2576), le quali crescono in adesione e hanno un tempo di duplicazione di circa 24 ore. Queste cellule sono state coltivate nel mezzo SmGM-2, come mezzo-base in presenza di insulina, fattore di crescita fibroblastico umano basico (hFGF-B), fattore di crescita epidermico umano (hEGF) e siero fetale bovino (FBS).
Figura 11. Fotomicrografia BSMC in cultura
La coltura della linea cellulare è stata realizzata in fiasche T75 e T25 tenute in incubatori che mantengono una temperatura costante di 37°C e un’atmosfera controllata al 5% di CO2. Le cellule sono state
mantenute in crescita esponenziale fino al 70-80% di confluenza e successivamente sub-coltivate in rapporto 1:3.
Il modello di desensibilizzazione omologa in vitro è stato realizzato seminando 5.000 cellule/well in piastre da 96 wells. Dopo adesione cellulare, il mezzo di coltura è stato sostituito con un mezzo base in assenza di siero (condizioni serum-free) per 24 ore. Dopo la sostituzione del mezzo-base con il terreno di coltura completo, le
cellule sono state esposte al solo veicolo (controlli) o al salbutamolo 10-6 M (desensibilizzati) per 24 ore.
2.3.2 Misurazione dei livelli di cAMP
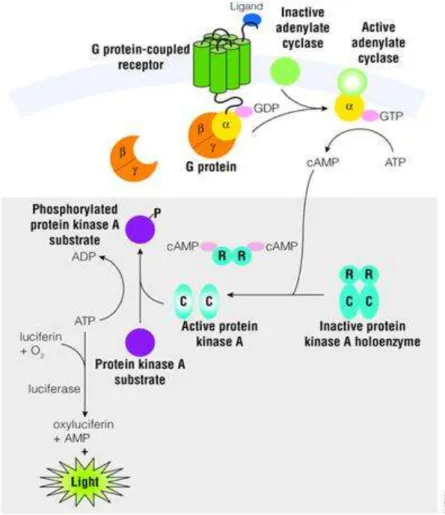
I livelli di cAMP dopo trattamento acuto con salbutamolo, nelle cellule di controllo e in quelle desensibilizzate, sono stati valutati impiegando un saggio che misura indirettamente la variazione dei livelli intracellulari di cAMP prodotta da agonisti dei recettori associati a proteine G, mediante un sistema di rivelazione a bioluminescenza (cAMP-GloTM Assay; Promega, Madison, WI, USA). In particolare il saggio si basa sul principio che il cAMP stimola la proteina chinasi A (PKA) riducendo la disponibilità di ATP per la reazione biochimica catalizzata dall’enzima luciferasi con la conseguente diminuzione dell’emissione di luce (Figura 10).
Figura 1. Principio del saggio per la misurazione dei livelli intracellulari di cAMP
2.3.3 Valutazione dell’espressione dei recettori β
2adrenergici
L’espressione dei recettori β2 adrenergici è stata valutata mediante
tecnica PCR (polymerase chain reaction). In particolare, circa 500.000 cellule sono state seminate in fiasche T25 in presenza o meno di salbutamolo 10-6 M. L’RNA totale è stato estratto mediante RNeasy
Mini kit (Qiagen, Valencia, CA, USA). La concentrazione ed il grado di purezza dell’RNA totale è stato misurato mediante l’assorbimento a
260 nm e la valutazione del rapporto dei valori ottenuti alle due lunghezze d’onda 260 nm e 280 nm, impiegando uno spettrofotometro
GeneQuant pro (Biochrom, UK). La qualità del materiale di partenza era indicato da un rapporto di densità ottica 260/280 nm > 1,9. L’integrità dell’RNA è stato inoltre verificata mediante elettroforesi su
gel di agarosio-formaldeide all’1 %.
Per ogni campione, è stato retrotrascritto 1 μg di RNA totale
mediante il QuantiTect Reverse Transcription kit (Qiagen, Valencia, CA, USA).
I primers per il recettore β2 adrenergico e per il gene housekeeping
GAPDH sono stati disegnati mediante il software Primer-Blast (NCBI) e sintetizzati da Sigma Genosys (Cambridge, UK). Le
sequenze dei primer sono le seguenti:
5’-ACCAGGAAGCCATCAACTG-3’ (forward) and
adrenergico; e GTGAAGGTCGGAGTCAACG-3’(forward) e
5’-GGTGAAGACGCCCAGTGGACTC-3’(reverse) per la GAPDH. La lunghezza prevista per i prodotti di amplificazione era rispettivamente di 119 e 300 bp.
La PCR è stata realizzata impiegando Hot-StartTaq Master Mix kit (Qiagen, Valencia, CA, USA) e l’apparecchio My Cycler (Bio-Rad,
Hercules, CA, USA). Le condizioni sperimentali adottate erano le seguenti: 15 min at 95 °C (attivazione della DNA polimerasi) e 36 cicli a 55 °C per 2 min (fase di annealing) e 72 °C per 1 min (fase di estensione).
La valutazione densitometrica delle bande elettroforetiche è stata realizzata mediante Image J (http://rsbweb.nih.gov/ij/).
2.4 Sostanze chimiche impiegate
I farmaci utilizzati sono stati:
Sodio pentobarbitale (Sessa, Milano, Italia) disciolto in acqua bidistillata alla concentrazione di 50 mg/ml.
Salbutamolo emisolfato (Sigma-Aldrich, St.Louis, MO, USA) disciolto in PBS sterile.
Montelukast (Merck, NJ, USA) sospeso in PBS sterile alla concentrazione di 8 mg/ml.
Per gli studi funzionali, il salbutamolo e il carbacolo venivano solubilizzati in una soluzione di Krebs-Henseleit, ottenuta disciogliendo in acqua bidistillata NaHCO3,
glucosio, NaCl, MgSO4, CaCl2 e KH2PO4.
2.5 Analisi dei dati e statistica
L’azione contratturante del carbacolo è stata espressa come tensione attiva (in grammi) sviluppata dall’organo.
L’effetto miorilasciante del salbutamolo e del montelukast è stato
espresso come riduzione della tensione (in grammi) sviluppata dall’organo precontratto con carbacolo.
Il pD2, un indice della potenza dell’agonista, veniva calcolato come
-log EC50 (concentrazione molare che produceva il 50% dell’effetto
media ± errore standard della media (SEM) e l’analisi statistica è stata effettuata mediante il test ANOVA seguito dal test di Newmann-Keuls per confronti multipli. Il valore P<0,05 è stato assunto come livello di significatività statistica.
I grafici, l’analisi dei dati e l’analisi statistica sono stati effettuati
con il software Prism versione 4.0 (Graphpad Software, San Diego, CA, USA).