sperimentali
6.0 Prove
preliminari
Una serie di esperimenti sono stati condotti in cella di Devanathan, realizzando prove di permeazione, per verificare quanto e in che modo questo tipo di prove si potesse adattare allo studio del fenomeno di decapaggio. Più che ottenere i risultati di diffusività in questo caso è stato importante testare il tipo di risposta dell’apparecchiatura nelle diverse condizioni di utilizzo, per valutare fattori quali riproducibilità, ripetibilità, l’ordine di grandezza dei risultati, la possibilità o meno di indagare le variazioni legate ai singoli parametri di processo (composizione del bagno, presenza dell’inibitore, etc.) e/o delle condizioni al contorno (temperatura, stato della superficie, tipologia e composizione della scaglia, etc.).
Di seguito sono riportate le misure più significative riferite a prove eseguite su diversi campioni di acciaio, utilizzando una soluzione decapante nella semicella catodica. Di volta in volta sono riportate le condizioni di prova.
Effetto dell’acidità della soluzione
Il grafico in fig.6 mostra risultati di permeazione di idrogeno proveniente da decapaggio, riferiti a soluzioni con diverse concentrazioni di HCl (g/L), senza aggiunta di inibitore né presenza di Fe++ in soluzione al tempo zero, temperatura di prova: 80°C.
Il campione analizzato è un acciaio PH10 laminato a freddo, spessore d=0.7mm, senza presenza di ossidi superficiali.
Figura 6.1 Curve di permeazione eseguite in soluzioni a diversa concentrazione di HCl. T=80°C, Acciaio IF laminato a freddo.
L’idrogeno che diffonde attraverso la membrana dà correnti che variano notevolmente tra le diverse prove: in questo caso passando da 20 a 200 g/L (concentrazione dell’acido), avremo correnti che variano da 180 a 610 µA (Iperm).
Effetto della concentrazione dell’inibitore
Prove realizzate alla stessa concentrazione costante di acido, [HCl]=90g/L, T=80°C costante, e variando il contenuto di inibitore dallo 0.36 al 3% in volume. E’ stato utilizzato un inibitore filmante di composizione organica (poliammina), indicato come inib1.
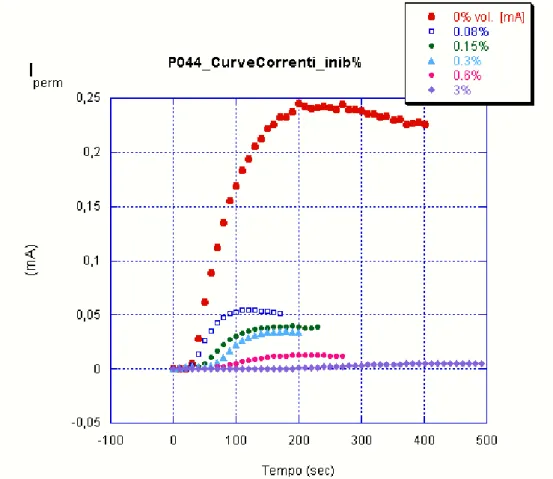
Nel primo grafico sono riportate le curve della corrente di idrogeno in uscita dal campione di acciaio, mentre il secondo grafico mette in relazione il valore massimo della corrente ottenuto nelle singole prove (condizioni stazionarie) con la concentrazione di inibitore (%vol) presente nella soluzione decapante.
Campione analizzato: acciaio P044 nero, spessore 1.5mm.
Figura 6.2 Relazione tra valore della corrente di permeazione allo stazionario e concentrazione di inibitore nel bagno.
Confrontabilità nell’uso di diversi inibitori
Confronto dei risultati ottenuti nelle medesime condizioni di prova ([HCl]=90g/L;T=80°C) usando inibitori diversi alle stesse concentrazioni
nella linea DEC1 dello stabilimento di Cornigliano (cap.5, par.5.1). Campione analizzato: acciaio P044 nero, spessore 1.5 mm.
I(mA)
Figura 6.3 Confronto dei valori di corrente allo stazionario con l’uso di diversi inibitori nelle medesime concentrazioni e senza inibitore.
La miscela speciale di HMTA e Propinolo è l’inibitore più diffuso industrialmente sulle linee di decapaggio ad acido cloridrico [30].
Infatti già in piccole concentrazioni risulta molto efficiente nella riduzione della corrente di corrosione (proporzionale alla quantità di idrogeno prodotto).
Effetto del tenore di ferro del bagno
La presenza di una concentrazione di Fe++ in soluzione nel bagno decapante varia il potenziale di corrosione dell’acciaio nella soluzione. Per evidenziare quanto e come la misura di permeazione eseguita in una doppia cella possa essere influenzata da questo parametro sono stata eseguite due prove nelle medesime condizioni sullo stesso acciaio, nella prima non c’è presenza di ferro in soluzione (al tempo t=0), mentre la seconda è condotta a partire da una concentrazione di ferro iniziale paria a quella media misurata nelle vasche di decapaggio (100g/L, al tempo t=0).
Si fa riferimento a soluzioni acide non inibite.
Campione analizzato: acciaio P044 nero, spessore 1.5 mm.
Soluzione
[HCl] (g/L)
T (°C)
[Fe++] (g/L)
v-1 90
80
0
v-2 90
80
100
Come si vede dalle curve di permeazione, nel secondo caso la quantità di idrogeno è leggermente superiore (il fenomeno di decapaggio è infatti accentuato dalla presenza degli ioni ferrosi nel bagno), ma in termini di diffusività e tempo di permeazione le misure effettuate si avvicinano molto.
Figura 6.4 Flusso di corrente permeata e integrale del flusso con: v1)assenza di ione ferroso nel bagno decapante; v2)presenza di Fe++ nel bagno.
Stato iniziale della superficie esposta all’idrogeno
I grafici sono relativi all’azione della stessa soluzione decapante, non inibita, alla stessa temperatura 80°C, variando però lo stato della superficie esposta (rimozione o meno della scaglia nella preparazione dei campioni precedente all’esecuzione della prova).
0%_scaglia Acciaio nero
0%_carte Rimozione meccanica dell’ossido
0%_dec Rimozione dell’ossido tramite decapaggio acido
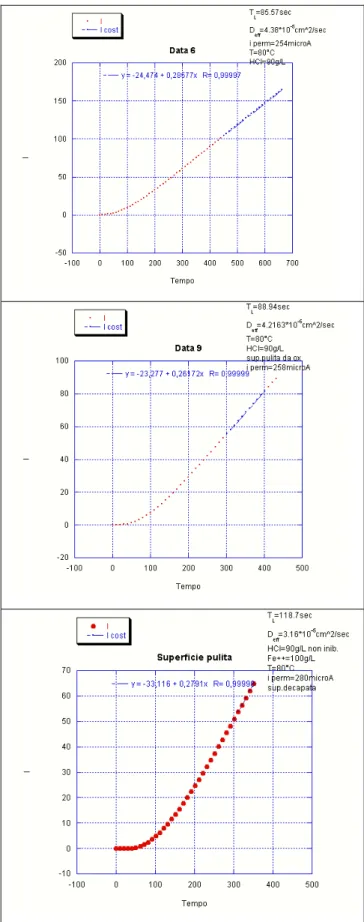
Figura 6.5 Flusso di idrogeno , C0(mol/cm 3
), permeato attraverso il metallo a partire da superfici diverse esposte a decapaggio
Anche in questo caso non ci sono variazioni rilevanti: la prova condotta su un campione che è stato precedentemente sottoposto a decapaggio acido al fine della rimozione della scaglia,dà una misura superiore alle altre due; lo scostamento rispetto ai test eseguiti su campioni di nero può essere
dell’adsorbimento di idrogeno sulla membrana metallica, o della corrosione stessa.. D’altra parte anche quando si effettua una rimozione meccanica dell’ossido permangono in superficie impedenze alla diffusione dovute al leggero incrudimento provocato dall’abrasione effettuata dalle carte.
Stato superficiale (presenza della scaglia)
Iperm[µA] Deff[cm2/sec] TL[sec]
Acciaio nero 254 4.38*10-6 85.57
Rimoz.meccanica della scaglia
258 4.22*10-6 88.9
Rimoz. dell’ossido tramite decapaggio acido
280 3.16*10-6 118.7
Tabella 6.1 Prove di permeazione durante decapaggio acido in relazione allo stato iniziale della superficie ( figura 28). Acciaio P044.
Nell’ultima figura è invece riportato l’immediato effetto dell’inibitore sulla corrente di diffusione: l’aggiunta di inibitore nella soluzione decapante riduce la corrente di corrosione a circa un quinto del valore iniziale.
Figura 6.7 Effetto dell’aggiunta di inibitore nel bagno decapante sulla corrente di permeazione.
Queste prove risultano molto efficienti nel dare l’immediata indicazione circa il contenuto di inibitore del bagno. Il processo di decapaggio viene condotto in continuo: il controllo sull’acidità delle soluzioni in vasca viene effettuato manipolando la portata F di alimentazione(con una composizione in acido e inibitore costante), ma non è detto che la concentrazione d’inibitore vari linearmente con il consumo di HCl, in linea generale non è così. Quindi le misure (titolazioni) eseguite in linea per controllare l’aggressività delle soluzioni, non danno in realtà indicazioni sulla bontà dell’inibizione. Questa è stata testata variando tutti i parametri e infine confrontando i risultati con quelli dei test eseguiti su soluzioni reali prelevate sull’impianto (par 6.1.2).
6.1
Prove di permeazione in cella elettrochimica
Prove eseguite su campioni di acciaio nero, il bagno decapante è quello che si riferisce ai valori medi di concentrazione della seconda vasca.
Composizione del bagno decapante: [HCl]=90g/L
[Fe++]=100g/L
[inib 2]=0÷3% vol (inibitore industriale: HMTA + Propinolo) T=80°C
6.1.1 Variazioni della concentrazione d’inibitore
Sono riportati i valori medi delle correnti di permeazione delle prove eseguite con la concentrazione di inibitore indicata (tab.6.2). Si riporta invece il grafico di tutte le misure effettuate al variare della concentrazione di inibitore(fig.6.8).Alla corrente letta in uscita corrisponde un valore di concentrazione C0, ossia di attività dell’idrogeno sulla superficie esposta al decapaggio.
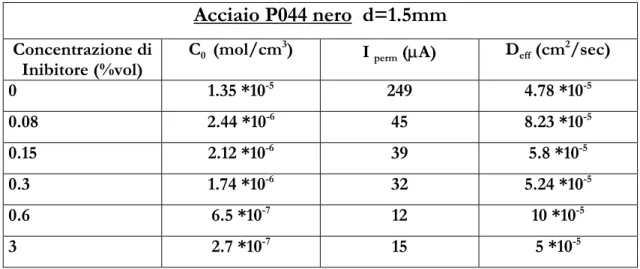
Acciaio P044 nero d=1.5mm
Concentrazione di
Inibitore (%vol) C0 (mol/cm 3)
I perm (µA) Deff (cm 2/sec) 0 1.35 *10-5 249 4.78 *10-5 0.08 2.44 *10-6 45 8.23 *10-5 0.15 2.12 *10-6 39 5.8 *10-5 0.3 1.74 *10-6 32 5.24 *10-5 0.6 6.5 *10-7 12 10 *10-5 3 2.7 *10-7 15 5 *10-5
Tabella 6.2 Valori medi delle correnti ottenute per diverse concentrazioni di inibitore e corrispondente attività dell’idrogeno in superficie. Acciaio P044, soluzione decapante: [HCl]=90g/L; [Fe++]=100g/L; T=80°C
Figura 6.8 Andamento della concentrazione di idrogeno sulla superficie del campione col variare dell’inibizione del bagno.
Si illustrano le curve reali ottenute dalle prove più rappresentative per ciascuna concentrazione di inibitore in soluzione.
Inibitore (%vol) 0 0.08 0.15 0.3 0.6 3 P044 nero I perm (µA) 244 50 39 32 12 5
Tabella 6.3 Curve di permeazione di sei prove eseguite al variare del parametro di concentrazione dell’inibitore. Acciaio P044.
Figura 6.9 Dati riportati in tabella 6.3.Curve di permeazione ottenute con concentrazioni diverse di inibitore
Le stesse prove di permeazione eseguite variando la concentrazione di inibitore nel bagno sono state eseguite sui campioni di acciaio PH10 nero. Lo spessore di partenza del campione (3.5mm) è stato ridotto ad un valore d=1.7mmtramite fresatura per agevolare l’esecuzione della prova.
Acciaio PH10 nero d=1.7mm
Concentrazione di
Inibitore (%vol) C0 (mol/cm 3)
I perm (µA) Deff (cm 2/sec) 0 7.69 *10-6 125 3.8 *10-5 0.02 2.83 *10-6 46 2.99 *10-5 0.04 2.34*10-6 38 3.34 *10-5 0.08 2.46 *10-6 40 2.8 *10-5 0.15 1.72 *10-6 28 3.19 *10-5 0.3 1.17 *10-6 19 4.1 *10-5 0.6 1.47 *10-6 24 1.9 *10-5
Tabella 6.4 Valori medi delle correnti ottenute per diverse concentrazioni di inibitore e corrispondente attività dell’idrogeno in superficie. Acciaio PH10, soluzione decapante: [HCl]=90g/L; [Fe++]=100g/L; T=80°C
Prove di permeazione più rappresentative per ciascuna concentrazione di inibitore in soluzione (acciaio PH10).
Inibitore (%vol) 0 0.02 0.04 0.08 0.15 0.3 0.6 PH10 nero I perm (µA) 125 46 38 40 28 20 24
Tabella 6.5 Curve di permeazione di prove eseguite al variare del parametro di concentrazione dell’inibitore. Acciaio PH10.
Figura 6.10 bis Curve di permeazione di sei prove eseguite al variare del parametro di concentrazione dell’inibitore. Acciaio PH10.
da vasca
Le prove nelle stesse condizioni di temperatura sono state condotte usando come soluzioni decapanti quelle della vasca 2 (V2) e vasca 3(V3) della linea DEC1, prelevate in loco.
Le titolazioni eseguite per determinare l’esatta composizione hanno dato i seguenti risultati:
V2 [HCl]= 100 g/L [Fe++]= 72 g/L
V3 [HCl]= 122 g/L [Fe++]= 55 g/L
L’informazione sul contenuto di inibitore è ricavabile appunto dai risultati dei test eseguiti.
Acciaio P044 nero d=1.5mm
Soluzione acida Iperm (µA) C0 (mol/cm3)
V2 150 8.14 *10-6
V3 96 5.23 *10-6
V2 + inib 0.15%vol 47 2.55 *10-6
V2 + inib 0.3%vol 32 1.75 *10-6
Tabella 6.6 Valori di corrente permeata, e corrispondente attività dell’idrogeno in superficie, proveniente da decapaggio acido. Soluzioni utilizzate: bagno della vasca3 e vasca 2 con aggiunta di inibitore in concentrazioni crescenti.T=80°C. Acciaio P044.
Figura 6.11 Confronto tra azione della vasca 2 e 3 in termini di corrente di permeazione. Acciaio P044.
Soluzione acida Iperm (µA) C0 (mol/cm3) Deff (cm2/sec)
V2 75 4.64 *10-6 4.02 *10-5
V3 72 4.44 *10-6 4.49 *10-5
Tabella 6.7 Valori di corrente permeata, e corrispondente attività dell’idrogeno in superficie, durante decapaggio acido effettuato con le soluzioni della vasca3 e vasca 2 .T=80°C. Acciaio P044
Figura 6.13 Risultati dei test condotti effettuando decapaggio con i bagni della vasca 2 e 3). T=80°C. Acciaio PH10.
6.1.3 Misura del potenziale di corrosione
La cinetica di dissoluzione della scaglia nella soluzione acida può essere studiata attraverso la variazione del potenziale di corrosione del metallo: una volta eliminato l’ossido superficiale la misura deve tendere a quella propria del potenziale di corrosione del metallo nelle condizioni di prova.
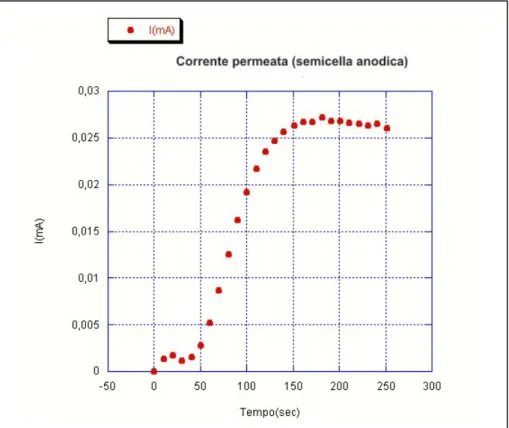
Figura 6.14 Curva della corrente permeata nella semicella anodica. Acciaio P044 nero.
Prova eseguita effettuando un decapaggio su un campione di acciaio P044 nero, d=1.5mm, a partire da una soluzione ideale:
[HCl]= 90g/L [Fe++]= 100 g/L [Inib 2]= 0.3% vol.
attraverso il campione, mentre contemporaneamente nell’altro scomparto della cella, dove sta avvenendo il decapaggio acido, registriamo il potenziale di corrosione del metallo nelle dette condizioni.
Figura 6.14 bis Corrispondente variazione del potenziale di corrosione nella semicella catodica.
6.1.4 Aspetto della superficie
Interrompendo prove di diffusione effettuate nelle stesse condizioni sullo stesso campione, acciaio P044 nero, ad intervalli di tempo successivi, e analizzando il campione al microscopio SEM, si è potuto mettere in relazione lo stato della superficie con i diversi punti della curva della corrente dell’idrogeno permeato.
Tempo di permanenza (sec) I perm (µA) 0 0 30 0.76 90 7.2 110 16.3 Composizione del bagno decapante: [HCl]= 90g/L [Fe2+]=100g/L T=80°C 290 34
Tempo di permanenza (sec) I perm (µA) 0 0 30 3.78 Composizione del bagno decapante: Soluzione reale V2 180 166
Figura 6.16 Aspetto della superficie durante una permeazione elettrochimica in corrispondenza di tempi diversi.Soluzione decapante: bagno della vasca2. Acciaio P044
6.2 Prove di perdita in peso per immersione
Composizione del bagno decapante: [HCl]= 90g/L [Fe++]= 100g/L [inib 2]= 0÷0.6% (vol.) T= 80°C Concentrazione inibitore [% vol] Tempo [sec] W [mg/dm2] 0 0 0 30 8480 60 13301 90 20200 120 26802 0.08 0 0 30 7748.7 60 8729.5 90 9370.5 0.15 0 0 30 7403.9 60 8606.3 90 8872.5 0.3 0 0 30 7216 60 8546.9 90 9040.9 120 9247.2 0.6 0 0
P044 d=1.5mm
60 7872.6 90 8865.2
Tabella 6.8 Dati relativi alle perdite in peso dei campioni di acciaio P044 nero per diversi tempi di permanenza al variare della concentrazione di inibitore nella soluzione decapante.
Figura 6.17 Andamento della perdita in peso nel tempo per diverse concentrazioni di inibitore (dati di tabella 6.8).Acciaio P044
Le stesse prove ad immersione sull’acciaio PH10 sono state eseguite, nelle medesime condizioni, anche su campioni privi della scaglia di ossido superficiale (dati riportati sotto la colonna W*).
PH10 d=3.5mm
Concentrazione inibitore [% vol] Tempo [sec] W [mg/dm2] W* [mg/dm2] 0 0 0 0 30 11840 1530.9 60 119740 8623.5 90 24310 11101 120 29764 15201 180 37029 23290 0.08 0 0 0 30 10855 652.4 60 13374 1221.7 90 14089 1836.1 0.15 0 0 0 30 10884 741.73 60 12467 1221.7 90 13956 1753.4 0.3 0 0 0 30 8775.5 301.07 60 12830 773.49 90 13535 1585.9 120 13281 1482.8 180 13701 1984.930 10682 403.6
60 12305 789
90 13246 1023.9
Tabella 6.9 Dati relativi alle perdite in peso dei campioni di acciaio PH10, nero (W) e decapato (W*), per diversi tempi di permanenza al variare della concentrazione di inibitore nella soluzione decapante
Figura 6.18 Andamento della perdita in peso nel tempo per diverse concentrazioni di inibitore (dati di tabella6.9 relativi ai campioni con scaglia in superficie, W).
P044
Soluzione prelevata da vasca Tempo [sec] W [mg/dm2] 0 0 30 5292.8 60 8399.8 V2 90 9805.7 0 0 30 5027.2 60 9471.5 V3 90 10318Tabella 6.10 Dati relativi alle perdite in peso dei campioni di acciaio P044 nero per diversi tempi di permanenza nei bagni delle vasche 2 e 3 della linea DEC1.
PH10
Soluzione prelevata da vasca Tempo [sec] W [mg/dm2] 0 0 30 13532 60 19419 90 20458 V2 180 21098 0 0 30 12683 60 15338 90 17710 V3 180 20342Tabella 6.11 Dati relativi alle perdite in peso dei campioni di acciaio PH10 nero per diversi tempi di permanenza nei bagni delle vasche 2 e 3 della linea DEC1.
Figura 6.19 Perdite in peso dell’acciaio P044 nella soluzione della vasca 2. Confronto con dati della soluzione non inibita.
Figura 6.20 Perdite in peso dell’acciaio PH10 nella soluzione della vasca 2. Confronto con dati della soluzione inibita con concentrazione 0.3%.
P044
Concentrazione Inibitore (% vol) Soluzioni prelevate da vasca Velocità media di perdita in peso [mdd] 0 0.08 0.15 0.3 0.6 V2 V3 v1 192.97*105 90.10*105 85.31*105 66.58*105 85.12*105 94.13*105 99.05*105 v2 175.89*105 23.35*105 21.14*105 19.49*105 29.70*105 64.98*105 76.18*105
Tabella 6.12 Velocità media di perdita in peso nel tempo calcolata negli intervalli 0<t<180s (v1) e 30s<t<180s (v2).Accaio P044 nero.
Figura 6.21 Andamento della velocità media di perdita in peso nel tempo al variare della concentrazione di inibitore nel bagno. Acciaio P044 nero.
Concentrazione Inibitore (% vol) Soluzioni prelevate da vasca Velocità media di perdita in peso [mdd] 0 0.08 0.15 0.3 0.6 V2 V3 v1 177.74*105 135.25*105 134.19*105 129.93*105 127.36*105 196.39*105 170.01*105 v2 145,08*105 46.56*105 44.26*105 28.37*105 36.92*105 99.73*105 72.39*105
Tabella 6.13 Velocità media di perdita in peso nel tempo calcolata negli intervalli 0<t<180s (v1) e 30s<t<180s (v2).Acciaio PH10 nero
Figura 6.22 Andamento della velocità media di perdita in peso nel tempo al variare della concentrazione di inibitore nel bagno. Acciaio PH10 nero.
PH10 *
P044*
Concentrazione Inibitore (% vol) Concentrazione Inibitore (% vol) Velocità media di perdita in peso [mdd] 0 0.08 0.15 0.3 0.6 0.3 v1 111.79*105 17.65*105 16.86*105 9.53*105 9.84*105 20.61*105 v2 125.33*105 17.04*105 14.57*105 9.69*105 8.93*105 21.07*105
Tabella 6.14 Velocità media di perdita in peso nel tempo calcolata nell’intero intervallo t0=0sec
(v1) e nell’intervallo successivo ai primi 30 sec di immersione (v2), per campioni di acciaio PH10 senza presenza di ossidi superficiali.
Figura 6.23 Andamento della velocità media di perdita in peso nel tempo al variare della concentrazione di inibitore nel bagno. Acciaio PH10 trattato con decapaggio (senza presenza di scaglia superficiale)
Figura 6.24 Confronto tra l’andamento della perdita in peso in presenza o assenza di scaglia in superficie. Acciaio P044, soluzione inibita [inib.2]=0.3% vol.
Figura 6.25 Confronto tra l’andamento della perdita in peso in presenza o assenza di scaglia in superficie. Acciaio PH10, soluzione inibita [inib.2]=0.3% vol.
Figura 6.26 Confronto tra l’andamento della perdita in peso in presenza o assenza di scaglia in superficie. Acciaio PH10. Soluzione non inibita. Fit dei valori ottenuti in assenza di ossidi superficiali.
6.3.1 Acciaio P044
Aspetto iniziale dell’ossido superficiale
Figura 6.27 Struttura e spessore dello strato di ossido superficiale (scaglia). Analisi al MO e al SEM. Acciaio P044.
Evoluzione della superficie nel tempo: immersione in bagno decapante in presenza di inibitore
Figura 6.28 t=30 sec Figura 6.29 t=90 sec
Figura 6.30 t=110 sec Figura 6.31 t=180 sec
Fig. 6.28÷6.31: Aspetto della superficie in sezione analizzata al SEM per diversi tempi di permanenza nel bagno decapante. Campioni analizzati: acciaio P044 nero. Composizione della soluzione acida: [HCl]=90g/L,[Fe++]=100g/L, [inib2]=0.3% vol; T=80°C.
Figura 6.32 t=90 sec Figura 6.33 t=110 sec Figura 6.34 t=180 sec bagno decapante in presenza di inibitore Fig 6.32÷6.34: Vista in sezione dell’interfaccia tra superficie trattata con decapaggio e superficie vergine (ricoperta da scaglia).
Composizione della soluzione acida: [HCl]=90g/L, [Fe++]=100g/L, [inib2]=0.3% vol; T=80°C.
Figura 6.35 Vista della superficie dopo 30 sec di permanenza in bagno e microanalisi degli elementi presenti in superficie effettuata al SEM.
Figura 6.36 Vista della superficie dopo 180 sec di permanenza in bagno e microanalisi degli elementi presenti in superficie effettuata al SEM.
Figura 6.37 t=30 sec
Figura 6.38 t=180 sec
nel tempo: immersione nel bagno decapante della vasca 2.
Aspetto della superficie in sezione analizzata al SEM per diversi tempi di permanenza nel bagno decapante. Campioni analizzati: acciaio P044 nero. Bagno decapante: soluzione V2 (vasca 2 linea DEC1) ; T=80°C.
6.3.2 Acciaio PH10
Aspetto iniziale dell’ossido superficiale
Figura 6.39 Struttura e spessore dello strato di ossido superficiale (scaglia). Analisi al MO e al SEM. Acciaio PH10.
Figura 6.40 t=30 sec
Figura 6.41 t=90 sec
Figura 6.42 t=180 sec
nel tempo: immersione in bagno decapante in presenza di inibitore
Analisi della superficie in sezione effettuata al SEM per diversi tempi di permanenza nel bagno decapante. Campioni analizzati: acciaio PH10 nero. Composizione della soluzione acida: [HCl]=90g/L,[Fe++]=100g/L,
Figura 6.43 t=30 sec
Figura 6.44 t=180 sec
Aspetti locali della trasformazione superficiale nel tempo: immersione in bagno decapante in presenza di inibitore
Le due figure mostrano situazioni particolari che interessano alcune zone della superficie dei campioni rappresentati in fig.6.40 e 6.42, ossia rispettivamente a 30 e 180 sec dal tempo di immersione in vasca, in presenza di inibitore: si nota come l’evolversi nel tempo del processo di decapaggio e il conseguente distacco della scaglia non sia uniforme se osservato sull’intera superficie dei provini.
Figura 6.45 t=30 sec
Figura 6.46 t=90 sec
Figura 6.47 t=180 sec
nel tempo: immersione in bagno decapante in assenza di inibitore
Aspetto della superficie in sezione analizzata al SEM per diversi tempi di permanenza in bagno decapante senza inibitore. Campioni analizzati: acciaio PH10 nero. Composizione della soluzione acida:
[HCl]=90g/L,[Fe++]=100g/L, T=80°C.
Figura 6.48 Analisi in sezione della scaglia dopo 30 sec di permanenza nella soluzione decapante non inibita. Si osserva il distacco della scaglia. Campione PH10 nero.
Figura 6.49 Analisi in sezione della superficie dopo 180 sec di permanenza nella soluzione decapante non inibita. Si osserva corrosione del metallo. Campione PH10 nero.
Figura 6.50 t=30 sec
Figura 6.51 t=90 sec
Figura 6.52 t=180 sec
nel tempo: immersione nel bagno decapante della vasca 2.
Aspetto della superficie in sezione analizzata al SEM per diversi tempi di permanenza nel bagno decapante. Campioni analizzati: acciaio PH10 nero. Bagno decapante: soluzione V2 (vasca 2 linea DEC1);T=80°C