Master Universitario di II livello
Trattamento percutaneo della malattia coronarica I ed
Anno Accademico
2016/2017
Strategie di trattamento interventistico
della trombosi coronarica massiva.
Autore
Dott. Alberto Massoni
Tutor Scientifico
Prof. Claudio Passino
Tutor Aziendale –
USOD Emodinamica Grosseto, USL Toscana SUDESTINDICE
1. Introduzione pag. 4
2. Caso clinico pag. 6
3. Discussione pag. 11
3.1 I primi studi sulla trattamento interventistico della trombosi coronarica pag. 11 3.2 L’utilizzo routinario dei device di prtotezione embolica durante PCI primaria pag. 12
3.3 I device da trombectomia pag. 12
3.4 I device da tromboaspirazione: letteratura pag. 14
3.4.1 Lo studio TAPAS pag. 14
3.4.2 Gli studi TASTE e TOTAL pag. 14
3.4.3 Revisione della letteratura pag. 15
3.5 Confronto tra tromboaspirazione e trombectomia reolitica pag. 18 3.6 Casi in cui la trombectomia potrebbe avere un ruolo realmente efficace pag. 19
3.7 Conclusioni pag. 21
INDICE DELLE FIGURE • Fig 1. pag. 6 • Fig 2. pag. 7 • Fig 3. pag. 7 • Fig 4. pag. 8 • Fig 5. pag. 8 • Fig 6. pag. 9
1. Introduzione
Il ripristino del flusso e la preservazione del miocardico sono gli obiettivi più importanti del trattamento dell’infarto miocardico acuto con sopraslivellamento del tratto ST-T (SCA STEMI). Tuttavia, in circa un terzo dei casi, il flusso a livello del tessuto miocardico non viene ristabilito anche in caso di efficace angioplastica coronarica, questo è dovuto tra le altre cause ad una mancata ripresa della perfusione nel comparto microvascolare, limitando quindi l’efficacia ed i benefici attesi dal trattamento riperfusivo della coronaria epicardica 1.
Inoltre la disfunzione microvascolare è stata associata con una più larga area infartuale, ad un aumentato rischio di eventi aritmici ventricolari, di scompenso cardiaco, di shock cardiogeno, di recidive ischemiche ed infine di morte2.
Differenti meccanismi sottendono al danno microvascolare durante angioplastica coronarica (PTCA) primaria oltre alla presenza di trombosi ed alla sua entità, quali l’effetto infiammatorio paracrino della stessa3, la produzione di radicali liberi dell’ossigeno, il sovraccarico di calcio intracellulare nei miociti, l’edema cellulare ed interstiziale, la disfunzione endoteliale, la vasocostrizione, l’embolizzazione distale sembra giocare un ruolo rilevante. Diversi studi hanno confermato questa ipotesi; l’embolizzazione distale può essere rilevata all’angiografia in circa il 15%4 dei casi; inoltre in un suo studio Okamura ha dimostrato come, utilizzando una guida Doppler per riconoscere i detriti embolici, l’embolizzazione distale sia un fenomeno pressoché costante durante PTCA primaria5. In tal senso il carico trombotico è un predittore del fenomeno del no-reflow e si è dimostrato avere una correlazione indipendente con outcomes avversi6,7
Dal momento che l’embolizzazione avviene prevalentemente al momento della dilatazione iniziale del pallone da angioplastica (POBA) o durante l’insufflazione dello stent una riduzione del burden trombotico mediante trombectomia potrebbe ridurre la probabilità di embolizzazione distale.
Attualmente i devices disponibili per uso clinico includono cateteri da aspirazione o prodotti specificatamente sviluppati per effettuare una trombectomia. Tra i primi si annoverano i sistemi di aspirazione Diver (Invatec®), Export (Medtronic®), Eliminate (Terumo®), QuickCat (Kensey Nash®) and Pronto (Vascular Solutions®); tra i secondi vi sono devices che utilizzano pompe di aspirazione prossimali come Rescue PT system (Boston Scientific®) eTVAC e strumenti che utilizzano un sistema di trombectomia reolitica come i cateteri AngioJet (Boston Scinetific®) e X-Sizer (ev3 Inc®).
I cateteri da aspirazione manuale sono quelli più comunemente usati, sia per il basso costo che per la loro facilità di utilizzo. Il caso clinico descritto riguarda la gestione di una trombosi coronarica massiva e le strategie interventistiche utilizzate nel trattamento di questa patologia coronarica.
2. Caso clinico
Una donna, di 79 anni, giunge attorno alle ore 12:15 nella sala di Emodinamica dell’Ospedale Misericordia di Grosseto, come previsto dal percorso stabilito dalla nostra azienda sanitaria per quadro clinico-strumentale di sindrome coronarica acuta STEMI (ST elevation myocardial infarction), direttamente dal proprio domicilio. Come fattori di rischio cardiovascolare riferiva solo forte tabagismo; in anamnesi i colleghi del 118 riferivano inoltre positività al fattore V di Leiden e deficit di proteina C.
La paziente lamentava insorgenza di epigastralgia e diaforesi dalle ore 10 circa della mattina; attivato il 118 all'ECG si documentava sopraslivellamento del tratto ST nelle derivazioni D1 ed aVL e V4-V6. Durante il tragitto in ambulanza la paziente presentava un progressivo peggioramento dell'ipotensione, non responsiva al carico di liquidi (250+250 cc di soluzione fisiologica). Veniva pertanto iniziata terapia inotropa con Dopamina ev; contestualmente la paziente veniva pretrattata con Acido salicilico 300 mg ev e somministrata Morfina 1/3 di fl per marcato angor. All'arrivo in Emodinamica durante la preparazione all’esame coronarografico, si osservava ulteriore aggravamento dell’ipotensione (80/50 mmHg) in quadro clinico di shock cardiogeno per cui si iniziava Noradrenalina e Dobutamina ev.
All’esame angiografico, condotto per via radiale destra, si osservava una coronaria destra indenne da stenosi significative (fig.1 ); il tronco comune (TC) presentava una occlusione trombotica acuta in sede distale (fig. 2) con flusso a valle TIMI 0. La paziente è stata trattata con Clopidogrel 600 mg per os ed è stata somministrata eparina non frazionata secondo peso per via venosa (6000 UI). Utilizzando un catetere guida XB 3 (Cordis®) 6 French (F), è stata sondata l’occlusione con un filo guida BMW HI-
TORQUE 0.014 (Abbott®) verso la discendente anteriore (DA) e posizionata una guida Whisper MS (Abbott®) in arteria circonflessa (Cx); è stata effettuata una dilatazione con pallone semicompliante Tazuna 2,5 mm x 20 mm (Terumo®) gonfiato a 14 atm a livello del TC distale Fig. 1: coronaria destra in proiezione craniale sinistra
ottenendo ripristino del flusso coronarico TIMI 3 su DA (collateralmente presenza di micorfistolizzazioni in cavità ventricolare sinistra) (fig. 3).
Al fine di ottenere una rivascolarizzazione completa si eseguiva gonfiaggio di pallone Tazuna 3,0 x 15 mm (Terumo®) a 14 atm e trombectomia meccanica con tromboaspirazione con sistema Eliminate Aspiration Catheter 6F (Terumo®) su circonflessa senza tuttavia ripristino di un flusso coronarico soddisfacente (Fig. 4).
Fig. 2: occlusione trombotica acuta del tronco comune distale
Fig. 3: ricanalizzazione della discendente anteriore dopo PTCA con solo pallone
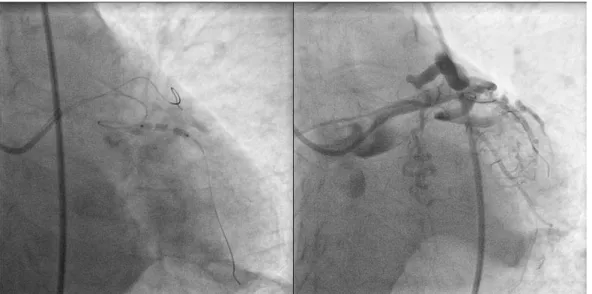
Al controllo angiografico si osservava la presenza di una marcata formazione trombotica residua al terzo distale del TC, si eseguiva per tanto tromboaspirazione manuale con device Eliminate Aspiration Catheter 6F (Terumo®) e si iniziava infusione endovenosa di Abciximab secondo peso. Dopo manovra di tromboaspirazione persisteva la presenza di trombosi a livello del TC (Fig. 5) per cui si decideva di eseguire trombectomia reolitica con sistema AngioJet TM 4 F (Boston Scinetific®) con totale rimozione della massa trombotica (Fig 6.).
In considerazione dell’assenza di una chiara malattia ateromasica parietale e della completa risoluzione del quadro trombotico si decideva di non impiantare stent.
Fig. 4: a sinistra: PTCA con pallone Tazuna 3,0 x 15 mm su Cx; a destra: mancato ripristino del flusso coronarico nonostante PTCA e tromboaspirazione.
Fig. 5: persistenza di marcata trombosi sul TC distale.
Al termine della procedura la paziente risultava vigile, cosciente, in ritmo sinusale 70 bpm e con pressione arteriosa sistemica 130 mmHg sostenuta da amine.
Per il persistere di un quadro di shock cardiogeno e congestione polmonare (cold & wet), nonostante supporto farmacologico massimale, il giorno successivo alla rivascolarizzazione veniva posizionato contropulsatore aortico (IABP) per via femorale destra. All’ecocardiogramma si rilevava una disfunzione sistolica ventricolare sinistra moderato-severa (FE 35%), da acinesia del setto interventricolare in toto, apice e parete anteriore in toto, insufficienza mitralica moderata (la valuvolpatia, alla luce della mancata rivascolarizzazione della arteria circonflessa, è stata valutata anche con ecocardiogramma transesofageo che ha escluso un meccanismo da disfunzione del papillare; contestualmente non sono emersi dati compatibili con forame ovale pervio).
Durante la degenza in UTIC si osservava episodio di fibrillazione atriale tachifrequente sottoposta a cardioversione elettrica; discusso collegialmente il caso, in considerazione della recente ischemia miocardica da trombosi coronarica, senza tuttavia l’impianto di uno stent, e la concomitante fibrillazione atriale persistente con elevato CHA2DS2-VASc (5) veniva impostata terapia con
Dabigatran 110 mg b.i.d. e Clopidogrel 75 mg 1 cp/die. Nei giorni successivi tuttavia veniva osservato un progressivo calo dei valori di emoglobina con comparsa di melena e rettorragia di importanza tale da richiedere la somministrazione di emazie concentrate e sospensione della terapia anticoagulante; alla gastroscopia rilievo di gastrite erosiva, mentre alla valutazione endoscopica del colon presenza di lesioni ulcerative a livello dell'ampolla rettale e di polipo in assenza tuttavia di sanguinamenti in atto.
Fig. 6: a sinistra: esecuzione di trombectomia reolitica con sistema AngioJet TM 4 F
Alla luce dell’evento emorragico , in considerazione delle condizioni cliniche della paziente, del basso peso corporeo, nonostante la fibrillazione atriale con alto rischio cardioembolico e la presenza do alterazioni genetiche pro-coagulanti si decideva di soprassedere dal ripristino della terapia anticoagulante orale.
Nei giorni seguenti la paziente ha recuperato un soddisfacente quadro di compenso cardiaco con emodinamica stabile per cui è stato possibile svezzarla dalle amine e rimuovere IABP. Alla dimissione la paziente presentava una progressivo recupero della funzione sistolica ventricolare sinistra (FE 53%), insufficienza mitralica moderata, veniva impostata terapia con la sola terapia antiaggregante con Clopidogrel. Ad un mese dalla dimissione la paziente ha eseguito nuova colonscopia di controllo della sospetta lesione substenosante a 10 cm dall'ano, risultata negativa e con completa regressione delle lesioni ulcerative precedentemente segnalate. Ai follow-up successivi veniva confermata la sola terapia antiaggregante piastrinica con Clopidogrel, oltre ovviamente alla terapia con ACE-I, β-bloccante, statina e gastroprotettore. La paziente ha recuperato un buon compenso emodinamico e non ha ripresentato, alla data attuale recidive ischemiche né emorragiche.
3. Discussione
3.1 I primi studi sulla trattamento interventistico della trombosi coronarica.
I primi studi di valutazione della sicurezza, fattibilità ed efficacia dei differenti devices di trombectomia durante sindrome coronarica acuta, di tipo monocentrico e con piccola casistica, hanno dimostrato che la protezione embolica può essere effettuata con accettabile profilo di sicurezza durante angioplastica primaria, con promettenti effetti positivi riguardo i markers di riperfusione8-13.
In uno studio di Limbruno et al.11 è stata valutata l’efficacia del sistema FilterWireTM (Boston Scientific®) in 53 pazienti arruolati consecutivamente durante angioplastica primaria in corso di SCA STEMI, comparandoli con un gruppo di controllo trattato con la sola angioplastica primaria; l’utilizzo del filtro è risultato fattibile e sicuro, la protezione dall’embolizzazione distale parrebbe esercitare un effetto benefico sui marker di riperfusione miocaridica e sulla funzione ventricolare sinistra a 30 giorni. Nello studio REMEDIA (Randomized Evaluation of the effect of MEchanical reduction of Distal embolization by thrombus aspiration In primary and rescue Angioplastyl)14, condotto su 99 pazienti con SCA STEMI, la tromboaspirazione (con device Diver CE Invatec®) ha mostrato di migliorare la perfusione miocardica espressa come myocardial blush grade e riduzione del sopraslivellamento ST-T senza tuttavia avere nessun impatto sugli end point clinici. Similmente, De Luca et al.15 hanno dimostrato in uno studio condotto su 76 pazienti con SCA STEMI anteriore, come la trombectomia con aspirazione (mediante sistema Diver CE, Invatec®) migliori gli indici di funzione microrvascolare valutati ancora secondo myocardial blush grade e risoluzione del tratto ST-T, riduca l’incidenza di rimodellamento negativo del ventricolo sinistro a 6 mesi senza tuttavia incidere sull’incidenza di MACE (major adverse cardiac events).
Ancora, il trial DEAR-MI (Dethrombosis to Enhance Acute Reperfusion in Myocardial Infarction)16, ha mostrato che l’utilizzo del catetere da aspirazione di trombi Porto extraction catheter (Vasc.solutions®) ha un effetto positivo sulla perfusione microvascolare senza però modificare in maniera significativa gli outcomes intraospedalieri.
Contrariamente ai lavori citati, l’utilizzo del catetere di tromboaspirazione Rescue (Boston Scientific®) non sembra avere nessun impatto sulla quantità di miocardio preservato, valutata mediante scintigrafia miocardica (SPECT: single-photon emission CT nuclear imaging ) perfusionale sestamibi17.
3.2 L’utilizzo routinario dei device di protezione embolica durante PCI primaria
Alla luce dei primi incoraggianti risultati, fu proposto con entusiasmo l’utilizzo sistematico dei device di protezione embolica. Tuttavia tre studi randomizzati sull’utilizzo routinario dei sistemi di trattamento della trombosi mediante aspirazione o dei device di protezione dell’embolizzazione hanno mostrato un effetto neutro o addirittura negativo sulla riperfusione miocardica e sul danno miocardico finale. Lo studio multicentrico, prospettico e randomizzato EMERALD (Enhanced Myocardial Efficacy and Recovery by Aspiration of Liberated Debris )18 ha testato un sistema di occlusione distale con pallone ed aspirazione (GuardWire Plus, Medtronic®) in 501 pazienti con SCA STEMI; anche se il materiale trombotico veniva effettivamente rimosso nella maggioranza dei pazienti, lo studio ha mostrato come la protezione dell’embolizzazione distale tuttavia non comportava nessun miglioramento del flusso microvascolare, nè una riduzione dell’entità dell’infarto, nè un aumento della sopravvivenza event-free.
Lo studio PROMISE19 ha arruolato 200 pazienti che avevano presentato angina nelle 48 ore precedenti più uno dei tre criteri aggiuntivi quali sopraslivellamento del tratto ST-T, un rialzo degli indici di citonecrosi miocardica e l’evidenza angiografica di un’occlusione trombotica. Lo studio prevedeva una randomizzazione ad un trattamento con la sola PCI oppure all’utilizzo, oltre alle normali tecniche, del sistema FilterWire (Boston Scientific®). L’utilizzo di tale sistema di protezione embolica non ha migliorato la riperfusione nè ha ridotto la misura dell’infarto valutata mediante risonanza magnetica cardiaca.
I sistemi di protezione embolica quali FilterWire e GuardWire non offrono una adeguata protezione alle diramazioni che forniscono flusso alle regione perinfartuali che rimangono esposte al rischio di embolizzazione. Infine I filtri distali potrebbero presentare fissurazioni troppo larghe (solitamente circa 0,1 mm) per poter proteggere efficacemente dalla micro-embolizzazione dei detriti più piccoli ed inoltre non proteggono dal passaggio a valle di mediatori solubili rilasciati dalla componente trombotica altamente reattiva I quali possono determinare effetti negativi sulla riperfusione miocardica.
3.3 I device da trombectomia
La trombectomia reolitica è stata valutata nel trial multicentrico, randomizzato AIMI20, nel quale sono stati arruolati 480 pazienti con STEMI entro 12 ore dall’inizio dei sintomi. L’utilizzo sistematico della trombectomia reolitica, mediante sistema AngioJetTM (Boston Scientific®), non ha ridotto le dimensioni dell’infarto confrontata con la sola PTCA e sembrerebbe avere un effetto
negativo sulla perfusione tissutale e sugli outcome; in particolare è stato ottenuto meno frequentemente un flusso finale TIMI 3 e l’incidenza a 30 giorni di MACE (Major adverse cardiac evnts) è risultata più elevata nei pazienti sottoposti a tromectomia. Ancora lo studio JETSTENT (Comparison of AngioJet Rheolytic Thrombectomy Before Direct Infarct Artery Stenting With Direct Stenting Alone in Patients With Acute Myocardial Infarction)21 ha confrontato il Sistema AngioJetTM (Boston Scientific®) e lo stenting diretto, in pazienti con SCA STEMI (presenza di trombosi grado 3 o 5, refernce vessel ≥ 2,5 mm), riguardo gli end point di risoluzione precoce del sopraslivellamento del tratto ST-T (a 30 minuti) e delle dimensioni dell’infarto alla scintigrafia; la risoluzione precoce del tratto ST-T è stata più frequente nel gruppo di studio rispetto a quello dello stenting diretto (85,8% e 78,8%, rispettivamente (p = 0,043), mentre non vi erano differenze negli altri end point surrogati di riperfusione miocardica. A 6 mesi i MACE erano minori nel gruppo di studio (11,2% e 19,4%, p = 0,.011). La sopravvivenza senza eventi ad un anno è stata ancora migliore nel gruppo sottoposto a trombectomia reolitica (85,.2 ±_ 2,.3% vs 75,0 ± 3,1% p = 0.009).Anche se gli end point primari non erano stati raggiunti, per gli autori lo studio pareva supportare l’utilizzo della tromebctomia reoltica prima dello stenting.
Lo studio X-AMINE ST trial22, ha valutato il sistema di trombectomia X-sizer (eV3) il quale ha mostrato comportare solo un lieve miglioramento nella risoluzione del tratto ST-T senza nessun impatto sul flusso TIMI, il blush miocardico o sugli outcomes clinici.
Questi studi hanno pertanto introdotto risultati discordanti e non parrebbero supportare l’utilizzo routinario della trombectomia nella PTCA primaria. Ci sono varie ragioni che potrebbero giustificare perché questi studio abbiano fallito nel dimostrare un beneficio in termini di perfusione miocardica ed outcome. L’embolizzazione distale durante PCI primaria potrebbe contribuire solo in maniera limitata alla necrosi finale e all’entità del danno, giocando un ruolo minore rispetto a quello determinato dal danno ischemia/riperfusione. Inoltre, più che le dimensioni finali dell’infarto (infarct size), sarebbe stato più corretto valutare come parametro di effettiva protezione e “salvataggio” di tessuto vitale il rapporto danno miocardico-area a rischio. Infine vi è un bias legato alla scelta operatore-dipendente nei trial che prevedevano la randomizzazione dopo la coronarografia diagnostica. I dispositivi di embolectomia reolitica come AngioJetTM potrebbero essere solo parzialmente efficaci rimuovendo solo una quota del materiale trombotico potenzialmente emboligeno.
3.4 I device da tromboaspirazione: letteratura 3.4.1 Lo studio TAPAS
Lo studio TAPAS 23,24 ha arruolato 1071 pazienti con SCA STEMI, randomizzandoli a PTCA convenzionale o trombectomia mediante aspirazione. L’end point primario, un grado di myocardial blush post procedurale 0 o 1, si è verificato nel 17,1% dei pazienti nel gruppo trombectomia contro il 26,3% nel gruppo trattato con PTCA convenzionale (P= 0,001). Anche gli outcomes secondari quali completa risoluzione del sopraslivellamento del tratto ST-T (56,6% versus 44.2%, P=0,001) e l’assenza di una persistente deviazione del tratto ST (53,1% versus 40,5%, P=0,001) sono risultati più frequentemente raggiunti nel gruppo trattato con trombectomia. Ancora più rilevante una migliore perfusione miocardica si è associata con un trend verso una minore mortalità a 30 giorni (2,1% versus 4,1%, P=0,07), anche se nello stesso frame temporale non vi erano differenze statisticamente significative per quanto riguarda reinafrto (0,8% versus 1,9%, P= 0,11), target-vessel revascularization (4,5% versus 5,8%, P=0,34), sanguinamenti maggiori (3,8% versus 3,4%,
P= 0,11) e MACE (major adverse cardiac events) (6,8% versus 9,4%, P= 0.12). Ad un anno di
follow-up la morte per cause cardiache si è verificata nel 3,6% dei pazienti sottoposto a tromboaspirazione e nel 6,7% di quelli trattati con PTCA convenzionale (P= 0,020). Gli autori hanno pertanto dimostrato come la procedura di tromboaspirazione sia fattibile nella larga maggioranza dei pazienti con SCA STEMI e che questa comporti una migliore riperfusione miocardica associata a migliori outcome clinici se confrontata alla sola PTCA.
3.4.2 Gli studi TASTE e TOTAL
Recentemente sono stati pubblicati due grandi trial randomizzati, adeguatamente potenziati per valutare la superiorità di una strategia di trombsoaspirazione manuale routinaria versus PTCA convenzionale.
Lo studio TOTAL 25,26 (ThrOmbecTomy with PCI vs. PCI ALone in patients with STEMI) ha randomizzato 10732 pazienti con SCA STEMI e prevedeva una analisi pre-specificata del sottogruppo di pazienti con elevato carico trombotico (TIMI thrombus grade ≥ 3). L’end point primario composito di morte cardiovascolare, infarto miocardico, shock cardiogeno o scompenso cardiaco non era statisticamente differente ad un anno con l’utilizzo della tromboaspirazione manuale sia nel gruppo con elevato carico trombotico (8.1% vs. 8.3% nella tromboaspirazione; hazard ratio [HR]: 0,97; 95% confidence interval [CI]: 0,84 - 1,13) che in quello con basso carico (6,0% vs. 5,0% thrombus aspiration; HR: 1,22; 95% CI: 0,73 - 2,05; interaction p = 0,41). Tra i pazienti con elevato burden trombotico sottoposto a tromboaspirazione è stato osservato un
aumento dell’incidenza di stroke a 30 giorni (31 [0,7%] vs. 16 [0,4%] nel gruppo solo PTCA, HR: 1,90; 95% CI: 1,04 - 3,48). In questo gruppo inoltre la tromboaspirazione non ha migliorato significativamente la mortalità cardio-vascolare a 30 giorni (HR: 0,78; 95% CI: 0,61 - 1,01; p = 0,06) ed a un anno (HR: 0,88; 95% CI: 0,72 to 1,09; p = 0,25). Indipendentemente dal trattamento ricevuto è stato rilevato come un elevato carico trombotico sia un predittore indipendente di morte (HR: 1,78; 95% CI: 1,05 - 3,01).
Nello studio TASTE 27,28 sono stati arruolati 7244 pazienti con SCA STEMI, randomizzati a tromboaspirazione seguita da PTCA o solo PTCA. L’end-point primario, la mortalità per tutte le cause a 30 giorni, è stato osservato nel 2,8% dei pazienti nel gruppo tromboaspirazione (103 di 3621) e nel 3,0% (110 su 3623) nel gruppi di controllo (hazard ratio: 0,94; 95% CI: 0,72 - 1,22; P=0,63). Il tasso di ospedalizzazione per infarto miocardico ricorrente a 30 giorni è stato del 0,5% e dello 0,9% (hazard ratio, 0,61; 95% CI: 0,34 - 1.07; P=0.09), la trombosi di stent si è verificata nello 0.2% e nello 0.5% dei pazienti rispettivamente nei due gruppi (hazard ratio: 0,47; 95% CI: 0,20 – 1,02; P=0,06). Non si sono rilevate differenze significative per quanto riguarda l’incidenza di stroke o complicanze neurologiche al momento della dimissione (P=0.87). I risultati si sono mantenuti coerenti in tutti i maggiori sottogruppi pre-specificati, anche quelli stratificati in base al carico trombotico e al flusso coronarico prima della PTCA.
3.4.3 Revisione della letteratura
I dati in letteratura, prima del TAPAS, non fornivano una chiara indicazione circa la reale utilità del trattamento di trombectomia in corso di PCI primaria; due metanalisi sono state condotte per chiarire questo argomento. Un primo lavoro pubblicato dal De Luca 29 nel 2007 ha incluso 21 trial con 3721 pazienti, l’utilizzo aggiuntivo di device meccanici per il trattamento specifico della trombosi è risultato associato ad un più alto tasso di flusso TIMI 3 finale (89,4% vs 87,1%, P = 0.03), ad un significativo incremento dell’incidenza di myocardial blush di terzo grado postprocedurale (48.8% vs 36.5%, P = 0.0001) ed a una minore embolizzazione distale (6,0% vs 9,3%, P = 0,008), senza tuttavia determinare a 30 giorni nessun beneficio in termini di mortalità (2,5% vs 2,6%, P = 0,88). Nel 2008 la metanalisi edita dal gruppo di Burzotta30 ha valutato diciotto studi randomizzati per un totale di 3180 pazienti affetti da SCA STEMI mostrando come l’utilizzo dei device complementari per il trattamento e la gestione della trombosi comporti migliori risultati pere quanto concerne flusso finale TIMI < 3 [OR (95% CI) 0,76 (95% CI 0,51–1,12)], myocardial blush grade (MBG) <3 [0,53 (0,37–0,76)], assenza di regressione del tratto ST-T 0,60 (0,45–0,78), ma ancora una volta senza nessun miglioramento riguardo gli outcome clinici.
Entrambi I lavori pertanto mostrano come l’utilizzo dei device di trombectomia possa ridurre l’evenienza di embolizzazione distale e migliori la perfusione tissutale senza che tuttavia ciò si rifletta sugli outcome clinici.
Questo apparente paradosso tra il miglioramento degli endpoint surrogati di perfusione miocardica e Ia concomitante mancanza di benefici clinici, può aver varie ragioni. La prima è che vi è una significativa eterogenicità tra I vari studi inclusi nelle metanalisi, essendo frequentemente di piccole dimensioni e single-center. La dimensione stessa degli studi non è adeguata ad una valutazione precisa di end point quali morte o recidive di infarto; I criteri di inclusione spesso non prevedevano una precisa definizione e valutazione del carico trombotico e del vaso culprit. Risulta quindi probabile che il maggior beneficio si concentri in pazienti con carico trombotico da moderato ad elevato in vasi di grande calibro che sono maggiormente a rischio di embolizzazione distale. Inoltre pazienti ad alto rischio, con shock cardiogeno o instabilità emodinamica non sono stati inclusi nella maggioranza degli studi, non potendo quindi valutare il possibile beneficio di questi device in un setting di pazienti che potenzialmente potrebbero beneficiarne.
In accordo con I risultati emersi nella maggior parte degli studi più piccoli precedentemente pubblicati il trial TAPAS ha confermato il miglioramento della perfusione tissutale miocardica con la tromboaspirazione, ma a differenza degli altri, ha anche dimostrato un significativo miglioramento degli outcomes clinici ad un anno. Questo è lo studio randomizzato più grande eseguito, con pazienti spesso trattati con stents e inibitori della gliproteina IIb/IIIa, e la cui allocazione nei diversi bracci dello studio veniva effettuata prima dell’esecuzione della coronarografia e quindi senza una valutazione del burden trombotico. Ovviamnete alcuni limiti sono presenti, il primo è che si tratto di uno studio condotto in uno solo centro ad alto volume e con operatori esperti. Il tempo medio door-to-aspiration di 28 minuti o door-to-balloon di 26 minuti sono risultati alquanto brevi e quindi I risultati non potrebbero essere trasferibili in altre condizioni di lavoro. Altro possibile fattore confondente risulta il fatto che nel braccio trombsoaspirazione la maggior parte dei pazienti venivano trattati con uno stenting diretto, mentre nel braccio PTCA convenzionale prima dell’impianto veniva eseguita una dilatazione con pallone. Probabilmente la tromboaspirazione ha migliorato la visibilità e la caratterizzazione della lesione, permettendo l’esecuzione dello stenting diretto, tecnica che comporta una minore embolizzazione distale31, ed un migliore sizing dello stent. Infine lo studio non era disegnato per valutare end point forti quali mortalità e le informazioni riguardo agli outcome clinici devono essere analizzate cautamente. Dopo la pubblicazione dello studio TAPAS sono uscite delle metanalisi che lo hanno incluso nella valutazione. La prima di De Luca32 coinvolgente nove trial e 2417 pazienti (50% nel gruppo dei
device di trombectomia manuale e 50% gruppo controllo) ha mostrato come l’utilizzo della trombectomia sia associato ad un incremento significativo del flusso TIMI 3 a fine procedura (87.1 vs. 81.2%, P < 0.0001), del myocardial blush grade (MBG) 3 (52,1 vs. 31,7%, P < 0,0001), ad una minore embolizzazione distale (7,9 vs. 19,5%, P < 0,0001), ed a un significativo beneficio in termini di mortalità a 30 giorni (1,7 vs. 3,1%, P = 0,04). Ancora, Bavry et al33 hanno analizzati i dati da 30 studi con 6145 trattati con trombectomia manuale o con devices di protezione embolica. Negli studi che prevedevano l’utilizzo della trombaspirazione la mortalità era del 2,7% nel gruppo trattato e del 4,4% nel gruppo controllo (solo PTCA) con P = 0,018; l’utilizzo della trombectomia meccanica presentava una mortalità del 5,3% vs 2,8% nel gruppo “PCI alone” (P=0,050) e per quanto riguarda i devices di protezione embolica la mortalità risultava del 3,1% vs 3,4% nel gruppo trattato con solo angioplastica (P= 0,69). Secondo gli autori quindi soltanto l’utilizzo dei cateteri di trombosapirazione comporta un beneficio in termini di mortalità rispetto alla sola PTCA e non l’applicazione di filtri o la trombectomia meccanica.
Nel 2009 Burzotta34 ha condotto una pooled analysis che ha coinvolto 2686 pazienti da 11 studi, al fine di valutare l’impatto della trombectomia sugli outcome clinic a lungo termine e per identifcare I pazienti con un più alto beneficio atteso. L’analisi Kaplan–Meier ha mostrato che l’utilizzo della trombectomia comporta una moratlaità per tute le cause più bassa (P = 0.049). inoltre tale tecnica si associa ad una significativa riduzione dei MACE (P= 0,011) e del composto morte ed infarto miocardico al follow up (P= 0,015). Una valutazione dei sottogruppi ha poi mostrato che la trombectomia migliori la sopravvivenza nei pazienti trattati con inibitori del GP Iib/IIIa (P0= 0,045) e che tale beneficio sulla sopravvivenza si concentra nei pazienti trattati con trombectomia manuale (P= 0,011).
Dopo la pubblicazione degli studi TOTAL e TASTE è stata condotta una metanalisi individual-patient35 per determinare i benefici e i rischi della tromboaspirazione durante PCI primaria. Sono stati valutati i dati di 19047 pazienti arruolati nei tre studi randomizzati più importanti (TAST, TOTAL e TAPAS); a 30 giorni 221 pazienti su 9155 (2,4%) del gruppo trattato con tromboaspirazione hanno presentato morte cardiovascolarela mentre nel gruppo trattato con sola PTCA le morti cardiovascolari sono risultate 262 su 9151 (2,9%) (hazard ratio: 0,84; 95% confidence interval: 0,70–1,01; P=0,06); lo stroke o un attacco ischemico transitorio TIA) si sono verificati in 66 pazienti randomizzati a tromboaspirazione (0,8%) e in 46 pazienti (0,5%) nel braccio di controllo (odds ratio: 1,43; 95% confidence interval: 0,98–2,10; P=0,06). Non si sono osservate differenze rilevanti per quanto concerne infarto miocardico ricorrente, trombosi di stent, scompenso cardiaco, target vessel re revascularization. Nell’analisi del sottogruppo con elevato
devices di tromboaspirazione si è associato ad un minore numero di morti per causa cardiovascolare (170 [2,5%] versus 205 [3,1%]; hazard ratio: 0,80; 95% confidence interval: 0,65–0,98; P=0,03) e con più casi di stroke o TIA (55 [0,9%] versus 34 [0,5%]; odds ratio: 1,56; 95% confidence interval: 1,02–2,42, P=0,04), senza tuttavia raggiungere la significatività statistica (valore della P 0.32 and 0.34, rispettivamente). Pertanto l’utilizzo della tromboaspirazione non pare avere un impatto sugli end-point clinici.
Sulla base dei risultati dei trial e delle metanalisi le recenti linee guida europee sulla sindrome coronarica acuta STEMI36 non raccomando (classe di indicazione III) l’utilizzo routinario della tromboaspirazione manuale, lasciando come possibile eccezione la presenza di un’importante trombosi residua dopo la riapertura del vaso con filo guida o pallone.
3.5 Confronto tra tromboaspirazione e trombectomia reolitica
I devices e le strategie a disposizione per il trattamento percutaneo della trombosi coronarica massiva sono molteplici e con diverse filosofie di base. Non sono molti gli studi che hanno
confrontato diversi approcci e device. Vink et al.37 hanno publicato lo studio TREAT‐MI (A
randomized comparison of manual versus mechanical thrombus removal in primary percutaneous
coronary intervention in the treatment of ST‐segment elevation myocardial infarction) che ha
confrontato l’efficacia egli outcome a lungo tempo di due device di trattamento della trombosi, il catetere da tromboaspirazione Export (Medtronic, Minneapolis, MN) ed il sistema di aspirazione e taglio del trombo X-sizer (eV3, White Bear Lake, MN), quest’ultimo costiutiuto da un catetere a doppio lume con una lama elicoidale ruotante localizzata al tip distale alimentata da un motore a batteria. Il lavoro non ha mostrato nessun vantaggio nell’utilizzo del device X-sizer risetto alla tromboiaspirazione manuale riguardo end point primario di morte cardiaca, reinafrto e target vessel revascularization a 3 anni (22.2% e 18.6%, rispettivamente; HR 1.20; 95% CI 0.65–2.22; P = 0.35).
Parodi et al.38 hanno condotto uno studio che ha confrontato la tromboaspirazione manuale con il device Export Aspiration catheter (Medtronic®, Minneapolis, MN) 6 Fr e la trombectomia reolitica mediante AngioJetTM catheter system (Boston Scinetific®) 4 Fr in pazienti con SCA STEMI; l’end point primario consisteva nella valutazione del carico trombotico residuo mediante OCT (optical coherence tomography), mentre come end point secondari venivano considerati: il TIMI thrombus grade residuo, il flusso TIMI e il myocardial blush finale, la risoluzione precoce del sopraslivellamento ST-T e la percentuale di stent malapposti, la restenosi a 6 mesi e eventi avversi cardiovascolari a 6 mesi.
I risultati hanno rilevato che tutti i pazienti tranne uno mostravano all’OCT post trombectomia persistenza di un certo grado di trombosi residua, maggiore nel gruppo tromboaspirazione manuale rispetto a quello trombectomia reolitica senza tuttavia raggiungere la significatività (P=0,083); allo stesso modo trombosi residue rilevanti sono state rilevate più frequentemente nel gruppo trattato con aspirazione manuale rispetto alla terapia con AngioJet (P=0,039). Tutti gli end-point secondari surrogati della riperfusione si sono mostrati migliori nel gruppo trombectomia reolitica; a 6 mesi non vi erano differenze tra i due gruppi per quanto riguarda gli outcome clinici di morte, reinfarto e stroke, mentre vi sono stati più casi di TVR e struts malapposti nel gruppo tromboaspirazione. Pertanto lo studio ha mostrato come l’utilizzo di questi device comporti solo una parziale rimozione della trombosi, la trombectomia reolitica rispetto alla tromboaspirazione manuale sembra essere più efficace nella rimozione del trombo e della riperfusione miocardica.
Nel 2016 Giglioli et al.39 hanno pubblicato lo studio COCOTH (COmparison between COronary THrombus aspiration with Angiojet® or Export® catheter in patients with Stelevation myocardial infarction submitted to primary angioplasty), un confronto tra trombectomia reolitica con sistema AngioJet e tromboaspirazione manuale con sistema Export in185 pazienti con SCA STEMI. L’ end point primario dello studio consisteva in un indice surrogato di riperfusione ovvero la riduzione del tratto ST-T dopo 90 minuti dopo riapertura del vaso culprit; endopoint secondari consistevano nella valutazione di alcuni parametri angiografici quali il flusso TIMI, il TIMI frame count e Myocardial Blush Grade ed una quantificazione dell’entità e delle dimensioni dell’infarto alla scintigrafia miocardica. Per quanto concerne l’end-point primario entrambe le metodiche hanno ottenuto una significativa riduzione del sopraslivellamento del tratto ST-T senza differenze statisticamente significative tra l’una e l’altra (P= 0,066); non si sono osservate differenze nemmeno per quel concerne gli end-point secondari di TIMI flow (P= 0,367), TIMI frame count (P= 0,109), blush grade (P= 0,605) e parametri scintigrafici di dimensioni (P= 0,603) e severità (P= 0,392). Gli autori concludevano affermando che le due metodiche sono efficaci nella rimozione del trombo, senza
3.6 Casi in cui la trombectomia potrebbe avere un ruolo realmente efficace
Dopo la pubblicazione dello studio TAPAS23,24 l’utilizzo routinario della tromboaspirazione fu appoggiato, stante anche la facilità di esecuzione e la sicurezza. Tuttavia alcuni aspetti tcnici e fisiooptaologici devono essere tenuti in considerazione nel processo terapeutico della trombosi coronarica. Innanzitutto il fenomeno del “no reflow”, che rispecchia la mancata riperfusione tissutale miocardica nonostante riapertura del vaso epicardico, occorre solo in una parte dei pazienti sottoposto a PTCA primaria. I molti dati clinici e sperimentali mostrano come questo fenomeno si verifiche in un range che va dal 5 al 50% in base ai metodi ed ai criteri utilizzati per definire il no reflow ed alla popolazione presa in esame40,41 . Un flusso TIMI finale inferiore a 3 è stato osseravto in una frazione che va dal 3 al 12% dei casi18,20, quando sono stati utilizzati altri indici surrogati di riperfusione miocardica come la risoluzione precoce del tratto ST-T o il blush miocardico, I percentili più bassi di questi marker (i.e. ST resolution < 50%, blush grade 0 o 1) si sono verificati nel 30% dei casi.
Il fenomeno del no reflow è determinato da più fattori e cause; l’embolizzazione distale è considerata una delle più importanti e prevalenti ma non può essere applicata a tutti I pazienti sottoposto a PTCA primaria e può giustificare la comparsa del fenomeno solo in una frazione dei casi di insoddisfacente riperfusione miocardica. In uno studio Limbruno42 ha mostrato come I detriti embolici raccolti con device di protezione embolica distali quali I filtri (Filter wire) avevano un volume medio di 1,2 ± 2,2 mm3 e che il 75% dei pazienti aveva un volume embolico < 1 mm3, così piccola da non poter determinare un’ostruzione microvascolare clinicamente importante. Inoltre la trombosi non sembra essere il solo meccanismo dell’embolismo coronarico: Tanaka et al.43 hanno dimostrato che la presenza di un elevato pool lipidico all’IVUS sia un forte predittore di no reflow dopo PCI primaria. La possibile embolizzazione di componenti lipidici della placca è stata ipotizzata anche in uno studio44 nel quale è stato rilevato un livello significativamente più elevato di detriti di placca e cristalli di colesterolo nel sangue aspirato dalla coronaria nei pazienti che avevano mostrato no reflow rispetto a quelli con buon flusso finale. I sistemi di aspirazione più comunemente utilizzati riescono probabilmente a rimuovere il materiale trombotico aggettante nel lume prima di effettuare la predilatazione senza avere nessun effetto sul materiale lipidico che viene schiacciato e filtrato dalla parete nel lume durante gonfiaggio del pallone o impianto di stent. Di conseguenza il beneficio del trattamento trombolitico può essere atteso solo in una parte dei pazienti e l’uso routinario su tutti I pazienti con SCA STEMI sembrerebbe inutile in una buona parte dei casi45.
Infine delle volte la trombectomia o la tromboaspirazione non risultano fattibile poiché il materiale trombotico si trova a valle di una stenosi impossibile da sondare con I device, rendendo obbligatoria una predilatazione e quindi incrementando molto il rischio di embolizzazione distale.
Dopo la pubblicazione degli studi TASTE e TOTAL, poi, l’utilizzo routinario della trombasopirazione è stato declassato in classe II dalle ultime linee guida ESC sullo SCA STEMI36. Tuttavia si parla di “routine”, lasciando aperto uno spiraglio all’utilizzo di questi device in situazioni particolari, soprattutto quando vi sia un’importante carica trombotica. Infatti le analisi pre-specificate dei sottogruppi con elevato carico trombotico dei principali studi randomizzati condotti sul tema, mostrano come vi sia una tendenza ad una migliore prognosi di questo gruppo di pazienti seppur senza arrivare ad una differenza statisticamente significativa.
Pertanto la ricerca di marker o dati indicativi di elevato carico trombotico sembra poter essere utili nella scelta dei pazienti da sottoporre a tromboectomia.
La presenza di una occlusione completa “a stampo” o la presenza di trombosi massiva con una lunghezza longitudinale tre volte più grande rispetto al lume del vaso si sono mostrate predittori indipendenti di un elevato carico trombotico all’analisi multivariata (OR 15,8; P < 0,005)42, questi markers angiografici si sono rilevati inoltre perditori di no reflow7 (tasso di no-reflow in presenza vs. assenza dei cut-off o dei segni di trombosi massiva: 52 vs. 10 %, P < 0,001 e 52 vs. 4%, P < 0,0001 rispettivamente). Nello stesso lavoro la stasi del mezzo di contrasto distalmente all’ostruzione o un lume ≤ 4.0 mm risultavano marker aggiuntivi di no-reflow.
Tutti questi segni di trombosi hanno una prevalenza variabile nella popolazione colpita da STEMI: un elevato carico trombotico è stato riportato in un range che va dal 32 al 63% dei pazienti7,42, l’evidenza angiografica di una placca rotta è stata rilevata in circa il 55% dei pazienti46), mentre la presenza all’IVUS di un trombo flottante o di una placca ricca di lipidi nel 21 e nel 34% dei pazienti rispettivamente43,46
3.7 Conclusioni.
Questi dati e queste percentuali pertanto supportano l’ipotesi che non tutti I pazienti con SCA STEMI possano beneficiare della trombectomia, ma la frazione di quelli con elevato carico trombotico, occlusione totale del vaso con scarso flusso nella arterie coronarie epicardiche probabilmente potranno più frequentemente presentare un fenomeno di embolismo e potrebbero essere buoni candidati per la trombectomia. Tra I vari device presenti sul mercato quelli da
Trombectomia reolitica AngioJet ha mostrato avere una tendenza ad una migliore rimozione del trombo e riperfusione miocardica. In una metanalisi del 2013 di confronto tra tromboaspirazione manuale e trombectomia meccanica (con più device valutati), quest’ultima parrebbe più indicate in pazienti con elevato carico trombotico dove risulta comportare migliori benefici in termini di reinfarto e stroke47.
Nel caso clinico descritto la tromboaspirazione non è risultata efficace nella rimozione dell’importante massa trombotica presente a livello del tronco comune, probabilmente per il fatto che trovandosi in un vaso di grande calibro il device non è riuscito ad agganciare la trombosi; la trombectomia reolitica mediante sistema AngioJetTM, in questo caso specifico, ha completamente risolto il quadro mostrando la sua efficacia nel trattamento della trombosi coronarica massiva, sottolineando ancora una volta come non esista un device unico che possa essere valido in ogni situazione ma che la gestione della trombosi coronarica massiva necessiti di una valutazione preparatoria del carico trombotico, della sua posizione nell’ambito della lesione coronarica nonché del calibro del vaso. Inoltre la possibilità di risolvere una trombosi in un albero coronarico apparentemente privo di stenosi coronariche e malattia parietale evidente ha permesso di non impiantare stent in una paziente che ha mostrato poi avere un’importante diatesi emorragica tale da rendere estremamente rischiosa una eventuale doppia terapia antiaggregante piastrinica.
BIBLIOGRAFIA
(1) Ito H, Tomooka T, Sakai N, Yu H, Higashino Y, Fujii K, Masuyama T, Kitabatake A, Minamino T. Lack of myocardial perfusion immediately after successful thrombolysis. A predictor of poor recovery of left ventricular function in anterior myocardial infarction. Circulation. 1992;85(5):1699-1705.
(2) Morishima I, Sone T, Okumura K, Tsuboi H, Kondo J, Mukawa H, Matsui H, Toki Y, Ito T, Hayakawa T. Angiographic no-reflow phenomenon as a predictor of adverse long-term outcome in patients treated with percutaneous transluminal coronary angioplasty for first acute myocardial infarction. J Am Coll Cardiol. 2000;36(4):1202-1209.
(3) Prasad A, Gersh BJ. Management of microvascular dysfunction and reperfusion injury. Heart. 2005;91(12):1530-1532
(4) Henriques JP, Zijlstra F, Ottervanger JP, de Boer MJ, van 't Hof AW, Hoorntje JC, Suryapranata H. Incidence and clinical significance of distal embolization during primary angioplasty for acute myocardial infarction. Eur Heart J. 2002;23(14):1112-1117.
(5) Okamura A, Ito H, Iwakura K, Kurotobi T, Koyama Y, Date M, Higuchi Y, Inoue K, Fujii K. Clinical implications of distal embolization during coronary interventional procedures in patients with acute myocardial infarction: quantitative study with Doppler guidewire. JACC Cardiovasc Interv. 2008;1(3):268-276.
(6) Sianos G, Papafaklis MI, Daemen J, Vaina S, van Mieghem CA, van Domburg RT, Michalis LK, Serruys PW. Angiographic stent thrombosis after routine use of drug-eluting stents in ST-segment elevation myocardial infarction: the importance of thrombus burden. J Am Coll Cardiol. 2007;50(7):573-583.
(7) Yip HK, Chen MC, Chang HW, Hang CL, Hsieh YK, Fang CY, Wu CJ. Angiographic morphologic features of infarct-related arteries and timely reperfusion in acute myocardial infarction: predictors of slow-flow and no-reflow phenomenon. Chest. 2002;122(4):1322-1332.
(8) Antoniucci D, Valenti R, Migliorini A, Parodi G, Memisha G, Santoro GM, Sciagra R. Comparison of rheolytic thrombectomy before direct infarct artery stenting versus direct stenting alone in patients undergoing percutaneous coronary intervention for acute myocardial infarction. Am J Cardiol. 2004;93(8):1033-1035.
(9) Belli G, Pezzano A, De Biase AM, Bonacina E, Silva P, Salvade P, Piccalo G, Klugmann S. Adjunctive thrombus aspiration and mechanical protection from distal embolization in primary percutaneous intervention for acute myocardial infarction. Catheter Cardiovasc Interv. 2000;50(3):362-370.
(10) Beran G, Lang I, Schreiber W, Denk S, Stefenelli T, Syeda B, Maurer G, Glogar D, Siostrzonek P. Intracoronary thrombectomy with the X-sizer catheter system improves epicardial flow and accelerates ST-segment resolution in patients with acute coronary
syndrome: a prospective, randomized, controlled study. Circulation. 2002;105(20):2355-2360. (11) Limbruno U, Micheli A, De Carlo M, Amoroso G, Rossini R, Palagi C, Di Bello V, Petronio
AS, Fontanini G, Mariani M. Mechanical prevention of distal embolization during primary angioplasty: safety, feasibility, and impact on myocardial reperfusion. Circulation.
2003;108(2):171-176.
(12) Napodano M, Pasquetto G, Sacca S, Cernetti C, Scarabeo V, Pascotto P, Reimers B.
Intracoronary thrombectomy improves myocardial reperfusion in patients undergoing direct angioplasty for acute myocardial infarction. J Am Coll Cardiol. 2003;42(8):1395-1402. (13) Yip HK, Wu CJ, Chang HW, Fang CY, Yang CH, Chen SM, Hung WC, Chen CJ, Cheng CI,
Hsieh YK. Effect of the PercuSurge GuardWire device on the integrity of microvasculature and clinical outcomes during primary transradial coronary intervention in acute myocardial infarction. Am J Cardiol. 2003;92(11):1331-1335.
(14) Burzotta F, Trani C, Romagnoli E, Mazzari MA, Rebuzzi AG, De Vita M, Garramone B, Giannico F, Niccoli G, Biondi-Zoccai GG, Schiavoni G, Mongiardo R, Crea F. Manual
thrombus-aspiration improves myocardial reperfusion: the randomized evaluation of the effect of mechanical reduction of distal embolization by thrombus-aspiration in primary and rescue angioplasty (REMEDIA) trial. J Am Coll Cardiol. 2005;46(2):371-376.
(15) De Luca L, Sardella G, Davidson CJ, De Persio G, Beraldi M, Tommasone T, Mancone M, Nguyen BL, Agati L, Gheorghiade M, Fedele F. Impact of intracoronary aspiration
thrombectomy during primary angioplasty on left ventricular remodelling in patients with anterior ST elevation myocardial infarction. Heart. 2006;92(7):951-957.
(16) Silva-Orrego P, Colombo P, Bigi R, Gregori D, Delgado A, Salvade P, Oreglia J, Orrico P, de Biase A, Piccalo G, Bossi I, Klugmann S. Thrombus aspiration before primary angioplasty improves myocardial reperfusion in acute myocardial infarction: the DEAR-MI
(Dethrombosis to Enhance Acute Reperfusion in Myocardial Infarction) study. J Am Coll Cardiol. 2006;48(8):1552-1559.
(17) Kaltoft A, Bottcher M, Nielsen SS, Hansen HH, Terkelsen C, Maeng M, Kristensen J, Thuesen L, Krusell LR, Kristensen SD, Andersen HR, Lassen JF, Rasmussen K, Rehling M, Nielsen TT, Botker HE. Routine thrombectomy in percutaneous coronary intervention for acute ST-segment-elevation myocardial infarction: a randomized, controlled trial. Circulation. 2006;114(1):40-47.
(18) Stone GW, Webb J, Cox DA, Brodie BR, Qureshi M, Kalynych A, Turco M, Schultheiss HP, Dulas D, Rutherford BD, Antoniucci D, Krucoff MW, Gibbons RJ, Jones D, Lansky AJ, Mehran R. Distal microcirculatory protection during percutaneous coronary intervention in acute ST-segment elevation myocardial infarction: a randomized controlled trial. JAMA. 2005;293(9):1063-1072.
(19) Gick M, Jander N, Bestehorn HP, Kienzle RP, Ferenc M, Werner K, Comberg T, Peitz K, Zohlnhofer D, Bassignana V, Buettner HJ, Neumann FJ. Randomized evaluation of the effects of filter-based distal protection on myocardial perfusion and infarct size after primary percutaneous catheter intervention in myocardial infarction with and without ST-segment elevation. Circulation. 2005;112(10):1462-1469.
(20) Ali A, Cox D, Dib N, Brodie B, Berman D, Gupta N, Browne K, Iwaoka R, Azrin M, Stapleton D, Setum C, Popma J. Rheolytic thrombectomy with percutaneous coronary intervention for infarct size reduction in acute myocardial infarction: 30-day results from a multicenter randomized study. J Am Coll Cardiol. 2006;48(2):244-252.
(21) Migliorini A, Stabile A, Rodriguez AE, Gandolfo C, Rodriguez Granillo AM, Valenti R, Parodi G, Neumann FJ, Colombo A, Antoniucci D; JETSTENT Trial Investigators. Comparison of AngioJet rheolytic thrombectomy before direct infarct artery stenting with direct stenting alone in patients with acute myocardial infarction. The JETSTENT trial. J Am Coll Cardiol. 2010;56:1298–1306.
(22) Lefevre T, Garcia E, Reimers B, Lang I, di Mario C, Colombo A, Neumann FJ, Chavarri MV, Brunel P, Grube E, Thomas M, Glatt B, Ludwig J. X-sizer for thrombectomy in acute
myocardial infarction improves ST-segment resolution: results of the X-sizer in AMI for negligible embolization and optimal ST resolution (X AMINE ST) trial. J Am Coll Cardiol. 2005;46(2):246-252.
(23) Svilaas T, Vlaar PJ, van der Horst IC, Diercks GF, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, Tan ES, Suurmeijer AJ, Zijlstra F. Thrombus aspiration during primary percutaneous coronary intervention. N Engl J Med. 2008;358:557–567. doi:
(24) Vlaar PJ, Svilaas T, van der Horst IC, Diercks GF, Fokkema ML, de Smet BJ, van den
Heuvel AF, Anthonio RL, Jessurun GA, Tan ES, Suurmeijer AJ, Zijlstra F. Cardiac death and reinfarction after 1 year in the Thrombus Aspiration during Percutaneous coronary
intervention in Acute myocardial infarction Study (TAPAS): a 1-year follow-up study. Lancet. 2008;371:1915–1920. doi: 10.1016/ S0140-6736(08)60833-8
(25) Jolly SS, Cairns JA, Yusuf S, Rokoss MJ, Gao P, Meeks B, Kedev S, Stankovic G, Moreno R, Gershlick A, Chowdhary S, Lavi S, Niemela K, Bernat I, Cantor WJ, Cheema AN, Steg PG, Welsh RC, Sheth T, Bertrand OF, Avezum A, Bhindi R, Natarajan MK, Horak D, Leung RC, Kassam S, Rao SV, El-Omar M, Mehta SR, Velianou JL, Pancholy S, Dzavik V, TOTAL Investigators. Outcomes after thrombus aspiration for ST elevation myocardial infarction: 1-year follow-up of the prospective randomised TOTAL trial. Lancet 2016;387(10014):127– 135.
(26) Jolly SS, Cairns JA, Yusuf S, Meeks B, Gao P, Hart RG, Kedev S, Stankovic G, Moreno R, Horak D, Kassam S, Rokoss MJ, Leung RC, El-Omar M, Romppanen HO, Alazzoni A, Alak A, Fung A, Alexopoulos D, Schwalm JD, Valettas N, Dzavik V, TOTAL Investigators. Stroke in the TOTAL trial: a randomized trial of routine thrombectomy vs. percutaneous coronary intervention alone in ST elevation myocardial infarction. Eur Heart J
2015;36(35):2364–2372.
(27) Frobert O, Lagerqvist B, Olivecrona GK, Omerovic E, Gudnason T, Maeng M, Aasa M, Angeras O, Calais F, Danielewicz M, Erlinge D, Hellsten L, Jensen U, Johansson AC, Karegren A, Nilsson J, Robertson L, Sandhall L, Sjogren I, Ostlund O, Harnek J, James SK, TASTE Trial. Thrombus aspiration during Stsegment elevation myocardial infarction. N Engl J Med 2013;369(17):1587–1597.
(28) Lagerqvist B, Frobert O, Olivecrona GK, Gudnason T, Maeng M, Alstrom P, Andersson J, Calais F, Carlsson J, Collste O, Gotberg M, Hardhammar P, Ioanes D, Kallryd A, Linder R, Lundin A, Odenstedt J, Omerovic E, Puskar V, Todt T, Zelleroth E, Ostlund O, James SK. Outcomes 1 year after thrombus aspiration for myocardial infarction. N Engl J Med 2014;371(12):1111–1120.
(29) De Luca G, Suryapranata H, Stone GW, Antoniucci D, Neumann FJ, Chiariello M. Adjunctive mechanical devices to prevent distal embolization in patients undergoing
mechanical revascularization for acute myocardial infarction: a meta-analysis of randomized trials. Am Heart J. 2007;153(3):343-353.
(30) Burzotta F, Testa L, Giannico F, Biondi-Zoccai GG, Trani C, Romagnoli E, Mazzari M, Mongiardo R, Siviglia M, Niccoli G, De Vita M, Porto I, Schiavoni G, Crea F. Adjunctive
devices in primary or rescue PCI: a meta-analysis of randomized trials. Int J Cardiol. 2008;123(3):313-321.
(31) Loubeyre C, Morice MC, Lefevre T, Piechaud JF, Louvard Y, Dumas P. A randomized comparison of direct stenting with conventional stent implantation in selected patients with acute myocardial infarction. J Am Coll Cardiol. 2002;39(1):15-21.
(32) De Luca G, Dudek D, Sardella G, Marino P, Chevalier B, Zijlstra F. Adjunctive manual thrombectomy improves myocardial perfusion and mortality in patients undergoing primary percutaneous coronary intervention for ST-elevation myocardial infarction: a meta-analysis of randomized trials. Eur Heart J. 2008;29(24):3002-3010.
(33) Bavry AA, Kumbhani DJ, Bhatt DL. Role of adjunctive thrombectomy and embolic protection devices in acute myocardial infarction: a comprehensive meta-analysis of randomized trials. Eur Heart J. 2008;29(24):2989-3001.
(34) Burzotta F, De Vita M, Gu YL, Isshiki T, Lefevre T, Kaltoft A, Dudek D, Sardella G, Orrego PS, Antoniucci D, De Luca L, Biondi-Zoccai GG, Crea F, Zijlstra F. Clinical impact of thrombectomy in acute ST-elevation myocardial infarction: an individual patient-data pooled analysis of 11 trials. Eur Heart J. 2009;30(18):2193-2203.
(35) Jolly SS, James S, Dzavik V, Cairns JA, Mahmoud KD, Zijlstra F, Yusuf S, Olivecrona GK, Renlund H, Gao P, Lagerqvist B, Alazzoni A, Kedev S, Stankovic G, Meeks B, Frobert O. Thrombus aspiration in ST-segment-elevation myocardial infarction. An individual patient meta-analysis: Thrombectomy Trialists Collaboration. Circulation 2017;135(2):143–152. (36) Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, Caforio ALP,
Crea F, Goudevenos JA, Halvorsen S, Hindricks G, Kastrati A, Lenzen MJ, Prescott E, Roffi M, Valgimigli M, Varenhorst C, Vranckx P, Widimsky P, ESC Scientific Document Group. 2017 ESC Guidelines for the management of acute myocardial infarction in patients
presenting with Stsegment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of
Cardiology (ESC). Eur Heart J 2018;39:119–177.
(37) M.A. Vink, M.S. Patterson, J. Van Etten, et al., A randomized comparison of manual versus mechanical thrombus removal in primary percutaneous coronary intervention in the treatment of ST-segment elevation myocardial infarction (TREAT-MI), Catheter. Cardiovasc. Interv. 78 (2011) 14–19.
(38) G. Parodi, A. Migliorini, A. Maehara, et al., Comparison of manual thrombus aspiration with rheolytic thrombectomy in acute myocardial infarction, Circ. Cardiovasc. Interv. 6 (2013) 224–230.
(39) C. Giglioli, E. Cecchi, R. Sciagrà et al., COmparison between COronary THrombus aspiration with Angiojet® or Export® catheter in patients with ST-elevation myocardial infarction submitted to primary angioplasty: The COCOTH Study, International Journal of Cardiology 203 (2016) 757–762
(40) Rezkalla SH, Kloner RA. Coronary no-reflow phenomenon: from the experimental laboratory to the cardiac catheterization laboratory. Catheter Cardiovasc Interv. 2008;72(7):950-957. (41) Eeckhout E, Kern MJ. The coronary no-reflow phenomenon: a review of mechanisms and
therapies. Eur Heart J. 2001;22(9):729-739.
(42) Limbruno U, De Carlo M, Pistolesi S, Micheli A, Petronio AS, Camacci T, Fontanini G, Balbarini A, Mariani M, De Caterina R. Distal embolization during primary angioplasty: histopathologic features and predictability. Am Heart J. 2005;150(1):102-108.
(43) Tanaka A, Kawarabayashi T, Nishibori Y, Sano T, Nishida Y, Fukuda D, Shimada K, Yoshikawa J. No-reflow phenomenon and lesion morphology in patients with acute myocardial infarction. Circulation. 2002;105(18):2148-2152.
(44) Kotani J, Nanto S, Mintz GS, Kitakaze M, Ohara T, Morozumi T, Nagata S, Hori M. Plaque gruel of atheromatous coronary lesion may contribute to the no-reflow phenomenon in patients with acute coronary syndrome. Circulation. 2002;106(13):1672-1677.
(45) Picchi A, Limbruno U. Thrombus aspiration during primary percutaneus coronary intervention. J Cardiovasc Med 012 Jan,;13(1):16-23.
(46) Mizote I, Ueda Y, Ohtani T, Shimizu M, Takeda Y, Oka T, Tsujimoto M, Hirayama A, Hori M, Kodama K. Distal protection improved reperfusion and reduced left ventricular
dysfunction in patients with acute myocardial infarction who had angioscopically defined ruptured plaque. Circulation. 2005;112(7):1001-1007.
(47) E.P. Navarese, G. Tarantini, G. Musumeci, et al., Manual vs mechanical thrombectomy during PCI for STEMI: a comprehensive direct and adjusted indirect meta-analysis of randomized trials, Am. J. Cardiovasc. Dis. 3 (2013) 146–157.