INDICE
-
Introduzione Pag. 2
-
Dissezioni coronariche spontanee Pag. 3
-
Caso clinico Pag. 4
-
Discussione Pag. 7
-
Conclusioni Pag. 10
-
Bibliografia Pag. 10
Contributo dell’imaging intracoronarico nello studio e nel trattamento delle
dissezioni coronariche spontanee.
INTRODUZIONE
La cardiopatia ischemica rappresenta la principale causa di morte nel mondo [1]. Sebbene la malattia aterosclerotica coronarica, insieme alle sue complicanze trombotiche, sia ritenuta essere la maggiore responsabile di sindrome coronarica acuta, il miglioramento delle tecniche diagnostiche invasive ha permesso di individuare nuove patologie responsabili e, tra queste, la dissezione coronarica spontanea sta emergendo come causa sempre più frequente di dolore toracico, sindrome coronarica acuta o morte improvvisa, soprattutto in donne giovani o di media età, molto spesso con pochi fattori di rischio convenzionali [2, 3]. In questo scenario emergente, in cui la strategia terapeutica rimane ancora molto dibattuta, l’imaging intracoronarico rappresenta una metodica sempre più necessaria come ausilio diagnostico e nella scelta della strategia terapeutica migliore da adottare [4]. Di seguito una breve revisione della letteratura ed il caso di una donna di 71 anni, giunta alla nostra osservazione per sindrome coronarica acuta con sopralivellamento del tratto ST (SCA-STE) e riscontro agiografico di occlusione di arteria circonflessa, associato ad immagine angiografica compatibile con dissezione cronica coronarica su arteria discendente anteriore.
DISSEZIONI CORONARICHE SPONTANEE
Si definisce dissezione coronarica spontanea (SCAD) una rottura longitudinale della parete arteriosa con conseguente separazione tra gli strati che la compongono e formazione di uno spazio intramurale, anche detto falso lume. Per definizione tale rottura avviene spontaneamente, in assenza di eventi traumatici, iatrogeni o legati a processi aterosclerotici.
I meccanismi fisiopatologici identificati alla base delle SCAD sono due: la formazione di una breccia intimale, attraverso cui il flusso ematico si fa strada oltre la lamina elastica interna nel contesto della tonaca media della parete arteriosa (anche nota come “inside-out model”); e la formazione di un ematoma intramurale che vede come primum movens il sanguinamento di vasa vasorum nel contesto della media (il cosiddetto “outside-in model”). In entrambi i casi si ha la formazione del suddetto falso lume, che può o meno comunicare con il vero lume attraverso una breccia intimale. La formazione di questi due spazi vascolari, separati dalla presenza di una lamina miointimale, rappresenta la caratteristica istopatologica patognomonica della dissezione coronarica [5].
La presentazione clinica di questa entità patologica emergente è più frequentemente una sindrome coronarica acuta (SCA), che si sviluppa però in soggetti con un apparente basso profilo di rischio per patologia aterosclerotica. La sua incidenza va dall’1.1 al 4% di tutte le SCA [6], con una prevalenza maggiore, che raggiunge il 15-40%, in pazienti specifici, come le giovani donne, donne in gravidanza o nel post-partum o comunque donne sotto i 50 anni, peraltro in apparente buona salute [7]. Più raramente la presentazione clinica è una aritmia pericolosa per la vita, fino alla morte cardiaca improvvisa di cui le SCAD sembrerebbero responsabili nello 0.5% del totale dei casi,
come emerge da dati derivati da casistiche inglesi [8]. L’età media di presentazione varia tra i 45 e i 56 anni con una media di 50+/-9.8, mentre i casi sotto i 30 anni e sopra gli 80 appaiono rari [7]. E’ stata descritta anche una distribuzione coronarica preferenziale per la discendente anteriore, coinvolta dal 32 al 46% dei casi, sebbene ogni arteria possa essere coinvolta [9, 6] compreso il tronco comune, coinvolto fino al 4% dei casi. Una localizzazione multi-vaso è stata, inoltre, descritta nel 9-26% dei casi [6]. Nelle stesse casistiche, i segmenti coronarici distali risultano essere maggiormente coinvolti [9].
Sebbene le SCAD vengano considerate ad eziologia multi-fattoriale, esistono delle condizioni considerate predisponenti come un’arteriopatia sottostante, ereditaria o acquisita, fattori genetici, l’influenza ormonale [10] o malattie infiammatorie sistemiche, oltre che fattori ambientali scatenanti come l’ esercizio fisico intenso (sia aerobico che isometrico), un forte stress emotivo, il parto, l’utilizzo di sostanze ricreative o di terapia corticosteroidea [9]. Tra le arteriopatie che possono associarsi, andrebbe sempre ricercata la displasia fibro-muscolare (FMD) data l’alta prevalenza riportata in pazienti che si presentano con SCAD, che può raggiungere l’86%[9,11,12,6].
In caso di forte sospetto clinico, la diagnosi di SCAD può essere posta eseguendo un’angiografia coronarica e, nel caso questa non fosse risolutiva, avvalersi di ulteriori tecniche diagnostiche invasive di imaging intra-coronarico, come la tomografia a coerenza ottica (OCT)
CASO CLINICO
Una donna di 71 anni, caucasica, veniva ammessa al pronto soccorso dell’Ospedale degli Infermi di Biella per un dolore toracico tipico, irradiato al dorso, alla spalla e al braccio sinistro, persistente da
circa 3 ore ed associato a sudorazione profusa. L’anamnesi patologica remota era negativa per storia cardiologica ma la paziente aveva come fattori di rischio cardiovascolare l’età, il tabagismo attivo, un diabete mellito tipo 2 non insulino-trattato ed una vasculopatia carotidea non significativa. L’ECG a 12 derivazioni eseguito all’ ingresso mostrava tachicardia sinusale con frequenza cardiaca di 113 battiti/minuto, un sopra-livellamento del tratto ST in sede inferiore con un sotto-livellamento da V3 aV6, per cui si poneva diagnosi di infarto miocardico acuto con sopralivellamento del tratto ST (STEMI). In pronto soccorso veniva prontamente avviata la terapia del caso con dose di carico di duplice terapia anti-antiaggregante piastrinica, rispettivamente 250 mg di acido acetilsalicilico a somministrazione endovenosa e 180 mg dell’inibitore del recettore P2Y12, ticagrelor, per os, e terapia anti-ischemica con betabloccante e la paziente veniva inviata in sala di emodinamica per essere sottoposta ad angioplastica primaria del vaso “culprit” (PPCI). Gli esami ematochimici, eseguiti in urgenza in pronto soccorso, mostravano un iniziale aumento dei marcatori di miocardiocitonecrosi (TnI 0.22 ng/ml, CK-MB 28 UI/l), una normale funzione renale (creatininemia 0.71mg/dl con un filtrato renale stimato di 81 ml/min con formula MDRD) ed una leucocitosi neutrofila (pari al 92.7% di 17 460 globuli bianchi).
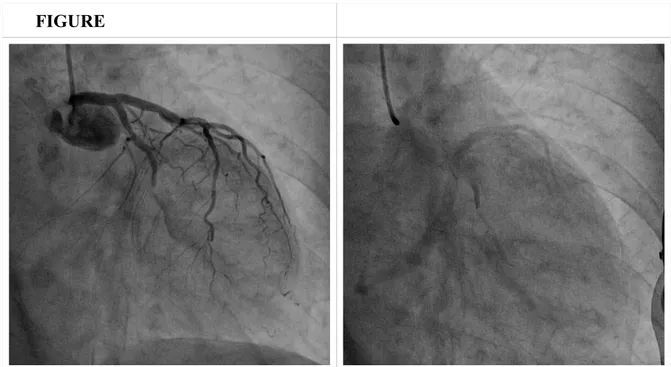
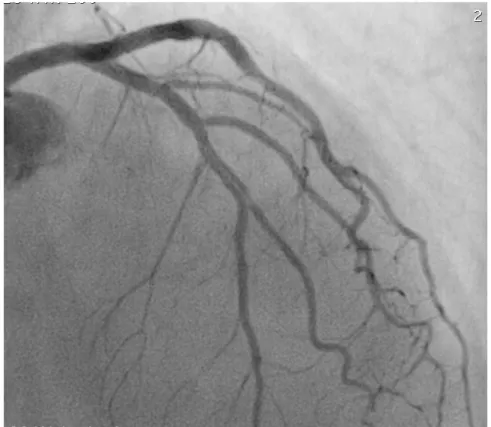
All’esame coronarografico, la canulazione selettiva della coronaria sinistra mostrava l’occlusione di un importante ramo marginale, con flusso TIMI 0 a valle, ed evidenza di omogenea persistenza di contrasto sia a monte che a valle del punto di occlusione del vaso (Figura 1). Si procedeva pertanto ad angioplastica del vaso culprit previa canulazione con catetere guida XB3.5 6F, superamento dell’occlusione con filoguida BMW Universal 0.014” con parziale ricanalizzazione del vaso, e stenting diretto con stent medicato BioMime 3.5 mm di diametro x 44mm di lunghezza. Il risultato agiografico finale veniva poi ottimizzato mediante post-dilatazione con pallone non compliante Pantera Leo 3.5 x 20mm espanso a 18 ATM e documentazione di flusso TIMI 3 finale (Figura 2).
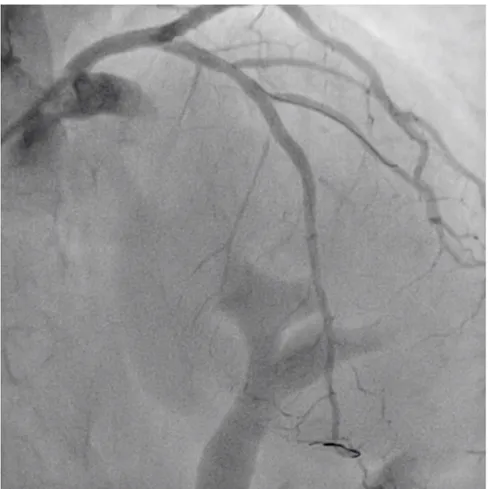
Contestualmente in corrispondenza dell’arteria discendente anteriore, nel segmento medio-distale, subito prima dell’origine di un importante ramo diagonale, veniva evidenziata una immagine sospetta di doppio lume radiolucente, non condizionate una riduzione di flusso nel territorio a valle (Figura 3). Dato il setting acuto, il miglioramento del sintomo e dei segni elettrocardiografici, si decideva di soprassedere temporaneamente ad ulteriori approfondimenti sulla discendente anteriore. La paziente veniva pertanto inviata in UTIC per il proseguo delle cure. Nei giorni seguenti veniva eseguito un ecocardiogramma che mostrava un’acinesia con perdita degli spessori del setto e della parete anteriore nei segmenti medio-apicali, ed una ipocinesia della parete inferiore e postero-laterale media, con una funzione ventricolare sinistra globale moderatamene ridotta (FE 44%). A distanza di 5 giorni la paziente, persistentemente asintomatica, veniva sottoposta a nuovo controllo angiografico con evidenza di quadro coronarografico invariato su discendente anteriore e buon risultato di stenting su ramo marginale ottuso; per chiarire il reperto agiografico su arteria discendente anteriore, si decideva di eseguire approfondimento diagnostico con imaging intravascolare. Dopo posizionamento di filoguida BMW 0.014” in arteria discendente anteriore si procedeva a scansione con OCT che mostrava immagine compatibile con esiti di dissezione coronarica e contestuale verosimile trombosi ricanalizzata del falso lume, con compressione focale subtotale del vero lume; la scansione mostrava inoltre, chiaramente, l’origine del ramo diagonale dal falso lume e il passaggio della guida dal vero lume, in posizione prossimale, ad una delle cavitazioni del falso lume a livello della dissezione, con successivo riattraversamento del flap mio-intimal verso il vero lume nella distalità del vaso (Figura 4). Per l’impossibilità a posizionare secondo filoguida a protezione di ramo diagonale coinvolto dalla dissezione, si decideva di tentare predilatazione con cutting-balloon Flextome 3.0x10 mm espanso a 6 atmosfere nel tentativo di creare un’ampia comunicazione tra i molteplici lumi. Il controllo OCT mostrava discreto risultato
con miglioramento delle comuncazioni, ma anche il successivo secondo tentativo di posizionare filoguida a protezione di ramo diagonale risultava infruttuoso. Si procedeva pertanto ad impianto di stent medicato allo zotarolimus Onyx Resolute 2.5x26 mm, post-dilatato con palloni non complianti a diametro crescente (Pantera Leo 2.5x12 e Pantera Leo 3.0x12). L’impianto dello stent risultava complicato dall’incarceramento dell’ostio del ramo diagonale con conseguente sua sub-occlusione (Figura 5). Data l’assenza di sintomi si decideva di non procedere a nuovo tentativo di posizionamento di guida nel diagonale attraverso le maglie dello stent. In conclusione della procedura veniva eseguito il controllo OCT dello stent impiantato nella discendente anteriore e dello stent precedentemente impiantato su ramo marginale ottuso, che mostrava ottimo risultato in assenza di aree di malapposizione o dissezioni residue ai loro margini.
DISCUSSIONE
Storicamente la prima descrizione agiografica delle dissezioni coronariche spontanee sottolineava l’importanza di individuare la presenza di multipli lumi radiolucenti associati alla persistenza di contrasto extra-luminale [13]. Il miglioramento delle capacità diagnostiche, nel tempo, ha però mostrato come questo aspetto patognomonico sia presente soltanto in una piccola percentuale di casi [2], tanto che nel 2013 è stata proposta una nuova classificazione, ormai ampiamente diffusa, che definisce tre diversi tipi agiografici di SCAD [11]:
• tipo 1: ovvero il modello classico, caratterizzato da una patognomonica presenza di multipli lumi radiolucenti associati alla persistenza di contrasto nella parete arteriosa, con o senza lento lavaggio del contrasto. Questa tipologia è riscontrabile dal 29 al 48% dei casi [5];
• tipo 2: caratterizzato da un restringimento lungo e diffuso (tipicamente superiore ai 20 mm), con profilo regolare che può determinare una stenosi di severità variabile, da non significativa, fino all’occlusione completa, riscontrabile nel 52-67% dei casi. Nell’ambito di questo gruppo si possono individuare due ulteriori sottotipi: il 2a, in cui vi è una normale ripresa distale del calibro del lume, e il 2b in cui la stenosi si estende angiograficamente fino alla fine del vaso [5];
• tipo 3: che mima una lesione aterosclerotica essendo caratterizzato da una stenosi focale o tubulare, in cui la diagnosi differenziale può essere difficile da raggiungere e può dipendere dall’utilizzo di tecniche di imaging intracoronarico che dimostrino la presenza di un ematoma di parete o la presenza di un doppio lume. Questo terzo tipo si osserva nello 0-3.9% dei casi [5]. Sebbene l’esame agiografico sia diagnostico in una discreta percentuale di casi, talvolta, il suo principale limite di essere un esame luminografico bidimensionale, non permette di escludere o confermare con certezza la diagnosi, che viene rimandata a tecniche di diagnostica invasiva intraluminale, e tra queste l’OCT.
Nel caso in oggetto, una successiva attenta revisione della prima angiografia, anche alla luce del successivo riscontro di dissezione ricanalizzata dimostrata su arteria discendente anteriore dallo studio di imaging intracoronarico, lasciava propendere per una occlusione acuta del ramo marginale da dissezione spontanea di tipo 2b, limitante il flusso, mentre il reperto sulla discendente anteriore era compatibile, già in prima analisi, con una dissezione cronica, spontanea; tuttavia l’aspetto irregolare, associato all’origine di un discreto ramo diagonale in corrispondenza della lesione, ci hanno indotto ad utilizzare l’OCT per definire la migliore strategia di trattamento. L’OCT è una tecnica invasiva che utilizza una luce non visibile, nello spettro dell’infrarosso, e permette una scansione ad altissima risoluzione (pari a circa 10-20 micron) del vaso coronarico. Questa altissima risoluzione spaziale longitudinale, è bilanciata da una più bassa capacità di penetrazione nella
parete del vaso (risoluzione assiale), che tuttavia, nella maggior parte dei casi, non preclude la possibilità di raggiungere la diagnosi in caso di SCAD, permettendo invece la visualizzazione della breccia intimale, di trombi intraluminali e del falso lume con un’accuratezza maggiore di quanto non facciano altre tecniche di imaging intravascolare con maggiore risoluzione assiale (che permette ad esempio l’intera visualizzazione di un ematoma intramurale, non sempre osservabile con l’OCT), ma minore risoluzione longitudinale.
Oltre che fondamentale nella diagnosi, l’OCT rappresenta un valido aiuto nella scelta della strategia terapeutica e nella ottimizzazione del trattamento una volta che si decida per una strategia interventistica, permettendo di visualizzare la posizione effettiva della guida, escludendone la posizione nel falso lume, permettendo di chiarire l’adeguata copertura del segmento malato e la eventuale completa espansione e apposizione degli struts dello stent [4].
Va ricordato però che nonostante l’indubbia importanza delle tecniche di imaging intracoronarico nella diagnosi di SCAD, queste metodiche racchiudono anche potenziali rischi, come quello di estendere la dissezione coronarica sia come conseguenza del passaggio della guida, che del passaggio della sonda [13], di creare nuove dissezioni iatrogene su un substrato vascolare suscettibile, o di estendere la rima di dissezione per effetto idraulico dell’iniezione di contrasto necessario per l’acquisizione delle immagini. In quest’ottica, pesando i potenziali rischi e i benefici, l’imaging intracoronarico dovrebbe essere eseguito solo quando la diagnosi agiografica sia incerta (come ad esempio nel caso di una SCAD di tipo 3 o per lesioni la cui natura non sia chiara) e quando la stessa lesione non interessi segmenti troppo distali che potrebbero non avere un diametro sufficientemente ampio per accogliere la sonda OCT, ancor più se consideriamo che la strategia terapeutica preferibile in caso di stabilità clinica è ad oggi conservativa [6].
CONCLUSIONI
Il caso clinico riportato mostra l’esempio di una paziente con SCAD multivaso a presentazione clinica con SCA-STEMI, in cui l’utilizzo dell’OCT ha permesso di raggiungere la diagnosi nel contesto di una immagine angiografica sospetta, di perseguire una strategia terapeutica finalizzata alla creazione di un nuovo unico lume aumentando la comunicazione tra vero e falso lume, e di ottimizzare il risultato dello stent impiantato per ridurre le complicanze a lungo termine.
BIBLIOGRAFIA
1. Townsend, N., et al. (2016). "Cardiovascular disease in Europe: epidemiological update 2016." Eur Heart J 37(42): 3232-3245.
2. Alfonso, F., et al. (2012). "Endovascular imaging of angiographically invisible spontaneous coronary artery dissection." JACC Cardiovasc Interv 5(4): 452-453.
3. Saw, J. (2013). "Spontaneous coronary artery dissection." Can J Cardiol 29(9): 1027-1033. 4. Alfonso, F., et al. (2012). "Diagnosis of spontaneous coronary artery dissection by optical coherence tomography." J Am Coll Cardiol 59(12): 1073-1079.
5. Adlam, D., et al. (2018). "European Society of Cardiology, acute cardiovascular care association, SCAD study group: a position paper on spontaneous coronary artery dissection." Eur Heart J 39(36): 3353-3368.
6. Hayes, S. N., et al. (2018). "Spontaneous Coronary Artery Dissection: Current State of the Science: A Scientific Statement From the American Heart Association." Circulation 137(19): e523-e557.
7. Macaya, F., et al. (2018). "Spontaneous coronary artery dissection: contemporary aspects of diagnosis and patient management." Open Heart 5(2): e000884.
8. Hill, S. F. and M. N. Sheppard (2010). "Non-atherosclerotic coronary artery disease associated with sudden cardiac death." Heart 96(14): 1119-1125.
9. Saw, J., et al. (2014). "Spontaneous coronary artery dissection: association with predisposing arteriopathies and precipitating stressors and cardiovascular outcomes." Circ Cardiovasc Interv 7(5): 645-655.
10. Elkayam, U., et al. (2014). "Pregnancy-associated acute myocardial infarction: a review of contemporary experience in 150 cases between 2006 and 2011." Circulation 129(16): 1695-1702.
11. Saw, J., et al. (2013). "Spontaneous coronary artery dissection: prevalence of predisposing conditions including fibromuscular dysplasia in a tertiary center cohort." JACC Cardiovasc Interv 6(1): 44-52.
12. Prasad, M., et al. (2015). "Prevalence of extracoronary vascular abnormalities and fibromuscular dysplasia in patients with spontaneous coronary artery dissection." Am J Cardiol 115(12): 1672-1677.
13. Rogers, J. H. and J. M. Lasala (2004). "Coronary artery dissection and perforation complicating percutaneous coronary intervention." J Invasive Cardiol 16(9): 493-499.
14. Prakash, R., et al. (2016). "Catheter-Induced Iatrogenic Coronary Artery Dissection in Patients With Spontaneous Coronary Artery Dissection." JACC Cardiovasc Interv 9(17): 1851-1853.
12 Figura 2. Risultato angiografico finale dopo angioplastica con
impianto di stent medicatone segmento medio di ramo per
FIGURE
Figura 1. Angiografia coronarica sinsitra. Occlusione del segmento medio del ramo circonflesso, con immagine di “Dye staining” a monte e valle della lesione occlusiva.
13 Figura 3. Immagine radiolucente nel contesto del segmento
medio-distale di discendente anteriore.
Figura 4. Scansione OCT che mostra immagine compatibile con dissezione coronarica e trombo ricanalizzato con compressione di vero lume. La guida appare posizionata nel vero lume in corrispondenza della distalità e del segmento prossimale del vaso, mentre appare nel contesto del falso lume e del trombo ricanalizzato nella porzione corrispondente alla
Figura 5. Angiografia finale che documenta occlusione di ramo diagonale da incarceramento tra le maglie dello stent impiantato nel tratto medio della discendente anteiore.