1
Indice
1. Introduzione
pag. 2
2. Effetti dell’invecchiamento sul sistema cardiovascolare pag. 4
3. Attività fisica e invecchiamento cardiovascolare
pag. 14
a. Il cuore d’atleta
b. Attività fisica ed invecchiamento cardiaco
4. Deformazione miocardica: definizione e metodiche di imaging
pag. 23
a. Strain e strain rate
b. Metodiche di imaging
5. Speckle tracking
pag. 31
a. Stato dell’arte
6. Finalità del lavoro
pag. 37
a. Protocollo di studio
b. Analisi statistica
7. Risultati
pag. 42
2
Introduzione
L’invecchiamento della popolazione mondiale, fino a qualche decennio fa limitato ai Paesi sviluppati, sta diventando sempre più un fenomeno generalizzato. Secondo stime della WHO tra il 2000 e il 2050 il numero di persone oltre i 60 anni sul globo terrestre passerà dall’11 al 22% del totale e in termini assoluti da 605 milioni a circa 2 miliardi. In Italia nel 2050 gli over 65 costituiranno più di un terzo di tutta la popolazione.
Con l’avanzare dell’età aumenta in maniera imponente l’incidenza di varie affezioni cronico-degenerative, come patologie cardiovascolari, tumori, diabete, demenze, osteoartrosi, le quali non sono unicamente causa di morte, ma anche di riduzione della qualità della vita e di limitazione dell’autosufficienza. Fra le varie patologie prima citate le cardiovascolari risultano senza dubbio quelle a più alta incidenza e impatto sociale. Diverse evidenze scientifiche dimostrano che l’ereditabilità dell’aspettativa di vita è legata in parte ad alcuni fattori genici, che possono modificare significativamente l’invecchiamento, con effetti sia positivi che negativi sulla longevità. Al contempo, dalla letteratura scientifica, emerge però che i determinanti che influiscono maggiormente sull’aspettativa e soprattutto sulla qualità della vita sono i fattori ambientali. In sintesi i nostri geni tracciano un limite entro il quale si pone la longevità individuale: la maggiore o minore “tendenza” a raggiungere tale limite dipende dai fattori ambientali e dallo stile di vita.
L’attività fisica è uno dei più studiati fra gli aspetti riguardanti lo stile di vita: la sua influenza benefica sulla longevità è stata a lungo dibattuta dalla comunità scientifica ed in particolar modo è in via di definizione il suo ruolo in soggetti over 65 e over 75. I dati in letteratura ad oggi disponibili sono ancora scarsi, in quanto per molto
3
tempo l’età maggiore di 65 anni è stata considerata criterio di esclusione dagli studi clinici.
Qui a Pisa da circa dieci anni è in corso uno studio su atleti anziani (Master), tramite il quale sono state ricavate diverse evidenze a sostegno dei benefici dell’attività fisica, praticata in maniera regolare da soggetti di età avanzata, sulla riduzione del rischio cardiovascolare. Su questi soggetti è stato effettuato un interessante follow-up della funzione endoteliale nel macrocircolo periferico tramite metodica FMD (Flow Mediated Dilation), e della VO2 max tramite ergospirometria. Quest’ultimo parametro correla molto bene con la fitness cardiorespiratoria.
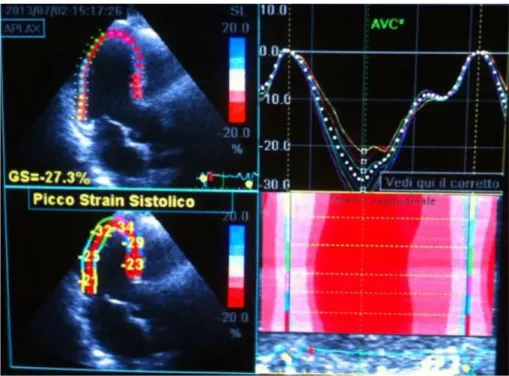
Recentemente all’interno di questo studio multilaterale è stata effettuata un’indagine della funzione ventricolare sinistra, ed in particolare della sistole, tramite la valutazione della deformazione miocardica regionale mediante STE (Speckle Tracking Echocardiography). La contrazione delle fibre miocardiche durante la sistole è un meccanismo complesso caratterizzato da ispessimento, accorciamento e torsione. Per questo motivo la sola determinazione della FE (frazione d’eiezione), parametro utilizzato routinariamente negli studi ecocardiografici per indicare globalmente la performance cardiaca, non è in grado di descrivere né la complessità della contrazione miocardica, né le differenze regionali nella contrattilità. L’ecocardiografia tradizionale stima solo in maniera qualitativa (ipocinesia, acinesia, discinesia) o al limite semiquantitativa la deformazione miocardica regionale; inoltre la valutazione è soggettiva quindi la concordanza sia inter che intra-operatore non risulta adeguatamente elevata. In questo contesto lo Speckle Tracking è utile sia per superare il problema della variabilità inter ed intra-osservatore, sia per ottenere una stima quantitativa e non più solo qualitativa della contrazione dei vari segmenti di miocardio.
4
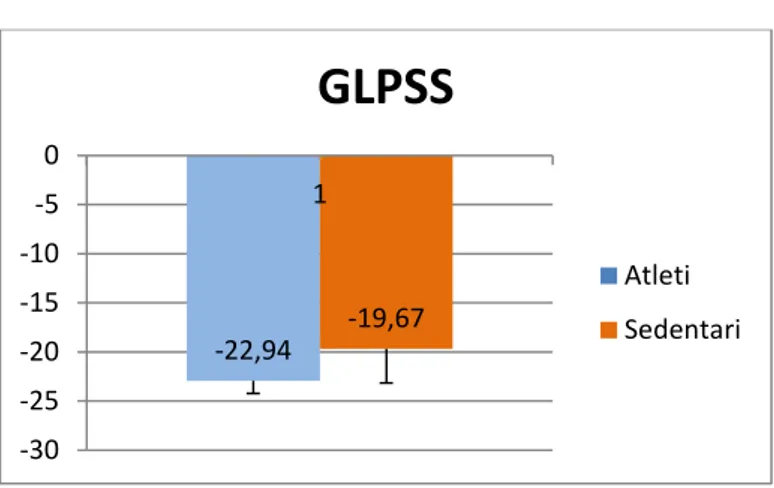
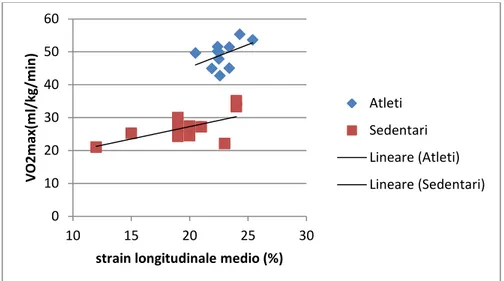
Con questo lavoro abbiamo confrontato i dati sulla deformazione miocardica regionale del ventricolo sinistro ricavati da atleti anziani che praticano attività fisica regolare con quelli ricavati da soggetti sedentari, di pari età, non affetti da patologie cardiovascolari significative. E’ ormai noto infatti che l’invecchiamento, anche in assenza di fattori di rischio aggiuntivi, come diabete, dislipidemie, fumo e ipertensione, causa progressive alterazioni sia funzionali che morfologiche del miocardio. Lo scopo è stato quello di dimostrare una significativa differenza nella contrattilità del ventricolo sinistro fra i due gruppi in studio, in modo da valutare in quali termini gli effetti dell’invecchiamento sulla funzionalità e sulla struttura cardiaca possano essere mitigati dall’attività fisica praticata in età avanzata. Infine abbiamo cercato di stabilire se il rallentamento dell’ ”invecchiamento cardiaco” dal punto di vista morfo-funzionale, evidenziato negli atleti anziani allenati rispetto ai soggetti sedentari, correla in maniera statisticamente significativa sia con il mantenimento di una migliore fitness cardiorespiratoria, buon indice di efficienza fisica, sia con un più modesto deterioramento della funzione endoteliale. La fitness cardiorespiratoria è valutata in termini di massimo consumo d’ossigeno (VO2 max) tramite ergospirometria, mentre la funzione endoteliale è valutata mediante lo studio della dilatazione endotelio-dipendente tramite FMD.
Effetti dell’invecchiamento sul sistema cardiovascolare
L’invecchiamento è un processo caratterizzato dalla progressiva perdita dell’integrità fisica, che porta ad una regressione funzionale di tutto l’organismo e ad un’aumentata suscettibilità allo sviluppo delle principali patologie cronico-degenerative, come tumori, diabete, malattie neurocronico-degenerative, osteoarticolari e
5
cardiovascolari; queste ultime sono sicuramente le più importanti, non solo per mortalità, ma anche per morbilità, impatto sociale ed economico. Tale processo è influenzato sia da fattori genetici1, sia da quelli ambientali e in particolar modo dallo stile di vita (fumo, sedentarietà, alimentazione). Diversi studi hanno evidenziato ad esempio che la dieta ipocalorica ha effetti positivi sull’aumento della longevità e della qualità di vita dell’anziano, in quanto favorisce una minore o più ritardata incidenza delle malattie età-correlate. Secondo alcuni autori, la dieta ipocalorica è correlata ad una maggiore attivazione di alcune vie di signaling intracellulare: adiponectina, insulina/IGF1, AMPK, mTOR, p53, sirtuine2.
Il sistema cardiovascolare è il principale bersaglio dell’invecchiamento. Negli Stati Uniti 75,4 milioni di adulti soffrono di ipertensione arteriosa, 16,3 di patologie coronariche (7,9 di IMA), 5,7 di scompenso cardiaco, 7 di stroke. Secondo uno studio del 2010 dell’AHA (American Heart Association) la prevalenza di queste patologie aumenta drammaticamente sia nell’uomo che nella donna con l’avanzare dell’età, ed è stato stimato che più dell’ 80% dei pazienti con sindrome coronarica, più del 75% con scompenso e del 70% con fibrillazione atriale ha più di 60 anni3. Le prime alterazioni che il sistema cardiovascolare subisce con l’invecchiamento sono a carico dell’endotelio dei vasi. Solo in seguito compaiono le importanti modificazioni morfologiche e funzionali che coinvolgono il cuore e i vasi di grosso calibro. L’invecchiamento quindi primariamente danneggia l’endotelio e ne altera le funzioni, diminuendone la capacità vasodilatatoria e le proprietà antiaterogene e antitrombotiche; in tal modo favorisce l’aumento d’incidenza degli eventi e delle patologie cardiovascolari (ipertensione, IMA, stroke). Ormai è ampiamente dimostrato che il declino della funzione endoteliale età-dipendente è determinato sia da una ridotta biodisponibilità del monossido d’azoto (NO), il quale ha un potente effetto anti-aterogeno, sia da un’aumentata sintesi degli EDCFs (endothelium derived
6
contracting factors), come l’endotelina, angiotensina II, alcuni prostanoidi ciclo-ossigenasi dipendenti (trombossano A2 e prostaglandina H2) e l’anione superossido, i
quali al contrario hanno un effetto globalmente pro-aterogeno. L’NO è un mediatore chimico, sintetizzato nelle cellule endoteliali dalla eNOS, che induce il rilassamento delle cellule muscolari lisce della tonaca media e inibisce l’aggregazione piastrinica, la migrazione e la proliferazione delle cellule muscolari lisce, l’adesione dei monociti e l’espressione delle molecole di adesione all’endotelio. La ridotta biodisponibilità di NO è dovuta in parte ad una sua ridotta sintesi da parte di eNOS, ma principalmente ad una sua aumenta distruzione da parte delle specie reattive dell’ossigeno (ROS), come l’anione superossido. La vasodilatazione endotelio-dipendente è parzialmente mantenuta dalla sintesi di mediatori come prostacicline e EDHFs (endothelium derived hyperpolarizing factors), i quali hanno un azione analoga a quella dell’NO. La funzione endoteliale non può essere studiata con dosaggi di marcatori sistemici a livello sierico, sia perché è distretto specifica e quindi anche all’interno del solito organo può essere presente un diverso grado di attivazione endoteliale, passando da un vaso ad un altro, sia perché l’NO, principale mediatore della vasodilatazione, ha un emivita molto breve e la sua quantificazione istante per istante all’interno di un determinato distretto vascolare è quasi impossibile4. Per questo la biodisponibilità distrettuale dell’NO può essere determinata solo indirettamente, tramite la misurazione della vasodilatazione in seguito ad uno stimolo farmacologico (acetilcolina, bradichinina, sostanza P), meccanico (shear stress) o misto che attivi l’endotelio (vasodilatazione endotelio-dipendente)4, 5. Il declino della funzione endoteliale età-dipendente è specchio del progressivo invecchiamento che colpisce il sistema cardiovascolare in toto.
Le arterie di grosso calibro generalmente sono allungate, tortuose, di dimensioni aumentate, e vanno incontro ad un ispessimento sia dell’intima che della media
7
(IMT), associato ad un aumento di rigidità della parete (ridotta compliance). Questo è dovuto ad una progressiva diminuzione e frammentazione dell’elastina della tonaca intima, alla quale si accompagnano l’aumento di deposizione e di cross-link del collagene (associato ad accumulo degli AGEs, i prodotti della glicosilazione avanzata), e la proliferazione delle cellule muscolari lisce della tonaca media6. Per monitorare le proprietà elastiche delle arterie sono usati prevalentemente due indici: la PWV(Pulse Wave Velocity), che misura la rigidità arteriosa e l’AIx(Augumentation Index), che è indice di riflessione dell’onda sfigmica7
. La compliance dei vasi arteriosi di grosso calibro misurata con queste metodiche è risultata essere maggiore di circa il 40-50% in soggetti giovani ( ≈25 anni) sani, rispetto a soggetti anziani ( ≈75 anni) sani e senza fattori di rischio cardiovascolare aggiuntivi oltre all’età8
. Dal punto di vista clinico questo correla con un aumento della pressione arteriosa sistolica che si accompagna ad una pressione diastolica generalmente normale o addirittura ridotta.
Il cuore dell’anziano va incontro ad alterazioni strutturali e funzionali, messe in evidenza tramite le principali metodiche di imaging, che riflettono modificazioni a livello cellulare. Queste alterazioni colpiscono non solo il miocardio, ma anche l’apparato valvolare e il sistema di conduzione. Secondo il Framingham Heart Study e il Baltimore Longitudinal Study on Aging (BLSA), basati su dati ricavati da adulti apparentemente sani, è presente un aumento età-dipendente dello spessore di parete del ventricolo sinistro, sia negli uomini che nelle donne, il quale indica una maggior tendenza con l’età a sviluppare ipertrofia del ventricolo sinistro (LVH) anche in assenza di ipertensione arteriosa e degli altri classici fattori di rischio cardiovascolare. Le dimensioni della camera ventricolare sinistra sono ridotte, sia il volume telesistolico che il volume telediastolico, ma questo si associa ad sostanziale mantenimento della frazione di eiezione a riposo. Inizialmente i rilevamenti
8
autoptici9, adeguatamente supportati da dati ecocardiografici che prendevano in considerazione l’aumento dello spessore di parete, suggerivano che l’invecchiamento fosse correlato ad un sostanziale aumento della massa cardiaca. Recenti studi autoptici effettuati su soggetti selezionati, non affetti da ipertensione o scompenso cardiaco, hanno invece mostrato che la massa cardiaca, indicizzata in base alla superficie corporea, si mantiene costante con l’avanzare dell’età, con una minima tendenza alla riduzione nel sesso maschile10 11. Questi studi trovano conferma nei dati ottenuti tramite la risonanza magnetica cardiaca (CMR) dai pazienti facenti parte del BLSA12, e nei diversi studi ecocardiografici recenti13. Ricordiamo che la stima ecocardiografica della massa ventricolare sinistra viene effettuata tramite la formula di Devereux, assumendo che la camera ventricolare abbia una forma ellissoidale, con rapporto asse lungo: asse corto di 2:1, tramite l’ M-Mode, con il quale vengono misurati in telediastole lo spessore del setto interventricolare (SIVd), quello della parete posteriore(PPd) e il diametro del ventricolo sinistro (VSd). Massa VS (g) = (0,8* (1,04*[(SIVd + PPd + VSd)3 – Vsd3]) + 0,6 g ; dove 1,04(g/cm3) rappresenta il peso specifico del miocardio, mentre 0,8 è il fattore di correzione per bilanciare la tendenza alla sovrastima della massa ventricolare. Dato che, come abbiamo visto, la massa cardiaca, e di conseguenza anche quella ventricolare, non si modifica in maniera significativa nell’anziano, mentre il volume ventricolare va incontro ad una marcata riduzione, il rapporto massa/volume ventricolare è aumentato14. La funzione diastolica è ampiamente modificata dall’invecchiamento cardiaco. Il riempimento ventricolare sinistro misurato con Doppler trans-mitralico mette in evidenza la presenza di due componenti: l’onda E protodiastolica che fa seguito all’apertura della valvola mitrale e rappresenta la fase passiva del riempimento, o riempimento rapido, l’onda A telediastolica che rappresenta la fase attiva del riempimento, cioè la contrazione atriale. In giovane età nei soggetti sani a riposo il rapporto E/A è
9
maggiore di 1, per loro quindi il riempimento passivo è più importante di quello attivo. Con l’avanzare dell’età il riempimento ventricolare passivo diventa più lento e l’ampiezza dell’onda E tende a ridursi, mentre aumenta la componente A dovuta alla contrazione atriale15 16 17. Aumentano inoltre il volume e la pressione dell’atrio sinistro; questi sono fattori che contribuiscono all’ipertrofia dell’atrio e ad un aumento del rischio di fibrillazione atriale. Diminuisce il rapporto E/A, quindi il volume telediastolico è influenzato sempre più dalla quota dovuta alla contrazione atriale rispetto a quella del riempimento passivo protodiastolico. Questo parametro è clinicamente interpretato come indice di disfunzione diastolica18. Il backscatter integrato (IBS) è un indice ecocardiografico che descrive l’ampiezza media del segnale retro-diffuso dal tessuto a livello di una determinata regione di interesse (ROI). Studi sperimentali hanno dimostrato che l’IBS misurato in telediastole correla con la componente connettivale del miocardio19: l’IBS aumenta in presenza di fibrosi, in maniera proporzionale alla quantità di collagene, quindi non solo nel miocardio infartuato, negli esiti cicatriziali delle miocarditi, nello scompenso, ma anche nelle fasi precoci dell’ipertrofia miocardica patologica20, 21
, che, come abbiamo visto, è tipica anche dell’anziano asintomatico senza fattori di rischio cardiovascolare. L’IBS, misurato generalmente a livello del setto interventricolare e della parete posteriore, risulta quindi utile per differenziare l’ipertrofia patologica da quella fisiologica, anche in assenza di segni ecocardiografici di disfunzione ventricolare. I modelli animali ci hanno permesso di chiarire che con l’invecchiamento, a livello istologico, anche in assenza di fattori di rischio, si verifica una riduzione del numero di cardiomiociti, da attribuire a morte cellulare sia per necrosi che per apoptosi, alla quale si associa l’ipertrofia dei cardiomiociti rimasti. Con l’avanzare dell’età le cellule del miocardio presentano una sempre minore resistenza allo stress ossidativo, dovuta sia ad una ridotta attività dei sistemi
10
antiossidanti che ad aumentata sintesi di radicali liberi. L’iperproduzione di specie reattive dell’O2 (ROS), correlata generalmente sia a fattori estrinseci come fumo,
sostanze inquinanti, radiazioni ionizzanti, farmaci, sia a quelli intrinseci, come l’infiammazione cronica, può essere determinata anche dal semplice “invecchiamento mitocondriale”. È’ stato dimostrato nei topi che l’incremento delle mutazioni del mtDNA, dovuto alla ridotta funzione della DNA polimerasi gamma mitocondriale, sono associate ad una precoce insorgenza di cardiomiopatie22. Mutazioni puntiformi del mtDNA possono causare alterazioni della fosforilazione ossidativa; ad esempio è stata dimostrata una tendenza alla riduzione di funzione dei complessi I e IV, appartenenti alla catena respiratoria23, che causa l’aumento di sintesi di ROS. Altre mutazioni frequenti nell’invecchiamento mitocondriale coinvolgono il gene mCAT responsabile della sintesi della catalasi mitocondriale, enzima che implicato nella riduzione dello stress ossidativo, tramite l’inattivazione del perossido di idrogeno. I roditori che iperesprimono il gene mCAT presentano rispetto agli wild type un rallentamento dell’invecchiamento cardiaco e un aumento del 18% l’aspettativa di vita24, 25
. Le mutazioni del DNA causano nelle cellule post-mitotiche (ovvero a differenziamento terminale), come i cardiomiociti, l’accumulo di lipofuscine, cioè granuli pigmentati costituiti da aggregati di proteine ossidate o mal ripiegate e di lipidi che non possono andare incontro a digestione lisosomiale. Un altro aspetto tipico della senescenza cellulare è l’accorciamento dei telomeri, regioni terminali dei cromosomi costituite da DNA altamente ripetuto, i quali hanno il compito di prevenire la degradazione dei cromosomi stessi e di impedire che le loro terminazioni vengano riconosciute dai sistemi di riparazione come DNA danneggiato. Una riduzione significativa della lunghezza dei telomeri è stata dimostrata nei cardiomiociti (tramite biopsia) e nei leucociti circolanti di pazienti con cardiomiopatie o scompenso cardiaco26, 27. I meccanismi che abbiamo citato sono i
11
principali responsabili della progressiva perdita e della riduzione di funzione dei cardiomiociti. Al contempo il miocardio dell’anziano presenta un aumento della componente collagene della matrice (circa un 50% in più nella settima decade di vita rispetto alla terza28), effetto dovuto non tanto all’aumento della sintesi di nuovo collagene da parte dei fibroblasti in risposta a stimoli infiammatori, quanto ad una sua ridotta distruzione. È stata dimostrata nell’anziano una ridotta espressione ed attività delle metalloproteasi (MMP1 e MMP2) da parte dei fibroblasti del miocardio29. Di conseguenza aumenta la rigidità della parete ventricolare, la quale costituisce la prima causa del rallentato riempimento di inizio diastole. Il secondo meccanismo implicato è il prolungamento della sistole, con conseguente ritardo del rilasciamento ventricolare attivo, al quale contribuisce il ridotto reuptake del calcio dovuto sia alla down-regulation delle ATPasi del reticolo sarcoplasmatico (SERCA2a) e degli scambiatori Na+/Ca2+, sia alla ridotta fosforilazione del fosfolambano3, 30, 31. Con l’età si riduce la funzione sistolica, anche se non in maniera così significativa come la funzione diastolica. Il parametro ecocardiografico storicamente usato per descrivere la funzione sistolica è la frazione d’eiezione (FE). Diversi studi clinici hanno dimostrato che la FE a riposo, in soggetti normotesi, non differisce in maniera significativa fra vari gruppi di età, e si mantiene mediamente intorno al 65%32. La misurazione delle velocità del miocardio a livello del piano valvolare mitrale tramite il Doppler tissutale (metodica di imaging sfruttata, come vedremo in seguito, anche per misurare strain e strain rate miocardico) è in grado di integrare le informazioni sulla funzione sistolica fornite dalla FE33. Come nel caso della FE, anche la velocità di picco sistolico misurata con Doppler tissutale tende a rimanere costante34. Però la contrazione del muscolo cardiaco è un meccanismo complesso, costituito da più componenti, per questo la sistole non può essere descritta unicamente in termini di frazione d’eiezione o velocità di picco sistolico. Se
12
inseriamo il cuore all’interno di un sistema di coordinate per identificare meglio le componenti della sua contrazione possiamo identificare un asse longitudinale, che va dalla base verso l’apice, un asse radiale, perpendicolare all’epicardio, che punta verso l’esterno delle cavità, e un asse circonferenziale, perpendicolare ai due precedenti. Il miocardio contraendosi riduce le dimensioni delle camere ventricolari lungo tutte e tre gli assi (longitudinale, circonferenziale e radiale), quindi il piano valvolare si avvicina all’apice e la parete libera al setto interventricolare; contemporaneamente i ventricoli compiono una rotazione in senso antiorario intorno al proprio asse longitudinale. Passando dalla seconda alla settima decade si verifica un sostanziale decremento dell’accorciamento longitudinale(-20%), mentre tende ad aumentare l’accorciamento radiale (+18%)35, 36
. Il sistema valvolare è interessato da ispessimento fibrotico dei lembi, noduli ialini e calcificazioni, che coinvolgono in particolare l’anulus mitralico e i lembi aortici. La sclerosi della valvola aortica, presente nel 30-80% degli anziani, porta all’ispessimento e all’irrigidimento dei lembi valvolari, limitandone l’escursione e causando con elevata frequenza stenosi aortica. Più rari, anche se tipici dell’anziano, sono il rigurgito aortico, con prevalenza del 13-16% in età avanzata, e le calcificazioni dell’anulus mitralico, fattore di rischio per stenosi mitralica, fibrillazione atriale, scompenso cardiaco, stroke tromboembolico, TIA37. Il sistema di conduzione presenta nell’anziano diverse alterazioni morfologiche che predispongono allo sviluppo di aritmie. Il nodo senoatriale va incontro alla progressiva perdita delle cellule pacemaker: dopo i 70 anni ne rimane un 10%; aumenta inoltre la deposizione di tessuto adiposo, sostanza amiloide e collagene, fenomeno che causa una parziale separazione del nodo dal resto del tessuto atriale. Il nodo atrio-ventricolare, il fascio di His, le due branche e le fibre del Purkinje subiscono le solite alterazioni, anche se in misura minore. L’ECG mostra la tendenza all’allungamento del tratto PR, che rappresenta la velocità di
13
conduzione atrioventricolare: il valore medio è 159 ms nei soggetti fra 20 e 35 anni, 172 ms oltre i 60 anni38. L’asse del QRS devia verso sinistra, probabilmente a causa dell’aumento di spessore del ventricolo sinistro, l’ampiezza delle onde R ed S si riduce e spesso si presentano anomalie aspecifiche del tratto ST-T. Aumenta la prevalenza di fibrillazione atriale, tachicardia parossistica sopraventricolare e aritmie ventricolari. Battiti ectopici ventricolari (BEV) si presentano con elevata frequenza rispetto ai soggetti giovani: uno studio su pazienti over 70, ospedalizzati per cause non cardiologiche, ha mostrato che l’8% di questi presentava all’ECG basale almeno un BEV. Diminuisce la sensibilità agli stimoli β-adrenergici, fenomeno dovuto sia alla riduzione del numero dei recettori, sia alla riduzione dell’attività delle vie di trasduzione del segnale (proteine G associate ai recettori β)39. Il parametro più influenzato è la frequenza cardiaca (HR): si riduce la frequenza cardiaca massima durante esercizio fisico intenso e la variabilità della frequenza cardiaca (HRV) in risposta agli stimoli del sistema nervoso autonomo. Per esempio nel passaggio dal clinostatismo all’ortostatismo l’incremento dell’HR è marcatamente minore nell’anziano rispetto al giovane. La diminuita HRV costituisce un fattore prognostico negativo. In relazione al declino della funzione cardiovascolare, con l’età diminuisce anche la capacità di trasporto e consumo di ossigeno, cioè la capacità aerobica, valutata come massimo consumo di ossigeno (VO2 max). A partire dai 30 anni, ogni
decade viene perso l’ 8-10% del VO2max. Secondo studi recenti a partire dai 70 anni
il declino è marcatamente più rapido (20-25% in meno per decade)40,41. L’equazione di Fick afferma che VO2 = Q (Ca 02 – Cv 02), dove Q è la gittata cardiaca (frequenza
cardiaca * gittata sistolica), Ca 02 il contenuto arterioso di ossigeno, Cv 02 quello
venoso. V02max è quindi modificata negativamente da diversi fattori: il globale
aumento della massa grassa accompagnato dalla riduzione della massa muscolare (massa magra); la riduzione della gittata cardiaca, causata sia dalla ridotta gittata
14
sistolica sotto sforzo, ma principalmente dal progressivo declino della frequenza cardiaca massima, correlata alla perdita di sensibilità agli stimoli del sistema simpatico; la diminuzione dell’estrazione di ossigeno a livello periferico (Ca 02 – Cv
02), attribuita alla perdita sia di volume muscolare sia di capacità ossidativa del
muscolo per unità di volume42. La VO2max risulta quindi un parametro clinico molto
utile per monitorare e quantificare gli effetti dell’invecchiamento sulle capacità fisiche del paziente e sulla qualità della vita; inoltre il suo declino è statisticamente correlato con l’aumentata prevalenza di patologie cardiovascolari42
.
Effetti dell’attività fisica sull’invecchiamento cardiovascolare
Un numero sempre maggiore di studi clinici, supportati adeguatamente da dati di laboratorio, indicano che l’esercizio fisico aerobico, praticato in maniera costante, è un ottimo presidio per mantenere, anche con l’avanzare dell’età, una buona performance fisica e per rallentare l’incremento del rischio cardiovascolare associato all’invecchiamento. Effetti importanti sono evidenti sulla riduzione dell’incidenza di altre patologie, come il diabete, l’obesità, l’osteoporosi e la depressione. Anche in assenza dei fattori di rischio modificabili classici per le malattie cardiovascolari (diabete, dislipidemie, fumo, ipertensione) l’attività fisica è in grado di ridurre marcatamente il rischio cardiovascolare. Gli effetti dell’attività fisica sui singoli fattori di rischio cardiovascolare sono importanti, ma non paragonabili a quelli sul rischio cardiovascolare globale: se praticata in maniera regolare riduce del 5% i lipidi plasmatici (prevalentemente colesterolo totale ed LDL, con un sensibile aumento delle HDL), di 3-5 mmHg la pressione arteriosa sia sistolica che diastolica e dell’1% l’emoglobina glicata, a fronte di una riduzione del rischio cardiovascolare del 30-50% 43. I meccanismi alla base di questi effetti benefici ancora oggi non sono del
15
tutto compresi e quindi risultano oggetto di ricerca. Ormai diversi studi hanno dimostrato che è presente nei soggetti allenati anziani, rispetto ai loro coetanei, una maggiore risposta vasodilatatoria endotelio-dipendente, sia a stimoli meccanici che farmacologici. La vasodilatazione flusso mediata (FMD) dell’arteria brachiale misura la vasodilatazione endotelio-dipendente indotta dallo shear stress, questa viene confrontata con la risposta al glicerolo trinitrato, che costituisce uno stimolo endotelio-indipendente, somministrato per via sublinguale. Il valore FMD ottenuto negli atleti Master è maggiore rispetto a quello dei coetanei sedentari e simile a quello dei soggetti giovani, mentre la risposta al glicerolo trinitrato è la solita per tutti e tre i gruppi. Simili risultati sono stati ottenuti inducendo farmacologicamente l’attivazione dell’endotelio, come ad esempio con l’acetilcolina44. La maggiore risposta endoteliale si esplica con un’incrementata biodisponibilità dell’NO. Questa dipende dall’attivazione intracellulare dell’eNOS (NO sintetasi endoteliale), dall’entità della neosintesi di eNOS, dall’eliminazione dei radicali liberi dell’ossigeno da parte dei sistemi scavengers. La maggiore espressione ed attivazione di eNOS è stata dimostrata sia nel modello animale (roditori allenati vs sedentari)45, sia nell’uomo, tramite uno studio sull’arteria mammaria interna di pazienti con angina stabile che, dopo l’intervento di rivascolarizzazione tramite bypass, sono stati sottoposti ad allenamento per 4 settimane. Rispetto ai controlli i pazienti sottoposti ad allenamento presentavano livelli più elevati di eNOS fosforilata (attivata) e di Akt fosforilata (serina/treonina chinasi attivante eNOS)46. La ridotta soppressione da stress ossidativo della vasodilatazione endotelio dipendente negli atleti anziani è supportata da diversi dati sperimentali. Il gruppo di Pisa ha studiato gli effetti dell’L-NMMA (N-monometil-L-arginina, inibitore di eNOS) e della vitamina C (scavenger antiradicalico) sulla vasodilatazione endotelio dipendente indotta da acetilcolina in quattro gruppi di soggetti: giovani allenati e sedentari e in anziani allenati e
16
sedentari. La vasodilatazione indotta dalla somministrazione solo di acetilcolina è maggiore nei giovani e negli anziani allenati rispetto agli anziani sedentari e l’inibizione della vasodilatazione dopo infusione di L-NMMA risulta avere un’entità maggiore nei gruppi che hanno risposto meglio all’acetilcolina. La vitamina C causa un significativo incremento di risposta all’acetilcolina nei soggetti anziani sedentari, mentre la risposta rimane invariata negli altri gruppi in studio, nei quali sono attivi dei meccanismi endogeni, non ancora identificati, che permettono una migliore risposta allo stress ossidativo da radicali 47. Le ipotesi attualmente al vaglio, già dimostrate sul modello animale, sono l’aumentata espressione della superossido-dismutasi (SOD) e la ridotta attività della NADPH ossidasi a livello endoteliale45. Le pareti delle grandi arterie elastiche dei soggetti anziani allenati presentano una minore rigidità rispetto a quelle dei pari età: nel Baltimore Longitudinal Study of Aging sono stati osservati valori ridotti di PWV (pulse wave velocity), AIx (Augumentation Index) e pressione arteriosa sistolica nei soggetti che da tempo praticavano attività fisica di endurance 48. Inoltre in soggetti di mezza età o anziani, prima sedentari, sottoposti ad un allenamento di 3 mesi (camminata veloce) la compliance dell’arteria carotide aumenta fino a livelli simili a quelli di soggetti che da tempo praticano attività fisica di endurance8. La funzione cardiovascolare dei soggetti che si sottopongono in maniera regolare ad allenamento di resistenza, nonostante declini in maniera inesorabile con l’avanzare dell’età, si mantiene al di sopra dei livelli che garantiscono una buona qualità di vita molto più a lungo rispetto a quella dei soggetti sedentari. Dal Baltimore Longitudinal Study of Aging si evince che la VO2max, che correla molto bene con la performance cardiovascolare, nei
soggetti fra 60 e 80 anni, che praticano corsa di fondo, supera del 30-40% quella dei pari età sedentari e si attesta su livelli simili a quella di soggetti di 2-3 decadi più giovani49. Allo stesso tempo i soggetti sedentari che si sottopongono ad allenamento
17
aerobico presentano un incremento della VO2max del 10-25%; generalmente,
maggiori sono l’intensità e la durata dell’allenamento, migliori sono i risultati40. La prescrizione dell’attività aerobica quindi risulta un presidio fondamentale non solo per aumentare la longevità, ma anche per mantenere il più a lungo possibile attivi ed indipendenti i pazienti anziani.
Il cuore d’atleta
Il cuore dei soggetti allenati (giovani ed anziani) va incontro a modificazioni morfologiche, strutturali e funzionali che lo differenziano da quello dei sedentari pari età. Queste modificazioni causano globalmente un’ipertrofia fisiologica, definita in maniera un po’ generica “cuore d’atleta”, che si esprime come un aumento della massa cardiaca associata al mantenimento di un’adeguata funzione sistolica e diastolica. L’ipertrofia assume caratteristiche differenti a seconda del tipo di allenamento. Secondo Morganroth (1975), anche se queste regole non sono valide per tutte le casistiche, tendenzialmente soggetti che praticano attività di endurance, come il ciclismo, lo sci di fondo e la corsa di resistenza presentano un’ipertrofia eccentrica, con modesto aumento dello spessore delle pareti ventricolari e marcato incremento delle dimensioni cavitarie, in particolare del ventricolo sinistro; al contrario soggetti che praticano attività di forza pura ed effettuano esercizi isometrici (es. il sollevamento pesi) presentano un’ipertrofia concentrica, con diametro ventricolare mantenuto o ridotto, e marcato aumento di spessore della parete ventricolare. Il cronico aumento della richiesta di lavoro cardiaco causa, dal punto di vista funzionale, un incremento della gittata cardiaca massima, della gittata sistolica e una ridotta frequenza cardiaca a riposo, oltre ad alterazioni ECG di ripolarizzazione
18
e conduzione50. Dal punto di vista clinico è importante differenziare l’ipertrofia “fisiologica”, nella quale il rimodellamento indotto dall’attività fisica costituisce un adattamento in grado di garantire un sostanziale incremento della performance cardiovascolare, dall’ipertrofia patologica, che al contrario non migliora la funzione di pompa ed è un importante fattore di rischio per morte cardiaca improvvisa. Nei soggetti normotesi, privi valvulopatie note, che praticano sport, una delle cause più frequenti di ipertrofia patologica è la cardiomiopatia ipertrofica (CMI). All’ecocardiografia, la presenza di uno spessore parietale spesso compreso tra i 13 e i 15 mm è vista con sospetto, quindi è suscettibile di ulteriori accertamenti. L’ipertrofia “fisiologica” presenta un diametro ventricolare sinistro proporzionalmente aumentato (>5,5 mm), a differenza della CMI dove solitamente d < 45mm51. L’ipertrofia patologica è infatti solitamente concentrica, mentre quella fisiologica, per quanto possa essere prevalente l’incremento dell’una o dell’altra componente, tende a sviluppare in maniera armonica l’aumento dello spessore di parete e delle dimensioni cavitarie. Se consideriamo la “relative wall thickness”, RWT = (PPd + SIVd)/VSd, dove PPd è lo spessore della parete libera, SIVd quello del setto e VSd il diametro del ventricolo sinistro (VS), possiamo affermare che valori di RWT > 0,42 sono compatibili con la diagnosi di ipertrofia patologica52. Il VS nel cuore sano presenta una forma ellissoide, mentre nella CMI ha un aspetto irregolare. Nel cuore d’atleta l’ipertrofia appare simmetrica: segmenti adiacenti di parete del VS mostrano differenze <2mm e il rapporto fra spessore del setto interventricolare e parete posteriore del VS a fine diastole è sempre <1,553. Nella CMI invece l’ipertrofia è asimmetrica e spesso coinvolge il setto interventricolare, causando durante la sistole un ostruzione dinamica al tratto di efflusso, che si evidenzia a riposo nel 25% e durante l’esercizio fisico nel 70% dei soggetti affetti54,
55
19
>4,0 mm. Nella CMI l’aumento delle dimensioni dell’AS non è accompagnato né da un proporzionale aumento del diametro del VS, né da un miglioramento del riempimento diastolico, tipico del cuore d’atleta. La rigidità delle pareti è marcatamente elevata, quindi risulta ridotta la compliance delle cavità cardiache. Tramite il Doppler trans-mitralico è possibile certificare che la quota di riempimento rapido di inizio diastole (E) tende ad essere ridotta, e risulta importante la componente di fine diastole dovuta alla contrazione atriale (A): il rapporto E/A diminuisce e talvolta è <1. L’ipertrofia fisiologica è al contrario caratterizzata da una funzione diastolica conservata, se non addirittura implementata. Le velocità miocardiche a livello peri-valvolare tramite il Doppler tissutale forniscono simili indicazioni sulla funzione diastolica. Il Doppler tissutale in M-mode viene sfruttato inoltre per il calcolo del gradiente di velocità transmurale: (Vsubepicardio – Vsubendocardio)/ spessore di parete. È stato osservata la presenza di velocità diverse nel miocardio fra la zona subepicardica e quella subendocardica. Nella fase proto-diastolica il gradiente di velocità transmurale, misurato a livello della parete posteriore del VS, è minore di 0.7s-1 nei soggetti con CMI, maggiore invece in quelli con ipertrofia fisiologica56. L’ECG dei soggetti con CMI presenta anomalie le quali, anche se aspecifiche, si presentano raramente negli sportivi sani: marcata deviazione verso sinistra dell’asse cardiaco, onde Q profonde, e diffuse inversioni dell’onda T. L’ergospirometria mostra solitamente un consumo massimo di ossigeno ridotto rispetto ai valori attesi: un VO2max < 40-45 ml/kg*min in presenza di evidente
ipertrofia cardiaca deve far sospettare CMI, mentre sono ritenuti nella norma tutti i valori >50 ml/kg*min. In caso di diagnosi differenziale incerta il soggetto viene sottoposto ad un periodo di decondizionamento fisico (astensione dagli allenamenti per 3 mesi), successivamente al quale viene nuovamente misurato lo spessore di parete del VS: nei soggetti sani si osserva una riduzione significativa, che oscilla fra
20
i 2 e i 5 mm57. I mutamenti fisiologici del cuore d’atleta sono causati dagli effetti sui cardiomiociti dell’aumento sia del carico di volume, tipico delle attività di resistenza, sia della pressione arteriosa (post-carico) che negli sport di forza pura può arrivare fino a valori di 480/350 mmHg58. I cardiomiociti sintetizzano nuove proteine contrattili e assemblano nuovi sarcomeri, preferenzialmente in serie o in parallelo a seconda della tipologia di allenamento, in modo da aumentare globalmente le dimensioni della cavità ventricolare e incrementare la forza contrattile di ciascuna cellula. Anche nell’ipertrofia patologica la sintesi dei sarcomeri è aumentata, ma essi vengono disposti in maniera disallineata (disarray), dunque la funzione contrattile non risente positivamente dell’incremento della massa miocardica, come in teoria ci aspetteremmo.
Non possiamo però ridurre il fenomeno dell’adattamento del miocardio all’attività fisica ad una semplice aumento delle proteine contrattili. Recenti studi di biologia molecolare hanno messo in luce diversi meccanismi che spiegano l’effetto protettivo dell’attività fisica sull’invecchiamento cardiaco.
Attività fisica ed invecchiamento cardiaco
Gli effetti dell’attività fisica di endurance sull’invecchiamento cardiaco sono stati ampiamente sviscerati nel corso degli ultimi anni. I principali meccanismi responsabili della cardio-protezione sono l’inibizione dell’apoptosi dei cardiomiciti, la maggiore attivazione delle vie di riparazione del danno cellulare, l’incremento di concentrazione dei vasi sanguigni all’interno del miocardio, la rigenerazione dei cardiomiociti a partire dalle eCSCs (endogenous cardiac stem cells). L’inibizione dell’apoptosi è correlata ad un’aumentata espressione a livello delle fibre
21
miocardiche sia di Bcl-2, con conseguente riduzione del rapporto Bax/Bcl-259, sia della HSP7060, implicata anche nei meccanismi di riparazione del danno da ischemia riperfusione. L’esercizio regolare, inducendo l’incremento dei livelli di alcune sirtuine (proteine implicate nella regolazione dell’espressione genica), come SIRT3, favorisce l’attivazione delle vie di riparazione del danno ossidativo. SIRT3 modula positivamente la trascrizione del gene FOXO3a, il quale, a sua volta, promuove la sintesi di superossido dismutasi a livello mitocondriale (MnSOD)61, 62. L’incremento in numero e dimensione dei vasi sanguigni nel miocardio è dovuto agli effetti sia dello shear stress, che favorisce la sintesi di NO, sia dell’aumentata sintesi di fattori di crescita (VEGF, FGF-2, HIF-1), i quali inducono la proliferazione delle cellule endoteliali e muscolari lisce. Sembra che i fattori di crescita prima elencati, oltre ad agire sulle cellule endoteliali già differenziate, siano in grado di attivare ed indurre la proliferazione di un pool di cellule endoteliali staminali definite EPCs (endothelial progentitor cells). Il numero di EPCs è generalmente ridotto in soggetti ipertesi, fumatori, diabetici e sedentari, mentre risulta elevato negli sportivi63. Evidenze emergenti hanno dimostrato la presenza all’interno del tessuto miocardico dell’adulto di cellule staminali cardiache (eCSC) multipotenti, positive per c-kit e negative per CD4564, marcatore delle cellule staminali ematopoietiche. L’attività fisica sembra in grado di modularne positivamente l’attivazione e la proliferazione, e inoltre di poterne rallentare la senescenza tramite la riduzione del danno da stress ossidativo e la protezione dell’integrità dei telomeri. Le eCSC si differenziano in cardiomiociti in risposta all’aumento del carico di lavoro cardiaco65
e rimpiazzano le cellule andate incontro a morte66. Oltre agli effetti protettivi sul miocardio l’attività fisica riveste un ruolo essenziale anche in altri meccanismi che permettono il mantenimento di una performance cardiaca superiore rispetto ai pari età sedentari. Alcuni studi hanno messo in luce che la compliance del ventricolo sinistro dei soggetti allenati anziani è
22
significativamente maggiore rispetto a quella dei sedentari. I volumi telediastolico e telesistolico del VS sono modicamente modificati nell’atleta anziano rispetto al sedentario. Se però tracciamo su un grafico la curva pressione/volume possiamo osservare che a parità di pressione il volume di sangue che riempie la cavità è maggiore nei soggetti che praticano attività fisica67. La legge di Laplace definisce lo stress di parete come T=P*R/2d, dove P è la pressione intracavitaria, R il raggio della cavità e d lo spessore della parete. Lo strain diastolico, cioè la deformazione del ventricolo durante il riempimento, è dato da (Vx-Vmin)/Vmin, dove Vx è il volume in un istante x della diastole, e Vmin quello di inizio diastole. Nei soggetti allenati il rapporto stress/strain durante la diastole è diminuito: ciò significa che a parità di volume di riempimento lo stress di parete è minore rispetto ai sedentari67. La conservazione di una migliore funzione diastolica, oltre che alla ridotta fibrosi, è imputabile al mantenimento di un’adeguata velocità di rilasciamento del muscolo cardiaco. I livelli di mRNA codificanti per le Ca2+ATPasi del reticolo sarcoplasmatico (SERCA2a) sono elevati, mentre rimane invariata l’espressione del fosfolambano68. La maggiore attività dei SERCA2a permette una più rapida reuptake del Ca2+ dal citoplasma al termine della sistole. Le aritmie letali, soprattutto le tachiaritmie ventricolari, le quali causano morte cardiaca improvvisa, sono frequenti nell’anziano. Sembra che la loro incidenza sia implementata in relazione alla riduzione del tono vagale. L’attività fisica di endurance è in grado di diminuire l’incidenza di tali aritmie, favorendo l’aumento del tono vagale e la riduzione dell’attività del sistema simpatico a riposo; essa inoltre migliora la stabilità elettrica delle cellule cardiache, modulando positivamente, tramite la via di segnalazione cellulare dell’Akt, la sintesi e l’attività dei canali al calcio di tipo L69
. Le aritmie di origine sopraventricolare, come fibrillazione e flutter, tendono invece ad avere elevata incidenza negli atleti Master, probabilmente a causa dell’aumento di
23
dimensioni e del rimodellamento dell’atrio sinistro70. L’incremento dell’attività dei canali L rispetto ai sedentari garantisce una maggiore contrattilità miocardica, e quindi anche una migliore funzione sistolica. Nell’anziano che pratica attività di endurance la massa cardiaca, calcolata con risonanza magnetica, è incrementata rispetto ai coetanei non allenati, ma non in maniera tale da pareggiare l’aumento volumetrico delle dimensioni cavitarie. Quindi nel soggetto allenato si riduce il rapporto massa/volume; al contrario nel sedentario questo rapporto tende ad aumentare, anche a fronte di una massa cardiaca ridotta.
Le nuove metodiche che studiano la deformazione regionale della parete cardiaca sono usate dal nostro gruppo per definire, in maniera più dettagliata, rispetto ai parametri ecocardiografici standard, le caratteristiche e l’entità della modificazioni, nella performance ventricolare sinistra, a cui vanno incontro i soggetti anziani che regolarmente praticano attività fisica.
Deformazione Miocardio: Definizione e metodiche di imaging
Strain e Strain Rate
Lo strain è una misura adimensionale che esprime in percentuale la deformazione di un oggetto, cioè la variazione delle sue dimensioni rispetto a quelle iniziali, in risposta ad uno stress. Lo strain degli oggetti unidimensionali è descritto dalla formula Lagrangiana:
ε = (L - L0)/L0
dove L0 è la lunghezza iniziale dell’oggetto, mentre L rappresenta la sua lunghezza
dopo la deformazione71. Se un oggetto ha tre dimensioni dobbiamo considerare sia la deformazione lungo gli assi principali (x,y,z), o deformazione normale, sia la
24
deformazione di taglio o di scorrimento (shear strain), che avviene lungo gli assi paralleli a ciascuno dei tre piani (xy, xz, yz). Quindi in totale nove possibili tipi di deformazione.
Quando descriviamo la deformazione del miocardio dobbiamo tener presente che questo è un oggetto incompressibile: la sua forma può variare, ma il suo volume rimane costante. Quindi, partendo dal presupposto che lo shear strain miocardico non sia significativo, possiamo affermare che la somma delle deformazioni lungo i tre assi principali deve essere zero:
εx + εy + εz = 0
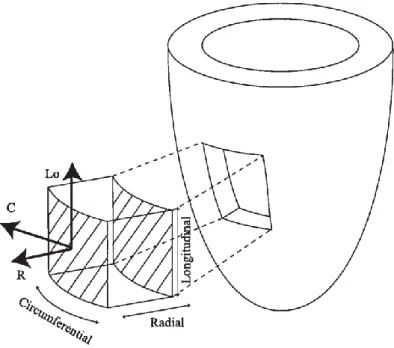
Per descrivere con le metodiche di imaging disponibili la deformazione del muscolo cardiaco utilizziamo un sistema di coordinate locale che identifichi il movimento di ciascun segmento (o punto) nello spazio. Quindi ogni punto del miocardio presenta tre assi, perpendicolari fra di loro, che ne identificano lo spostamento. L’asse longitudinale (L) è tangente all’epicardio e dalla base si dirige verso l’apice del ventricolo, l’asse radiale (R) è perpendicolare a L e all’epicardio, e punta verso l’esterno della cavità, l’asse circonferenziale (C) è perpendicolare agli altri due assi.
25
Figura 1 Il sistema di coordinate locale del cuore
Durante la sistole, con la discesa della base verso l’apice, lo strain longitudinale, secondo la formula Lagrangiana, è negativo, in quanto le fibre tendono ad accorciarsi lungo l’asse L; allo stesso tempo è negativo anche lo strain circonferenziale, mentre è positivo quello radiale, in quanto, secondo il principio di incompressibilità, deve essere presente un ispessimento della parete ventricolare in grado di controbilanciare l’accorciamento lungo gli altri due assi. Durante la diastole i segni dello strain lungo i tre assi sono invertiti rispetto alla sistole.
Lo strain rate (SR) è la derivata dello strain in funzione del tempo, quindi descrive la velocità della deformazione miocardica e si esprime in s-1:
ε(t) = (L(t) – L0)/ L0
SR = = ( ) = (t) =
dove L0 è la lunghezza originaria del segmento preso in considerazione e L(t) è la sua
lunghezza al tempo t72. Lo strain rate presenta i soliti segni dello strain lungo i vari assi nelle diverse fasi del ciclo cardiaco: in sistole sono negativi lo SR longitudinale
26
e circonferenziale, positivo quello radiale; in diastole è negativo lo SR radiale, positivi gli altri due.
Strain ventricolare sinistro e destro
Per comprendere meglio le caratteristiche dello strain del muscolo cardiaco nel ventricolo sinistro, è giusto premettere alcuni dettagli sulla struttura del miocardio di lavoro. Nella muscolatura del VS si possono individuare tre strati sovrapposti: uno subepicardico formato da fibre che dal piano valvolare discendono longitudinalmente e obliquamente, sia anteriormente che posteriormente, verso l’apice, uno intermedio, con fibre orientate in senso circolare, uno subendocardico in cui, dall’apice, esse risalgono obliquamente e longitudinalmente verso la base. Come risultato di questa particolare disposizione, le fibre subendocardiche e subepicardiche variano costantemente angolo nei confronti dello strato intermedio andando a formare due spirali rispettivamente in senso orario ed antiorario73. A livello del subendocardio il gradiente angolare fra le fibre oblique e quelle circonferenziali è di 80°, tende a 0° a livello dello strato intermedio, mentre raggiunge i -60° a livello del subepicardio. La particolare disposizione delle fibre implica durante la sistole l’avvicinamento del piano valvolare all’apice, l’accorciamento circonferenziale, l’ispessimento parietale lungo l’asse R e la torsione in senso antiorario, corrispondente alla disposizione delle fibre subepicardiche, che dominano su quelle subendocardiche in quanto presentano un raggio e quindi un braccio di leva maggiore.
27
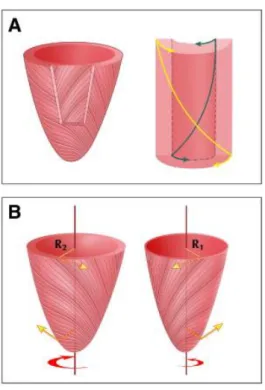
Figura 2 Architettura delle fibre miocardiche del VS. L’orientamento delle fibre miocardiche del VS cambia da un orientamento ad elica sinistrorsa nel subepicardio ad elica destrorsa nel subendocardio (A). Le frecce (B) rappresentano le componenti circonferenziali. I raggi
(R1 per il subendocardio e R2 per il subepicardio) sono i bracci di leva. Le fibre subepicardiche hanno un braccio di leva più lungo di quelle subendocardiche e dominano il
processo di rotazione cardiaca (R1 < R2).
Lo strain lungitudinale è il principale determinante dell’avvicinamento del piano valvolare all’apice. Se ne tracciamo il grafico durante tutto il ciclo cardiaco possiamo valutare la presenza di un onda S negativa in sistole, la quale presenta un picco (peak sistolic strain), in corrispondenza della chiusura della valvola aortica. Durante la diastole invece lo strain tende a ritornare a valori vicini allo zero. In questa fase si possono individuare tre componenti della curva: una iniziale con pendenza elevata, che rappresenta il riempimento rapido, un plateau che corrisponde alla diastasi ed una conclusiva, a pendenza minore rispetto a quella iniziale, che descrive la contrazione atriale. Lo strain lungo l’asse C, molto importante nella determinazione della frazione d’eiezione, è dovuto per lo più alla contrazione delle fibre circonferenziali, le quali, secondo Ingles, sono responsabili dello sviluppo della
28
maggior quota della pressione intracavitaria del VS74. La torsione del VS durante la sistole eiettiva è l’elemento chiave nella determinazione della FE: a fronte di un 15-20% di accorciamento delle fibre miocardiche, permette una riduzione volumetrica del 60%. Dobbiamo specificare che prendendo come punto di osservazione l’apice, la porzione apicale del VS ruota in senso antiorario (positivo), mente quella basale in senso orario (negativo). Il gradiente torsionale (gradi/cm), definito come differenza netta di rotazione fra base ed apice, normalizzata rispetto alla lunghezza del ventricolo, descrive in maniera ideale l’efficienza della torsione del VS. Durante la diastole avviene una rotazione in senso opposto, definita “riavvolgimento” o “untwisting”, che si verifica, in buona parte (40%), durante il rilasciamento isovolumetrico, prima dell’apertura della valvola mitralica. L’untwisting è responsabile della genesi del gradiente di pressione intraventricolare che permette al ventricolo di assolvere alla funzione di suzione del sangue proveniente dall’atrio durante la fase di riempimento rapido. Alcuni autori considerano i valori di untwist e untwist rate buoni parametri di funzione diastolica.
Il ventricolo destro presenta una forma triangolare, con una parete destra più curva che forma un angolo acuto, distinguendosi così dal sinistro che è approssimativamente conico. Le fibre miocardiche hanno un’architettura diversa: è assente lo strato intermedio, quindi la componente circonferenziale dell’accorciamento viene a mancare, mentre è molto rappresentata la componente longitudinale, la quale risulta la principale determinante della FE.
29
La determinazione quantitativa dello strain e dello strain rate miocardico si avvale di tre metodiche di imaging, di cui due ecografiche, il Tissue Doppler Imaging (TDI) e lo speckle tracking, e una di risonanza magnetica.
Risonanza magnetica
La risonanza magnetica sfrutta la tecnica del tagging. I tags sono markers indotti da perturbazioni della magnetizzazione, ottenute con la saturazione selettiva di una radiofrequenza. Queste perturbazioni producono delle zone di ridotta intensità del segnale che appaiono come linee nere (tags) sull’immagine acquisita. I tags sono disposti, in maniera ortogonale fra di loro, a formare una sorta di griglia. Essi accompagnano durante il ciclo cardiaco i movimenti del miocardio, ed è per questo che la loro deformazione e velocità di deformazione descrive con precisione lo strain e lo strain rate miocardico75. La risonanza magnetica offre il vantaggio di un’ottima risoluzione spaziale, ma la risoluzione temporale peggiore, rispetto alle altre metodiche, ed i costi elevati dei software ne sconsigliano per ora l’uso nella pratica clinica76.
Tissue Doppler Imaging
Il Tissue Doppler Imaging (TDI) è una metodica ecocardiografica che si avvale della tecnica Doppler per misurare la velocità di uno specifico punto all’interno del tessuto miocardico durante la contrazione. Il principio è identico a quello che permette di individuare la velocità del flusso ematico nei vasi e nelle camere cardiache. I segnali derivati rispettivamente dal tessuto miocardico e dal sangue sono facilmente distinguibili per due motivi. Per prima cosa la velocità che il flusso ematico raggiunge nelle cavità ventricolari è molto elevata (100-150 cm/s), mentre il miocardio si muove molto più lentamente (5-15 cm/s). In secondo luogo dal
30
miocardio perviene un segnale Doppler di ampiezza maggiore rispetto a quello del flusso ematico. Quindi il TDI isola i segnali a elevata ampiezza e bassa velocità, mentre gli altri sono eliminati tramite un apposito algoritmo. Lo strain rate (SR) regionale viene calcolato come gradiente di velocità fra due punti (A , B) della parete miocardica. SR = (V2 – V1)/ d , dove V1 è la velocità del punto A e V2 quella del
punto B, mentre d è la distanza fra A e B. Lo strain regionale si ottiene calcolando l’integrale dello SR regionale77
.
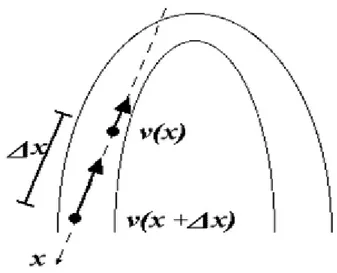
Figura 3 La figura illustra la valutazione longitudinale dello strain rate dalle velocità di due punti del miocardio che si accorcia ad una distanza ∆x, dove v2 è la velocità misurata al punto x, cioè la v (x), mentre v1 è misurata seguendo la stessa linea, ad un punto v (x+∆x) cioè alla distanza ∆x dal x. Pertanto lo SR = [v(x)- v(x +∆x)]/ ∆x = ∆v/∆x = v2-v1/r dove r è la
distanza tra i due punti.
Il TDI rispetto alle altre metodiche disponibili per determinare lo Strain/Strain Rate ha un elevata risoluzione temporale ( >150 Hz) ed è utile nella pratica clinica in special modo per lo studio di pazienti con elevata frequenza cardiaca (es. test da sforzo con dobutamina o dipiridamolo)78. Il limite maggiore del TDI è la dipendenza dall’angolo di insonazione (θ), che si forma tra il fascio di ultrasuoni ed la direzione di deformazione della parete ventricolare. Idealmente θ dovrebbe essere 0°, anche se esistono software in grado di correggere il disallineamento tra fascio di ultrasuoni e direzione di deformazione; se però θ = 90°, non può essere registrata alcuna
31
componente di deformazione. Per questo motivo TDI non è adeguato per lo studio dello strain a livello dell’apice del cuore79.
Speckle tracking
Lo speckle tracking ecocardiografico (STE) è una metodica per il calcolo dello strain/strain rate, alternativa al TDI, introdotta recentemente (2004) da Leitman e Lysyansky. Lo STE si avvale della classica ecocardiografia B-Mode real time (frame-by-frame) che tramite una scala di grigi identifica dei markers acustici che si muovono insieme al tessuto miocardico da un frame a quello successivo. Questi markers sono gli “speckles acustici”, i quali sono generati dalla parziale retrodiffusione di un fascio di ultrasuoni incidente un’interfaccia irregolare. Gli speckles sono equamente presenti all’interno dell’immagine ecografica del miocardio, però la loro distribuzione è casuale. Ogni singola regione di miocardio presenta un pattern di speckles diverso rispetto a quelle adiacenti. Durante il movimento dovuto al ciclo cardiaco ciascuna regione tende a mantenere più o meno stabile il proprio pattern di speckles. Lo STE si avvale di un software in grado di identificare speckle pattern simili da un frame all’altro, in modo da seguire nel tempo lo spostamento di una specifica regione miocardica. L’operatore sceglie delle regioni di interesse (kernel), che delimitano uno specifico speckle pattern; il kernel con lo speckle pattern più simile a quello selezionato originariamente dall’operatore viene ricercato ed identificato dal software, nel frame successivo, all’interno di un’area di ricerca più ampia denominata search region. Il vettore che unisce i due kernel identifica lo spostamento, da un frame a quello successivo, della regione miocardica di interesse80.
32
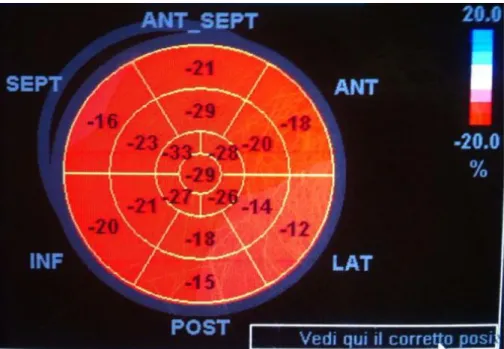
Figura 4 Il software, tramite l’algoritmo di ricerca, identifica il nuovo kernel (verde) del frame successivo sulla base della similitudine dello speckle pattern con quello del kernel di
origine (rosso) del frame precedente. La freccia in blu rappresenta il vettore spostamento
Bisogna tener presente che gli speckle pattern della solita regione di interesse, nonostante rimangano sostanzialmente stabili, presentano comunque delle differenze, che tendono ad aumentare se si dilata il tempo fra un frame e l’altro. È quindi importante usare un frame rate (frame/secondo) adeguatamente elevato (generalmente fra 60 e 110 frame/sec) per ridurre la probabilità di errore nel riconoscimento. Lo STE offre il vantaggio rispetto al TDI di una minore angolo-dipendenza, che lo rende adeguato a calcolare più accuratamente lo strain a livello dell’apice del cuore. Inoltre lo STE è in grado di studiare adeguatamente non solo lo strain longitudinale, ma anche quello circonferenziale e radiale, e di descrivere il gradiente di torsione. I limiti maggiori di questa metodica sono la ridotta risoluzione temporale rispetto al TDI e la maggiore sensibilità ad “acoustic shadowing” e “reverberations” che riducono la qualità dell’immagine e possono far sottostimare la deformazione79. Per ridurre adeguatamente il rumore di fondo, lo strain e lo strain rate vengono calcolati come valori medi su 3 cicli cardiaci consecutivi. Il software deve essere sincronizzato con un tracciato ECG stabile, in quanto la lunghezza L0 di
33
inizio sistole, dalla quale deve partire il calcolo dello strain, è quella misurata al termine del QRS; per questo motivo il ritmo deve essere sinusale81.
L’analisi dello strain longitudinale del VS viene effettuata su tre acquisizioni dalla finestra apicale: proiezione 4 camere; 2 camere e 3 camere (asse lungo apicale). La finestra apicale 4 camere è sfruttata anche per misurare lo strain longitudinale del ventricolo destro. Per il calcolo dello lo strain circonferenziale e radiale, e per le analisi di rotazione e torsione sono sfruttate due acquisizioni in asse corto, una per il piano basale ed una per l’apice. Dopo aver posizionato la sonda in posizione parasternale, il piano basale è identificato come quello che include i margini dei lembi mitralici. La sonda viene spostata distalmente ed anterolateralmente per ottenere un piano che includa l’apice: il piano ideale è posizionato subito prossimalmente a quello che mostra in fase telesistolica il lume della cavità ventricolare completamente obliterato82.
Nonostante sia una metodica di recente introduzione lo STE ha già numerose applicazioni in campo clinico, in quanto permette, rispetto alle tradizionali tecniche ecocardiografiche, una più approfondita valutazione della dinamica sistolica e diastolica del miocardio attraverso un ampio range di condizioni fisiologiche e patologiche81, 83. Ad esempio, non solo è stata osservata un’ottima correlazione tra strain longitudinale globale (misurato con STE) e frazione d’eiezione del ventricolo sinistro, ma lo strain longitudinale regionale è in grado di identificare e determinare quantitativamente la disfunzione di un segmento miocardico anche in presenza di una frazione d’eiezione conservata84
. Oltre che per la diagnosi differenziale fra ipertrofia fisiologica e patologica (cardiopatia ipertensiva, stenosi aortica, CMI, ecc.), di cui discuteremo successivamente, lo STE è risultato utile in diverse altre situazioni cliniche. Lo strain longitudinale ha un valore rilevante nel predire le possibilità di
34
recupero funzionale del miocardio, in soggetti con stenosi coronarica significativa, in seguito ad un intervento di rivascolarizzazione85; inoltre è utile nel follow-up post-operatorio. Lo STE è sfruttato anche per evidenziare il danno miocardico subclinico da patologie sistemiche, come diabete e sindrome di Cushing, oppure da xenobiotici cardiotossici, come alcuni chemioterapici, fra i quali le antracicline e il trastuzumab86. Infine, considerando che lo STE è in grado di rilevare la dissincronia nella contrazione dei vari segmenti ventricolari, alcune pubblicazioni hanno proposto che questa metodica possa avere un ruolo nel definire quando sia opportuna una terapia di resincronizzazione cardiaca (CRT) in pazienti con scompenso87.
Stato dell’arte
La funzione ventricolare sinistra degli atleti è da tempo oggetto di ricerca da parte di cardiologi e medici dello sport. L’ecocardiografia standard fornisce informazioni scarse ed unicamente di tipo qualitativo sulla cinetica del VS, mentre le uniche metodiche fino a poco tempo fa disponibili per lo studio della deformazione del miocardio, risonanza magnetica e tissue Doppler imaging, hanno limitazioni evidenti nella pratica clinica: la prima ha costi troppo elevati, la seconda presenta la forte limitazione dell’angolo dipendenza che permette di valutare solamente lo strain longitudinale non apicale. La recente introduzione dello speckle tracking ecocardiografico (STE) ha reso più semplice ed accessibile la descrizione dettagliata e la determinazione quantitativa della deformazione del VS durante tutto il ciclo cardiaco. È ormai ampiamente dimostrato che rispetto ai classici parametri ecocardiografici (FE, massa e diametro ventricolare, spessore parietale ecc), quelli di deformazione permettono di distinguere, fra un serie di ventricoli funzionalmente nei limiti della norma, quelli con performance migliore. Numerose sono le pubblicazioni
35
in cui lo STE è la metodica di scelta per studiare la cinetica del VS in soggetti che praticano attività sportiva a livello agonistico. Galanti et al., concentrandosi sullo strain longitudinale del VS in atleti elité adulti, hanno dimostrato l’importanza della contrattilità della componente regionale medio-apicale nella determinazione della funzione ventricolare globale: in seguito ad un esercizio di forza pura (Hand Grip test) il gruppo di atleti presentava un incremento del picco di strain sistolico longitudinale apicale significativo, mentre nel gruppo di controllo, in seguito al test, lo strain si manteneva simile a quello misurato in condizioni di riposo88. Questi risultati hanno spinto il gruppo di Galanti ad approfondire le ricerche sulla deformazione del VS: sono stati valutati, in giovani atleti suddivisi in base allo sport praticato (calcio, basket, ciclismo), non solo lo strain longitudinale, ma anche quello circonferenziale, la torsione e la rotazione89. I parametri maggiormente implementati negli atleti, anche in questo caso, sono stati riscontrati a livello apicale. In special modo la rotazione dello strato subepicardico era incrementata nei ciclisti rispetto ai sedentari e ai giovani che praticavano altre attività. I classici studi caso-controllo, nei quali la deformazione ventricolare viene determinata un'unica volta, nei soggetti che praticano sport a livello agonistico e nei controlli sedentari, sono indicativi, ma non sufficienti a concludere che tramite l’allenamento qualsiasi soggetto sano sia in grado di migliorare la performance del proprio VS. Diversi autori hanno provato a determinare attraverso studi longitudinali quale fosse l’entità dei benefici di un allenamento incrementale di endurance sulla funzione del VS mediante STE. Weiner e coll. hanno certificato l’aumento della torsione ventricolare dopo un periodo di condizionamento di 90 giorni in soggetti che non avevano mai praticato precedentemente sport a livello agonistico90. Kurt e coll. dell’ Atatürk University (2013) hanno invece scelto un periodo di condizionamento più lungo (6 mesi), dopo il quale gli atleti mostravano un miglioramento sia del gradiente torsionale, valutato
36
in parasternale asse corto, che dello strain longitudinale a livello apicale, soprattutto nelle proiezioni 4 e 2-camere91.Alcuni articoli indicano lo STE come possibile futura metodica di ruotine per effettuare diagnosi differenziale tra l’ipertrofia fisiologica dei soggetti allenati e quella patologica92, 93. Il gruppo di Firenze per esempio ha coinvolto pazienti con ipertensione essenziale, atleti di endurance e controlli sani, e ne ha confrontato le misure di strain longitudinale, circonferenziale e la torsione del VS. I pazienti con ipertensione essenziale (ipertrofia patologica) presentano livelli ridotti di strain longitudinale, ma aumentati di strain circonferenziale e di torsione94. Nel 2009 Stefani e coll. hanno effettuato uno studio su atleti giovani (≈ 25 anni) con valvola aortica bicuspide (BAV), in presenza di stenosi lieve oppure di un piccolo jet da rigurgito. In questi pazienti, nonostante il picco di strain sistolico longitudinale risultasse entro i limiti della norma, la deformazione a livello dei segmenti basali era moderatamente ridotta rispetto agli atleti di controllo, cioè con normale valvola tricuspide95. Lo speckle tracking è stato ulteriormente sfruttato negli sportivi per valutare gli adattamenti esercizio-indotti del ventricolo destro96 e dell’atrio sinistro97,
98
, che fino a poco tempo fa, anche a causa della povertà di metodiche a disposizione, risultavano di minimo interesse.
Scarsi sono invece gli studi effettuati sugli atleti anziani. L’unico lavoro degno di nota è una pubblicazione di F. Knabel e coll. (2009), nella quale sono stati analizzati i parametri di strain longitudinale dei ventricoli sinistro e destro in atleti amatori giovani (22-59 anni) e anziani (60-72 anni) partecipanti alla maratona di Berlino. Gli studi sugli effetti acuti di un’attività fisica intensa di durata prolungata (es. maratona, iron man) sul miocardio erano e sono ancora oggi molto discordanti99. Alcuni evidenziano una riduzione della funzione ventricolare sinistra100, mentre per altri questa si mantiene costante101. Una delle ipotesi è che l’età possa influenzare l’entità