4. Fisiopatologia delle disfunzioni del tratto
gastrointestinale nella malattia di Parkinson
Mentre l’alterazione dopaminergica associata a danno
nigro-striatale potrebbe essere responsabile di alcuni aspetti della disfunzione gastrointestinale nei pazienti affetti da MP, risulta abbastanza evidente che ulteriori siti di coinvolgimento, come il SNC, svolgano un ruolo fondamentale. Il DMV, implicato nella trasmissione nervosa parasimpatica della maggior parte del tratto GI, è ampiamente coinvolto nella MP (Jellinger, 1987; Halliday et al., 1990). Infatti recenti studi di Braak e colleghi hanno dimostrato che il DMV è uno dei due siti in cui la patologia si sviluppa precocemente nel SNC (Del Tredici et al., 2002).
I corpi di Lewy sono stati identificati dapprima nel SNE nel 1984 (Qualman et al., 1884) e la loro presenza è stata successivamente confermata, da diversi ricercatori, in diversi siti di questo sistema (Kupsky et al., 1987; Wakabayashi et al., 1988). Recentemente è stato osservato che la presenza di α-syn (Braak et al., 2006) all’interno del SNE potrebbe rappresentare l’origine della patologia.
Tabella 1. Neurotrasmissione chimica nel Sistema Nervoso Enterico
Neuroni Neurotrasmettitori Recettori Effetti
IPAN Acetilcolina Nicotinico Iniziazione del riflesso peristaltico e secretomotore. Interneuroni mienterici ascendenti Acetilcolina Sostanza P Nicotinico NK1 Attivazione dei motoneuroni ascendenti Interneuroni mienterici discendenti Acetilcolina Serotonina ATP Nicotinico 5-HT4 P2X Attivazione dei motoneuroni mienterici discendenti. Motoneuroni mienterici ascendenti (eccitatori) Acetilcolina Sostanza P M3 muscarinico NK1 Contrazione delle cellule muscolari lisce prossimali. Motoneuroni mienterici discendenti (inibitori) VIP Ossido nitrico NPY ATP VIP1, VIP2 – Y2 P2Y Rilassamento delle cellule muscolari lisce distali. Neuroni ganglionici della sottomucosa Acetilcolina
VIP M3 (via NO)
Vasodilatazione e secrezione ghiandolare. Neuroni mienerici modulatori Serotonina 5-HT4 Attivazione presinaptica del rilascio di ACh. Neuroni mienerici modulatori Dopamina D2 Inibizione presinaptica del rilascio di ACh. Neurone intestinofugal Acetilcolina M1 Innesco di riflessi ganglionici sinaptici prevertebrali che inibiscono la motilità dell’intestino. Cellule enterocromaffine Serotonina 5-HT3 Attivazione degli IPAN Cellule interstiziali
di Cajal Ossido nitrico –
Regolazione dei neuroni del SNE sulla muscolatura liscia
ATP, adenosina trifosfato; ENS, sistema nervoso enterico; GABA, acido γ-amminobutirrico; 5-HT, 5-idrossitriptamina; IPANs, neuroni afferenti primari intrinseci; M3, recettore muscarinico M3; NK1, neurochinina-1; NPY, neuropeptide Y; VIP, polipeptide intestinale vasoattivo.
Su questa base, i neuroni dopaminergici del SNE potrebbero essere coinvolti (Singaram et al., 1995) come lo sono anche altri sistemi neuronali dell’intestino (Wakabayashi et al.,
1990).
4.1 Riduzione della peristalsi intestinale
La riduzione della peristalsi intestinale è probabilmente il sintomo più frequente nell’ambito delle alterazioni gastrointestinali. L’effettiva frequenza con cui si manifesta,
comunque, non è ancora ben chiara (Edwards et al., 1991; Siddiqui et al., 2002; Kaye et al., 2006; Stocchi et al., 2000). Recenti studi hanno indicato che la gravità della costipazione è correlata alla gravità della patologia (Edwards et al., 1991; Sakakibara et al., 2001) ma il rallentamento del transito a livello del colon può essere una condizione già presente in pazienti affetti da MP allo stato iniziale (Jost et al., 1998). Inoltre, altri studi hanno dimostrato che la costipazione può precedere lo sviluppo dei disturbi motori somatici nei pazienti affetti da MP (Ashraf et al., 1997), a volte anche di anni (Abbott et al., 2001; Abbott et al., 2007).
4.2 Rete neuronale e neurotrasmettitori del tratto gastrointestinale nella malattia di Parkinson
La sintomatologia gastrointestinale associata alla MP può essere associata ad un processo neurodegenerativo del SNE (Singaram et al., 1995; Wakabayashi et al., 1988), rispecchiando ciò che avviene nel SNC, sebbene le correlazioni biochimiche restino ancora poco chiare. Inoltre, l’entità della compromissione del sistema noradrenergico e
colinergico rimane ancora poco chiara.
Sono stati quindi utilizzati i modelli sperimentali che prevedono l’iniezione intraperitoneale di MPTP e l’iniezione
stereotassica di 6-OHDA per la valutazione delle modificazioni del SNE. L’iniezione intraperitoneale di MPTP descritta da Mori (1988) determina una riduzione dei neuroni immunoreattivi per la DA dopo 4 giorni dall’iniezione che
diventa più marcata dopo 25 giorni; per quanto riguarda invece i neuroni immunoreattivi per la TH, si riducono dopo 4 giorni dall’iniezione e 25 giorni dopo tornano ai valori normali.
Questo è dovuto al fatto che l’iniezione intraperitoneale di MPTP determina solo una neurotossicità transitoria che non rispecchia ciò che accade nella MP, e in particolare nel SNE, in quanto trattasi di una patologia progressiva, cronica e
neurodegenerativa. Questo ha portato allo studio di un diverso modello sperimentale caratterizzato da una perdita di neuroni dopaminergici nigro-striatali mediante l’iniezione stereotassica di 6-OHDA nel fascio mediale destro del prosencefalo. In recenti studi infatti, un’ analisi immunoistochimica condotta su preparati cerebrali, ha evidenziato lesioni nello striato in seguito a iniezione di questa neurotossina a causa dello stress ossidativo dovuto alla formazione di specie reattive dell’ossigeno (ROS). I ratti in esame sono stati sacrificati dopo
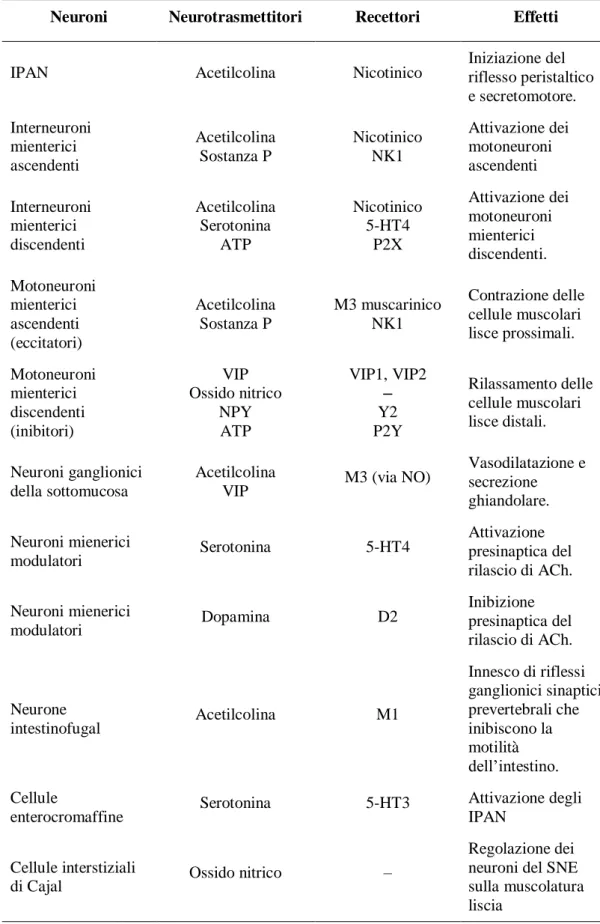
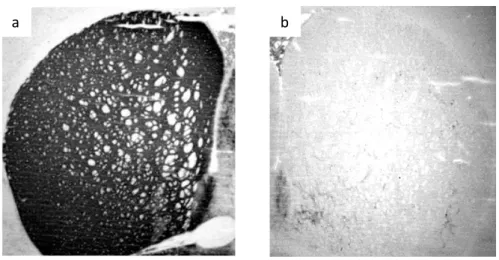
quattro e otto settimane dall’induzione della lesione (Figura 2) (Colucci et al., 2012). I ratti mostravano una completa perdita dei terminali dopaminergici (TH-positivi) e dei corpi cellulari nello striato, mentre nei ratti di controllo non sono stati individuati cambiamenti di immunoreattività per TH.
Figura 2. Analisi immunoistochimica della TH dello striato di ratto. a:
lato non lesionato; b: lato lesionato. Si osserva la marcata riduzione delle fibre dopaminergiche e dei corpi cellulari neuronali.
a b
a
Questi modelli sperimentali hanno permesso di approfondire lo studio sulle alterazioni neurochimiche del SNE nervoso enterico, tuttavia, in studi precedenti è stato visto che la DA sembra essere il miglior candidato per l’alterazione della funzionalità del tratto GI, in quanto è stata osservata una riduzione di questo mediatore nel colon ascendente (Tabella 2) (Singaram et al., 1995). Nel ratto è stato osservato che la DA modula la secrezione esocrina, l’assorbimento dei fluidi, la motilità, il flusso sanguigno e la citoprotezione, e sembra che la sua azione sia dovuta all’attivazione del sottotipo
recettoriale D1A largamente distribuito nel tratto
gastrointestinale (Vaughan et al., 2000). Nei pazienti affetti da costipazione cronica, Singaram e colleghi (1995) hanno riportato una riduzione dei neuroni dopaminergici mienterici e la presenza di corpi di Lewy soprattutto in quei neuroni contenenti VIP o TH.
Non è ancora chiaro perché la perdita dei neuroni dopaminergici dell’intestino determini l’inibizione della
contrattilità muscolare e la costipazione. Un recente studio, condotto su topi transgenici per assenza di recettori DA, ha suggerito che, oltre agli effetti mediati dai recettori D1A, la
Questo effetto inibisce il rilascio di ACh dai neuroni enterici, determinando una riduzione della forza di neurotrasmissione delle vie procinetiche (Li, et al., 2006; Walker et al., 2000). Questo meccanismo è in contrasto con il ruolo fisiologico della NA, che deriva principalmente dalla innervazione estrinseca. In realtà, la NA delle vie simpatiche del tratto GI inibisce la motilità e la contrazione degli sfinteri. Si potrebbe ipotizzare quindi, che la perdita dei neuroni dopaminergici del plesso mienterico nei pazienti affetti da MP sia compensata dall’attività dei nervi simpatici noradrenergici postganglionici, contribuendo così all’inibizione dell’attività contrattile dell’intestino con conseguente alterazione della motilità.
Tabella 2. Alterazioni neuronali ed enteriche nella malattia di Parkinson
SNC Tratto GI
Perdita di TH striatale, DA e metaboliti Riduzione dei livelli di DA Perdita dei neuroni DA nella substantia
nigra pars compacta
Perdita dei neuroni TH positivi Perdita delle fibre NA in varie regioni
Perdita dei neuroni NA nel nucleo pontino LC
Perdita delle fibre catecolaminiche Aumento delle cellule microgliali
all’interno dei nuclei cerebrali affetti
Perdita di NA Inclusioni neuronali all’interno di corpi
cellulari contenenti alfa-sinucleina
Inclusioni neuronali simili ai corpi di Lewy dall’estremità superiore dell’esofago al retto Sintomi motori: tremori a riposo, rigidità,
bradicinesia, instabilità posturale, postura flessa, sensazione di freddo, ridotta rotazione delle braccia, passo strascicato, festinazione
Ipersalivazione, disfagia, gastroparesi, dispepsia, bruciore di stomaco, costipazione
Sintomi non motori: alterazioni cognitive, apatia, depressione, anedonia, senso di fatica, alterazioni del sonno
I sintomi motori compaiono a distanza di 10 anni dall’insorgenza della disfunzione GI
Insorgenza di sintomi digestivi e alterazione del GI 10 anni prima dell’insorgenza dei
Un’altra ipotesi potrebbe consistere nel fatto che il deficit di
DA permetta un legame della NA ai recettori dopaminergici sovraespressi, determinando così effetti sulla motilità simili a quelli indotti dalla DA (effetti procinetici) (Tabella 2). La scarsa conoscenza sul ruolo dei recettori D2 e D1, non ha
permesso di stabilire quale delle due attività recettoriali prevale in presenza di differenti concentrazioni di dopamina (nello stato di salute e in quello di malattia) e non è ancora chiaro cosa accade all’espressione dei sottotipi recettoriali in conseguenza della degenerazione dei neuroni dopaminergici.