Introduzione ai metodi cromatografici per l’analisi degli oli essenziali e degli
estratti con solvente
Il timo comune (Thymus vulgaris L.) è una pianta1originaria del bacino del Mediterraneo ed è usata da molto tempo come fonte di olio essenziale e di estratti da diverse parti della pianta (Leung e Foster, 1996; Stahl-‐Biskup e Saez, 2002). Il timo comune, come altre specie di timo, esiste in diversi chemotipi, e la composizione dell’olio da diverse fonti e in diversi periodi dell’anno è stata investigata in diversi lavori (Nickavar et al, 2005; Goodner et al, 2006; Jordan et al, 2006). Nell’olio di timo comune sono stati individuati oltre 60 composti, e tra questi timolo e carvcacrolo sono, in media, i più abbondanti (Nijssen et al., 1999). Le caratteristiche aromatiche dell’olio essenziale di timo ne hanno reso comune l’impiego in campo alimentare e cosmetico (Soulier, 1995). Inoltre, la pianta ha trovato applicazioni in medicina grazie alle proprietà farmacologiche che la caratterizzano. Infatti, l’olio essenziale è stato riportato possedere attività antimicrobica (sia antibatterica che antifungina), carminativa, espettorante, spasmolitica ed antiossidante (Reddy et al., 1998; Sokmen et al., 2004), e molte di queste sono mediate dalla componente fenolica contenuta nell’olio, rappresentata principalmente da timolo e carvacrolo. Proprietà spasmolitica e antiossidante sono state riportate anche per l’estratto etanolico e il decotto acquoso (Schwarz et al., 1996; Meister et al., 1999) e sembrano essere associate a componenti non fenolici.
Il controllo di qualità e lo screening dell’olio di timo vengono effettuati generalmente tramite gas cromatografia – spettrometria di massa (European Pharmacopoeia, 2002; Hudaib et al., 2002; Goodner et al, 2006), mentre non è consueto l’uso di tecniche veloci come la cromatografia su strato sottile (Pothier et al., 2001; Balladin e Headley, 1999).
Anche il finocchio (Foeniculum vulgare Mill.) è una pianta aromatica originaria dell’area mediterranea, molto diffusa in Italia, conosciuta fin dall’antichità ed utilizzata come erba aromatica per la preparazione di cibi e liquori e come ingrediente in cosmetica (Piccaglia e Marotti, 2001; Ferrazzi, 1986). E’ utilizzato nella medicina popolare ed in vari preparati per problemi digestivi, mestruali e respiratori.
La Farmacopea europea (3° ediz.) riporta due diverse droghe, ottenute dal finocchio amaro (F. vulgare Miller spp. vulgare var. vulgare) e dal finocchio dolce (F. vulgare Miller spp.
estragolo, insieme ad altri minori quali α-‐pinene, α-‐phellandrene, limonene e anisaldeide (Miraldi 1999, Marotti et al., 1994); questi composti vengono utilizzati come marcatori per la caratterizzazione della varietà e del chemiotipo.
Il controllo di qualità e lo screening fitochimico dell’olio essenziale di finocchio vengono di norma effettuati con metodiche GC-‐FID o GC-‐MS (Piccaglia e Marotti, 2001; Damjanovic et al., 2005; Minija e Thoppil, 2003; Krizman et al., 2006). Non sono stati trovati riferimenti ad analisi di controllo di qualità dell’olio di finocchio con tecniche di cromatografia su strato sottile.
L’OPLC (Overpressured Layer Chromatography) è una tecnica cromatografica su strato sottile che si è rivelata interessante per la separazione di composti e lo screening di miscele grazie ad alcuni vantaggi rispetto ad altre tecniche cromatografiche normalmente utilizzate, come i tempi di analisi molto brevi e la riproducibilità degli Rf (Tyihak et al., 1979), ed è già stata applicata alla separazione ed al riconoscimento di diverse classi di composti naturali (Galand et al., 2002 a; Galand et al., 2002 b; Nyiredy 2001), ma le applicazioni di questa tecnica allo screening di olii essenziali ed al riconoscimento dei loro componenti presentate in letteratura sono ancora poche (Pothier et al., 2001; Mincsovics 1980; Dugo et al., 1996).
In questo lavoro sono state effettuate alcune prove sullo strumento OPLC (Overpressured Laminar Chromatography) per la messa a punto di un metodo analitico di screening per gli olii essenziali di timo e finocchio. I composti presi in considerazione come marker di qualità sono timolo e carvacrolo per il timo, anetolo e fenchone per il finocchio. I risulati ottenuti sono stati confrontati con quelli relativi alle prove su TLC classica.
La composizione di alcuni estratti ottenuti mediante la tecnica ASE (“accelerated solvent extraction”) di due specie di anice, Illiciium verum L. (a. stellato) e Illiciium anisatum Louer (a. bastardo) é stata analizzata tramite cromatografia OPLC. L’analisi è stata condotta anche sull’olio essenziale di anice stellato. I risultati ottenuti sono stati poi paragonati a quelli ottenuti con la tecnica TLC per gli stessi campioni.
Tra gli analiti considerati, è stato fatto particolare riferimento ai composti anetolo e safrolo: il primo è un marcatore dell’anice stellato, mentre il secondo è un composto tossico, caratteristico dell’anice bastardo, che può essere utilizzato per la sofisticazione della droga.
L’indagine ha riguardato anche un altro composto caratteristico dell’olio essenziale, l’anisaldeide.
L’acerola è una delle fonti naturali più importanti di acido ascorbico (vitamina C) che si conosca (Philips, 2004; Leung e Foster, 1996; Gomez 1999), ma alcuni lavori sono già stati pubblicati anche sul contenuto di flavonoidi ed acidi idrossicinnamici, nel frutto o in derivati alimentari processati (succhi, estratti concentrati, etc.), poiché concorre al potere antiossidante totale di questi prodotti (Righetto et al., 2005; Vendramini e Trugo, 2000; Lima et al., 2005; Vendramini e Trugo, 2004). Il frutto acerbo contiene non solo una percentuale maggiore di vitamina C rispetto al frutto maturo, ma presenta una componente fenolica, relativa ad alcuni acidi idrossicinnamici (caffeico, clorogenico, ferulico e p-‐cumarico), che viene persa nel frutto a completa maturazione (Righetto et al., 2005).
In questi lavori, la determinazione quali-‐quantitativa dei composti fenolici negli estratti o nei derivati alimentari di acerola viene effettuata tramite HPLC a fase inversa (Hanamura et al., 2005; Righetto et al., 2005; Vendramini e Trugo, 2004).
L’OPLC (Overpressured Layer Chromatography) è una tecnica cromatografica su strato sottile che si è rivelata interessante per la separazione di composti e lo screening di miscele grazie ad alcuni vantaggi rispetto ad altre tecniche cromatografiche normalmente utilizzate, come i tempi di analisi molto brevi e la riproducibilità degli Rf (Tyihak et al., 1979), ed è già stata applicata alla separazione ed al riconoscimento di diverse classi di composti naturali (Galand et al., 2002 a; Galand et al., 2002 b; Nyiredy 2001), anche se in letteratura esistono poche applicazioni di questa tecnica alla separazione e al riconoscimento di flavonoidi e altri composti fenolici (Dugo et al., 1996; Galand et al., 1999; Csomos et al., 2002; Gillon et al., 2004) e nessuna riporta metodiche basate sull’utilizzo della fase inversa.
L’OPLC è stata utilizzata in questo lavoro su supporti sia a fase diretta che a fase inversa per la messa a punto di metodo per la determinazione qualitativa di alcuni flavonoidi ed acidi idrossicinnamici la cui presenza nel frutto di acerola è documentato in letteratura, e vengono discussi i risultati ottenuti con le condizioni ottimizzate in fase inversa. Anche il comportamento dell’acido ascorbico con entrambe le tecniche è stato verificato.
Bibliografia
Pothier J., Galand N. et al.: “Comparison of planar chromatographic methods (TLC, OPLC, AMD) applied to essential oil of wild thyme and seven chemotypes of thyme” Il farmaco 56 (2001), 505-‐511.
Wagner H., Bladt S. e Zgainski E.M.: “Plant drug analysis” ed. Springer-‐Verlag, 1984.
Tyihak E., Mincsovics E. et al.: “New planar liquid chromatography technique: over pressured thin layer chromatography” J. Chromatogr. 174 (1979), 75-‐81.
Nyiredy S., Meszaros S.Y. et al.: “The “disturbing zone” in overpressured layer chromatography (OPLC)” J. High Resolut. Chromatogr. 10 (1987), 352-‐356.
Galand N., Pothier J. et al.: “Plant drug analisys by planar chromatography”, Jour. Chromatogr. Sci. 40 (2002), 585-‐597.
Galand N. et al.: “OPLC and AMD, recent techniques of planar chromatography: their interest for separations and characterization of extractive and synthetic compounds.” Fitoterapia 73 (2002), 121-‐134.
Nyiredy S.: “The role of planar chromatography in medicinal plant research” J. AOAC Inter. 84 (2001), 1219-‐1231.
Dugo P., Mondello L. et al.: “OPLC analysis of heterocyclic oxygen compounds from citrus fruit essential oils” Jour. Plan. Chrom. 9 (1996), 120-‐125.
Mincsovics E., Tyihak E. et al.: “Thin-‐layer investigation of components of essential oil of Matricaria chamomilla L. by means of classical and pressurized chamber systems” Acta Horticulturae 96 (1980) ,
Meister A., Bernhardt G. et al.: “Antispasmodic activity of Thymus vulgaris extract on the isolated guinea-‐pig trachea: discrimination between drug and ethanol effects” Planta medica 65 (1999), 512-‐516.
Schwarz K., Ernst W. et al.: “Evaluation of antioxidative constituents from thyme” Jour. Sci. Food Agric. 70 (1996), 217-‐223.
Ferrazzi, P.: “Finocchio” Apic. Mod. 77 (1986), 169-‐173.
Marotti M., Piccaglia R. et al.: “Effects of variety and ontogenic stage on the essential oil composition and biological activity of fennel (Foeniculum vulgare Miller)” Jour. Essent. Oil Res. 6 (1994), 57-‐62.
Minija J. e Thoppil E.: “Studies on essential oil composition and microbicidal activities of two south indian spices of the Apiaceae” Inter. Jour. Aromatherapy 12 (2002) 213-‐215.
Krizman M., Baricevic D. et al.: “Fast quantitative determination of volatile constituents in fennel by headspace-‐gas chromatography” Anal. Chim. Acta 557 (2006) 267-‐271.
Damjanovic B., Lepojevic Z. et al.: “Extraction of fennel (Foeniculum vulgare Mill.) seeds with supercritical CO2: comparison with hydrodistillation” Food Chemistry 92 (2005), 143-‐ 149.
Piccaglia R. e Marotti M.: “Characterization of some italian types of wild fennel (Foeniculum vulgare Mill.) Jour. Agric. Food Chem. 49 (2001), 239-‐244.
Miraldi E.: “Comparison of the essential oil from ten Foeniculum vulgare Miller samples of fruits of different origin” Flavour and Fragrance Journal 14 (1999), 379-‐382.
Philips R.L.: "Barbados cherry", fact sheet FC-‐28, 2004, University of Florida. Available at
http://edis.ifas.ufl.edu
Leung A.Y., Foster S. et al.: ‘Acerola’ in "Encyclopedia of common natural ingredients used in food, drugs and cosmetics" 2nd ed., Wiley, NY(1996).
Gomez P, Reynes M. et al.: "La cerise des Antilles: une exceptionelle source de vitamine C naturelle" Fruits 54 (1999) 247-‐260.
Righetto A.M., Netto F.M. et al.: "Chemical composition and antioxidant activity of juices from mature and immature acerola (Malpighia emarginata DC.)" Food Sci. Tech. Int. 11 (2005) 315-‐321.
Vendramini A., Trugo L.: “Chemical composition of acerola fruit (Malpighia punicifolia L.) at three stages of maturity” Food Chemistry 71 (2000) 195-‐198.
Lima V., Mélo E. et al.: “Total phenolics and carotenoid contents in Acerola genotypes harvested at three ripening stages” Food Chemistry 90 (2005) 565-‐568.
Vendramini A., Trugo L.: “Phenolic compounds in acerola fruit (Malpighia punicifolia L.)” Jour. Braz. Chem. Soc. 15 (2004) 664-‐668.
Hanamura T., Hagiwara T. et al.: “Structural and functional characterization of polyphenols from acerola (Malpighia emarginata DC.) fruit” Biosci. Biotechnol. Biochem. 69 (2005) 280-‐
pressured thin layer chromatography” Jour. Chromatogr. 174 (1979) 75-‐81.
Nyiredy S., Meszaros S.Y. et al.: “The “disturbing zone” in overpressured layer chromatography (OPLC)” J. High Resolut. Chromatogr. 10 (1987) 352-‐356.
Galand N., Pothier J. et al.: “Plant drug analisys by planar chromatography”, Jour. Chrom. Sci. 2002 (40) 585-‐597.
Galand N. et al.: “OPLC and AMD, recent techniques of planar chromatography: their interest for separations and characterization of extractive and synthetic compounds.” Fitoterapia 73 (2002) 121-‐134.
Dugo P., Mondello L. et al.: “OPLC analysis of heterocyclic oxygen compounds from citrus fruit essential oils” Jour. Plan. Chrom. 1996 (9) 120-‐125.
Csomos E., Heberger K. et al.: “Principal component analysis of biogenic amines and poliphenols in hungarian wines” J. Agric. Food Chem. 2002 (80) 3768-‐3774.
Gillon A., Amoyal W. et al.: “Comparisons of saponins and flavonoids in various african species of Desmodium Adscendens from different countries: analysis and OPLC purification” atti 8th Conference of the Israel Analytical Chemistry Society, Tel Aviv, 2005.
N Galand, J Pothier et al.: “Separation of flavonoids, coumarins and anthocyanins in plant extracts by overpressured layer chromatography” Pharmazie 54 (1999) 468-‐471.
Nyiredy S.: “The role of planar chromatography in medicinal plant research” Jour. AOAC Inter. 84 (2001) 1219-‐1231.
OPLC 50 – Method Development Guide, september 2004, Bionisis.
Swaroop A., Prakash Gupta A. et al.: “Simultaneous determination of quercetin, rutin and coumaric acid in flowers of Rhododenron arboreum by HPTLC” Chromatographia 62 (2005) 649-‐652.
Scopo del lavoro
La produzione di strumentazioni analitiche a costo contenuto e di facile utilizzo possono costituire uno strumento efficace per il controllo di qualità, piuttosto che un indagine fitochimica approfondita uno studio di fingerprinting, e costituire un valido aiuto a tutte quelle realtà di produzione, distribuzione e controllo delle piante medicinali e aromatiche o loro estratti.
Lo scopo del lavoro effettuato è stato quello di verificare le potenzialità dello strumento OPLC nell’analisi di olii essenziali (timo, finocchio, anice) ed estratti di piante aromatiche (anice), confrontando l’efficienza separativa, la velocità delle procedure e la capacità con quanto ottenuto dalle analisi tramite TLC classica.
Sviluppo del metodo cromatografico OPLC per l’analisi degli oli essenziali
Composti standard di riferimento
Nella prima parte del lavoro è stato studiato il comportamento in fase diretta di alcuni standard di riferimento che si ritrovano in diversi olii essenziali, con particolare attenzione ai marcatori principali dei due olii in esame, vale a dire timolo e carvacrolo per l’olio essenziale di timo, anetolo e fenchone per l’olio essenziale di finocchio. Le indicazioni sul comportamento dell’anetolo sono state considerate anche per l’analisi dell’olio essenzale di anice stellato. Come punto di partenza, sono state seguite le specifiche indicate in due metodiche, una ricavata dalla recente letteratura e relativa all’analisi dell’olio di timo con l’OPLC (Pothier et al., 2001), l’altra ricavata da un testo che descrive l’analisi di principi attivi di origine vegetale e degli estratti di piante medicinali e aromatiche su TLC classica (Wagner, 1984).
Tab. 1: composti di riferimento utilizzati per le prove preliminari
Composti di riferimento utilizzati
1 α-‐pinene 2 Estragolo 3 α-‐terpineolo 4 Fenchone 5 Isobornil acetato 6 Carvacrolo 7 d-‐limonene 8 Timolo 9 o-‐cimene 10 Anetolo 11 Linalolo
12 Olio di timo
Per lo sviluppo del metodo cromatografico sono state effettuate prove su TLC ed OPLC in diverse condizioni sperimentali:
TLC:
• Fase stazionaria: gel di silice 60 F254, 5 x 10 cm.
• Fase mobile: miscele esano–etile acetato (E-‐AE) e toluene-‐etile acetato (T-‐AE) in diverse proporzioni. • Esano-‐etile acetato: 100-‐0; 99:1; 98:2; 95:5; 80-‐20. • Toluene etile-‐acetato: 100-‐0; 95:5; 93:7. OPLC:
• Fase stazionaria: gel di silice F254 11 µm (5 x 20 cm) e 5 µm (20 x 20 cm).
• Fase mobile: miscele esano–etile acetato (E-‐AE) e toluene-‐etile acetato (T-‐AE) in diverse proporzioni.
• Esano-‐etile acetato: 100-‐0; 99:1; 98:2; 95:5; 80-‐20. • Toluene etile-‐acetato: 100-‐0; 95:5; 93:7.
I parametri strumentali di volume di fase mobile (Vtot), flusso (fl), volume iniziale o “flash” (Vr) e pressione esterna applicata (Pext) sono stati diversi nelle diverse prove effettuate.
Dopo l’applicazione dei reattivi, le lastrine sono state scaldate in stufa (110 °C per 10’) per consentire lo sviluppo delle colorazioni.
Per le analisi effettuate con miscele T-‐AE 93:7, una fase di presaturazione delle lastrine in tanica è stata applicata prima della cromatografia (toluene-‐etile acetato 90:10, durata 30-‐40’).
Per gli analiti considerati, dalle analisi sono stati determinati i valori di fattore di ritenzione (Rf), limite di rilevabilità (“limit of detection”, LOD) e riproducibilità come indicato nella tabella 3.
un volume di eluizione di 6,00 ml (Vtot) ed un flusso pari a 0,3 ml/min. In queste condizioni si nota la comparsa di una linea trasversale che copre alcuni composti tra cui estragolo e anetolo, anche se è apprezzabile la risoluzione di timolo e carvacrolo nell’olio di timo, che conferma il dato pubblicato; l’olio di finocchio presenta una macchia lungo la linea trasversale in corrispondenza dell’anetolo, suo marker principale (dato non mostrato).
Alcuni composti, però, non sono presenti sul cromatogramma, e si pensa che siano rimasti nel punto di deposizione e che necessitino di fase mobile a polarità maggiore per potersi muovere.
E’ stata quindi effettuata una prova con miscela esano-‐etile acetato 80:20 e Vtot = 4,00 ml per avere un riferimento su una miscela a potere eluente maggiore, e si nota che alcuni analiti sono sensibili alla percentuale di etile acetato e presentano un valore di Rf maggiore rispetto alla prova precedente (3, 6, 11). Altri invece, come l’anetolo e l’isobornilacetato, non compaiono sulla cromatografia: visto il potere eluente maggiore, si pensa siano eluiti fuori dalla lastrina insieme al solvente in eccesso (il volume di una lastina 20x20 è ca. 3,2 ml) (figura 1). Inoltre, molti dei composti standard in esame tendono a diffondere e a creare macchie diffuse via via che corrono e raggiungono Rf maggiori.
Fig 1: cromatografia OPLC degli standard e degli olii considerati ottenuta con fase mobile esano-‐etile acetato
80:20 (Vtot = 4,00 ml, fl = 0,30 ml/min, Vr = 300 µl, Pext = 50 bar). I campioni deposti sono elencati in tabella 1. Reattivo: vanillina solforica
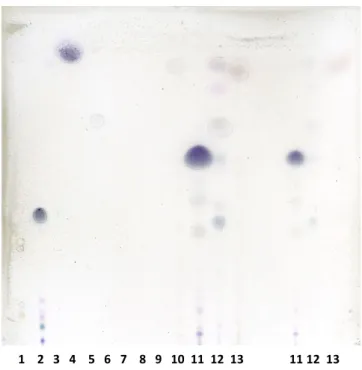
Sono state quindi effettuate una serie di prove con miscela esano-‐etile acetato a polarità via via crescente (da 100/0 a 90/10) limitando il volume di eluizione a 3,00 ml per contenere lo sviluppo all’interno di 1 CV (volume di colonna) e applicando un deposito maggiore di campione nel pozzetto. In particolare, uno sviluppo multiplo costituito da tre passaggi in sequenza (E 100% / E-‐AE 99:1 / E-‐AE 95-‐5) con Vtot = 3,00 ml ha prodotto una buona risoluzione per alcuni degli standard utilizzati (esclusi fenchone, d-‐limonene e o-‐cimene, che probabilmente non reagiscono con il reattivo), e tutti i composti hanno Rf compreso tra 0 e 0,4 (fig 2). Purtroppo, si crea ancora una linea trasversale, dovuta probabilmente a fenomeni di demixing della fase mobile o alla parziale solubilità in essa del gas adsorbito sulla fase stazionaria (con la creazione della cosiddetta “zona di disturbo”, Nyiredy et al., 1987), sulla quale compaiono le macchie in corrispondenza di 2, 5 e 10 (estragolo, isobornilacetato e anetolo), e che ne impedisce la separazione. Il manuale di sviluppo metodo consiglia di provare fasi mobili a potere eluente minore per far sì che i composti rimangano al di sotto della zona di disturbo e possano essere separati e riconosciuti anche se il fenomeno continua ad avvenire.
Fig 2: cromatografia OPLC degli standard e degli olii considerati ottenuta con miscele esano-‐etile acetato in
sequenza (E 100% / E-‐AE 99:1 / E-‐AE 95-‐5; Vtot = 3,00 ml ciascuna, fl = 0,30 ml/min, Vr = 300 µl, Pext = 50 bar). I campioni deposti sono elencati in tabella 1. Reattivo: vanillina solforica.
L’utilizzo di uno sviluppo unico con miscela esano-‐etile acetato 98:2 e volume raddoppiato (6,00 ml) comporta risultati simili: si crea un fronte, presso il bordo superiore, che trascina i composti estragolo e anetolo, mentre non si ha separazione tra timolo e carvacrolo (pozzetti 6 e 8, Rf = 0,21 entrambi, fig. 3), diversamente da quanto visto con la miscela 95:5. L’utilizzo di miscele esano–etile acetato, quindi, non ci ha permesso di ottenere risultati soddisfacenti per una buona risoluzione dell’anetolo, e ha messo in evidenza la diversa sensibilità dei composti alla percentuale di etile acetato nella fase mobile ed al volume totale utlizzato, presupponendo l’applicazione di metodiche diverse per la risoluzione di composti gruppi di composti scelti tra tutti quelli in esame.
Anche la metodica riportata da Wagner et al. nel relativo testo (pag. 41) è stata applicata, utilizzando una miscela toluene-‐etile acetato (T-‐AE) 93:7 con volume di eluizione pari
Fig 3: cromatografia OPLC degli standard e degli olii considerati ottenuta con fase mobile esano-‐etile acetato
98:2 (Vtot = 6,00 ml, fl = 0,30 ml/min, Vr = 300 µl, Pext = 50 bar). I campioni deposti sono elencati in tabella 1. Reattivo: vanillina solforica
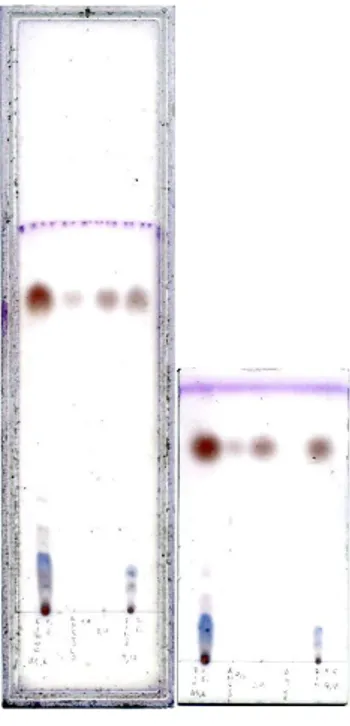
a 1 volume di colonna (CV, ca. 3 ml). In questo caso, si ottiene una buona risoluzione di entrambi gli olii e di molti composti standard, con il vantaggio che non si nota la comparsa di zone di disturbo e di linee trasversali lungo la cromatografia (fig. 4). Inoltre, si nota una buona risoluzione dell’anetolo nell’olio di finocchio (pozzetto 10, Rf = 0,78 ca.) e di timolo e carvacrolo (pozzetto 6 e 8, Rf = 0,50 e 0,55 ca.). I composti depositati in posizione vicina ai bordi laterali hanno Rf leggermente più alto, ed il profilo della lastrina sviluppata risulta leggermente ad ‘u’; l’effetto si può verificare anche con la TLC normale, e probabilmente risulta maggiore a causa del flusso forzato.
Proseguendo lo sviluppo del metodo su lastrine 5x20 cm a granulometria maggiore (11 µm) 1 2 3 4 5 6 7 8 9 10 11 12 13 11 12 13
Fig 4: cromatografia OPLC degli standard e degli olii considerati ottenuta con fase mobile toluene-‐etile acetato
93:7 (Vtot = 3,00 ml, fl = 0,30 ml/min, Vr = 300 µl, Pext = 50 bar). I campioni deposti sono elencati in tabella 1. Reattivo: vanillina solforica.
le condizioni con la miscela T-‐AE 93:7 e con T 100 %.
Olii essenziale di timo e finocchio
Con la fase T-‐AE 93:7 sono state analizzate soluzioni di olio di timo e finocchio a diversa concentrazione per verificare la rilevabilità dei loro componenti (figura 5).
La fase mobile T 100 % ha comportato una migliore separazione dei marcatori timolo e carvacrolo, nonostante una loro migrazione minore sulla lastrina (Rf = 0,24-‐0,29 per carvacrolo
1 3 2 3 4 5 1
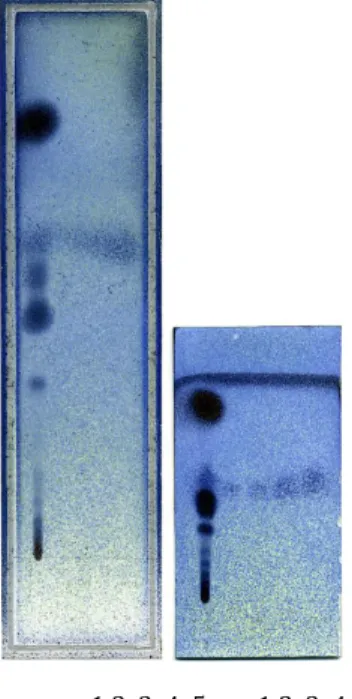
Fig. 5: cromatografia OPLC di soluzioni di olio essenziale di timo e finocchio a diversa concentrazione in CH2Cl2
ottenuta con fase mobile toluene-‐etile acetato 93:7 (Vtot = 800 µl, fl = 75 µl/min, Vr = 75 µl, Pext = 50 bar); Pozz 1: timo 100 mg/ml; pozz 2: timo 10 mg/ml; pozz 3-‐5: finocchio 10 -‐ 50 – 100 mg/ml. Reattivo: vanillina solforica.
e timolo, rispettivamente; figura 6) rispetto all’uso di toluene–etile acetato 93:7 (Rf = 0,48-‐0,51; fig. 6).
Per quanto riguarda l’olio di finocchio, con la fase mobile T 100 % si nota una migliore definizione della macchia relativa all’anetolo nonostante il Rf più alto (Rf = 0,80-‐0,67 in T 100 % e in T-‐AE 93:7 rispettivamente), ed i composti minori, che hanno Rf inferiore, vengono compressi entro Rf = 0,20. Alcuni di questi composti risultano ben separati con la fase 93:7, pertanto le due fasi mobili potrebbero essere complementari per riconoscere composti diversi. Da notare che con T-‐EA 93:7 si crea una leggera linea di disturbo trasversale ad Rf = 0,55 ca., mentre in T 100 % la cromatografia è omogenea e priva di linee trasversali (figura 7).
1 2 3 5 1 2 3 4
Fig 6: cromatografia OPLC di olio essenziale di timo (pozz 2, 10 mg/ml in CH2Cl2) a confronto con soluzioni di
standards (pozz 1: carvacrolo 0,65mg/ml; pozz 3-‐4: timolo 1,61 mg/ml -‐ 0,40 mg/ml; pozz 5: α-‐terpineolo 1,00 mg/ml; 5 µl in ogni pozzetto). Sviluppi ottenuti con toluene 100 % (a) e toluene–etile acetato 93:7 (b). Reattivo: vanillina solforica.
Per quanto riguarda l’olio essenziale di timo, una buona risoluzione dei diversi componenti è stata ottenuta utilizzando la fase mobile T-‐AE 100 % ed i seguenti parametri strumentali: Vtot = 600 µl, Vr = 75 µl, flusso = 0,1 ml/min (figura 8). Questo volume totale di fase mobile utilizzato corrisponde a 2/3 del volume di colonna (CV). In queste condizioni, l’olio essenziale mostra 4-‐5 composti principali, tra cui entrambi i marcatori principali ben visibili e separati (in OPLC, Rf = 0,24 e 0,29 per carvacrolo e timolo rispettivamente, entrambi rosa-‐fucsia dopo vanillina solforica) ed uno dei componenti minori, l’α-‐terpineolo (Rf = 0,045 in OPLC). Si può notare come la separazione di timolo e carvacrolo sia migliore con la tecnica OPLC nonostante tutti i composti abbiano comunque Rf inferiore a 0,3.
1 2 3 4 1 2 3 4
Fig 7: cromatografia OPLC di olio essenziale di finocchio (pozz. 1 e 4 in (a): 45,6 mg/ml -‐ 9,12 mg/ml in CH2Cl2;
pozz. 1 in (b): 50,0 mg/ml in CH2Cl2) a confronto con soluzioni di anetolo (pozz 2-‐3 in (a): 0,40-‐2,00 mg/ml; pozz
2-‐4 in (b): 1,450-‐0,725-‐0,40 mg/ml). 5 µl in ogni pozzetto. Sviluppi ottenuti con toluene 100 % (a) e toluene– etile acetato 93:7 (b). Reattivo: vanillina solforica.
Per determinare il limite di rilevabilità del timolo, é stata preparata una lastrina con olio di timo a confronto con soluzioni di timolo a concentrazione crescente (figura 9): esso risulta essere inferiore o uguale a 0,08 mg/ml (x 5 µl).
1 2 3 4 1 2 3 4
Fig 8: cromatografia OPLC (a) e TLC (b) di olio essenziale di timo (pozz 2, 10 mg/ml) e soluzioni di standards
(pozz 1: carvacrolo 0,65 mg/ml; pozz 3: timolo 0,40 mg/ml; pozz 4: α-‐terpineolo 1,00 mg/ml); 5 µl in ogni pozzetto. Rf (OPLC-‐TLC): timolo 0,29-‐0,29; carvacrolo 0,24-‐0,25.
In modo simile si è cercato di determinare il limite di rilevabilità (LOD) del carvacrolo (figura 10): anche la soluzione più diluita risulta visibile, di conseguenza il valore risulta essere inferiore a 0,165 mg/ml (x 5 µl).
1 2 3 4 5 1 2 3 4 5
Fig. 9: cromatografia OPLC (a) e TLC (b) di olio di timo (pozz 1) e soluzioni di timolo a diversa concentrazione
(pozz 2 – 5: 0,8 – 0,4 – 0,16 – 0,08 mg/ml); 5 µl in ogni pozzetto. Rf (OPLC-‐TLC): 0,28-‐0,33.
Sono state preparate soluzioni ulteriormente diluite sia per il timolo che per il carvacrolo, allo scopo di definire meglio il limite di rilevabilità, e lo sviluppo corrispondente viene mostrato in figura 11: per la tecnica OPLC, il LOD del timolo è pari a 0,022 mg/ml, mentre per il carvacrolo è pari a 0,116 mg/ml (x 5 µl).
Fig. 10: cromatografia OPLC (a) e TLC (b) di olio di timo (pozz 1) e soluzioni di carvacrolo a diversa
concentrazione (pozz 2 – 5: 1,31 – 0,65 – 0,33 – 0,165 mg/ml; 5 µl in ogni pozzetto). Rf (OPLC-‐TLC): 0,22-‐0,29.
1 2 3 4 5 6 1 2 3 4 5 6
Fig. 11: cromatografia OPLC (a) e TLC (b) di soluzioni di timolo e carvacrolo a diversa concentrazione (pozzetto 1
– 3: carvacrolo 0,116 – 0,058 – 0,023 mg/ml; pozzetto 4 – 6: timolo 0,022 – 0,055 – 0,11 mg/ml; 5 µl in ogni pozzetto). Rf (OPLC-‐TLC): timolo 0,26-‐0,32; carvacrolo 0,21-‐0,26.
Per quanto riguarda l’olio di finocchio, è stata ottenuta una buona separazione dei componenti utilizzando la stessa fase mobile dell’esempio precedente (T 100 %) e gli stessi parametri strumentali: Vtot = 600 µl, Vr = 75 µl, flusso = 0,1 ml/min. La figura 12 mostra lo sviluppo cromatografico in OPLC ed in TLC di olio di finocchio a due diverse diluizioni (45,6 – 9,12 mg/ml) e di due soluzioni di anetolo, suo marker principale: l’olio è visibile in tutti i suoi componenti nella soluzione più concentrata, ma per l’identificazione dell’anetolo possono essere utilizzate soluzioni più diluite.
Il limite di rilevabilità dell’anetolo è stato determinato con l’OPLC in un campione di olio essenziale di anice stellato, poiché anche in quel caso tale composto costituisce il marcatore
1 2 3 4 1 2 3 4
Fig 12: cromatografia OPLC (a) e TLC (b) di olio di finocchio (45,6 – 9,12 mg/ml, pozzetto 1 e 4) e soluzioni di
principale. L’anetolo appare di colore arancio e corrisponde al composto con l’Rf più alto tra quelli presenti nell’olio; inoltre, la soluzione 0,055 mg/ml risulta appena visibile e può quindi essere considerata il suo LOD con questa tecnica (figura 13 a). Con la TLC, il risultato è del tutto analogo (figura 13 b).
Il fenchone, come riporta il testo di riferimento, non è visibile con vanillina solforica, e quindi non dovrebbe corrispondere, col nostro metodo, a nessuna delle macchie visibili, bensì può essere evidenziato con fosfomolibdato-‐permanganato (PMA-‐PM) come macchia biancastra (nel finocchio amaro) o bluastra (nel finocchio dolce), oppure con acido solforico concentrato come macchia gialla, ma solo per quantità superiori a 0,1 mg. Con T 100 % ed i parametri strumentali da noi applicati, in OPLC il fenchone appare come macchia blu (reattivo fosfomolibdato-‐permanganato) con Rf pari a 0,22, nonostante l’olio essenziale presenti una serie di composti con Rf compreso tra 0 e 0,35 ca. che ne rendono difficile la rivelazione al suo interno (figura 14 a). In TLC, i risultati sono analoghi (figura 14 b). Tra le due soluzioni di fenchone utilizzate, la 1,23 mg/ml corrisponde al LOD ottenuto in queste condizioni sperimentali.
1 2 3 4 5
1 2 3 4 5
Fig. 13: cromatografia OPLC (a) e TLC (b) di olio di anice stellato (pozz 1) e soluzioni di anetolo a diversa
Per migliorare la risoluzione di questi composti, è stata effettuata una cromatografia analoga utilizzando la miscela eluente toluene – etile acetato 93:7 ed un volume di eluizione maggiore, pari a 750 µl, lasciando invariati i valori di flusso e di Vr. L’aumento del volume totale di eluizione e il potere eluente maggiore causano un innalzamento del fronte del solvente e del valore degli Rf dei composti presenti: il fenchone presenta un Rf = 0,58 e corrisponde ad una macchia ben separata nell’olio essenziale. Anche in questo caso, la soluzione 1,23 mg/ml risulta corrispondente al limite di rilevabilità del fenchone con la metodica applicata (figura 15).
1 2 3 4 5 1 2 3 4 5
Fig. 14: cromatografia OPLC (a) e TLC (b) di olio essenziale di finocchio (pozz 1) a confonto con due soluzioni di
anetolo (2,0 – 0,4 mg/ml, pozz 2 e 3) e due di fenchone (2,46 – 1,23 mg/ml, pozz 4 e 5); 5 µl in ogni pozzetto. Rf (OPLC-‐TLC): anetolo 0,79-‐0,81; fenchone 0,22-‐0,21.
La pressione esterna applicata alle lastrine durante l’analisi costituisce un parametro importante per la messa a punto di una metodica analitica valida, poiché influenza la stabilità della miscela eluente e la sua capacità di allontanare l’aria dalla fase stazionaria durante il suo flusso all’interno di questa. L’effetto della variazione di questo parametro è stato valutato nell’impiego di T 100 %. La figura 16 mostra l’analisi di olio di finocchio, anetolo e fenchone con T 100 % dopo applicazione di un Pext pari a 10 bar (invece che 50 bar, come mostrato in figura 14): non si notano particolari variazioni in termini di risoluzione dei composti e della loro mobilità (Rf), anche se i contorni delle macchie appaiono leggermente meno definiti.
1 2 3 4 5 1 2 3 4 5
Fig. 15: cromatografia OPLC (a) e TLC (b) di olio essenziale di finocchio (pozz 1) e soluzioni di fenchone a
concentrazione crescente (1,23 – 2,46 – 6,15 – 12,3 mg/ml, pozz 2 – 5) con miscela eluente T-‐AE 93:7 e Vtot = 750 µl. 5 µl in ogni pozzetto. Presaturazione: 40’ in T-‐AE 90:10. Rf (OPLC-‐TLC): anetolo 0,80-‐0,84; fenchone 0,58-‐0,49.
Nel caso venga utilizzata una miscela costituita da due o più componenti, devono essere considerate alcune fasi di pretrattamento delle lastrine cromatografiche tra cui la cosiddetta “presaturazione”, vale a dire la saturazione passiva dei siti di adsorbimento della lastrina con i vapori di solvente, per un periodo compreso tra 10’ e 1 h, in una camera chiusa (il solvente è generalmente costituito dagli stessi componenti della miscela eluente ma con percentuale maggiore del componente più polare). La mancanza della fase di presaturazione causa spesso la separazione dei componenti della miscela eluente nella lastrina una volta che questa viene posta sotto pressione, provocando il cosiddetto fenomeno del “demixing”: i due (o più) componenti si distribuiscono in zone diverse della lastrina, separate tra loro dal fronte di demixing. In base alla loro ripartizione, gli analiti si distribuiscono nelle due zone o si schiacciano insieme al fronte di demixing, dando spesso risultati non riproducibili e soprattutto non completi o fuorvianti.
L’effetto della presaturazione è stato valutato sulla miscela T-‐AE 93:7 da noi impiegata, confrontando i risultati ottenuti in analisi svolte con o senza una fase di presaturazione in T-‐AE 90:10 (durata 30’ – 45’): la figura 17 mostra il risultato di un analisi di olio di finocchio, anetolo e fenchone con T-‐AE 93:7 senza pretrattamento della lastrina, mentre in figura 15 veniva
1 2 3 4 5
Fig. 16: cromatografia OPLC di olio essenziale di finocchio (pozz 1) a confonto anetolo e fenchone, come in fig.
mostrato il risultato corrispondente dopo l’applicazione della presaturazione. Come si può notare, la fase di presaturazione sembra essere cruciale per le analisi svolte in queste condizioni, poiché la sua assenza provoca la comparsa del fronte di demixing a circa la metà della porzione sviluppata proprio nella zona in cui compariva il fenchone, schiacciando quest’ultimo sul fronte stesso.
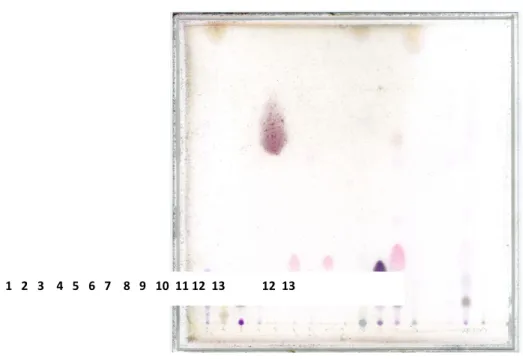
(La ricerca dell’anisaldeide è stata effettuata nell’olio essenziale di finocchio e anice stellato contemporaneamente, utilizzando miscela eluente T-‐AE 93:7 e rivelazione con acido solforico; il risultato viene mostrato qui di seguito, oltre che nella sezione riguardante l’analisi dell’olio di anice stellato).
La ricerca dell’anisaldeide è stata effettuata anche con l’utilizzo di acido solforico come reagente spray per la sua identificazione, applicata ad un campione di olio essenziale di anice ed uno di finocchio, con la fase mobile T-‐AE 93:7; i parametri strumentali sono i soliti fatta
1 2 3 4 5
Fig. 17: cromatografia OPLC di olio di finocchio e soluzioni di fenchone a concentrazione crescente, come in fig.
la lastrina raffredda vira al rosa.
In TLC, la soluzioni standard sono tutte chiaramente visibili, così come la presenza del composto nell’olio essenziale di anice stellato, mentre nell’olio di finocchio il composto non può essere rilevato con certezza perché coperto da una macchia di colore azzurro.
In OPLC i colori delle macchie sono più sbiaditi, e non può essere confermato quanto appena detto per l’olio di anice. Gli Rf non sono stati determinati perché il fronte del solvente non è visibile a fine cromatografia (fuori dal bordo superiore; ricordo che 900 µl sono equivalenti, all’incirca, ad un volume di colonna o CV).
La prova analoga col reattivo PMA-‐PM è visibile in figura 19; anche in questo caso, in OPLC non é visibile il fronte del solvente, e viene riportato il valore di Rf solo per la TLC.
1 2 3 4 5 1 2 3 4 5
Fig. 18: cromatografia OPLC (a) e TLC (b) di olio essenziale di anice stellato (pozz 5: campione A) e di finocchio
(pozz 1: 45,6 mg/ml) e soluzioni di anisaldeide a diversa concentrazione (pozz 2 – 4: 0,40 – 0,80 – 1,60 mg/ml); 5 µl in ogni pozzetto. Rf (TLC): anisaldeide 0,44.
Conclusioni
Le diverse prove effettuate con l’OPLC su composti standard comunemente individuati in diversi olii essenziali hanno dimostrato come l’utilizzo della fase mobile mono-‐componente (toluene 100 %) consenta di evitare la comparsa di “demixing zone” e di altri fenomeni di disturbo che sono invece associati all’utilizzo di eluenti costituiti da due o più componenti, ad es. esano-‐etile acetato e, in maniera minore, toluene-‐etile acetato.
La fase mobile T 100 % si è rivelata efficace per ottenere una buona separazione dei composti principali dell’olio essenziale di timo (timolo e carvacrolo) e di finocchio (anetolo) tramite OPLC su lastrine a fase diretta; sono stati provati diversi reattivi per la rivelazione dei composti in esame ed è stato determinato il limite di rilevabilità per i marcatori più significativi; inoltre, è stata determinata la ripetibilità della metodica considerando gli Rf come parametro di
1 2 3 4 5 1 2 3 4 5
Fig. 19: cromatografia OPLC (a) e TLC (b) di olio essenziale di anice stellato (pozz 5: campione A) e di finocchio
(pozz 1, 45,6 mg/ml) e soluzioni di anisaldeide a diversa concentrazione (pozz 2 – 4: 0,80 – 0,20); 5 µl in ogni pozzetto. Rf (TLC): anisaldeide 0,43.
(presaturazione).
Per quanto riguarda l’olio essenziale di timo, la metodica ha fornito una migliore separazione di timolo e carvacrolo rispetto alla TLC, con limiti di rilevabilità dei composti principali del tutto paragonabili.
Per quanto riguarda l’olio di finocchio, l’utilizzo della fase mobile T 100 % comporta una definizione migliore per l’anetolo rispetto alla TLC classica. E’ stata valutata anche l’efficacia della fase mobile T-‐AE 93:7 per migliorare la separazione degli altri componenti ed il riconoscimento del fenchone. In questo caso, è stato valutato l’effetto della variazione della pressione esterna sul risultato dell’analisi; inoltre, è stata confermata l’importanza della fase di presaturazione delle lastrine nell’attenuare i fenomeni di demixing associati all’utilizzo di miscele a due o più componenti.
Nel complesso, con il lavoro svolto è stato possibile trovare le condizioni per ottenere, con la tecnica OPLC, una separazione migliore dei composti considerati rispetto alla TLC classica; questo, insieme alla ripetibilità della metodica, nonché al risparmio di tempo e di solventi, può costituire un fattore di interesse all’applicazione dell’OPLC al controllo di qualità ed allo screening degli olii essenziali di timo e di finocchio.
Olio essenziale ed estratti di anice
Dopo una prima fase in cui è stato saggiato il comportamento dell’anetolo in fase diretta con miscele eluenti a base di cloroformio-‐metanolo (si veda la parte di sviluppo del metodo per quanto riguarda timo e finocchio), la messa a punto del metodo è proseguita esaminando l’efficacia di miscele toluene-‐etile acetato 93:7 come suggerito dal testo di riferimento (Wagner, 1984). Queste indicazioni sono state prese come punto di partenza sia per l’analisi degli olii essenziali che per l’analisi degli estratti ASE. In un secondo momento il metodo è stato trasferito e messo a punto anche sull’OPLC.
Parametri iniziali TLC
• Fase mobile: miscela toluene / etile acetato (T/AE) 93:7 • Fase stazionaria: gel di silice 60 F254.
• Rivelazione: vanillina solforica (oppure reattivo fosfomolibdico/permanganato)
L’estratto ASE di anice stellato in esano (figura 1, pozzetto 3) mostra una strisciata piuttosto complessa e intensa, di colore grigio-‐viola, compresa tra Rf = 0 e Rf = 0,65; inoltre, entrambi gli estratti (esano e CH2Cl2) presentano una macchia slargata, di colore grigio-‐rosso scuro, a Rf = 0,8 -‐ 0,92, che probabilmente copre la presenza dell’anetolo (Rf = 0,88 come standard). L’effetto è più marcato per l’estratto esanico in quanto più concentrato (a parità di diluizione iniziale, si veda tabella 1).
composti, sono state effettuate diverse prove abbassando la percentuale di etile acetato (95:5, 99:1, 100:0) ed è stato osservato un sensibile miglioramento: con toluene 100 %, gli standard anetolo e safrolo non risentono molto del cambiamento, mantengono un Rf alto (0,82 e 0,87 rispettivamente) e risultano ben distinti, mentre nell’estratto i componenti della strisciata centrale arretrano entro Rf = 0,4, e la macchia superiore risulta distinta chiaramente in due zone di colore diverso (figura 2).
La fase mobile (T 100 %) è stata utlizzata anche per l’analisi OPLC su lastrine 5 x 20 in silice (11 µm). Una buona separazione di anetolo e safrolo si ottiene contenendo la corsa cromatografica entro i 2/3 della lastrina, utilizzando un volume di 600 µl di eluente, fl. = 0,1 ml/min e Vr = 75 µl, limitando i fenomeni di diffusione associati alla lunghezza della corsa (figura 3); anche la maggiore velocità di migrazione associata alla tecnica a flusso forzato limita gli effetti di diffusione dei composti, e le macchie appaiono ben definite nonostante abbiano percorso una distanza maggiore rispetto alla TLC (Pothier et al., 2001). Nel caso della tecnica OPLC, il flusso di eluente risulta costante per tutta l’analisi, mentre nel caso della TLC la velocità del fronte diminuisce man mano che l’analisi procede; questo comporta una migliore
Fig. 2: cromatografia TLC di estratti ASE (esano e CH2Cl2) di anice stellato con eluente toluene 100 %. Pozz 1:
anetolo 1,45 mg/ml; pozz 2: safrolo 2,78 mg/ml; pozz 3: estr. ASE esano 0,2 g/ml; pozz 4: estr. ASE CH2Cl2 0,2