C
C
a
a
p
p
i
i
t
t
o
o
l
l
o
o
I
I
C
C
e
e
n
n
n
n
i
i
d
d
i
i
e
e
l
l
e
e
t
t
t
t
r
r
o
o
e
e
n
n
c
c
e
e
f
f
a
a
l
l
o
o
g
g
r
r
a
a
f
f
i
i
a
a
L’elettroencefalografia (EEG) è una tecnica per la registrazione non invasiva del segnale elettrico cerebrale. L’EEG rileva la differenza di potenziale elettrico tra un elettrodo posto nella zona dove si ha l’attività neuronale e un elettrodo di riferimento (collocato ad una certa distanza dal primo): quest’ultimo può essere posizionato o sullo scalpo, o in altri distretti corporei ritenuti elettricamente inerti, o comunque non dotati di attività elettrica propria.
I.1 Aspetti anatomici del sistema nervoso centrale
Il sistema nervoso è costituito da un complesso di organi e di tessuti specializzati, la cui funzione può essere definita attraverso la loro capacità di ricevere e riconoscere stimoli provenienti dall’ambiente esterno e dall’interno dell’organismo, e di elaborare risposte coordinate volontarie o involontarie.
Il sistema nervoso centrale (SNC) è composto da due classi di cellule:
le cellule della glia;
le cellule nervose (i neuroni).
Le cellule della glia hanno soprattutto funzioni strutturali, fungono cioè da supporto, separano tra loro gruppi di neuroni e guidano la crescita neuronale durante lo sviluppo.
Il neurone, invece, costituisce l’unità fondamentale del sistema nervoso centrale.
1.1.1 Il neurone
Il neurone è una cellula eccitabile in grado di ricevere, elaborare e trasmettere informazioni alle cellule adiacenti per mezzo di impulsi (potenziali d’azione o spike).
Strutturalmente il neurone presenta un corpo cellulare o soma, contenente il nucleo della cellula separato dal resto della cellula, da esso partono i dendriti e l’assone (figura 1).
I dendriti sono delle brevi ramificazioni che possono avere più ramificazioni successive con relativa diminuzione del diametro. Costituiscono il corpo recettore principale della cellula, in quanto su di essi terminano i prolungamenti di altre cellule nervose in regioni di contatto specializzate, dette sinapsi.
L’assone ha come scopo di trasmettere l’impulso nervoso. Gli impulsi si propagano al suo interno con una velocità che può arrivare fino a 100m/s. Le proprietà della conduzione sono legate esclusivamente alla membrana. L’assone è rivestito, in alcuni tratti, da una guaina detta mielina (cellula di Schwann). Gli spazi tra una cellula e l’altra sono detti Nodi di Ranvier.
Figura 1
Un modo di classificare i neuroni è sulla base del numero di estensioni che originano dal suo corpo cellulare.
I neuroni bipolari hanno un corpo cellulare di forma ovoidale da cui si dipartono due prolungamenti.
Le cellule pseudo unipolari hanno un unico prolungamento vicino al corpo cellulare che poi si divide in due tronchi che prendono direzioni opposte; l’impulso viaggia in direzioni diverse: uno stimolo si avvicina verso il corpo cellulare e l’altro si allontana.
I neuroni multipolari hanno un gran numero di dendriti e un assone; in questo caso la direzionalità è molteplice.
A livello della corteccia cerebrale i due tipi di cellule più importanti sono le cellule piramidali e non piramidali.
Cellule piramidali
Le cellule piramidali hanno corpi cellulari grandi di forma piramidale e possiedono lunghi dendriti. Sono neuroni eccitatori i cui assoni vanno a terminare in altre regioni cerebrali e nel midollo spinale. La loro caratteristica principale è la disposizione corticale: i loro dendriti apicali attraversano diversi strati corticali e sono sempre orientati perpendicolarmente alla superficie della corteccia. Questo tipo di organizzazione facilita l’integrazione dei vari segnali afferenti. I neuroni piramidali possiedono anche collaterali assoniche ricorrenti che si
proiettano, localmente, all’interno dell’area in cui si originano. Le connessioni stabilite dalle collaterali assoniche hanno un ruolo fondamentale nella genesi dell’attività elettrica degli aggregati neuronali. I campi generati dalle cellule piramidali sono campi “aperti” in cui la corrente extracellulare si estende oltre i limiti del tessuto attivo; questi campi, se sincroni, possono sommarsi ed essere registrati mediante elettrodi posti sullo scalpo (EEG).
Cellule non piramidali
Le cellule non piramidali sono piccole, di forma stellata e hanno assoni corti che si proiettano su neuroni locali. Sono disposte radialmente o con orientamenti casuali, quindi non preferenziali rispetto alla superficie della corteccia. In generale i loro assoni non lasciano la corteccia, ma terminano su neuroni vicini.
I campi da esse generati sono campi “chiusi” e non si sommano, quindi le correnti intra ed extracellulari non producono campi elettrici e magnetici.
I.2 Segnali bioelettrici
Per lo studio dell’attività elettrica cerebrale si utilizza come grandezza fisica di riferimento il potenziale elettrico. Tale grandezza è caratterizzata da una serie continua di valori assunti sia nel tempo (periodo di acquisizione) che nello spazio (superficie dalla quale viene prelevato).
I segnali elettrici sono prodotti, quasi esclusivamente, dai potenziali post-sinaptici (eccitatori o inibitori). I principali motivi sono:
1. l’ampiezza del campo elettrico prodotto dalla propagazione di un potenziale d’azione diminuisce molto più rapidamente dell’ampiezza dei campi prodotti dai potenziali post-sinaptici;
2. la durata dei potenziali d’azione è molto breve (dell’ordine di 1msec) e per produrre un’attività registrabile, in modo non invasivo, si dovrebbe avere un alto livello di sincronizzazione tra i diversi neuroni. Anche una minima asincronia, di pochi millisecondi, non rende possibile il sommarsi dei potenziali d’azione.
I flussi di correnti sinaptiche durano circa 10-40 msec , essendo più lenti, anche in assenza di perfetta sincronizzazione, questi potenziali si possono sommare più efficacemente dei potenziali d’azione e creare cosi differenze di campi elettrici abbastanza grandi da poter essere registrati dall’esterno. Quindi i potenziali registrati dall’EEG derivano da flussi di corrente extracellulare e di corrente intracellulare generati dai potenziali postsinaptici (PPS) di diverse cellule corticali, che grazie alla loro relativa lunga durata, riescono a sommarsi nel tempo a differenza dei potenziali d’azione.
1.2.1 Potenziale di membrana
I neuroni generano ed inviano messaggi tramite processi elettrochimici. Nel sistema nervoso gli ioni più importanti sono il sodio (Na), il potassio (K) entrambi con una carica positiva, il calcio (Ca) con due cariche positive e il cloro (Cl) con una carica negativa. Le cellule sono inoltre avvolte da una membrana che consente il passaggio di alcuni ioni e non di altri (membrana semipermeabile).
In condizioni di riposo la corrente ionica totale è nulla e le concentrazioni di Na+ e K+ sono:
Na+ intracellulare << Na+ extracellulare
K+ intracellulare >> K+ extracellulare
Anche se le diverse concentrazioni ioniche ai due lati della membrana tendono a bilanciarsi ciò non avviene in quanto i canali selettivi consentono il passaggio degli ioni potassio (K+) mentre ostacolano gli ioni cloro (Cl-) e sodio (Na+).
Questo gradiente di concentrazione è mantenuto anche grazie ad una grossa quantità di energia metabolica spesa dalla pompa sodio–potassio che scambia tre ioni sodio fuori dal neurone ogni due ioni potassio che vengono presi dentro. Quando tutte queste forze (di concentrazione, elettriche e attive) sono in equilibrio, si stabilisce una differenza di potenziale di riposo tra l’interno e l’esterno della cellula di circa 70 mV (con l’esterno positivo rispetto all’interno).
Tutti i segnali elettrici sono la conseguenza delle variazioni del potenziale d’azione di membrana a riposo, dovute a flussi di corrente attraverso la membrana.
1.2.2 Potenziale d’azione
Quando il potenziale di membrana passa dal valore a riposo ad uno superiore di -60 mV (potenziale di soglia) si genera un potenziale d’azione che, transitoriamente, annulla il potenziale di membrana e ne inverte la polarità. Il potenziale sale fino a valori positivi di circa 40 mV, quindi scende rapidamente verso valori più negativi del potenziale di riposo (-90 mV) ed infine si ristabilisce il valore di riposo (figura 2):
Figura 2
Il tratto con pendenza positiva corrisponde ad una depolarizzazione molto elevata, mentre il tratto successivo rappresenta una iperpolarizzazione della membrana nervosa.
La genesi del potenziale d’azione deriva dalla capacità della membrana di modificare la conduttanza agli ioni sodio e potassio.
Un sufficiente aumento del flusso di sodio verso l’interno della cellula provoca immediatamente una depolarizzazione (il potenziale tende verso il valore di riposo del sodio 58 mV); il processo è molto rapido a causa di un meccanismo autoattivante dell’apertura dei canali del sodio; tale processo è funzione del potenziale, per cui, aumentando il potenziale, la capacità di attivare altri canali diminuisce. In contemporanea l’aumento del flusso di potassio verso l’esterno provoca uno sbilanciamento del potenziale di membrana verso il potenziale del potassio a riposo (-96 mV), ma la crescita della conduttanza del potassio avviene lentamente (manca l’effetto autoattivante). Questi fenomeni portano il potenziale a 40 mV.
L’iperpolarizzazione è spiegata dalla capacità del potenziale di rendere inattivi i canali del sodio e dal fatto che i canali del potassio, pur lentamente, si attivano. A questo punto la conduttanza del sodio tende al suo valore di riposo, tuttavia la conduttanza del potassio, non avendo un effetto disattivante, tende a decrescere, dunque si verifica uno sbilanciamento verso il potenziale di riposo del potassio, con conseguente overshoot negativo (-90 mV).
Una proprietà importante del potenziale d’azione è il “tutto o nulla”, secondo il quale il fenomeno diventa rigenerativo soltanto se la depolarizzazione iniziale ha un valore sufficiente.
I.3 L’elettroencefalografo digitale
L’elettroencefalografo (figura 3) è l’insieme delle apparecchiature idonee per la registrazione di segnali bioelettrici neuronali. E’ composto da:
un sistema di filtraggio; un sistema di amplificazione;
una sezione di campionamento e conversione analogico digitale; una sezione d’interfaccia per permettere al computer di gestire
gli amplificatori;
Figura 3
1.3.1 Il sistema di filtraggio
Con questi dispositivi è possibile selezionare, dato lo spettro di frequenza di un segnale in ingresso, una o più bande prestabilite.
Tipi di filtri:
Filtro passa-basso ideale:
Lo spettro del segnale in uscita dal filtro
S
u(f)
, ha la stessa composizione spettrale dis(t)
fino ad una frequenza ft (frequenza di taglio) e valore nullo altrove.( )
f
S
( ) ( )
f
F
f
S
u=
i*
dove:
Si(f) è lo spettro in ingresso;
F(f) è la funzione di trasferimento del filtro.
Filtro passa-alto ideale:
E’ analogo al precedente ma taglia le basse frequenze.
Filtro passa-banda ideale:
Restituisce in uscita un segnale con uno spettro identico a
S(f)
tra f1 e f2 e 0 altrove.Figura 6
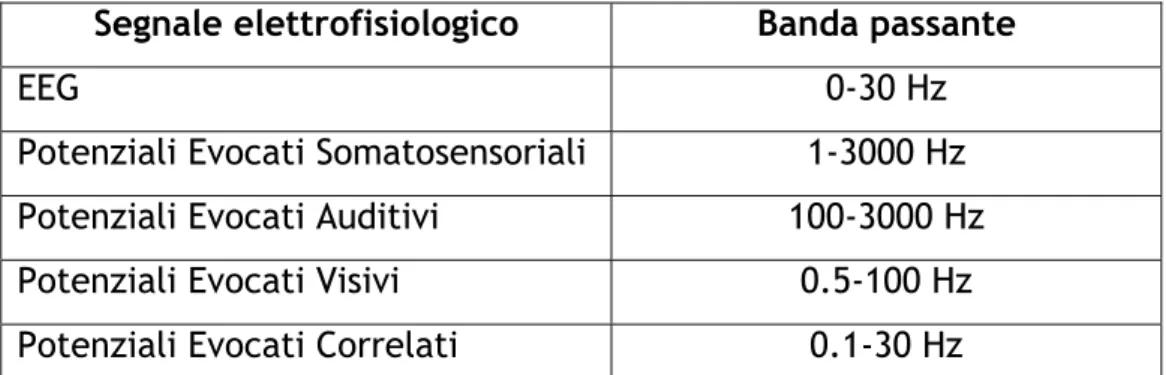
In tabella 1 sono riportate le bande passanti dei potenziali elettrofisiologici prelevati sullo scalpo:
Segnale elettrofisiologico Banda passante
EEG 0-30 Hz
Potenziali Evocati Somatosensoriali 1-3000 Hz Potenziali Evocati Auditivi 100-3000 Hz Potenziali Evocati Visivi 0.5-100 Hz Potenziali Evocati Correlati 0.1-30 Hz
1.3.2 Il sistema di amplificazione
Il sistema di amplificazione comprende:
i preamplificatori; gli amplificatori.
I preamplificatori prevedono una pre-amplificazione del segnale bioelettrico e adattano l’impedenza degli elettrodi a quella d’ingresso dell’amplificatore. Sono posizionati tra il paziente e l’elettroencefalografo all’interno di una scatola detta “testina del paziente” ; da un lato della scatola arrivano i cavi degli elettrodi applicati allo scalpo, mentre dall’altro, mediante un cavo multipolare schermato, inviano il segnale preamplificato agli amplificatori.
Il segnale bioelettrico prelevato dagli elettrodi ha un’ampiezza di alcune centinaia di microvolt; l’ampiezza del rumore elettrico dovuto ai disturbi esterni è di poco superiore a quello dei segnali EEG.
Gli amplificatori, quindi, hanno il compito di eliminare il contributo delle sorgenti di rumore sui segnali prelevati dagli elettrodi.
Il principio di funzionamento può essere schematizzato come:
dove:
•
A
è l’amplificazione imposta dall’apparecchio (guadagno); •s
i(t)
è il segnale d’ingresso prelevato da un elettrodo;•
s
r(t)
è la variazione del potenziale rispetto ad un punto situatoall’infinito (di riferimento);
•
s
u(t)
è il potenziale d’uscita dell’amplificatore;•
n(t)
è il rumore che va a sovrapporsi as
i(t)
ed as
r(t)
.Il segnale in uscita
s
u(t)
è completamente insensibile al rumore n(t).Ad ogni elettrodo corrisponde un amplificatore, rigidamente connesso all’elettrodo stesso e ad un riferimento comune.
L’elettrodo di riferimento può essere collegato ad un punto qualsiasi del paziente, tuttavia, quanto più è lontano dagli altri elettrodi dell’EEG, tanto maggiore sarà l’ampiezza dei potenziali non cefalici. La presenza di segnali di grande ampiezza può portare ad avere problemi di saturazione o non linearità degli amplificatori. Pertanto è conveniente sistemare l’elettrodo di riferimento il più vicino possibile agli elettrodi assicurandosi che abbia una bassa resistenza di contatto.
1.3.3 Convertitore A/D
I convertitori normalmente impiegati nelle registrazioni EEG sono a 12 bit, si hanno così 212 livelli di restituzione dei valori di ampiezza positivi e negativi codificati.
Il convertitore A/D funziona in un certo intervallo di valori di ampiezza compreso tra –5 e 5 Volt; possono esserci variazioni del livello in continua
del segnale EEG che possono portare a valori maggiori di quelli codificabili dal convertitore stesso, in questo caso il convertitore satura e si possono perdere delle informazioni.
Le registrazioni vengono effettuate con convertitori A/D con un numero di ingressi simultanei pari a 8 o 16. Le schede di conversione dispongono di n ingressi ma hanno un solo dispositivo di conversione numerica. Per regolare gli accessi si usa un semaforo interno:
Figura 8
Una volta effettuata la conversione il valore numerico è indirizzato ad un demultiplexer. Il ritardo con cui viene trattato il ch 16 rispetto al ch 1 è pari a 16 (tempo di trattamento per la conversione numerica dell’A/D). Se è abbastanza lungo può accadere che il ritardo superi l’intervallo temporale tra il prelievo di un campione e il successivo, causando così il disallineamento dei campioni (shift di campionamento). Per evitare ciò si utilizza un dispositivo sample & hold, posto all’ingresso dell’A/D: un valore tipico è 2 µsec.
t
∆
t
1.3.4 Pre- processing del segnale
Esistono tre tecniche di elaborazione per aumentare il contenuto d’informazione dei dati acquisiti:
Filtraggi digitali: il filtraggio digitale è vantaggioso in termini di
distorsione di fase, è infatti possibile implementare filtri a fase lineare che non alterano la polarità del segnale.
Averaging: il principio su cui si basa questa tecnica consiste nel
fatto che le componenti correlate allo stimolo si mantengono in fase tra loro durante i vari trials registrati, e si conservano nell’effettuare la media matematica dei trials; mentre le variazioni del potenziale non correlate allo stimolo (ad esempio il rumore) si elidono nella media. Questo processo si basa sulle ipotesi che:
l’interazione tra il rumore e il potenziale è lineare; il valor medio del rumore è nullo su tutti i trial registrati:
( )
0 1 =∑
= N t n N i iL’uscita del processo di averaging , ripetuto su N trials, è:
r
i( ) ( ) ( )
t
=
s
it
+
n
it
i=1,…,N
( )
( )
[
( )
( )
]
N t n t s N t r t r =∑
i i =∑
i i − iper la linearità della sommatoria si può scrivere:
( )
( )
( )
( )
( )
s( )
t N t n t s N t n N t s t r =∑
i i +∑
i i = +∑
i i =In particolare, aumentando il numero di trials da mediare, l’uguaglianza diventa sempre più significativa.
Reiezione e filtraggio degli artefatti: i segnali che producono
artefatti sono: il battito cardiaco, i movimenti dei lobi oculari e le contrazioni muscolari. Esistono due metodi per eliminare questi artefatti:
la reiezione: consiste nell’eliminare i trials che presentano artefatti evidenti, in questo caso è necessario aumentare i tempi di registrazione per avere un numero di segnali utili sufficiente all’analisi. E’ molto diffusa la reiezione mediante un criterio “di soglia” dove si estrae il trial che supera una certa soglia (figura 9):
Questo metodo può portare a degli errori nel caso in cui si voglia registare uno spike di ampiezza notevole (ad esempio spikes epilettici).
il filtraggio: acquisisce ugualmente il trial contaminato, cercando di rimuovere l’artefatto solo successivamente. Per fare ciò, le tecniche di filtraggio devono disporre di un modello matematico che descriva l’interazione tra segnale utile ed artefatti.
I.4 Conclusioni
La risoluzione temporale delle rilevazioni effettuate attraverso l’EEG è fra le migliori ottenibili con tecniche di registrazione dell’attività cerebrale (dell’ordine del millisecondo, pari a quella della registrazione intracorticale), la risoluzione spaziale rappresenta, invece, il limite maggiore. Infatti i segnali elettrici rilevati forniscono un’immagine in tempo reale dell’attività cerebrale in termini di tracciati dinamici dei segnali in vari punti del cranio. Tuttavia determinare la collocazione del tessuto neuronale attivo con questo tipo di dati è un problema che può dar luogo a un numero infinito di soluzioni (problema inverso). Per cercare di ridurre il numero di soluzioni si utilizzano dati provenienti da altre modalità di visualizzazione funzionale (ad esempio fMRI), specificandone il numero di fonti in esame e la loro approssimativa collocazione. I metodi basati su principi in grado di integrare queste modalità sono ancora in fase di sviluppo, e si basano su informazioni o supposizioni addizionali che riguardano il funzionamento del sistema nervoso.