Capitolo 1
Introduzione e scopo di questo lavoro di Tesi
1. 1 Le reazioni di Suzuki e le alchinilazioni
tipo-Sonogashira nel contesto delle reazioni di formazione
di legami C-C promosse da metalli di transizione
Nell’ambito della sintesi organica, la disponibilità di efficienti metodi generali chemio-, regio- e stereoselettivi per la formazione di legami C-C ha indubbiamente un’importanza strategica determinante nella costruzione di molecole complesse a partire da precursori semplici e facilmente disponibili. In questo contesto, le reazioni di cross-coupling catalizzate da metalli di transizione quali il Nichel e, soprattutto, il Palladio, hanno senz’altro un ruolo di primo piano: sviluppate nell’ultimo quarto del secolo scorso ma ancora oggi oggetto d’intensi studi, sono parte essenziale di quella “rivoluzione” delle possibilità della sintesi organica che è iniziata negli anni ’70-’80 e che è derivata per buona parte dallo sviluppo delle potenzialità dei metalli di transizione come catalizzatori.1
Per quanto tutti i tipi di reazioni di cross-coupling promosse da metalli di transizione siano oggi oggetto non solo di applicazione (anche industriale) ma anche di studi volti a renderli sempre più efficienti e convenienti, negli ultimi anni una particolare attenzione è stata dedicata, sia dalla ricerca accademica che da quella industriale, alle alchinilazioni tipo-Sonogashira2 ed alle reazioni di Suzuki3. L’attuale crescente interesse verso questi due tipi di cross-coupling è dimostrato dal continuo, significativo, incremento del numero di pubblicazioni di cui sono oggetto ogni anno ed è dovuto alle loro caratteristiche di generalità, efficienza, selettività, varietà e importanza strategica dei composti che permettono di ottenere, ma soprattutto alla loro intrinseca praticità, semplicità e aderenza a quei principi della “green chemistry” che stanno sempre più influenzando il mondo della ricerca e quello dell’industria4,1a.2,3 Buona parte delle loro doti di praticità e “greeness” dipendono dal fatto che non richiedono l’impiego di composti organometallici o impiegano organometalli non tossici, manipolabili semplicemente senza particolari precauzioni e facilmente smaltibili. Infatti le reazioni tipo-Sonogashira (Schema 1) consistono in
un cross-coupling diretto fra 1-alchini e vinil- o arilalogenuri, nella versione originale (reazione di Sonogashira-Hagihara), promosso da quantità almeno stechiometriche di un’ammina e co-catalizzato da complessi di Pd e CuI;5 nel capitolo 3 sarà meglio descritto come in luogo dell’ammina possano essere adoperate anche basi ossigenate6 oppure fluoruri7, così come simili alchinilazioni possano essere promosse solo da specie di Pd oppure di Cu.2,6,7
Schema 1: Schema generale delle reazioni di Sonogashira-Hagihara
D’altra parte, le reazioni di Suzuki (Schema 2) impiegano un tipo di composti organometallici fra i più sicuramente manipolabili e “environmentally friendly”. Infatti consistono in un cross-coupling fra specie organoboro (borani o boronati, ma recentemente sono usati soprattutto acidi o esteri boronici) ed alogenuri arilici o alchenilici (oppure solfonati), catalizzato da specie di Pd ed effettuato in presenza di basi di diversa natura1,3,8.
Schema 2: Schema generale delle reazioni di Suzuki-Miayura
Una più accurata descrizione delle caratteristiche, dei meccanismi e dell’evoluzione di questi due tipi di reazioni sarà riportata nei paragrafi 2.1 (Suzuki) e 3.1 (Sonogashira), ma per una miglior comprensione degli scopi di questo lavoro di
Tesi può essere opportuno ricordare subito che ambedue procedono seguendo un meccanismo che prevede i tre stadi essenziali tipici dei cicli catalitici di tutte le reazioni di cross-coupling C-C catalizzate da metalli di transizione, eccetto la reazione di Heck (Schema 3, per semplicità viene indicato solo per il Palladio, il metallo più usato a questo scopo, ma il decorso con altri metalli è analogo): i) una specie di Pd(0) da luogo ad un’addizione ossidativa con un’alogenuro o pseudo-alogenuro; ii) il complesso di Pd(II) così formatosi subisce un processo di transmetallazione con il composto organometallico presente (nel caso della Sonogashira, un’acetiluro formatosi “in situ” in quantità catalitica); iii) il nuovo complesso di P(II) così formatosi si sottopone ad una eliminazione riduttiva, che fornisce il prodotto di cross-coupling e rigenera una specie di Pd(0) in grado di iniziare un nuovo ciclo.2,3 Possono essere usate anche specie di Pd(II), che vengono ridotte “in situ” a Pd(0) a spese del composto organometallico presente. Questo meccanismo di reazione comporta che i) le reazioni procedono meglio su alogenuri alchenilici che arilici (i quali peraltro sono ancora meno reattivi se sostituiti con gruppi elettronricchi), ii) assai difficilmente alogenuri alchilici si sottopongono a tali reazioni e iii) in ogni caso gli ioduri (ed i solfonati) reagiscono meglio dei bromuri, mentre i cloruri sono ancora meno reattivi, tanto che l’impiego dei cloruri arilici in queste reazioni è estremamente difficoltoso.2,3
Schema 3: Schema generale semplificato delle reazioni di cross-coupling Pd catalizzate
Proprio con lo scopo di superare questi limiti è stata sviluppata una grande varietà di catalizzatori omogenei e, più recentemente, eterogenei utilizzabili nelle reazioni tipo-Sonogashira e di Suzuki, così come in altre reazioni di cross-coupling, spesso anche non commerciali ed a volte molto complessi.2,3d-m,9
1. 2 Catalizzatori omogenei e catalizzatori eterogenei
La nascita e lo sviluppo negli ultimi 30 anni delle reazioni di Sonogashira e di Suzuki (ma anche quelli delle altre reazioni di cross-coupling, quali la Stille, la Heck, la Negishi e la Kumada), si deve alla catalisi omogenea, che permise di ottenere per la prima volta, o in modo più efficiente di prima, molecole complesse di vario interesse.
Questa tipologia di catalisi di norma permette, soprattutto nei suoi sviluppi più moderni, la possibilità di avere alte velocità di reazione ed elevati turn over number (TON), oltre ad offrire spesso alte selettività e rese. Infatti i catalizzatori si presentano come sistemi che si disciolgono nella miscela di reazione avendo così tutti i siti catalitici accessibili per i reagenti presenti in soluzione. Comunque queste caratteristiche dipendono molto dal particolare sistema catalitico che, in generale, è costituito da complessi fra legandi mono-, di- o polidentati e metalli di transizione di varia natura, anche se nelle reazioni di formazione di legami C-C viene impiegato soprattutto il Pd. I legandi possono essere costituiti, ad esempio, da sistemi fosfinici, arsinici, amminici o carbenici; comunque sia, sono proprio i legandi che per le loro proprietà di -donazione e/o di ingombro sterico permettono ai catalizzatori di esibire alti TON e rese elevate, ottimizzando la stabilità del sistema cataliticamente attivo e permettendogli di operare anche in presenza di substrati difficili quali i cloruri arilici. Purtroppo l’uso dei legandi, spesso proprio di quelli più nuovi ed efficienti, può comportare problemi di stabilità del legando stesso negli ambienti di reazione (talvolta sono necessarie opportune precauzioni e condizioni di reazione idonee), di tossicità, di difficile reperibilità (spesso non sono commerciali) e di costo, tanto da rendere il loro uso su larga scala un carico economico pari se non superiore al metallo stesso e annullare i vantaggi di una elevata efficienza. Queste difficoltà, assieme alla tendenza degli ultimi anni di sviluppare processi più semplici e “green”, hanno portato allo sviluppo di catalizzatori omogenei “ligand-free”, che
rappresentano interessanti e pratiche alternative ai sistemi “ligand-assisted”. In ogni caso, però, la catalisi omogenea di norma comporta inconvenienti dovuti comunque alla presenza del metallo in soluzione ed alla perdita del metallo stesso, tanto più gravi quanto maggiore è il carico di catalizzatore impiegato (spesso, soprattutto nei sistemi più classici dall’ 1 al 5 %). Infatti, in primo luogo di solito è molto difficile separare completamente i metalli (talvolta anche i legandi) dai prodotti finali, con conseguenti significative contaminazioni dei prodotti stessi.10 Ciò rappresenta un problema molto serio per l’industria, soprattutto per quella farmaceutica, e può quindi inficiare la possibilità d’impiego industriale delle reazioni così catalizzate.11 In secondo luogo di norma i sistemi catalitici omogenei non possono essere recuperati e riciclati (o almeno non è possibile farlo in modo conveniente), con conseguenti costi d’acquisto e di smaltimento che industrialmente possono risultare inaccettabili.
Proprio per ovviare a tutti questi inconvenienti dei catalizzatori omogenei, nell’ultimo decennio ha preso avvio un’ampia serie di studi sull’impiego di catalizzatori supportati nelle reazioni di cross-coupling catalizzate da metalli di transizione, e in particolare nelle reazioni di Suzuki e, più recentemente, in quelle tipo-Sonogashira.
A questo scopo i metalli di transizione, in particolare il Pd, sono stati in qualche modo supportati su matrici inorganiche di varia natura,12 quali carbone attivato,13 sistemi zeolitici,14 ossidi metallici (silice, allumina ma anche TiO2, MgO ecc.)15 e
sali alcalini o alcalino terrosi (CaCO3, BaSO4 ecc.), nonché su polimeri organici ed
altri supporti solidi di vario tipo.12b,16 E’ da ricordare che la catalisi eterogenea, usata da molto tempo in sintesi organica per altri scopi, era stata saggiata in reazioni di cross-coupling già nei primi anni settanta,17 ma il suo impiego in queste reazioni è “esploso” solo negli ultimi anni.12-16,18 Infatti i catalizzatori supportati possono presentare numerosi vantaggi rispetto a quelli omogenei, risultando molto più attraenti sia dal punto di vista scientifico che da quello applicativo. Senz’altro sono di uso più pratico e versatile, essendo di solito sistemi molto stabili che spesso possono essere maneggiati ed utilizzati all’aria senza dover temere l’acqua e l’ossigeno.19 Purtroppo di norma richiedono condizioni leggermente più drastiche rispetto ai sistemi omogenei, ma ciò non crea grossi problemi se la più “bassa” attività catalitica può essere compensata innalzando le temperature di reazione e
giocando sul carico catalitico.20 Ma l’aspetto più attraente di questi catalizzatori è che possono permettere di ovviare a buona parte dei già citati inconvenienti mostrati dai sistemi omogenei. Infatti possono semplificare gli isolamenti, effettuabili mediante semplici estrazioni, e rendere possibile il recupero del catalizzatore tramite agevoli filtrazioni o centrifugazioni,21 fornendo direttamente prodotti contenenti quantità minime, spesso trascurabili, di metalli e il catalizzatore recuperato di nuovo impiegabile; in alcuni casi portano anche a migliori efficienze e/o minori costi.22 In conclusione, sotto molti aspetti i catalizzatori supportati sono ormai ritenuti più convenienti oltre che più “green” di corrispondenti sistemi omogenei.18
In questo contesto, stanno trovando applicazione nelle reazioni di Suzuki e, più recentemente, nelle alchinilazioni tipo Sonogashira, così come in altri tipi di reazioni di cross-coupling, sia catalizzatori considerati realmente eterogenei che precursori catalitici di tipo “boomerang”i, sia nanoclaster che metalli supportati, nonché sistemi catalitici solubili in H2O.18 Peraltro catalizzatori con queste
caratteristiche esaltano la praticità, l’economicità e le proprietà “green” tipiche delle reazioni di Suzuki e di Sonogashira, che sono state condotte efficientemente sotto catalisi eterogenea anche in solventi acquosi o addirittura in acqua, oppure di fatto in massa, così come in ambienti aerobici, con bassissime quantità di catalizzatore (talvolta 10-3 equivalenti di Pd, ma anche di meno), senza legandi per il Pd, utilizzando sia sistemi a base di Pd(II) che di Pd(0),ii e relativamente alla Sonogashira, in condizioni “copper-free”;2,3,9e come sarà meglio specificato nel paragrafo 3.1.
Per permettere una migliore comprensione delle motivazioni e degli scopi di questo lavoro di Tesi, nel paragrafo seguente (1.3) saranno brevemente discusse e commentate alcune questioni riguardanti le preparazioni e l’uso di catalizzatori eterogenei, mentre il paragrafo 1.4 sarà dedicato ad una classe di catalizzatori eterogenei ed omogenei particolarmente interessanti e promettenti: quelli ottenuti da
i
Vengono così chiamati quei sistemi metallici supportati che nell’ambiente di reazione, a caldo, rilasciano una certa quantità di metallo in forma solubile (che quindi agisce come un catalizzatore omogeneo) per poi, terminata la reazione e/o tornati ad temperatura ambiente, funziona da “scavenger” del metallo stesso.
ii
Oltre a sistemi convenzionali come Pd(0) su carbone o su allumina, sono attualmente commercializzati anche sistemi più complessi come il Pd(0)-EnCat TM 30 NP, commercializzato dalla Aldrich
solvatati di nanoparticolati metallici preparati “via” Metal Vapour Synthesis (MVS)23. Da quanto riportato in quest’ultimo paragrafo, risulteranno evidenti le peculiarità e le interessanti prospettive di catalizzatori di questo tipo, finora pochissimo saggiati in reazioni di cross-coupling e oggetto di questo lavoro di Tesi.23,24
1. 3 Metodi di preparazione, caratteristiche e problemati-
che dei catalizzatori eterogenei
Le tecniche utilizzate per preparare catalizzatori eterogenei sono molte e possono influenzare il delicato bilanciamento tra elevata attività, alta selettività, e tempo di vita del sistema catalitico ottenuto. Infatti la scelta del modo di fissaggio di un metallo ad un certo supporto, oltre a dipendere dalla natura del metallo e del supporto, può portare a risultati diversi per quanto riguarda le caratteristiche, e quindi proprietà, di un catalizzatore.15a Più in dettaglio, questi sistemi possono essere preparati a partire da sali del metallo di transizione oppure da nanoparticolati del metallo zero-valente.
Nel primo caso le tecniche utilizzate, fra le quali si trovano quelle più convenzionali, prevedono il fissaggio del sale metallico alla matrice mediante procedure di deposizione-riduzione e deposizione-precipitazione (principalmente con ossidi e carbone come supporti), oppure attraverso processi più complessi quali impregnamento, intrappolamento (Sol-gel process) e scambio ionico (con supporti silicici ed alluminici, tipo zeoliti). La riduzione del metallo può essere effettuata durante la precipitazione del catalizzatore, ma nella maggior parte dei casi il metallo viene lasciato tal quale, visto che la riduzione può avvenire “in situ” durante il cross-coupling.19 Comunque tutte queste tecniche possono comportare problemi di facile lisciviazione del metallo dal supporto stesso, lisciviazione che dipende anche dal tipo di legame d’immobilizzazione che si viene a formare tra il metallo e un dato supporto.25 Inoltre i sistemi così ottenuti in genere portano alla formazione di cristalliti metallici di dimensioni superiori ai 10 nm e ad una loro distribuzione sul supporto che rende disponibile solo una minima percentuale (10-60 %) del metallo presente, il che ha un grande impatto sull’attività del sistema catalitico.26
Per ovviare a questi problemi e disporre di specie catalitiche più efficienti e selettive, attualmente sia la ricerca che lo sviluppo di processi industriali si stanno
sempre più orientando verso l’impiego di nanoparticolati metallici solvatati o direttamente come catalizzatori oppure per la preparazione di catalizzatori metallici supportati; infatti, poiché il comportamento di un sistema metallico è strettamente correlato alle dimensioni delle sue singole particelle, i sistemi nanostrutturati possono presentare diverse e insolite proprietà elettroniche e catalitiche rispetto a quelle dello stesso metallo atomico, molecolare o allo stato massivo.27 Il loro impiego nella deposizione di particelle di metalli di transizione su supporti organici ed inorganici con le più svariate caratteristiche consente l’ottenimento di sistemi supportati contenenti particelle metalliche di dimensioni altamente omogenee ed estremamente piccole (< 10 nm), ampiamente distribuite e già in forma attiva cataliticamente, il che non avviene invece con la deposizione di sali metallici, che poi richiedono comunque una riduzione per dare il sistema attivo.28 Queste differenze nelle dimensioni e nella distribuzione delle particelle si traducono in un diverso comportamento catalitico; infatti di solito l’attività catalitica decresce con l’aumentare del diametro medio delle particelle,29 come recentemente è stato osservato anche in processi di idrogenazione30 e di idrosililazione,31 nonché in alchenilazioni di Heck32. Per quanto riguarda queste ultime è da rilevare che nanoparticolati di palladio supportati su polimeri quali polivinilpiridina32c,d o polidimetilfosfazene,32e contenenti particelle aventi un diametro di circa 2 nm, hanno mostrato un’attività catalitica più elevata di quella fornita da sistemi catalitici omogenei ed eterogenei disponibili in commercio, risultando peraltro completamente recuperabili senza perdite di Palladio.32
I nanoparticolati di metalli di transizione impiegati direttamente nella catalisi oppure come precursori di catalizzatori metallici supportati su solidi possono essere preparati mediante: a) opportuni metodi di riduzione chimica di sali metallici, b) procedure di vaporizzazione di metalli sotto vuoto, c) decomposizioni controllate di complessi organometallici, d) riduzioni elettrochimiche di sali dei metalli;33 i primi tre metodi risultano essere quelli più utilizzati e di maggiore interesse.
La riduzione chimica di sali di norma è effettuata in presenza di stabilizzanti quali sali di ammonio, tioli e polimeri funzionalizzati. Ciò permette di evitare l’aggregazione del metallo a “bulk metal” e costituisce un metodo particolarmente versatile per la preparazione di sospensioni colloidali di metalli di transizione; gli
PdCl2 H2PtCl6 Pd(OAc)2 Rh2(OAc)4
PtCl2 RuCl3
Soluzione di complessi metallici Complesso metallico/supporto supporto stabilizzante riducente o Ultrasuoni Catalizzatore nanosupportato Sospensione Colloidale (Catalizzatore Omogeneo) (a) (b) supporto
agenti riducenti più comunemente impiegati sono alcoli,34 idrogeno35 e idruri quali il sodioboroidruro [NaBH4] o i triorganoboro idruri di tetralchilammonio
[NR4(BR’3H)]36. I sistemi così ottenuti contengono particelle metalliche di
dimensioni molto piccole (3≤ dm ≤10 nm) e possono essere utilizzati nella catalisi
direttamente, sotto forma di sospensioni colloidali, oppure dopo deposizione su matrici solide (Schema 4a); però la loro attività catalitica è in genere fortemente condizionata dal tipo di stabilizzante utilizzato.37 I vantaggi di questo approccio consistono nella facilità di esecuzione e nel costo relativamente basso del processo. D’altra parte gli inconvenienti che comportano sono la difficoltà di ottenere una riduzione completa degli ioni metallici allo stato zero-valente e la sinterizzazione, che ha luogo durante il trattamento alle alte temperature. E’ inoltre da rilevare che l’impiego dell’idrogeno35 come riducente è limitato ai metalli nobili, più facilmente riducibili.
Le decomposizioni controllate di complessi organometallici sono effettuate termicamente o mediante ultrasuoni. Più in particolare, opportuni composti organometallici disciolti in un solvente o portati allo stato di vapore vengono adsorbiti su di un supporto; una volta adsorbiti, la termolisi controllata conduce alla perdita dei leganti ed alla crescita delle particelle metalliche (Schema 4b).33bSpesso queste procedure necessitano di temperature molto elevate, che danno luogo a processi di sinterizzazione. Per evitare questo problema sono impiegati solitamente composti organometallici che richiedono, per la loro decomposizione, temperature molto più basse.
Molto più vantaggiosa può risultare la vaporizzazione sotto vuoto di metalli in presenza di leganti organici debolmente stabilizzanti, nota come Metal Vapour Synthesis (MVS),23 che consente la preparazione di particelle metalliche “ligand free” e che quindi è molto interessante anche da un punto di vista “green”.28,38
1. 4 Preparazione di catalizzatori mediante Metal Vapour
Synthesis: pregi e lacune
La Metal Vapour Synthesis (MVS)23 è un’efficiente tecnica che permette l’ottenimento di nanoaggregati metallici; si basa sulla vaporizzazione del metallo sotto alto vuoto in presenza di leganti organici e risulta particolarmente efficace nella preparazione di sistemi catalitici altamente attivi e selettivi.28,38 Il vantaggio dell’impiego di vapori di metalli, generalmente costituiti da specie monoatomiche, rispetto a quello di metalli allo stato massivo è legato a fattori sia cinetici che termodinamici. Infatti gli atomi generati per vaporizzazione sotto vuoto non presentano barriere cinetiche alla coordinazione a leganti organici e sono molto più attivi dei comuni metalli che per reagire, anche se finemente suddivisi, devono superare l’energia di coesione del reticolo nel solido.23g
Il metodo consiste nella co-condensazione dei vapori di un metallo (generati per riscaldamento mediante effetto joule o per impatto elettronico) con quelli di uno o più solventi organici debolmente coordinanti (toluene, tetraidrofurano, n-pentano, ecc.). La co-condensazione avviene sulle pareti fredde (-196 °C) di idonei reattori (oggi commerciali) posti sotto alto vuoto (10-4-10-6 mbar). La temperatura del sistema viene poi portata intorno ai -40 °C, fino a quando la matrice solida formatasi sulle pareti fonde e si ottiene una soluzione stabile, almeno a quella temperatura, contenente nanoparticelle metalliche con stato d’ossidazione zero (solvatato metallico) e solubili nell’eccesso di legante organico. In genere fino a – 40 °C i solvatati sono costituiti da cluster contenenti non più di dieci atomi di metallo e le interazioni tra il solvente organico e il cluster metallico sono talmente deboli che quest’ultimo può essere considerato “ligand free”.39 Questi solvatati metallici possono essere utilizzati come precursori catalitici in fase omogenea o come materiali di partenza per la preparazione di catalizzatori eterogenei sia sotto forma di polveri ultrafini che di materiali supportati (Schema 5), fornendo comunque specie
con particelle di piccole dimensioni (3≤ dm ≤ 5 nm) e che non richiedono ulteriori
processi di attivazione prima dell’impiego.
Schema 5
M(V)+ Solvente (V)
M/Solvente 1)-196°C
2) -40°C
Supporto = Carbone, ossidi inorganici, polimeri... , 25°C
Mn polveri ultrafini
, 25°C supporto
[Solvated metal atoms] Catalisi Omogenea [A]
Mn'/Supporto
Catalisi Eterogenea [B]
Solvente = areni, nitrili, olefine, eteri...
M = Fe, Co, Rh, Pd, Pt, Ni, Cu, Ag, Au...
Più in dettaglio, il semplice riscaldamento delle soluzioni dalla temperatura di isolamento (-40/-50° C) a quella ambiente favorisce un’aggregazione controllata che permette di ottenere polveri ultrafini costituite da particelle metalliche di circa 3 ÷ 4 nm di diametro (Schema 5). Inoltre questa instabilità a temperatura ambiente dei solvatati metallici ottenuti “via” MVS può essere opportunamente utilizzata per ottenere più interessanti sistemi catalitici supportati. Infatti, se il riscaldamento fino a temperatura ambiente di tali solvatati viene effettuato in presenza di idonei supporti, si ottiene la deposizione degli aggregati metallici sulla superficie dei supporti stessi (Schema 5 e 6).40
Schema 6
Questa procedura consente di ottenere particelle metalliche supportate altamente omogenee sia nelle dimensioni, con valori del diametro medio compreso tra 1 e 3 nm, che nella distribuzione sulla matrice, a differenza di quello che si può ottenere con altri metodi di preparazione (Figura 1); questa differenza può rendere questi catalizzatori molto più attivi di quanto lo siano altri sistemi supportati nanoparticellari o meno.41
Figura 1: distribuzione e dimensioni delle particelle in un sistema di Pd supportato; a) ottenuto mediante procedure classiche di riduzione-deposizione; b) ottenuto mediante MVS.
E’ da rilevare che possono essere utilizzati supporti di varia natura (ad esempio, carbone, polimeri organici, ossidi solidi, membrane inorganiche micro- o mesoporose a base di allumina o silice, ecc)42; in funzione del supporto si possono ottenere sistemi con proprietà di stabilità e riciclabilità variabili. Infatti con alcuni tipi di supporti si osserva solo un semplice “foderamento” del supporto stesso da parte del metallo nanoparticellare, senza significative interazioni tra i due partners e quindi con una bassa forza di coesione metallo-supporto. I catalizzatori così costituiti, per lo più ottenuti usando sali metallici, tendono con più probabilità a subire fenomeni di lisciviazione. Invece altri tipi di supporti, caratterizzati dalla presenza di opportuni gruppi e/o strutture, permettono l’instaurarsi di forti o comunque migliori interazioni metallo-supporto. Di solito ciò può avvenire con polimeri organici o con zeoliti. Questi possono presentare porosità o addirittura microcavità, all’interno delle quali le nanoparticelle metalliche possono rimanere saldamente bloccate; purtroppo in questi casi si può avere, nel corso delle reazioni
catalizzate, una riduzione dell’attività a causa del possibile e progressivo intasamento delle cavità da parte di sali o altro, con conseguente difficoltà per i substrati ad entrare in contatto con il metallo.
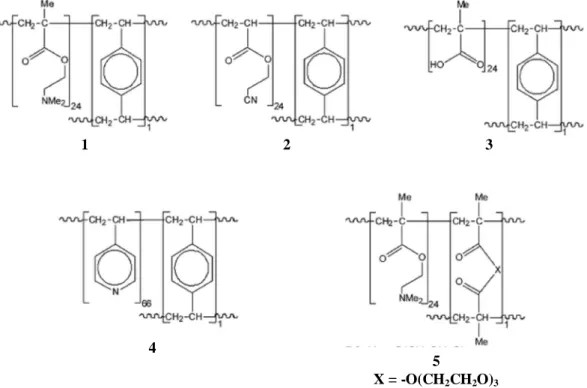
Quando i supporti possiedono gruppi funzionali capaci di dar luogo a significative interazioni con il metallo particellare, allora si possono ottenere sistemi particolarmente stabili alla lisciviazione. E’ questo il caso di polimeri funzionalizzati come quelli schematizzati in Figura 2.32d,43
Figura 2: polimeri contenenti i gruppi: ammino, ciano, carbossile o piridinico.
Uno dei più interessanti di questi supporti è il polimero organico commerciale comunemente chiamato polivinilpiridina (PVPy, 4),31c,d in realtà costituito da un copolimero 4-vinilpiridina (98 %) / 1,4-divinilbenzene (2 %). Già Antonietti nel 1997 aveva riportato che 4 poteva funzionare da “scavenger”iii di specie solubili di palladio (catalizzatori di Pd omogenei).32b Sulla base di questo dato è stata investigata la possibilità di impiegare tale polimero anche come supporto per nanocluster di Pd(0) ottenuti mediante MVS; in seguito analsi XPS sulla struttura del
iii
sistemi con queste proprietà sono stati sviluppati per permettere la decontaminazione di prodotti di vario interesse dai metalli (catalizzatori) contaminanti, residuo di reazioni effettuate con catalisi omogenea, mediante semplici filtrazioni, allo scopo di rendere tali reazioni più compatibili alle necessità dell’industria, soprattutto farmaceutica.
1 2 3
4
5
sistema supportato Pd/PVPy (6) ottenuto “via” MVS hanno permesso di osservare un’interazione tra l’atomo d’azoto basico del residuo piridinico del polimero e il metallo, il che fornisce al sistema un’alta stabilità.32d,44 Stabilità che è stata verificata in reazioni di idrogenazione e in alchenilazioni di Heck,32d,44 nelle quali ha fornito buoni risultati, sia per quanto riguarda le rese che il leaching e la riciclabilità. E’ stato altresì rilevato che questa interazione non appare modificata neanche dopo il coupling. Peraltro, in base ai dati ottenuti nella reazione di Heck, questo sistema risulta anche più attivo di altri catalizzatori omogenei ed eterogenei disponibili in commercio. D’altra parte simili risultati sono stati ottenuti, sempre in reazioni di Heck, anche supportando un nanoparticolato di Pd, sempre ottenuto “via” MVS, su polidimetilfosfazene (DPMP),32e,f un supporto non commerciale.
Ma questi sono gli unici esempi di impiego di catalizzatori preparati mediante MVS in reazioni di cross-coupling.
In conclusione, questo approccio alla preparazione di catalizzatori supportati, oltre a risultare più “green” di altri (minor consumo di reagenti e solventi), può comportare vantaggi quali una maggiore versatilità e minori limiti nella scelta dei supporti, dimensioni delle particelle minori e più omogenee, migliore distribuzione del metallo sul supporto e più facile accessibilità al metallo; comunque sia, a causa delle loro diverse caratteristiche, i catalizzatori così preparati possono rappresentare una valida alternativa o un utile complemento a quelli ottenuti per altra via.23,24 Nonostante ciò i lavori sull’applicazione di questi catalizzatori in reazioni di cross-coupling sono solo 4 e limitati ad alchenilazioni di Heck.32e-f,44
1. 5
Scopo e obiettivi di questo lavoro di Tesi
Quanto riportato nei paragrafi precedenti permette quindi di affermare che:
a) nell’ambito delle formazioni di legami C-C catalizzate da metalli di transizione, le reazioni di Suzuki e le alchinilazioni tipo-Sonogashira sono oggi da considerare particolarmente interessanti e importanti sotto vari punti di vista; b) la possibilità di impiegare in queste reazioni, così come in altri tipi di
cross-coupling catalizzati, sistemi catalitici eterogenei, a basso rilascio di metallo e possibilmente riciclabili è attualmente ritenuta di grande rilievo scientifico ed estremamente attraente, talvolta determinante, da un punto di vista industriale; c) fra la grande varietà di catalizzatori eterogenei sviluppati negli ultimi anni, quelli
ottenuti a partire da nanoparticolati metallici preparati “via” MVS, nonostante le loro peculiari e promettenti caratteristiche, sono stati finora pochissimo saggiati in reazioni di cross-coupling, e solo per quanto riguarda alchenilazioni tipo-Heck. D’altra parte, nel nostro gruppo di ricerca ha recentemente preso avvio una serie di studi sull’impiego di catalizzatori eterogenei in reazioni di formazione di legami C-C e C-eteroatomo.45 In questo contesto, e tenendo conto delle considerazioni sopra riportate, è stato quindi formulato un progetto di ricerca il cui fine ultimo è l’individuazione e la valorizzazione delle possibilità applicative di catalizzatori supportati ottenuti “via” MVS nell’ambito di reazioni di formazione di legami C-C di particolare interesse quali, soprattutto ma non solo, le alchinilazioni tipo-Sonogashira e le reazioni di Suzuki.
Lo scopo principale di questo progetto non è solo quello di verificare e dimostrare se opportune reazioni modello possano essere condotte convenientemente con catalizzatori di questo tipo, ma soprattutto quello di evidenziare se, come e dove l’impiego di tali catalizzatori possa risultare competitivo in termini di efficienza, generalità, praticità d’uso, “greeness”, riciclabilità e leaching del metallo, rispetto a quello di altri tipi di catalizzatori supportati commerciali o comunque noti e facilmente disponibili. In altre parole, l’obiettivo del progetto è quello di identificare i possibili ruoli, le eventuali peculiarità, gli scopi e i campi d’applicazione di questi catalizzatori nel contesto delle reazioni di cross-coupling, con particolare attenzione per quelle di Suzuki e di Sonogashira.
Come prima fase di questo progetto è stato deciso di prendere in esame alcuni nanoparticolati di Pd supportati, preparati “via” MVS e con caratteristiche già note, investigandone le possibilità applicative, i limiti ed i vantaggi come catalizzatori per le sopra citate reazioni di Suzuki e di Sonogashira.
Gli stadi successivi del progetto, anche in relazione ai risultati ottenuti e all’esperienza fatta, comprenderanno studi a più ampio raggio, sia per quanto riguarda i catalizzatori ed i confronti delle loro proprietà (compreso la progettazione di nuove specie) che le reazioni da testare e le tecniche con cui effettuare le reazioni (ad esempio, uso di microonde per promuoverle o di liquidi ionici come solventi). Più in dettaglio nella sua prima fase il progetto prevede di:
a) saggiare il comportamento, in alchinilazioni tipo-Sonogashira e reazioni di
Suzuki, di alcuni catalizzatori preparati da nanoparticolati metallici ottenuti mediante MVS, scelti tra quelli già noti e supportati su matrici facilmente reperibili;
b) individuare le condizioni più efficienti, pratiche e “green” (se possibile) in cui gli
stessi sono in grado di promuovere queste reazioni;
c) verificare le caratteristiche di leaching e riciclabilità dei catalizzatori nelle
condizioni individuate;
d) confrontare il comportamento dei catalizzatori studiati con quello, in analoghe
condizioni di reazione, di altri catalizzatori supportati commerciali o facilmente disponibili;
e) delineare infine scopi, limiti e utilità dell’impiego dei catalizzatori in oggetto
grazie alla realizzazione di un’ampia e significativa casistica.
Questo lavoro di Tesi rappresenta l’inizio dello svolgimento del progetto sopra delineato, ed in particolare l’avvio della sua prima fase. Il programma preventivato ha compreso:
i) la scelta di un primo nanoparticolato di Pd supportato, ovviamente preparato “via” MVS, da saggiare;
ii) uno studio accurato delle sue possibilità applicative nella reazione di Suzuki,
effettuato seguendo la traccia generale riportata nei precedenti punti b-e;
Per quanto riguarda queste ultime reazioni, è stato inoltre deciso, in accordo con gli intenti esposti nel già citato punto b, di cercare esclusivamente condizioni “copper-free” (per una descrizione delle motivazioni e degli scopi dell’eliminazione del CuI, co-catalizzatore tipico delle reazioni di Sonogashira vere e proprie, vedere i paragrafi 3.1.1 e 3.1.2).
Per quanto riguarda invece il primo catalizzatore da saggiare, la scelta è caduta sul sistema PdVp/PVPy (6), già descritto nel paragrafo 1.4. Infatti 6 fa uso di un supporto disponibile commercialmente a basso costo, le sue caratteristiche strutturali sono già state pienamente studiate e, assieme al sistema PdVp/DPMP (che però impiega una matrice non commerciale), è l’unico dei catalizzatori di questo tipo ad essere stato testato in reazioni di cross-coupling, anche se limitatamente alle alchenilazioni di Heck.