6 Classificazione delle acque ed interpretazione dei
dati chimici
6.1 Introduzione
Una classificazione è la suddivisione sistematica di molte "cose" in varie classi, gruppi, categorie aventi in comune determinate caratteristiche. Partendo da una loro generica suddivisione fondamentale, si procede gradualmente ricercandone le analogie e distribuendoli in gruppi il più possibile omogenei per particolari caratteristiche. La classificazione presiede alla formazione delle idee generali e costituisce la base indispensabile dell'attività scientifica e tecnologica.
Per le acque naturali, è necessario definire la qualità dei diversi tipi di acque reperibili in natura, cioè le loro caratteristiche fondamentali: queste infatti variano con il variare delle origini, delle condizioni idrogeologiche delle sorgenti, delle condizioni climatiche ed atmosferiche, delle stagioni dell’anno e di numerosi altri fattori. Di norma si usa fare una distinzione delle acque naturali in funzione della loro origine, trascurando tutti gli altri fattori che possono farne variare la qualità: la conoscenza delle variazioni specifiche di qualità di acque di una medesima classe, diventa pertanto l’obiettivo di approfondite indagini analitiche.
Se invece si vuole riconoscere gruppi di acque con precise affinità chimiche per studiare le possibili relazioni tra di essi e la genesi di ciascun gruppo è indispensabile procedere ad una classificazione che si basa sulle sostanze chimiche disciolte. (Massarani, 1987)
6.2 Qualità
analitica
Prima di eseguire la classificazione delle acque è opportuno verificare la qualità dei dati analitici ottenuti. Questa verifica deve essere fatta anche se nella fase analitica sono stati utilizzati tutti i mezzi atti ad eliminare ogni incertezza dovuta ad interferenze reciproche fra i vari composti presenti in soluzione. Uno dei metodi più utilizzati è quello che si basa sul principio dell’elettroneutralità delle soluzioni. Tuttavia, è opportuno ricordare che il bilanciamento tra gli anioni ed i cationi è una
condizione necessaria ma non sufficiente a provare l’attendibilità di un’analisi chimica. Infatti, quando un catione ed un anione prevalgono nettamente sopra agli altri, il bilanciamento ionico dipende essenzialmente dalla qualità delle determinazioni di queste due specie chimiche.
In teoria la somma degli anioni in meq/l dovrebbe coincidere esattamente alla somma dei cationi, pure espressi in meq/l. In pratica, per gli inevitabili errori propri delle procedure analitiche, questo non avviene. (La chimica delle acque, 1987).
La deviazione % dalla coincendenza è detta sbilanciamento. Esso generalmente viene definito nel modo seguente:
Sbilanciamento % = 100 * (( ∑anioni - ∑cationi) / ( ∑anioni + ∑cationi)) In prima approssimazione si considerano “accettabili” quelle analisi che presentano valori di sbilanciamento compresi entro ± 5%.
In questa tesi sono stati accettati valori di sbilanciamento ≤ ± 2,5%.
Nelle tabelle 6.1, 6.2 e 6.3, insieme ai dati espressi in meq/l, sono riportati i risultati dei bilanci ionici. Dall’analisi delle tabelle 6.1, 6.2 e 6.3 si osserva quanto segue:
1. Nella prima campagna sono stati prelevati 23 punti d’acqua, di cui 19 presentano uno sbilanciamento inferiore all’1,5%, solo 4 campioni hanno uno sbilanciamento tra il 1,5% e il 2,5%.
2. Dei 27 campioni prelevati durante la seconda campagna, 19 mostrano uno sbilanciamento inferiore al 1.5%, 6 campioni presentano uno sbilanciamento tra l’1,5 e il 2,5%, i restanti 2 campioni hanno uno sbilanciamento maggiore del 2.5%.
3. Durante la terza campagna sono stati prelevati 35 campioni, di cui 18 esibiscono uno sbilanciamento inferiore al 1.5% e 17 presentano uno sbilanciamento tra l’1,5 e il 2,5%.
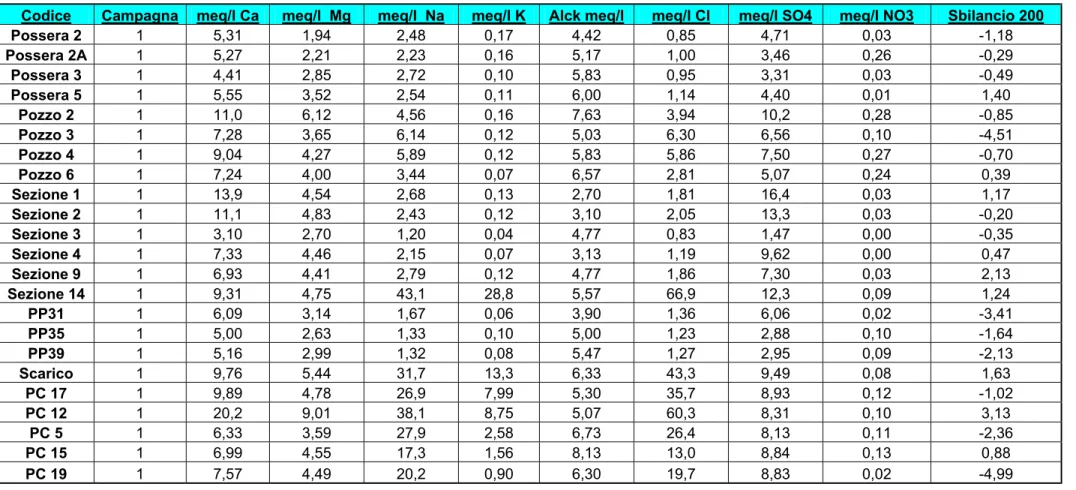
Tabella 6.1 - Valori in meq/l e relativo sbilanciamento dei campioni prelevati durante la prima campagna.
Codice Campagna meq/l Ca meq/l Mg meq/l Na meq/l K Alck meq/l meq/l Cl meq/l SO4 meq/l NO3 Sbilancio 200
Possera 2 1 5,31 1,94 2,48 0,17 4,42 0,85 4,71 0,03 -1,18 Possera 2A 1 5,27 2,21 2,23 0,16 5,17 1,00 3,46 0,26 -0,29 Possera 3 1 4,41 2,85 2,72 0,10 5,83 0,95 3,31 0,03 -0,49 Possera 5 1 5,55 3,52 2,54 0,11 6,00 1,14 4,40 0,01 1,40 Pozzo 2 1 11,0 6,12 4,56 0,16 7,63 3,94 10,2 0,28 -0,85 Pozzo 3 1 7,28 3,65 6,14 0,12 5,03 6,30 6,56 0,10 -4,51 Pozzo 4 1 9,04 4,27 5,89 0,12 5,83 5,86 7,50 0,27 -0,70 Pozzo 6 1 7,24 4,00 3,44 0,07 6,57 2,81 5,07 0,24 0,39 Sezione 1 1 13,9 4,54 2,68 0,13 2,70 1,81 16,4 0,03 1,17 Sezione 2 1 11,1 4,83 2,43 0,12 3,10 2,05 13,3 0,03 -0,20 Sezione 3 1 3,10 2,70 1,20 0,04 4,77 0,83 1,47 0,00 -0,35 Sezione 4 1 7,33 4,46 2,15 0,07 3,13 1,19 9,62 0,00 0,47 Sezione 9 1 6,93 4,41 2,79 0,12 4,77 1,86 7,30 0,03 2,13 Sezione 14 1 9,31 4,75 43,1 28,8 5,57 66,9 12,3 0,09 1,24 PP31 1 6,09 3,14 1,67 0,06 3,90 1,36 6,06 0,02 -3,41 PP35 1 5,00 2,63 1,33 0,10 5,00 1,23 2,88 0,10 -1,64 PP39 1 5,16 2,99 1,32 0,08 5,47 1,27 2,95 0,09 -2,13 Scarico 1 9,76 5,44 31,7 13,3 6,33 43,3 9,49 0,08 1,63 PC 17 1 9,89 4,78 26,9 7,99 5,30 35,7 8,93 0,12 -1,02 PC 12 1 20,2 9,01 38,1 8,75 5,07 60,3 8,31 0,10 3,13 PC 5 1 6,33 3,59 27,9 2,58 6,73 26,4 8,13 0,11 -2,36 PC 15 1 6,99 4,55 17,3 1,56 8,13 13,0 8,84 0,13 0,88 PC 19 1 7,57 4,49 20,2 0,90 6,30 19,7 8,83 0,02 -4,99
Tabella 6.2 - Valori in meq/l e relativo sbilanciamento delle analisi dei campioni prelevati durante la seconda campagna
Codice Campagna meq/l Ca meq/l Mg meq/l Na meq/l K Alck meq/l meq/l Cl meq/l SO4 meq/l NO3 Sbilancio 200
Possera 2 2 5,23 1,96 2,08 0,14 4,47 0,84 4,13 0,06 -0,81 Possera 2A 2 5,29 2,18 1,94 0,14 4,87 0,95 3,91 0,13 -3,18 Possera 3 2 4,79 2,54 2,53 0,11 5,60 0,86 3,31 0,08 1,20 Possera 5 2 5,23 3,20 2,39 0,10 6,07 0,96 3,93 0,02 -0,54 Possera 6 2 4,86 3,63 2,18 0,09 5,33 1,22 4,35 0,00 -1,42 Sezione 1 2 7,66 3,09 2,44 0,09 3,37 2,06 8,31 0,00 -3,34 Sezione 2 2 8,75 4,47 2,15 0,14 4,07 1,63 10,4 0,00 -3,60 Sezione 3 2 3,09 2,99 1,04 0,04 5,07 0,81 1,39 0,00 -1,55 Sezione 4 2 6,29 3,71 1,85 0,06 3,23 1,30 7,59 0,00 -1,84 Sezione 9 2 6,96 4,74 2,77 0,09 4,90 2,14 7,58 0,03 -0,69 Sezione 14 2 9,29 4,65 25,6 21,0 5,37 45,6 11,1 0,05 -2,55 Scarico 2 9,12 4,98 24,5 12,8 6,00 36,8 9,56 0,08 -2,06 Possera 5C 2 4,82 3,83 2,13 0,08 5,67 1,21 3,39 0,01 5,60 Possera 5D 2 5,06 3,80 2,11 0,17 5,63 1,27 4,18 0,00 0,48 Pozzo 2 2 10,9 6,09 4,86 0,08 7,20 3,72 10,5 0,27 0,81 Pozzo 3 2 5,84 2,60 3,87 0,12 4,47 3,30 4,74 0,21 -2,23 Pozzo 6 2 7,36 3,86 4,99 0,09 6,13 4,53 5,67 0,25 -1,72 A1 2 14,7 8,70 4,57 0,12 8,10 9,13 13,2 0,21 -8,69 PC 17 2 5,46 2,62 11,3 3,40 4,73 12,4 5,57 0,12 -0,48 PC 12 2 13,2 6,02 23,7 5,51 5,30 36,1 8,69 0,18 -3,57 PC 6 2 3,13 1,75 13,6 1,36 5,57 9,27 5,03 0,20 -1,27 PC 19 2 6,66 3,71 15,7 1,09 6,30 14,4 7,04 0,06 -2,26 Pozzo 4 2 7,36 3,40 5,24 0,13 5,47 4,39 6,42 0,19 -2,06 PC 15 2 5,93 3,70 16,5 1,14 6,70 14,5 6,80 0,12 -3,03 PP31 2 4,74 2,48 1,20 0,05 4,30 0,96 3,48 0,10 -4,50 PP35 2 5,40 2,78 1,26 0,04 4,77 1,13 4,00 0,06 -4,87 PP39 2 5,63 3,20 1,29 0,04 4,87 1,29 4,12 0,08 -1,92
Tabella 6.3 - Valori in meq/l e relativo sbilanciamento delle analisi dei campioni prelevati durante la terza campagna.
Codice Campagna meq/l Ca meq/l Mg meq/l Na meq/l K Alck meq/l meq/l Cl meq/l SO4 meq/l NO3 Sbilancio 200
Possera 1 3 4,61 1,13 1,00 0,04 5,30 0,63 1,00 0,07 -3,24 Possera 2 3 5,42 1,83 1,27 0,09 4,70 0,64 3,46 0,18 -4,25 Possera 6 3 5,75 3,87 1,87 0,04 5,97 0,92 4,13 0,21 2,59 Possera 2A 3 6,39 2,63 1,40 0,11 5,53 0,77 4,47 0,22 -4,24 Possera 3 3 5,87 2,67 1,83 0,11 5,53 0,85 4,15 0,24 -2,82 Possera 4 3 11,8 8,84 8,17 0,22 4,60 5,16 20,1 0,61 -4,83 Possera 5 3 5,75 3,17 1,85 0,09 5,80 1,02 4,22 0,24 -3,77 Possera 5D 3 5,38 3,65 1,92 0,09 5,60 1,13 4,58 0,17 -3,95 Possera 5C 3 5,36 3,65 1,89 0,08 5,70 1,07 4,51 0,18 -4,31 Sezione 2 3 6,29 2,53 1,37 0,04 4,33 1,13 4,97 0,10 -2,89 Sezione 3 3 3,39 2,48 0,98 0,03 4,83 0,73 1,47 0,05 -2,79 Sezione 1 3 6,52 2,33 1,37 0,04 4,40 1,04 5,01 0,10 -2,67 Sezione 4 3 4,85 2,76 1,23 0,04 4,40 0,91 3,61 0,07 -1,02 Sezione 7 3 4,99 2,66 1,36 0,05 4,40 1,08 3,75 0,08 -2,74 Sezione 9 3 5,30 2,88 1,65 0,06 4,63 1,32 4,33 0,09 -4,84 Sezione 11 3 5,58 3,03 1,76 0,06 4,43 1,49 4,68 0,08 -2,40 Sezione 12 3 5,62 3,09 2,42 0,05 4,67 1,91 5,07 0,08 -4,61 Sezione 14 3 9,68 4,07 25,8 17,0 5,77 40,1 12,4 0,38 -3,65 Sezione 14/2 3 7,84 3,35 28,0 26,0 5,30 48,0 12,6 0,60 -1,97 Sezione 13 3 5,84 3,15 2,46 0,10 4,77 2,04 5,17 0,08 -4,29 Sezione 15 3 6,28 3,17 5,70 2,88 4,60 7,54 6,02 0,12 -1,40 Sezione 17 3 6,21 3,17 5,98 2,62 4,77 7,60 5,97 0,09 -2,40 Sezione 18 3 6,21 3,55 5,55 0,60 4,40 5,88 6,13 0,08 -3,55 Pozzo 3 3 6,40 2,98 3,60 0,11 4,77 3,18 5,04 0,15 -0,28 Pozzo 6 3 7,08 3,98 5,26 0,09 5,87 4,58 5,63 0,00 2,04 PC 17 3 5,49 2,81 5,61 2,03 5,47 5,56 5,34 0,17 -3,69 PC 12 3 6,45 3,08 13,3 3,49 5,20 15,3 6,46 0,74 -4,92 PC 6 3 4,67 2,51 10,0 1,63 5,73 8,15 5,41 0,18 -3,47
PC 19 3 5,48 3,09 11,4 0,91 5,97 9,81 5,51 0,15 -2,53 PC 15 3 4,95 3,01 11,5 1,15 5,80 8,70 6,32 0,16 -1,61 Pozzo 4 3 9,05 3,83 5,98 0,12 5,03 5,99 8,18 0,17 -1,98 PP31 3 4,73 2,47 1,05 0,04 4,20 0,84 3,24 0,15 -1,75 PP35 3 4,85 2,57 1,10 0,04 4,77 0,84 2,99 0,08 -1,38 PP39 3 4,90 2,79 1,06 0,04 5,17 0,89 2,95 0,09 -3,39 A1 3 14,7 8,67 4,65 0,08 8,37 3,77 16,8 0,18 -3,78
6.3 Classificazione chimica delle acque
6.3.1 Premessa
La classificazione chimica permette di distinguere famiglie di acque significative dal punto di vista dell'interazione acqua-roccia, mentre le caratteristiche isotopiche degli atomi che costituiscono le caratteristiche isotopiche degli atomi che costituiscono le molecole d'acqua (idrogeno e ossigeno) forniscono indicazioni sulla storia delle molecole stesse.
In accordo a Tonani (1970), una classificazione delle acque, che abbia la pretesa di essere significativa, deve riferirsi ai processi che ne determinano la composizione. Ogni classe deve riferirsi ad un qualche tipo di associazione tra i suoi membri, per esempio che abbiano la stessa composizione chimica (che di regola significa che hanno la stessa storia, per esempio che provengono dalla stessa formazione).
E' opportuno sottolineare che i corpi d'acqua naturali sono, di fatto, un'astrazione (prossimi ad una qualche realtà quanto si voglia, ma sempre un'astrazione) alla quale si giunge in seguito alla classificazione e che la natura del risultato dipende dalla struttura dell'insieme dei dati su cui si lavora e non su quella dell'oggetto naturale (che è quella a cui tentiamo di risalire). Inoltre la struttura dei dati dipende dal criterio con cui sono stati raccolti i campioni per le analisi.
Già da vari decenni sono stati proposti numerosi diagrammi per la classificazione chimica delle acque. Per lo più essi sono facili da costruire e permettono un rapido confronto visuale di analisi chimiche individuali (per esempio i diagrammi di Stiff). Essi tuttavia non si prestano per una presentazione grafica di un grande numero di analisi. Per una classificazione delle acque a scopi geochimici è invece indispensabile disporre di un sistema classificativo che permetta l'interpretazione, la più immediata possibile, di un numero anche molto grande di campioni.
I diagrammi sviluppati da Piper (1944) e da Schoeller (1955) permettono di visualizzare le composizioni dei cationi e degli anioni di molti campioni su un unico grafico, in cui sono immediatamente distinguibili i principali raggruppamenti e/o possibili trends evolutivi.
Si pensi ai diagrammi ternari Mg-(Na+K)-Ca e Cl-SO4-HCO3 (nei quali si utilizzano i dati chimici espressi in eq/l o meq/l).
Dopo un attento esame comparato dei vari diagrammi classificativi proposti, si è scelto per questo lavoro di tesi, il diagramma quadrato di Langelier Ludwig, di seguito citato come LL, (Langelier Ludwig, 1942; Ottonello, 1997). Tale diagramma permette una più immediata interpretazione rispetto ai diagrammi sopra citati. Esso utilizza le concentrazioni delle specie ioniche principali Ca2+, Mg2+, Na+, K+, Cl, SO42-, HCO3 (+ CO3). Un diagramma LL è costituito da un quadrato i cui lati sono suddivisi in 50 parti uguali. La composizione chimica di un'acqua è riportata nel diagramma LL usando i valori di reazione ricalcolati a partire dalle concentrazioni dei principali costituenti cationici e anionici (ci) rispettivamente, espresse in eq/l o in meq/l.
Per esempio:
R(Na) = 50 * CNa / (CNa + CK + CCa + CMg) R(Cl) = 50 * CCl / (CCl + CSO4 + CHCO3)
Avendo a disposizione 7 variabili (4 cationi e 3 anioni) è teoricamente possibile costruire molti diagrammi quadrangolari. Tuttavia, risulta conveniente selezionare opportuni raggruppamenti di anioni e cationi, per esempio sulla base della matrice dei coefficienti di correlazione tra le 7 variabili. Nel diagramma classico R(Na) viene sommato a R(K) e riportato sull'asse Y, mentre R(HCO3) viene riportato sull'asse X. Pertanto, a causa dell'elettroneutralità, in questo diagramma (LLHCO3) si ha:
R(Ca) + R(Mg) = 50 - (R(Na) + R(K)) e R(Cl + RS04) = 50 – R(HCO3)
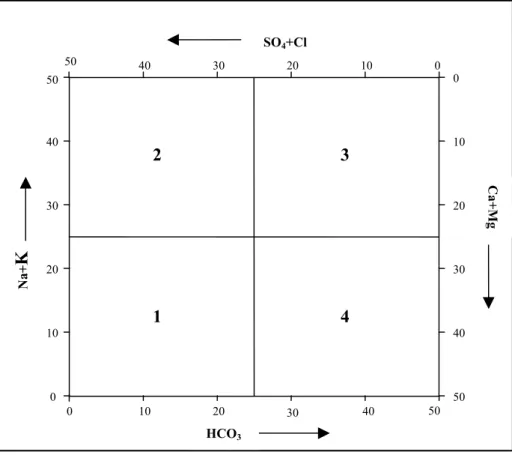
A seconda della loro posizione all'interno del diagramma di figura 6.1, le acque sono classificate come: alcalino terrose (quadrante 1), solfato-clorurato-alcaline (quadrante 2), bicarbonato-solfato-clorurato-alcaline (quadrante 3) e bicarbonato-alcalino terrose (quadrante 4).
Mantenendo costante i raggruppamenti dei cationi, si possono costruire gli altri due diagrammi LL (LLCl e LLSO4) che hanno cloro e solfato, rispettivamente, come anioni isolati. Questi due diagrammi permettono di distinguere, all'interno delle acque solfato-clorurate quelle a cloruro o solfato dominante. Infine, i diagrammi binari (figura 6.2), K vs Na e Mg vs Ca, permettono di affinare la classificazione distinguendo, all'interno delle acque alcaline, quelle a Na o K dominante e all'interno delle acque alcalino terrose, quelle a calcio o magnesio dominante.
HCO3 4 1 3 2 10 20 10 30 40 30 40 40 30 20 40 30 20 10 10 20 50 50 0 50 0 50 0 0 Na+ K C a+ M g SO4+Cl
Figura 6.1 – Esempio di diagramma LLHCO3.
b a potassiche sodiche X=Y Na (meq/l) K (meq/l) calciche magnesiache X=Y Mg (meq/l) Ca (meq/l) Figura 6.2 – Diagrammi binari: a) Mg 2+
TDS
Cl+SO4
HCO3
B A
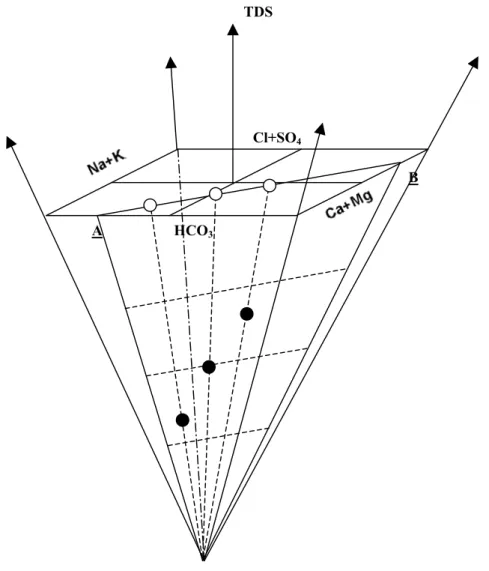
Figura 6.3 – Piramide composizionale di Langelier-Ludwig con la traccia della sezione A-B sulla base quadrata che rappresenta l’LLHCO3.
○ punti allineati sul diagramma LLHCO3
● distribuzione dei punti nello spazio in base alla loro salinità
Nei diagrammi classificativi LL vengono esaminati i rapporti tra le sette principali specie disciolte, ma non sono considerate le concentrazioni assolute, cioè riferite al solvente, delle singole specie ioniche. Ne consegue che due o più campioni che occupano la stessa posizione potrebbero differire per la loro salinità ionica totale (SIT o TDS: Total Dissolved Solid). Per avere un diagramma con una capacità discriminante in tal senso, bisogna interpretare il diagramma quadrato LL come la base di una piramide il cui asse rappresenta la SIT espressa in eq/l o meq/l. Opportune sezioni triangolari di tale piramide, passanti per il suo vertice, permettono di recuperare l'informazione relativa alla SIT. In queste sezioni triangolari, le linee con pendenza -1 sono linee di uguale salinità o iso-saline, mentre l'origine degli assi corrisponde al vertice della piramide, dove la salinità è uguale a 0. La piramide di LL (Fig. 6.3) può pertanto permettere di individuare mescolamenti tra acque
appartenenti a differenti famiglie. In tal caso, se non intervengono fenomeni di precipitazione nel processo di miscelazione, i punti rappresentativi delle acque devono cadere su uno stesso allineamento non solo sul diagramma quadrato (sezione basale della piramide LL) ma anche nelle sezioni triangolari sopra descritte.
6.3.2 I diagrammi LL e diagrammi binari
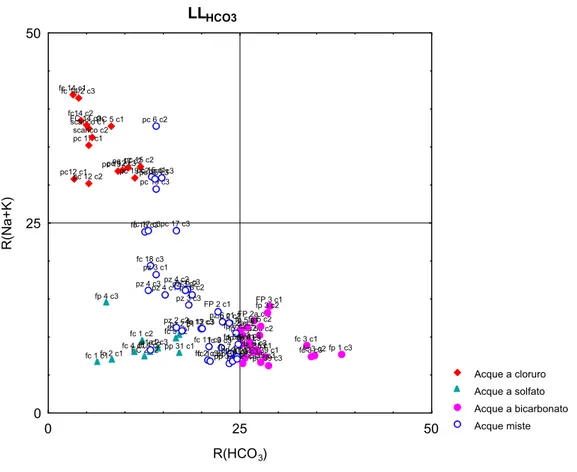
LLHCO3 Acque a cloruro Acque a solfato Acque a bicarbonato Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3PC 5 c1 pc 12 c3 pc 19 c1pc 17 c2 pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2 fc 9 c2fc 9 c1 a1 c3pp 31 c1 fc 2 c1 FC 2 c2fc 4 c2 fc 1 c1 fc 4 c1 pp35 c1pp 39 c1 fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3 pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2 fp 5 c2 fp 6 c3 fp 3 c3 FP 2 c3 fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1pc 15 c3pc 6 c3 fc 15 c3fc 17 c3 fc 18 c3 pz 3 c1 pc 17 c3 pz 4 c3pz 4 c1 a1 c2 pz 6 c3pz 6 c2 pz 4 c2pz 3 c2 pz 3 c3 pz 6 c1 pz 2 c1 pz 2 c2fc 13 c3fc 12 c3 fc 11 c3fc 9 c3 pp 39 c2pp 35 c2fc 7 c3 fp 6 c2 pp 31 c2 fc 2 c3 fc 4 c3 fp 5d c3 fc 1 c3 fp 2 c2 FP 2 c1 0 25 50 R(HCO3) 0 25 50 R(Na+K)
Figura 6.4. Diagramma LLHCO3.
Nel diagramma LLHCO3 di figura 6.4 le acque che hanno lo ione bicarbonato come ione dominante, rappresentate da un pallino di colore rosa, sono:
− I campioni: FP2A, FP3, FP5, FC3, PP35 e PP39 della I campagna. − I campioni: FP2A, FP3, FP5, FP5C, FP5D e FC3 della II campagna.
− I campioni: FP1, FP2, FP2A, FP3, FP5, FP5C, FP6, FC3, PP31, PP35 e PP39 della III campagna.
Nel diagramma LLCl le acque per le quali il cloruro costituisce lo ione dominante e la somma Na+K prevale sulla somma Ca+Mg (contraddistinte dal simbolo “rombo” di colore rosso in figura 6.5), sono:
LLCl Acque a cloruro Acque a solfato Acque a bicarbonato Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3 pc 19 c1 pc 17 c2 pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2 fc 9 c2 fc 9 c1 a1 c3 pp 31 c1 fc 2 c1 fc 4 c2 FC 2 c2 fc 1 c1 fc 4 c1 pp35 c1 pp 39 c1 fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3 pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2 fp 5 c2 fp 6 c3 fp 3 c3 FP 2 c3 fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3 pc 15 c3 fc 15 c3 fc 17 c3 fc 18 c3 pz 3 c1 pc 17 c3 pz 4 c3 pz 4 c1 a1 c2 pz 6 c3 pz 6 c2 pz 4 c2 pz 3 c2 pz 3 c3 pz 6 c1 pz 2 c1 pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3 fc 9 c3 pp 39 c2 fc 7 c3 pp 35 c2 fp 6 c2 pp 31 c2fc 2 c3 fc 4 c3 fp 5d c3 fc 1 c3 fp 2 c2 FP 2 c1 0 25 50 R(Cl) 0 25 50 R(Na+K) A B Figura 6.5. Diagramma LLCl
− I campioni: FC14, PC12, PC17, PC19, SC e PC5 della I campagna. − I campioni: FC14, PC12, PC19, PC15, PC17 e SC della II campagna. − I campioni: FC14, FC14/2 e PC12 della III campagna.
Le acque in cui lo ione dominante è il solfato (rappresentate nel digramma di figura 6.6 con un triangolo verde) sono:
− I campioni: FC1, FC2, FC4, FC9 e PP31 della I campagna. − I campioni sono: FC1, FC2, FC4 e FC9 della II campagna. − I campioni: FP4 e A1 della III campagna.
LLSO4 Acque a cloruro Acque a solfato Acque a bicarbonato Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3pc 17 c2pc 19 c1 pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2 fc 9 c2fc 9 c1 a1 c3 pp 31 c1 fc 2 c1 fc 4 c2 FC 2 c2 fc 1 c1 fc 4 c1 pp35 c1 pp 39 c1 fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3 pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2 fp 5 c2 fp 6 c3 fp 3 c3 FP 2 c3 fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3pc 15 c3 fc 15 c3 fc 17 c3 fc 18 c3 pz 3 c1 pc 17 c3 pz 4 c3 pz 4 c1 a1 c2 pz 6 c3 pz 6 c2 pz 4 c2 pz 3 c2 pz 3 c3 pz 6 c1 pz 2 c1pz 2 c2 fc 13 c3fc 12 c3 fc 11 c3 fc 9 c3 pp 39 c2 fc 7 c3 pp 35 c2 fp 6 c2 pp 31 c2fc 4 c3 fc 2 c3 fp 5d c3 fc 1 c3 fp 2 c2 FP 2 c1 0 25 50 R(SO4) 0 25 50 R(Na+K)
Figura 6.6 Diagramma LLSO4
Infine, il gruppo di acque, raffigurate mediante un cerchio blu nei diagrammi LL sopra mostrati, sono classificabili come acque miste. Tali acque sono rappresentate dai seguenti campioni:
− I campioni: FP2, PZ3, PZ6, PZ4, PC15 e PZ2 della I campagna.
− I campioni: FP2, FP6, PZ3, PZ6, PZ4, PP31, A1 e PZ2 della II campagna. − I campioni: FP5D, FC1, FC2, FC4, FC7, FC9, FC11, FC12, FC13, FC15,
FC17, FC18, PZ6, PZ4, PZ3, PC17, PC6, PC19 e PC15 della III campagna.
I risultati sopra descritti sono sintetizzati in tabella 6.5. In tale tabella è riportata la diversa classe di appartenenza: i numeri 1,2 e 3 indicano in quale campagna è stato prelevato il campione. Inoltre, sono evidenziati in rosso quei campioni che in tutte e tre le campagne risultano nella stessa famiglia, in rosa quei campioni che mostrano un diverso comportamento in tutte le campagne, rimangono così in blu quelli che almeno in una campagna cambiano idrotipo ed in nero quelli campionati soltanto una volta. Per chiarire meglio quanto appena descritto analizziamo la tabella 6.5:
− i campioni FP2A, FP3, FP5 (torrente Possera), FC3, FC14 (fiume Cecina), PZ2 PZ3 PZ6 PZ4 (pozzi privati dell’Eti e Altair), SC (scarico) e PC6, PC12 (pozzo della Cacciatina), non mostrano variazioni di composizione chimica tra le diverse campagne di campionamento eseguite.
− I campioni FP2 (torrente Possera), FC1, FC2, FC4, FC9 (fiume Cecina), PC17, PC19 (pozzi della Cacciatina), mantengono la stessa composizione tra la prima e la seconda campagna e cambiano composizione nella terza. − I campioni PP35, PP39 (pozzi Puretta) cambiano composizione solo nella
seconda campagna.
− I campioni FP5D, FP6 (torrente Possera), PP31 (pozzi Puretta), A1 (piezometro privato), cambiano composizione in ogni campagna.
− I punti FP1, FP4 (torrente Possera), FC7, FC11, FC12, FC13, FC14/2, FC15, FC17 FC18 (fiume Cecina) e PC5 (pozzo della Cacciatina) sono stati campionati solo una volta.
Le variazioni di composizione chimica tra una campagna e l’altra sono probabilmente da imputare ad un diverso regime di circolazione delle acque nel sottosuolo. Questo argomento verrà trattato in maniera esaustiva nel capitolo 8.
Tabella 6.5 – Classi di appartenenza dei campioni per campagna di campionamento. NOME Codice clorurate solfate bicarbonate miste
Possera 1 FP 1 3 Possera 2 FP 2 3 12 Possera 4 FP 4 3 Possera 5C FP 5C 23 Possera 5D FP 5D 2 3 Possera 6 FP 6 3 2 Sezione 1 FC 1 12 3 Sezione 2 FC 2 12 3 Sezione 4 FC 4 12 3 Sezione 7 FC 7 3 Sezione 9 FC 9 12 3 Sezione 11 FC 11 3 Sezione 12 FC 12 3 Sezione 13 FC 13 3 Sezione 14/2 FC 14/2 3 Sezione 15 FC 15 3 Sezione 17 FC 17 3 Sezione 18 FC 18 3 Pozzo Cacciatana 17 PC 17 12 3 Pozzo Cacciatina 6 PC 6 23 Pozzo Cacciatina 19 PC 19 12 3 Pozzo Cacciatina 15 PC 15 2 13 Pozzo Puretta 31 PP31 1 3 2 Pozzo Puretta 35 PP35 13 2 Pozzo Puretta 39 PP39 13 2 Piezometro A1 3 2 Scarico Scarico 12 Pozzo Cacciatina 5 PC 5 1 Pozzo2 PZ2 12 Possera 2A FP 2A 123 Possera 3 FP 3 123 Possera 5 FP 5 123 Sezione 3 FC 3 123 Sezione 14 FC 14 123 Pozzo Eti 3 PZ 3 123 Pozzo Eti 6 PZ 6 123 Pozzo Altair 4 PZ 4 123 Pozzo Cacciatina 12 PC 12 123
Per affinare ulteriormente la classificazione sono stati utilizzati i diagrammi binari Na vs K e Ca vs Mg (Figs. 6.7 e 6.8), che permettono di evidenziare il catione alcalino e quello alcalino-terroso dominante. Tutte le acque di tipo clorurato alcalino presentano il Na come catione dominante (Fig 6.7).
Figura 6.7 - Diagramma binario Na versus K. Na vs K Acque a cloruri Acque a solfati Acque a bicarbonati Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3 pc 19 c1 pc 17 c2 pc 19 c2pc 15 c2 fp 4 c3 fc 1 c2fc 9 c2fc 9 c1a1 c3 pp 31 c1fc 4 c2FC 2 c2fc 4 c1fc 2 c1fc 1 c1 pp35 c1 pp 39 c1fc 3 c2fc 3 c1FP 2a c1fp 5d c2fp 5d c2 fc 3 c3p 31 c3fp 5 c1 pp 39 c3FP 2a c2 pp 35 c3fp 1 c3FP 2 c3fp 2a c3fp 5c c3fp 5 c3fp 3 c3fp 6 c3fp 5 c2FP 3 c1fp 3 c2 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3pc 15 c3 fc 15 c3fc 17 c3 fc 18 c3pz 3 c1 pc 17 c3 pz 4 c3 pz 4 c1 a1 c2pz 6 c2pz 6 c3pz 4 c2 pz 3 c2 pz 3 c3 pz 6 c1pz 2 c1pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3fc 9 c3 pp 39 c2fc 7 c3 pp 35 c2fp 6 c2 pp 31 c2fc 4 c3fc 2 c3fc 1 c3fp 5d c3fp 2 c2FP 2 c1 0 10 20 30 40 50 milli eq. Na 0 10 20 30 40 50 milli eq. K
Inoltre il grafico di figura 6.7 mostra per questa famiglia una notevole variabilità del rapporto Na/K (di circa un fattore 10).
Dal diagramma binario Ca vs Mg (Fig 6.8), si rileva, per tutti i campioni, la dominanza dello ione calcio rispetto al Mg, ad eccezione del campione FC3. Inoltre, il rapporto Ca/Mg è piuttosto costante variando tra 1,2 e circa 3.
In particolare, il campione FC3, prelevato sia nella prima che nella seconda campagna, mostra un rapporto prossimo all’unità (cerchio rosso) mentre il campione PC12c1, molto più salino presenta un rapporto Ca/Mg di circa 2,5. Tra le acque di composizione solfato-calcica il più alto valore di Ca/Mg è mostrato dal campione FC1c1.
Ca vs Mg Acque a cloruri Acque a solfati Acque a bicarbonati Acque miste pc12 c1 fc 14 c1fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3 pc 19 c1 pc 17 c2 pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2 fc 9 c2 fc 9 c1 a1 c3 pp 31 c1 fc 2 c1 fc 4 c2 FC 2 c2 fc 1 c1 fc 4 c1 pp35 c1pp 39 c1 fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1fp 5 c3 fp 1 c3 fp 3 c2 fp 5 c2 fp 6 c3 fp 3 c3 FP 2 c3 fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3pc 15 c3fc 15 c3 fc 17 c3 fc 18 c3pz 3 c1 pc 17 c3 pz 4 c3 pz 4 c1 a1 c2 pz 6 c3pz 6 c2 pz 4 c2 pz 3 c2pz 3 c3 pz 6 c1 pz 2 c1 pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3 fc 9 c3pp 39 c2 fc 7 c3pp 35 c2 fp 6 c2 pp 31 c2 fc 2 c3fc 4 c3 fp 5d c3 fc 1 c3 fp 2 c2 FP 2 c1 0 2 4 6 8 10 12 14 16 18 20 22 milli eq. Ca 0 2 4 6 8 10 12 14 16 18 20 22 milli eq. Mg
Figura 6.8 – Diagramma binario Ca vs Mg
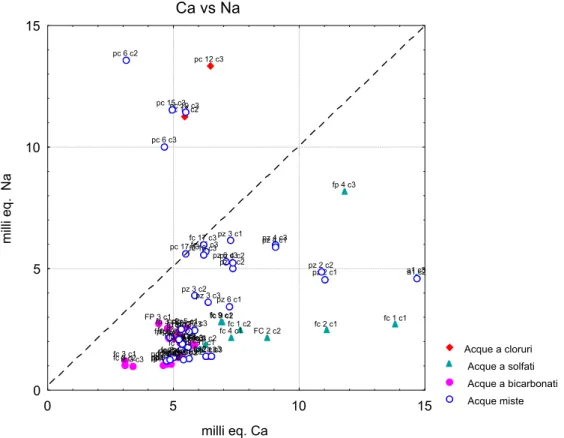
igura 6.9(a) – Diagramma binario Ca vs Na Ca vs Na Acque a cloruri Acque a solfati Acque a bicarbonati Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3 pc 19 c1 pc 17 c2 pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2 fc 9 c2 fc 9 c1 a1 c3 pp 31 c1fc 4 c2FC 2 c2fc 4 c1 fc 2 c1fc 1 c1 pp35 c1 pp 39 c1 fp 5d c2 fc 3 c1fp 5d c2 fc 3 c2fc 3 c3pp 31 c3FP 2a c1 fp 5 c1 pp 39 c3FP 2a c2 pp 35 c3fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2fp 5 c2fp 6 c3fp 3 c3 FP 2 c3fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3 pc 15 c3 fc 15 c3 fc 17 c3 fc 18 c3pz 3 c1 pc 17 c3 pz 4 c3pz 4 c1 a1 c2 pz 6 c3pz 6 c2pz 4 c2 pz 3 c2pz 3 c3pz 6 c1 pz 2 c1 pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3 fc 9 c3 pp 39 c2 fc 7 c3pp 35 c2 fp 6 c2 pp 31 c2fc 4 c3FP 2 c1fp 5d c3fp 2 c2fc 2 c3fc 1 c3 0 10 20 30 40 50 milli eq. Ca 0 10 20 30 40 50 milli eq. Na F
La figura 6.9(a) mostra, la presenza di cinque campioni (PC6c2, PC6c3, PC15c3, , PC15c1 e PC19c3), di composizione mista, che hanno il Na come ione dominante. Osservando le figure 6.9(a) e 6.9(b) si nota per le acque bicarbonato alcalino terrose solfato-alcalino terrose e miste la dominanza dello ione Ca rispetto al Na: soltanto i campioni PC17c3, FC17c3, FC15c3 e FC18c3, appartenenti alla famiglia delle acque miste, hanno un rapporto Ca/Na prossimo ad 1.
Ca vs Na Acque a cloruri Acque a solfati Acque a bicarbonati Acque miste pc 12 c3 pc 17 c2 fp 4 c3 fc 1 c2 fc 9 c2 fc 9 c1 a1 c3 pp 31 c1 fc 2 c1 fc 4 c2 FC 2 c2 fc 1 c1 fc 4 c1 pp35 c1pp 39 c1 fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3 pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2fp 5 c2 fp 6 c3fp 3 c3 FP 2 c3fp 2a c3 pc 6 c2 pc 19 c3 pc 6 c3 pc 15 c3 fc 15 c3 fc 17 c3 fc 18 c3 pz 3 c1 pc 17 c3 pz 4 c3pz 4 c1 a1 c2 pz 6 c3 pz 6 c2 pz 4 c2 pz 3 c2 pz 3 c3pz 6 c1 pz 2 c1 pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3 fc 9 c3 pp 39 c2 fc 7 c3pp 35 c2 fp 6 c2 pp 31 c2fc 4 c3 fc 2 c3 fp 5d c3 fc 1 c3 fp 2 c2 FP 2 c1 0 5 10 15 milli eq. Ca 0 5 10 15 milli eq. Na
Figura 6.9(b) – Ingrandimento diagramma binario della figura 4.9(a) evidenziato in rosso
6.4 Sezioni di Langelier-Ludwig
Il diagramma LL, come già spiegato nel paragrafo 6.3.2, non tiene conto delle diverse salinità delle acque. Per tanto affinché un all’allineamento dei punti nei diagrammi LL possa essere interpretato come miscelamento fra i due termini estremi è necessario che lo stesso allineamento (e stessa sequenza dei singoli punti in esso) si ottenga anche nella sezione della piramide che passa per l’allineamento sull’LL e per il vertice della piramide stessa. Tutto ciò è comunque valido se non intervengono fenomeni secondari di precipitazione. Analizzando i tre diagrammi LL riportati nelle figure 6.4, 6.5 e 6.6, abbiamo scelto la sezione AB del diagramma LLCl (di figura
6.10). Questa sezione è la più rappresentativa, dato che la maggior parte dei campioni si dispone grosso modo lungo un unico allineamento.
Dalla figura 6.10(a) si nota una notevole variabilità di TDS per le acque
clorurato-a quclorurato-anto precedentemente osservclorurato-ato possiclorurato-amo schemclorurato-atizzclorurato-are quclorurato-anto segue: cque a bicarbonato di calcio
sodiche (salinità tra 20 e 165 meq/l). Al contrario le acque solfato-calciche (TDS tra 20 e 45 meq/l) e le acque bicarbonato- alcalino terrose (TDS 10 e 25 meq/l) mostrano un più limitato range di variazione della salinità. Infine le acque miste presentano un TDS che varia tra 15 meq/l e 45 meq/l.
D A i campioni: 9 (della I campagna); ; PP39 (della III La composizione riflette il drenaggio di zone di bacino caratterizzate da affioramenti
cque a cloruro di sodio
Tali acque sono rappresentate da
− FP2A, FP3, FP5, FC3, PP35 e PP3
− FP2A, FP3, FP5, FP5C, FP5D e FC3 (della II campagna) − FP1, FP2, FP2A, FP3, FP5, FP5C, FP6, FC3, PP31, PP35 e
campagna).
calcarei (vedi anche carta geologica riportata in figura 1.3). Queste acque hanno un rapporto Ca/Mg nettamente superiore ad 1. Il campione con il rapporto Ca/Mg più basso è quello siglato FC3 (Ca/Mg ≈ 1).
A
tate dai campioni:
5 (della I campagna); ;
La co a lisciviazione di formazioni
cque a solfato di calcio Tali acque sono rappresen
− FC14, PC17, PC12, PC19, SC e PC
− FC14, PC17, PC12, PC19, PC15 e SC (della II campagna) − FC14, FC14/2 e PC12 (della III campagna).
mposizione di queste acque può riflettere sia l
evaporitiche ricche in alite, sia l’attività antropica di vario tipo. Per esempio possiamo considerare i campioni FC14 e FC14/2 relativi al Botro S.Marta che oltre a drenare vasti affioramenti evaporatici, riceve scarichi sia civili che industriali.
A
sentate dai campioni:
ampagna); Queste acque sono rappre
− FC1, FC2, FC4 e FC9 (della II campagna); − FP4 e A1 (della III campagna).
La com l drenaggio di zone di bacino caratterizzate
cque miste solfato-bicarbonato-clorurato posizione di queste acque riflette i da estesi affioramenti di gessi.
A on sodio dominante c pioni: I campagna); on calcio dominante Rappresentate dai cam
− PC15 e PC6 (della
− PC15, PC6 e PC19 (della III campagna). c
pioni:
(della I campagna);
, FP6, PP31 (della II campagna);
con rapporto Ca/Na prossimo all’unità Rappresentate dai cam
− PZ2, PZ4, PZ6, FP2
− A1, PZ2, PZ3, PZ6, PZ4 PP35, PP39, FP2
− PZ4, PZ3, PZ6, FC1, FC2, FC11, FC9, FC7, FP5D e FC4 (della III campagna).
ella III campagna).
Tale composizione può essere dovuta sia all’effetto della lisciviazione di depositi di
oltre dall’analisi delle figura 6.10 (a) e 6.10 (b) si notano due principali primo si trovano tutte le acque a composizione clorurato-sodica (rombi
− individuano tutti i campioni con composizione solfato-calcica (triangoli verdi) e tutti i campioni, con composizione bicarbonato-− FC17, FC15, FC18 e PC17 (d
evaporiti e/o carbonatici sia all’effetto di diluizione da parte delle precipitazioni In
allineamenti: − Nel
rossi) delle quali il termine più salino è rappresentato dal campione FC14c1. Nel trend sono presenti anche alcune acque con composizione mista. Tale disposizione di punti è compatibile con un processo di evoluzione per progressiva interazione acqua roccia e/o con un processo di mescolamento.
calcica (pallini rosa). In questo trend sono presenti alcune acque con composizione mista. Anche questo andamento è spiegabile sia con processi di mescolamento sia con un processo di evoluzione per progressiva interazione acqua-roccia.
Sezione LLCl Acque a cloruro Acque a solftato Acque a bicarbonato Acque miste pc12 c1 fc 14 c1 fc14 c2 scarico c1 fc 14/2 c3 pc 12 c2 pc 17 c1 scarico c2 FC 14 c3 PC 5 c1 pc 12 c3 pc 19 c1 pc 17 c2pc 19 c2 pc 15 c2 fp 4 c3 fc 1 c2fc 9 c1fc 9 c2 a1 c3 pp 31 c1fc 2 c1fc 4 c2fc 4 c1FC 2 c2fc 1 c1 pp35 c1 pp 39 c1fp 5d c2 fc 3 c1fc 3 c2FP 2a c1fp 5d c2 fc 3 c3pp 31 c3pp 35 c3pp 39 c3FP 2a c2FP 3 c1fp 5c c3fp 5 c3fp 5 c1 fp 1 c3FP 2 c3fp 3 c2fp 2a c3fp 5 c2fp 3 c3fp 6 c3 pc 6 c2pc 19 c3 pc 15 c1 pc 6 c3pc 15 c3 fc 15 c3 fc 17 c3 fc 18 c3pz 3 c1 pc 17 c3pz 6 c3pz 4 c2pz 6 c2pz 4 c3pz 4 c1 a1 c2 pz 3 c2pz 3 c3pz 6 c1pz 2 c1pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3fc 9 c3 pp 39 c2 fc 7 c3 pp 35 c2fp 6 c2 pp 31 c2fc 4 c3fp 2 c2FP 2 c1fc 2 c3fp 5d c3fc 1 c3 0 20 40 60 80 100 120 140 160
(HCO3+SO4+Ca+Mg) 0 20 40 60 80 100 120 140 160 (Cl+Na+K)
Sezione LLCl Acque a cloruro Acque a solftato Acque a bicarbonato Acque miste pc 12 c3 pc 17 c2 pc 19 c2 pc 15 c2 fc 1 c2fc 9 c1fc 9 c2 pp 31 c1 fc 2 c1 fc 4 c2 FC 2 c2 fc 1 c1 fc 4 c1 pp35 c1pp 39 c1fp 5d c2 fc 3 c1 fp 5d c2 fc 3 c2 FP 2a c1 fc 3 c3 pp 31 c3 fp 5 c1 pp 39 c3 FP 2a c2 pp 35 c3 fp 5c c3 FP 3 c1 fp 5 c3 fp 1 c3 fp 3 c2 fp 5 c2 fp 6 c3 fp 3 c3 FP 2 c3 fp 2a c3 pc 6 c2 pc 19 c3 pc 15 c1 pc 6 c3 pc 15 c3 fc 15 c3fc 17 c3 fc 18 c3pz 3 c1 pc 17 c3 pz 4 c3pz 4 c1 pz 6 c3pz 6 c2 pz 4 c2 pz 3 c2pz 3 c3 pz 6 c1 pz 2 c1 pz 2 c2 fc 13 c3 fc 12 c3 fc 11 c3 fc 9 c3pp 39 c2 fc 7 c3pp 35 c2 fp 6 c2 pp 31 c2 fc 2 c3fc 4 c3 fp 5d c3 fc 1 c3 fp 2 c2FP 2 c1 0 5 10 15 20 25 30 35 40
(HCO3+SO4+Ca+Mg) 0 5 10 15 20 25 30 35 40 (Cl+Na+K)
Figura 6.10(b) – Ingrandimento di figura 4.10(a) evidenziato mediante un quadrato blu.
6.5 Variazioni
temporali
Il grafico della sezione LLCl viene utilizzato per ottenere informazioni qualitative su eventuali processi di mescolamento nel tempo esclusivamente per i pozzi (Fig. 6.11). Per evidenziare i singoli andamenti temporali sono stati utilizzati differenti simboli per ciascun pozzo:
• Pozzi Eti e Altair: “quadrato vuoto” blu;
• Pozzi Puretta e Piezometro: “triangolo vuoto” verde scuro; • Pozzo Cacciatina 17 (PC17): “pallino” rosa;
• Pozzo Cacciatina 12 (PC12): “rombo” blu;
• Pozzo Cacciatina 6 e 5 (PC6 e PC5): “pallino” verde chiaro; • Pozzo Cacciatina 15 (PC15): “triangolo” rosso;
• Pozzo Cacciatina 19 (PC19): “quadrato” celeste.
La figura 6.11 mostra che le acque di tutti i pozzi della Cacciatina presentano il medesimo andamento: la loro concentrazione salina tende a diminuire dalla prima alla terza campagna di campionamento. Ciò indica un processo di diluizione per
mescolamento con acque superficiali di bassa salinità e di composizione bicarbonato alcaline-terrose. Questo processo ha fatto si che le acque passassero da una composizione clorurato-sodica ad acque a composizione mista. L’entità della diluizione è differente per i vari pozzi ed è da mettere in relazione con la variazione del livello piezometrico.
Nella prima campagna l’altezza piezometrica era di circa -8 metri per tutti i pozzi eccetto per il PC17 e PC12 (circa -5 metri). Al contrario nella terza campagna il livello piezometrico era a circa -4 metri per tutti i pozzi eccetto il PC6 (-5,20 metri).
Sezione LLCl
Pozzi Eti e Altair Pozzi Puretta PC17 PC12 PC6 e PC5 PC15 PC19 PZ2c1 PZ3c1 PZ4c1 PZ6c1 PP31c1 PP35c1PP39c1 PC17c1 PC12c1 PC5c1 PC15c1 PC19c1 PZ2c2 PZ3c2 PZ6c2 A1c2 PC17c2 PC12c2 PC6c2 PC19c2 PZ4c2 PC15c2 PP31c2PP35c2PP39c2 PZ3c3 PZ6c3 PC17c3 PC12c3 PC6c3 PC19c3PC15c3 PZ4c3 PP31c3PP35c3PP39c3 A1c3 0 10 20 30 40 50 HCO3+SO4+Ca+Mg 0 20 40 60 80 100 120 Cl+Na+K
Figura 6.11 – Diagramma sezione LLCL per i pozzi campionati nelle tre campagne di prelievo.
In figura 6.12 vengono riportati i pozzi di Puretta, dell’Eti e dell’Altair con l’utilizzo di simboli diversi per una migliore interpretazione:
• Pozzo Eti (PZ3): “triangolo” verde chiaro; • Pozzo Eti (PZ6): “rombo” blu;
• Pozzo privato (PZ2): “rombo vuoto” rosso; • Pozzo Puretta (PP31): “rombo” rosso; • Pozzo Puretta (PP35): “triangolo” nero; • Pozzo Puretta (PP39): “pallino” giallo; • Piezometro (A1): “quadrato” acqua marina.
Sezione LLCl Pozzo 2 Pozzo 3 (Eti) Pozzo 4 (Altair) Pozzo 6 (Eti) PP 31 PP35 PP39 A1 PZ2c1 PZ3c1 PZ4c1 PZ6c1 PP31c1 PP35c1PP39c1 PZ2c2 PZ3c2 PZ6c2 A1c2 PZ4c2 PP31c2PP35c2 PP39c2 PZ3c3 PZ6c3 PZ4c3 PP31c3PP35c3PP39c3 A1c3 10 15 20 25 30 35 40 45 50 HCO3+SO4+Ca+Mg 0 2 4 6 8 10 12 14 16 Cl+Na+K
Figura 6.12 – Diagramma sezione LLCL per i pozzi Puretta, Eti e Altair campionati nelle tre campagne di campionamento.
Per i pozzi Eti, Altair e piezometro (Fig. 6.12) si riscontra un fenomeno di diluizione tra la prima e la seconda campagna, mentre nella terza si risente di un possibile mescolamento con acque con composizione diversa, tale da mostrare un arricchimento in bicarbonati e solfati.
Per i pozzi di puretta (Fig. 6.12) si evidenzia una differenza tra il PP31 e i pozzi PP35 e PP39. Il PP31 mantiene il medesimo comportamento riscontrato nei pozzi della Cacciatina, diminuisce la concentrazione nel tempo. I pozzi PP35 e PP39
mostrano nella seconda campagna una diminuzione in Cl, Na e K, mentre presentano un arricchimento in HCO3, SO4, Ca e Mg. Invece, nella terza campagna, si ha una diluizione delle sostanze disciolte.
6.6 Diagrammi binari per valutare il carico antropico
Per descrivere lo stato ambientale delle acque sotterranee si vanno a considerare quelle specie ioniche che possono essere indicatori di una contaminazione delle falde da parte di agenti inquinanti.
La possibilità che le acque sotterranee possano essere inquinate, infatti, è legata alla velocità con la quale avviene il trasferimento della sostanza contaminante dalla superficie alla falda, all’entità dell’infiltrazione, al percorso seguito e ai processi chimico-fisici-biologici che operano selettivamente in relazione al tipo di terreno e di sostanze.
Quando si parla di vulnerabilità di un acquifero, dunque, si fa riferimento alla suscettibilità di questo ad assorbire e diffondere, anche mitigandone gli effetti, un inquinante fluido o idroveicolato, tale da produrre impatto sulla qualità delle acque sotterranee nello spazio e nel tempo. (Civita, 1987)
I liquami domestici sono considerati da un punto di vista igienico molto più pericolosi degli scarichi industriali e questo dipende dalle loro caratteristiche; infatti, oltre ad un certo contenuto minerale, trasportano un particolare carico di sostanze organiche che possono essere presenti sotto forma di sospensioni fini, sospensioni colloidali, soluzioni ma il contributo principale è dovuto alle sostanze fecali.
Gli scarichi industriali di industrie per l’estrazione di olii e grassi vegetali e animali sono costituiti da acque di rifiuto con acidi e grassi.
Fra le specie inquinanti i nitrati, NO3-, possono derivare sia dai processi di ossidazione dell’ammoniaca che a sua volta è il prodotto finale della degradazione batterica della sostanza proteica, anche dal diretto impiego di fertilizzanti azotati in agricoltura. Lo ione nitrato, infatti, rappresenta un componente di sali molto solubili usati come fertilizzanti e perciò può facilmente passare nelle acque sotterranee per dilavamento del suolo agricolo.
Anche i cloruri, pur essendo sempre presenti nelle acque naturali, nel caso in cui il loro tenore superi una certa soglia, possono rappresentare inquinamento da liquame domestico (sono presenti infatti nelle urine) e/o da scarichi industriali.
La misura del COD (richiesta chimica dell’ossigeno) fornisce la valutazione della quantità di ossigeno consumato nei processi di ossidazione di tutte le sostanze che determinano una richiesta di ossigeno. In altre parole esprime il carico totale di sostanze organiche ed inorganiche chimicamente e biologicamente ossidabili con la sola esclusione dell’ammoniaca e dei nitrati. Se pertanto il campione contenesse sostanze tossiche che possono inibire la misura del BOD, il COD diventa l’unico mezzo per la misura del carico organico totale.
Allo scopo di mettere in luce eventuali fenomeni di inquinamento dell’acquifero e delle acque superficiali campionate, sono stati realizzati diagrammi binari utilizzando le concentrazioni analitiche delle specie ioniche significative.
I diagrammi binari di figura 6.13, Cl-K, Cl-NO3, Cl-NH4 e Cl- COD, sono stati scelti per le loro tipiche caratteristiche di indicatori antropici.
Il grafico Cl vs K può indicare la contaminazione da scarichi di origine industriale. In tale grafico (vedi 6.13, Cl vs K) vengono identificati con i campioni FC14c1, FC14c2, FC14c3 e FC14/2c3, che presentano un contenuto in potassio superiore al valore medio della famiglia.
I grafici Cl-NO3 e Cl-NH4+, sono caratteristici di inquinamento civile e/o agricolo. Per i campioni FC14/2c3 e FC14c3 si nota un arricchimento in nitrati e in ammoniaca rispetto agli altri campioni, poiché raccolgono le acque del centro abitato di Saline di Volterra e dei campi circostanti.
FP2c1 FP2Ac1FC3c1FP3c1FP5c1FC4c1FC1c1FC2c1FC9c1PZ6c1PZ2c1PZ4c1PZ3c1 FC14c1 PP31c1 PP35c1PP39c1 SCc1 PC17c1 PC12c1 PC5c1 PC15c1PC19c1 FP2c2 FP2Ac2FP3c2FC3c2FP5c2FP6c2FC2c2FC4c2FC1c2FC9c2 FC14c2 SCc2 FP5Cc2 FP5Dc2PZ3c2PZ2c2PZ6c2A1c2 PC17c2 PC12c2 PC6c2PC19c2 PZ4c2PC15c2 PP31c2 PP35c2PP39c2FP1c3FP2c3FP6c3 FP2Ac3FP3c3FP5c3FP4c3 FP5Dc3 FP5Cc3FC2c3FC3c3FC1c3FC4c3FC7c3FC9c3 FC11c3FC12c3 FC14c3 FC14/2c3 FC13c3 FC15c3 FC17c3 FC18c3 PZ3c3PZ6c3 PC17c3PZ4c3PC15c3PC6c3PC19c3PC12c3 PP31c3 PP35c3 PP39c3A1c3 -10 0 10 20 30 40 50 60 70 80 meq/l Cl -10 0 10 20 30 40 meq/l K FP2c1 FP2Ac1 FP3c1 FP5c1 PZ2c1 PZ3c1 PZ4c1 PZ6c1 FC1c1FC2c1 FC3c1FC4c1FC9c1 FC14c1 PP31c1 PP35c1 PP39c1 PC5c1PC17c1SCc1 PC12c1 PC15c1 PC19c1 FP2c2 FP2Ac2 FP3c2 FP5c2 FP6c2FC2c2FC1c2 FC3c2FC4c2FC9c2 FC14c2 SCc2 FP5Cc2 FP5Dc2 PZ2c2 PZ3c2PZ6c2A1c2 PC17c2 PC12c2 PC6c2 PC19c2 PZ4c2 PC15c2 PP31c2 PP35c2 PP39c2 FP1c3 FP2c3FP6c3 FP2Ac3FP3c3 FP4c3 FP5c3 FP5Dc3 FP5Cc3 FC2c3 FC3c3 FC1c3 FC4c3FC7c3FC9c3 FC11c3FC12c3 FC14c3 FC14/2c3 FC13c3FC18c3FC15c3FC17c3 PZ3c3 PZ6c3 PC17c3 PC12c3 PC6c3 PC19c3 PC15c3 PZ4c3 PP31c3 PP35c3 PP39c3 A1c3 0 10 20 30 40 50 60 70 meq/l Cl -0,2 0,0 0,2 0,4 0,6 0,8 1,0 meq/l NO3 FP2c1 FP2Ac1 FP3c1FP5c1FC1c1FC2c1PZ6c1PZ2c1PZ4c1PZ3c1 FC3c1FC4c1FC9c1 FC14c1 PP31c1 PP35c1 PP39c1 SCc1 PC17c1 PC12c1 PC5c1 PC15c1PC19c1 FP2c2 FP2Ac2 FP3c2 FP5c2FP6c2FC2c2FC1c2 FC3c2FC4c2FC9c2 FC14c2 SCc2 FP5Cc2 FP5Dc2PZ3c2PZ2c2PZ6c2PZ4c2 PC15c2PC6c2A1c2PC17c2PC19c2 PC12c2 PP31c2 PP35c2 PP39c2FP1c3FP2c3FP6c3 FP2Ac3 FP3c3FP4c3 FP5c3 FP5Dc3 FP5Cc3FC3c3FC11c3FC2c3FC1c3FC4c3FC7c3FC12c3FC9c3 FC14c3 FC14/2c3 FC13c3PZ3c3PZ6c3PC17c3 PC12c3FC18c3PZ4c3FC15c3FC17c3PC6c3PC15c3PC19c3 PP31c3 PP35c3 PP39c3A1c3 -10 0 10 20 30 40 50 60 70 meq/l Cl -0,1 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 NH 4 + mmol/l FP2c1 FP2Ac1 FP3c1 FP5c1 PZ2c1PZ4c1PZ3c1 PZ6c1 FC1c1 FC2c1 FC3c1FC4c1 FC9c1 FC14c1 PP31c1 PP35c1 PP39c1 SCc1 PC17c1 PC12c1 PC5c1 PC15c1 PC19c1 FP2c2 FP2Ac2 FP3c2 FP5c2 FP6c2 FC1c2 FC2c2 FC3c2 FC4c2FC9c2 FC14c2 SCc2 FP5Cc2 FP5Dc2PZ2c2 PZ3c2 PZ6c2 A1c2 PC17c2 PC12c2 PC6c2 PC19c2 PZ4c2 PC15c2 PP31c2 PP35c2 PP39c2 FP1c3 FP2c3 FP6c3 FP2Ac3 FP3c3 FP4c3 FP5c3 FP5Dc3 FP5Cc3 FC2c3 FC3c3FC1c3FC4c3FC7c3FC9c3 FC11c3FC12c3 FC14c3 FC14/2c3 FC13c3 FC15c3 FC17c3 FC18c3 PZ3c3 PZ6c3 PC17c3 PC12c3 PC6c3 PC19c3 PC15c3 PZ4c3 PP31c3 PP35c3 PP39c3 A1c3 -10 0 10 20 30 40 50 60 70 meq/l Cl -2 0 2 4 6 8 10 12 14 16 18 20 22 24 COD ppm
Figura 6.13 – Diagrammi binari.
Da rilevare la posizione dei campioni FP4c3 e PC12c3 nei due diagrammi Cl vs NO3 e Cl vs NH4+, che presentano alto valore di nitrati, ma non di ammoniaca, caratteristico di un’acqua con bassa circolazione, in altre parole di un ambiente più ossidante.
Il diagramma Cl vs COD evidenzia una grande variazione nel rapporto Cl/COD per i campioni delle acque a composizione clorurato-sodiche, mentre per le acque a composizione solfato calciche e bicarbonato alcaline terrose, si nota una bassissima e circa costante concentrazione in cloruri, mentre il COD ha un valore che varia da circa 0 a circa 15 ppm. Per le acque a composizione mista il rapporto Cl/COD presenta valori vicini ad uno, anche se le concentrazioni di Cl e COD sono molto variabili.
Dalla figura 6.14, dove è riportato il diagramma binario NH4-NO3, si osserva che i campioni FP4c3 e PC12c3 presentano un alto contenuto di nitrati ed un basso contenuto di ammoniaca. Ciò indica che queste acque hanno avuto tempo di circolazione sufficiente per la completa ossidazione dell’azoto di origine organica. Invece, tre campioni FC14c2, Fc14C3 e FC14/2c3 hanno un comportamento opposto, perché in ambiente anossico non si verifica l’ossidazione dell’ammoniaca.
FP2c1 FP2Ac1 FP3c1 FP5c1 PZ2c1 PZ3c1 PZ4c1 PZ6c1 FC1c1 FC2c1 FC3c1FC4c1 FC9c1 FC14c1 PP31c1 PP35c1 PP39c1SCc1 PC17c1 PC12c1 PC5c1 PC15c1 PC19c1 FP2c2 FP2Ac2 FP3c2 FP5c2 FP6c2 FC1c2 FC2c2 FC3c2 FC4c2 FC9c2 FC14c2 SCc2 FP5Cc2 FP5Dc2 PZ2c2 PZ3c2 PZ6c2 A1c2 PC17c2 PC12c2PC6c2 PC19c2 PZ4c2 PC15c2 PP31c2 PP35c2 PP39c2 FP1c3 FP2c3 FP6c3FP2Ac3 FP3c3 FP4c3 FP5c3 FP5Dc3 FP5Cc3 FC2c3 FC3c3 FC1c3 FC4c3 FC7c3FC9c3 FC11c3 FC12c3 FC14c3 FC14/2c3 FC13c3 FC15c3 FC17c3 FC18c3 PZ3c3 PZ6c3 PC17c3 PC12c3 PC6c3 PC19c3 PC15c3PZ4c3 PP31c3 PP35c3 PP39c3 A1c3 -0,1 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 NH4+ mmol/l -0,1 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 meq/l NO 3
Figura6.14 – Diagramma binario NH4+-NO3.
6.7 Conclusioni
Come espresso in tabella 6.5 si osserva che le acque superficiali del fiume Cecina nelle prime due campagne sono classificate come acque di tipo solfato-calciche, mentre nella terza campagna sono in prevalenza di tipo misto. Le acque del torrente Pavone sono acque bicarbonato-calciche, le acque del torrente Possera sono in prevalenza di tipo bicarbonato-calciche e le acque del Botro Santa Marta sono di tipo clorurato-sodiche. Le acque sotterranee sono suddivisibili in tre gruppi, i pozzi di Puretta sono acque in prevalenza di tipo solfato-calciche, i pozzi dell’Eti e dell’ Altair sono acque di tipo misto, infine, le acque dei pozzi della Cacciatina sono acque a prevalenza clorurato-sodiche.
In estrema sintesi, per ciò che concerne gli scarichi civili e industriali, questi rappresentano nella medio alta Val di Cecina una minaccia alla qualità delle acque soprattutto nei periodi di minima diluizioni.
Un ulteriore degrado della qualità delle acque, oltre a cause naturali, può essere indotto ad una estesa attività agricola e di allevamento.