1 GLI OSSIDI DI AZOTO
1.1 O
SSIDI DIA
ZOTO: G
ENERALITÀ [1],[2]L'azoto può combinarsi con l'ossigeno per dare origine ad un gruppo di composti binari che viene indicato con la dicitura “Ossidi d'azoto”; in tabella 1.1 riportiamo l'elenco di tali composti.
tabella 1.1 [1],[2] – Ossidi d'azoto
for m u la no me va le nza p ro pr ie tà
N2O Ossido di diazoto 1 Gas incolore, solubile in acqua
NO Ossido di azoto N2O2 Biossido di diazoto
2 Gas incolore, poco solubile in acqua
N2O3 Triossido di diazoto 3 Solido nero, solubile in acqua, si decompone in
acqua NO2 Biossido di azoto
N2O4 Tetraossido di
diazoto
4
Gas rosso-bruno, molto solubile in acqua, si decompone in acqua
N2O5 Pentaossido di
diazoto 5 Solido bianco, molto solubile in acqua, sidecompone in acqua, sublima senza fondere N2O6 Esaossido di
diazoto 5 Si decompone rapidamente NO3 Triossido di azoto Estremamente instabile
In aria pulita[1],[3] gli ossidi d'azoto più abbondanti sono NO ed NO
2, ma la loro presenza
viene incrementata considerevolmente a causa dall'attività umana, come è facile vedere dai dati riportati in tabella 1.2. A causa della sua estrema ossidabilità[2], NO non dovrebbe, infatti,
rinvenirsi in natura in quanto la sua formazione sarebbe immediatamente seguita dalla trasformazione in ossidi superiori.
La presenza del composto N2O in atmosfera è dovuta soprattutto all'attività biologica e
perciò non va soggetta a normative, tuttavia questa molecola risulta dannosa per l'ozono ed ha una vita media di 100-150 anni[1]. Nonostante infatti sia una specie chimica poco stabile[3]
Gf0
tabella 1.2 – concentrazioni di NOx in aria Aria puli ta a l iv ell o
de l s uol o T ipi c i live lli ba s erile v at i Pic c hi in aree u rbane ( NOMila no Los Ang e le sx)
µg/m3 ppm µg/m3 ppm µg/m3 ppm µg/m3 ppm
NO 0.75 0.6·10-3 3.7-5.6 (2-3)·10-3
NO2 1.9 1·10-3 7.5-9.4 (4-5)·10-3
450-500 0.24-0.27 7·103 3.75
Nell'atmosfera esiste in tracce: la sua percentuale nell'aria è di circa 5·10-7% in volume. E'
indicato con i nomi di: ossido di diazoto, ossido nitroso, ossidulo d'azoto, protossido d'azoto e gas esilarante; in effetti, se respirato per qualche minuto, provoca eccitazione, riso nervoso e gesti incoordinati fino alla perdita di conoscenza. Un tempo era usato come anestetico per piccole operazioni chirurgiche.
Le due specie N2O3 e N2O4 sono rintracciabili in atmosfera in concentrazioni talmente
piccole che la loro presenza ed i loro effetti possono essere ignorati. Riguardo N2O3 è bene
precisare che non solo è termodinamicamente instabile[4]
Gf
0
=135 kJ /mol
, ma non esiste puro se non allo stato solido per T < -100 °C. N2O4 esiste solo a basse temperature e dimerizzafacilmente a dare NO2.
L'ossido N2O5 si forma in aria in concentrazioni piccolissime ed è estremamente reattivo.
Sembra che esista in tracce nell'alta atmosfera. In acqua reagisce a dare acido nitrico. E' un composto termodinamicamente instabile[3] che facilmente si decompone in ossidi inferiori ed in
effetti, se analizzato ai raggi X allo stato solido, rivela una struttura ionica del tipo [NO2]+[NO3]-.
Il rarissimo NO3 è stato ottenuto[2] nel 1929 da Schumacher e Sprenger senza, tuttavia, che
si riuscisse ad isolarlo per via della sua estrema instabilità.
Ed infine N2O6 è nettamente distinto dal triossido visto sopra e non ne rappresenta un
dimero, come erroneamente potrebbe far pensare l'associazione con N2O4 ed NO2. Questa specie
si decompone rapidamente con perdita di ossigeno.
In conclusione le sole specie effettivamente presenti in atmosfera sono NO e NO2 e sono
proprio queste due specie che affliggono l'ambiente. Per brevità (e secondo la legge) vengono indicate con la sigla NOx e si stabilisce di indicare la concentrazione dei due ossidi come la somma
1.2 E
FFETTIN
OCIVI DEGLINO
XGli ossidi di azoto provocano effetti dannosi su tre fronti:
• Interazione con Ozono (smog fotochimico). Da un lato gli NOx interagiscono con
l'ozono della stratosfera[4] diminuendone la concentrazione in modo da ridurne
l'effetto assorbente nei confronti delle radiazioni ultraviolette del sole: NO + O3 → NO2 + O2 e NO2 + O → NO + O2; d'altra parte l'effetto più nocivo si
rivela all'altezza della troposfera[3],[5] dove, sotto l'azione della luce solare,
l'ozono viene prodotto: NO2 + hν → NO + O e successivamente O2 + O →
O3. L'ozono così formato reagisce con gli idrocarburi incombusti o
parzialmente combusti dovuti soprattutto ai motori delle automobili. Ne risultano delle complesse reazioni chimiche che portano a composti (tra cui ad es. perossiacilnitrati) pericolosi per la salute umana.
• Origine del fenomeno delle Piogge Acide[1],[3]. Quando gli NO
x vengono a contatto con
l'umidità atmosferica in presenza di luce solare vengono convertiti in acido nitrico che, successivamente, ricade al suolo provocando danni sia in aree urbane che agricole. Da non trascurare è la capacità di tali sostanze di percorrere grandi distanze e perciò di inquinare vaste zone; è noto infatti che negli USA le emissioni dovute al Midwest possono affliggere anche il New England e ed il Canada.
• Affezioni gravi delle vie respiratorie[3]. L'effetto degli ossidi d'azoto sull'uomo è
rappresentato in tab. 1.3; in sostanza, essi irritano gli alveoli polmonari e possono provocare riduzione della capacità respiratoria, emicrania, faringiti, laringiti, irritazione ad occhi, naso e gola. In soggetti sani sono stati riscontrati significativi effetti sulla salute già in presenza di 725 µg/m3 (0.37 ppm); per
valori di concentrazione di 7.5 mg/m3 (4 ppm) sono stati sufficienti 10 min di
esposizione perché il soggetto presentasse un aumento della resistenza delle vie respiratorie e 15 min per una diminuzione della capacità polmonare. Una esposizione prolungata può portare a edema polmonare[6].
In realtà si possono individuare altri effetti sull'ambiente correlati all'interazione degli ossidi d'azoto con altre sostanze chimiche (come gli ossidi di zolfo) o con organismi viventi (fitoplancton); per maggiori dettagli si veda [1] pagg. 7-8.
tabella 1.3 – effetti degli NOx sull'uomo[3]
1.3 F
ORMAZIONEDEGLIO
SSIDI DIA
ZOTO[7],[8]Gli ossidi di azoto di origine antropica sono essenzialmente dovuti ai processi di combustione e sono composti quasi completamente da NO (> 95%); la restante parte è costituita da NO2 (≈ 5%) ed in piccolissima parte da N2O.
I meccanismi attraverso cui si formano gli ossidi di azoto sono tre e vengono trattati qui di seguito.
1.3.1 Thermal NO
xVengono indicati come Thermal NOx quegli ossidi che si formano per ossidazione
dell'azoto contenuto nell'aria di combustione. Il meccanismo, proposto da Zeldovich, prevede la formazione di radicali di ossigeno dalla dissociazione di O2 nelle zone ad alta temperature e ricche
di ossigeno:
O2⇔2O⋅
O⋅N2⇔ NON
NO2⇔ NOO⋅
NOH ⇔ NOH
La seconda reazione è fortemente dipendente dalla temperatura e non avviene apprezzabilmente al di sotto dei 1800 °C. La quantità di ossidi formata mediante questo meccanismo dipende essenzialmente dalla temperatura massima locale di fiamma e dal tempo di residenza e, in minor misura, dalla concentrazione locale di O2. Questo si può osservare dal grafico seguente (figura 1.1).
In conclusione, per contenere la produzione di Thermal NOx si può pensare di diminuire la
concentrazione di azoto e di ossigeno nelle zone di massima temperatura, di ridurne il tempo di permanenza oppure di abbassare il picco di temperatura.
1.3.2 Fuel NO
xFonte di azoto può essere anche l'anello eterociclico di composti organici contenuti in combustibili quali carbone ed oli pesanti. Nel fronte di fiamma questi composti pirolizzano ed i prodotti vengono ossidati con formazione di intermedi (HCN e NH3) che successivamente reagiscono per dare N2 o NO in base alla disponibilità di ossigeno. Nonostante si abbia formazione di Fuel NOx a temperature più basse delle precedenti, il tenore di azoto presente nel
combustibile influenza la concentrazione degli ossidi in modo meno che proporzionale. Il fattore determinante risulta quindi essere la concentrazione di ossigeno.
1.3.3 Prompt NO
xL'interazione dell'azoto atmosferico e dei radicali idrocarburici (CH·) dovuti alla combustione provoca una rapidissima reazione all'interno della fiamma i cui prodotti sono detti Prompt NOx. Secondo Glassman si ha:
CHN2⇔ HCN N
CH2N2⇔ HCN NH
L'acido cianidrico viene poi ridotto per formare NO e quindi NOx. Questo tipo di
formazione non apporta comunque un contributo significativo in termini di concentrazioni finali.
figura 1.1 – Formazione di NOx in funzione del tempo di residenza e della temperatura di fiamma
1.3.4 Fattori che influenzano le emissioni di NO
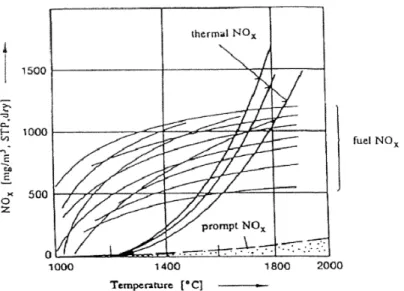
xDa quanto visto sopra possiamo concludere che i fattori che influenzano la formazione degli ossidi d'azoto sono la temperatura di combustione, il tempo di permanenza e la turbolenza. Per limitare le emissioni sono state sviluppate delle tecniche per il controllo della combustione e nel contempo sono state affinate le tecniche per l'abbattimento a posteriori. Nello schema riassuntivo, riportato in tabella 1.4, si notano le caratteristiche fondamentali dei tre diversi meccanismi di formazione, mentre nel grafico di seguito (fig. 1.2) si può osservare la dipendenza dalla temperatura nei tre casi.
Figura 1.2 - Formazione di NOx in funzione della temperatura.
Tabella 1.4 - Caratteristiche fondamentali dei tre meccanismi di formazione.
p rovenienza
de ll'a zo to zona di r e azione m e c can is mo difo rm azio ne gr ande zze c o n troll an ti ilp roces s o
aria interno della fiamma Thermal NOx
• temperatura di fiamma
• tempo di permanenza
• concentrazione di O2
combustibile fronte di fiamma Fuel NOx
• concentrazione di O2
• concentrazione di N2 nel
combustibile
aria interno della fiamma Prompt NOx
• temperatura di fiamma
• concentrazione di O2
L’emissione di questi inquinanti è causata soprattutto dall’ossidazione dei combustibili fossili quindi le sorgenti principali sono il traffico autoveicolare, le centrali termiche, termoelettriche e gli inceneritori urbani.
In ordine di importanza poi abbiamo vari processi industriali come la produzione di acido nitrico o adipico, le industrie di plastica, fertilizzanti, esplosivi, le industrie che usano HNO3 per trattamenti dei metalli e infine i fenomeni naturali come l’irradiazione solare e l’attività microbica del suolo. Nel paragrafo seguente vengono riportati alcuni valori riguardanti l'entità delle emissioni.
1.4 I
NQUINAMENTO DELL'
ARIA[12]L'inquinamento dell'aria esiste da quando esiste la civiltà umana; altrettanto antica è l'ammissione che esso costituisce un aspetto secondario inevitabile dell'attività umana. L'uomo respira in media circa 16 m3 d'aria al giorno e consuma circa 3 kg di cibo e di acqua e, suo
malgrado, non può fare a meno di utilizzare l'aria che lo circonda. Lo stesso vale per i prodotti alimentari, animali o vegetali che siano, che rimangono esposti all'aria inquinata. E per ultimi rimangono colpiti gli edifici ed i materiali lasciati in deposito all'aperto.
La definizione di inquinamento dell'aria più largamente accettata lo indica come l'eccessiva
concentrazione di materie estranee nell'aria, che agisce negativamente sul benessere dell'individuo e che arreca danni alla proprietà. Direttamente associata al problema delle quantità sopportabili è, ovviamente, la
durata dell'esposizione; anche i danni risentiti dalla vegetazione dipendono molto dalla durata dell'esposizione. Di conseguenza, la valutazione dei possibili effetti delle emissioni in atmosfera deve tenere conto tanto della concentrazione quanto della durata. Altro fattore importante è costituito dalle condizioni topografiche e da quelle climatiche. Le valli od i bacini geografici più grandi possono trattenere i contaminanti atmosferici. Per contro, i venti forti esercitano un'azione molto favorevole alla loro dispersione.
Di tutti i vari inquinanti atmosferici, in questo lavoro interessano solo gli NOx. In tabella 1.5
riportiamo i dati delle emissioni in riferimento agli ultimi trent'anni negli Stati Uniti. In tabella 1.6 i dati della ripartizione delle sorgenti di NOx in Italia. La tabelle dalla 1.7 riporta la distribuzione
delle emissioni nella regione Lombardia al 2003 (il maggiore dettaglio è dovuto alle nuove leggi).
Tabella 1.5 – Emissioni di NOx in USA[13]
1970 1975 1980 1985 1990 1995 2000
NOx
(Gton/y) 26,9 26,4 27,1 25,8 25,2 24,7 22,3
Tabella 1.6 – Ripartizione percentuale delle emissioni di NOx in Italia[3]
fon te perc ent uale
trasporti 51,0
centrali termoelettriche 27,9
industria 16,9
riscaldamento 4,2
Tabella 1.7 – Distribuzione percentuale delle emissioni di NOx in Lombardia nel 2003[14]
fon ti NOx (t/y) NOx (%)
Produzione energia e trasformazione combustibili 19.611 11
combustione non industriale 17.888 10
combustione nell'industria 39.653 22
processi produttivi 3.140 2
uso di solventi 20 0
trasporto su strada 80.592 44
altre sorgenti mobili e macchinari 18.324 10
trattamento e smaltimento rifiuti 2.073 1
agricoltura 1.687 1
altre sorgenti e assorbimenti 276 0
totale 183.262 100
La figura 1.3 mostra l'andamento medio giornaliero misurato in alcune stazioni di rilevamento in Toscana nel 2003.
Figura 1.3 – Andamento giornaliero della concentrazione di NOx in Toscana nel 2003[15]
Nelle figura 1.4 ed 1.5 si mostra l'andamento delle emissioni nell'arco degli anni relativa a due mesi molto diversi per clima e per attività umana: è interessante notare come i valori delle emissioni di NOx diminuiscano molto dopo l'attuazione delle leggi dei primi anni novanta.
Figura 1.4 – Valori di NOx misurati in Novembre a Milano[16]
1.5 A
SPETTI NORMATIVI1.5.1 Cenni storici
[9],[10]In Italia la prima legge che prende in considerazione l'inquinamento atmosferico è la legge ordinaria del Parlamento n° 615 del 13/07/66. All'art. 20 possiamo leggere: “Tutti gli stabilimenti
industriali [...] devono, in conformità al regolamento di esecuzione della presente legge, possedere impianti, installazioni o dispositivi tali da contenere entro i più ristretti limiti che il progresso della tecnica consenta la emissione di fumi o gas o polveri o esalazioni che, oltre a costituire comunque, pericolo per la salute pubblica, possono contribuire all'inquinamento atmosferico”. La legge ad ogni modo non fissa valori precisi per le
emissioni e si basa sull'idea di un intervento “a posteriori”. E' negli anni '70 che si delinea l'idea di prevenzione e che vengono definiti dei valori limite con il D.P.R. n° 1391 del 22 dicembre 1970 e con il D.P.R. n° 322 del 15 aprile 1971 (poi sostituito nel 1983). Il primo riporta valori di soglia precisi e tecniche ben chiare per la loro valutazione, tuttavia non si occupa di ossidi d'azoto; il secondo fissa un tetto per i valori di NOx pari a 0.30 ppm (0.56 mg/m3) ed una media giornaliera
di 0.10 ppm (0.19 mg/m3). Queste leggi comunque si propongono di misurare solo alcuni
inquinanti nel breve periodo e solo nel perimetro industriale.
Gli anni '80 vedono una radicale modifica nel concetto di emissione. In primo luogo vengono dilatati i tempi nei quali deve essere effettuato il controllo portandosi a verificare medie annuali; in seconda battuta si delineano dei ben definiti criteri per la valutazione della qualità dell'aria; infine vengono definiti gli “Standard di Qualità dell'Aria” (SQA) visti come “Limiti
massimi di accettabilità delle concentrazioni e di esposizione relativi ad inquinanti dell'aria nell'ambiente esterno”
(D.P.C.M. 28/03/83) e pensati come i valori massimi il cui superamento deve essere immediatamente contenuto mediante appropriati interventi. In buona sostanza si richiede che i limiti da rispettare siano quelli che salvaguardano la salute a prescindere dalla loro origine e dall'ubicazione di questa sul territorio nazionale. Con il D.P.R n° 203 del 24 maggio 1988 questi limiti sono stati ulteriormente ridotti: per gli NOx l'allegato I assegna il valore massimo di 200 mg/m3 alle “concentrazioni medie di 1 ora rilevate durante l'anno”. Nel 1988, inoltre, la direttiva CEE, recepita in Italia con il D.M. 8/5/1989, impone la riduzione delle emissioni del 10%, entro il 1993 e del 30% entro il 1998 (allegato 8).
1.5.2 Le norme degli anni '90
registrano gli effetti dei gas di scarico delle automobili. Dapprima viene promulgato il D.M. del 12 luglio 1990 che riporta le “Linee guida per il contenimento delle emissioni inquinanti degli impianti industriali
e la fissazione dei valori minimi di emissione” ed a seguire viene emanato il D.M. del 20 maggio 1991 nel
quale si individua un piano organizzativo per il monitoraggio delle aree urbane. Nell'Art. 1 del D.M. del 12 luglio 1990 si indicano le sue Finalità:
“1. Il presente decreto stabilisce:
a) le linee guida per il contenimento delle emissioni degli impianti esistenti come definiti dal [...]decreto n. 203/88 [...];
b) i valori di emissione minimi e massimi per gli impianti esistenti;
c) i metodi generali di campionamento, analisi e valutazione delle emissioni; d) i criteri per l'utilizzazione di tecnologie disponibili per il controllo delle emissioni;
e) i criteri temporali per l'adeguamento progressivo degli impianti esistenti.” Nell'Art. 3 (“Valori limite di emissione”) si legge:
“1. Le emissioni possono essere caratterizzate come segue:
a) per concentrazione: rapporto tra massa di sostanza inquinante emessa e volume dell’effluente gassoso (es. mg/m³);
b) per flusso di massa: massa di sostanza inquinante emessa per unità di tempo (es. g/h);
c) per fattore di emissione: rapporto tra massa di sostanza inquinante emessa e unità di misura specifica di
prodotto elaborato o fabbricato (es. kg/t; g/m)”.
In questi anni si comincia a guardare anche alle automobili come fonti di inquinamento (L. 15 gennaio 1992 n° 21) e possiamo vedere nella figura 1.6 come siano stati allo stesso tempo necessari ed efficaci gli interventi in merito.
Nella filosofia degli “Standard di Qualità dell'Aria” si inserisce il D.M. del 15 aprile 1994 il quale “stabilisce i criteri di individuazione degli stati di attenzione e di allarme in base ai quali adottare
provvedimenti per prevenire episodi acuti di inquinamento atmosferico”. Si indica inoltre molto chiaramente
che la rilevazione deve essere continuativa nell'arco delle 24 ore e che devono essere almeno il 50% delle stazione di rilevamento (tabella II dell'allegato I) a denunciare il superamento dei limiti: quanto sopra può essere utile per dare un'idea dei notevoli investimenti economici ed organizzativi che tali leggi hanno imposto sia all'industria che allo stato. Per gli NOx troviamo
indicati i suddetti valori di attenzione e di allarme per le medie orarie rispettivamente di 200 e 400 mg/m3.
Un approccio completamente diverso al problema della gestione e del controllo della qualità dell'aria si deve al recente recepimento delle norme comunitarie. Si attua, così, un vero e proprio
sovvertimento normativo con il passaggio da un'ottica di emergenza ad una pianificazione previdenziale. Il D.L. n° 351 del 4 agosto 1999 altro non è che l' “Attuazione della direttiva
96/62/CE in materia di valutazione e di gestione della qualità dell'aria” e definisce:
fig. 1.6 - Emissioni di NOx in Italia[11]
• all'art. 4 i “Valori limite, soglie di allarme e valori obiettivo” ed i margini di tolleranza;
• dall'art. 6 all'art. i 10 nuovi criteri per la “Valutazione della qualità dell'aria ambiente”
mediante la pianificazione di interventi volti al miglioramento ed al mantenimento della qualità dell'aria;
• all' Art. 11 una capillare “Informazione al pubblico”.
Con il D.M. n° 60 del 2 aprile 2002 si ha il “Recepimento della direttiva 1999/30/CE del
Consiglio del 22 aprile 1999 concernente i valori limite di qualità dell'aria ambiente per il biossido di zolfo, il biossido di azoto, gli ossidi di azoto, le particelle e il piombo e della direttiva 2000/69/CE relativa ai valori limite di qualità dell'aria ambiente per il benzene ed il monossido di carbonio”. Al Capo III e nell'Allegato II
sez. I si concretizzano le cifre dei valori da rispettare (si veda la tab. 1.8).
Nella sez. II si indica poi la “Soglia di allarme per il biossido di azoto” in “400 µg/m3 misurati su
tre ore consecutive in un sito rappresentativo della qualità dell’aria di un’area di almeno 100 km2 oppure in una
intera zona o un intero agglomerato, nel caso siano meno estesi”.
0 0,5 1 1,5 2 1980 1982 1984 1986 1988 1990 1992 1994 1996 1998 2000 2002
M
t
(dato
naz
ional
e)
obiettivo direttiva NEC (rec. Dlgs 171/04)
NO
xLe novità introdotte da questo decreto sono rappresentate, oltre che dai nuovi valori limite, dall'aver fissato valori sia a breve che a medio termine; dall'aver fissato limiti sia per la salute umana che per gli ecosistemi; dall'aver definito dei limiti temporali per l'adeguamento della qualità dell'aria ed infine dall'aver attribuito una fondamentale importanza all'informazione.
tabella 1.8
Valori limite per NO2 e NOx secondo il D.M. 60/2002
pe riodo d i m e diazione
v alo re li mi te m arg ine d i
to lleran za da ta a lla quale il v alo re li mi te deve esser e raggiunt o 1. valore limite orario per la protezione della salute umana 1 ora 200 µg/m 3 NO 2 da
non superare più di 18 volte per anno civile
50% del valore limite, pari a 100 µg/m3, al 19/7/99.
Tale valore è ridotto il 1° gennaio 2001 e successivamente ogni 12 mesi, per raggiungere lo 0% al 1° gennaio 2010
1° gennaio 2010
2. valore limite annuale per la protezione della
salute umana anno civile 240 µg/m
3 NO 2
50% del valore limite, pari a 100 µg/m3, al 19/7/99.
Tale valore è ridotto il 1° gennaio 2001 e successivamente ogni 12 mesi, per raggiungere lo 0% al 1° gennaio 2010 1° gennaio 2010 3. valore limite annuale per la protezione della vegetazione anno civile 30 µg/m3 NO x Nessuno 19 luglio 2001
1.5.3 Norme attuali
Il D.L. n° 171 del 21 maggio 2004 limita, in conformità alle direttive europee, le emissioni annuali nazionali di NOx a 990 kton, indicando il 2010 come ultimo anno in cui raggiungere tale
valore.
Attualmente è in vigore il D.L. n° 133 dell' 11 maggio 2005 che regola le emissioni dovute all'incenerimento dei rifiuti:
• Valori limite di emissione medi giornalieri: 200 mg/m3 (Allegato 1, paragrafo A, punto 1) • Valori limite di emissione medi su 30 minuti: 400 o 200 mg/m3 per il 100% e per il 97%
rispettivamente (Allegato 1, paragrafo A, punto 2)
secco e tenore di ossigeno di riferimento pari all'11% in volume nell'effluente gassoso secco.
![tabella 1.1 [1],[2] – Ossidi d'azoto](https://thumb-eu.123doks.com/thumbv2/123dokorg/7254939.81269/1.918.126.813.399.785/tabella-ossidi-d-azoto.webp)

![tabella 1.3 – effetti degli NO x sull'uomo [3]](https://thumb-eu.123doks.com/thumbv2/123dokorg/7254939.81269/4.918.230.711.248.816/tabella-effetti-no-x-uomo.webp)

![Figura 1.3 – Andamento giornaliero della concentrazione di NO x in Toscana nel 2003 [15]](https://thumb-eu.123doks.com/thumbv2/123dokorg/7254939.81269/9.918.227.714.637.943/figura-andamento-giornaliero-concentrazione-no-x-toscana.webp)
![Figura 1.4 – Valori di NO x misurati in Novembre a Milano [16]](https://thumb-eu.123doks.com/thumbv2/123dokorg/7254939.81269/10.918.166.774.146.501/figura-valori-di-no-misurati-novembre-milano.webp)
![fig. 1.6 - Emissioni di NO x in Italia [11]](https://thumb-eu.123doks.com/thumbv2/123dokorg/7254939.81269/13.918.183.753.295.668/fig-emissioni-di-no-x-in-italia.webp)