Comunicazione all’adunanza del 23 marzo 2012
Esiste una relazione tra l’aderenza alla terapia e
la progressione del glaucoma?
Massimo Vento
1, Gian Maria Pasinetti
2, Luigia Scudeller
3, Gemma Caterina Maria Rossi
1 1Clinica Oculistica, Università degli Studi di Pavia, Fondazione IRCCS Policlinico San Matteo, Pavia, 2
U.O. di Oculistica, Istituto Beato Palazzolo, Bergamo, e 3Laboratorio di Epidemiologia e Statistica, Fondazione IRCCS Policlinico San Matteo, Pavia, Italia
Esiste una relazione tra l’ aderenza alla terapia e la progressione del glaucoma?
Scopo. Valutare la relazione tra la progressione dell’alterazione del campo visivo e il tasso di aderenza alla
tera-pia registrato con Travatan Dosing Aid (TDA) nei pazienti glaucomatosi.
Materiali e metodi. Studio retrospettivo di 36 mesi. 35 pazienti con glaucoma primario ad angolo aperto in
monoterapia con Travoprost o con l’associazione fissa Travoprost/timololo, sono stati sottoposti a visita ocu-listica ed esame del campo visivo (CV) dal 2007 al 2009. L’aderenza è stata registrata tramite il TDA. L’associazione tra progressione dell’alterazione del CV (dal 2007 fino alla fine del periodo di follow-up) e i vari parametri, tra cui il più importante è stato il tasso di aderenza a 12 mesi è stata valutata mediante il test Chi-quadrato o il test di Fisher o il test Mann-Whitney come appropriato.
Risultati. La media (±SD) del tasso di aderenza dopo un mese di follow-up è stata del 71.9±27.8% e dopo dodici mesi del 76.8±20.9%. Nei 25 pazienti (71.4%) con CV stabile la mediana dell’aderenza è stata del 85% (IQR 75-97%), nei 10 pazienti (28.6%) con CV peggiorato la mediana è stata del 21% (IQR 9-45%) (p <0.001). Nessuna associazione è stata trovata tra la progressione del CV e una qualsiasi delle altre variabili (età, sesso, istruzione, acuità visiva, pressio-ne intraoculare basale e pressio-nel tempo, altre malattie oculari, tempo dalla diagnosi, tempo dal momento in cui la terapia in atto è stata iniziata, numero di terapie sistemiche concomitanti). I pazienti con almeno il 90% di aderenza non hanno avuto una progressione del danno, mentre il 43.5% di quelli con bassa aderenza sono peggiorati (p=0.01).
Conclusioni. I nostri dati suggeriscono che il tasso di aderenza alla terapia può giocare un ruolo nel danno
glau-comatoso e/o nella sua progressione, l’obiettivo pressorio quindi deve essere stabilito anche in base ad essa. Per conservare la funzione visiva sono da attuare tutti i modi per migliorare l’aderenza del paziente alla terapia.
There is a relationship between adherence to therapy and progression of glaucoma?
Purpose. To assess relation between visual field progression and adherence rate in glaucoma patients
using Travatan Dosing Aid (TDA).
Materials and methods. 36-month retrospective study. 35 primary open angle glaucoma patients on Travoprost
or Travoprost/Timolol fixed combination monotherapy were submitted to ophthalmic examination and to visual field (VF) test from 2007 to 2009. Adherence was recorded with TDA. The association between VF progression (from 2007 to the end of the follow-up period) and a number of predictors (adherence rates at 12 months) was
Results. The mean (±SD) adherence rates were 71.9±27.8% after one month of follow-up and 76.8±20.9% at twelve months. 25 (71.4%) patients with VF stable had a median adherence rate of 85% (IQ 75-97%); patients that worsened (n=10, 28.6%) recorded a median adherence of 21% (IQ 9-45%) (p<0.001). No association was found between VF progression and any of the other variables (age, sex, schooling, visual acuity, IOP at baseline and over time, other ocu-lar diseases, time since diagnosis and actual therapy, number of concomitant systemic therapies). Patients who were at least 90% adherent did not progressed, while 43.5% of the patients with lower adherence worsened (p=0.01).
Conclusions. Our data suggest that adherence rate may play a role in glaucomatous damage and/or
pro-gression; the target IOP therefore should be adjusted also by adherence rates. All means that can improve adherence are desirable and necessary to preserve visual function.
Introduzione
È noto che il glaucoma è una neuropatia cronica e progressiva del nervo ottico e che la cecità può veri-ficarsi nonostante la terapia [1-4]. I metodi standard di monitoraggio dell’evoluzione del glaucoma comprendono la valutazione della pressione intraoculare (PIO), la valutazione del disco ottico e del campo visivo (CV). Gli oculisti hanno evidenziato il ruolo svolto dalla presenza di danno avanzato del disco ottico e / o del CV alla diagnosi [1, 5-6] nella progressione verso la cecità. Il rischio invece negli occhi senza tali alterazioni al momento della diagnosi ma con ipertensione oculare è più basso, ma aumenta con la durata del follow-up [7]. C’è una forte evidenza che la PIO giochi un ruolo importante in questa neuropatia ed è stato dimostrato che abbassare la PIO riduce il rischio di progressione [8-12]. La relazione tra pressione intraoculare elevata e neuropatia ottica glaucomatosa è molto variabile; ci sono questioni irrisolte riguardanti il rapporto tra il controllo della PIO e il danno del campo visivo. In discussione è anche quale aspetto della PIO sia più importante nella progressione: la PIO media o le fluttuazioni nel tempo? [13-15] Tuttavia la pressione intraoculare elevata è un fattore di rischio per la progressione della malattia e attualmente la sua riduzione rappresenta l’intervento terapeutico princi-pale [16]. La pratica clinica ha mostrato che nel momento in cui il danno glaucomatoso peggiora, i pazienti richiedono un ulteriore abbassamento della PIO per prevenirne la progressione [17-19]. Si può fare affidamento su una pressione con valori entro la norma misurata durante le visite? I pazienti di solito sono aderenti nei giorni prima della visite previste e pertanto, gli oculisti generalmente rile-vano valori di PIO ben controllati, ma i pazienti assumono regolarmente le proprie gocce? La scarsa aderenza può indurre fluttuazioni della pressione intraoculare e/o un suo inadeguato controllo con con-seguente progressione della malattia. Nel 1985, Kass ha affermato che la scarsa compliance del pa-ziente alla terapia prescritta può essere un fattore limitante grave nella gestione del glaucoma [20]. L’equazione bassa PIO=prevenzione della progressione del danno visivo non è sempre vera. Visto che la PIO non è sempre associata a cambiamenti del campo visivo, il valore della PIO non è un parametro ottimale per determinare l’effetto dell’aderenza sulla storia naturale della malattia. Il glaucoma è una malattia multifattoriale in cui sia i pazienti che i medici svolgono un ruolo importante; si pensa che la scarsa compliance e la bassa aderenza al trattamento possano rappresentare fattori di rischio per la progressione della malattia, ma finora nessuna prova definitiva è stata trovata a riguardo.
Scopo del lavoro
Valutare la relazione tra la progressione dell’alterazione del campo visivo ed il tasso di aderenza alla terapia registrato con Travatan Dosing Aid (TDA) nei pazienti glaucomatosi.
Materiali e metodi
È stato effettuato uno studio retrospettivo di coorte della durata di 36 mesi, approvato dal Comitato Etico Locale. Lo studio si basa sui dati provenienti da 35 pazienti affetti da glaucoma primario ad an-golo aperto, facenti parte di un campione più ampio di 59 soggetti [21] (in quanto solo 35 avevano 12 mesi di follow-up dei dati), trattati o con Travoprost o con la combinazione fissa Travoprost/timololo e monitorati con TDA (dal 2007 al 2009). Il Travatan Dosing Aid (TDA, Alcon Research Labs, Fort Worth, TX) è uno degli strumenti utilizzati per il monitoraggio elettronico [22] dell’aderenza alla tera-pia prescritta ed è considerato un metodo valido e affidabile [23]. Esso ricorda ai pazienti quando somministrare il collirio ipotonizzante (sia con un richiamo visivo, sia con uno acustico), fornisce le percentuali di aderenza e la cronologia delle somministrazioni. Le caratteristiche, la precisione, l’efficacia, i vantaggi e gli svantaggi di TDA sono già stati studiati e descritti [24-25].
Nei nostri pazienti la diagnosi di glaucoma è stata definita in base a: PIO>21 mmHg in almeno due visite consecutive, al momento della prima diagnosi, escavazione patologica della testa del nervo otti-co all’esame del fundus oculi e presenza di un difetto glauotti-comatoso o sospetto glauotti-comatoso in alme-no tre esami affidabili del campo visivo eseguiti in giorni diversi con tecnica Humphrey 24-2 soglia piena. I pazienti assumevano la stessa terapia topica dal 2006.
L’esaminatore dei CV (GCR), non era a conoscenza dei tassi di aderenza registrati; i CV sono stati giudicati clinicamente alla fine del periodo di osservazione dei dodici mesi (2009) e classificati come stabile o progredito. Il CV è stato considerato stabile se: MD, PSD e stadio del glaucoma (è stato ap-plicato il sistema di stadiazione: Glaucoma Staging System di Brusini-GSS 2 [26]) erano rimasti stabi-li o migstabi-liorati rispetto ai valori iniziastabi-li, negstabi-li altri casi il CV è stato considerato progredito. Il tasso di aderenza è stato definito come la percentuale di instillazione delle gocce registrata nei 12 mesi dal TDA. Al momento non esiste uno standard consensuale riguardo l’aderenza adeguata, infatti mentre alcuni studi considerano accettabili tassi superiori all’80%, altri considerano obbligatori tassi superiori al 95% [27]. Il glaucoma è una condizione cronica che richiede una terapia quotidiana per conservare la visione, per questo motivo in questo studio abbiamo scelto di definire pazienti aderenti solo coloro i quali avevano un TDA registrato >90%. I campi visivi eseguiti ogni 4-6 mesi dal 2005 al 2009 sono stati inclusi per l’analisi. Riepilogando: la valutazione della progressione della malattia è stata basata sui campi visivi dal 2005 al 2009 mentre l’aderenza è stata basata sui dati di un anno di utilizzo del TDA corrispondente ai dati del campo visivo dell’ultimo anno.
Analisi statistica
Statistiche descrittive sono state prodotte per le caratteristiche demografiche, cliniche e di laboratorio. La media e la deviazione standard sono state utilizzate per le variabili distribuite normalmente, la me-diana e i quartili (IQR) invece per le variabili non distribuite normalmente. Il test T di Student (o il Mann-Whitney per le distribuzioni asimmetriche) è stato utilizzato per confrontare le variabili quanti-tative, mentre il test di Pearson’s χ2 (o il Fisher exact, quando appropriato) per le variabili categoriche. In particolare, è stata valutata per ogni occhio l’associazione tra l’evoluzione del CV (variabile
dipen-dente) e un numero di variabili (età, sesso, istruzione, acuità visiva, pressione intraoculare basale e nel tempo, altre malattie oculari, tempo dalla diagnosi, tempo dal momento in cui la terapia in atto è stata iniziata, numero di terapie concomitanti sistemiche assunte, tasso di aderenza a 12 mesi). L’aderenza è stata classificata cattiva quando <50%, intermedia quando tra 51% e 89% e buona quando >90%. Un test per il trend è stato utilizzato per valutare l’associazione tra l’aderenza e la progressione del danno. Inoltre, è stato preparato un modello di regressione logistica univariata per il pannello di dati (al fine di tenere in considerazione che il paziente stesso poteva contribuire per 2 occhi) con l’obiettivo di valutare l’associazione tra aderenza, come variabile lineare e probabilità che il campo visivo fosse stabile.
Risultati
Tutti i pazienti erano caucasici, l’età media era 68.5 (±11 DS) anni. La PIO media prima di iniziare il trattamento era di 23.4±4.3 mmHg. Durante una visita di routine i pazienti hanno ricevuto un campio-ne gratuito del TDA, e in quel momento la pressiocampio-ne intraoculare media era 17.1±3.4 mmHg; 12 mesi dopo la PIO era 16.0±2.6 mmHg. In entrambe le visite, la PIO era ridotta rispetto ai valori pre-trattamento (p<0.001 e p=0.007 rispettivamente), ma non c’era alcuna differenza di PIO tra coloro i quali avevano il CV stabile e quelli che lo avevano peggiorato nel tempo (Tabella 1).
Il tasso medio di aderenza è stato 71.9 (±27.8% DS) dopo un mese di follow-up e 76.8 (±20.9%) dopo dodici mesi di follow-up. Per ogni paziente sono stati considerati 7-8 campi visivi affidabili. Nessuno dei pazienti ha mostrato discrepanze tra i 2 occhi (cioè i campi visivi erano progrediti o stabili in entrambi gli occhi).
In 25 pazienti (72.4%) il CV è rimasto stabile: in questi soggetti la mediana dell’aderenza era dell’85% (IQR 75-97%), in 10 pazienti (28.6%) il CV è peggiorato, con una mediana dell’aderenza del 21% (IQR 9-45%) (p<0.001). Il test per il trend tra il CV stabile e l’aderenza è stato altamente si-gnificativo (p<0.001). Non è stata trovata nessuna associazione tra la progressione del campo visivo e una qualsiasi delle altre variabili (età, sesso, istruzione, acuità visiva, PIO basale e nel tempo, altre malattie oculari, tempo dalla diagnosi, tempo dal momento in cui la terapia in atto è stata iniziata, nu-mero di terapie sistemiche concomitanti assunte) (Tabella 1).
Da notare che dei 12 pazienti (34.3%) che avevano almeno il 90% di aderenza, nessuno ha avuto una progressione del danno visivo, mentre dei 23 pazienti (65.7%) con aderenza più bassa 10 (43.5%) hanno avuto una progressione (p=0.01). Alla regressione logistica, il CV stabile è risultato fortemente associato all’aderenza (Odds Ratio=2.25, 95% IC 1.7-3.0, p<0.001).
Discussione
Nel 2002, Oliver e colleghi in uno studio di coorte retrospettivo di 34 anni, hanno esaminato 295 pazienti seguiti da oftalmologi del territorio e hanno sottolineato che la pressione intraoculare media in terapia nei pazienti con danno progressivo verso la cecità era inferiore o simile in confronto ai pazienti che non avevano progressione del danno [5]. Questo significa che l’abbassamento della pressione intraoculare non impedisce la progressione del glaucoma?
Pochi studi hanno seguito i pazienti con glaucoma fino alla cecità [1-4, 19].
Alcuni studi prospettici randomizzati hanno associato la PIO e la progressione del campo visivo. Molti hanno scoperto che l’abbassamento della pressione intraoculare era associato ad una minore progres-sione del danno del campo visivo [10, 17-18] in altri invece tale correlazione non è emersa [3, 28-29].
Il Normal Tension Glaucoma Study ha evidenziato che un minor numero di pazienti ha avuto una progres-sione del danno visivo quando la PIO è stata ridotta del 30% [10, 17]. L’Advanced Glaucoma Intervention Study (AGIS) ha trovato che i pazienti con pressione intraoculare media di 12 mmHg avevano un CV sta-bile, invece i pazienti con pressione intraoculare media di 14 mmHg o superiore (circa il 75% dei pazienti dello studio), avevano un CV in progressione [18]. L’Early Manifest Glaucoma Trial nel 2007 ha dichiara-to che il trattamendichiara-to ha una forte influenza sulla progressione del danno e anche altri fatdichiara-tori quali esfolia-zione, malattia bilaterale, età avanzata, MD, ed emorragie del disco ottico sono importanti per la progres-sione [30]. Altri studi hanno trovato che la variabilità della presprogres-sione intraoculare era più alta in pazienti con danno progredito [5, 15]. Il tasso di aderenza alla terapia prescritta può avere un ruolo nel controllo delle fluttuazioni della PIO? Possiamo rilevare se i pazienti aderenti hanno una minore progressione del danno visivo? Il presente studio ha cercato di dare risposta a queste domande. Il nostro studio si differenzia dagli altri pubblicati sul TDA [31-32] per molti aspetti: è retrospettivo; non c’è stato un rigido protocollo di trattamento con obiettivi pressori fissi, non c’è stata randomizzazione ma ha avuto un follow-up lun-go, la dimensione del campione è però troppo piccola per trarre conclusioni definitive. Considerato ciò, i nostri dati suggeriscono che esclusi i fattori non pressori, come l’insufficienza vascolare e la neurodege-nerazione, il tasso di aderenza potrebbe essere responsabile del danno glaucomatoso e/o della sua pro-gressione. Dal momento che l’obiettivo pressorio è una pietra miliare della moderna pratica clinica [16], dovrebbero essere prese in considerazione terapie alternative indipendenti dalla collaborazione del pa-ziente (ad esempio la trabeculoplastica con Argon Laser o l’intervento chirurgico) nei pazienti poco ade-renti alla terapia poiché altrimenti essi non raggiungono l’obiettivo pressorio.
In conclusione, se il tasso di aderenza influenza direttamente la progressione del campo visivo, come i nostri dati sembrano indicare, sono auspicabili tutti quei metodi per migliorare l’aderenza e conservare dunque la funzione visiva. Sarebbe auspicabile che venissero effettuati altri studi come il nostro con un disegno scientifico più solido (studio prospettico, campione più grande, ecc).
Tabelle e figure
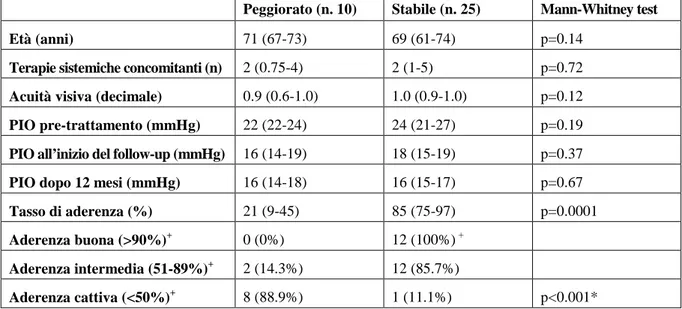
Tabella 1. Confronto tra le variabili e il campo visivo. I dati sono espressi come mediana e IQR e come frequenza assoluta e percentuale (Abbreviazioni: *= test per il trend).
Peggiorato (n. 10) Stabile (n. 25) Mann-Whitney test
Età (anni) 71 (67-73) 69 (61-74) p=0.14
Terapie sistemiche concomitanti (n) 2 (0.75-4) 2 (1-5) p=0.72
Acuità visiva (decimale) 0.9 (0.6-1.0) 1.0 (0.9-1.0) p=0.12
PIO pre-trattamento (mmHg) 22 (22-24) 24 (21-27) p=0.19
PIO all’inizio del follow-up (mmHg) 16 (14-19) 18 (15-19) p=0.37
PIO dopo 12 mesi (mmHg) 16 (14-18) 16 (15-17) p=0.67
Tasso di aderenza (%) 21 (9-45) 85 (75-97) p=0.0001
Aderenza buona (>90%)+ 0 (0%) 12 (100%) +
Aderenza intermedia (51-89%)+ 2 (14.3%) 12 (85.7%)
Bibliografia
1. Hattenhauer M, Johnson D, Ing H. The probability of blindness from open-angle glaucoma. Ophthalmology 1998;105:2099-2104. 2. Grant WM, Burke JF. Why do some people go blind from glaucoma? Ophthalmology 1982;89:991-998.
3. Kwon YH, Kim CS, Zimmerman MB et al. Rate of visual field loss and long-term visual outcome in primary
open-angle glaucoma. Am J Ophthalmol 2001;132:47-56.
4. Molteno ACB, Bosma NJ, Kittelson JM. Otago glaucoma surgery outcome study. Long-term results of trabe-culectomy 1976–1995. Ophthalmology 1999;106:1742-1750.
5. Oliver JE, Hattenhauer MG, David DH et al. Blindness and glaucoma: a comparison of patients progressing to blind-ness from glaucoma with patients maintaining vision. Am J Ophthalmol 2002;133:764-772.
6. Chen PP. Blindness in patients with treated open angle glaucoma. Ophthalmology 2003;110:721-733.
7. Weinreb R, Friedman D, Fechtner R et al. Risk assessment in the management of patients with ocular hyper-tension. Am J Ophthalmol 2004;138:458-467.
8. Le A, Mukesh BN, McCarty CA et al. Risk factors associated with the incidence of open-angle glaucoma: the
visual impairment project. Invest Ophthalmol Vis Sci 2003;44:3783-3789.
9. Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthal 1998;126:487-497. 10. Collaborative Normal-Tension Glaucoma Study Group. The effectiveness of intraocular pressure reduction in the
treatment of normal-tension glaucoma. Am J Ophthalmol 1998; 126:498-505.
11. Gordon MO, Beiser JA, Brandt JD et al. The Ocular Hypertension Treatment Study: baseline factors that predict the onset of primary open-angle glaucoma. Arch Ophthalmol 2002;120:714-720,829-830.
12. Leske MC, Heijl A, Hussein M, et al. Factors for glaucoma progression and the effect of treatment: the Early Manifest Glaucoma Trial. Arch Ophthalmol 2003;121:48-56.
13. Bengtsson B, Leske MC, Hyman L et al. Early Manifest Glaucoma Trial Group. Fluctuation of intraocular pressure and glaucoma progression in the Early Manifest Glaucoma Trial. Ophthalmology 2007;114:205-209.
14. Nouri-Mahdavi K, Hoffman D, Coleman AL et al. Predictive factors for glaucomatous visual field progression in the Advanced Glaucoma Intervention Study. Ophthalmology 2004;111:1627-1635.
15. Asrani S, Zeimer R, Wilensky J et al. Large diurnal fluctuations in intraocular pressure are an independent risk factor in patients with glaucoma. J Glaucoma 2000;9:134-142.
16. EGS Terminology and guidelines for glaucoma, 3rd ed. Dogma, Savona, IT, 2008.
17. Collaborative normal-tension glaucoma study group. The effectiveness of intraocular pressure reduction in the treatment of normal-tension glaucoma. Am J Ophthalmol 1998;126:498-505.
18. AGIS investigators. The AGIS study: The relationship between control of intraocular pressure and visual field deterioration. Am J Ophthalmol 2000;130:429-440.
19. Parc C, Johnson DH. Long-term outcome of glaucoma filtration surgery. Am J Ophthalmol 2001;132:27-35. 20. Kass MA. Compliance and prognosis in glaucoma (editorial). Arch Ophthalmol 1985;103:504.
21. Rossi GCM, Pasinetti GM, Scudeller L et al. Monitoring adherence rates in glaucoma patients using Travatan Dosing Aid. A six months study comparing patients on Travoprost 0.004% and patients on Travoprost 0.004%/Timolol 0.5% fixed combination. Expert Opin Pharmacother 2010;11:499-504.
22. Farmer KC. Methods for measuring and monitoring medication regimen adherence in clinical trials and clini-cal practice. Clin Ther 1999;21:1074-1090.
23. Friedman DS, Jampel HD, Congdom NG et al. The Travatan Dosing Aid accurately records when drops taken.
Am J Ophthalmol 2007;143:699-701.
24. Flowers B, Wand M, Piltz-Seymour J et al. Patients’ and physicians’ perception of the Travoprost Dosing Aid: an open-label, multicenter study of adherence with prostaglandin analogue therapy for open angle glaucoma or ocular hypertension. Clin Ther 2006;28:1803-1811.
25. Cronin TH, Kahook MY, Lathrop KL et al. Accuracy and performance of a commercially available Dosing Aid. Br J Ophthalmol 2007;91:497-499.
26. Brusini P, Filacorda S. Enhanced Glaucoma Staging System (GSS 2) for classifying functional damage in glaucoma. J Glaucoma 2006;15:40-46.
27. Osterberg L, Blaschke T. Adherence to medication. N Engl J Med 2005;353:487-497.
28. Martinez C, Chauhan BC, Nicolela MT et al. Intraocular pressure and progression of glaucomatous visual field loss. Am J Ophthalmol 2000;129:302-308.
29. Tezel G, Siegmund KD, Trinkaus K et al. Clinical factors associated with progression of glaucomatous optic disc damage in treated patients. Arch Ophthalmol 2001;119:813-818.
30. Leske MC, Heijl A, Hyman L et al. Predictors of long-term progression in the Early Manifest Glaucoma Trial. Ophthalmology 2007;114:1965-1972.
31. Okeke CO, Quigley HA, Jampel HD et al. Interventions improve poor adherence with once daily glaucoma medica-tions in electronically monitored patients. Ophthalmology 2009;116:2286-2293.
32. Okeke CO, Quigley HA, Jampel HD et al. Adherence with topical glaucoma medication monitored electroni-cally. The Travatan Dosing Aid Study. Ophthalmology 2009;116:191-199.