5 Campionamento e analisi delle acque
5.1 Introduzione
Lo scopo della presente tesi, come già descritto nel capitolo introduttivo è finalizzato alla definizione quantitativa delle risorse idriche superficiali e sotterranee del bacino idrografico del Fiume Cecina, alla caratterizzazione idrogeochimica delle risorse stesse (qualità delle acque), alla identificazione dei rischi cui le risorse sono sottoposte a causa delle attività antropiche.
Prima di organizzare le campagne di rilevamento ed acquisizione diretta dei dati è stato necessario reperire, studiare e sistematizzare le documentazioni esistenti, al fine di poter mirare le campagne all’identificazione ed allo studio di fenomeni in rapida evoluzione sfruttando appieno le informazioni derivanti dai precedenti lavori. Per questo motivo sono stati consultati il Dott. S. Grassi e il Dott. P. Squarci, autori di numerose pubblicazione effettuate sulla zona di studio. (Celati R., Grassi S., et al., 1987); (Capazzoli P., Rossi S., et al., 1996); (Barghigiani C., 2001); (Pennisi M., Gonfiantini R., et al., 1999). La maglia di campionamento è stata scelta anche in base alle loro indicazioni.
5.2 Metodo di campionamento
In base alle considerazioni descritte nel capitolo precedente, sono stati effettuati tre campionamenti in tre diversi periodi, nei mesi tra Settembre e Dicembre. Questi campionamenti corrispondevano ai periodi di magra e di morbida. La scelta di affrontare tre periodi di campionamento si è basato sulla disponibilità economica e sulle condizioni meteorologiche verificatesi nell’anno.
La prima campagna di campionamento è durata dal 17 settembre al 7 ottobre 2003 e ha avuto lo scopo di determinare le caratteristiche chimico-fisiche delle acque durante il periodo di minima portata. In questa campagna data la mancanza di acqua sono stati scelti tutti i possibili punti di campionamento e sono: 6 punti di campionamento sul fiume Cecina, 4 punti sul torrente Possera e infine per una
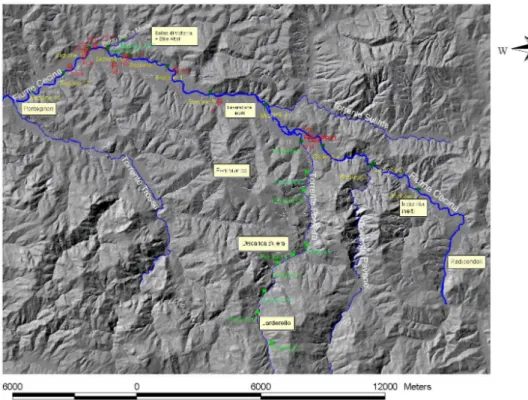
valutazione sulle acque sotterranee sono stati campionati 5 pozzi della cacciatina (proprietà Solvay), 2 pozzi della società Eti, 1 pozzo della società Altair, 1 pozzo privato e 3 pozzi dell’ASA. I 23 siti di campionamentosono riportati nella mappa di figura 5.1.
La seconda campagna è stata effettuata nel periodo dal 9 ottobre al 12 novembre 2003, in questa fase sono stati campionati alcuni punti in più per l’arrivo delle prime piogge (3 punti in più sul torrente Possera, 1 pozzo della cacciatina diverso dalla prima campagna per impossibilità di accesso ed in più un piezometro privato); è stata fatta questa campagna allo scopo di valutare eventuali variazioni di composizione chimica in funzione del tempo. I 27 siti di campionamento sono riportati nella mappa di figura 5.1.
La terza campagna è stata svolta nel periodo da 12 novembre al 18 dicembre, durante il periodo di morbida, in questa fase sono stati campionati ulteriori punti, rispetto alla campagna precedente, data la presenza di acqua (9 punti in più sul fiume Cecina, 2 in più sul Possera, ed il pozzo 2 non campionato per impossibilità di accesso). I 35 siti di campionamento sono riportati nella mappa di figura 5.1.
I pozzi, escluso durante la prima campagna, sono stati campionati sempre nel periodo finale di ogni campagna e con un certo ritardo rispetto al Cecina e al Possera, questo perché le acque superficiali sono direttamente ed immediatamente influenzate dalle condizioni atmosferiche, mentre le acque del sottosuolo variano con un certo ritardo in funzione del regime delle precipitazioni.
Il campionamento dei pozzi è stato effettuato dopo un periodo sufficientemente lungo da permettere lo spurgo dei tubi. Occorre precisare, comunque, che la maggioranza dei pozzi campionati sono pozzi in continua erogazione.
Per quanto riguarda il fiume Cecina e i suoi affluenti sono stati campionati nei punti di maggior scorrimento. In genere, quando era possibile, nel punto di mezzo della sezione.
Per ogni campione sono stati prelevati:
• n. 2 bottiglie di polietilene da 125 ml di acqua “tal quale”. Queste aliquote
sono utilizzate per le determinazioni di Cl, SO4, NO3, B, isotopi del deuterio,
ossigeno e del boro.
• n. 1 bottiglia di polietilene da 50 ml di acqua filtrata (filtro da 0,45) ed
acidificata con acido cloridrico (1 ml di HCl 1: 1). Questa aliquota si usa per la determinazione di Ca, Mg, Na, K.
• n. 1 bottiglia di polietilene da 50 ml di acqua “tal quale” ed acidificata con
acido nitrico (1 ml di H2SO4 1:1). Questa aliquota si usa per la
determinazione del COD.
• n. 1 bottiglia di vetro scuro da 125 ml di acqua “tal quale”. Questa aliquota è
utilizzata per la determinazione dell’NH4+.
• n. 1 bottiglia di vetro scuro da 125 ml di acqua filtrata (filtro da 0,45) ed
acidificata con acido nitrico (1 ml di HNO3 1:1). La bottiglia è stata
precedentemente lavata in laboratorio con HNO3 e acqua deionizzata. Questa
aliquota si usa per la determinazione di Hg.
Le bottiglie sono state avvinate e poi riempite fino all’orlo, per evitare il contatto con l’aria che potrebbe alterare la chimica delle acque. Nella attesa di essere portate in laboratorio sono state tenute in un frigorifero portatile, mentre in laboratorio nella attesa di essere analizzate sono state mantenute in frigorifero.
5.3 Determinazione dei parametri in campagna
Le modalità di prelievo e conservazione sono state scelte in funzione del carattere degli esami analitici da eseguire, dalla natura dell’acqua, delle variazioni delle sue caratteristiche nel tempo e delle variazioni di portata del deflusso.
Il campionamento delle acque è stato condotto in modo tale che le loro caratteristiche chimiche non si modifichino nel tempo che intercorre tra il campionamento e l’analisi in laboratorio. Per questi motivi, nel limite del possibile, l’esame dei campioni sono state effettuate immediatamente dopo il prelievo, altrimenti la conservazione del campione per tempi prolungati può determinare nell’analisi chimiche delle interferenze analitiche. (Massaroni Rovere, 1987). Inoltre, sono state effettuati direttamente in campo le misure di quei parametri che non possono essere conservati inalterati.
Figura 5.1 – Il corso del fiume Cecina, area di indagine.
5.3.1 Alcalinità
L’alcalinità di un’acqua esprime la presenza di bicarbonati, carbonati e idrati. Molte acque sono però considerate alcaline se contengono anidride carbonica libera che al contatto con l’acqua produce acido carbonico.(Massaroni Rovere, 1987)
L’alcalinità è determinata con un
microdosimetro titolando 1 ml di campione con HCl 0,1N, ed usando come indicatore il metilarancio (viraggio dal giallo all’arancio). I ml di HCl consumati danno il valore di alcalinità. La titolazione è stata eseguita 3 volte ed è stata considerando il valore medio.
Il microdosimetro (figura 5.2) date le sue
dimensione è facilmente trasportabile in campo, attraverso l’utilizzo di una valigetta metallica, nella quale sono contenuti oltre al microdosimetro anche l’HCl 0,1N e il metilarancio con due pipette eppendorf da 1 ml (per il campione) e da 25 ml (per il metilarancio).
5.3.2 Conducibilità
L’acqua pura è un pessimo conduttore di corrente, ma bastano piccole quantità di sali disciolti in essa per aumentarne la conducibilità. La circolazione della corrente nell’acqua avviene con il movimento degli ioni salini verso gli elettrodi, per questo si parla di conducibilità ionica. I valori vengono misurati generalmente in microsiemens per centimetro ( S/cm), oppure in S/cm ed in ohm 1*cm 1.
Poiché la conducibilità dipende fortemente dalla temperatura, è necessario stabilire una temperatura di riferimento alla quale devono essere rilevati i valori di conducibilità, questa è generalmente 20º o 25º.
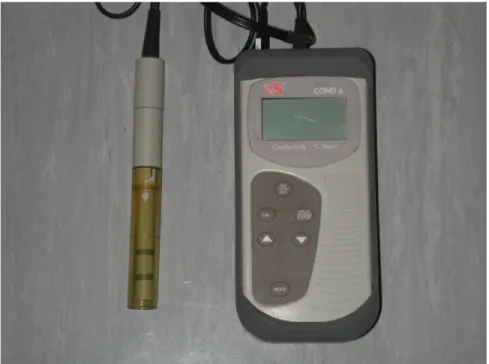
Prima di ogni giorno di campionamento il conducimetro veniva tarato con due soluzioni standard: una da 1413 S/cm e una da 12880 S/cm. La conducibilità è stata misurata direttamente nel fiume, mentre per i pozzi in un recipiente, dopo che i pozzi erano stati spurgati.
Il modello da noi utilizzato è l’XC COND 600 (figura 5.3), con il quale era possibile misurare anche la temperatura dell’acqua.
5.3.3 PH
Le acque naturali hanno generalmente pH vicini a 7, mentre si hanno valori maggiori per acque che circolano in rocce calcaree e minori nel caso di rocce silicee o povere di carbonato di calcio.
Il pH ha un ruolo importantissimo nella solubilità dei vari ioni. Come per il conducimetro ogni giorno di
campionamento era effettuata la taratura dello strumento con due soluzioni standard: pH =7 e pH = 4.
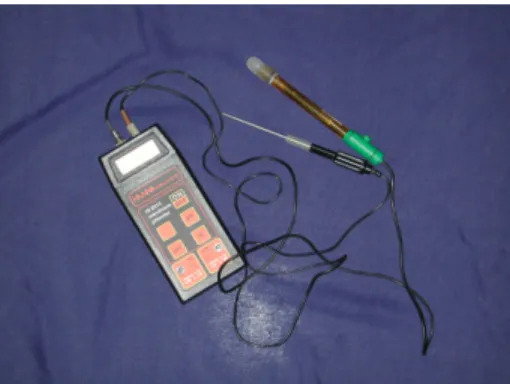
La misura del pH (figura 5.4) nel lavoro di campagna è stata fatta con un HI 8314 membrane pHmeter.
5.3.4 Temperatura
La conoscenza della temperatura è determinante perché questa influenza il pH, la conducibilità e la solubilità dei sali disciolti. Inoltre può dare informazioni sui mescolamenti di acque diverse. Le acque superficiali possono subire escursioni di temperatura legate alle vicende stagionali, in quanto influenzate dalla temperatura esterna. In acque di superficie di scarsa profondità sono rilevabili anche variazioni di temperatura diurne. Le acque di falda presentano temperature indipendenti dalle oscillazioni stagionali. (Massaroni Rovere, 1987)
La temperatura dell’acqua è stata misurata al momento del campionamento, insieme alla temperatura dell’aria, utilizzando un termometro - pHmetro portatile HI 8314 membrane pHmeter (figura 5.4).
5.3.5 Ossigeno disciolto
L’ossigeno disciolto è un parametro significativo in un’acqua superficiale, è la condizione indispensabile alla vita dei pesci e di ogni altro organismo acquatico. La sua concentrazione è, infatti, uno degli indici più significativi della purezza di un corso d’acqua, ed è influenzato sia dalla natura e dalla quantità dell’ossigeno presente, che dalla temperatura, dall’attività batterica, dai processi di fotosintesi (Massaroni Rovere, 1987). L’ossigeno disciolto è stato misurato utilizzando un HI 9142 portable dissolved oxygen meter (figura 5.5). Anche per questo strumento come per il conducimetro ed il pHmetro è stato utilizzato la soluzione standard per la taratura prima di ogni giorno di campionamento.
Figura 5.5 – Ossimetro.
Le misure sopra descritte e misurate direttamente al momento del campionamento sono riportate in tabella 5.1.
Da un rapido esame della tabella 5.1, risulta che:
• La temperatura massima delle acque registrata durante la prima campagna è
(25,7ºC) è quello del campione FC 9, una sezione del fiume Cecina, mentre la minima (15,2ºC) è quello del campione PP 39, un pozzo della zona di Puretta di proprietà dell’ASA. Per le due campagne successive, soprattutto per l’ultima si nota una diminuzione delle temperature, sia per il fiume che per i pozzi.
• Il pH per la prima campagna ha un range di variabilità tra 6,61 dello scarico e
8,07 della sezione 14 del fiume Cecina. Per la seconda campagna il pH varia tra 7,01 del campione A1, piezometro situato nel campo pozzi ASA Puretta (spurgato con una pompa fornita dal proprietario), mentre il valore più alto è di 8,30 del campione FP 6, sezione del torrente Possera, punto di confluenza con il fiume Cecina. Nella terza campagna il valore più basso rilevato di pH è di 6,98 del campione A1, come nella campagna 2, mentre il valore maggiore misurato è di 8,39 del FP 6, anche questa volta come la campagna precedente. Quello che si evidenzia dalla tabella è l’aumento del pH nell’ultima campagna.
• Le acque analizzate nella prima campagna presentano valori di conducibilità
variabili tra 634 S/cm del campione FC 3, sezione del torrente Pavone alla confluenza con il fiume Cecina e 8910 S/cm del campione FC 14, sezione del fiume Cecina a valle delle centrali chimiche di Saline di Volterra. Anche nella seconda Campagna il valore di minima conducibilità corrisponde al campione FC 3 con un valore di 604 S/cm e quello di massima a FC 14 con 6430 S/cm. Tuttavia i valori rilevati nella seconda campagna sono inferiori. Analogo andamento in linea generale per i campioni della terza campagna con il valore più basso di 568 S/cm del FC 3, mentre il valore più alto è di 6900 S/cm del FC 14/2, campione a valle delle industrie chimiche, precedente alla sezione del campione FC 14, non campionato prima per assenza di acqua.
• L’alcalinità per la prima campagna presenta una variazione tra un minimo di
2,7 meq/l del campione FC 1, sezione del fiume Cecina nella zona di Radicondoli, a monte di tutte le affluenze, mentre il valore più alto è di 7,63 meq/l del PZ 2, pozzo privato in località La Canova (vedi figura 5.1). Nella seconda campagna il valore di alcalinità più basso rilevato è di 3,2 meq/l del campione FC 4, sezione del fiume Cecina a valle della confluenza con il torrente Pavone nel campo pozzi ASA puretta, il massimo valore (8,2 meq/l) è quello del campione A1, piezometro situato nelle vicinanze del campo pozzi ASA di Puretta, a valle di un industria di lavorazione di inerti e di alabastro. Nella terza campagna il minimo valore (4,2 meq/l) si è registrato nel campione PP 31, pozzo di proprietà dell’ASA situato nel campo pozzi
ASA puretta, mentre il massimo (8,3 meq/l) è quello del campione A1, come nella campagna precedente.
• L’ossigeno disciolto ha un range di variabilità tra 5,5 mg/l del campione FP 2
(torrente Possera alla Centrale geotermica del Larderello) e 15,2 mg/l del campione FC 14 (sezione del fiume Cecina a valle delle industrie chimiche), lo scarico presente nella sezione 14 ha un valore di 2,24 mg/l. Nella seconda campagna è stato rilevato un minimo (5,5 mg/l) del campione FP 2A, campione del torrente Possera a valle dei condotti della centrale geotermica del Larderello, mentre il massimo valore (9,8 mg/l) del FP 5C, punto del torrente Possera a monte della confluenza con il fiume Cecina situato in una zona boschiva. Nella terza campagna il valore più basso misurato è di 4,5 mg/l del campione FC 14 (sezione del fiume Cecina a valle delle industrie chimiche), mentre il valore più alto è di 11,9 mg/l del campione FC 9, sezione del fiume Cecina.
NOME DATA Codice CAMPAGNA pH T acqua T aria Cond uS O2 mg/l AlK meq/l Possera 2 17/09/2003 FP 2 1 7,68 17,5 18,3 885 5,5 4,42 Possera 2A 17/09/2003 FP 2A 1 7,43 15,5 22,9 845 5,7 5,17 Possera 3 17/09/2003 FP 3 1 7,73 20,2 27,4 846 6,9 5,83 Possera 5 17/09/2003 FP 5 1 7,77 17,1 28,5 974 6,5 6,00 Pozzo 2 19/09/2003 PZ 2 1 6,64 18,0 1700 7,63 Pozzo 3 19/09/2003 PZ 3 1 7,04 19,5 1487 5,03 Pozzo 4 19/09/2003 PZ 4 1 7,07 18,5 1563 5,83 Pozzo 6 19/09/2003 PZ 6 1 7,07 16,8 1232 6,57 Sezione 1 24/09/2003 FC 1 1 7,84 19,3 23 1650 8,1 2,70 Sezione 2 24/09/2003 FC 2 1 8,02 20,0 27,4 1520 9,8 3,10 Sezione 3 24/09/2003 FC 3 1 7,89 19,8 23,7 634 9,4 4,77 Sezione 4 24/09/2003 FC 4 1 8,06 25,0 25,9 1203 8,5 3,13 Sezione 9 24/09/2003 FC 9 1 7,79 25,7 28 1246 9,6 4,77 Sezione 14 24/09/2003 FC 14 1 8,07 23,4 24,4 8910 15,2 5,57 PP31 26/09/2003 PP31 1 7,50 20,6 22,8 987 3,90 PP35 26/09/2003 PP35 1 7,50 17,7 21,6 821 5,00 PP39 26/09/2003 PP39 1 7,56 15,2 22 866 5,47 Scarico 26/09/2003 Scarico 1 6,61 19,8 25,5 6570 2.24 6,33 PC 17 07/10/2003 PC 17 1 7,63 19,6 13,3 5020 5,30 PC 12 07/10/2003 PC 12 1 7,20 19,7 15,4 7288 5,07 PC 5 07/10/2003 PC 5 1 7,48 16,8 20,4 3940 6,73 PC 15 07/10/2003 PC 15 1 7,24 16,9 21,7 2780 8,13 PC 19 07/10/2003 PC 19 1 7,37 17,6 23,6 3180 6,30
NOME DATA CODICE CAMPAGNA pH T acqua T aria Cond uS O2 mg/l AlK meq/l
Possera 2 09/10/2003 FP 2 2 7,90 15,8 16,2 810 7,5 4,47 Possera 2A 09/10/2003 FP 2A 2 7,66 14,1 17,2 821 5,5 4,87 Possera 3 09/10/2003 FP 3 2 7,98 17,3 19,9 826 8,2 5,60 Possera 5 09/10/2003 FP 5 2 7,92 14,8 22,1 893 8,6 6,07 Possera 6 09/10/2003 FP 6 2 8,30 19,6 22,6 873 9,6 5,33 Tabella 5.1 - Parametri misurati direttamente in sito al momento del campionamento.
C ap ito lo 5 : C am pi on am en to e a na lis i d el le a cq ue S ez io ne 1 14 /1 0/ 20 03 FC 1 2 8, 12 16 ,7 25 ,5 10 94 9, 4 3, 37 S ez io ne 2 14 /1 0/ 20 03 FC 2 2 8, 00 15 ,2 14 ,7 12 12 9, 4 4, 07 S ez io ne 3 14 /1 0/ 20 03 FC 3 2 7, 90 15 ,9 14 ,2 60 4 8, 4 5, 07 S ez io ne 4 14 /1 0/ 20 03 FC 4 2 8, 21 19 ,1 21 ,0 98 1 8, 1 3, 23 S ez io ne 9 14 /1 0/ 20 03 FC 9 2 7, 86 19 ,6 22 ,4 12 25 9, 4 4, 90 S ez io ne 1 4 14 /1 0/ 20 03 FC 1 4 2 7, 66 19 ,3 20 ,0 64 30 6, 4 5, 37 S ca ri co 14 /1 0/ 20 03 S C A R IC O 2 7, 50 19 ,3 20 ,0 51 40 6, 4 6, 00 P os se ra 5 C 14 /1 0/ 20 03 FP 5 C 2 7, 81 16 ,3 22 ,8 95 1 9, 8 5, 67 P os se ra 5 D 14 /1 0/ 20 03 FP 5 D 2 7, 70 15 ,6 22 ,6 91 0 8, 3 5, 63 P oz zo 2 14 /1 0/ 20 03 P Z 2 2 7, 12 18 ,1 19 ,0 15 23 7, 20 P oz zo 3 14 /1 0/ 20 03 P Z 3 2 7, 56 20 ,3 24 ,6 10 08 4, 47 P oz zo 6 14 /1 0/ 20 03 P Z 6 2 7, 45 18 ,4 19 ,6 12 78 6, 13 P ie zo m et ro 14 /1 0/ 20 03 A 1 2 7, 01 14 ,7 18 ,7 17 59 8, 10 P C 1 7 05 /1 1/ 20 03 P C 1 7 2 7, 33 17 ,9 17 ,4 22 70 4, 73 P C 1 2 05 /1 1/ 20 03 P C 1 2 2 7, 10 21 ,5 19 ,5 46 60 5, 30 P C 6 05 /1 1/ 20 03 P C 6 2 7, 46 17 ,2 18 ,8 18 62 5, 57 P C 1 9 05 /1 1/ 20 03 P C 1 9 2 7, 35 17 ,8 19 ,4 25 20 6, 30 P oz zo 4 06 /1 1/ 20 03 P Z 4 2 7, 35 19 ,6 18 ,4 13 46 5, 47 P C 1 5 06 /1 1/ 20 03 P C 1 5 2 7, 35 16 ,4 15 ,6 25 00 6, 70 P P 31 12 /1 1/ 20 03 P P 31 2 7, 56 15 ,8 12 ,3 71 1 4, 30 P P 35 12 /1 1/ 20 03 P P 35 2 7, 5 16 ,7 13 ,7 80 9 4, 77 P P 39 12 /1 1/ 20 03 P P 39 2 7, 41 15 ,2 13 ,2 83 9 4, 87 N O M E D A T A C O D IC E C A M P A G N A pH T ac qu a T ar ia C on d uS O 2 m g/ l A lK m eq /l P os se ra 1 12 /1 1/ 20 03 FP 1 3 8, 2 12 ,3 10 ,5 58 6 7, 3 5, 30 P os se ra 2 12 /1 1/ 20 03 FP 2 3 8, 16 11 ,9 12 ,2 75 8 6, 7 4, 70 P os se ra 6 12 /1 1/ 20 03 FP 6 3 8, 39 11 ,8 14 ,2 95 7 8, 2 5, 97 P os se ra 2 A 13 /1 1/ 20 03 FP 2 A 3 7, 85 9, 3 8, 5 84 9 5, 6 5, 53 P os se ra 3 13 /1 1/ 20 03 FP 3 3 8, 19 10 ,5 11 ,1 87 6 6, 6 5, 53 P os se ra 4 13 /1 1/ 20 03 FP 4 3 8, 08 9, 8 12 ,6 23 20 7, 5 4, 60 P os se ra 5 13 /1 1/ 20 03 FP 5 3 8, 08 12 ,4 14 ,2 94 7 7, 1 5, 80 P os se ra 5 D 18 /1 1/ 20 03 FP 5 D 3 8, 37 13 ,9 19 ,3 88 0 8, 1 5, 60 co nt in ua
Possera 5C 18/11/2003 FP 5C 3 8,16 13,6 19,2 930 6,8 5,70 Sezione 2 18/11/2003 FC 2 3 8,23 14,2 18,4 841 8,5 4,33 Sezione 3 18/11/2003 FC 3 3 8,37 14,9 18,2 568 7,1 4,83 Sezione 1 20/11/2003 FC 1 3 8,13 10,9 8,8 839 9,8 4,40 Sezione 4 20/11/2003 FC 4 3 8,29 11,0 11,7 720 9,8 4,40 Sezione 7 20/11/2003 FC 7 3 8,26 14,3 15,4 760 10,3 4,40 Sezione 9 20/11/2003 FC 9 3 8,34 14,2 17,2 843 11,9 4,63 Sezione 11 20/11/2003 FC 11 3 8,15 14,0 18,5 886 10,5 4,43 Sezione 12 20/11/2003 FC 12 3 8,31 15,0 18,0 924 10 4,67 Sezione 14 20/11/2003 FC 14 3 7,81 15,3 16,0 5620 4,5 5,77 Sezione 14/2 20/11/2003 FC 14/2 3 7,96 20,5 17,0 6900 2,8 5,30 Sezione 13 21/11/2003 FC 13 3 8,22 12,1 11,1 1016 8,3 4,77 Sezione 15 21/11/2003 FC 15 3 8,31 12,6 13,4 1650 9,5 4,60 Sezione 17 21/11/2003 FC 17 3 8,37 12,8 13,7 1665 9,1 4,77 Sezione 18 21/11/2003 FC 18 3 8,13 13,4 12,8 1441 9,4 4,40 Pozzo 3 09/12/2003 PZ 3 3 7,52 14,3 6,20 1088 4,77 Pozzo 6 09/12/2003 PZ 6 3 7,60 8,4 6,80 1363 5,87 PC 17 10/12/2003 PC 17 3 7,30 12,0 3,60 1436 5,47 PC 12 10/12/2003 PC 12 3 7,28 11,7 3,80 1331 5,20 PC 6 10/12/2003 PC 6 3 7,38 12,0 5,40 1639 5,73 PC 19 10/12/2003 PC 19 3 7,38 11,9 7,20 1824 5,97 PC 15 10/12/2003 PC 15 3 7,33 11,5 8,10 1836 5,80 Pozzo 4 10/12/2003 PZ 4 3 7,16 16,1 9,00 1576 5,03 PP31 18/12/2003 PP31 3 7,53 11,0 5,80 667 4,20 PP35 18/12/2003 PP35 3 7,37 11,4 5,90 688 4,77 PP39 18/12/2003 PP39 3 7,38 9,8,0 6,00 709 5,17 Piezometro 18/12/2003 A1 3 6,98 13,8 10,0 1912 8,37
5.4 Analisi delle acque
Le analisi chimiche sono state effettuate nel laboratorio dell’Istituto di Geoscienze e Georisorse del CNR di PISA seguendo le procedure di routine del laboratorio.
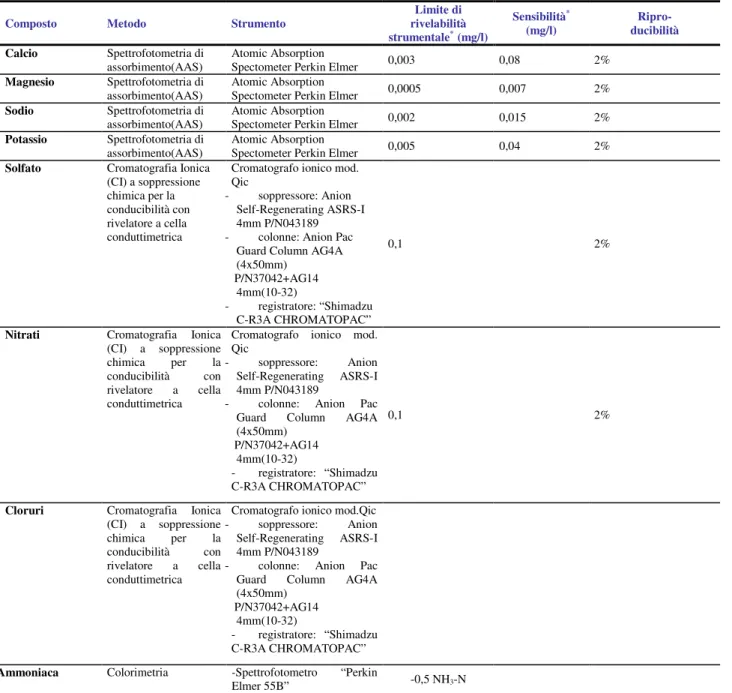
In tabella 5.2 sono descritte in modo sintetico i metodi utilizzati per le analisi delle acque, mentre nei paragrafi che seguiranno, ogni metodo sarà descritto più dettagliatamente.
Tabella 5.2 – Schema dei metodi utilizzati per le analisi delle acque.
Composto Metodo Strumento rivelabilità Limite di
strumentale* (mg/l)
Sensibilità*
(mg/l) ducibilità Ripro-
Calcio Spettrofotometria di
assorbimento(AAS) Atomic Absorption Spectometer Perkin Elmer 0,003 0,08 2%
Magnesio Spettrofotometria di
assorbimento(AAS) Atomic Absorption Spectometer Perkin Elmer 0,0005 0,007 2%
Sodio Spettrofotometria di
assorbimento(AAS) Atomic Absorption Spectometer Perkin Elmer 0,002 0,015 2%
Potassio Spettrofotometria di
assorbimento(AAS) Atomic Absorption Spectometer Perkin Elmer 0,005 0,04 2%
Solfato Cromatografia Ionica
(CI) a soppressione chimica per la conducibilità con rivelatore a cella conduttimetrica
Cromatografo ionico mod. Qic
- soppressore: Anion Self-Regenerating ASRS-I 4mm P/N043189 - colonne: Anion Pac
Guard Column AG4A (4x50mm) P/N37042+AG14 4mm(10-32) - registratore: “Shimadzu C-R3A CHROMATOPAC” 0,1 2%
Nitrati Cromatografia Ionica
(CI) a soppressione chimica per la conducibilità con rivelatore a cella conduttimetrica
Cromatografo ionico mod. Qic
- soppressore: Anion Self-Regenerating ASRS-I 4mm P/N043189
- colonne: Anion Pac Guard Column AG4A (4x50mm) P/N37042+AG14 4mm(10-32) - registratore: “Shimadzu C-R3A CHROMATOPAC” 0,1 2%
Cloruri Cromatografia Ionica
(CI) a soppressione chimica per la conducibilità con rivelatore a cella conduttimetrica
Cromatografo ionico mod.Qic - soppressore: Anion Self-Regenerating ASRS-I 4mm P/N043189
- colonne: Anion Pac Guard Column AG4A (4x50mm)
P/N37042+AG14 4mm(10-32)
- registratore: “Shimadzu C-R3A CHROMATOPAC”
Ammoniaca Colorimetria -Spettrofotometro “Perkin
5.4.1
Calcio, magnesio, sodio e potassio
Il metodo impiegato è quello dell’assorbimento atomico (figura 5.6). Con esso si sfrutta l’assorbimento prodotto dal catione in esame, alla lunghezza d’onda specifica per quel dato elemento utilizzando una lampada dello stesso elemento da analizzare. Una sorgente emette una radiazione alla lunghezza d’onda specifica per quel catione. Il compito è quello di eccitare soltanto il catione da analizzare presente nel campione. L’eccitazione provoca un assorbimento (proporzionale alla concentrazione del catione nella soluzione analizzata) di una parte della radiazione in uscita dalla sorgente. La fornace ha il compito di fornire l’energia necessaria a scindere qualsiasi tipo di composto, anche quelli più refrattari, nel quale l’elemento analizzato può essere bloccato. Secondo il tipo di elemento si utilizzano fiamme diverse, cioè miscele combustibile comburente diverse (caratterizzate da temperature diverse). Nel caso specifico si utilizza la fiamma aria-acetilene con una temperatura intorno a 2300°C circa.
Si preparano degli standard a concentrazione nota e si costruisce la curva di calibrazione. Dall’equazione di essa si ricavano, mediante le letture dei campioni, le concentrazioni incognite dell’elemento analizzato nei campioni stessi. Sono utilizzati i campioni acidificati (al momento del campionamento mediante HCl 1:1 circa) per eliminare qualsiasi possibilità di precipitazione di composti che potrebbero contenere metalli alcalino-terrosi, togliendoli dalla soluzione.
Visto che la fiamma sarebbe in grado di ionizzare gli elementi in analisi, si aggiunge agli standard ed ai campioni un eccesso di una sostanza che si ionizza più facilmente degli elementi che interessano, liberando elettroni e creando una nube riducente che si oppone ulteriormente alla ionizzazione. Per il Calcio e Magnesio è utilizzato lo Stronzio, mentre per il Sodio e Potassio si utilizza il Cesio. (Standard Methods, 1998)
Figura 5.6 – Spettrometro di assorbimento atomico.
5.4.2 Cloruri (con il metodo potenziometrico)
Si determinano i cloruri mediante unatitolazione potenziometrica utilizzando un elettrodo ad “argento/ argento cloruro ” e come titolante una soluzione di AgNO3 0.1
N. Il tutto è collegato ad un potenziografo che misura la variazione del potenziale che si instaura tra i due elettrodi a mano a mano che è aggiunta la soluzione titolante (figura
5.7). Le aggiunte sono effettuate
automaticamente dallo strumento munito di pompa e misuratore di volume di reagente. Mediante i picchi disegnati è possibile rappresentare il potenziale. Il punto equivalente è indicato dalla maggior variazione del potenziale per aggiunte piccole e costanti di AgNO3. Nel caso specifico è rappresentato dal massimo del picco (questo
è a sua volta marcato dal rallentamento della velocità di scorrimento della carta). Visto che i cloruri sono debolmente influenzati dal pH è opportuno lavorare a valori leggermente acidi e per controllare questo parametro viene aggiunto il metilarancio alla soluzione da analizzare. (Standard Methods, 1998)
5.4.3 Anioni (cromatografia ionica)
Lo strumento utilizzato è un cromatografo ionico con rivelatore di anioni, figura 5.8. Il principio del metodo è identico a quello della gas-cromatografia, basato sul diverso tempo di ritenzione delle specie chimiche nei confronti di sostanze che costituiscono il riempimento delle colonne cromatografiche. Per questo tipo di analisi si ricercano cloruri, solfati e nitrati e le colonne sono pre-colonne tipo AG-4a e AG14-4 messe in serie. Attaccato allo strumento è presente un integratore il quale fornisce, oltre alla traccia dei picchi, la loro altezza: è proprio quest’ultimo parametro che viene preso in considerazione, visto che è
proporzionale alla concentrazione della specie chimica ricercata. Figura 5.8 –
Cromatografo ionico.
Anche in questo caso si preparano degli standard a concentrazione nota dai quali si costruisce la curva di calibrazione. Con questo tipo di analisi è possibile determinare cloruri solfati e nitrati nello stesso istante. (Standard Methods, 1998)
5.4.4
Ammoniaca e boro
Questo tipo di analisi sfrutta il metodo spettrofotometrico utilizzano uno strumento detto spettrofotometro (figura 5.9). Il principio è molto semplice: si sfrutta l’assorbimento di una radiazione da parte complesso colorato contenente la specie da determinare. La lunghezza d’onda è definita in base al principio del metodo da utilizzare.
Emettendo una radiazione di intensità nota che incide sulla cella contenente il complesso colorato, misurando l’intensità nota della sorgente in uscita, è possibile ottenere una lettura numerica.
L’analisi è permessa grazie all’esecuzione di una serie di standard a concentrazione nota, compreso il bianco.
Boro: la lunghezza d’onda utilizzata 420 nm, il volume finale deve essere 5 cc e la
cella da utilizzare è in quarzo puro.
L’assorbimento è dovuto alla formazione di un complesso di colore giallo contenente Boro, ottenuto grazie all’aggiunta di un baffer e di un reattivo (Azometina). Quest’ultimo è molto instabile perciò la preparazione deve essere effettuata tutte le volte che viene eseguita l’analisi ed immediatamente dopo la preparazione delle diluizioni dei campioni.
Il volume totale sia degli standard che dei campioni è di 5 cc ed a meno di campioni molto concentrati si utilizza 1 cc di campione, 2 cc di buffer e 2 cc di Azometina. Una volta aggiunto il reattivo i campioni devono essere agitati molto bene e posti al buio per circa 2 ore.
Ammoniaca La lunghezza d’onda utilizzata 690 nm, il volume finale deve essere 20
cc e la cella da utilizzare anche in questa occasione è di quarzo puro. L’assorbimento è dovuto alla formazione di un complesso di colore verde contenente ammonio. Il volume totale sia degli standard che dei campioni è di 20 cc e l'acqua da utilizzare sia per la preparazione degli standard che dei campioni è l'acqua millipore.
La scala degli standard viene preparata a partire da cloruro di ammonio NH4Cl (PM
Per lo sviluppo del colore si aggiungono 2,5 cc del reagente 1B (NaOH circa 8N e Tartrato di Sodio) ed 1 microcucchiaino di reagente 2B (ipoclorito), si attendono 15 minuti e si aggiungono 2 gocce del reagente 3B (timolo e nitroprusiato sodico). Si attendono circa 30 minuti dopodiché si esegue la lettura allo strumento. (Standard Methods, 1998)
5.4.5
Mercurio con sistema ad idruri
Questo tipo di analisi permette la determinazione delle tracce di mercurio sfruttando la formazione di idruri e misurando l’assorbimento che si verifica ad una specifica lunghezza d’onda. Pertanto il dispositivo è accoppiato ad un assorbimento atomico. Al campione, che deve essere in fase liquida, viene aggiunto un potente agente riducente (NaBH4 = sodio-boro-idruro) il quale porta allo stato ridotto l’elemento da
determinare e sul quale viene determinato l’assorbimento. Il vantaggio di tale metodologia risiede nei bassi limiti di rivelabilità (scendendo tranquillamente ai p.p.b.) e nella elevata versatilità visto che per la determinazione dei diversi elementi non si richiedono particolari modifiche del sistema. Entrambi vengono analizzati all’interno della cella di quarzo, per il mercurio non occorre la fiamma. (Standard Methods, 1998)
5.4.6 C.O.D. (Chemical oxygen demand)
La seguente metodologia si basa sulla digestione acida del mio analita. Si prendono aliquote note del nostro campione in esame (2 cc) e si mettono all’interno di una
provetta in vetro che ha la caratteristica di essere una cella spettrofotometrica. All’interno della provetta è presente acido solforico (86%) per mantenere la soluzione a pH acido, solfato di mercurio che permette di precipitare i cloruri a cloruro di mercurio poiché è molto insolubile e triossido di cromo che opera l’ossidazione della materia organica a CO2 .
Appena chiusa la provetta e agitata la si immette in un reattore a 150 °C per 2 ore. La fase finale, cioè la misura, avviene dopo che si sono raffreddati i campioni e dopo aver pulito l’esterno della celletta da possibili interferenze ottiche. La misura avviene con una lunghezza d’onda di 420 nm (figura 5.10).
(Hach Spectrophotometer Handbook, (USEPA approved method: FEDERAL REGISTER 21 Aprile 1980))
Figura 5.10 – Spettrofotometro per la misura del C.O.D.
Nelle tabelle 5.3, 5.4 e 5.5 sono riportati i risultati analitici, rispettivamente della I, II e III campagna, espressi in mg/l.
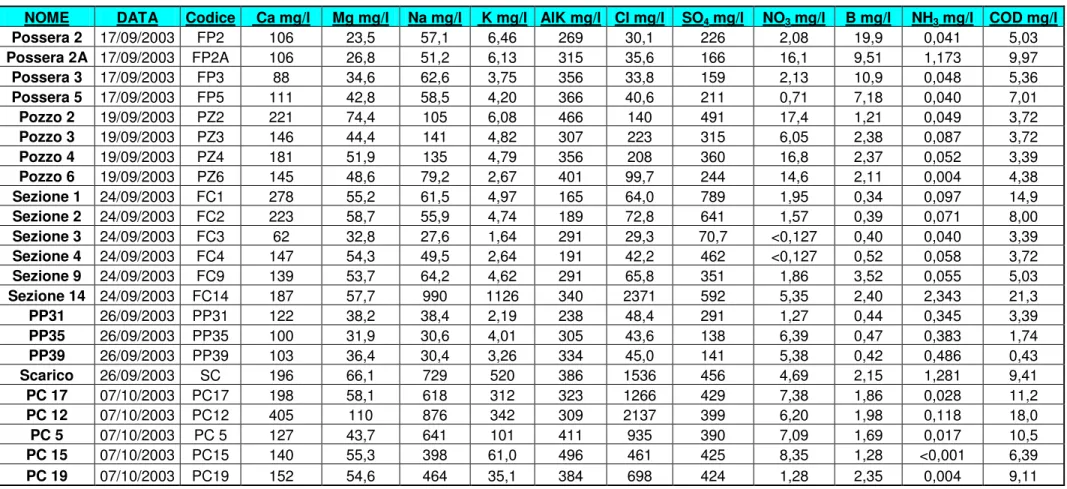
Tabella 5.3 - Parametri misurati in laboratorio nella campagna 1 espressi in mg/l.
NOME DATA Codice Ca mg/l Mg mg/l Na mg/l K mg/l AlK mg/l Cl mg/l SO4 mg/l NO3 mg/l B mg/l NH3 mg/l COD mg/l
Possera 2 17/09/2003 FP2 106 23,5 57,1 6,46 269 30,1 226 2,08 19,9 0,041 5,03 Possera 2A 17/09/2003 FP2A 106 26,8 51,2 6,13 315 35,6 166 16,1 9,51 1,173 9,97 Possera 3 17/09/2003 FP3 88 34,6 62,6 3,75 356 33,8 159 2,13 10,9 0,048 5,36 Possera 5 17/09/2003 FP5 111 42,8 58,5 4,20 366 40,6 211 0,71 7,18 0,040 7,01 Pozzo 2 19/09/2003 PZ2 221 74,4 105 6,08 466 140 491 17,4 1,21 0,049 3,72 Pozzo 3 19/09/2003 PZ3 146 44,4 141 4,82 307 223 315 6,05 2,38 0,087 3,72 Pozzo 4 19/09/2003 PZ4 181 51,9 135 4,79 356 208 360 16,8 2,37 0,052 3,39 Pozzo 6 19/09/2003 PZ6 145 48,6 79,2 2,67 401 99,7 244 14,6 2,11 0,004 4,38 Sezione 1 24/09/2003 FC1 278 55,2 61,5 4,97 165 64,0 789 1,95 0,34 0,097 14,9 Sezione 2 24/09/2003 FC2 223 58,7 55,9 4,74 189 72,8 641 1,57 0,39 0,071 8,00 Sezione 3 24/09/2003 FC3 62 32,8 27,6 1,64 291 29,3 70,7 <0,127 0,40 0,040 3,39 Sezione 4 24/09/2003 FC4 147 54,3 49,5 2,64 191 42,2 462 <0,127 0,52 0,058 3,72 Sezione 9 24/09/2003 FC9 139 53,7 64,2 4,62 291 65,8 351 1,86 3,52 0,055 5,03 Sezione 14 24/09/2003 FC14 187 57,7 990 1126 340 2371 592 5,35 2,40 2,343 21,3 PP31 26/09/2003 PP31 122 38,2 38,4 2,19 238 48,4 291 1,27 0,44 0,345 3,39 PP35 26/09/2003 PP35 100 31,9 30,6 4,01 305 43,6 138 6,39 0,47 0,383 1,74 PP39 26/09/2003 PP39 103 36,4 30,4 3,26 334 45,0 141 5,38 0,42 0,486 0,43 Scarico 26/09/2003 SC 196 66,1 729 520 386 1536 456 4,69 2,15 1,281 9,41 PC 17 07/10/2003 PC17 198 58,1 618 312 323 1266 429 7,38 1,86 0,028 11,2 PC 12 07/10/2003 PC12 405 110 876 342 309 2137 399 6,20 1,98 0,118 18,0 PC 5 07/10/2003 PC 5 127 43,7 641 101 411 935 390 7,09 1,69 0,017 10,5 PC 15 07/10/2003 PC15 140 55,3 398 61,0 496 461 425 8,35 1,28 <0,001 6,39 PC 19 07/10/2003 PC19 152 54,6 464 35,1 384 698 424 1,28 2,35 0,004 9,11
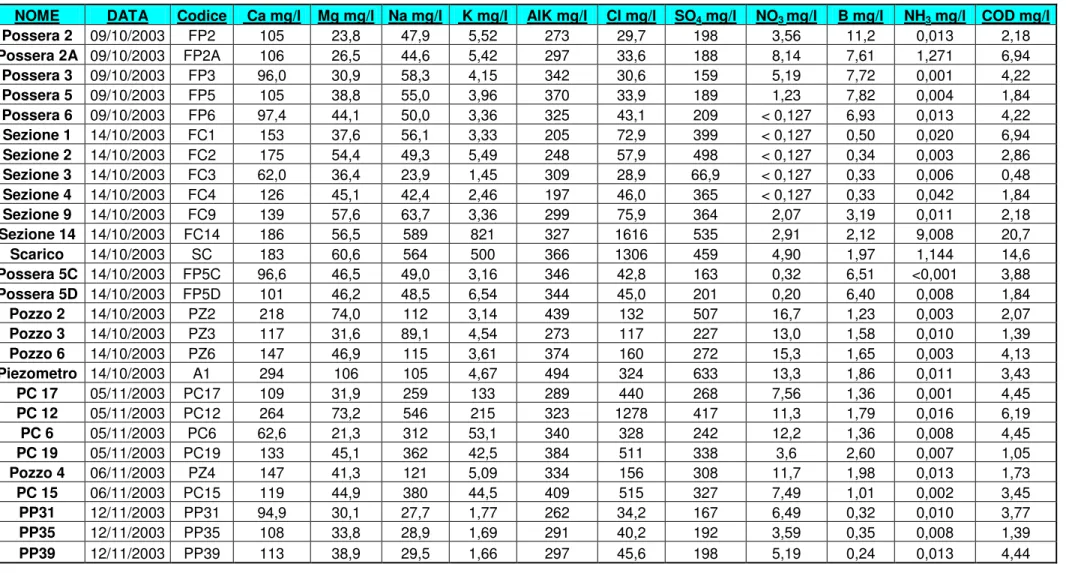
Tabella 5.4– Parametri misurati in laboratorio nella campagna 2 espressi in mg/l.
NOME DATA Codice Ca mg/l Mg mg/l Na mg/l K mg/l AlK mg/l Cl mg/l SO4 mg/l NO3 mg/l B mg/l NH3 mg/l COD mg/l
Possera 2 09/10/2003 FP2 105 23,8 47,9 5,52 273 29,7 198 3,56 11,2 0,013 2,18 Possera 2A 09/10/2003 FP2A 106 26,5 44,6 5,42 297 33,6 188 8,14 7,61 1,271 6,94 Possera 3 09/10/2003 FP3 96,0 30,9 58,3 4,15 342 30,6 159 5,19 7,72 0,001 4,22 Possera 5 09/10/2003 FP5 105 38,8 55,0 3,96 370 33,9 189 1,23 7,82 0,004 1,84 Possera 6 09/10/2003 FP6 97,4 44,1 50,0 3,36 325 43,1 209 < 0,127 6,93 0,013 4,22 Sezione 1 14/10/2003 FC1 153 37,6 56,1 3,33 205 72,9 399 < 0,127 0,50 0,020 6,94 Sezione 2 14/10/2003 FC2 175 54,4 49,3 5,49 248 57,9 498 < 0,127 0,34 0,003 2,86 Sezione 3 14/10/2003 FC3 62,0 36,4 23,9 1,45 309 28,9 66,9 < 0,127 0,33 0,006 0,48 Sezione 4 14/10/2003 FC4 126 45,1 42,4 2,46 197 46,0 365 < 0,127 0,33 0,042 1,84 Sezione 9 14/10/2003 FC9 139 57,6 63,7 3,36 299 75,9 364 2,07 3,19 0,011 2,18 Sezione 14 14/10/2003 FC14 186 56,5 589 821 327 1616 535 2,91 2,12 9,008 20,7 Scarico 14/10/2003 SC 183 60,6 564 500 366 1306 459 4,90 1,97 1,144 14,6 Possera 5C 14/10/2003 FP5C 96,6 46,5 49,0 3,16 346 42,8 163 0,32 6,51 <0,001 3,88 Possera 5D 14/10/2003 FP5D 101 46,2 48,5 6,54 344 45,0 201 0,20 6,40 0,008 1,84 Pozzo 2 14/10/2003 PZ2 218 74,0 112 3,14 439 132 507 16,7 1,23 0,003 2,07 Pozzo 3 14/10/2003 PZ3 117 31,6 89,1 4,54 273 117 227 13,0 1,58 0,010 1,39 Pozzo 6 14/10/2003 PZ6 147 46,9 115 3,61 374 160 272 15,3 1,65 0,003 4,13 Piezometro 14/10/2003 A1 294 106 105 4,67 494 324 633 13,3 1,86 0,011 3,43 PC 17 05/11/2003 PC17 109 31,9 259 133 289 440 268 7,56 1,36 0,001 4,45 PC 12 05/11/2003 PC12 264 73,2 546 215 323 1278 417 11,3 1,79 0,016 6,19 PC 6 05/11/2003 PC6 62,6 21,3 312 53,1 340 328 242 12,2 1,36 0,008 4,45 PC 19 05/11/2003 PC19 133 45,1 362 42,5 384 511 338 3,6 2,60 0,007 1,05 Pozzo 4 06/11/2003 PZ4 147 41,3 121 5,09 334 156 308 11,7 1,98 0,013 1,73 PC 15 06/11/2003 PC15 119 44,9 380 44,5 409 515 327 7,49 1,01 0,002 3,45 PP31 12/11/2003 PP31 94,9 30,1 27,7 1,77 262 34,2 167 6,49 0,32 0,010 3,77 PP35 12/11/2003 PP35 108 33,8 28,9 1,69 291 40,2 192 3,59 0,35 0,008 1,39 PP39 12/11/2003 PP39 113 38,9 29,5 1,66 297 45,6 198 5,19 0,24 0,013 4,44
Tabella 5.5– Parametri misurati in laboratorio nella campagna 3 espressi in mg/l.
NOME DATA Codice Ca mg/l Mg mg/l Na mg/l K mg/l AlK mg/l Cl mg/l SO4 mg/l NO3 mg/l B mg/l NH3 mg/l COD mg/l
Possera 1 12/11/2003 FP1 92,3 13,8 23,0 1,55 323 22,4 48,1 4,12 0,53 0,024 3,09 Possera 2 12/11/2003 FP2 109 22,2 29,3 3,48 287 22,8 166 11,3 7,36 0,011 2,41 Possera 6 12/11/2003 FP6 115 47,1 43,0 1,60 364 32,8 199 13,2 3,93 0,013 5,13 Possera 2A 13/11/2003 FP2A 128 32,0 32,2 4,47 338 27,3 215 13,6 6,10 1,097 4,45 Possera 3 13/11/2003 FP3 118 32,5 42,2 4,11 338 30,3 199 14,8 5,07 0,009 5,47 Possera 4 13/11/2003 FP4 237 108 188 8,63 281 183 966 38,0 30,3 0,024 11,9 Possera 5 13/11/2003 FP5 115 38,5 42,6 3,40 354 36,1 203 14,9 4,59 0,003 5,13 Possera 5D 18/11/2003 FP5D 108 44,4 44,1 3,35 342 40,0 220 10,8 4,40 0,021 4,79 Possera 5C 18/11/2003 FP5C 107 44,4 43,5 3,30 348 38,1 217 11,4 4,30 0,018 5,13 Sezione 2 18/11/2003 FC2 126 30,7 31,6 1,63 264 40,0 239 5,90 0,64 <0,001 <0,30 Sezione 3 18/11/2003 FC3 68,0 30,2 22,5 1,31 295 25,9 70,7 2,89 0,23 <0,001 <0,30 Sezione 1 20/11/2003 FC1 131 28,3 31,6 1,53 268 36,9 241 5,96 0,76 0,0743 <0,30 Sezione 4 20/11/2003 FC4 97,3 33,6 28,4 1,55 268 32,2 173 4,21 0,47 0,0251 <0,30 Sezione 7 20/11/2003 FC7 100 32,3 31,4 1,88 268 38,2 180 5,21 1,16 0,0021 <0,30 Sezione 9 20/11/2003 FC9 106 35,0 37,8 2,29 283 46,7 208 5,37 1,41 0,0939 <0,30 Sezione 11 20/11/2003 FC11 112 36,9 40,4 2,16 270 52,8 225 4,96 1,44 0,0087 <0,30 Sezione 12 20/11/2003 FC12 113 37,6 55,7 1,94 285 67,7 243 4,90 1,44 0,0021 <0,30 Sezione 14 20/11/2003 FC14 194 49,5 593 663 352 1421 594 23,6 1,70 3,715 3,63 Sezione 14/2 20/11/2003 FC14/2 157 40,7 644 1015 323 1700 605 37,3 1,72 7,426 11,7 Sezione 13 21/11/2003 FC13 117 38,3 56,5 3,87 291 72,3 248 5,16 1,41 0,068 1,40 Sezione 15 21/11/2003 FC15 126 38,5 131 113 281 267 289 7,46 1,43 0,473 0,77 Sezione 17 21/11/2003 FC17 125 38,5 137 103 291 269 287 5,34 1,45 0,197 0,77 Sezione 18 21/11/2003 FC18 125 43,2 128 23,3 268 209 295 4,98 1,33 0,010 1,40 Pozzo 3 09/12/2003 PZ3 128 36,3 82,9 4,17 291 113 242 9,57 1,39 <0,001 2,80 Pozzo 6 09/12/2003 PZ6 142 48,3 121 3,57 358 162 271 <0,127 1,50 0,011 <0,30 PC 17 10/12/2003 PC17 110 34,2 129 79,2 334 197 257 10,4 1,26 <0,001 4,11
C ap ito lo 5 : C am pi on am en to e a na lis i d el le a cq ue P C 1 2 10 /1 2/ 20 03 P C 12 12 9 37 ,4 30 6 13 6 31 7 54 2 31 0 45 ,8 1, 31 0, 01 8 4, 11 P C 6 10 /1 2/ 20 03 P C 6 93 ,5 30 ,5 23 0 63 ,6 35 0 28 9 26 0 11 ,3 1, 09 0, 01 1 3, 13 P C 1 9 10 /1 2/ 20 03 P C 19 11 0 37 ,6 26 2 35 ,7 36 4 34 8 26 5 9, 29 1, 65 0, 01 0 4, 44 P C 1 5 10 /1 2/ 20 03 P C 15 99 ,2 36 ,6 26 5 44 ,9 35 4 30 8 30 4 9, 82 0, 96 <0 ,0 01 2, 80 P oz zo 4 10 /1 2/ 20 03 P Z4 18 1 46 ,5 13 8 4, 86 30 7 21 2 39 3 10 ,6 1, 65 <0 ,0 01 1, 81 P P 31 18 /1 2/ 20 03 P P 31 94 ,7 30 ,1 24 ,1 1, 51 25 6 29 ,9 15 6 9, 10 0, 28 0, 00 1 2, 17 P P 35 18 /1 2/ 20 03 P P 35 97 ,1 31 ,2 25 ,4 1, 48 29 1 29 ,6 14 4 5, 24 0, 29 0, 00 6 5, 27 P P 39 18 /1 2/ 20 03 P P 39 98 ,1 33 ,9 24 ,4 1, 67 31 5 31 ,6 14 2 5, 45 0, 24 <0 ,0 01 4, 65 P ie zo m et ro 18 /1 2/ 20 03 A 1 29 4 10 5 10 7 2, 99 51 0 13 4 80 9 11 ,4 1, 78 0, 05 8 2, 79