7
LA DISPLASIA DELL’ANCA
La displasia dell’anca nel cane è stata descritta per la prima volta in Nord America da Schnelle negli anni trenta, che la definì “sublussazione congenita dell’articolazione coxofemorale” (Schnelle, 1937).
Una definizione più descrittiva fu presentata da Henricson nel 1966, che la definì come un diverso grado di lassità dell’articolazione dell’anca che permette la sublussazione nel primo periodo di vita, dando origine a diversi gradi di profondità acetabolare ed appiattimento della testa femorale, ed infine conducendo inevitabilmente ad osteoartrite (Henricson e coll., 1966).
Oggi la displasia dell’anca costituisce la patologia ortopedica più comune nei cani di taglia grande e gigante, ed è intesa come un’alterazione del normale sviluppo dell’articolazione, caratterizzata da lassità articolare che risulta in un’alterata o insufficiente corrispondenza dei capi articolari, lussazione o sublussazione articolare e dallo sviluppo di osteoartrosi; quest’ultima nei cani displasici non sembra ereditaria, ma conseguente all’incongruità articolare (Kealy e coll., 1997 e 2000).
Il quadro anatomopatologico è rappresentato da appiattimento acetabolare, formazione di osteofiti (becchi ossei) lungo il margine dell’acetabolo, rimodellamento della testa femorale, marcato ispessimento della capsula articolare, ispessimento e lacerazione del legamento rotondo, abnorme consumo della cartilagine articolare ed instabilità articolare, da una sublussazione minima alla lussazione completa (Kealy e McAllister, 2000).
8 Eziologia
L’esatta eziologia della displasia dell’anca nel cane rimane un problema aperto. È riconosciuta come malattia ereditaria poligenica, ma il numero esatto dei geni coinvolti non è noto; l’ereditabilità (h2) sembra essere pari allo 0.4-0.5% (Hedhammer e coll., 1979). L’espressione fenotipica della malattia sembra essere determinata da un’interazione tra eredità genetica e fattori contribuenti non genetici: lo sviluppo rapido (Gustafsson e coll., 1975), la distrofia del muscolo pettineo (Cardinet e coll., 1969), l’ipernutrizione (Kasström, 1975) e l’effetto della dieta sulla gravità dell’osteoartrite (Kealy e coll., 1997), l’eccessivo livello di attività fisica nel neonato (Lust e coll., 1978), la muscolatura pelvica scarsa (Riser e Shirer, 1967), l’osteocondrosi (Olsson, 1976), gli estrogeni esogeni eccessivi (Gustafsson, 1975), l’ipovitaminosi C (Belfield, 1977) e l’inclinazione interna della parete pelvica che risulta in una maggiore obliquità della volta acetabolare e, quindi, in un minor sostegno della testa femorale dovuto al ridotto grado di copertura acetabolare (Olsson e Kasström, 1972).
Ognuno di questi fattori può influenzare l’incidenza, l’aspetto della displasia dell’anca, l’età di insorgenza e la gravità della lesione articolare secondaria nei cani portatori del tratto genetico che controlla la condizione responsabile della displasia.
Patogenesi
Nonostante l’eziologia della displasia dell’anca sia multifattoriale, la patogenesi delle alterazioni che si instaurano a livello dell’articolazione patologica sono probabilmente simili.
9
Indipendentemente dall’eziologia, le anche subiscono progressive alterazioni strutturali, con il coinvolgimento dei tessuti molli, che portano a lassità articolare e sublussazione, tumefazione, sfilacciamento e rottura del legamento rotondo della testa femorale (Henricson e coll., 1966). Seguono l’erosione della cartilagine articolare con eburneazione dell’osso subcondrale; il rimodellamento del margine acetabolare; l’appiattimento della testa femorale; la produzione di osteofiti periarticolari ed il rimodellamento del collo femorale (Riser, 1973).
La sublussazione coxofemorale causa un carico non fisiologico sulla testa femorale, sull’acetabolo e sulla capsula articolare; questo determina l’erosione della cartilagine, l’ispessimento della sinoviale, la formazione di osteofiti ed altri segni di osteoartrosi (Morgan e Stephens, 1985).
Le alterazioni della capsula articolare sono rappresentate da stiramento ed ispessimento della stessa fino a 5-7 mm, rispetto al normale spessore di 1-2 mm, aumento generalizzato del tessuto connettivo fibroso nella sinovia, ialinizzazione del tessuto connettivo con metaplasia condroide e calcificazione distrofica, infiammazione sinoviale negli stadi iniziali della displasia dell’anca e modificazioni infiammatorie croniche intorno ai frammenti cartilaginei intrappolati nei recessi sinoviali (Lust e Summers, 1981). L’instabilità articolare ed i microtraumi possono anche determinare edema dello strato fibroso della capsula articolare, aumentandone ulteriormente la sclerosi e lo spessore (Morgan e Stephens, 1985).
Per quanto riguarda il legamento rotondo della testa femorale, la lassità ed un aumento del suo spessore possono impedire alla testa femorale di ritornare nella fossa acetabolare; queste modificazioni sono dovute alla maggiore sollecitazione gravante sul legamento durante la lussazione della testa femorale. Tuttavia, si ritiene che il legamento rotondo abbia la sua massima importanza, nello stabilizzare l’articolazione dell’anca, dalla nascita fino all’età di 3-4 mesi; dopo questo periodo l’importanza del legamento nello stabilizzare l’articolazione diminuisce (Riser e Shirer, 1966).
10
A livello cartilagineo le lesioni che si osservano sono un’area di depressione della cartilagine articolare con una variazione del colore dal normale bianco al bianco grigiastro o giallastro; macroscopicamente possono essere visibili linee di fessurazione irregolari e un aspetto vellutato della superficie
articolare (Morgan, 1997). Con il deterioramento della cartilagine articolare,
le forze meccaniche legate al sostegno del peso ed al movimento vengono trasferite direttamente all’osso subcondrale che reagisce con la sclerosi, rappresentata da un aumento dello spessore e della densità (Fig. 1). Quando le fessurazioni raggiungono l’osso subcondrale, si verifica una separazione della giunzione osteocondrale unitamente ad emorragie ed a necrosi di vario grado;
il risultante difetto osteocondrale si ripara con tessuto di granulazione e fibrocartilagine ed è visibile radiograficamente come irregolarità subcondrali (Pedersen e coll., 1982).
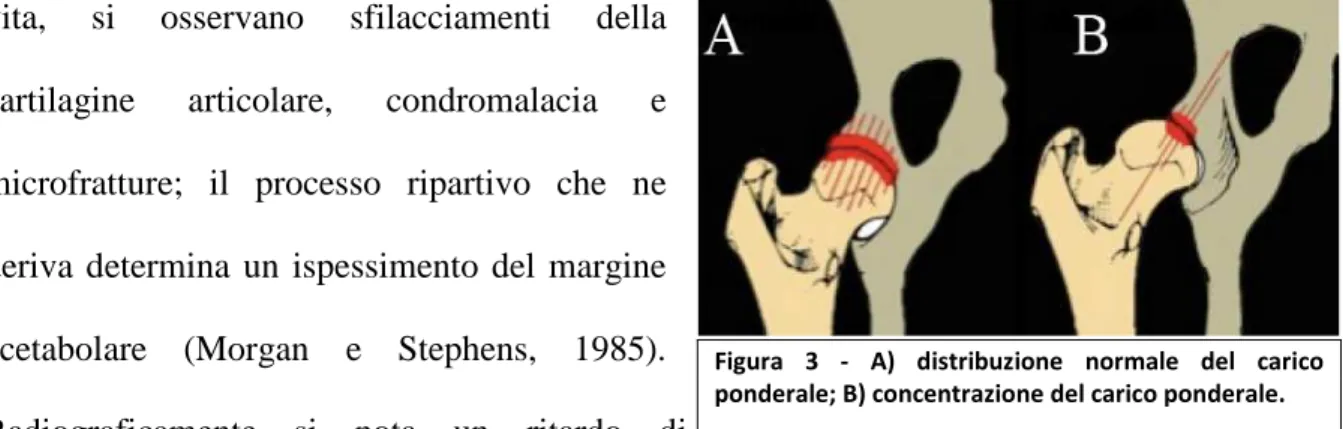
Per la particolare anatomia dell’articolazione coxofemorale, la lassità determina sempre una dislocazione della testa femorale verso il lato dorsolaterale di gravità variabile (Fig. 2); perciò, la superficie mediale della testa del femore ed il margine acetabolare dorsale, in una piccola area compresa tra la posizione di ore 10 e ore 2, devono sostenere un maggiore carico ponderale rispetto a quanto si verifica in un’articolazione normale (Fig. 3). Da 5-9 mesi di
Figura 1 - Sezione trasversale di una testa femorale. Estesa sclerosi dell'osso subcondrale (freccia) dovuta a perdita della cartilagine articolare. (Morgan, 1992)
Figura 2 - A) anca normale; B) anca displasica con lassità capsulare.
11
vita, si osservano sfilacciamenti della cartilagine articolare, condromalacia e microfratture; il processo ripartivo che ne deriva determina un ispessimento del margine acetabolare (Morgan e Stephens, 1985). Radiograficamente si nota un ritardo di
ossificazione dei margini acetabolari craniale e dorsale dovuto ai traumi che si ripercuotono su quest’area, determinando un ripiegamento dorsocaudale dei margini. Questo permette una maggiore sublussazione della testa femorale di modo che solo una piccola area delle superfici articolari entra in reciproco contatto. Il ripiegamento ed eccessivo carico causano microfratture che determinano appiattimento e perdita della curvatura della cavità acetabolare; le fibre di Sharpey (inserzione dei tessuti molli sul’osso) si lacerano e sanguinano, stimolando la formazione di osteofiti attorno all’acetabolo. A circa 11-13 mesi di età la pelvi completa la sua ossificazione, le articolazioni coxofemorali diventano stabili e di solito non dolenti poiché da questo momento in poi non si verificano microfratture (Morgan e Stephens, 1985).
Altre modificazioni hanno luogo nella fossa acetabolare che, in seguito a sublussazione ed alla conseguente assenza di una normale distribuzione delle forze, inizia a riempirsi di tessuto fibroso che si trasforma in tessuto osseo (Morgan e Stephens, 1985).
Per quanto concerne la testa femorale, essa, nelle fasi iniziali dello sviluppo, è costituita da cartilagine con un nucleo di tessuto osseo al centro; tale nucleo si espande e può riempire l’intera matrice cartilaginea, mentre rimane un sottile strato di cartilagine articolare che persiste per tutta la vita del cane. L’età in cui si verifica l’iniziale instabilità articolare determina il tipo di alterazione a livello della testa femorale: quanto maggiore è la quantità di cartilagine molle presente al momento della comparsa della lassità articolare, tanto più estese sono le risultanti alterazioni della testa femorale. Un altro fattore importante è il grado di
Figura 3 - A) distribuzione normale del carico ponderale; B) concentrazione del carico ponderale.
12
lussazione: la sublussazione determina effetti di rimodellamento della testa femorale più gravi di quanto si osserva nella lussazione completa. Infatti, maggiore è il grado di sublussazione, minore è il contatto della testa femorale con il margine acetabolare e minore è l’entità del rimodellamento che si instaura (Morgan e Stephens, 1985).
L’esame radiografico permette solo l’esame del tessuto ossificato, pertanto, le alterazioni iniziali che coinvolgono la porzione cartilaginea non sono apprezzabili (Morgan e Stephens, 1985).
Le alterazioni della cartilagine articolare e dell’osso subcondrale conducono alla perdita del normale profilo delle superfici articolari, predisponendo l’articolazione ad ulteriori anomali movimenti; nel tentativo di rispondere a questi nuovi stress e di contenere l’abnorme movimento, i margini delle superfici articolari vanno incontro ad un rimodellamento allo scopo di aumentare l’area della superficie articolare. Questo processo è accompagnato ad una proliferazione ossea caratterizzata da osteofiti a livello delle superfici ossee periarticolari adiacenti od all’interno della linea di inserzione della capsula articolare (Pedersen e coll., 1982).