d
e
f
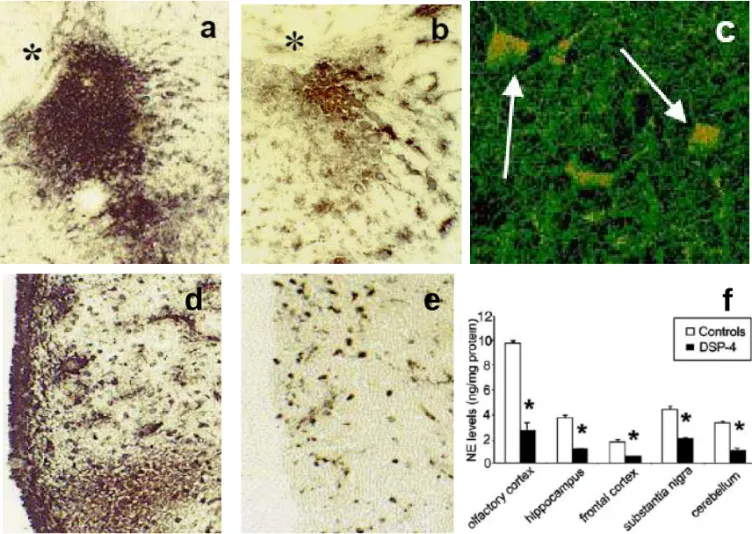
Fig. 1. Analisi degli effetti morfologici e biochimici indotti da DSP-4 sul LC e le aree cerebrali da esso innervate. La marcatura per dopamina-β-idrossilasi mostra i neuroni NA del LC vicino al pavimento del IV ventricolo (*) in ratti di controllo (a), rispetto ad animali trattati con DSP-4 60 mg/kg somministrato 3 giorni prima del sacrificio (b); 6 settimane dopo trattamento con DSP-4 i corpi cellulari dei neuroni degeneranti del LC sono visualizzati mediante il metodo F-J B (c). La corteccia piriforme dell’animale di controllo presenta una ricca innervazione NA (d), mentre una marcata perdita
delle fibre NA si verifica nella stessa regione 3 giorni dopo il trattamento con DSP-4 (e). Livelli di NA in regioni cerebrali selezionate misurati 3 giorni dopo trattamento con DSP-4 o salina (f); il contenuto più elevato di NA si osserva a livello della corteccia olfattiva.
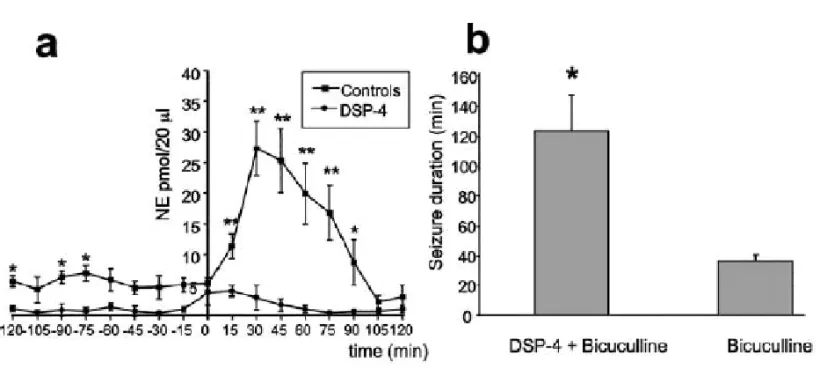
Fig. 2. Effetti della perdita di NA sui livelli extracellulari di NA e sulla durata delle crisi. Gli animali erano trattati con DSP-4 o salina 2 giorni prima di essere sottoposti a chirurgia stereotassica che prevedeva il posizionamento di una fibra per la microdialisi cerebrale nella corteccia piriforme anteriore di un lato e di una cannula da microinfusione per il trattamento con bicucillina (118 pmol) nella stessa area controlateralmente. L’infusione di bicucullina produce un marcato incremento dei livelli extracellulari di NE nei ratti di controllo, mentre non produce modificazioni significative negli animali lesi con DSP-4 (a). Negli animali trattati con DSP-4 e bicucullina la durata delle crisi è significativamente maggiore di quella dei controlli,
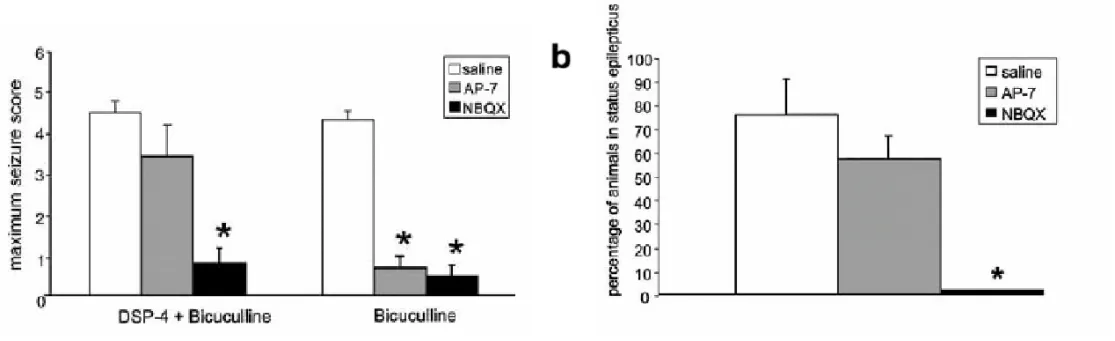
Fig. 3. Effetti della preinfusione di antagonisti selettivi per i recettori NMDA e AMPA sulla severità delle crisi e sullo stato epilettico. Nell’animale con LC integro la bicucullina in APC induce crisi in serie che vengono soppresse dalla preinfusione dell’antagonista selettivo NMDA AP-7 e non-NMDA (AMPA) NBQX. Nell’animale pretrattato con DSP-4, AP-7 non è più in grado di prevenire le crisi, mentre NBQX continua ad essere in grado (a). Nell’animale con LC leso la bicucullina
produce uno stato epilettico; anche in questo caso AP-7 non è in grado di prevenire l’insorgenza dello stato, mentre NBQX ne previne pienamente l’insorgenza.
Fig. 10. Captazione del [14C]2-DG in aree limbiche dopo MDMA e/o dosi subconvulsivanti di KA.(A) Sezioni coronali rappresentative ottenute da topi sacrificati 1h dopo l’iniezione di [14C]2-DG; si riportano due sezioni per gruppo di trattamento. Nelle autoradiografie il livello di radioattività è rappresentato secondo una scala colorimetrica che va dal blu (nessuna captazione) al rosso (massima captazione).
I gruppi di trattamento sono i seguenti: salina (1h)= salina x 2 con intervallo di 2 ore tra le 2 iniezioni, 1h prima del sacrificio; MDMA (1h)= MDMA 5 mg/kg x 2 con intervallo di 2 ore tra le 2 iniezioni, 1h prima del sacrificio; MDMA (2w)= MDMA 5 mg/kg x 2 con intervallo di 2 ore tra le 2 iniezioni, 2 settimane prima del sacrificio; KA (1h)= KA 5 mg/kg 1h prima del sacrificio in precedente trattamento con salina 2 settimane prima; MDMA (2w) + KA= KA 5 mg/kg 1h prima del sacrificio in precedente trattamento con MDMA 5 mg/kg x 2 con intervallo di 2 ore tra le 2 iniezioni 2 settimane prima. (B) Captazione di [14C]2-DG a livello dell’ippocampo e della corteccia entorinale.
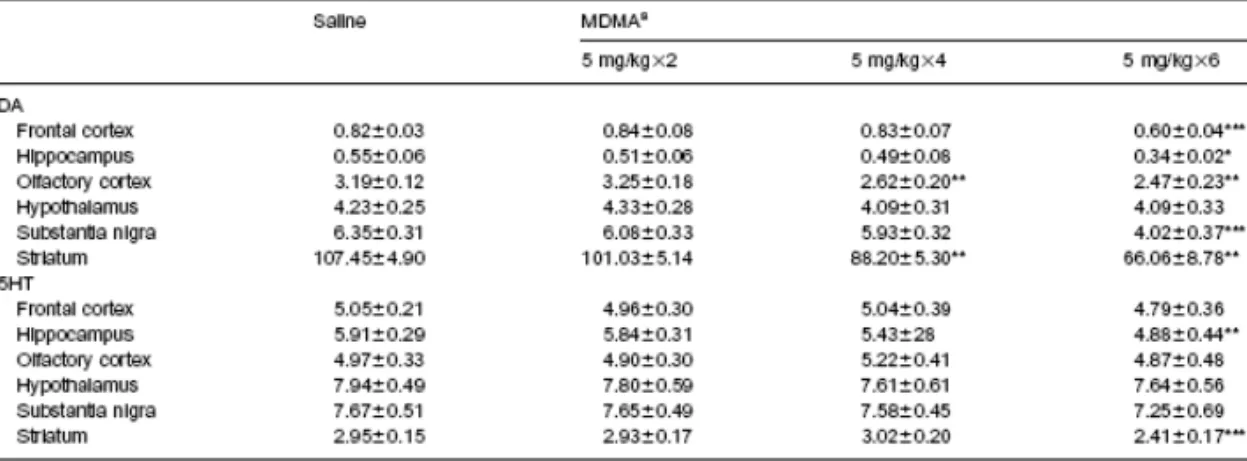
Tab. 1. Livelli di DA e 5HT misurati in varie regioni cerebrali 2 settimane dopo somministrazione di MDMA o salina. I valori sono espressi come media ± SEM di 6 animali per gruppo di trattamento.
*p<0.5 vs salina
**p<0.05 vs salina e MDMA 5 mg/kg x 2
***p<0.05 vs salina, MDMA 5 mg/kg x 2, MDMA 5 mg/kg x 4 a: valori espressi come ng/mg di proteine
a
b
KA 35 mg/kg KA 35 + 35 mg/kg 100% crisi punteggio 1 65% punteggio 2 10% punteggio 5 25% 70% crisi punteggio 1 40% punteggio 2 25% PIL 200 mg/kg PIL 200 + 200 mg/kg 30% crisi 100% crisi punteggio 1 30% punteggio 1 10% punteggio 2 20% punteggio 5 70% 60% crisi punteggio 1 40% punteggio 2 15% punteggio 5 5% WT 0% crisi KO punteggio 5 5% WT non eseguito 0% crisi KOTab.2. Valutazione dell’attività epilettica indotta dalla somministrazione di KA (a) e PIL (b) in animali wild-type e knockout. Gli animali
knockout sono resistenti alle crisi; nessun animale knockout infatti presenta crisi per dosi di KA (35 mg/kg) che risultano convulsivanti per il 100% dei wild-type e per dosi di PIL (200 mg/kg) che risultano convulsivanti per 30% dei wild-type. Per dosi doppie di KA e PIL i knockout vanno
incontro in genere a crisi di basso grado e, solo occasionalmente, di grado elevato.
c
KA 10 mg/kg 100% crisi punteggio 1 10% punteggio 2 25% punteggio 3 40% punteggio 5 25% WT + MDMA 2.5 mg x 25 KO + MDMA 2.5 mg x 25 0% crisi(c) Valutazione della suscettibilità epilettica in animali wild-type e knockout precedentemente esposti a MDMA. Mentre il 100% dei wild-type presenta crisi dopo somministrazione di KA 10 mg/kg, nessun knockout va incontro a crisi.
KA 70 mg/kg in knockout (1) F1-R F1-R
b
KA 35 mg/kg in wild-type (2) KA 35 mg/kg in knockout (1) F1-R F1-R KA 35 mg/kg in wild-type (2) F1-Ra
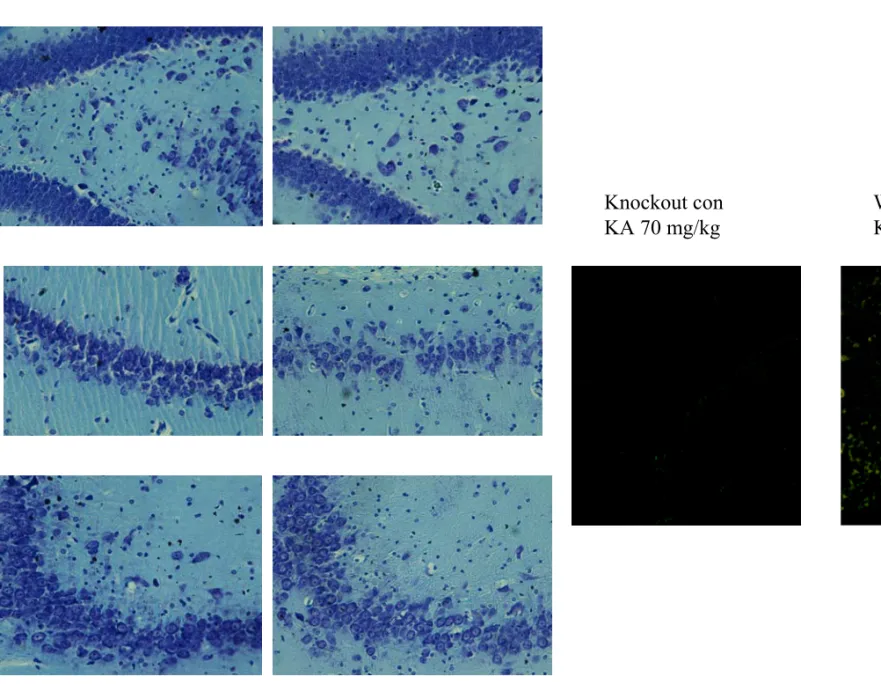
Fig 11: Resistenza dei topi knockout a KA somministrato a dosi convulsivanti: gli animali knockout non hanno crisi dopo somministrazione di KA 35 mg/kg (a1) che producono invece nel wild-type crisi, in genere di basso grado (a2); si ottengono crisi limbiche di grado elevato e sovrapponibili sul piano EEG nel wild-type trattato con KA 35 mg/kg e nel knockout trattato con KA 70 mg/kg (b1 e 2); diversa è la % degli animali nei vari gradi di severità delle crisi e diverse le conseguenze neuropatologiche (v. Tab.2 e Fig 13-14).
saline MDMA (WT) MDMA (KO)
Attività
loco
motoria
in
open-f
ield
Numero di iniezioni Numero di iniezioni
Rearing
0 20 40 60 80 100 0 5 10 15 20 25 0 20 40 60 80 100 120 140 0 5 10 15 20 25 0 1 2 3 4 5 6 0 5 10 15 20 25 0 2 4 6 8 10 12 14 16 0 5 10 15 20 25Numero di iniezioni Numero di iniezioni
Numero di rearing/2 m in Numero di rearing/2 min boxes/2m in boxes/2m in
*
*
*
*
*
*
*
*
*
*
*
*
*
*
*
Prima della somministrazione di MDMA Dopo la somministrazione di MDMA
Fig.12: Effetti di ripetute somministrazioni di MDMA 2.5 mg/kg x 25 sull’attività locomotoria in open field e sul rearing. Gli animali wild-type presentano un incremento dell’attività locomotoria e del rearing, sia prima che dopo somministrazione di MDMA, mentre i knockout non hanno alcuna modificazione comportamentale e non sono distinguibili dai wild-type tratti con salina.
Knockout con PIL 400 mg/kg Wild-type con PIL 400 mg/kg
Ilo
Wild-type con KA 35 mg/kg Knockout con KA 70 mg/kgCA1
CA3
Fig. 13. L’assenza del recettore α1B protegge dal danno indotto da PIL e KA in svariate aree limbiche. Quelle riportate sono immagini rappresentative degli effetti neuropatologici che si osservano in animali wild-type e knockout che hanno presentato crisi limbiche di
grado elevato. Il danno che si osserva nei wild-type è esteso a livello dell’ilo dell’ippocampo e delle regioni CA1 e CA3, mentre gli animali knockout presentano una normale cellularità nelle stesse aree in assenza di fenomeni di degenerazione neuronale.
Knockout con KA
70 mg/kg
Wild-type con KA
35 mg/kg
Knockout con KA
70 mg/kg
Wild-type con KA
35 mg/kg
e
f
g
h
a
d
b
c
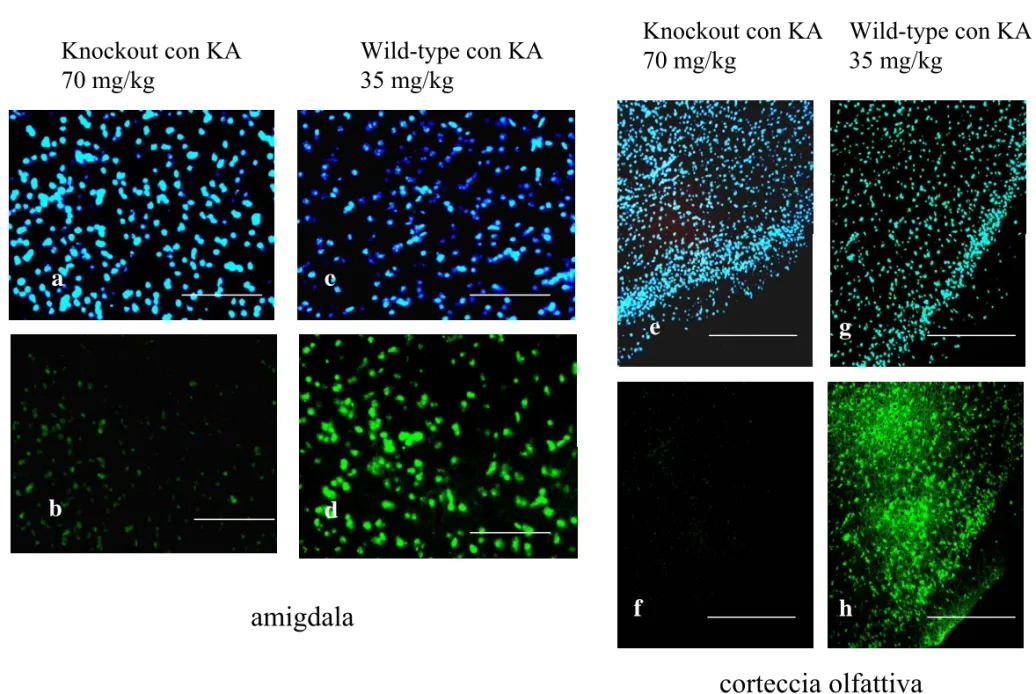
amigdala
corteccia olfattiva
Fig. 14 L’assenza del recettore α1B protegge dal danno indotto da PIL e KA in svariate aree limbiche. Quelle riportate sono immagini rappresentative degli effetti di neuropatologici a livello di amigdala e corteccia olfattiva in animali wild-type e knockout che hanno presentato crisi di grado elevato.
![Fig. 10. Captazione del [ 14 C]2-DG in aree limbiche dopo MDMA e/o dosi subconvulsivanti di KA.(A) Sezioni coronali rappresentative ottenute da topi sacrificati 1h dopo l’iniezione di [ 14 C]2-DG; si riportano due sezioni per gruppo di trattamento](https://thumb-eu.123doks.com/thumbv2/123dokorg/7293651.86184/4.1263.272.931.166.582/captazione-limbiche-subconvulsivanti-rappresentative-sacrificati-iniezione-riportano-trattamento.webp)