4 Reazione'di'HeckHMizoroki'
La!reazione!HeckDMizoroki,!riportata!indipendentemente!da!Mizoroki!et.!al!18!e!Heck!et!
al. 17!è!certamente!uno!dei!metodi!chiave!per!la!formazione!di!legami!CDC.!Nel!corso!degli!
anni! sono! state! sviluppate! varianti! intermolecolari! e! intramolecolari,! spesso! regioD! e! stereoDselettive,! al! fine! di! raggiungere! elevate! selettività! e! rese.! Questa! reazione! catalizzata!da!palladio!è!il!più!efficiente!metodo!per!la!vinilazione!di!alogenuri!arilici!o! vinilici.! Questa! reazione,! in! cui! è! formato! un! legame! C–C,! procede! in! presenza! di! una! base!(Schema!4D1).!
!
Schema 4-1 Reazione di Heck
È!una!reazione!estremamente!versatile!che!tollera!la!presenza!di!sostituenti!di!natura! diversa!sull’olefina,!quali!ad!esempio!gruppi!arilici,!vinilici,!esterei.!In!genere,!le!olefine! più!impiegate!sono!le!monosostituite,!dato!che!esse!presentano!una!maggiore!reattività,! anche! se! esistono! esempi! di! reazioni! condotte! in! presenza! di! olefine! tetrasostituite,! specialmente! nella! variante! intramolecolare.! La! scala! di! reattività! degli! alogenuri! è! la! stessa!delle!altre!reazioni!di!crossDcoupling!(I>!OTf!>!Br>>!Cl).!
La!reazione!di!Heck!è!meccanicisticamente!distinta!dalle!altre!reazioni!di!crossDcoupling,! con!le!quali!ha!in!comune!solo!il!primo!stadio!di!addizione!ossidativa.!Si!ipotizza!che!la! specie!attiva!sia!il!complesso!di!palladio(0)!coordinativamente!insaturo!a!14!elettroni.! La!reazione!inizia!quando!il!catalizzatore!attivato!reagisce!con!l’alogenuro!organico!nello! stadio! di! addizione! ossidativa.! Il! complesso! di! palladio(II)! formatosi! risulta! molto! più! elettrofilo!rispetto!al!suo!precursore!e!questo!facilità!la!coordinazione!dell’olefina.!Nello! stadio!successivo!si!ha!la!formazione!del!nuovo!legame!carbonio–carbonio!insieme!a!un! nuovo! legame! palladio–carbonio.! Questo! stadio! della! reazione! è! verosimilmente! responsabile! della! regioselettività! e! della! stereoselettività! del! ciclo! catalitico.! La! fase! finale! del! processo! prevede! la! β–eliminazione! di! un! idruro! e! l’allontanamento! del! prodotto! dal! metallo:! in! questo! stadio! si! ha! la! formazione! di! un! complesso! di!
R1 H R3 R2 + R4-X R1 R4 R3 R2 cat. [Pd0L n] base R4 = aril, benzil, vinil
palladio(II)–idruro! che! verrà! ridotto! in! seguito! dalla! base,! ripristinando! la! specie! di! palladio(0)!(Schema!4D2).!
!
Schema 4-2 Ciclo catalitico della reazione di Heck 111
A!differenza!della!reazione!di!Suzuki,!il!coupling!di!Heck!può!portare!alla!formazione!di! regioisomeri!e!di!stereoisomeri.!Il!gruppo!organico!R!dell’alogenuro!può!infatti!legarsi! ad! uno! dei! due! atomi! di! carbonio! del! doppio! legame! in! dipendenza! sia! da! fattori! elettronici!che!sterici.!Con!olefine!non!funzionalizzate!gli!effetti!sterici!prevalgono!ed!il! gruppo! R! si! lega! al! carbonio! meno! sostituito.! Con! olefine! elettronDpovere! gli! effetti! sterici!ed!elettronici!solitamente!favoriscono!il!prodotto!di!addizione!al!carbonio!meno! ingombrato!stericamente,!cioè!quello!terminale.!Con!olefine!elettronDricche!i!due!effetti! si!contrastano,!e!si!ottengono!in!genere!miscele!di!più!prodotti!(Figura!4D1).!
!
Figura 4-1 Regioselettività in olefine sostituite
La! reazione! di! Heck! è! condotta! con! catalizzatori! di! Pd,! generalmente! Pd(OAc)2,! in!
eccesso! di! legante! fosfinico,! e! in! presenza! di! una! base! organica! o! inorganica! che! ha! l’importante!funzione!di!intervenire!dopo!lo!stadio!di!deidropalladazione!a!ripristinare! la!specie!cataliticamente!attiva!di!Pd(0).!!
! Già!a!partire!dal!1973!il!lavoro!pioneristico!di!Julia!et!al.!aveva!permesso!l’impiego!di! Pd/C!per!questa!reazione,!e!da!allora!è!stato!il!catalizzatore!eterogeneo!più!importante! grazie!alla!sua!efficienza!e!alla!sua!diffusione!commerciale. 112! In!questi!primi!studi!lo!stirene!era!fatto!reagire!con!cloruri!o!ioduri!aromatici!dando!rese! di!circa!il!50%!nei!casi!più!favorevoli!(Schema!4D3).!Le!rese!migliori!vennero!ottenute!in! metanolo!a!120°C!in!autoclave,!con!conversioni!dello!stirene!dell’80%!e!selettività!del! 75%.! È! stato! osservato! che! l’uso! di! trifenilfosfina,! un! legante! tipico! della! reazione! di! Heck! condotta! in! fase! omogenea,! inibisce! la! reazione! invece! che! promuoverla.! Per! questa!ragione!negli!studi!successivi!è!stato!abbandonato!l’uso!di!leganti.!!
!
Schema 4-3 Reazione di Heck catalizzata da Pd/C tra clorobenzene e stirene
Le!reazioni!eterogenee!catalizzate!da!Pd/C!hanno!giunto!un!grado!di!efficienza!tale!da! poter! essere! usate! industrialmente! per,! ad! esempio,! il! coupling! dell’1DbromoD4D metossibenzene! con! ottilacrilato! per! la! produzione! di! ottil! 4Dmetossicinnamato,! un! importante!assorbitore!UV!usato!nella!produzione!di!creme!solari!(Schema!4D4)."113,114!
!
Schema 4-4 Reazione di Heck tra 1-bromo-4-metossibenzene e ottilacrilato
Un’analisi! molto! dettagliata! riguardo! l’applicazione! di! Pd/C! con! bromuri! arilici! e! differenti!olefine!è!stata!svolta!da!Köhler!et!al.!testando!catalizzatori!che!differivano!per! dispersione,! distribuzione! e! stato! di! ossidazione! del! metallo,! nonché! nel! contenuto! di! acqua."115,116!
Gli! esperimenti! condotti! hanno! evidenziato! un! meccanismo! (quasi)Domogeneo,! in! cui! i! complessi! di! palladio! o! le! particelle! colloidali! in! soluzione! agivano! da! specie! attive.! Lavorando! nelle! migliori! condizioni! individuate,! ovvero! NDmetilpirrolidinone! come! solvente!ed!acetato!di!sodio!come!base!a!140°C!in!atmosfera!di!argon!per!diminuire!il! rilascio! mantenendo! l’elevata! attività! catalitica,! ottengono! TON! fino! a! 36000,! di! due!
Cl + Pd/C, MeOH Na2CO3, 120°C, 4 h autoclave (E, Z) 62% O OOct Br + Pd/C MeO OOct O MeO
ordini! di! grandezza! inferiori! a! quelli! ottenuti! con! catalizzatori! omogenei! nella! stessa! reazione."117!
Prove! che! il! metallo! rilasciato! dal! supporto! sia! effettivamente! il! catalizzatore! della! reazione!sono!state!descritte!anche!da!Arai!e!collaboratori!nel!caso!d’impiego!di!ioduri! arilici! in! NDmetilpirrolidinone! e! carbonato! di! sodio.! Tuttavia,! quasi! tutto! il! palladio! disciolto!in!soluzione!si!rideposita!sul!supporto!a!fine!reazione,!permettendone!il!riciclo! senza! perdita! di! attività.! Nel! caso! dei! bromuri! e! dei! cloruri,! invece,! il! catalizzatore! è! risultato! possedere! una! bassa! attività,! fornendo! principalmente! prodotti! di! dealogenazione.!
La! reazione! di! Heck! è! stata! ampiamente! studiata! per! quanto! riguarda! l’impiego! di! nanoparticelle!magnetiche!come!supporto!del!metallo!catalitico.!
Per! quanto! riguarda! i! catalizzatori! trattati! con! leganti,! He! e! i! suoi! collaboratori! hanno! sintetizzato!un!catalizzatore!basato!su!palladio!supportato!su!magnetite!pretrattata!con! (3Damminopropil)trimetossisilano! (APTES).! Il! palladio(0)! è! stato! legato! alla! superficie! tramite!riduzione!di!Pd(OAc)2.!118!
!
Schema 4-5 Sintesi ed attività catalitica di Pd@APTES/Fe3O4
Il!catalizzatore!è!stato!applicato!al!crossDcoupling!dello!iodobenzene!con!acido!acrilico!in! presenza!di!Na2CO3!in!acetonitrile!acquoso.!Gli!esperimenti!di!riciclo!hanno!dimostrato!
un!calo!di!resa!dall’81%!del!primo!impiego!fino!al!53%!del!quinto;!la!resa!è!poi!rimasta! costante! nelle! successive! prove.! La! diminuzione! della! resa! è! stata! attribuita! all’aggregazione!delle!particelle!di!magnetite,!con!perdita!di!area!superficiale!e!difficoltà! nel!disperdere!il!catalizzatore.!
Li!e!Ma!hanno!preparato!un!catalizzatore!di!palladio!supportato!su!magnetite!attraverso! la! tecnica! di! coDprecipitazione! a! partire! da! nitrato! di! ferro! (III)! e! PdCl2! a! temperatura!
Fe3O4 Fe3O4 Fe3O4 APTES Pd(OAc)2 Na2CO3/H2O DMF, 50°C, 16 h Pd@APTES/Fe3O4 = Si O O O NH2 Fe3O4 I OH O + OH O Pd@APTES/Fe3O4 (15 mg) Na2CO3, MeCN/H2O riflusso, 12 h
ambiente.! La! soluzione! è! stata! basificata! con! Na2CO3! fino! a! pH! 8.5! e! lasciata! sotto!
agitazione!per!24!h.!Il!prodotto!è!stato!seccato,!calcinato!ed!infine!ridotto!con!H2.!!
!
!
Schema 4-6 Attività catalitica del catalizzatore supportato Pd/Fe3O4
L’attività! catalitica! è! stata! testata! in! una! razione! di! Heck! tra! bromuri! e! ioduri! arilici! e! alcheni!in!NMP!ed!ha!dato!rese!tra!il!54%!e!>99%!a!seconda!dell’alogenuro!impiegato.!È! stato! testato! anche! il! riciclo! del! catalizzatore! ed! ha! mostrato! attività! invariata! per! almeno!sei!cicli!catalitici,!mentre!il!rilascio!è!risultato!trascurabile.!
Lo!stesso!sistema!catalitico!messo!a!punto!da!Manorama!per!la!reazione!di!Suzuki!(pag.! 44)! è! stato! impiegato! anche! per! il! coupling! di! Heck! tra! cloruri! arilici! e! stirene! in! presenza!di!K2CO3!e!DMF!a!130°C;!anche!in!questo!caso!gli!autori!hanno!ottenuto!buone!
rese!sia!con!i!cloruri!che!con!gli!altri!alogenuri.!102!Gli!autori!imputano!l’elevata!attività!
all’alta! dispersione! delle! nanoparticelle! di! palladio! ed! all’effetto! stabilizzante! della! dopamina.!
!
!
Schema 4-7 Sintesi e attività catalitica di Pd@DA/NiFe2O4 nella reazioni di Suzuki
Anche!Laska!(pag.!45)!ha!approfondito!il!suo!studio!entrando!nel!merito!di!una!reazione! di! Heck! ed! ha! ottenuto! risultati! migliori! rispetto! a! quelli! osservati! nell’applicazione! al! crossDcoupling!di!Suzuki,!lavorando!a!130°C!in!NMP!in!presenza!di!un!carico!di!palladio! pari!al!5%.!!
In!questo!caso,!il!palladio!metallico!ha!dato!ottimi!risultati,!ed!è!stato!possibile!riciclarlo! almeno! tre! volte! senza! visibile! diminuzione! delle! prestazioni,! così! come! l’acetato! di! palladio!impregnato!su!particelle!magnetiche!(MNPD[Pd(OAc)2]),!mentre!il!catalizzatore!
formato! da! nanoparticelle! di! magnetite! funzionalizzate! con! bis(trifenilfosfina)palladio(ii)!diacetato!!(MNPD[Pd(TPP) (OAc) ])!ha!mostrato!un!netto!
X
R + Z R Z
5.0 mol% Pd/Fe3O4
NMP, K2CO3, 130°C R: H, 4-Me, 4-NO2, 4-COMe
Z: Ph, CO2tBu 5-12 h 53.6, >99 X: Br, I R X (1.2 equiv) 45-130°C, 24-36 h R Pd@DA/NiFe2O4 (50 mg) K2CO3 (3 equiv), DMF (1.0 equiv) X = Cl, Br, I
R = H, Me, Ac, OMe, NO2 +
calo! di! attività! a! partire! dal! secondo! riciclo,! a! causa! dell’aggregazione,! confermata! tramite! TEM,! delle! nanoparticelle,! che! ne! ha! diminuito! l’area! superficiale! e! quindi! la! disponibilità!di!siti!attivi.!
!
!
Schema 4-8 Reazione di Heck catalizzata da MNP impregnate con diversi precursori
Per! stabilire! quali! fossero! le! condizioni! migliori! nelle! quali! testare! i! catalizzatori! magnetici!oggetto!di!questo!lavoro!di!Tesi,!abbiamo!effettuato!alcune!prove!prendendo!a! riferimento! le! condizioni! operative! utilizzate! con! i! più! comuni! catalizzatori! eterogenei! solitamente!impiegati.!!
Köhler!riporta,!ad!esempio,!l’impiego!di!Pd/C!in!dimetilacetammide!(DMA)!in!presenza! di!acetato!di!sodio!per!dare!con!rese!pressoché!quantitative!i!due!isomeri!del!prodotto"
119.! Nota! anche! come! il! rilascio! sia! fortemente! influenzato! dalla! temperatura,!
risultando! minore! a! temperature! più! elevate.! Questo! può! essere! spiegato! imputando! l’andamento! alla! stabilità! delle! specie! di! palladio! cataliticamente! attive! in! soluzione,! minore! alle! alte! temperature.! Osservano! inoltre! che! il! rilascio! è! identico! in! NDmetilD pirrolidinone!(NMP),!mentre!è!più!basso!in!toluene,!solvente!in!cui!la!reazione!però!non! avviene.!Per!il!catalizzatore!studiato!non!è!stata!individuata!una!relazione!significativa! tra!l’atmosfera!impiegata!(argon!o!aria)!e!l’attività!catalitica,!mentre!è!stata!rilevata!un! rilascio!del!26%!del!palladio!nel!caso!in!cui!la!reazione!sia!stata!condotta!in!aria,!rispetto! al!rilascio!modesto!del’1%!in!atmosfera!di!argon.! Sono!state!applicate!quindi!le!condizioni!riportate!da!Köhler!anche!alle!nostre!prove!di! attività.! Sono! stati! fatti! reagire! bromoacetofenone! e! stirene! (1.5! equiv)! lavorando! in! DMA! a! 100°C! ed! impiegando! come! base! acetato! di! sodio! (1.2! equiv),! secondo! quanto! riportato! nello! Schema! 4D9.! Lavorando! a! 100°C! il! nostro! catalizzatore! ha! mostrato! un’attività!inferiore!al!palladio!su!carbone!commerciale,!come!riportato!in!Tabella!4D1,! prove! 1,2;! abbiamo! quindi! deciso! di! spingere! le! condizioni! aumentando! il! carico! catalitico! e! la! temperatura,! con! il! risultato! di! aver! ottenuto! rese! superiori! al! 50%! in! tempi!notevolmente!inferiori,!avendo!ridotto!il!tempo!necessario!da!venti!ore!a!una!sola,! come!riportato!in!prova!4.! Br NO2 MNP-Pd cat. (5 mol% Pd) NMP, KOAc, 130°C + NO2 Catalizzatore MNP-[Pd(OAc)2] MNP-[Pd(TPP)2(OAc)2] MNP-Pd(0) MNP nuda Conversione (%) 100 >99 >99 0
È!stata!inoltre!effettuata!una!prova!anche!in!NMP,!notando!che,!come!nell’articolo!citato,! la!reattività!è!stata!pressoché!identica.!!
!
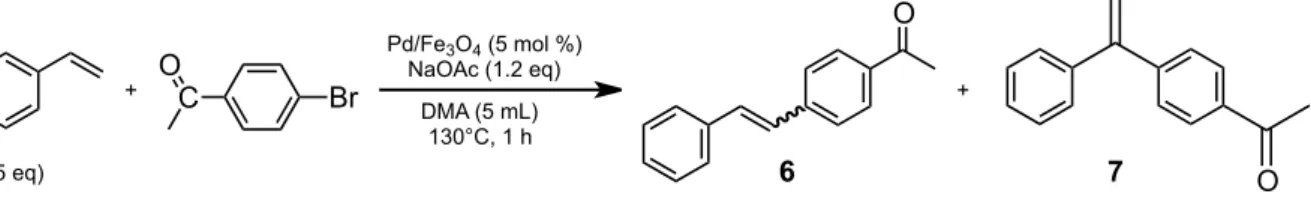
Schema 4-9 Reazione di Heck studiata in questo lavoro di Tesi
Il!catalizzatore!è!stato!confrontato!anche!in!questo!caso!con!Pd/C!al!5%!della!Engelhard,! Pd/Al2O3! al! 5%! della! Aldrich,! palladio! impregnato! su! magnetite! nanometrica!
commerciale! della! Aldrich! e! successivamente! con! vari! metodi! di! preparazione! del! catalizzatore!bimetallico.!
Per!semplicità!sono!riportate!in!Tabella!4D1!le!rese!dei!vari!catalizzatori:!
Tabella 4-1 Risultati ottenuti per la reazione di Heck
Prova" Catalizzatore" Carica"cat."[mol"%]" T"[°C]" Durata"[h]" Resa"[%]a"
1! Pd/C! 0.1! 100! 20! 66! 2! A! 0.1! 100! 20! 17! 3! Pd/C! 5! 130! 1! 66! 4! A! 5! 130! 1! 55! 5b! A! 5! 130! 21! 50! 6c! Fe3O4! D! 130! 1! D! 7! Pd/Al2O3! 5! 130! 1! 26! 8! D! 5! 130! 1! 3! 9! E! 5! 130! 1! 5! 10! E! 5! 130! 24! 40! La!reazione!è!stata!condotta!impiegando!1!mmol!di!pDbromoacetofenone,!1.5!mmol!di!stirene,!1.2!mmol!di!NaOAc,!5!ml!di!DMA.!! a!resa!GLC! b!reazione!condotta!in!NMP,!base!K2CO3! c!la!quantità!di!magnetite!impiegata!è!pari!a!100!mg,!pari!alla!quantità!introdotta!aggiungendo!5!mol!%!di!catalizzatore!al!5%!di!Pd! !
In! Tabella! 4D1! vediamo! che! il! catalizzatore! magnetico! bimetallico! prodotto! per! via! idrotermale! (catalizzatore! A)! mostra! una! resa! in! prodotto! 6! minore! del! Pd/C! commerciale,!imputabile!alla!migliore!stabilità!del!nostro!catalizzatore!nelle!condizioni! di!reazione!e!quindi!al!minore!rilascio!in!soluzione,!dato!che!è!noto!in!letteratura!che!la! reazione! proceda! in! fase! omogenea." 51! Il! prodotto! 7" risulta! essere! presente! solo! in!
tracce,!<!3%!da!analisi!GLC.!! Aumentando!il!carico!catalitico!e!la!temperatura!è!stato!possibile!ridurre!notevolmente!i! Br C O O + Pd/Fe3O4 (5 mol %) NaOAc (1.2 eq) DMA (5 mL) 130°C, 1 h (1.5 eq) O + 6 7
preparato!per!via!idrotermale,!risulta!avere!un’attività!paragonabile!a!quella!del!palladio! su! carbone! e! nettamente! maggiore! del! palladio! su! allumina,! mentre! le! prestazioni! dei! catalizzatori! prodotti! per! impregnazione! (D! ed! E)! sono! paragonabili! tra! loro,! ma! insufficienti! in! senso! generico.! Aumentando! i! tempi,! la! reazione! procede! anche! con! il! catalizzatore!impregnato!E,!dando!però!risultati!modesti!(prova!10).!!
Dai!risultati!della!prova!cinetica!condotta!con!il!catalizzatore!A!(Figura!4D2),!si!nota!la! presenza! di! un! periodo! d’induzione! in! cui! la! velocità! di! reazione! è! ridotta,! per! poi! aumentare! la! velocità! dopo! 30! minuti! circa.! Questo! fenomeno,! che! si! verifica! nella! catalisi!eterogenea!della!Heck,!è!noto!in!letteratura!ed!è!spiegato!tramite!l’esistenza!di! un!periodo!d’induzione!corrispondente!al!rilascio!del!metallo!catalitico!dal!supporto.!120!!
!
!
Figura 4-2 Andamento cinetico della reazione di Heck
0! 10! 20! 30! 40! 50! 60! 70! 80! 90! 100! 0! 10! 20! 30! 40! 50! 60! 70! Resa"[%]" Tempo"[min]"

![Figura 4-2 Andamento cinetico della reazione di Heck 0!10!20!30!40!50!60!70!80!90!100!0!10!20!30!40!50! 60! 70!Resa"[%]"Tempo"[min]"](https://thumb-eu.123doks.com/thumbv2/123dokorg/7627311.116874/8.892.131.774.455.808/figura-andamento-cinetico-reazione-heck-resa-tempo-min.webp)