VIII
CLINICA E DIAGNOSI DELLA MALATTIA DI MENIÈRE
1. Introduzione
Secondo i criteri del “Committee on Hearing and Equilibrium of the AAO-HNS” del 1995, la MdM è:
“una malattia definita come la sindrome idiopatica dell’idrope endolinfatico. Questa sindrome è caratterizzata dalla presenza di vertigine episodica spontanea ricorrente, ipoacusia, sensazione di ovattamento auricolare (fullness) e acufeni”.
Il 60% dei pazienti sviluppa l’intero complesso dei sintomi entro 6 mesi; il 30% presenta all’esordio ipoacusia e/o acufeni; nel 20% la malattia esordisce con la vertigine (Morrison AW, 1975).
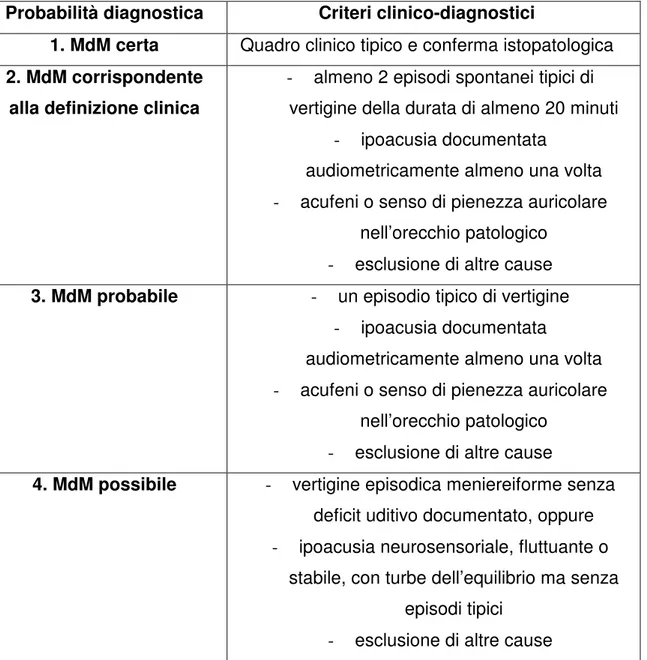
In base ai criteri clinici del 1995, sono distinguibili quattro livelli diagnostici di MdM (tabella I).
Probabilità diagnostica Criteri clinico-diagnostici
1. MdM certa Quadro clinico tipico e conferma istopatologica 2. MdM corrispondente
alla definizione clinica
- almeno 2 episodi spontanei tipici di vertigine della durata di almeno 20 minuti
- ipoacusia documentata
audiometricamente almeno una volta - acufeni o senso di pienezza auricolare
nell’orecchio patologico - esclusione di altre cause 3. MdM probabile - un episodio tipico di vertigine
- ipoacusia documentata
audiometricamente almeno una volta - acufeni o senso di pienezza auricolare
nell’orecchio patologico - esclusione di altre cause
4. MdM possibile - vertigine episodica meniereiforme senza deficit uditivo documentato, oppure - ipoacusia neurosensoriale, fluttuante o
stabile, con turbe dell’equilibrio ma senza episodi tipici
- esclusione di altre cause
Tabella I: Livelli diagnostici per la MdM in base al Committee on Hearing and Equilibrium, 1995
2. Ipoacusia
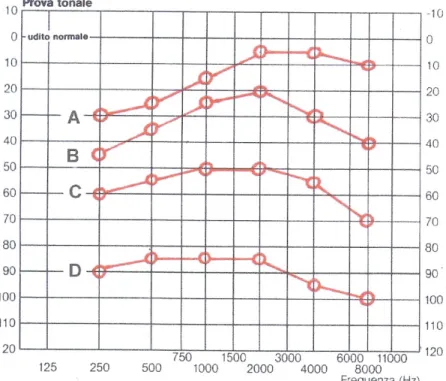
La chiave diagnostica della MdM è rappresentata dalla documentazione di un’ipoacusia fluttuante associata ad una storia clinica caratteristica. L'andamento della ipoacusia nel tempo segue una evoluzione che è simile in molti pazienti: inizialmente l'ipoacusia neurosensoriale di 10-15 dB, coinvolge le basse frequenze (250-500 Hz) con una curva in salita (Figura 6, curva A) (Katsarkis A, 1996), al contrario di quanto succede nelle ipoacusie di altra causa, quali agenti ototossici o trauma acustico. Successivamente l’ipoacusia si accentua alle basse frequenze, presenta una soglia minore a 2.000 Hz, e peggiora anche alle alte frequenze (peaked pattern) (Figura 6, curva B). Nelle forme di ipoacusia di più vecchia data la soglia aumenta per tutte le frequenze e la curva diventa piatta (Figura 6, curva C) con una soglia media molto variabile (Green JD Jr et al, 1991; Katsarkis A, 1996), ma che si attesta mediamente fra i 60-70 dB. Talvolta raggiunge valori di 90-100 dB (Figura 6, curva D) (Stahle J et al, 1991).
Figura 6: curve audiometriche
Inizialmente l'ipoacusia è fluttuante soprattutto per le basse frequenze nel 50-70% dei casi (Green JD Jr et al, 1991), ed il test al glicerolo è positivo. Questo test, che permette di dimostrare il recupero uditivo, non viene accettato da tutti perché in quasi il 10% dei pazienti, il glicerolo provoca violenti cefalee, nausea e vomito. Oggi viene comunque impiegato come test diagnostico soprattutto nelle fasi precoci della MdM (Magliulo G et al, 2004).
La discriminazione vocale rimane buona soprattutto nelle fasi iniziali del danno uditivo, ed il recruitment, dimostrabile anche con lo studio del riflesso stapediale, conferma la sede cocleare della malattia. Il
recruitment è responsabile dell’iperacusia, un sintomo riferito come molto fastidioso dai pazienti (Herraiz C et al, 2006). Anche una diplacusia, cioè la percezione di un tono con intensità diversa nei due orecchi, è indicativa della localizzazione cocleare dell’affezione (Brookes GE e Coelho A, 1994).
Le otoemissioni acustiche in anni recenti sono state utilizzate per cercare di classificare in senso topografico le ipoacusie. Nella diagnosi di MdM però, le otoemissioni acustiche non si sono dimostrate di grande aiuto. Gli unici dati di rilievo sono rappresentati dal fatto che se l'ipoacusia è superiore a 30-40dB, le otoemissioni acustiche sono assenti e se la loro ampiezza è minore nell'orecchio controlaterale, potremmo aspettarci un’evoluzione bilaterale della malattia (Lonsbury-Martin BL e Martin GK, 1990).
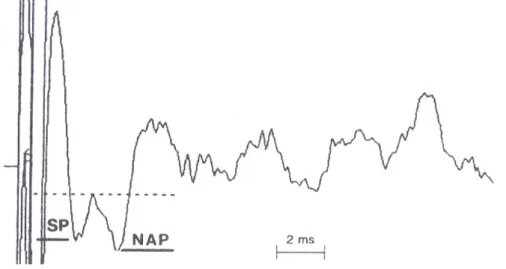
L'elettrococleografia (ECoG) al contrario, può essere di grande utilità nella diagnosi di MdM (Gibson WP, 1991): il potenziale di sommazione (SP), infatti, è significativamente più alto nei pazienti menierici. L'aumento di SP è correlato con la distensione della membrana basilare verso la scala timpanica, caratteristica propria dell'idrope endolinfatico. L'ampiezza di SP, però, presenta una notevole variazione individuale; per questo è stato introdotto il concetto di SP/NAP ratio, cioè del rapporto tra ampiezza del potenziale di sommazione e potenziale d'azione del nervo cocleare
(Eggerment JJ, 1979). Si può fare diagnosi di idrope endolinfatico se il rapporto è superiore al 35% (Figura 7).
Figura 7: Tracciato elettrococleografico
Allo stato attuale, la EcoG è considerata il metodo obiettivo migliore nel dimostrare un idrope endolinfatico: indubbiamente, l’aumento di SP e la gravità della MdM sono proporzionali (Wuyts FL et al, 2001). Appare evidente come il valore diagnostico dell'EcoG sia importante se il test è positivo, ma se il SP/NAP ratio è inferiore al 35%, non si può escludere che l'idrope non si sia risolta spontaneamente prima dell'esecuzione del test.
I potenziali evocati acustici (BAEP; Brainstem Auditory Evoked Potentials) sono un mezzo diagnostico obiettivo e non invasivo, che permette di individuare precocemente lesioni subcliniche del
sistema uditivo e di rilevare anche sordità parziali o unilaterali. Il tracciato è costituito da onde identificate con i numeri romani da I a VII. Ciascuna di queste onde corrisponde ad una determinata componente della via acustica. Questa relazione tra potenziale elettrico e struttura anatomica consente di localizzare con notevole precisione le lesioni della via acustica. In presenza di idrope endolinfatico, è alterata l’onda V (Don M et al, 2005).
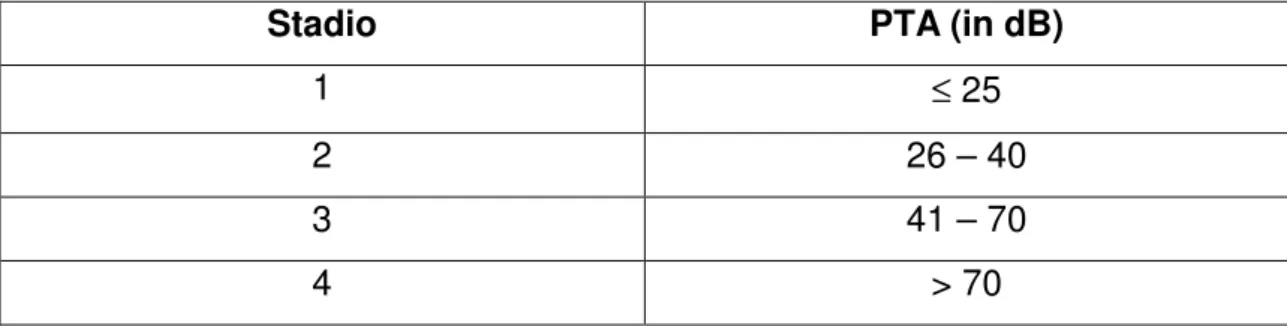
In base alla perdita uditiva, calcolata eseguendo la media aritmetica dei valori di soglia tonale per 0,5; 1; 2; 3 KHz (PTA; pure tone average) dell'audiogramma peggiore del semestre antecedente la prima osservazione, la MdM può essere differenziata in 4 stadi (tabella II), utilizzabili soprattutto per monitorare l'evoluzione dei risultati terapeutici.
Stadio PTA (in dB)
1 ≤ 25
2 26 – 40
3 41 – 70
4 > 70
Tabella II: Classificazione dell’ipoacusia in base ai criteri del Committee on Hearing and Equilibrium, 1995
2. Fullness
Una sensazione di pressione o pienezza auricolare (fullness) non è un sintomo che fa parte della triade sintomatologica classica, ma viene riferito frequentemente (50-75%), e può risultare molto fastidioso per il paziente (Green JD Jr et al, 1991). Spesso la sensazione di fullness precede la crisi di vertigine, come se fosse una "specie" di aura. Una spiegazione soddisfacente di questo sintomo non è ancora stata formulata, tuttavia, alcuni Autori (Choo D et al, 2004) sottolineano la possibilità che la sensazione di fullness sia legata ad una distensione del labirinto membranoso. Spesso la fullness segue l’andamento delle fluttuazioni dell’ipoacusia: quando essa si stabilizza, anche la fullness scompare (Tokumasu K et al, 1996).
3. Acufeni
Gli acufeni fanno parte della triade sintomatologica della MdM. Essi possono persistere anche dopo la fine dell'attacco di vertigine o dopo la stabilizzazione dei sintomi. Hanno un'intensità fluttuante e sono in genere percepiti nella crisi acuta come un rumore forte di tonalità grave, o, nei periodi intercritici, come rumore di tonalità
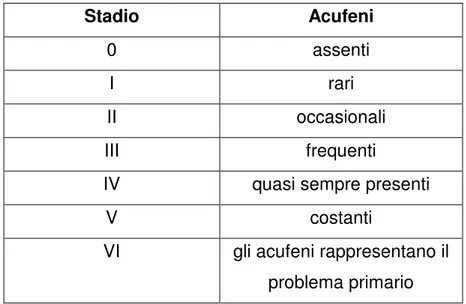
acuta (fischio) costante (Herraiz C et al, 2006). Il substrato fisiopatologico degli acufeni è da correlarsi con il danno cocleare. Secondo i criteri dell’American Academy del 1995, gli acufeni sono difficilmente classificabili. Stahle (1981) ha proposto una classificazione in sette classi (tabella III).
Stadio Acufeni
0 assenti
I rari
II occasionali
III frequenti
IV quasi sempre presenti
V costanti
VI gli acufeni rappresentano il problema primario
Tabella III: classificazione degli acufeni secondo Stahle, 1981
4. Vertigini
La MdM è caratterizzata da crisi ricorrenti di vertigine oggettiva, spesso accompagnate da sintomi neurovegetativi (nausea, vomito). La frequenza degli attacchi è irregolare e non preventivabile: alcuni pazienti presentano un singolo attacco di vertigine nell'arco di molti anni, altri invece presentano più crisi la settimana (Stahle J, 1991).
La durata dell'attacco varia da alcuni minuti ad alcune ore, ma mai secondi. L'unica eccezione è rappresentata dalla prima crisi, che in alcuni pazienti dura più di 24 ore. In genere, nelle fasi avanzate, la vertigine oggettiva lascia spazio ad un costante senso di instabilità (Mateijsen DJ et al, 2001).
Alcuni Autori hanno osservato una diminuzione della gravità e del numero delle crisi nelle forme di MdM di più vecchia data (Stahle J, 1991).
L'esame vestibolare può rendere evidente, all'inizio della fase acuta, per un periodo molto breve, un nistagmo (ny) spontaneo diretto verso il lato patologico di tipo irritativo (cosiddetto ny da intossicazione di potassio); successivamente si osserva un ny di tipo paralitico che batte verso il lato sano. Il test calorico mostra un deficit labirintico dal lato patologico. Nelle fasi iniziali, durante il periodo intercritico, il test calorico si può normalizzare, ma nelle fasi avanzate rimarrà evidente il deficit.
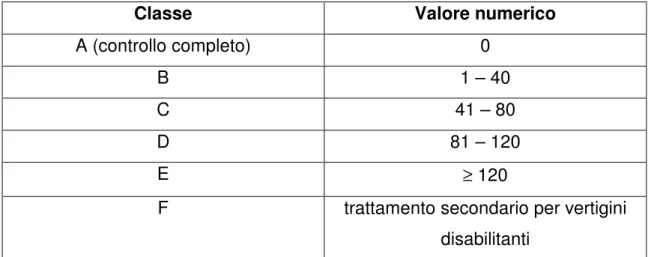
In base ai criteri del 1995, si distinguono cinque gradi di controllo sintomatologico delle vertigini (classi A-F) in base a dei valori numerici ottenuti dal rapporto tra il numero medio delle crisi nei sei mesi precedenti la terapia ed il numero delle crisi nei 6 mesi (tra il 18esimo ed il 24esimo mese) terminata la terapia x100 (tabella IV).
Classe Valore numerico A (controllo completo) 0 B 1 – 40 C 41 – 80 D 81 – 120 E ≥ 120
F trattamento secondario per vertigini disabilitanti
Tabella IV: Classificazione del controllo sintomatologico delle vertigini in base ai criteri del Committe on Hearing and Equilibrium,
1995
5. Diagnosi differenziale
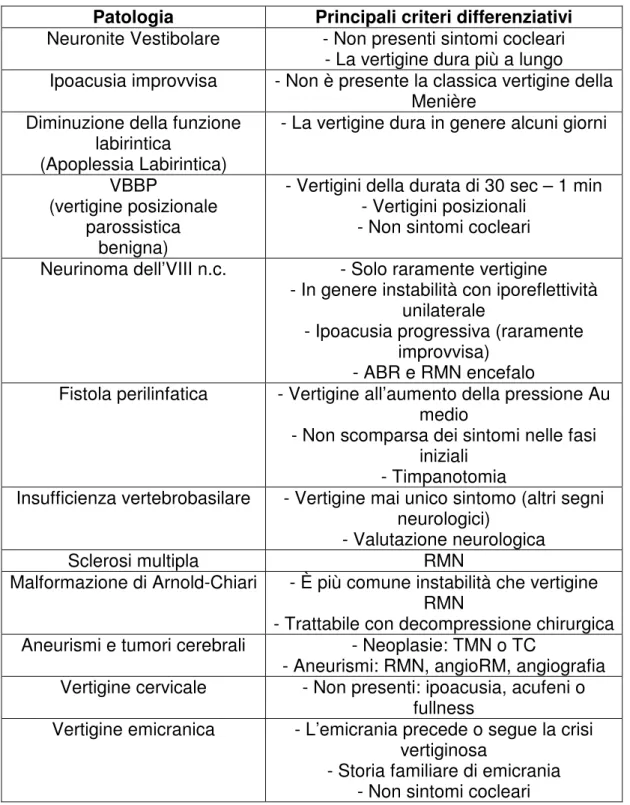
La tabella III riassume le patologie per le quali è necessario effettuare una diagnosi differenziale con la MdM, elencando alcuni semplici criteri di differenziazione, sia di tipo clinico, sia di tipo strumentale.
Patologia Principali criteri differenziativi Neuronite Vestibolare - Non presenti sintomi cocleari
- La vertigine dura più a lungo Ipoacusia improvvisa - Non è presente la classica vertigine della
Menière Diminuzione della funzione
labirintica
(Apoplessia Labirintica)
- La vertigine dura in genere alcuni giorni
VBBP
(vertigine posizionale parossistica
benigna)
- Vertigini della durata di 30 sec – 1 min - Vertigini posizionali
- Non sintomi cocleari Neurinoma dell’VIII n.c. - Solo raramente vertigine
- In genere instabilità con iporeflettività unilaterale
- Ipoacusia progressiva (raramente improvvisa)
- ABR e RMN encefalo
Fistola perilinfatica - Vertigine all’aumento della pressione Au medio
- Non scomparsa dei sintomi nelle fasi iniziali
- Timpanotomia
Insufficienza vertebrobasilare - Vertigine mai unico sintomo (altri segni neurologici)
- Valutazione neurologica
Sclerosi multipla RMN
Malformazione di Arnold-Chiari - È più comune instabilità che vertigine RMN
- Trattabile con decompressione chirurgica Aneurismi e tumori cerebrali - Neoplasie: TMN o TC
- Aneurismi: RMN, angioRM, angiografia Vertigine cervicale - Non presenti: ipoacusia, acufeni o
fullness
Vertigine emicranica - L’emicrania precede o segue la crisi vertiginosa
- Storia familiare di emicrania - Non sintomi cocleari
Tabella V: Diagnosi differenziale tra MdM ed altre patologie otoneurologiche