10.0 RISULTATI
10.1 Caratteristiche dei pazienti
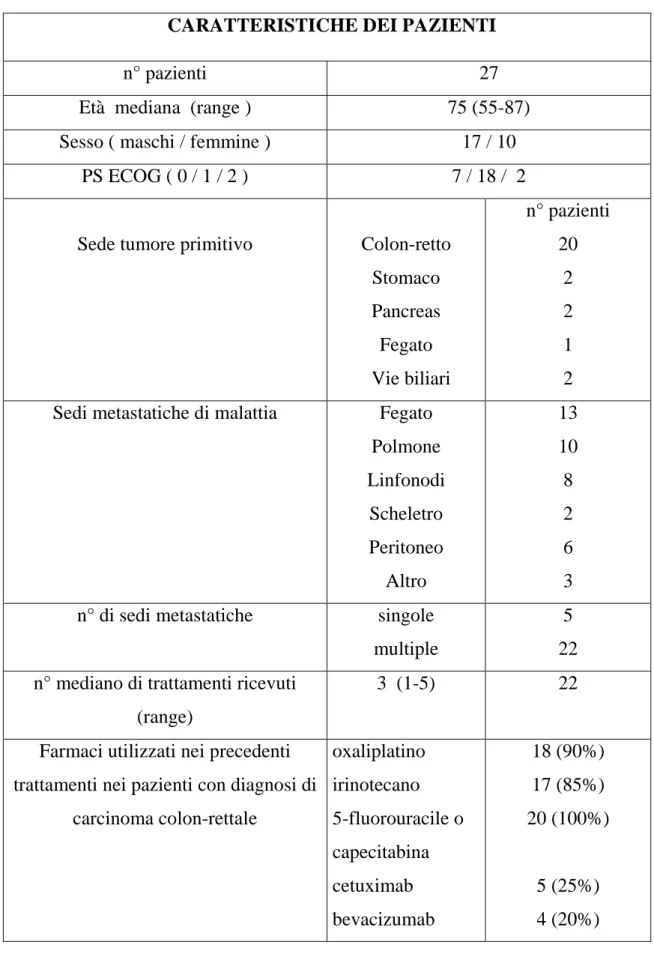
Ad oggi sono stati inseriti nello studio 27 pazienti. Le caratteristiche dei pazienti in studio sono riportate nella tabella n°1.
Tabella n°1: caratteristiche dei pazienti.
CARATTERISTICHE DEI PAZIENTI
n° pazienti 27
Età mediana (range ) 75 (55-87)
Sesso ( maschi / femmine ) 17 / 10
PS ECOG ( 0 / 1 / 2 ) 7 / 18 / 2
Sede tumore primitivo Colon-retto
Stomaco Pancreas Fegato Vie biliari n° pazienti 20 2 2 1 2 Sedi metastatiche di malattia Fegato
Polmone Linfonodi Scheletro Peritoneo Altro 13 10 8 2 6 3
n° di sedi metastatiche singole
multiple
5 22 n° mediano di trattamenti ricevuti
(range)
3 (1-5) 22
Farmaci utilizzati nei precedenti trattamenti nei pazienti con diagnosi di
carcinoma colon-rettale oxaliplatino irinotecano 5-fluorouracile o capecitabina cetuximab bevacizumab 18 (90%) 17 (85%) 20 (100%) 5 (25%) 4 (20%)
10.2 Tossicità globale e attività
In totale il numero mediano di settimane di terapia eseguite è stata di 12 (range 4-45). Il trattamento è stato ben tollerato dai pazienti, infatti non sono state osservate tossicità ematologiche e non ematologiche di grado superiore al I della scala NCI. In particolare è stata osservata unicamente una iper-transaminasemia transitoria di grado 2 nell’8% dei pazienti che non ha comportato interruzione del trattamento o riduzioni di dose. Al momento sono stati valutati 20 pazienti per la risposta al trattamento. Benché non siano state osservate risposte obiettive, 9 pazienti (45%) hanno riportato una stazionarietà del quadro di malattia con una durata mediana di 5.06 mesi (range 2.07+ - 8.52+). In particolare, delle 9 stazionarietà osservate 7 erano pazienti con diagnosi di carcinoma colon-rettale (su un totale di 15 pazienti valutabili) e 2 erano pazienti con diagnosi di carcinoma pancreatico (entrambi ancora in SD). Dei 20 pazienti valutabili sulla base dell’andamento dei marcatori tumorali, in un paziente (5%) abbiamo osservato una riduzione del CEA del 47% rispetto al valore basale dopo 4 settimane dall’inizio del trattamento e in 3 pazienti (15%) è stata osservata una stabilità dei valori del CEA di circa 12 settimane (range 8-20).
10.3 Tempo a progressione e sopravvivenza.
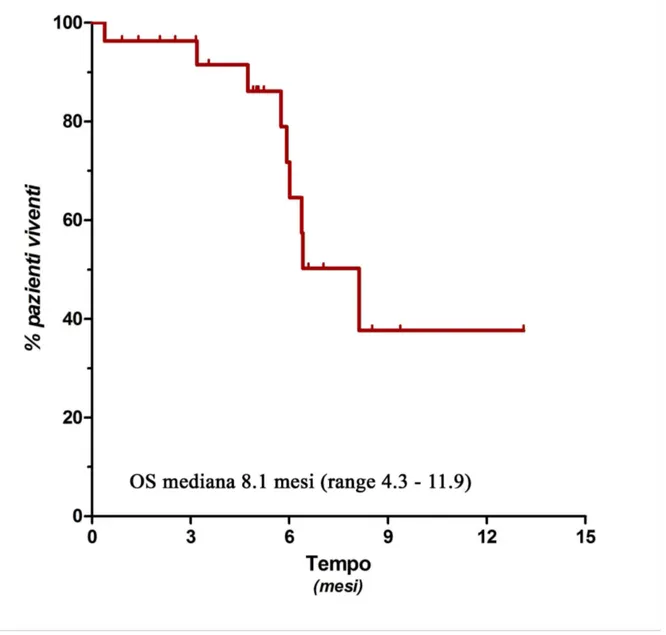
Dopo un follow up mediano di 6.6 mesi ( range 4.5 - 8.7) la durata mediana del tempo libero da progressione (PFS) e della sopravvivenza globale (OS) è risultata essere rispettivamente di 3.85 mesi (range 2.1 - 8.52+) e di 8,1 mesi (range 4.3 - 11.9). Nella figura n° 1 sono riportate le curve attuariali della PFS e della OS calcolate secondo il metodo di Kaplan-Meier.
Figura n°1: curve attuariali della PFS e della OS calcolate secondo il metodo di Kaplan-Meier.
10.4 Analisi farmacodinamica
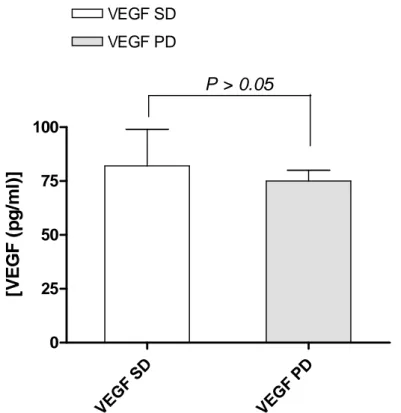
Ad oggi è stata valutata la concentrazione plasmatica del recettore solubile del VEGF (sVEGFR-2) e del VEGF su prelievi di sangue venoso periferico in un primo gruppo di 11 pazienti. L’ analisi preliminare è stata eseguita andando a confrontare le differenze tra le concentrazioni basali del sVEGFR-2 e del VEGF tra 6 pazienti con stabilità di malattia (SD) e 5 pazienti in progressione di malattia (PD). L’ analisi dei risultati ha evidenziato una differenza statisticamente significativa nelle concentrazioni del sVEGFR-2 basale tra il gruppo dei pazienti con SD e il gruppo dei pazienti in PD (rispettivamente 1671 pg/ml ± 110 vs 2058 pg/ml ± 113, p=0.038), mentre la differenza tra i livelli di concentrazione del VEGF è risultata essere non statisticamente significativa tra i due gruppi (rispettivamente 82 pg/ml ± 17 vs 75 pg/ml ± 5, p>0.05).
Nelle figure n°2 e n°3 sono riportate le concentrazioni medie basali del VEGF e del sVEGFR-2.
VE GF SD VE GF PD 0 25 50 75 100 VEGF SD VEGF PD P > 0.05 [V E G F ( p g /m l) ]
Figura n°2: concentrazioni medie basali del VEGF nei pazienti con SD e con PD.
VE GFR 2 S D VE GFR 2 P D 0 500 1000 1500 2000 2500 VEGFR2 SD VEGFR2 PD P = 0.038 [V E G F R 2 ( p g /m l) ]
Figura n°3: concentrazioni medie basali del sVEGR-2 nei pazienti con SD e con PD. 10.5 Analisi farmacocinetica
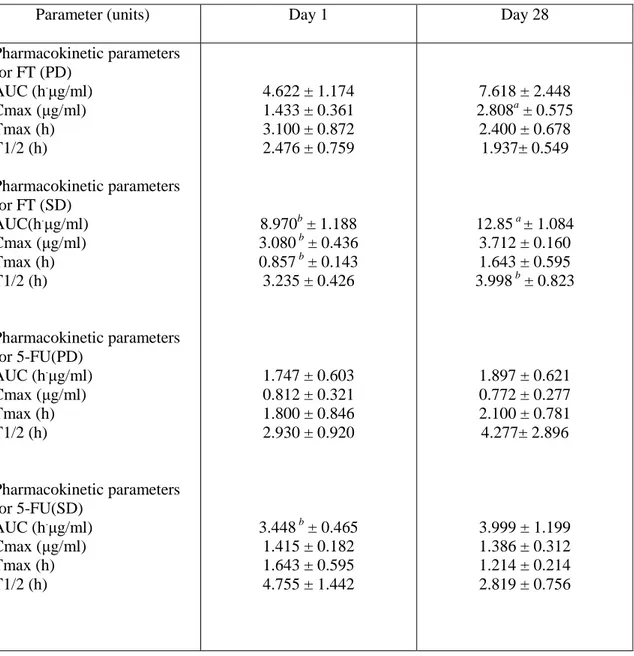
Per quanto riguarda la farmacocinetica, nei 6 pazienti con stabilità di malattia (SD) e nei 5 pazienti in progressione di malattia (PD) è stata eseguita un’analisi preliminare dei seguenti parametri: Area Under Curve (AUC), Concentrazione plasmatica Massima (Cmax), Tempo di picco Massimo (Tmax) ed Emivita (T1/2) del FT e del 5-FU. Al momento i dati ottenuti hanno dimostrato una differenza statisticamente significativa nei valori dell’AUC, della Cmax e del Tmax del FT al giorno 1 che risultano essere maggiori nei pazienti con SD vs i pazienti con PD (rispettivamente 8.970 h.µg/ml ± 1.188, 3.080 µg/ml ± 0.436, 0.857 h ± 0.143 vs 4.622 h.µg/ml ± 1.174, 1.433 µg/ml ± 0.361, 3.100 h ± 0.872) e del T1/2 al giorno 28 che risulta essere maggiore nei pazienti con SD vs i pazienti con PD (rispettivamente 3.998h ± 0.823 vs 1.937 h ± 0.549). Anche la differenza dell’AUC del 5-FU tra gruppo di pazienti con SD e gruppo di pazienti con PD è risultata essere statisticamente significativa (rispettivamente 3.448 h.µg/ml ± 0.465 vs 1.747 h.µg/ml ± 0.603). Sono state inoltre osservate delle differenze statisticamente significative nei valori della AUC del FT nei pazienti con SD al giorno 28 vs il giorno 1 (rispettivamente 12.85h.µg/ml ± 1.084 vs 8.970 h.µg/ml ± 1.188) e nei valori della Cmax del FT nei pazienti con PD al giorno 28 vs il giorno 1 (rispettivamente 2.808 µg/ml ± 0.575 vs 1.433 µg/ml ± 0.361).
Parameter (units) Day 1 Day 28 Pharmacokinetic parameters for FT (PD) AUC (h.µg/ml) Cmax (µg/ml) Tmax (h) T1/2 (h) Pharmacokinetic parameters for FT (SD) AUC(h.µg/ml) Cmax (µg/ml) Tmax (h) T1/2 (h) Pharmacokinetic parameters for 5-FU(PD) AUC (h.µg/ml) Cmax (µg/ml) Tmax (h) T1/2 (h) Pharmacokinetic parameters for 5-FU(SD) AUC (h.µg/ml) Cmax (µg/ml) Tmax (h) T1/2 (h) 4.622 ± 1.174 1.433 ± 0.361 3.100 ± 0.872 2.476 ± 0.759 8.970b ± 1.188 3.080 b ± 0.436 0.857 b ± 0.143 3.235 ± 0.426 1.747 ± 0.603 0.812 ± 0.321 1.800 ± 0.846 2.930 ± 0.920 3.448 b ± 0.465 1.415 ± 0.182 1.643 ± 0.595 4.755 ± 1.442 7.618 ± 2.448 2.808a ± 0.575 2.400 ± 0.678 1.937± 0.549 12.85 a ± 1.084 3.712 ± 0.160 1.643 ± 0.595 3.998 b ± 0.823 1.897 ± 0.621 0.772 ± 0.277 2.100 ± 0.781 4.277± 2.896 3.999 ± 1.199 1.386 ± 0.312 1.214 ± 0.214 2.819 ± 0.756 a p<0.05 giorno 28 vs giorno 1 b p<0.05 SD vs PD
AUC= area sotto la curva; Cmax= massima concentrazione plasmatica; Tmax= tempo di picco massimo; T1/2=
emivita del farmaco.
Tabella n°2: dati preliminari di farmacocinetica nei pazienti con SD e PD al giorno 1 e al giorno 28
A seguire riportiamo i grafici dell’andamento dei valori medi di concentrazione plasmatica del FT al giorno 1 (fig. n°4) e al giorno 28 (fig. n°5) e del 5-FU al giorno 1 (fig. n°6) e al giorno 28 (fig. n°7) nei 20 pazienti valutabili per risposta.
0 1 2 3 4 5 6 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 FT giorno1 pazienti in SD FT giorno 1 pazienti in PD Tempo (h) c o n c e n tr a z io n e T e g a fu r ( µµµµ g /m l)
Figura n°4: andamento dei valori medi di concentrazione plasmatica del FT al giorno 1 nei 20 pazienti.
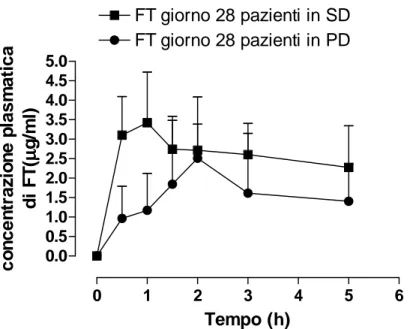
0 1 2 3 4 5 6 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 FT giorno 28 pazienti in SD FT giorno 28 pazienti in PD Tempo (h) c o n c e n tr a z io n e p la s m a ti c a d i F T ( µµµµ g /m l)
Figura n°5: andamento dei valori medi di concentrazione plasmatica del FT al giorno 28 nei 20 pazienti.
0 1 2 3 4 5 6 0.0 0.5 1.0 1.5 2.0 5-FU giorno1 SD 5-FU giorno1 PD Tempo (h) c o n c e n tr a z io n e p la s m a ti c a d i 5 -F U ( µµµµ g /m l)
Figura n°6: andamento dei valori medi di concentrazione plasmatica del 5-FU al giorno 1 nei 20 pazienti.
0 1 2 3 4 5 6 0.0 0.5 1.0 1.5 2.0 2.5 3.0
5-FU giorno 28 pazienti in SD 5-FU giorno 28 pazienti in PD
Tempo (h) c o n c e n tr a z io n e p la s m a ti c a d i 5 -F U ( µµµµ g /m l)
Figura n°7: andamento dei valori medi di concentrazione plasmatica del 5-FU al giorno 28 nei 20 pazienti.