INTRODUZIONE ALLA
PARTE SPERIMENTALE
Scopo della tesi Scopo della tesi Scopo della tesi Scopo della tesi
Da alcuni anni nel nostro laboratorio di ricerca sono allo studio
molecole con proprietà attivanti verso i canali al potassio BKCa;
molti dei composti scoperti rispondono ad un modello farmacoforico comune (fig. 1) costituito da :
- due ANELLI AROMATICI che possono essere simmetrici o no i quali portano siti donatori di legami a idrogeno e gruppi elettron-attrattori
- una unità spaziatrice detta regione LINKER che li lega e può essere ciclica, eterociclica o lineare.
Di solito uno dei due anelli aromatici è rappresentato da un gruppo o- idrossifenilico, infatti sembra che la funzione ossidrilica sia
indispensabile per conferire alla molecola l’attività di BK-opener e talvolta è presente anche un alogeno preferibilmente in posizione para rispetto all’ossidrile.
L’altro anello aromatico invece porta gruppi elettron-attrattori.
I primi composti attivi scoperti sono stati NS004 e NS1619 (111,21222) che pur non possedendo potenza o selettività d’azione tali per essere utilizzati a scopo terapeutico, ancora oggi rappresentano il modello di riferimento per la progettazione e la sintesi di potenziali BK – openers.
La ricerca è finalizzata soprattutto alla variazione della regione LINKER, l’unità spaziatrice, variamente eterogenea in quanto i due fenili possono essere separati da :
- un solo legame, senza uno spaziatore (3333,444) 4 - un ponte metilenico o un atomo di zolfo (5555,6666) - un gruppo ureico (7777). N N F3C H O OH X 1 (NS004), X = Cl 2 (NS1619), X = CF3 HO Cl Cl OH Cl Cl HO OH 3 4 CH OH Cl Cl S OH Cl Cl NH F3C
I composti più significativi sintetizzati nel nostro laboratorio negli ultimi anni, utilizzando come molecola lead il benzimidazolo NS004, sono mostrati in figura 2 : N H N R O N NH N H2NOC N N N OH NO2 R NH OH O N N N R X OH A B C D A B C D A B C D A B C D Fig. 2 Cmpd Cmpd Cmpd Cmpd RRRR XXXX A AA A H, CH 3, OCH3,Cl, F,CF3. C C C C H, CH3, Cl, F, CF3, C6H5 D D D D H, CH3, Cl, F, CF3C6H5. H. CO. CH2
A partire dal 1997 una particolare attenzione è stata rivolta a derivati 1,2,3, triazolici di struttura generale
4 N 3 N 1 N 2 X Z R3 R4 R2 R1
per cui sono stati sintetizzati :
- derivati 5 – (4’ – sostituiti – 2’ – nitroanilino) – 1,2,3 – triazolici [1][1][1][1] (EEE) E - derivati triazolil – benzimidazolonici e benzotriazolici [2][2][2] [3][2][3][3][3](FFF, GF GGG) - derivati 5 – sostituiti – 1 – (2 – idrossibenzoil) – benzotriazolici [4][4][4] (H[4] HHH)
NH N N NH H2NOC NO2 CF3 E R NH N O N H N N CONH2 F N N N R N H N N CONH2 G N N N R OH O H H H H
Molti di questi composti talvolta hanno mostrato un’attività superiore ai composti di riferimento.
In seguito la ricerca è proseguita con la sintesi e la sperimentazione di derivati 1,2,3 – triazolici :
- 1,5 – diaril-sostituiti 1,2,3, - triazoli [5][5][5] (IIII) [5]
- 1,4 – sostituiti e 2,4 – sostituiti – 1,2,3, - triazoli [6][6][6][6](LLLL) - benzoil o benzil – sostituiti – 1,2,3 – triazoli [7][7][7][7](MMM,NMNNN).
N N N GWE OH GWE I N NH N X Z R3 R4 R2 R1 L N N N X OH R M N N N X OH R N X = CO; CH2
Tra questi il composto della serie M, 1 – (2 – idrossibenzil) – 4 – benzil – 1,2,3 triazolo, ha mostrato una elevata attività vasorilasciante sui canali BKCa.
Per quanto riguarda i composti della serie C (fig. 2) il linker è costituito da una funzione ammidica piuttosto che dall’anello triazolico [8][8][8][8], pertanto usando come riferimento questo modello, sono state sintetizzate delle benzanilidi polisostituite sugli anelli aromatici (Tab. 2):
Cmpd CmpdCmpd Cmpd RRRR1 RRRR2 RRRR3 RRRR4 RRRR5555 1 11 1 NO2 H H H CH3 2 22 2 NO2 OH H H H 3 33 3 OCH3 NO2 H H H 4 44 4 OH NO2 H H H 5 55 5 OCH3 H H NO2 H 6 66 6 OH H H NO2 H 7 77 7 OH H H Cl H 8 88 8 OH H CH3 OCH3 Cl 9 99 9 OH H Cl OCH3 Cl 10 10 10 10 OH H Cl OH Cl Tabella 2 N O H R3 R1 R5 R2 R4
Queste benzanilidi hanno rivelato spiccate proprietà vasorilascianti (Tab. 3).
Cmpd Cmpd Cmpd
Cmpd Efficacy (Emax %)Efficacy (Emax %)Efficacy (Emax %)Efficacy (Emax %) pICpICpICpIC5050 5050 1 1 1 1 100a 6.60 ± 0.052 2 2 2 2 41.2 ± 9.7 N.C 3 3 3 3 100 6.72 ± 0.23 4 4 4 4 100 5.84 ± 0.039 5 5 5 5 100 6.35 ± 0.17 6 6 6 6 54.6 ± 10.6 5.09 ± 0.095 7 7 7 7 90.2 ± 6.4 6.87 ± 0.37 8 8 8 8 86.4 ± 6.6 7.56 ± 0.10 9 9 9 9 100 8.49 ± 0.091 10 1010 10 89.8 ± 2.3 6.43 ± 0.11 NS 1619 NS 1619 NS 1619 NS 1619 100 5.18 ± 0.055 Tabella 3
In particolare il composto 9999 ha dimostrato di avere una totale efficacia ed una potenza superiore a quella di NS1619 di riferimento.
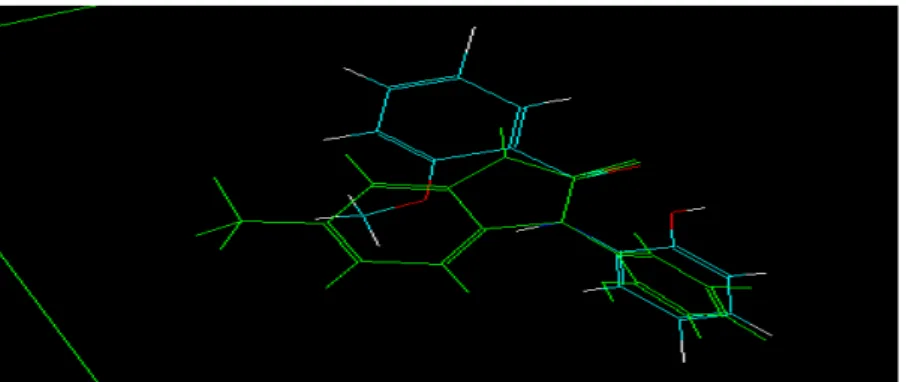
Sovrapponendo il composto 9999 alla molecola lead NS004 è stato
riscontrato che le caratteristiche del template di riferimento venivano tutte rispettate (fig. 3) :
- un gruppo – OH donatore di legame ad idrogeno - un anello povero di elettroni
-
Fig. 3 Sovrapposizione del composto 9999 con NS004
OCH3 Cl NH Cl OH O 9 9 9 9 F3C NH N O OH Cl NS004
Lo studio è proseguito al fine di ricavare informazioni sulla relazione struttura – attività ed è stato esteso alle principali molecole BK – openers, di origine naturale e sintetica, già presenti in letteratura; tali studi hanno dimostrato che le conformazioni a più bassa energia conducono ad un template comune [9][9][9]. [9]
Ulteriori modificazioni dei derivati benzanilidici col linker
ammidico e la combinazione di quest’ultimo con quello 1,2,3 triazolico hanno condotto a risultati deludenti [10] [11] [12][10] [11] [12][10] [11] [12][10] [11] [12].
Invece esperimenti recenti [13][13][13] sulla deannulazione del prototipo NS004 [13] hanno fornito composti con una notevole attività vasorilasciante.
Nella struttura generale (fig. 4.) il linker è rappresentato da un eterociclo 1,2,4, - triazolico o 1,3,4 - ossadiazolico. Eterociclo F3C Cl OH Fig. 4
Tale struttura è geometricamente sovrapponibile al 1 – (2 – idrossibenzil) – 4 – benzil – 1,2,3 – triazolo che rappresenta il composto più attivo sintetizzato nel nostro laboratorio, quindi la ricerca è proseguita introducendo come linker un anello 1,3,4 – ossadiazolico legato
direttamente o indirettamente a due anelli aromatici variamente sostituiti (fig. 5-6)[14][14][14].Questa scelta è stata fatta considerando l’analogia con le [14] strutture triazoliche e ossadiazoloniche e con lo scopo di verificare se la presenza del gruppo – CO fosse indispensabile per l’azione vasorilasciante sui canali BK o se fossero sufficienti gli atomi accettori di legami ad
idrogeno (O, N) nelle posizioni 1,3,4.
O N N NH R R3 R4 R5 R1
R1 R2 R3 R4 R5 H OCH3 H H Cl H H CF3 H H H H H CF3 H H Cl H H Cl H H H F H F Cl H H Cl F H H F H H OH H H Cl Fig. 5 R3 R4 R5 R2 O N N R1 R1 R2 R3 R4 R4 H OCH3 H H Cl H H CF3 H H H H H CF3 H H H H F H F OCH3 H H Cl F H H F H F OH H H Cl Fig. 6
I risultati dei test farmacologici hanno evidenziato che queste molecole presentano dei valori di attività non soddisfacenti.
Successivamente facendo riferimento, oltre che ai noti benzimidazoloni NS004 e NS1619 al nuovo efficace derivato difenilureidico NS1608 (fig. 7), in laboratorio è stata sintetizzata una estesa serie di sostituite diariluree sia simmetriche che asimmetriche, le quali mostravano interessanti profili farmacologici [15][15][15][15].
F3C NH N O OH Cl F3C NH N O OH F3C F3C NH N H O OH F3C NS004 NS1619 NS1608 Fig. 7
Pertanto allo scopo di ottenere migliori informazioni sul modello
farmacoforico, tramite l’ introduzione del linker ureidico, e nello stesso tempo per valutare l’introduzione di un nuovo linker eterociclico similare, in questa tesi abbiamo ritenuto interessante formare un anello eterociclico sulla funzione ureidica, sintetizzando alcuni nuovi derivati dibenzil e difenil – imidazolidinonici corrispondenti alla formula generale di figura 8. [ ]n [ ]n N N O R1 R1
Nello SCHEMA 1 è riportata la sintesi dei derivati N,N – (sostituiti benzil) – imidazolidin – 2 – oni 3a3a3a e 3b3a 3b3b3b.
SCHEMA 1 R1 R2 CHO + N H2 NH2 R1 R2 N N R1 R2 2 1 a,b 1 a,b1 a,b 1 a,b R1 R2 NH NH R1 R2
2 a,b 2 a,b 2 a,b 2 a,b TEA COCl2 t.o. Toluene N N O R1 R1 R2 R2 3 a,b 3 a,b3 a,b 3 a,b EtOH ∆ 2 h NaBH4 MeOH a, b a, b a, b a, b Comp. Comp. Comp. Comp. RRRR1 111 RRRR2222 a aa a F H b b b b OCH3 Br
Il disegno di questi nuovi composti è partito dalla considerazione delle diariluree simmetriche e della benzanilidi riportate in figura 9, composti farmacologicamente attivi, rilevando che le uree non presentano la funzione ossidrilica in posizione orto.
OCH3 Cl NH NH O OCH3 Cl F NH NH O F OH Cl NH O OCH3 Cl Fig. 9
Quindi la sperimentazione dei composti 3a3a3a e 3b 3a 3b 3b 3b poteva chiarire se l’introduzione di un secondo gruppo –NH nel linker ammidico poteva simulare la funzione –OH nella interazione con il canale.
Infatti i nostri derivati simmetrici presentano due atomi di azoto trivalenti, incapaci di interagire con il canale al potassio.
Questi derivati benzilici presentano comunque due ponti metilenici, tra gli anelli aromatici e il linker eterociclico, che conferiscono flessibilità alla struttura.
La reazione delle opportune aldeidi 2 – fluoro – benzoica (aaaa) o
2 – metossi – 5 – bromo – benzoica (bbb) con etilendiamina in EtOH b
anidro a reflusso per 2 ore, forniva le corrispondenti doppie basi di Schiff 1a
1a 1a
1a e 1b 1b 1b che erano poi ridotte con boroidruro di sodio in MeOH alle 1b attese N,N’ – (sostituito - benzil) – etilendiammine 2a2a2a e 2b2a 2b2b2b.
Come ulteriore modificazione dei precedenti derivati, nello SCHEMA 4 è riportata la sintesi degli analoghi derivati N,N – (sostituito - fenil) –
imidazolidinonici 9a9a9a9a, 9b9b9b9b, 9d9d9d che, mancando dei ponti metilenici, 9d presentano strutture più rigide e quasi planari in virtù della risonanza elettronica. SCHEMA 4 + Br Br R1 R3 NH R2 R1 R3 NH R2 8 a,b,c,d 8 a,b,c,d 8 a,b,c,d 8 a,b,c,d R1 NH2 R3 R2 a, b, c, d a, b, c, d a, b, c, d a, b, c, d N N O R1 R3 R2 R1 R3 R2 9 a,b,d 9 a,b,d9 a,b,d 9 a,b,d N O O Cl N O O Cl 10 10 10 10 2 DMF CaCO3 COCl2 Toluene TEA t.o. BBr3 CH2Cl2 X ∆ 2h Comp. Comp.Comp. Comp. RRRR1111 RRRR2222 RRRR3333 a aa a F H H b bb b OCH3 Cl H cccc OH Cl H d dd d H H F
Così, a partire dalle opportune aniline commerciali 2 – fluoro - anilina (aaaa), 2 – metossi – 5 – cloro- anilina (bbbb), 2 – idrossi – 5 – cloro – anilina (cccc) o 3 – fluoro – anilina (dddd), per reazione con dibromoetano in
dimetilformammide ed in presenza di carbonato di calcio erano preparate le corrispondenti N,N’ – difenil – etilendiammine simmetriche 8a8a8a8a , 8b8b8b8b, 8c8c8c 8c e 8d8d8d8d (Tabella 4).
I composti 8a8a8a8a, 8b8b8b8b, 8d8d8d erano poi convertiti nei derivati eterociclici 9a8d 9a9a, 9b9a 9b9b9b, 9d
9d 9d
9d per reazione con fosgene come descritto sopra (Tabella 5).
Il derivato con la funzione ossidrilica 8c8c8c8c è stato preparato perché vari tentativi di demetilare il derivato imidazolidinonico 8b8b8b8b con tribromuro di boro in diclorometano anidro a – 20°C erano andati falliti, recuperando sempre il prodotto di partenza.
Tuttavia anche questo tentativo per ottenere il derivato eterociclico con il fenile portante la funzione ossidrilica in posizione orto è andato fallito in quanto la reazione di ciclizzazione di 8c8c8c8c con fosgene non è avvenuta, come prima, esclusivamente sui due atomi di azoto ma sull’azoto e l’ossidrile in posizione orto, dando il derivato benzisossazolonico 10 10 10 10 (Tabella 5)....
La sintesi e la sperimentazione dei derivati difenilureidici simmetrici e asimmetrici, come detto in precedenza, aveva mostrato interessanti profili farmacologici [15][15][15][15].
Evidentemente la modificazione del linker da ammidico in ureidico introduceva un ulteriore donatore di legame a idrogeno (due funzioni NH) che determinava un incremento dell’attività biologica, in particolare per i composti riportati in figura 10, i quali mostravano una buona attività vasorilasciante indotta dall’apertura dei canali del potassio e comparabile con quella del riferimento NS1619.
F NH NH O F OCH3 NH NH O H3CO Cl Cl OCH3 NH NH O O H Cl Cl Fig. 10
Per questo motivo, come ulteriore modificazione del linker ureidico, sono stati sintetizzati nuovi derivati corrispondenti alle strutture generali OOOO e PPPP (fig. 11) che mostrano differenti ma similari linkers aciclici mantenenti due funzioni ammidiche.
NH NH O O R1 R2 R1 R2 O R1 R2 R3 R4 NH NH O O P Fig. 11
I sostituenti sugli anelli aromatici sono stati scelti facendo riferimento a quelli dei derivati ureidici di figura 10 più attivi farmacologicamente.
SCHEMA 3 NH2 R1 R2 + COCl COCl NH NH O O R1 R2 R1 R2 2 TEA Toluene ∆ 6a, 6b 6a, 6b6a, 6b 6a, 6b NH NH O O OCH3 Cl O H Cl 7 7 7 7 BBr3 CH2Cl2 - 35°C a, b a, b a, b a, b Comp. Comp.Comp. Comp. RRRR1 111 RRRR2222 a aa a F H b b b b OCH3 Cl
Così nello SCHEMA 3 è riportata l’introduzione di due gruppi carbonilici nello spaziatore, in modo da ridurre la libertà rotazionale della struttura, avendo due funzioni accettori e due funzioni donatori di legame a
idrogeno.
La sintesi è stata realizzata a partire dalle opportune ammine, 2 – fluoro – anilina (aaaa) o 2 – metossi – 5 – cloro – anilina (bbbb) che reagivano con cloruro di ossalile in toluene anidro e in presenza di trietilammina a 70°C per dare le corrispondenti ossammidi 6a6a6a6a e 6b6b6b in buona resa 6b
(Tabella 3).
Il derivato 6b6b6b6b portante due gruppi metossilici era sottoposto ad una successiva reazione di demetilazione, condotta in condizioni sperimentali tali da favorire una monodemetilazione.
La reazione era condotta con quantità stechiometriche di tribromuro di
boro a – 40°C per una notte dando l’atteso composto 7777 in resa modesta
ma con gli anelli fenilici sostituiti come nel composto attivo di figura 10 (Tabella 3). OCH3 NH NH O O H Cl Cl
SCHEMA 2 COCl R1 R3 R2 + NH2 NH2 R1 R3 R2 NH NH R1 R2 R3 O O 4a, 4b, 4c 4a, 4b, 4c4a, 4b, 4c 4a, 4b, 4c NH NH O O O H Cl OH Cl TEA Toluene ∆ - 40°C BBr3 CH2Cl2 2 a, b, c a, b, ca, b, c a, b, c 5 55 5 Comp. Comp.Comp. Comp. RRRR11 11 RRRR2222 RRRR3333 a aa a F H H b b b b OCH3 Cl H cccc H H CF3
Nello SCHEMA 2 è riportata la sintesi di tre bis – 1,2 – etano – N,N’ – (sostituite) – benzammidi 4a4a4a4a, 4b4b4b4b e 4c4c4c4c, aventi uno spaziatore a 7 termini che può essere considerato di due porzioni :
- una parte funzionale rappresentata dai donatori di legame a idrogeno (due funzioni ammidiche)
- una parte non funzionale rappresentata dai ponti metilenici il cui ruolo
è quello di incrementare la distanza tra i due anelli aromatici.
La successiva reazione dei cloruri acilici con etilendiammina in toluene a reflusso, in presenza di trietilammina, forniva gli attesi derivati 4a4a4a, 4b4a 4b4b4b e 4c 4c 4c 4c (Tabella 2).
Anche in questo caso il dimetossi-derivato 3b3b3b3b per trattamento con un eccesso di tribromuro di boro in diclorometano a bassa temperatura subiva una reazione di demetilazione per dare il corrispondente diidrossi-derivato 5 5 5 5 (Tabella 2).
Le strutture di tutti i nuovi composti preparati sono state assegnate sulla base dei noti meccanismi delle reazioni utilizzate (Tabelle 1 a – 5 a) e confermate con dati analitici e spettroscopici
Bibliografia Bibliografia Bibliografia Bibliografia [1] [1] [1]
[1] Biagi, G., Calderone, V., Giorgi, I., Livi, O., Scartoni, V., Baragatti, B., Martinotti, E.,
Eur. J. Med. Chem
., 35, 715 – 720, 200020002000. 2000[2] [2] [2]
[2] Baragatti, B., Biagi, G., Calderone, V., Giorgi, I., Livi, O., Martinotti, E., Scartoni, V.,
Eur. J. Med. Chem
, 35, 949 – 955, 2000.2000.2000. 2000.[3] [3] [3]
[3] Biagi, G., Calderone, V., Giorgi, I., Livi, O., et al.,
Il Farmaco
, 56, 841 – 849, 2001200120012001.[4] [4] [4]
[4] Biagi, G., Giorgi, I., Livi, O., Scartoni, V., et al.,
Il Farmaco
, 56, 827 – 834, 2001200120012001.[5] [5] [5]
[5] Biagi, G., Giorgi, I., Livi, O., Nardi, A., Calderone, V., Martelli, A.,
Martinotti, E., LeRoy Salerni, O.,
Eur. J. Med. Chem,
39, 491 – 498,2004 2004 2004 2004. [6]. [6]. [6].
[6]. Biagi, G., Calderone, V., Giorgi, I., Livi, O., Martinotti, E., Martelli, A., Nardi, A.,
Il Farmaco
, 59, 397 – 404, 200420042004. 2004[7] [7] [7]
[7] Calderone, V., Giorgi, I., Livi, O., Martinotti, E., Martelli, A., Nardi, A.,
Il Farmaco
, 60, 367 – 375, 2004200420042004.[8] [8] [8]
[8] Calderone, V., Giorgi, I., Livi, O., Martinotti, E., Mantuano, E., Martelli, A., Nardi, A.,
Eur. J. Med. Chem
, 40, 521 – 528, 2005200520052005. [9][9] [9]
[9] Calderone, V., Fiamingo, F.L., Giorgi, I., Leonardi, M., Livi, O., et al.,
Eur. J. Med. Chem
, 41, 761 – 767, 200620062006. 2006 [10][10] [10]
[10] Calderone, V., Coi, A., Fiamingo, F.L., Giorgi, I., Leonardi, M., Livi,
O., Martelli, A., Martinotti, E.,
Eur. J. Med. Chem
, 41, 1421 – 1429,2006 2006 2006 2006. [11] [11] [11]
[13] [13] [13]
[13] Romine, Martin, Meanwell, Gribkoff, Boissard, et al.
J. Med. Chem
.,50, 528 – 542, 2007200720072007. [14].
[14]. [14].
[14]. Tesi Dott. Andrea Gestri, Ottobre 2007200720072007. [15]
[15] [15]