INTRODUZIONE
2
CASO
CLINICI………...3
Angioplastica coronarica dopo protesi autoespandibile………3
Angioplastica coronarica dopo protesi pallone espandibile………..4
DISCUSSIONE………...4
La valvola autoespandibile Medtronic……….……….4
La valvola pallone espandibile Edwards……….………..5
CONCLUSIONI………...6
BIBLIOGRAFIA……….7
INTRODUZIONE
Nell'ultimo decennio l'impianto transcatetere di valvola aortica (TAVI) ha rivoluzionato il trattamento della stenosi aortica severa in pazienti ad alto e intermedio rischio chirurgico (1-5). La prevelanza della malattia coronarica in questi pazienti varia dal 45% al 70% (6), anche in quelli a rischio intermedio (4,5). Nei pazienti sottoposti ad impianto transcatetere della valvola aortica (TAVI) l’imaging coronarico prima della procedura è sempre raccomandato (6). Nonostante ciò, il significato prognostico della coronaropatia e dell’eventuale rivascolarizzazione prima della TAVI rimane controverso (7,8,9). In attesa dei risultati dei trial randomizzati (i.e. ACTIVATION trial), in atto un approccio individualizzato a ciascun paziente appare..
Data la storia naturale della patologia coronarica, dopo la TAVI una parte di questi pazienti necessiterà uno studio coronarografico e probabilmente successiva angioplastica coronarica percutanea. Pochi sono i dati riguardanti la fattibilità di coronarografia e/o angioplastica coronarica dopo impianto di protesi via transcatetere , con un tasso di successo variabile a causa delle difficoltà tecniche nel cannulare gli osti coronarici dopo TAVI, soprattutto dopo impianto di protesi autoespandibili.
Lo scopo di questo project-work è quello di esporre le difficoltà tecniche che si possono incontrare nell'esecuzione dello studio coronarografico e dell'angioplastica coronarica in pazienti sottoposti a TAVI.
CASO CLINICI
Angioplastica coronarica dopo impianto di protesi auto-espandibile
Paziente di 79 anni, riferita al nostro Istituto per dolore toracico associato a lieve scarto enzimatico e turbe all’ECG in sede antero-laterale. La storia clinica del paziente include ipertensione, diabete insulino-dipendente, insufficienza renale di grado moderato, cardiopatia ischemica e stenosi aortica severa trattata con impianto di TAVI con protesi autoespandibile da 23 mm Medtronic Evolut R circa 1 anno prima.
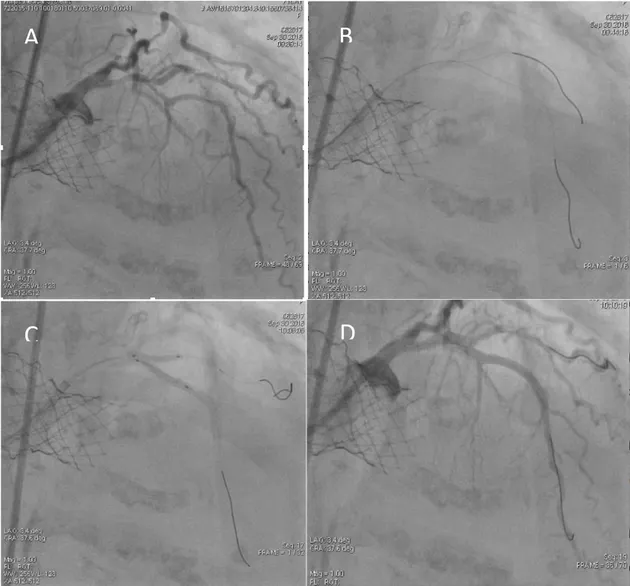
La paziente viene condotta in sala di emodinamica per essere sottoposta a coronarografia. Dopo aver guadagnato l’accesso femorale, e tentato senza successo di cannulare l’ostio coronarico sinistro con un catetere JL-4, si riesce ad ottenere un’iniezione semiselettiva con un catetere con curva minore il JL-3.5. L’esame mostra patologia critica sull’arteria interventricolare anteriore (IVA) al tratto medio coinvolgente la biforcazione con il primo ramo diagonale (D1). La coronaria destra cannulata con un JR4, è ateromasica ma esente da stenosi angiograficamente significative. Si sceglie un catetere guida EBU 3.0 con il quale si ottiene una cannulazione non ottimale attraverso le maglie del frame della valvola(Figura 1-A). Pertanto si posizionano 2 guide BMW alla periferia dei vasi (Figura 1-B) e vengono utilizzate come railtrack per il catetere guida stesso e migliorare la cannulazione. Dopo aver predilatato con palloni NC 2.5 and 3.0 mm si procede all’impianto di 2 stent medicati da 2.75/24 mm e 2.5/24 mm SYNERGY in overlapping disto-prossimale. Si esegue kissing balloon finale (Figura
1-C) (provisional stenting technique). Buon risultato angiografico finale (Figura 1-D). Dopo il
controllo angiografico, il ritiro del catetere guida viene eseguito mantenendo le guide in coronaria al fine di evitare qualsiasi kinging del catetere tra le maglie della valvola.
Angioplastica coronarica dopo impianto di protesi pallone-espandibile
Paziente di 80 anni, ipertesa con insufficienza di grado moderato affetta stenosi aortica severa sintomatica per dispnea in classe NYHA III con recente ricovera per edema polmonare. Nega angina. Riferita al nostro Istituto per il trattamento della patologia valvolare aortica. La coronarografia pre-procedurale ha mostrato stenosi critica al tratto medio-prossimale dell’arteria interventricolare anteriore subito a valle del primo ramo diagonale (Figura 2-A). La CT ha mostrato anatomia favorevole a TAVI. Dopo discussione in Heart team, si decide di trattare prima la stenosi aortica severa con TAVI quindi in una seduta successiva di eseguire la rivascolarizzazione coronarica percutanea. La paziente è stata sottoposta a TAVI con protesi Sapien 3 da 23 mm con impianto ottimale (Figura 2-B). Dopo un mese, la paziente è ammessa in elezione per il trattamento della stenosi coronarica. La cannulazione dell’ostio coronarico sinistro viene eseguita con EBU 3.0 senza particolari difficoltà in quanto l’ostio risulta essere immediatamente sopra la protesi. Si predilata la lesione e si procede all’impianto di 1 stent medicato 4.0/16 mm (Figura 2-C). Si esegue post-dilatazione con pallone NC 4.0/8 mm. Ottimo il risultato angiografico finale (Figura 2-D).
DISCUSSIONE
Dal 2007 sono stati eseguiti oltre 500000 impianti di TAVI, e il numero è destinato a crescere nei prossimi anni. Di conseguenza, data l’elevata prevalenza di patologia coronarica in questi pazienti, incrementerà anche la necessità di trattamento percutaneo della coronaropatia post-TAVI.
Case reports e piccoli studi (10,11,12,13,14,15,16) suggeriscono che l’angiografia coronarica e l’angioplastica possono essere associate a difficoltà tecniche di cannulazione degli osti coronarici in pazienti sottoposti a TAVI, soprattutto dopo impianto di protesi autoespandibile. Queste difficoltà tecniche diventano un fattore importante soprattutto nell’infarto miocardico acuto e/o quando il paziente è riferito ad un centro periferico non familiare con la procedura di TAVI.
Il limitato numero di studi pubblicati non ci permette di fare una stima dell’incidenza, del tasso di fattibilità e di successo nell’esecuzione di coronarografia ed angioplastica coronarica in pazienti sottoposti a TAVI. Di certo, il design della protesi impiantata ha un ruolo cruciale nell’influenzare la fattibilità e il successo di queste procedure in pazienti sottoposti a TAVI.
Le due protesi più utilizzate su larga scala sono la valvola autoespandibile Medtronic (Evolut R or Evolut PRO) e la pallone-espandibile Sapien 3 Edwards Lifesciencies. E’ importante conoscere le caratteristiche della protesi valvolare impiantata e la sua interazione con le specifiche caratteristiche della radice aortica del paziente al fine di prevedere le eventuali difficoltà tecniche nella cannulazione degli osti coronarici.
La valvola autoespandibile Medtronic Corevalve (Evolut R o PRO)
La valvola autoespandibile Medtronic Corevalve (Evolut R o PRO) è composta da un frame in nitinolo all’interno del quale è suturata la valvola in pericardio porcino in posizione supra-anulare. Il frame ha 3 livelli (Figura 3): “inflow” la porzione della valvola che viene a contatto con l’anulus ed ha elevata forza radiale; il “waist” centrale, è la parte concava che permette di evitare il contatto del frame con gli osti coronarici; l’“ouflow” che è la parte più larga e permette l’ancoraggio in aorta ascendente.
Considerando le caratteristiche anatomiche di questa valvola, tre sono i fattori principali che possono influenzare il ri-accesso coronarico dopo impianto di protesi auto-espandibile Evolut R o PRO. Il primo fattore da considerare è l’altezza di impianto: è necessario impiantare la valvola almeno 4 mm al di sotto dell’annulus in modo da evitare che la skirt dell’Evolut PRO si sovrapponga all’ostio coronarico rendendo così difficoltosa la cannulazione degli osti coronarici. Il secondo elemento da tenere in considerazione è il “waist” centrale che ha dimensioni ridotte rispetto alla naturale anatomia della radice aortica, quindi per la cannulazione dell’ostio coronarico sinistro i cateteri con curva più piccola quali JL 3.5 e JL 3.0 sono di scelta sia che l’accesso sia radiale o femorale; talvolta anche un
JR 4.0 può essere utile in questi casi. Per quanto concerne l’utilizzo dei cateteri guida, di scelta sono JL 3.5 e 3.0 o l’extra back-up anche se è stato associato a kinking, quindi va utilizzato con particolare attenzione.
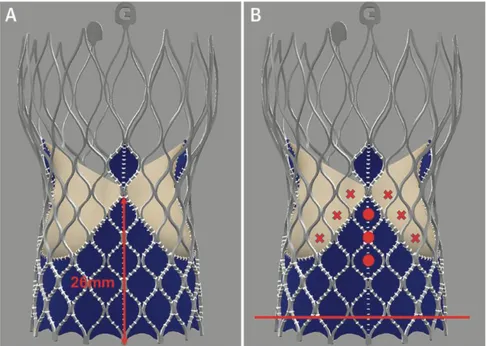
Il terzo fattore è il rapporto tra le commissure della nuova valvola (Figura 4) e la radice aortica: qualora le commissure si vengano a trovare davanti l’ostio coronarico, la cannulazione potrebbe essere molto difficile, talora impossibile, se associata a seni di Valsalva di ampiezza ridotta. In questo caso sarà necessario passare attraverso le celle a diamante che si trovano superiormente o lateralmente all’ostio (Figura 4). In questi casi, l’utilizzo dell’Ikari come catetere guida di seconda linea per cannulare l’ostio sinistro può essere un’opzione.
Per quanto riguarda la cannulazione della coronaria destra JR4 è di scelta sia come diagnostico che come catetere guida, mentre un AR-2 è preferito se c’è grande distanza tra il frame della valvola e gli osti a causa di ampi seni di Valsalva. Talvolta è necessario l’utilizzo di catetere MP quando all’ostio si può accedere solo dall’alto.
Inoltre, a causa delle caratteristiche anatomiche della protesi, la cannulazione selettiva può essere difficoltosa. Quando accessibile, è meglio utilizzare la cella di fronte all’ostio. Una guida J può essere utile per trovare la cella a diamante più vicina all’ostio; talvolta una guida coronarica può essere utilizzata come railway per il catetere guida, se necessario è possibile anche utilizzare un pallone di piccolo calibro come ancora nel tronco comune (“balloon-assisted tracking”) (17). In altri casi si può ricorrere ad estensioni del catetere guida per ottenere una cannulazione selettiva.
Infine anche il ritiro del catetere guida deve essere fatto con molta attenzione per evitare kinging tra le maglie della protesi. Spesso è meglio eseguire il ritiro del catetere sulla guida stessa.
La valvola pallone-espandibile Sapien 3 Edwards Lifesciencies
La valvola pallone-espandibile Sapien 3 Edwards Lifesciencies è in pericardio bovino e suturata in un corto frame formato da 12 celle larghe (FIG..). Sebbene l’occlusione coronarica durante l’impianto di TAVI è risultato più frequente con questo tipo di valvola (18), non sono stati riportati significative difficoltà tecniche nella cannulazione degli osti coronarici. Quindi nella maggior parte dei casi non è necessario modificare la tecnica standard di cannulazione coronarica. Tuttavia, anche con questo modello di valvola è necessario tener conto del rapporto delle commissure con gli osti coronarici.
Inoltre, in alcuni casi è necessario considerare anche le dimensioni della giunzione seno-tubulare: il frame della valvola, non avendo il il waist centrale, può estendersi oltre la giunzione sino-tubulare rendendo complesso il ri-accesso agli osti coronarici soprattutto se associato ad un impianto alto (con la parte aortica del frame maggiore dell’80%) e ridotta altezza degli osti coronarici (<10mm dal piano valvolare). In questi casi è necessario cannulare posizionando il catetere nella cella adiacente all’ostio; se si procede ad angioplastica, la guida coronarica può essere utilizzata come “railtrack” oppure si può ricorrere ad estensioni del catetere guida o al “balloon-assisted tracking”(17).
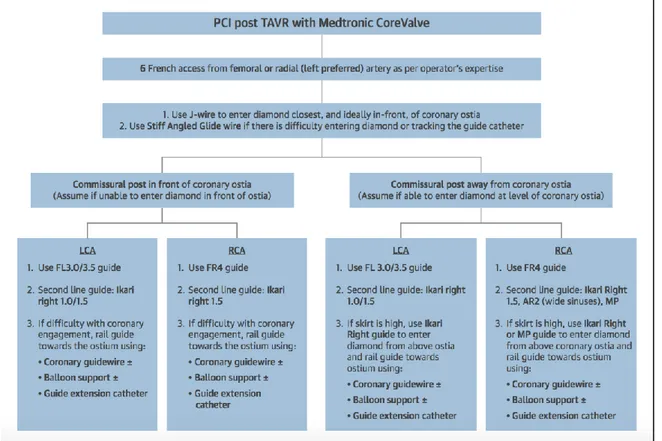
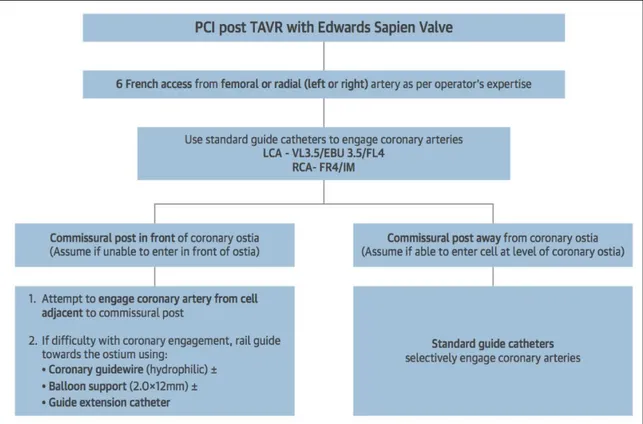
Yudi et al(19) hanno creato un algoritmo (Figura 5-6) che può essere di grande aiuto per superare le possibili difficoltà tecniche nella cannulazione degli osti coronarici e velocizzare la procedura soprattutto nello scenario clinico delle sindromi coronariche acute.
Poiché è evidente che il design valvolare, in termini di ri-accesso agli osti coronarici gioca un ruolo fondamentale, durante la pianificazione della TAVI, la presenza di coronaropatia dovrebbe essere un fattore da prendere in considerazione nella selezione della valvola. Probabilmente in futuro, la tecnologia condurrà allo sviluppo di nuove protesi e sistemi di rilascio che ci permetteranno di orientare le commissure della protesi durante l’impianto, e di specifici cateteri che faciliteranno il riaccesso agli osti coronarici post-TAVI.
CONCLUSIONI
La cannulazione dopo impianto transcatetere di valvola aortica (TAVI) può essere tecnicamente difficile, soprattutto dopo impianto di protesi autoespandibile. E’ fondamentale per il cardiologo interventista la conoscenza del design della protesi impiantata in rapporto alle specifiche caratteristiche anatomiche del paziente al fine di predire e superare le potenziali difficoltà tecniche che si possono riscontrare nell’esecuzione della coronarografia e dell’angioplastica in questo setting di pazienti.
BIBLIOGRAFIA
1.
Leon MB, Smith CR, Mack M, et al., PARTNER Trial Investigators. Transcatheter aortic-valve im- plantation for aortic stenosis in patients who cannot undergo surgery. N Engl J Med 2010;363: 1597–607.2.
Popma JJ, Adams DH, Reardon MJ, et al., Cor- eValve United States Clinical Investigators. Transcatheter aortic valve replacement using a self-expanding bioprosthesis in patients with se- vere aortic stenosis at extreme risk for surgery. J Am Coll Cardiol 2014;63:1972–81.3.
Smith CR, Leon MB, Mack MJ, et al., PARTNER Trial Investigators. Transcatheter versus surgical aortic-valve replacement in high-risk patients. N Engl J Med 2011;364:2187–98.4.
Leon MB, Smith CR, Mack MJ, et al., PARTNER 2 Investigators. Transcatheter or surgical aortic- valve replacement in intermediate-risk patients. N Engl J Med 2016;374:1609–20.5.
Reardon MJ, Van Mieghem NM, Popma JJ, et al., SURTAVI Investigators. Surgical or transcatheter aortic-valve replacement in intermediate-risk patients. N Engl J Med 2017; 376:1321–31.6.
Goel SS, Ige M, Tuzcu EM, et al. Severe aortic stenosis and coronary artery disease– implications for management in the transcatheter aortic valve replacement era: a comprehensive review. J Am Coll Cardiol 2013;62:1–10.7.
Danson E, Hansen P, Sen S, Davies J, Meredith I, Bhindi R. Assessment, treatment, and prognostic implications of CAD in patients undergoing TAVI. Nat Rev Cardiol8. Patel MR, Calhoon JH, Dehmer GJ, et al. ACC/AATS/AHA/ASE/ASNC/SCAI/SCCT/STS
2017 appropriate use criteria for coronary revascularization in patients with stable ischemic heart dis- ease: a report of the American College of Cardiology appropriate use criteria task force, American Association for Thoracic Surgery, American Heart Association, American Society of Echocardiography, American Society of Nuclear Cardiology, Society for
Cardiovascular Angiography and Interventions, Society of Cardiovascular Computed Tomography, and Society of Thoracic Surgeons. J Am Coll Cardiol 2017;69:2212–41.
9. Kotronias RA, Kwok CS, George S, et al. Transcatheter aortic valve implantation with or
without percutaneous coronary artery revascularization strategy: a systematic review and meta- analysis. J Am Heart Assoc 2017;6:e005960.
10. Chetcuti S, Kleiman NS, Matthews R, Popma JJ, Moore J. TCT-743 Percutaneous coro-
nary intervention after self-expanding trans- catheter aortic valve replacement. J Am Coll Cardiol 2016;68:B300–1.
11. 19. Zivelonghi C, Pesarini G, Scarsini R, et al. Coronary catheterization and percutaneous
in- terventions after transcatheter aortic valve im- plantation. Am J Cardiol 2017;120:625– 31.
12. Blumenstein J, Kim WK, Liebetrau C, et al. Challenges of coronary angiography and inter-
vention in patients previously treated by TAVI. Clin Res Cardiol 2015;104:632–9.
13. Htun WW, Grines C, Schreiber T. Feasibility of coronary angiography and percutaneous
coronary intervention after transcatheter aortic valve replacement using a Medtronic self-expandable bioprosthetic valve. Catheter Cardiovasc Interv 2017 Oct 8 [E-pub ahead of print].
14. Allali A, El-Mawardy M, Schwarz B, et al. Incidence, feasibility and outcome of percuta-
neous coronary intervention after transcatheter aortic valve implantation with a self-expanding prosthesis. Results from a single center experi- ence. Cardiovasc Revasc Med 2016;17:391–8.
15. Boukantar M, Gallet R, Mouillet G, et al. Coronary procedures after TAVI with the
self-expanding aortic bioprosthesis Medtronic CoreValve, not an easy matter. J Interv Cardiol 2017;30:56–62.
16. Chakravarty T, Sharma R, Abramowitz Y, et al. Outcomes in patients with transcatheter
aortic valve replacement and left main stenting: the TAVR-LM registry. J Am Coll Cardiol 2016;67: 951–60.
17. Jackson M, Williams PD. Coronary access following TAVI: selective coronary engagement
using balloon-assisted tracking of a guide catheter extension. Cardiovasc Revasc Med 2017 Jul 31 [E-pub ahead of print].
18. Ribeiro HB, Webb JG, Makkar RR, et al. Pre- dictive factors, management, and clinical
out- comes of coronary obstruction following transcatheter aortic valve implantation insights from a large multicenter registry. J Am Coll Cardiol 2013;62:1552–62.
19. M. B. Yudi, S. K. Sharma, a Gilbert H.L. Tang, MD et at J Am Coll Cardiol 2018 JACC
Figura 1. (A) Angiogramma non selettiva con catetere EBU attraverso le maglie del frame
della valvola. (B) Posizionamento di guide-coronariche che fungono da railtrack per il catetere guida stesso. (C) Kissing balloon-finale. (D) Risultato angiografico finale.
A
B
D
C
Figure 2: (A) Coronarografia pre-TAVI mostra stenosi critica al tratto medio dell’arteria interventricolare anteriore; (B) Aortografia che mostra posizione ottimale della protesi Sapien 3; (C) Angioplastica con impianto di stent medicato; (D) risultato angiografico finale
Figura 3: La valvola autoespandibile Medtronic Ecolut R/Evolut PRO
Figura 4 : L’altezza della commissure della vavola Evolut R è 26 mm(A).
Qualora la commissura si venga a trovare di fronte l’ostio coronarico (punti in rosso) è necessario utilizzare le cellule adiacenti (x in rosso) per accedere all’ostio coronarico (B).
Figura 5 : Algoritmo per la scelta dei cateteri guida durante PCI dopo impianto di valvola
Figura 6 : Algoritmo per la scelta dei cateteri guida durante PCI dopo impianto di valvola pallone