Le terapie oggi a disposizione per la risoluzione delle patologie prostatiche sono sicuramente più efficaci rispetto al passato, permettendo non solo di ottenere un elevato numero di guarigioni riducendo il numero delle recidive, ma anche di salvaguardare l’attività riproduttiva dell’animale.
Sia le terapie di tipo medico che quelle di tipo chirurgico, come l’omentalizzazione prostatica, consentono di evitare la classica terapia consigliata in passato per tutte le patologie prostatiche: l’orchiectomia. Tale procedura, sicuramente molto utile in alcuni casi come ad esempio forme di iperplasia benigna particolarmente gravi, può essere a volte evitata al fine di non perdere, dal punto di vista riproduttivo, soggetti di elevato valore (Zambelli, 2007).
L’ orchiectomia è la terapia chirurgica consigliata in caso di iperplasia prostatica benigna clinicamente manifesta (Zambelli, 2007) e l’unica terapia prevista in seguito a diagnosi di metaplasia squamosa. Per la prima di queste due affezioni, risulta efficace in quanto, venendo a mancare lo stimolo ormonale si favorisce, infatti, la riduzione del volume della prostata, pari al 70% entro 9 settimane dall’intervento (Huggins e Clark, 1940; Huggins, 1947; Schlotthauer, 1932), evitando così l’insorgenza di recidive. La prostata inizia ad involvere entro alcuni giorni e, dopo 3 settimane, la diminuzione delle dimensioni diventa percepibile alla palpazione (la riduzione è pari circa al 50%) (Barsanti, 1997; Barsanti e Finco, 1995). Per la metaplasia squamosa, rappresenta invece l’unico intervento possibile quando questa consegue ad iperestrogenismo endogeno.
Questa terapia viene comunque consigliata in tutti i casi di patologia prostatica associata ad eventuali altre terapie di tipo medico-chirurgiche (Zambelli, 2007). Per la descrizione della tecnica si rimanda ai testi di Clinica Chirurgica Veterinaria mentre saranno trattate, di seguito, le varie tecniche per la cura delle altre patologie prostatiche.
3.1. Considerazioni generali ed approccio chirurgico
3.1.1. Trattamento pre-operatorio
La terapia medica comprende il trattamento della costipazione, tenesmo e ritenzione urinaria, quando presenti. Possono essere somministrati degli emollienti fecali e, se necessario, si può drenare la vescica mediante centesi o cateterizzazione (Fossum et al., 2004).
3.1.2. Trattamento post-operatorio
Secondo la necessità bisogna somministrare degli analgesici ed una terapia di supporto con fluidi ed elettroliti; inoltre si deve controllare che non compaiano shock ed infezioni. Può essere necessario continuare il trattamento sintomatico per la costipazione, il tenesmo e la ritenzione urinaria (Fossum et al., 2004). Somministrati per 7-10 giorni antibiotici come β-lattamine ma soprattutto chinoloni.
3.1.3. Approccio chirurgico
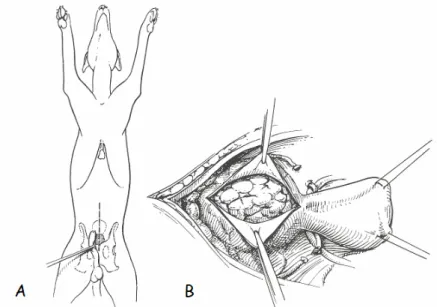
Generalmente la prostata viene raggiunta attraverso una laparotomia caudale eseguibile attraverso una incisione cutanea che si estende dalla cicatrice ombelicale, deviando lateralmente a livello del prepuzio, fino al margine craniale del pube. Si può anche arrivare alla ghiandola dal perineo, di solito come intervento riparatore di una ernia perineale (Slatter, 2005). Come per ogni altro intervento chirurgico dell’apparato urogenitale, prima di procedere si dovrebbe introdurre un catetere urinario al fine di permettere l’identificazione dell’uretra durante la dissezione chirurgica e promuovere la riduzione della tensione nel punto di intervento. La cateterizazione uretrale è inoltre utile per determinare la decompressione vescicale e per monitorare il flusso urinario (Larari e Dupuis, 1995).
Con il paziente in decubito dorsale , tricotomizzare e preparare per la chirurgia asettica la superficie ventrale dell’addome e quella mediale delle cosce, mentre il prepuzio viene risciacquato con una soluzione allo 0,1% di iodopovidone oppure con una soluzione di clorexidina al 2%, diluita 1:40 (Fossum et al., 2004). A questo punto si procede con una celiotomia caudale e se necessario, per esporre adeguatamente la prostata, estendere l’incisione caudalmente e praticare l’osteotomia pubica (Howard, 1969) per esporre la metà craniale del canale pelvico. Al fine di facilitare ulteriormente l’esposizione della ghiandola, applicare il retrattore di Balfour quindi procedere all’esplorazione dell’addome e all’ isolamento della vescica e della prostata con garze laparotomiche umide. Per retrarre la prostata cranialmente, applicare dei punti di ancoraggio sulla parete vescicale dopo aver separato il legamento ombelicale mediano dalla parete addominale ventrale. La prostata può essere ulteriormente mobilizzata sezionando il tessuto connettivo tra il pavimento pubico e la superficie ventrale dell’uretra (Slatter, 2005). Si evidenzia la ghiandola dissezionando il cuscinetto adiposo ventrale dalla capsula prostatica (Fossum et al., 2004), facendo attenzione a non sezionare il legamento ombelicale laterale ed il conseguente apporto neurovascolare alla vescica, alla prostata e all’uretra. Se necessario, sezionare e legare le due brevi arterie prostatiche il più vicino possibile alla ghiandola.
Il sanguinamento dell’incisione prostatica può essere notevole; le vene subcapsulari sono quelle che sanguinano maggiormente, possono essere cauterizzate o legate dopo aver identificato la loro posizione (Slatter, 2005).
3.2. Drenaggio chirurgico
Il drenaggio chirurgico è una delle tecniche che più frequentemente viene utilizzata per la risoluzione di cisti e ascessi prostatici.
Vi sono varie metodologie di drenaggio: quello meccanico o di Penrose, quello anatomico o marsupializzazione e il drenaggio fisiologico o omentalizzazione (Slatter, 2005).
3.2.1. Drenaggio multiplo di Penrose
Una volta evidenziata la prostata, si procde all’introduzione di un ago di grosso calibro nel lume dell’ascesso/cisti per prelevare sia un campione del contenuto, per l’esame colturale e per l’antibiogramma, sia per aspirare il materiale rimanente. Successivamente si procede all’incisione della superficie ventrale della ghiandola sopra la cavità ascessuale/cistica e si frammentano con le dita tutte le trabecole e le bande fibrose presenti nella cavità per porre in comunicazione tutti gli ascessi/cisti adiacenti, creando una cavità unica; in seguito aspirare e lavare per rimuovere gli accumuli di fluido. A questo punto, inserire 2-4 drenaggi di Penrose da ½ pollice trasversalmente attraverso le facce ventrolaterali di entrambi i lobi della prostata ed esteriorizzarne l’estremità 2-3 cm lateralmente all’incisione addominale ed al prepuzio; assicurare i drenaggi alla cute con punti di sutura crociati (Figura 3.2.1.).
Figura 3.2.1. Trattamento di ascessi e cisti prostatiche mediante l'impiego di numerosi drenaggi di Penrose che fuoriescono dall'addome nella regione prepubica (Fossum et al., 2004).
In caso si sia verificata una contaminazione, lavare il campo chirurgico e l’intera cavità addominale. Circondare il sito chirurgico con omento e grasso periprostatico e chiudere la breccia laparotomica. I drenaggi vengono lasciati in situ per 2-3 settimane.
Questa tecnica oggi non viene più utilizzata (Zambelli,2007) per le notevoli complicazioni post-operatorie che ne derivavano. Quelle a breve termine (inferiori a 2 settimane) includono: disturbi addominali, edema inguinale e degli arti
posteriori, fistolizzazione urtrale, incontinenza urinaria, anemia, ipoproteinemia, ipoglicemia, shock settico e morte. Quelle a lungo termine, invece, sono rappresentate da incontinenza urinaria, infezioni urinarie e recidive (Larari e Dupuis, 1995).
3.2.2. Marsupializzazione
Così come il drenaggio di Penrose, anche la marsupializzazione oggi rappresenta una tecnica chirurgica ormai abbandonata e sostituita dalla più sicura omentalizzazione. La masupalizzazione veniva utilizzata per il trattamento delle cisti prostatiche, soprattutto per quelle paraprostatiche, e per gli ascessi abbinata ad intervento di orchiectomia al fine di evitare possibili recidive (Zambelli, 2007). Era ritenuto l’intervento di elezione nel caso in cui l’ascesso/cisti potesse essere mobilizzato, avvicinato alla parete addominale ventrale e la capsula fosse sufficientemente forte da tenere una sutura senza lacerarsi.
Per quanto concerne la tecnica chirurgica di esecuzione, una volta evidenziata ed isolata la prostata, come descritto precedentemente, si pratica una seconda incisione di 5-8cm attraverso la parete addominale, in sede parapeniena lateralmente all’incisione laparotomica, al di sopra della cavità asessuale o cistica (Figura 3.2.2.).
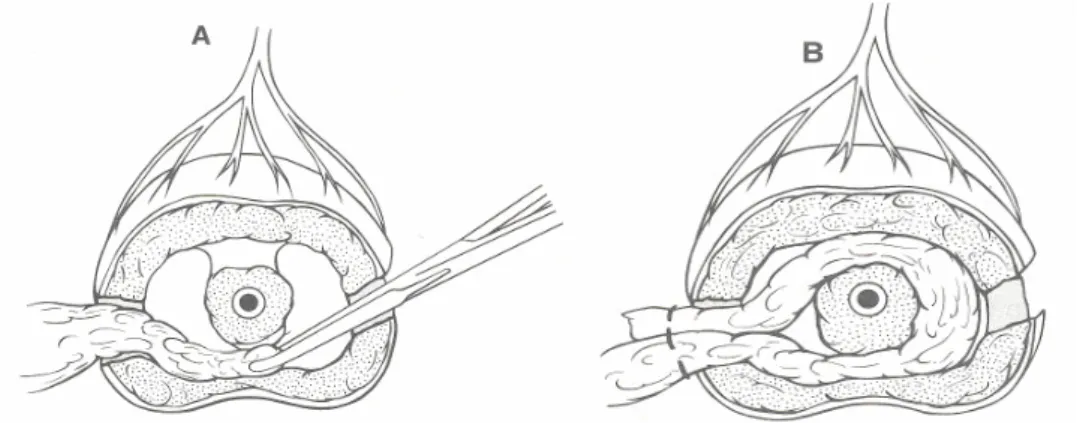
Successivamente, si asporta un tratto di 0,5-1cm di muscolo addominale (Figura 3.2.3.A.) e si suturata la parete della capsula o della cisti con la fascia esterna del muscolo retto dell’addome usando una sutura continua o a punti staccati (Figura 3.2.3.B.).
Figura 3.2.3. A: asportazione di un tratto ellittico di muscolo addominale. B: sutura della capsula prostatica alla fascia esterna del muscolo retto dell’addome (Fossum et al., 2004).
Quindi, incidere la parete dell’ascesso o della cisti, aspirarne il contenuto e lavare la cavità con una soluzione diluita di clorexidina o iodopovidone (Larari e Dupuis, 1995) e applicare un secondo strato di punti di sutura continui o staccati tra il margine della capsula/cisti e la cute (Figura 3.2.3.C-D.). Rompere con le dita le trabecole e le bande fibrose per creare una cavità confluente; lavare la cavità e il campo chirurgico, porre l’omento attorno alla marsupializzazione e chiudere la breccia laparotomica.
I vantaggi della marsupializzazione comprendono: la facilità di esecuzione, il drenaggio continuo, la possibilità di eseguire lavaggi post-operatori all’interno della cisti o dell’ascesso, la minor morbilità rispetto alla prostatectomia e la possibilità di intervenire chirurgicamente, in un secondo tempo, in modo più aggressivo eseguendo la rimozione del parenchima prostatico (Slatter, 2005). Tuttavia con questa tecnica di drenaggio permanente sono state descritte complicazioni quali: persistenza del drenaggio per diverse settimane con il rischio di infezioni secondarie (Zambelli,2007), recidive (Harari e Dupuis, 1995), necessita di operare nuovamente per persistenza dello stoma, ascessi e incontinenza urinaria (Slatter, 2005). Sono stati questi i motivi principali per i quali si è preferito abbandonare l’intervento di marsupializzazione a vantaggio della omentalizzazione, ritenuta la tecnica di drenaggio più efficace e esente da complicazioni.
3.2.3. Omentalizzazione
Questa metodica chirurgica di recente impiego è stata inizialmente proposta nell’uomo e successivamente impiegata anche nei carnivori domestici per il trattamento delle cisti prostatiche parenchimali di grandi dimensioni, per le cisti paraprostatiche, non asportabili, e per gli ascessi. Come detto in precedenza, tale procedura permette di ottenere buoni risultati anche a lungo termine fornendo al paziente un periodo post operatorio migliore ed al proprietario una miglior gestione dell’animale. Offre, inoltre, il vantaggio di essere di semplice esecuzione e di presentare un’incidenza molto bassa di complicanze post-operatorie, come l’incontinenza urinaria (Zambelli, 2007).
L’omento è una membrana mesoteliale e grazie alle sue caratteristiche angiogeniche e immunogene fornisce un supporto ideale nei processi riparativi; fornisce, infatti, un incremento nell’apporto vascolare e linfatico ai tessuti danneggiati, favorendone così la ricostruzione. Per queste proprietà l’omento è utilizzato nella risoluzione chirurgica di diverse patologie, soprattutto in campo
umano per la ricostruzione della parete toracica, nella chirurgia dell’apparato gastrointestinale e di quello urogenitale. È anche utilizzato per aumentare i processi riparativi in seguito a traumi e per rivascolarizzare aree ischemiche dell’apparato cardiovascolare, nervoso, respiratorio e delle estremità del corpo (Ross e Pardo, 1993).
È opportuno associare la castrazione del soggetto durante l’esecuzione dell’intervento.
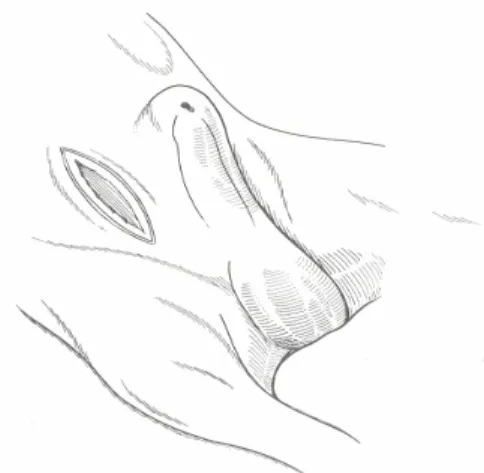
Dopo inserimento di un catetere urinario ed esposizione, isolamento e preparazione della prostata, come descritto sopra, praticare delle piccole incisioni bilateralmente sulle facce laterali della ghiandola prostatica e rimuovere il materiale mediante aspirazione. In seguito, identificare l’uretra prostatica palpando il catetere uretrale, precedentemente inserito, e introdurre un drenaggio di Penrose all’interno del parenchima attorno all’uretra per elevare la ghiandola e facilitare l’irrigazione delle cavità con soluzioni sterili saline aggiunte di antibiotici o tintura di iodio. A questo punto un lembo di omento viene introdotto in una delle ferite capsulotomiche utilizzando una pinza emostatica inserita nella apertura controlaterale e viene fatto passare attorno all’uretra prostatica per estrarlo, poi, attraverso la stessa incisione d’entrata (Figura 3.2.4.A-B). Infine viene ancorato su se stesso con sutura da materassaio in materiale riassorbibile e viene suturata la breccia laparotomica (Fossum et al., 2004).
Figura 3.2.4. Omentalizzazione di un ascesso. A: passaggio dell’omento attorno all’uretra prostatica. B: fuoriuscita dell’omento dall’incisione di entrata e ancoraggio a se stesso (Fossum et
3.3. Resezione parziale e Omentalizzazzione
Oltre alla tecnica appena descritta di omentalizzazione intracapsulare (Intracapsular prostatic omentalization), si può procedere anche all’asportazione parziale di cisti/ascesso con successiva sutura dell’omento attorno al residuo dell’ascesso oppure nella cavità cistica (Vannozzi, 2003; Slatter, 2005). La successiva omentalizzazione del residuo è finalizzata ad evitare la comparsa di recidive e l’insorgenza di complicazioni dovute alle aderenze che potrebbero crearsi tra il residuo di cisti/ascesso e gli altri organi addominali.
È preferibile effettuare una resezione parziale in quanto numerose cisti presentano aderenze con gli ureteri , con il collo della vescica, con la prostata e quindi, la resezione totale tenderebbe ad incrementare l’incidenza di incontinenza/ritenzione urinaria post-operatoria per compromissione nervosa e vascolare (Bray, White et al., 1997); questo lo si riscontra spasso anche in presenza di cisti paraprostatiche per le quali, in questi casi, non è possibile effettuare l’intervento di asportazione. È consigliabile eseguire una prostatectomia parziale quando la cisti/ascesso è confluente con la prostata (Fossum et al., 2004).
Una volta individuata la cisti/ascesso (Figura 3.3.1.), aspirarne il contenuto (Figura 3.3.2.) e procedere incidendo a tutto spessore la parete (Figura 3.3.3.).
Figura 3.3.2. Aspirazione del contenuto.
Scontinuare e asportare la maggior parte della parete della cavità, dopo aver prelevato campioni per l’esame colturale, citologico e istopatologico, senza danneggiare l’innervazione e la vascolarizzazione della prostata e della vescica (Figura 3.3.3.).
Figura 3.3.3. Scontinuazione della parete cistica e sua asportazione.
Colmare con l’omento il residuo e fissarlo con punti da materassaio orizzontali riassorbibili (Figura 3.3.4.). Lavare e suturare l’addome come di routine (Fossum et al., 2004).
Figura 3.3.4. Applicazione dell’omento sul residuo di cisti 3.3.1. Mobilizzazione di un lembo peduncolato di omento
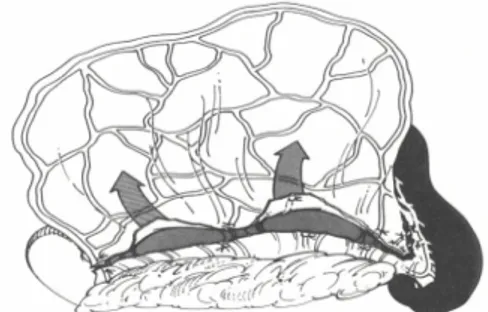
In genere, l’omento è facilmente mobilizzato fino alla prostata ma, se necessario, può essere allungato con incisioni che risparmiano l’apporto ematico e consentono la mobilizzazione caudale. La tecnica di mobilizzare un lembo peduncolato di omento, utilizzata nel campo della chirurgia umana, è stata studiata e adattata anche nel cane. Per ottenere tale peduncolo di omento in seguito ad una incisione laparotomica, si procede all’esteriorizzazione della milza e dell’omento, la cui lamina dorsale viene retratta cranialmente per identificare la sua inserzione pancreatica.
Successivamente, legare e recidere i vasi dell’omento che originano dall’arteria splenica e liberare il foglietto dorsale dal pancreas (Figura 3.3.5. e in modo da poterlo estendere caudalmente. Il foglietto omentale dorsale può, adesso, essere esteso (figura 3.3.6.).
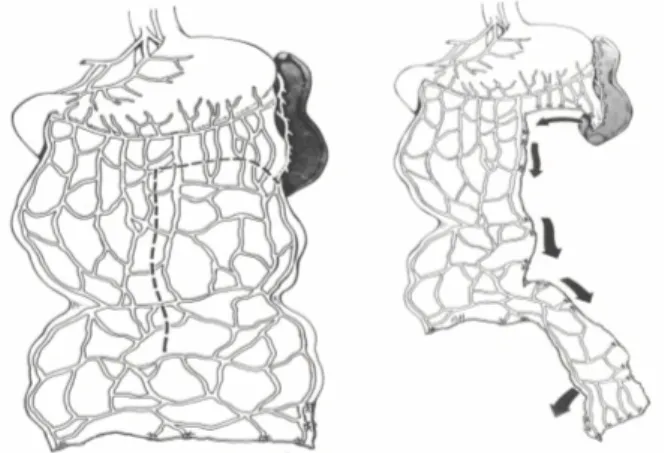
Figura 3.3.6. Estensione caudale del foglietto dorsale dell'omento (Ross e Pardo, 1993). Il secondo passaggio consiste nell’effetuare una incisione a “L” invertita, partendo dal lato sinistro, caudalmente al legamento gastrosplenico, avendo cura di effettuare una doppia legatura dei vasi omentali prima di procedere alla dissezione (Figura 3.3.7.). Al termine, il peduncolo ottenuto viene ruotato cudalmente per ottenere la massima estensione (Figura 3.3.7.).
Figura 3.3.7. Incisione a "L" invertita e ruotazione caudale del peduncolo ( Ross e Parod, 1993).
3.4. Asportazione cisti paraprostatica
Le cisti paraprostatiche di discrete dimensioni sono idonee alla resezione locale. L’intervento è di “semplice” esecuzione, infatti, in seguito a laparotomia caudale, dopo visualizzazione della cisti, procedere all’isolamento dai tessuti circostanti,
alla resezione e alla sua asportazione. Controllare eventuale emorragia mediante cauterizzazione dei vasi e suturare la breccia laparotomica.
3.5. Prostatectomia
3.5.1. Prostatectomia totale o escissionale
La prostatectomia totale può essere utilizzata nei pazienti che hanno dei tumori non metastatizzati, in caso di lesioni traumatiche gravi (Fossum et al., 2004), di ascessi o cisti prostatiche diffuse (Harari e Dupuis, 1995) o in caso di ascessi/cisti ricorrenti anche se in questo caso risulta meno consigliabile a causa dell’elevato tasso di incontinenza urinaria che ne consegue (Zimbelli, 2007).
Dopo aver inserito un catetere urinario si procede con una accurata dissezione dell’organo, come descritto precedentemente. Recidere i peduncoli e scollare il grasso periprostatico direttamente dalla capsula senza danneggiare il plesso vascolonervoso dorsale; in seguito, legare e recidere i vasi prostatici ed il dotto deferente quanto più vicino possibile alla prostata (Figura 3.5.1. A-B) (Fossum et al., 2004).
Evitare di interessare il trigono ed il collo vescicale e porre, quindi, attenzione a non ledere le arterie prostatiche uretrali e vescicale e le terminazioni nervose che servono la vescica urinaria e l’uretra membranosa.
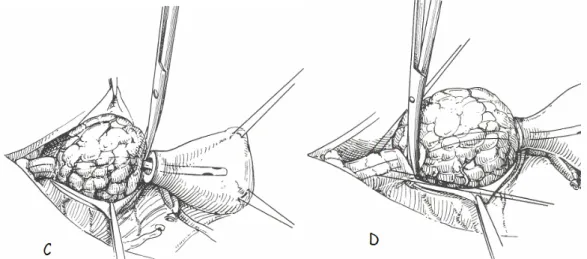
L’intervento procede con l’asportazione dell’organo incidendo a tutto spessore cranialmente e caudalmente alla prostata dopo aver retratto momentaneamente il catetere (Zimbelli, 2007). La resezione ha quindi inizio tra la vescica e la prostata cranialmente (Figura 3.5.1.C), e fra la prostata e l’uretra membranosa caudalmente (Figura 3.5.1. D). Dopo aver completato questa dissezione, si recide l’uretra in posizione craniale cercando di lasciare la maggiore porzione possibile del collo della vescica e successivamente si recide l’uretra membranosa quanto più vicino possibile alla ghiandola (Basinger e Rawlings, 1989).
Figura 3.5.1. C: resezione dell’uretra a livello del margine craniale della prostata. D: resezione dell’uretra a livello del margine caudale della prostata (Slatter, 2005).
Successivamente, far avanzare il catetere fino nella vescica ed avvicinare i monconi dell’uretra con dei punti di sutura semplici staccati in materiale sintetico assorbibile in modo tale da eseguire una anastomosi termino-terminale del collo della vescica con l’uretra membranosa (Figura 3.5.1. E-F).
Applicare i primi due punti di sutura nelle posizioni di ore 6 e di ore 12, lasciando i capi dei fili lunghi in modo da poter ruotare l’uretra durante l’esecuzione delle suture. Praticare per prima la sutura dorsale e distanziare i punti
approssimativamente di 2mm uno dall’altro e di 1.5-2mm dall’estremità del moncone (Fossum et al., 2004).
Figura 3.5.1. E: asportazione della prostata e inserimento del catetere in vescica. F: anastomosi termino-terminale tra il collo della vescica e l’uretra membranosa (Slatter, 2005).
Inserire un catetere transuretrale di Foley per deviare il flusso urinario per 5-7 giorni al fine di mantenere decompressa la vescica e limitare la tensione a livello dell’anastomosi (Harari e Dupuis, 1995). Il catetere uretrale viene, invece, rimosso molti giorni più tardi (Slatter, 2005).
A questo punto viene lavato il sito dell’intervento e la cavità addominale e disposto l’omento attorno all’anastomosi; nel caso in cui si sia resa necessaria una osteotomia pubica, fissare il segmento osteotomizzato del pube con filo metallico. Infine, suturare la breccia laparotomica.
3.5.2. Prostatectomia parziale
La prostatectomia parziale è indicata nei pazienti in condizioni stabili, per il trattamento degli ascessi ricorrenti o delle cisti che non hanno risposto alle procedure di drenaggio (Fossum et al., 2004). Questa procedura chirurgica rimuove il parenchima ghiandolare con minori possibilità di causare incontinenza urinaria rispetto alla prostatectomia totale (Slatter, 2005). Sono state sperimentate
numerose tecniche, con o senza chiusura della capsula prostatica e che prevedono l’utilizzo di diversi metodi di escissione del parenchima ghiandolare.
È stata descritta la prostatectomia parziale mediante elettrocoagulazione, con elettrobisturi, con il neodymium: ytrium-aluminum-garnet (Nd: YAG) laser o con l’aspiratore chirurgico ultrasonico, quest’ultimo utilizzato per asportare l’85% del tessuto ghiandolare senza danneggiare vasi e nervi e quindi evitare e emorragie e incontinenza urinara post-operatorie. (Harari e Dupuis, 1995).
Indipendentemente dalla metodologia di scelta, la prostata è raggiunta ed esposta come descritto in precedenza, previo inserimento di un catetere urinario.
a. Prostatectomia parziale con capsulectomia
Isolare ed allacciare o cauterizzare i vasi prostatici dorsali e laterali al loro ingresso nella capsula prima di dissezionare la capsula ed il parenchima ghiandolare; è consigliabile effettuare una occlusione temporanea dell’aorta, applicando un laccio emostatico, subito cranialmente alla sua biforcazione nelle arterie iliache esterne. Procedere, a questo punto, sezionando la prostata fino a 5mm dall’uretra impiegando le forbici, l’elettrobisturi o laser e successivamente lavare il sito operatorio. Infine, circondata l’uretra prostatica con l’omento o con il grasso periprostatico, suturare la breccia laparotomica (Figura 3.5.2.) (Fossum et al., 2004).
b. Prostatectomia parziale intracapsulare
Incidere il setto mediano ventrale della ghiandola con un elettrobisturi o con laser ed approfondire l’incisione fino a penetrare nell’uretra dalla sua superficie ventrale. Asportare tutto il parenchima, tranne uno strato di 2 o 3mm a contatto con la capsula (Figura 3.5.3.) e tutta l’uretra, tranne una striscia dorsale di 3-5mm (Fossum et al., 2004) che rappresenta la fonte per il successivo processo di riepitelizzazione (Harari e Dupuis, 1995). Lavare la parete della prostata e richiudere la capsula su di un catetere uretrale introdotto nella vescica, usando una sutura di apposizione per il primo strato ed una introflettente per il secondo in materiale riassorbibile. Il catetere è mantenuto in sede per 10 giorni.
Figura 3.5.3. Prostatectomia parziale con tecnica intracapsulare (Fossum et al., 2004). In alternativa, per conservare l’uretra, è possibile utilizzare un aspiratore chirurgico ultrasonico, strumento che frantuma, emulsiona e quindi aspira il tessuto ghiandolare prostatico, mantenendo integri gli elementi neurologici, vascolari ed il tessuto connettivo (Fossum et al., 2004; Rawlings, Mahaffey et al., 1997). Anche in questo caso, si posiziona un laccio emostatico aortico subito cranialmente alla biforcazione dell’aorta nelle arterie iliache esterne e si solleva la ghiandola tramite suture di trazione poste attorno all’urtra prossimale e distale alla
prostata inserendo, successivamente, un catetere uretrale per evidenziare ed evitare di danneggiare l’uretra stessa. Vengono eseguite due incisioni parallele nella parte ventrale della capsula prostatica utilizzando un elettrbisturi, dopo di che si inserisce l’aspiratore. Dopo aver suturato ogni piccola lacerazione dell’uretra prostatica e dopo aver asportato gli emisferi ventrali della capsula prostatica, si sutura la capsula residua attorno all’uretra prostatica con punti nodosi staccati (Slatter, 2005).
Il catetere urinario è lasciato in sede per decomprimere la vescica durante il primo periodo post-operatorio (prime 18 ore dopo l’intervento) (Rawlings, Mahaffey et al., 1997).
3.6. Alcoolizzazione
L’alcoolizzazione ecoguidata, tecnica per-cutanea utilizzata per il trattamento di cisti ed ascessi prostatici permette il drenaggio ed il successivo trattamento della cavità. È stata proposta come tecnica non invasiva e relativamente indolore e come tale può essere eseguita anche in assenza di anestesia. Inoltre, è una procedura che comporta un ridotto tasso di morbilità post-operatoria, evita il ricovero dei pazienti ed ha un costo notevolmente più basso rispetto alle altre procedure chirurgiche (Boland et al., 2003).
L’alcoolizzazione consente di evitare interventi chirurgici diretti sulla prostata e/o di orchiectomia in soggetti anziani o di posticipare, se necessario, tali trattamenti in soggetti riproduttori.
L’alcool, come agente terapeutico è già stato utilizzato in passato in medicina umana per il trattamento delle lesioni neoplastiche del fegato. L’effetto tossico dell’alcool sarebbe legato ad un danno diretto sulla cellula per un meccanismo di disidratazione ed un danno indiretto per l’ischemia da arresto o riduzione del flusso ematico in seguito alla formazione di trombi endovasali. Il tessuto danneggiato andrebbe quindi incontro ad una immediata necrosi coagulativa seguita dalla formazione di tessuto fibrotico.
Dopo tricotomia e disinfezione cutanea, si procede all’aspirazione ecoguidata del liquido contenuto all’interno delle lesioni prostatiche mediante l’utilizzo di aghi spinali (14G in caso di ascesso, 21G per le cisti). Spesso in visto dell’intervento di alcolizzazione viene somministrata al paziente una terapia a base di antiipertrofizzanti in modo tale da indurre una iniziale riduzione d volume non solo della ghiandola ma anche delle formazioni cistiche/ascessuali.
Effetuata l’aspirazione del materiale, lavare la cavità residua con soluzione fisiologica in caso di cisti o fisiologica e addizionata con antibiotico se presente ascesso. Successivamente, introdurre, mediante lo stesso ago spinale, una quantità di alcool assoluto pari ad 1/3 circa del contenuto precedentemente aspirato. Alla fine delle iniezioni, l’ago deve essere lasciato in sede per circa 30 secondi e poi estratto lentamente al fine di evitare il reflusso dell’alcool nella cavità peritoneale. Questo tipo d trattamento permette di ottenere ottimi risultati in caso di ascessi/cisti soprattutto se di piccole dimensioni e monocavitari (Zambelli, 2007).