CAPITOLO 5
SVILUPPO DI UN MODELLO PER
L’OTTIMIZZAZIONE DELLA WGSR (Water Gas
Shift Reaction)
5.1 Descrizione del Contesto Generale in cui si inserisce il Modello
sviluppato
Il contesto in cui si va a collocare il nostro lavoro è quello della produzione di Idrogeno a partire da combustibili solidi. Il processo di Gasificazione del carbone offre risultati migliori rispetto al processo di Pirolisi il quale risulta meno costoso, ma offre rese di conversione più basse, e quindi non è adatto per quei processi destinati ad elevate produzioni di idrogeno. Nell’ottica di ottenere rendimenti di conversione più elevati, quindi, un possibile scenario è quello di prendere in considerazione il processo di Gasificazione del Carbone. Questa tipologia di approccio comporta però soluzioni impiantistiche molto più complesse e quindi più costose: si rende perciò necessario realizzare impianti di grosse potenzialità per cercare di ottenere significative economie di scala.
La Gasificazione Integrata con Ciclo Combinato (IGCC) è la tecnologia più avanzata e pulita per la generazione di elettricità dal carbone. La produzione di SOX, NOX e particolato solido,
per questa tipologia di impianto, è paragonabile ai valori tipici di emissione di un sistema alimentato a gas naturale [67]. Inoltre, grazie alle alte temperature raggiunte nel gasificatore, le scorie ottenute non presentano necessità di successivi processi di inertizzazione. L’efficienza termica media è superiore ai convenzionali impianti a polverino di carbone e ciò si traduce in un abbassamento delle emissioni di CO2 di circa il 20%, per unità di energia
elettrica prodotta [67].
La tecnologia IGCC può essere favorevolmente modificata al fine di ottenere un prodotto ad alto valore aggiunto come l’idrogeno, impiegando reattori dedicati alla reazione di Shift del monossido di carbonio, seguiti da adeguati sistemi di separazione. L’idrogeno così prodotto potrà essere utilizzato come vettore energetico pulito.
Di seguito si descrive il processo di gasificazione del carbone per la produzione di idrogeno, all’interno del quale si inserisce il modello sviluppato.
Il Sistema Complessivo è costituito dall’interconnessione di quattro macro-blocchi principali costituiti da (Figura: 3.1):
• Gasificazione del carbone
• Pulizia del Syngas e Recuperi Energetici • Reazione di Water Shift (WGSR)
• Separazione dell’Idrogeno
5.1.1 Gasificazione
Nella sezione dedicata alla Gasificazione del carbone si va a produrre il Syngas, mediante conversione del combustibile solido in prodotto gassoso, che poi sarà trattato per massimizzare la resa in idrogeno e le efficienze energetiche. La Gasificazione Diretta del
carbone viene realizzata in un reattore singolo, dove carbone, ossigeno ed acqua vengono
alimentati al gasificatore; la parziale combustione del carbone fornisce l’energia necessaria alla gasificazione stessa. L’uso di ossigeno puro evita l’effetto di diluizione dell’azoto nei confronti del syngas.
Nel gasificatore si ha la produzione di Syngas ricco di CO ed H2. L’alimentazione al reattore
di gasificazione è costituita da polverino di carbone, ossigeno ad elevata purezza e vapore. Il reattore è adiabatico, pressurizzato a 25 atm ed opera a temperature comprese tra i 1200°C e 1400°C, in funzione della composizione dell’alimentazione. L’alimentazione del combustibile alimentato al gasificatore è costituita da carbone Ashland, avente composizione riportata nelle seguenti tabelle:
% Umidità 8,9
% Carbonio fisso 47,9 % Materie volatili 32,5
% Ceneri 8,9
Tabella 5.1: Analisi del carbone alimentato al Gasificatore
% Ceneri 8,9
% Carbonio 69,71
% Idrogeno 4,8
% Azoto 1,4
Il carbone in ingresso, che subisce un fortissimo riscaldamento, è soggetto a devolatilizzazione con liberazione di materiale gassoso; il char residuo subisce le reazioni di gasificazione da parte degli agenti gasificanti quali O2, CO2, H2O ed H2, mentre in fase
gassosa avvengono le reazioni di combustione, di reforming e di shift. Le principali reazioni che avvengono nel gasificatore sono quelle tra:
• Char e Ossigeno C+1O2 →2(1−1)CO+(2−1)CO2 φ φ φ con φ=(2Z+2)/(Z+2) per dp < 0.005 cm )/( 2) 095 . 0 005 . 0 ( ) 2 2 [( + − − + = Z Z dp z φ per 0.005 < dp < 0.1 cm φ=1 per 1 cm < dp Z = [CO]/[CO2]
dp = diametro della particella di char
• Char ed Anidride Carbonica C + CO2 = 2CO per T>1100°C
• Char e Vapore Acqueo C + H2O = CO + H2 per T > 1100°C
Il gas in uscita dal reattore di gasificazione raggiunge la temperatura di circa 1200°C, e la conversione del carbone risulta essere molto spinta. Le ceneri liquefatte vanno a separarsi sul fondo del gasificatore e vengono espulse.
Coal PYROLYSIS/ GASIFICATION REACTOR Oxygen Air Nitrogen Steam Fluidization Gas (from clean gas section) AIR
SEPARATION COLUMN
DIRECT GASIFICATION
SCHEME recovery to heat and gas clean up sections Char Ash
All’interno del gasificatore è possibile ottenere rese di conversione del char molto elevate ( > 95%) operando con temperature di circa 1200°C, pressioni di almeno 25 atm, e diametri delle particelle inferiori ai 100 μm (dimensioni tipiche del polverino di carbone).
5.1.2 Trattamenti primari eseguiti sul Syngas
Il syngas ottenuto viene “quenchato” con del syngas freddo di riciclo (miscelazione del syngas caldo proveniente dal gasificatore con il syngas freddo di riciclo) per ottenere una temperatura di 800°C, viene, poi, raffreddato a 380°C in un primo scambiatore, e successivamente raffreddato ancora a 235°C per un secondo recupero energetico, in cui si produce vapore a media pressione (20 atm). A questo punto si esegue una filtrazione delle ceneri volanti residue (fly ash) utilizzando un filtro a maniche. Questa tipologia di filtri non può lavorare a temperature troppo elevate (massimo a 300°C) perché avremmo un degrado delle maniche filtranti molto spinto, che porterebbe a frequenti soste dell’impianto, dovute alla sostituzione del supporto filtrante (esistono anche supporti che possono lavorare a temperature più elevate, ma sono particolarmente costosi).
La corrente di syngas, così trattata, viene separata: una parte si utilizza come gas di “quench”, l’altra parte è inviata ai processi a valle. Il primo dei processi a valle consiste nella rimozione a secco dei gas acidi per mezzo di sorbenti solidi, al fine di eliminare i problemi di corrosione e di avvelenamento relativi al catalizzatore utilizzato nel Reattore di Shift.
5.1.3 Sezione di Shift
Il syngas “ripulito” dai gas acidi è alimentato, insieme ad una corrente di vapore, al reattore catalitico di shift in cui reagiscono CO ed H2O per dare CO2 ed H2. Le condizioni operative
sono quelle tipiche di questa reazione, quindi reattore isotermo a 300°C e pressione di alimentazione dei prodotti (25 atm); il mantenimento della temperatura è ottenuto mediante produzione di vapore a bassa pressione (6.5 atm) il quale viene impiegato nel ciclo a vapore presente nell’impianto per la generazione di energia elettrica. Si utilizza una configurazione di reattore a letto fisso.
5.1.4 Separazione dell’Idrogeno
A valle dello shift è presente il sistema di separazione di idrogeno PSA (Pressure Swing Adsorption) da cui si ottiene la corrente di idrogeno desiderata ad elevata purezza ( > 99.99%). Si utilizzano una serie di reattori batch che lavorano in parallelo, permettendo la produzione di un flusso continuo di idrogeno: mentre alcuni eseguono l’adsorbimento, altri effettuano il desorbimento. L’efficienza di separazione di una tipica unità PSA è di circa il 98%.
La corrente povera di idrogeno, ma ricca ancora in CO, è impiegata come combustibile in un turbogas: essa è inviata in un combustore operante a 15 atm insieme ad una portata di aria (comburente), i fumi caldi della combustione vengono fatti espandere in una turbina a gas. A valle della turbina è presente un HRSG (Heat Recovering Steam Generator) che utilizza il calore residuo dei fumi esausti per la produzione di vapore a 70 atm.
Il vapore prodotto nei recuperi termici presenti nell’impianto è utilizzato per produrre energia elettrica mediante espansione in turbina a vapore, la condensazione è effettuata supponendo di utilizzare acqua di mare disponibile a 15-20°C.
Nella tabella seguente riportiamo i parametri operativi relativi all’intero processo:
TEMPERATURA (°C) PRESSIONE (atm)
Gasificatore 1200 Gasificazione 25 Quench 800 Recupero HP 400 Recupero MP/Pulizia 235 Shift 300 Camera combustion e 1300 Turbogas 15
5.2 Sviluppo del modello per la progettazione di massima del
Reattore di WGSR
Il lavoro che andremo a svolgere, come già detto, consiste nell’ottimizzazione della resa in Idrogeno all’interno della Water Gas Shift Section. La WGSR è quindi la reazione della quale ci occuperemo per l’ottenimento di idrogeno. Dovremo cercare di ottimizzare la resa di tale reazione mediante l’uso di adatti catalizzatori operanti alle condizioni operative più redditizie.
Procedimento Adottato
Lo Scopo del nostro studio è quello di ottimizzare la resa in idrogeno cercando di minimizzare la quantità di catalizzatore necessaria a tale fine.
Per l’individuazione delle migliori condizioni operative a cui condurre la WGSR faremo uso di un Plug Flow Reactor catalitico con catalizzatore a letto fisso (scelta dettata dalla consultazione di diversi articoli riportati in letteratura) [23, 25, 68, ecc].
Si effettua l’ipotesi di Reattore Isotermo (ipotesi di cui verificheremo la validità in seguito) e di miscela gassosa ideale.
Letto fisso di catalizzatore OUTPUT Xco out Xh2o out Xh2 out Xco2 out P out = 25 atm T out Portata out = 2770 kmol/hr INPUT Xco in = 0,36 Xh2o in = 0,36 Xh2 in = 0,22 Xco2 in = 0,06 P in = 25 atm T in (Cu=473K (Fe=673K) Portata in = 2770 kmol/hr
Per quanto riguarda le Condizioni Operative:
• Pressione: lavoreremo alla P alla quale arriva la corrente gassosa dalle lavorazioni precedenti (25 atm).
• Portata Gassosa: useremo la portata in arrivo dalle precedenti lavorazioni (2570 kmol/hr), con le rispettive composizioni. In una seconda analisi aggiungeremo una corrente di vapore (200 kmol/hr) per raggiungere un rapporto H2O/CO = 1 al fine di migliorare la
resa in termini di produzione di idrogeno.
• Temperatura: ogni reattore opererà alla T caratteristica del catalizzatore utilizzato (la temperatura a cui opera il catalizzatore di WGS ad alta T, coincide con la temperatura a cui arriva la corrente gassosa dalle lavorazioni precedenti ; 400°C).
Proprietà Termodinamiche: per la valutazione della Costante di Equilibrio Termodinamico
della reazione, useremo la relazione fornita da Moe [68]:
Keq e
4577.8 K⋅ T1 −4.33
:=
Per quanto riguarda la Cinetica di Reazione useremo la seguente equazione empirica (ricavata dalla letteratura [68]):
rco k Pco Ph2o⋅ Pco2 Ph2⋅
Keq − ⎛⎜
⎝ ⎞⎟⎠
⋅
che esprime la velocità di scomparsa del CO in funzione della: • Costante di Equilibrio (Keq)
• Costante Cinetica (k)
• Composizione della Portata Gassosa; espressa in termini di Pressione parziale (Pi)
(la Frazione Molare, dell’elemento i-esimo di una miscela gassosa è data dalla pressione parziale dell’elemento i-esimo stesso diviso la Pressione tot del sistema: xi = Pi/P).
La costante cinetica k è data dall’equazione:
k ko e E − R1 T1⋅ ⋅ := con
k0 Fattore preesponenziale della costante di velocità
E Energia di Attivazione
R1 Costante dei gas (8,314 J/mol K nell’ipotesi di gas ideali) T1 Temperatura assoluta (K)
(i dati citati relativi ai singoli catalizzatori sono stati ricavati dalla letteratura)
Per ricavare le composizioni in uscita dai reattori studiati si sono utilizzate le seguenti relazioni relative al Bilancio di Materia (CO + H2O = H2 + CO2):
• moli di CO reagite = moli di CO iniziali * Conversione Effettiva del CO nel reattore • moli di CO = moli di CO entrate - moli di CO reagite
• moli di H2O = moli di H2O entrate - moli di CO reagite
• moli di H2 = moli di H2 entrate + moli di CO reagite
• moli di CO2 = moli di CO2 + moli di CO reagite
Tramite la seguente equazione integrale:
Mcat mi Xcoi Xcof Xco 1 rco − ⎛⎜ ⎝ ⎞⎟⎠ ⌠ ⎮ ⎮ ⌡ d ⎡ ⎢ ⎢ ⎣ ⎤ ⎥ ⎥ ⎦ ⋅ := con
Xcof = frazione molare del CO in uscita al reattore Xcoi = frazione molare del CO in ingresso al reattore
siamo in grado di ricavare la massa del catalizzatore necessaria affinché, per mezzo della WGSR, avvenga nel reattore, la Conversione Effettiva ipotizzata.
Effettuiamo delle Analisi di Sensitività (ipotizzando una conversione del CO pari al 60% della conversione di equilibrio al fine di identificare il miglior catalizzatore operante a bassa T e le sue migliori condizioni operative, ed identificheremo le migliori condizioni operative del catalizzatore operante ad alta T) nelle quali ricaviamo la Massa Catalitica e la Conversione del CO nel reattore (frazione molare del CO nel gas in uscita) al variare della:
• Temperatura: - fra 170 e 230°C per catalizzatori di shift a bassa T a base di Cu - fra 370 e 430°C per catalizzatori di shift ad alta T a base di Fe/Cr
• Pressione: - fra 19 e 31 atm
• Quantità di Acqua alimentata al reattore: (rapporto molare XH2O/XCO: fra 0,5 ed 1,1)
Per ogni catalizzatore studiato si ricava la configurazione ottimale del reattore catalitico (T, Portata di Vapore, Massa del Catalizzatore), in termini di produzione di idrogeno.
Si sviluppa una configurazione impiantistica con due Reattori in Serie (al fine di una migliore ottimizzazione nella resa in idrogeno espressa in termini di conversione del CO), il primo operante ad alta T alle proprie condizioni ottimali, il secondo operante a bassa T, anch’esso operante alle proprie condizioni ottimali (si ipotizza una conversione del CO pari all’80% della conversione di equilibrio).
Le condizioni operative di entrambi i reattori, ed il catalizzatore operante a bassa T, sono stati scelti in base ai risultati delle analisi di sensitività.
T in1 = 673K T in2 = 473K Xco in = 0,36 Xh2o in = 0,36 Xh2 in = 0,22 Xco2 in = 0,06 P in = 25 atm T in = 673K Portata in = 2770 kmol/hr heat
recovery LOW T REACTOR HIGH T
REACTOR Steam
Figura 5.3: Schematizzazione della configurazione dei due reattori in serie
Si effettua un confronto, alle stesse condizioni operative (stessa portata, composizione e pressione) fra i due singoli reattori operanti alle loro condizioni ottimali, ed il modello con i due stessi reattori messi in serie, al fine di individuare la soluzione impiantistica che offra la migliore resa in idrogeno ottimizzando la massa catalitica utilizzata.
Sul modello scelto, attraverso un bilancio energetico, ricaviamo la Temperatura della corrente gassosa in uscita dal reattore, al fine di verificare la validità dell’ipotesi, fatta all’inizio, di reattore isotermo. Equazione di bilancio dell’energia dalla quale ricaviamo la Tout:
ΣMini hini⋅ −ΣMouti houti⋅ +Qreaz 0
5.2.1 Soluzione Impiantistica
La reazione di WGSR, generalmente, viene condotta in reattori tubolari all’interno dei quali si mette un letto fisso catalitico al fine di spostare la reazione verso la produzione di idrogeno. Si sceglie di operare in reattori convenzionali a letto fisso.
Sono in fase di studio anche Membrane Selettive, poste all’interno dei reattori catalitici, che hanno il compito di allontanare l’idrogeno dalla zona di reazione al fine di promuoverne la
formazione, spostando l’equilibrio della reazione verso la formazione del prodotto desiderato, ma tali membrane, allo stato attuale, non trovano ancora grandi applicazioni a livello industriale a causa di problematiche non ancora risolte fra le quali:
• Costi troppo elevati: non sono state testate in maniera sufficiente a determinare la loro potenziale convenienza in un’applicazione su scala industriale.
• Avvelenamento della superficie
• Limitazioni dal punto di vista operativo: operano con efficienze accettabili solo in un preciso range di temperature
• Decadimento termico: sottoporre membrane a cicli termici provoca il decadimento della loro efficienza di separazione e quindi la durata della membrana stessa
• Perdita di integrità strutturale: in certe condizioni le membrane possono subire un ri-arrangiamento della loro struttura atomica, variazioni della rugosità superficiale, corrosione di tipo pitting, formazione di uno strato di impurezze, effetti che possono inficiare l’integrità strutturale della membrana e le sue performance.
La reazione di formazione dell’idrogeno è ad equilibrio limitato; il grado di conversione è limitato dalla chimica del sistema, dalla T di reazione e dalla P del sistema stesso. La reazione di WGS è reversibile e mediamente esotermica. La conversione dei reagenti in CO2 ed in H2 è
termodinamicamente favorita alle basse temperature, ma queste condizioni sfavoriscono la cinetica di reazione. Viceversa, alle alte temperature la massima resa termodinamica ottenibile si abbassa, ma aumenta la cinetica di reazione. Per aumentare la conversione del CO, e per raggiungere una conversione adeguata ai processi industriali, si conduce la reazione in due
stadi catalitici separati operanti a T diverse:
• il Primo stadio opera ad elevate T in un range di 300°C-450°C. In questa fase si favorisce la cinetica di reazione della WGSR ed avviene la maggior parte della conversione del CO, ma non si raggiunge una conversione di equilibrio soddisfacente a causa della bassa resa termodinamica ottenibile (vi è ancora la presenza di una quantità troppo elevata di CO), quindi si invia la corrente gassosa, arricchita in Idrogeno, ad una seconda fase di trattamento
rispetto alla fase precedente, ma dove si otterrà una buona resa del CO dal punto di vista della conversione termodinamica.
Fra il 1° ed il 2° stadio si effettua un raffreddamento del flusso gassoso ed il calore recuperato dal raffreddamento della corrente gassosa viene utilizzato per produrre vapore o per riscaldare il boiler dell’acqua di alimentazione. Il vapore a sua volta può essere utilizzato per la produzione di energia elettrica mediante espansione in turbina.
I fattori che contribuiscono all’adozione del processo a due stadi sono prevalentemente:
1 l’alternanza fra velocità di reazione e conversione di equilibrio: la WGSR è una reazione esotermica e reversibile, quindi, alte T portano ad elevate velocità di reazione ma basse conversioni di equilibrio. La > parte della conversione ha luogo nel primo reattore dove le velocità sono >; nel secondo reattore si ottengono conversioni elevate.
2 l’adattabilità al contesto operativo: l’alimentazione a tale processo proviene dalla gasificazione del carbone dove le T in uscita sono già alte e questo si integra bene col tipo di processo trattato.
I vantaggi dello shift eseguito a due livelli di temperatura sono:
• Minimizzazione reazioni parassite indesiderate nello stadio a bassa T (Fisher Tropsch) • Buona integrazione con le temperature di uscita della corrente gassosa dallo stadio di
pulizia del syngas
• Basse richieste di vapore aggiuntivo • Possibilità di operare ad alte pressioni
• Alta resistenza all’avvelenamento del Catalizzatore operante ad alta T
Altri processi catalitici sono in fase di studio ma allo stato delle conoscenze attuali presentano ancora delle problematiche irrisolte e delle controindicazioni che li rendono ancora poco appetibili rispetto al metodo “tradizionale” scelto.
5.2.2 Scelta dei Catalizzatori
Per quanto riguarda la scelta dei catalizzatori si cerca di muoverci all’interno di soluzioni consolidate che trovano già applicazione a livello industriale (l’attività catalitica è espressa mediante il grado di conversione del CO):
• WGSR condotta su Catalizzatori ad alta T: si usano catalizzatori a base di ossidi di Ferro (Fe2O3) e Cromo di (Cr2O3); in questa fase, dove è favorita la cinetica di reazione, avviene
la maggior parte della conversione del CO, ma non si raggiunge una conversione di equilibrio soddisfacente per il successivo utilizzo della corrente gassosa (vi è ancora la presenza di una quantità troppo elevata di CO). Si opera in un range di T che va dai 350°C ai 450°C.
Un tipico catalizzatore è composto al 92% peso da ematite (Fe2O3) e all’8% peso da
Cr2O3. Sotto le condizioni della WGSR l’ematite è rapidamente ridotta a magnetite
(Fe3O4), sostanza attiva per la WGSR, mentre il Cr rimane allo stato di ossidazione +3. Il
Cr funziona come stabilizzatore strutturale, inibendo la ri-cristallizzazione della magnetite
e la ri-formazione dell’ematite, quindi è ritenuto il responsabile dell’attività e della stabilità, del catalizzatore, a lungo termine.
I gruppi di piccole particelle di ematite, che si formano sotto le condizioni della WGSR ad elevata T, riducono l’area superficiale disponibile del catalizzatore, riducendo l’attività catalitica verso la WGSR stessa. In conclusione si può affermare che le proprietà catalitiche (attività e stabilità), dei catalizzatori per la WGSR ad elevate T, dipendono dalle dimensioni delle particelle di catalizzatore e dal contenuto di Cr sottoforma di ossido bimetallico.
Questi catalizzatori sono solitamente sottoforma di “tablets” di 6*6 mm o 9,5*9,5mm. I gas convertiti sono raffreddati, fuori dal reattore per poi essere inviati al convertitore di shift a circa 200-215°C per completare la WGSR sui catalizzatori a bassa T. Il calore recuperato dal raffreddamento della corrente gassosa viene utilizzato per produrre vapore o per riscaldare il boiler dell’acqua di alimentazione.
• WGSR condotta su Catalizzatori a bassa T: si usano catalizzatori a base di ossidi di Cu/Zn che operano per T che vanno dai 150°C ai 300°C circa. Normalmente sono usati in presenza di Al2O3, che dà una > stabilità termica al catalizzatore e riduce l’effetto
disattivante del CO. L’ossido di Zinco (ZnO) funge da stabilizzatore strutturale. I catalizzatori Cu/ZnO/Al2O3, usati nel secondo stadio, devono essere più attivi di quelli
usati nel primo, perché a basse T la cinetica della WGSR risulta più sfavorita. In questo stadio viene completata la conversione del CO e si raggiunge una buona conversione di equilibrio. La WGSR a bassa T viene condotta in reattori tubolari a letto fisso il cui
Si ritiene che il componente chiave della WGSR a bassa T sia il Cu, in quanto la trasformazione del CO in CO2 avviene proprio sulla superficie di questo elemento,
secondo due ipotesi di meccanismo di reazione formulate per la WGSR (già trattate nel capitolo 4):
1 Meccanismo Associativo 2 Meccanismo Rigenerativo
L’area superficiale dei catalizzatori utilizzati diminuisce all’aumentare della T di calcinazione con la quale vengono preparati i catalizzatori stessi (probabilmente a causa della parziale sinterizzazione delle particelle catalitiche). All’aumentare della T di calcinazione aumentano le dimensioni delle particelle dei cristalliti di Rame ed aumenta l’attività catalitica (misurata come mmol di idrogeno prodotto, per ora, per unità di area superficiale di rame). La distribuzione delle dimensioni delle particelle dei cristalliti di Rame deve rientrare nel range di 10-20 nm. L’osservazione dell’aumento delle dimensioni delle particelle dei cristalliti di Cu e dell’aumento dell’attività catalitica all’aumentare della T di calcinazione, dimostra l’importante contributo dato dalla fase dei cristalliti di Cu all’attività totale dei catalizzatori.
Uno svantaggio dei catalizzatori a base di Rame è la loro tendenza alla disattivazione in presenza di aria, ed acqua condensata, durante le fasi di start-up e di shut-down.
Per questi motivi negli ultimi anni è aumentato l’interesse verso i catalizzatori a base di ossidi di metalli nobili che non presentano questo tipo di problemi e che risultano essere più attivi dei catalizzatori tradizionali. I catalizzatori per la WGSR a bassa T più promettenti da questo punto di vista sono quelli a base di Au o Pt, supportati su CeO2, ma a loro sfavore vi sono
delle problematiche non ancora risolte:
• Costi elevati
• La loro attività e stabilità catalitica diminuisce rapidamente col tempo • Non sono ancora consolidati dal punto di vista industriale
Le basse T sono le più favorevoli per l’equilibrio della WGSR finalizzata alla produzione di idrogeno. Ipotizziamo di operare in condizioni isoterme, condizione operativa che ci consente di ottenere la massima produzione di idrogeno espressa in termini di conversione del CO (più avanti effettueremo la verifica dell’applicabilità di questa ipotesi al modello sviluppato).
I catalizzatori trattati in questo capitolo, sia quelli operanti a bassa T che quelli operanti ad alta T, sono sensibili all’avvelenamento da parte di impurità contenenti cloro e zolfo, ma trattando una corrente gassosa proveniente da una fase di “pulizia” del syngas, nella quale si riducono tali sostanze a quantità insignificanti, non ci soffermeremo su questo tipo di problema.
L’uso di un eccesso di vapore, per entrambe le reazioni di WGSR, alle diverse T: • favorisce una > conversione di equilibrio
• riduce la T raggiunta nel reattore
• aiuta a prevenire la formazione di depositi di carbonio nella zona di ingresso del reattore
• permette di minimizzare le reazioni indesiderate competitive con la WGSR.
Bisogna stare attenti, però, ad evitare la formazione di condense, all’interno del reattore, che possono danneggiare il catalizzatore e ridurne l’attività catalitica con conseguente perdita in termini di conversione del CO. Per evitare questo si integrerà la portata gassosa con una quantità di vapore non troppo elevata (vedi paragrafi successivi).
La corrente di syngas che andremo a trattare è quella proveniente dallo stadio di “Clean up and Steam Recovery” nella quale si eliminano le impurità contenenti S ed Cl, dannose per i catalizzatori che andiamo a studiare in quanto ne disattivano i siti attivi riducendone l’attività catalitica.
La composizione di tale gas è espressa nella tabella 5.1:
Composizione del Syngas
Portata
(kmol/hr) Frazione Molare
CO 1000 0,39 H2O 800 0,31 H2 600 0,23 CO2 170 0,07 CH4 (tracce) - H2S (tracce) -
Nei due paragrafi seguenti andremo a studiare:
• il comportamento di tre catalizzatori, a base di Cu, per la WGSR a bassa T, al variare delle condizioni operative, al fine di individuare quello che ci permetterà di raggiungere la migliore configurazione per il raggiungimento di una buona resa in termini di conversione del CO, cercando di minimizzare la massa di catalizzatore necessario a tale proposito
• il comportamento del catalizzatore di WGSR operante ad alta T, a base di Fe/Cr, di uso ormai consolidato nell’industria chimica, al fine di raggiungere la migliore configurazione in termini di condizioni operative adeguate, per il raggiungimento della configurazione che ci permetterà di raggiungere una buona resa in CO con una ragionevole quantità di massa catalitica.
5.3 Studi su Catalizzatori (a base di Cu e Cu/Zn) per la WGSR
condotta a bassa T
Le condizioni operative a cui operiamo sono:
- T = 473K (200°C) (T intermedia a cui operano i catalizzatori per la WGSR a bassa T) - P = 25 atm (Pressione alla quale arrivano i gas dai trattamenti precedenti)
- Portata di gas = 2570 kmol/hr (Portata gassosa in arrivo dai trattamenti precedenti)
Per la valutazione della costante di equilibrio termodinamico della reazione, useremo la relazione fornita da Moe [68]:
Keq e
4577.8 K⋅ T1 −4.33
:=
Per quanto riguarda la cinetica di reazione useremo la seguente equazione empirica [68]:
rco k Pco Ph2o⋅ Pco2 Ph2⋅
Keq − ⎛⎜
⎝ ⎞⎟⎠
⋅
che esprime la velocità di scomparsa del CO in funzione della: • Costante di Equilibrio (Keq)
• Costante Cinetica (k)
(la Frazione Molare, dell’elemento i-esimo di una miscela gassosa è data dalla pressione parziale dell’elemento i-esimo stesso diviso la Pressione tot del sistema: xi = Pi/P).
La costante cinetica k è data dall’equazione:
k ko e E − R1 T1⋅ ⋅ := con
k0 Fattore preesponenziale della costante di velocità
E Energia di Attivazione
R1 Costante dei gas (8,314 J/mol K nell’ipotesi di gas ideali) T1 Temperatura assoluta (K)
I tre catalizzatori (a base di Cu) studiati sono:
1) Cu/Al
2O
3Le proprietà di questo catalizzatore sono state reperite dagli articoli [68, 69]
- k0 = 7,4*107
- E = 69,3*103 J/mol - Porosità = 0,7 - Densità = 380 kg/m3
- v0 = 0,5 m/s (velocità del gas in ingresso al reattore)
- Composizione (% in peso) = 35% Cu, 65% Al2O3
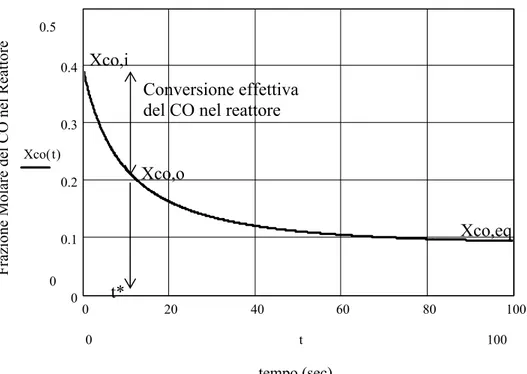
Implementando le relative formule su Mathcad otteniamo l’andamento della composizione del CO nel tempo, all’interno del reattore (figura 5.2):
0 20 40 60 80 100 0 0.1 0.2 0.3 0.4 tempo (sec)
Frazione Molare del CO nel Reattore
0.5 0 Xco t( ) 100 0 t Xco,i Conversione effettiva del CO nel reattore
Xco,o
t*
Xco,eq
Figura 5.4: Andamento della Frazione Molare del CO, nel tempo, all’interno del reattore (Reattore singolo: T = 473 K, P = 25 atm, Portata = 2570 kmol/hr)
Come si vede dalla figura 5.2, all’Equilibrio Termodinamico, si ottengono i seguenti valori:
•
Frazione Molare del CO = 0,096•
Conversione del CO = 75,8%.•
Tempo necessario per raggiungere l’Equilibrio TD = 90 secIpotizzando, all’interno del reattore, una Conversione del CO del 60%, rispetto alla conversione teorica di equilibrio, si ottengono i seguenti valori:
• Frazione Molare del CO = 0,213
• Tempo di Residenza del gas (t*) = 12 sec. • Conversione Effettiva = 0,455 (45%)
A questo punto tramite la seguente equazione integrale:
Mcat mi Xcoi Xcof Xco 1 rco − ⎛⎜ ⎝ ⎞⎟⎠ ⌠ ⎮ ⎮ ⌡ d ⎡ ⎢ ⎢ ⎣ ⎤ ⎥ ⎥ ⎦ ⋅ := con
Xcof = frazione molare del CO in uscita al reattore (con conversione al 60% di quella di
equilibrio)
Xcoi = frazione molare del CO in ingresso al reattore
siamo in grado di ricavare la massa del catalizzatore necessaria affinché, per mezzo della WGSR, avvenga nel reattore, la Conversione Effettiva ipotizzata:
• Massa Catalitica = 27,5 kg • Diametro del Reattore = 1,7 m • Lunghezza del Reattore = 12,2 m
(Per l’esecuzione dei calcoli vedi Appendice A).
2) Cu/ZnO/Al
2O
3Le proprietà di questo catalizzatore sono state reperite dagli articoli [68, 14]
- k0 = 2,97*105
- E = 47,4*103 J/mol - Porosità = 0,5 - Densità = 414 kg/m3
- v0 = 0,5 m/s (velocità del gas in ingresso al reattore)
- Composizione (% in peso) = 33% Cu, 47% ZnO, 20% Al2O3
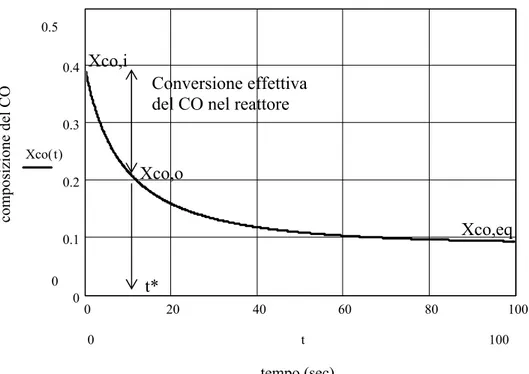
Implementando le relative formule su Mathcad otteniamo l’andamento della composizione del CO nel tempo, all’interno del reattore (figura 5.3):
0 20 40 60 80 100 0 0.1 0.2 0.3 0.4 tempo (sec) composizione del CO 0.5 0 Xco t( ) 100 0 t Xco,i Conversione effettiva del CO nel reattore
Xco,o
t*
Xco,eq
Figura 5.5: Andamento della frazione molare del CO, nel tempo, all’interno del Reattore (Reattore singolo: T = 473 K, P = 25 atm, Portata = 2570 kmol/hr)
Come si vede dalla figura 5.3, all’Equilibrio Termodinamico, si ottengono i seguenti valori:
• Frazione Molare del CO = 0,094 (molto simile a quella del catalizzatore precedente) • Conversione del CO = 0,76 (76%)
• Tempo necessario per raggiungere l’Equilibrio TD = 87 sec
La differenza con il caso precedente sta nella cinetica di reazione che in questo secondo caso, risulta leggermente favorita.
Ipotizzando all’interno del reattore una Conversione del CO del 60%, rispetto alla conversione teorica di equilibrio, si ottengono i seguenti valori:
• Frazione molare del CO = 0,212
• Tempo di Residenza del gas (t*) = 16 sec. • Conversione Effettiva = 0,456 (45,6%)
Mcat mi Xcoi Xcof Xco 1 rco − ⎛⎜ ⎝ ⎞⎟⎠ ⌠ ⎮ ⎮ ⌡ d ⎡ ⎢ ⎢ ⎣ ⎤ ⎥ ⎥ ⎦ ⋅ := con
Xcof = frazione molare del CO in uscita al reattore (con conversione al 60% di quella di
equilibrio)
Xcoi = frazione molare del CO in ingresso al reattore
siamo in grado di ricavare la massa del catalizzatore necessario affinché, per mezzo della WGSR, avvenga nel reattore, la Conversione Effettiva ipotizzata:
• Massa Catalitica = 26,2 kg • Diametro del Reattore = 1,7 m • Lunghezza del Reattore = 12 m
(Per l’esecuzione dei calcoli vedi Appendice B).
3) ICI-Cu/ZnO/Al
2O
3Le proprietà di questo catalizzatore sono state reperite dagli articoli [68, 70]
(il prefisso “ICI” è dato dal nome dell’industria che produce tale catalizzatore: “Industrial Commodities Incorporation”)
- k0 = 3,99*106
- E = 52,8*103 J/mol - Porosità = 0,5 - Densità = 523 Kg/m3
- v0 = 0,5 m/s (velocità del gas in ingresso al reattore)
- Composizione (% in peso) = 60% Cu, 30% ZnO, 10% Al2O3
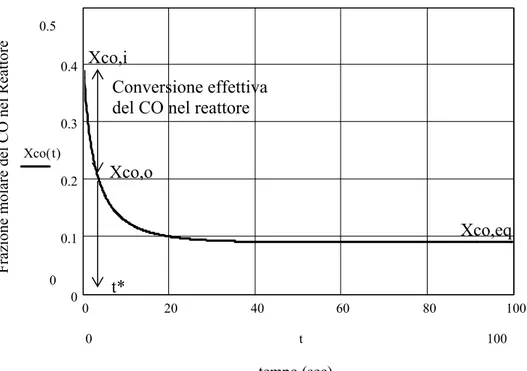
Implementando le relative formule su Mathcad otteniamo l’andamento della composizione del CO nel tempo, all’interno del reattore (figura 5.4):
0 20 40 60 80 100 0 0.1 0.2 0.3 0.4 tempo (sec)
Frazione molare del CO nel Reattore
0.5
Xco t( )
100
0 t
Conversione effettiva del CO nel reattore
Xco,o Xco,i
Xco,eq
0 t*
Figura 5.6: Andamento della frazione molare del CO, nel tempo, all’interno del Reattore (Reattore singolo: T = 473 K, P = 25 atm, Portata = 2570 kmol/hr)
Come si vede dalla figura 5.4, all’Equilibrio Termodinamico, si ottengono i seguenti valori:
• Frazione molare del CO = 0,091 (molto simile a quella dei catalizzatori precedenti) • Conversione del CO = 0,767 (76,7%)
• Tempo necessario per raggiungere l’Equilibrio TD = 40 sec
La differenza con i casi precedenti sta nella cinetica di reazione che in quest’ultimo caso, come si può osservare dal confronto delle tre curve, risulta ampiamente favorita (la curva converge molto più velocemente al valore di equilibrio). Se si considerano gli ultimi due catalizzatori (Cu/ZnO/Al2O3 ed ICI-Cu/ZnO/Al2O3) si può osservare come raddoppiando la %
in peso del Rame (consideriamo catalizzatori composti dalle stesse sostanze) la cinetica della reazione aumenta notevolmente, e questo asseconda la teoria che i Siti Attivi dei catalizzatori a base di Cu e Cu/Zn stiano sulla superficie dei cristalliti di Rame [23]. Si può notare, inoltre anche il fatto che l’allumina (Al2O3) e l’ossido di Zn (ZnO) non hanno un ruolo diretto
nell’attività catalitica della WGSR, infatti la loro funzione è quella di incrementare la stabilità termica del catalizzatore e di ridurre l’effetto disattivante del CO (al diminuire delle loro quantità è aumentata notevolmente la cinetica di reazione e leggermente la conversione di equilibrio).
Ipotizzando all’interno del reattore una Conversione del CO del 60%, rispetto alla conversione teorica di equilibrio, si ottengono i seguenti valori:
• Frazione Molare del CO in uscita = 0,21 • Conversione Effettiva = 46,1%
• Tempo di Residenza del gas (t*) = 3 sec (sensibilmente ridotto rispetto a quello dei due casi precedenti)
A questo punto tramite l’equazione integrale:
Mcat mi Xcoi Xcof Xco 1 rco − ⎛⎜ ⎝ ⎞⎟⎠ ⌠ ⎮ ⎮ ⌡ d ⎡ ⎢ ⎢ ⎣ ⎤ ⎥ ⎥ ⎦ ⋅ := con
Xcof = frazione molare del CO in uscita al reattore (con conversione al 60% di quella di
equilibrio)
Xcoi = frazione molare del CO in ingresso al reattore
siamo in grado di ricavare la massa del catalizzatore necessario affinché, per mezzo della WGSR, avvenga nel reattore, la Conversione Effettiva ipotizzata:
• Massa Catalitica = 8 kg (nettamente inferiore a quella dei due casi precedenti)
• Diametro del Reattore = 1,7 m • Lunghezza del Reattore = 3,4 m
(Per l’esecuzione dei calcoli vedi Appendice C).
Conclusione:
Dall’analisi dei dati ottenuti studiando i tre catalizzatori per la WGSR a bassa T, funzionanti alle stesse condizioni operative, si può stabilire che, alle condizioni operative adottate, il catalizzatore ICI-Cu/ZnO/Al2O3 è quello che raggiunge risultati leggermente migliori, in
5.3.1 Analisi di Sensitività sui Catalizzatori, a base di Cu e Cu/Zn, utilizzati
per la WGSR condotta a bassa T
Effettuiamo delle Analisi di Sensitività sui catalizzatori studiati al fine di ricavare:
• Massa del Catalizzatore affinché si realizzi, nel reattore, la Conversione Effettiva • Conversione di Equilibrio del CO nel Reattore
• Frazione Molare del CO in uscita dal Reattore, all’Equilibrio
al variare, nel reattore, di:
• Temperatura (fra i 443K ed i 503K per i catalizzatori a operanti a bassa T; e fra i 643K ed i 703K per il catalizzatore operante ad alta T )
• Pressione (fra 19 e 31 atm; intervallo attorno al valore di 25 atm alla quale arriva il gas dalle precedenti fasi di lavorazione)
• Quantità di Vapore Acqueo in ingresso (ovvero variando il rapporto H2O/CO in
alimentazione fra 0,5 ed 1,1; intervallo attorno al rapporto di 0,8 proveniente dalle lavorazioni precedenti)
fissando di volta in volta gli altri parametri. Lo scopo di quest’analisi è quello di ricavare la configurazione ottimale a cui possono operare i singoli Reattori Catalitici.
Risultati dell’analisi di Sensitività al variare della T, avendo fissato la Portata (2570 kmol/hr) e la Pressione del sistema (25 atm):
CATALIZZATORI per la WGSR a bassa T. Vario la T da 170 a 230°C:
TEMPERATURA CATALIZZATORE MASSA del del CO nel Reattore CONVERSIONE FRAZIONE MOLARE del CO in uscita dal Reattore
Cu/ZnO/Al2O3 T0 = 443 K T1 = 453 K T2 = 463 K T3 = 473 K T4 = 483 K T5 = 493 K T6 = 503 K M0 = 51,90 kg M1 = 41,88 kg M2 = 33,32 kg M3 = 26,23 kg M4 = 20,52 kg M5 = 16,04 kg M6 = 12,58 kg C0 = 0,712 C1 = 0,737 C2 = 0,752 C3 = 0,760 C4 = 0,760 C5 = 0,757 C6 = 0,752 X0 = 0,112 X1 = 0,102 X2 = 0,097 X3 = 0,094 X4 = 0,093 ← config. migliore X5 = 0,095 X6 = 0,097 ICI-Cu/ZnO/Al2O3 T0 = 443 K T1 = 453 K T2 = 463 K T3 = 473 K T4 = 483 K T5 = 493 K T6 = 503 K M0 = 18,57 kg M1 = 14,07 kg M2 = 10,55 kg M3 = 7,88 kg M4 = 5,91 kg M5 = 4,47 kg M6 = 3,41 kg C0 = 0,750 C1 = 0,764 C2 = 0,769 C3 = 0,767 C4 = 0,763 C5 = 0,758 C6 = 0,752 X0 = 0,097 X1 = 0,092 X2 = 0,090 ← config. migliore X3 = 0,091 X4 = 0,092 X5 = 0,094 X6 = 0,097 Cu/Al2O3 T0 = 443 K T1 = 453 K T2 = 463 K T3 = 473 K T4 = 483 K T5 = 493 K T6 = 503 K M0 = 68,27 kg M1 = 52,22 kg M2 = 38,46 kg M3 = 27,48 kg M4 = 19,28 kg M5 = 13,48 kg M6 = 9,50 kg C0 = 0,656 C1 = 0,710 C2 = 0,742 C3 = 0,758 C4 = 0,761 C5 = 0,758 C6 = 0,752 X0 = 0,134 X1 = 0,113 X2 = 0,100 X3 = 0,094 X4 = 0,093 ← config. migliore X5 = 0,094 X6 = 0,097
Per quanto riguarda i singoli Catalizzatori si osserva che:
Come si può vedere anche dai seguenti grafici, (figure 5.4, 5.5 e 5.6) al variare della T si ottiene la configurazione migliore per il catalizzatore ICI-Cu/ZnO/Al2O3 che fornisce la
migliore conversione del CO (anche se di poco) alla T più bassa e con la minore massa catalitica impiegata (circa la metà rispetto agli altri due casi).
Dai seguenti grafici (figure 5.5, 5.6 e 5.7), si può avere un quadro più chiaro dei risultati ottenuti:
Andamento della Massa del Catalizzatore in funzione della T
0 10 20 30 40 50 60 70 80 440 450 460 470 480 490 500 510 Temperatura (K) M a ssa C a ta liz z a tor e ( k g) Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.7: Andamento della Massa Catalitica in funzione della T (P=25atm, Portata=2570kmol/hr)
Andamento della Frazione Molare del CO in uscita dal Reattore, in funzione della T 0,08 0,09 0,1 0,11 0,12 0,13 0,14 440 450 460 470 480 490 500 510 Temperatura (K) Fr a z ione Mol a re de l CO Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.8: Andamento della Frazione Molare del CO, all’equilibrio, in uscita dal Reattore, in funzione della T (P=25atm, Portata=2570kmol/hr)
Andamento della conversione del CO in funzione della T
0,64 0,66 0,68 0,7 0,72 0,74 0,76 0,78 440 450 460 470 480 490 500 510 Temperatura (K) Conv e rs ione Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.9: Andamento della Conversione di equilibrio del CO nel Reattore, in funzione della T (P=25atm, Portata=2570kmol/hr)
Come si può osservare dalla figura 5.5, la Massa Catalitica necessaria per la catalisi della WGSR diminuisce all’aumentare della T perché aumentando la T si favorisce la cinetica del sistema.
Lo stesso andamento non si riscontra per quanto riguarda la conversione del CO (figura 5.5), dove si osserva che all’aumentare della T, questi aumenta fino a raggiungere un valore massimo, per poi diminuire nuovamente; questo si spiega col fatto che nonostante aumenti la cinetica del sistema la reazione di WGSR, essendo moderatamente esotermica risulta sfavorita termodinamicamente.
Risultati dell’analisi di Sensitività al variare della P avendo fissato la Portata (2570 kmol/hr) e la Temperatura del sistema (473K):
CATALIZZATORI per la WGSR a bassa T. Vario la P da 19 a 31 atm:
PRESSIONE MASSA del
CATALIZZATORE
CONVERSIONE del CO nel Reattore
FRAZIONE MOLARE del CO in uscita dal Reattore
Cu/ZnO/Al2O3 P0 = 19 atm P1 = 21 atm P2 = 23 atm P3 = 25 atm P4 = 27 atm P5 = 29 atm P6 = 31 atm M0 = 42,03 kg M1 = 35,69 kg M2 = 30,49 kg M3 = 26,23 kg M4 = 22,72 kg M5 = 19,18 kg M6 = 17,40 kg C0 = 0,732 C1 = 0,745 C2 = 0,754 C3 = 0,760 C4 = 0,763 C5 = 0,766 C6 = 0,767 X0 = 0,105 X1 = 0,099 X2 = 0,096 X3 = 0,094 X4 = 0,092 X5 = 0,091 X6 = 0,091 ← config. migliore ICI-Cu/ZnO/Al2O3 P0 = 19 atm P1 = 21 atm P2 = 23 atm P3 = 25 atm P4 = 27 atm P5 = 29 atm P6 = 31 atm M0 = 13,33 kg M1 = 11,05 kg M2 = 9,28 kg M3 = 7,88 kg M4 = 6,76 kg M5 = 5,87 kg M6 = 5,14 kg C0 = 0,759 C1 = 0,764 C2 = 0,766 C3 = 0,767 C4 = 0,768 C5 = 0,768 C6 = 0,768 X0 = 0,094 X1 = 0,092 X2 = 0,091 X3 = 0,091 X4 = 0,090 X5 = 0,090 X6 = 0,090 ← config. migliore Cu/Al2O3 P0 = 19 atm P1 = 21 atm P2 = 23 atm P3 = 25 atm P4 = 27 atm P5 = 29 atm M0 = 43,74 kg M1 = 37,24 kg M2 = 31,89 kg M3 = 27,48 kg M4 = 23,83 kg M5 = 20,81 kg C0 = 0,728 C1 = 0,742 C2 = 0,752 C3 = 0,758 C4 = 0,762 C5 = 0,765 X0 = 0,106 X1 = 0,101 X2 = 0,097 X3 = 0,094 X4 = 0,093 X5 = 0,092
Per tutti e tre i catalizzatori, nel range di P analizzato, si nota un incremento della conversione all’aumentare della P. Anche in questo caso il catalizzatore ICI-Cu/ZnO/Al2O3 fornisce le
migliori prestazioni, non tanto in termini di conversione, che più o meno si equivalgono, quanto in termini di catalizzatore utilizzato. Si nota, inoltre che per valori della Pressione al di sopra delle 25 atm la conversione di tale catalizzatore resta pressoché immutata.
Dai seguenti grafici (figure 5.7, 5.8 e 5.9), ottenuti implementando su Excel i valori riportati nella tabella 5.6, si può avere un quadro più chiaro dei risultati ottenuti:
Andamento della Massa del Catalizzatore al variare della P
0 5 10 15 20 25 30 35 40 45 50 15 20 25 30 35 Pressione (atm) Massa d e l C a ta lizzato re (kg ) Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.10: Andamento della Massa Catalitica in funzione della P (T=473K, Portata=2570kmol/hr)
Andamento della Conversione del CO al variare della P 0,725 0,73 0,735 0,74 0,745 0,75 0,755 0,76 0,765 0,77 0,775 15 20 25 30 35 Pressione (atm) Conversione Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.11: Andamento della Conversione di equilibrio del CO nel Reattore, in funzione della P (T=473K, Portata=2570kmol/hr)
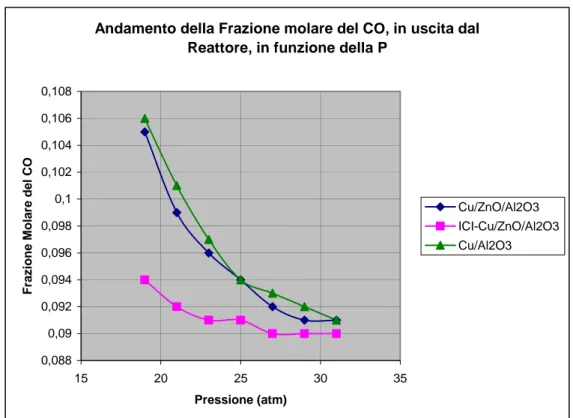
Andamento della Frazione molare del CO, in uscita dal Reattore, in funzione della P
0,088 0,09 0,092 0,094 0,096 0,098 0,1 0,102 0,104 0,106 0,108 15 20 25 30 35 Pressione (atm) Fraz ione M ola re del CO Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.12: Andamento della Frazione Molare del CO, all’equilibrio, in uscita dal Reattore, in funzione della P (T=473K, Portata=2570kmol/hr)
Come si può osservare dalla figura 5.8, la Massa Catalitica necessaria per la catalisi della WGSR diminuisce all’aumentare della P, perché la fase gassosa viene adsorbita più facilmente sulla superficie dei cristalliti di Cu (siti attivi del catalizzatore per la catalisi della WGSR a bassa T) quindi la reazione catalizzata risulta essere maggiormente favorita, e questo lo si può riscontrare anche con l’aumento della conversione del CO all’aumentare della P nel range studiato.Mettiamo nuovamente in evidenza che, per quanto riguarda la configurazione catalitica migliore, cioè quella relativa all’ ICI-Cu/ZnO/Al2O3, la conversione del CO cambia
in maniera impercettibile superando la P di 25 atm. Questo assume un valore importante per quanto riguarderà la scelta della configurazione ottimale, in quanto avendo una corrente in entrata al reattore già a 25 atm possiamo evitare di dover comprimere o espandere tale corrente (ai fini dell’ottimizzazione della resa espressa in termini di conversione del CO) con i relativi risparmi in termini economici e di energia utilizzata.
Risultati dell’analisi di Sensitività al variare della Portata d’Acqua avendo fissato la Pressione (25atm) e la Temperatura del sistema(473K):
Effettuiamo delle prove alimentando al Reattore diverse quantità di Vapore, tenendo fissi tutti gli altri parametri, per vedere qual’è l’effetto dell’aumento della frazione di vapore sulla conversione studiata. Come detto in precedenza, e come risulta anche dalle prove effettuate e riportate di seguito (vedi tabella 5.7 e grafici 5.11, 5.12, e 5.13), un aumento della Portata di Vapore Acqueo facilita una maggiore conversione di equilibrio, riduce la T nel reattore (o il calore generato all’interno del reattore, a seconda che si operi in condizioni adiabatiche o isoterme), aiuta a prevenire la formazione di depositi di carbonio nella zona di ingresso del reattore e permette di minimizzare le reazioni indesiderate competitive con la WGSR, ma un suo uso in quantità troppo elevate può portare alla formazione di condense, che danneggiano il catalizzatore riducendone il potere catalitico, con una conseguente perdita di resa in termini di conversione del CO. Per evitare questo integriamo la portata gassosa, in ingresso al reattore, con una portata di Vapore Acqueo non troppo elevata. Dagli studi riportati in letteratura si è visto che si ottengono buoni risultati in termini di conversione del CO per rapporti H2O/CO circa uguali ad 1 [16].
Nella tabella seguente (tabella 5.7) riportiamo i dati ottenuti variando la portata d’Acqua in ingresso al reattore, mantenendo inalterati gli altri parametri (T=473K, P=25atm).
CATALIZZATORI per la WGSR a bassa T. Vario la portata di H2O
da 500 a 1100kmol/hr: PORTATA d’ACQUA FRAZIONE MOLARE dell’ACQUA in ingresso al Reattore MASSA del CATALIZZATORE CONVERSIONE del CO nel Reattore
FRAZIONE MOLARE del CO in uscita dal Reattore
Cu/ZnO/Al2O3 m0 = 500 kmol/hr m1 = 600 kmol/hr m2 = 700 kmol/hr m3 = 800 kmol/hr m4 = 900 kmol/hr m5 = 1000 kmol/hr m6 = 1100 kmol/hr Xh2o0 = 0,22 Xh2o1 = 0,25 Xh2o2 = 0,28 Xh2o3 = 0,31 Xh2o4 = 0,34 Xh2o5 = 0,36 Xh2o6 = 0,38 M0 = 18,83 kg M1 = 20,76 kg M2 = 23,46 kg M3 = 26,23 kg M4 = 28,45 kg M5 = 29,48 kg M6 = 29,93 kg C0 = 0,493 C1 = 0,571 C2 = 0,665 C3 = 0,760 C4 = 0,846 C5 = 0,889 C6 = 0,922 X0 = 0,223 X1 = 0,184 X2 = 0,137 X3 = 0,094 X4 = 0,057 X5 = 0,040 X6 = 0,027 ← config. migliore ICI-Cu/ZnO/Al2O3 m0 = 500 kmol/hr m1 = 600 kmol/hr m2 = 700 kmol/hr m3 = 800 kmol/hr m4 = 900 kmol/hr m5 = 1000 kmol/hr m6 = 1100 kmol/hr Xh2o0 = 0,22 Xh2o1 = 0,25 Xh2o2 = 0,28 Xh2o3 = 0,31 Xh2o4 = 0,34 Xh2o5 = 0,36 Xh2o6 = 0,38 M0 = 5,34 kg M1 = 6,12 kg M2 = 6,95 kg M3 = 7,88 kg M4 = 8,70 kg M5 = 9,05 kg M6 = 9,14 kg C0 = 0,493 C1 = 0,572 C2 = 0,668 C3 = 0,767 C4 = 0,861 C5 = 0,907 C6 = 0,939 X0 = 0,223 X1 = 0,184 X2 = 0,136 X3 = 0,091 X4 = 0,051 X5 = 0,034 X6 = 0,021 ← config. migliore Cu/Al2O3 m0 = 500 kmol/hr m1 = 600 kmol/hr m2 = 700 kmol/hr m3 = 800 kmol/hr m4 = 900 kmol/hr m5 = 1000 kmol/hr Xh2o0 = 0,22 Xh2o1 = 0,25 Xh2o2 = 0,28 Xh2o3 = 0,31 Xh2o4 = 0,34 Xh2o5 = 0,36 M0 = 12,89 kg M1 = 14,24 kg M2 = 16,18 kg M3 = 18,29 kg M4 = 20,11 kg M5 = 20,90 kg C0 = 0,493 C1 = 0,572 C2 = 0,667 C3 = 0,766 C4 = 0,859 C5 = 0,903 X0 = 0,223 X1 = 0,184 X2 = 0,136 X3 = 0,091 X4 = 0,052 X5 = 0,035
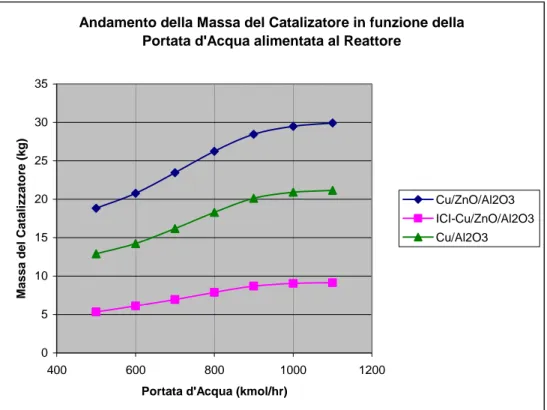
I dati riportati in tabella sono in accordo con quanto detto sopra riguardo i vantaggi apportati dal vapore in termini di una maggiore conversione del CO mediante WGSR. Per avere una visione più chiara si possono consultare i diagrammi riportati qui di seguito (Figure 5.11, 5.12 e 5.13):
Andamento della Massa del Catalizatore in funzione della Portata d'Acqua alimentata al Reattore
0 5 10 15 20 25 30 35 400 600 800 1000 1200
Portata d'Acqua (kmol/hr)
M assa del Catali z z ato re (kg ) Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.13: Andamento della Massa Catalitica in funzione della Portata di Vapore alimentato al Reattore (T=473K, P=25atm)
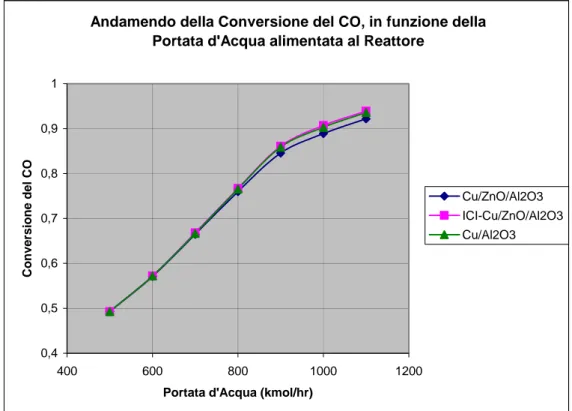
Andamendo della Conversione del CO, in funzione della Portata d'Acqua alimentata al Reattore
0,4 0,5 0,6 0,7 0,8 0,9 1 400 600 800 1000 1200
Portata d'Acqua (kmol/hr)
C onver sione del C O Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Figura 5.14: Andamento della Conversione del CO in funzione della Portata di Vapore alimentato al Reattore (T=473K, P=25atm)
Andamento della Frazione Molare del CO in funzione della Portata d'Acqua alimentata al Reattore
0 0,05 0,1 0,15 0,2 0,25 400 600 800 1000 1200
Portata d'Acqua (kmol/hr)
Fraz ione M o la re del C O Cu/ZnO/Al2O3 ICI-Cu/ZnO/Al2O3 Cu/Al2O3
Anche in questo caso il catalizzatore che meglio risponde alle caratteristiche richieste è l’ICI-Cu/ZnO/Al2O3, dove a fronte della migliore conversione, se pure di poco, impiega una massa
catalitica nettamente inferiore rispetto agli altri due catalizzatori considerati: circa 9kg di catalizzaote ICI-Cu/ZnO/Al2O3 contro i 30kg circa di Cu/ZnO/Al2O3 ed i 21kg del
catalizzatore Cu/Al2O3.
Nella prospettiva di una successiva configurazione ottimale delle condizioni operative a cui far operare tale catalizzatore, si può ipotizzare di utilizzare una quantità stechiometrica di vapore acqueo, in relazione alla portata di CO presente nella corrente da trattare, al fine di evitare i problemi suddetti relativi alla formazione di condense nel Reattore.
5.4 Studi sul catalizzatore (a base di Fe/Cr) per la WGSR condotta
ad alta T
Le condizioni operative a cui operiamo sono:
- T = 673K (400°C) (T intermedia nel range in cui opera il catal. per la WGSR ad alta T)
- P = 25 atm (Pressione alla quale arrivano i gas dai trattamenti precedenti) - Portata di gas = 2570 kmol/hr (Portata gassosa in arrivo dai trattamenti
precedenti)
Per la valutazione della costante di equilibrio termodinamico della reazione, faremo uso della relazione fornita da Moe [68]:
Keq e
4577.8 K⋅ T1 −4.33
:=
Per quanto riguarda la cinetica di reazione useremo la seguente equazione empirica che esprime la velocità di scomparsa del CO in funzione: della costante di equilibrio, della costante cinetica e della composizione della portata gassosa, espressa in termini di Pressione parziale [68].
(Frazione Molare dell’elemento i-esimo di una miscela gassosa = pressione parziale dell’elemento i-esimo (Pi) diviso la Pressione tot del sistema: xi = Pi/P):
rco k Pco Ph2o⋅ Pco2 Ph2⋅
Keq − ⎛⎜
⎝ ⎞⎟⎠
in funzione della costante cinetica k per la WGSR: k ko e E − R1 T1⋅ ⋅ := con
k0 Fattore preesponenziale della costante di velocità
E Energia di Attivazione
R1 Costante dei gas (8,314 J/mol K nell’ipotesi di gas ideali) T1 Temperatura assoluta (K)
Catalizzatore (a base di Fe/Cr) studiato:
1) Fe
2O
3/Cr
2O
3Le proprietà di questo catalizzatore sono state reperite dagli articoli [71, 72, 73]
- k0 = 109,098*103
- E = 112*103 J/mol - Porosità = 0,6 - Densità = 210 Kg/m3
- v0 = 2 m/s (velocità del gas in ingresso al reattore)
- Composizione = 92% Fe2O3, 8% Cr2O3 (% in peso)
Implementando le relative formule su Mathcad otteniamo l’andamento della composizione del CO nel tempo, all’interno del reattore (figura 5.14):
0 20 40 60 80 100 0 0.1 0.2 0.3 0.4 tempo (sec)
Frazione Molare del CO nel Reattore
0.5 0 Xco t( ) 100 0 t Xco,i t* Conversione effettiva del CO nel reattore
Xco,o
Xco,eq
Figura 5.16: Andamento della frazione molare del CO, nel tempo, all’interno del Reattore (Reattore singolo: T=673K, P=25atm, Portata=2570kmol/hr)
Come si vede dalla figura 5.14, all’Equilibrio Termodinamico, si ottiene:
• Frazione Molare del CO = 0,158; superiore rispetto a quella ottenuta con i catalizzatori per la WGSR a bassa T, in quanto operando ad elevate T si sfavorisce la termodinamica della reazione ottenendo, così, una più bassa conversione di equilibrio. • Conversione del CO = 59,4%
• Tempo necessario per raggiungere l’Equilibrio TD = 98 sec
Ipotizzando all’interno del reattore una Conversione del CO del 60%, rispetto alla conversione teorica di equilibrio, si ottengono i seguenti valori:
• Frazione Molare del CO = 0,251
• Tempo di Residenza del gas (t*) = 16 sec • Conversione Effettiva = 0,356 (35,6%)
A questo punto tramite la seguente equazione integrale:
Mcat mi Xcoi Xcof Xco 1 rco − ⎛⎜ ⎝ ⎞⎟⎠ ⌠ ⎮ ⎮ ⌡ d ⎡ ⎢ ⎢ ⎣ ⎤ ⎥ ⎥ ⎦ ⋅ :=
con
Xcof = frazione molare del CO in uscita al reattore (con conversione al 60% di quella di
equilibrio)
Xcoi = frazione molare del CO in ingresso al reattore
siamo in grado di ricavare la massa del catalizzatore necessaria affinché, per mezzo della WGSR, avvenga nel reattore, la Conversione Effettiva ipotizzata:
• Massa Catalitica = 38,5 kg • Diametro del Reattore = 1 m • Lunghezza del Reattore = 3,3 m
(Per l’esecuzione dei calcoli vedi Appendice D).
5.4.1 Analisi di Sensitività sul Catal. a base di Fe/Cr per la WGSR ad alta T
Effettuiamo delle Analisi di Sensitività sui catalizzatori studiati al fine di ricavare:
• Massa del Catalizzatore affinché si realizzi, nel reattore, la Conversione Effettiva • Conversione di Equilibrio del CO nel Reattore
• Frazione Molare del CO in uscita dal Reattore, all’Equilibrio
al variare, nel reattore, di:
• Temperatura • Pressione
• Quantità di Vapore Acqueo in ingresso
fissando di volta in volta gli altri parametri. Lo scopo di quest’analisi è quello di ricavare la configurazione ottimale a cui possono operare i singoli Reattori Catalitici.
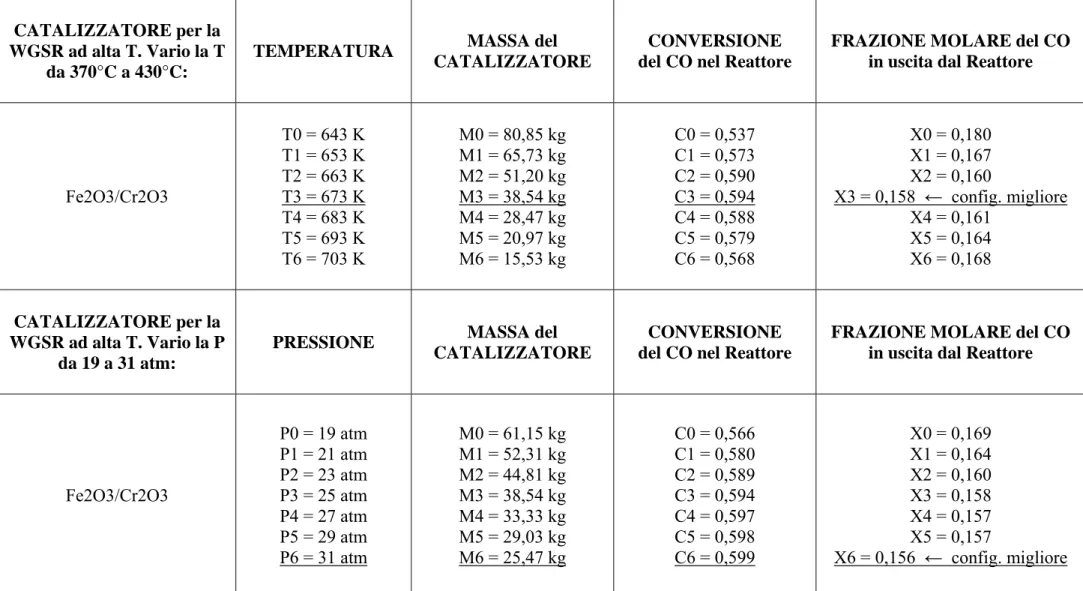
CATALIZZATORE per la WGSR ad alta T. Vario la T
da 370°C a 430°C:
TEMPERATURA MASSA del
CATALIZZATORE
CONVERSIONE del CO nel Reattore
FRAZIONE MOLARE del CO in uscita dal Reattore
Fe2O3/Cr2O3 T0 = 643 K T1 = 653 K T2 = 663 K T3 = 673 K T4 = 683 K T5 = 693 K T6 = 703 K M0 = 80,85 kg M1 = 65,73 kg M2 = 51,20 kg M3 = 38,54 kg M4 = 28,47 kg M5 = 20,97 kg M6 = 15,53 kg C0 = 0,537 C1 = 0,573 C2 = 0,590 C3 = 0,594 C4 = 0,588 C5 = 0,579 C6 = 0,568 X0 = 0,180 X1 = 0,167 X2 = 0,160 X3 = 0,158 ← config. migliore X4 = 0,161 X5 = 0,164 X6 = 0,168 CATALIZZATORE per la WGSR ad alta T. Vario la P da 19 a 31 atm:
PRESSIONE MASSA del
CATALIZZATORE
CONVERSIONE del CO nel Reattore
FRAZIONE MOLARE del CO in uscita dal Reattore
Fe2O3/Cr2O3 P0 = 19 atm P1 = 21 atm P2 = 23 atm P3 = 25 atm P4 = 27 atm P5 = 29 atm P6 = 31 atm M0 = 61,15 kg M1 = 52,31 kg M2 = 44,81 kg M3 = 38,54 kg M4 = 33,33 kg M5 = 29,03 kg M6 = 25,47 kg C0 = 0,566 C1 = 0,580 C2 = 0,589 C3 = 0,594 C4 = 0,597 C5 = 0,598 C6 = 0,599 X0 = 0,169 X1 = 0,164 X2 = 0,160 X3 = 0,158 X4 = 0,157 X5 = 0,157 X6 = 0,156 ← config. migliore Tabella 5.8: Risultati dell’Analisi di Sensitività al variare della T mantenendo costanti gli altri parametri (P=25atm, Portata di
Acqua=2570kmol/hr)
Tabella 5.9: Risultati dell’Analisi di Sensitività al variare della P mantenendo costanti gli altri parametri (T=673K, Portata di Acqua=2570kmol/hr)
Nelle tabelle 5.8 e 5.9 sono riportati rispettivamente i:
1) Risultati dell’analisi di Sensitività al variare della T avendo fissato la Portata (2570 kmol/hr) e la Pressione del sistema(25 atm):
Andamento dalla Massa del Catalizzatore in funzione della T
0 10 20 30 40 50 60 70 80 90 640 650 660 670 680 690 700 710 Temperatura (K) M assa del C a taliz z a to re ( k g) Fe2O3/Cr2O3
Andamento della Conversione del CO nel Reattore e Frazione Molare del CO in uscita dal Reatore in funzione della T.
Catalizzatore Fe2O3/Cr2O3 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 630 650 670 690 710 Temperatura (K)
Conversione del CO nel Reattore
Frazione Molare del CO in uscita dal Reattore
Figura 5.18: Andamento della conversione e della frazione molare del CO in funzione della T (con P e Portata fissate)
Si osserva un massimo della resa, in termini di Conversione del CO, all’interno del reattore, alla T di 673K, alla quale corrispondono;
• Frazione Molare del CO = 0,158 • Conversione all’Equilibrio = 0,594
• Massa Catalitica affinché avvenga la Conversione Effettiva = 38,54 kg.
2) Risultati dell’analisi di Sensitività al variare della P avendo fissato la Portata (2570 kmol/hr) e la Temperatura del sistema (673K):
Andamento della Massa del Catalizzatore in funzione della P 0 10 20 30 40 50 60 70 15 20 25 30 35 Pressione (atm) Ma s s a de l C a ta lizza to re ( k g) Fe2O3/Cr2O3
Figura 5.19: Andamento della Massa Catalitica in funzione della P (con T e Portata fissate)
Andamento della Conversione del CO nel Reattore e della Frazione Molare del CO in uscita dal Reattore.
Catalizzatore Fe2O3/Cr2O3 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 15 20 25 30 35 Pressione (atm)
Conversione del CO nel Reattore
Frazione Molare del CO in uscita dal Reattore
Figura 5.20: Andamento della Conversione e della Frazione Molare del CO (con T e Portata fissate)
uscita varia in maniera poco significativa, quindi resta conveniente operare alla Pressione di 25 atm alla quale arrivano i gas dalle lavorazioni precedenti, perché un’ulteriore compressione della corrente gassosa, con i relativi costi in termini economici ed energetici, porterebbe a risultati più o meno simili ed i guadagni in termini di una minore massa catalitica non sarebbero sufficienti a bilanciare tali costi.
3) Risultati dell’analisi di Sensitività al variare della Portata d’Acqua avendo fissato la Pressione (25atm) e la Temperatura del sistema (673K):
CATALIZZATORE per la WGSR ad alta T. Vario la portata di H2O da 500 a 1100 kmol/hr: PORTATA d’ACQUA FRAZIONE MOLARE dell’ACQUA in ingresso al Reattore MASSA del CATALIZZATORE CONVERSIONE del CO nel Reattore
FRAZIONE MOLARE del CO in
uscita dal Reattore
Fe2O3/Cr2O3 m0 = 500 kmol/hr m1 = 600 kmol/hr m2 = 700 kmol/hr m3 = 800 kmol/hr m4 = 900 kmol/hr m5 = 1000 kmol/hr m6 = 1100 kmol/hr Xh2o0 = 0,22 Xh2o1 = 0,25 Xh2o2 = 0,28 Xh2o3 = 0,31 Xh2o4 = 0,34 Xh2o5 = 0,36 Xh2o6 = 0,38 M0 = 32,23 kg M1 = 34,22 kg M2 = 36,50 kg M3 = 38,54 kg M4 = 40,27 kg M5 = 41,56 kg M6 = 42,68 kg C0 = 0,412 C1 = 0,417 C2 = 0,533 C3 = 0,594 C4 = 0,652 C5 = 0,685 C6 = 0,716 X0 = 0,259 X1 = 0,228 X2 = 0,191 X3 = 0,158 X4 = 0,129 X5 = 0,113 X6 = 0,099 ← config. migliore
Tabella 5.10: Risultati dell’Analisi di Sensitività al variare della Portata di Vapore Acqueo, mantenendo costanti gli altri parametri (T=673K, P=25atm)
Andamento della Massa del Catalizzatore in funzione della Portata d'Acqua 30 32 34 36 38 40 42 44 400 600 800 1000 1200
Portata d'Acqua (kmol/hr)
M assa del C a ta liz z a to re ( k g) Fe2O3/Cr2O3
Figura 5.21: Andamento della Massa Catalitica in funzione della Portata di Vapore (con T e P fissati)
Andamento della Conversione del CO, e della Frazione Molare del CO in uscita dal Reattore, in funzione della Portata d'Acqua.
Catalizzatore Fe2O3/Cr2O3 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 400 600 800 1000 1200
Portata d'Acqua (kmol/hr)
Conversione del CO nel Reattore
Frazione Molare del CO in uscita dal Reattore
Figura 5.22: Andamento della Conversione e della Frazione Molare del CO al variare della Portata di Vapore (con T e P fissati)
Come già osservato nel caso dei catalizzatori di Shift operanti a bassa T anche in questo caso la conversione del CO aumenta all’aumentare della quantità di vapore alimentato al Reattore, ma essendo anche i catalizzatori a base di Fe/Cr suscettibili alla diminuzione di attività dovuta alla formazione di condense, anche in questo caso si può pensare di operare con una quantità di vapore stechiometrico in funzione della quantità di CO entrante nel reattore.
5.5 Configurazione dei due reattori in serie
Sulla base dei risultati ottenuti dalle Analisi di Sensitività siamo adesso in grado di fornire una soluzione impiantistica più dettagliata di quello che sarà il modello scelto per l’ottimizzazione della produzione di Idrogeno in termini di conversione del CO.
Abbiamo scelto di operare con due reattori in serie perché, come già detto precedentemente, così facendo si riesce ad ottimizzare sia la cinetica che la conversione di equilibrio della WGSR e perché operando con un primo reattore ad alta T possiamo sfruttare la corrente gassosa, ad elevata T, proveniente dai precedenti trattamenti del syngas, senza, quindi, dover effettuare un raffreddamento della corrente stessa.
Alla portata di syngas proveniente dai trattamenti precedenti abbiamo scelto di aggiungere 200 kmol/hr di vapore per avere un rapporto CO/H2O = 1 che mi garantisce un miglior
rendimento in termini di conversione del CO, limitando i problemi derivanti da un’eventuale condensa del vapore.
Nella figura seguente riportiamo una schematizzazione dei due reattori tubolari cilindrici (Plug Flow Reactor) catalitici operanti in serie:
heat
recovery
REACTOR
LOW T
HIGH T
REACTOR
Steam
1° Reattore: per la WGSR ad alta T.
Catalizzatore Fe
2O
3/Cr
2O
3:
Le condizioni operative a cui andremo ad operare nel primo Reattore sono quelle ottimali ricavate dalle Analisi di Sensitività condotte in precedenza sul Catalizzatore Fe2O3/Cr2O3:
• P = 25 atm • T = 673 K
• Portata Syngas = 2770 kmol/hr
Per quanto riguarda i calcoli svolti, abbiamo usato le stesse equazioni utilizzate nella precedente Analisi di Sensitività effettuata sul singolo Reattore con Catalizzatore a base di Fe2O3/Cr2O3.
Dai dati della tabella 5.4 relativi alla composizione del syngas in arrivo dai trattamenti
precedenti e con l’aggiunta di 200 kmol/hr di Vapore Acqueo, possiamo ricavare i dati relativi alla composizione in ingresso al primo reattore di Shift, dati che riportiamo per comodità nella seguente tabella:
Composizione del Syngas
Portata
(kmol/hr) Frazione Molare
CO 1000 0,36 H2O 1000 0,36 H2 600 0,22 CO2 170 0,06 CH4 (tracce) 0 H2S (tracce) 0
Portata tot (kmol/hr) 2770 -
Tabella 5.11: Composizione del Syngas in entrata al primo Reattore di Shift
Implementando le suddette formule su Mathcad, si ottiene l’andamento della composizione del CO nel tempo, all’interno del reattore (figura 5.22):
0 20 40 60 80 100 0 0.1 0.2 0.3 0.4 tempo (sec)
Frazione Molare del CO nel Reattore
0.5 0 Xco t( ) 100 0 t Xco,i t* Conversione effettiva del CO nel reattore
Xco,o
Xco,eq
Figura 5.24: Andamento della Frazione Molare del CO, nel tempo, all’interno del Reattore
Come si vede dalla figura 5.22, all’Equilibrio Termodinamico, si ottengono i seguenti valori:
• Frazione Molare del CO = 0,113
• Conversione del CO = 0,685 (68,5%)
• Tempo necessario per raggiungere l’equilibrio TD = 99 sec
Ipotizzando all’interno del reattore una Conversione Effettiva dell’ 80%, rispetto alla conversione teorica di equilibrio, si ottengono i seguenti valori:
• Frazione Molare del CO = 0,163 • Conversione del CO = 0,548 (54,8%) • Massa Catalitica = 79 kg
• Diametro Reattore = 1 m • Lunghezza Reattore = 6,2 m
• Tempo di Residenza del Gas (t*) = 36 sec
Nella WGSR una mole di CO reagisce con una mole di H2O per dare una mole di H2 ed una
mole di CO2, da questo seguono i bilanci di materia sul primo reattore (tenendo conto che la
portata gassosa totale rimane invariata):
• 1) moli di CO reagite = moli di CO iniziali * Conversione • 2) moli di CO = moli di CO entrate - moli di CO reagite • 3) moli di H2O = moli di H2O entrate - moli di CO reagite
• 4) moli di H2 = moli di H2 entrate + moli di CO reagite
• 5) moli di CO2 = moli di CO2 + moli di CO reagite
Riportiamo i dati ricavati dalle precedenti equazioni nella seguente tabella:
Composizione del Syngas
Portata
(kmol/hr) Frazione Molare
CO 450 0,16 H2O 450 0,16 H2 1150 0,42 CO2 720 0,26 CH4 (tracce) 0 H2S (tracce) 0
Portata tot (kmol/hr) 2770 -
Tabella 5.12: Composizione del Syngas in uscita dal primo Reattore di Shift
2° Reattore: per la WGSR a bassa T.
Catalizzatore ICI-Cu/ZnO/Al
2O
3:
Le condizioni operative a cui andremo ad operare nel secondo Reattore sono quelle ricavate dalle Analisi di Sensitività condotte in precedenza sul Catalizzatore ICI-Cu/ZnO/Al2O3:
• P = 25 atm • T = 473 K