4. Risultati
In questo studio la possibile riattivazione del Polyomavirus JCV, durante il trattamento con i mAbs, è stata valutata esaminando la presenza di JCV nel sangue e nelle urine di pazienti affetti da diverse patologie immuno-mediate e da sclerosi multipla recidivante remittente (RRSM), sottoposti a terapia farmacologica rispettivamente con i mAbs infliximab e natalizumab.
4.1 Caratteristiche dei pazienti trattati con infliximab
I pazienti arruolati, le cui principali caratteristiche sono sintetizzate nella tabella 4.1, sono stati divisi in tre gruppi.
a
Le patologie immunomediate dei pazienti esaminati includono: artrite reumatoide, vasculiti sistemiche, spondiloartropatie sieronegative.
b
Farmaci immunomodulanti somministrati insieme o no al mAb: P, Prednisone; PM, 6-metilprednisolone; MTX, Metotrexato.
Il gruppo 1 comprende 40 pazienti affetti da diverse patologie immuno-mediate (artrite reumatoide (AR), varie forme di vasculiti, spondiloartropatie) trattati, ogni due mesi, con una somministrazione endovenosa di 3-5 mg/kg del mAb. Tali pazienti, sulla base
del numero di infusioni di mAb ricevute al momento dell’arruolamento, sono stati ulteriormente suddivisi in cinque sottogruppi; le dosi di mAb somministrate vanno da 1 a 51 (media di 20 dosi). La maggior parte dei pazienti in esame, ha ricevuto in associazione ad infliximab, dosi giornaliere di steroidi e farmaci immunosoppressivi, generalmente utilizzati in clinica per la cura di tali patologie. In particolare sono stati loro somministrati: prednisone (9,3 ± 2,9 mg) o 6-metilprednisolone (8 ± 2,7 mg) e metotrexato (10,7 ± 0,5 mg). Tutti i pazienti trattati con il mAb non hanno manifestato reazioni avverse al trattamento e sono risultati tutti buoni responders alla terapia. Il gruppo 2 è costituito da 21 pazienti controllo malattia, non trattati quindi con il mAb ma con dosi giornaliere di prednisone (10 ± 0,7 mg) o 6-methylprednisolone (10,9 ± 1,3 mg); infine, il gruppo 3, comprende 20 controlli sani. L’età e il sesso sono equamente distribuiti tra i tre gruppi di pazienti analizzati.
4.2 Ricerca di JCV nel sangue e nell’urina dei pazienti trattati con
infliximab
La presenza di JCV nel sangue e nell’urina dei tre gruppi di pazienti, è stata valutata, come descritto nel capitolo dei Materiali e metodi, mediante un saggio, altamente specifico e sensibile, di PCR real-time quantitativa. Come è riportato in tabella 4.2, per quanto riguarda la viremia, come prima cosa si nota che all’interno del gruppo 1 (pazienti trattati con infliximab) è stata osserva una maggiore positività a JCV nei PBMC piuttosto che nel plasma. Inoltre, si osserva che 12 dei 40 pazienti di tale gruppo sono risultati positivi al virus nei PBMC, mostrando una maggiore prevalenza (30%) sia rispetto a quella osservata nei pazienti del gruppo 2, non trattati con il mAb (9%), sia rispetto a quella del gruppo 3 dei controlli sani (5%). Una differenza statisticamente significativa è stata riscontrata solo tra i pazienti del gruppo 1 e del gruppo 3 (÷2 p < 0.05). Sono invece risultati positivi nel plasma solo 5 dei 40 pazienti del gruppo 1 (12%) e 1 dei 20 del gruppo 3 (5%). Inoltre, solo 4 dei 5 pazienti del gruppo 1, risultati positivi nel plasma, lo erano anche nei PBMC separati dal sangue intero dello stesso prelievo. Tuttavia, nel complesso non sono state osservate differenze significative relativamente alla carica virale dei tre gruppi che è risultata bassa sia nei PBMC che nel plasma di tutti i pazienti analizzati (Tabella 4.2). Viceversa, elevati valori di viruria sono stati riscontrati in tutti i gruppi: una prevalenza del 72%, 28% e 55% è stata osservata rispettivamente nei gruppi 1, 2 e 3, con una differenza statisticamente significativa tra il gruppo 1 dei pazienti trattati e il gruppo 2 dei pazienti non trattati con
infliximab (÷2 p < 0.01). Le prevalenze del gruppo 3 osservate sia nel sangue (5%) che nell’urina (55%), sono in linea con quanto riportato in letteratura; anche i valori della carica virale osservati nelle urine, maggiori di quelli riscontrati sia nei PMBC che nel plasma, confermano quanto è descritto in altri studi.
a
Carica virale di JCV espressa come media del numero di copie ottenuta nei campioni positivi di ciascun gruppo. In parentesi, è riportato il range del numero di copie.
b
Nd: non disponibile.
La più alta positività che si osserva nelle urine di tutti i gruppi, associata ad un maggiore numero di copie di virus (in media 106 copie/ml), probabilmente è da attribuire ad una maggiore replicazione di JCV nel rene (uno dei suoi principali siti di latenza). Negli adulti infatti,come i pazienti da noi studiati, con età media di 40 anni, è comune osservare una maggiore escrezione urinaria asintomatica del virus. Una transiente viruria di JCV sembra infatti aumentare linearmente con l’età. Infine, è importante
sottolineare come una positività costante è stata osservata solo nei campioni ripetuti di urina dei pazienti del gruppo 1 e 2, e non in quelli di PBMC e plasma (dati non mostrati), evidenziando come la replicazione di JCV possa essere difficile da monitorare nel sangue, distretto cellulare dove il virus generalmente si replica raramente e a bassi livelli in pazienti immunocompromessi non PML. Inoltre, in base a quanto osservato, la presenza variabile di JCV, riscontrata a livello dei PBMC, del plasma e dell’urina dei pazienti analizzati, non sembra correlare in maniera significativa con il numero di dosi del trattamento.
4.3 Sequenziamento della regione di controllo trascrizionale NCCR
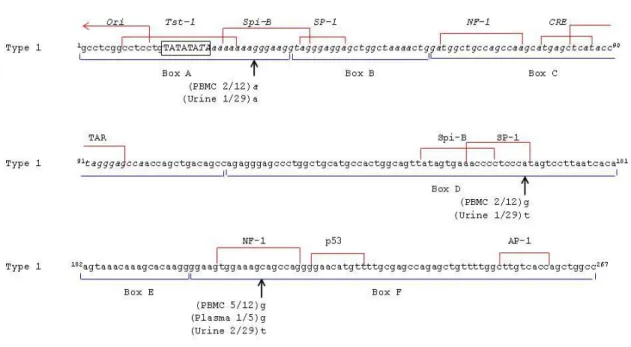
La possibile riattivazione virale nei pazienti risultati positivi a JCV trattati con il mAb, è stata successivamente valutata, studiando l’eventuale evoluzione molecolare della regione genomica virale NCCR. A tale scopo, la NCCR di JCV dei suddetti pazienti è stata sequenziata e confrontata con la struttura della NCCR archetipo non patogenetica osservata negli isolati virali appartenenti al genotipo 1. Il genotipo 1 infatti, risulta essere sulla base del sequenziamento della proteina VP1 (40), il genotipo di JCV più frequentemente diffuso anche tra i pazienti qui esaminati. L’analisi della sequenza ha evidenziato una struttura NCCR archetipo in tutti i pazienti positivi analizzati (Figura 4.1). Tuttavia, nei pazienti trattati con il mAb (gruppo 1) è stata identificata qualche mutazione puntiforme in siti di legame per alcuni fattori cellulari di trascrizione aventi un sito di legame sulla NCCR, insieme anche a qualche mismatches, non importante da un punto di vista patogenetico (non mostrati in figura). Le mutazioni osservate, sono state individuate nel sito di legame per il fattore di trascrizione cellulare Spi-B (mutazione G30A), SP-1 (mutazione A166G/T) e NF-1 (mutazione C211G/T). In particolare, tutte e tre le mutazioni sono state contemporaneamente individuate in 2 delle 12 sequenze NCCR analizzate e ottenute dai PBMC dei pazienti analizzati e solo in 1 delle 29 ottenute dalle urine. La mutazione nel sito di legame per il fattore NF-1 è stata quella più frequentemente osservata. E’ stata infatti identificata in 5 delle 12 sequenze ottenute dai PMBC, in 1 delle 5 sequenze ottenute dal plasma e in 2 delle 29 ottenute dalle urine. E’ importante sottolineare come le stesse mutazioni individuate nelle NCCR sequenziate dai campioni di PBMC e urina, derivino dallo stesso paziente. Il clonaggio di alcune delle suddette sequenze ha confermato la presenza delle mutazioni descritte anche in singoli cloni molecolari della NCCR (dati non mostrati). Sebbene le mutazioni da noi individuate siano localizzate principalmente in siti di
legame per fattori di trascrizione cellulare, descritti come specifici regolatori linfoidi dell’espressione genica di JCV (119), nessuno di tali cambiamenti nucleotidici è stato precedentemente osservato nella NCCR del ceppo Mad-1 o di altri ceppi PML-type, associati all’insorgenza della malattia, presenti nel database di tutte le sequenze NCCR di JCV ad oggi identificate ed analizzate.
Figura 4.1. Sequenza della NCCR con in evidenza le mutazioni individuate nei campioni esaminati. Le differenze nucleotidiche osservate nei campioni analizzati rispetto alla sequenza consenso di JCV di genotipo 1 sono indicate dalla freccia sotto la sequenza. Il numero di campioni in cui sono stati osservati i cambiamenti nei PBMC, plasma e urina sono indicati in parentesi. Ori, origine di replicazione. Tata box è indicata nel riquadro. Sopra le sequenze sono indicate le regioni di legame per gli specifici fattori di trascrizione. Sotto la sequenza sono indicate le regioni A-F in cui è suddivisa la regione NCCR.
4.4 Effetti del trattamento anti-TNFá sulla persistenza virale
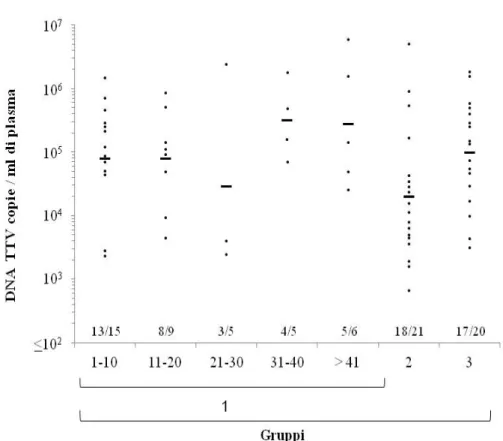
Successivamente per capire se la diversa prevalenza di JCV, osservata nei campioni di sangue dei tre gruppi di pazienti analizzati, potesse essere legata agli effetti immunomodulanti indotti dal trattamento anti-TNFá, abbiamo studiato la carica virale del Torquetenovirus (TTV), virus persistente diffuso in più dell’80% della popolazione. Come riportato in figura 4.2, la presenza di TTV, in generale, non sembra differire tra i
gruppi di pazienti esaminati: la prevalenza appare abbastanza alta sia tra i pazienti trattati con il mAb (gruppo 1) che tra quelli non trattati (gruppo 2) e i controlli sani (gruppo 3), con un range dell’82-86%. Tuttavia, è stata osservata una correlazione positiva tra la carica virale plasmatica di TTV e il numero di infusioni di mAb ricevute dai pazienti del gruppo 1 (Spearman’s Rho di 0,299, p < 0.05).
Figura 4.2 Ricerca di TTV nel plasma dei pazienti studiati. In figura è riportata la carica plasmatica di TTV dei tre gruppi di pazienti analizzati. La barra orizzontale rappresenta la media dei valori della carica virale. Il numero di pazienti positivi a TTV è indicato in rapporto al numero totale di pazienti analizzati.
4.5 Effetti del trattamento anti-TNFá sull’espressione di miRNAs
cellulari
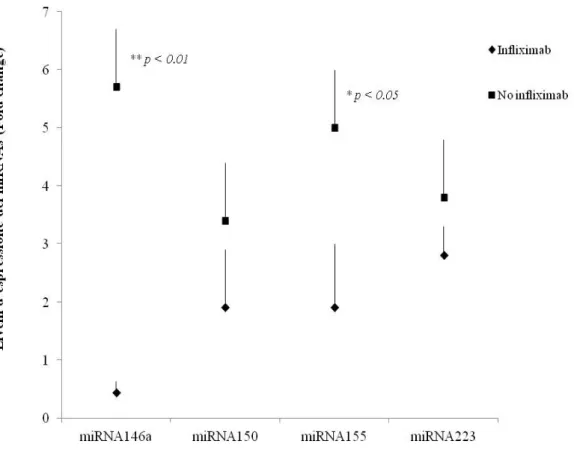
Nel tentativo di indagare gli eventuali fattori cellulari coinvolti nell’evoluzione molecolare di JCV è stato valutato l’effetto del trattamento anti-TNFá sull’espressione di alcuni miRNAs cellulari. In particolare, come è riportato in figura 4.3, a tale scopo sono stati selezionati quattro miRNAs: il miR-146a, miR-150, miR-155 e miR-223. In figura, sono riportati i livelli d’espressione dei quattro miRNAs, espressi come incremento del valore d’espressione osservato nei pazienti affetti da patologie
immuno-mediate trattati e non trattati con infliximab rispetto ai controlli sani. In generale è evidente una over-espressione dei miRNAs analizzati nei pazienti malati rispetto ai controlli sani. Tuttavia tutti i pazienti trattati con il mAb mostrano livelli d’espressione dei miRNAs più bassi rispetto a quelli ottenuti nei pazienti non trattati, con valori statisticamente significativi soprattutto per il miR-146a e il miR-155. In particolare, i livelli d’espressione del miR-146a sono stati costantemente rilevati più bassi rispetto a quelli dei controlli sani (p<0.01). Al contrario, i livelli d’espressione dei miR-150, -155 e -223 sono rimasti fino a 2,5 log superiori a quelli osservati nei controlli sani.
Figura 4.3 Livelli d’espressione dei miRNAs cellulari. I valori riportati sono espressi come incremento del valore d’espressione dei relativi miRNAs osservato nei pazienti con patologie immuno-mediate trattati o no con infliximab rispetto a quelli ottenuti nei controlli sani. I valori mostrati in figura sono le medie + la deviazione standard di tre prove sperimentali indipendenti. Gli asterischi indicano i livelli d’espressione significativi (test t di Student: p<0.01 (**) e p< 0.05 (*)) ottenuti rispettivamente per il miR-146a e miR-155 nei pazienti trattati con il mAb rispetto ai pazienti non trattati.
4.6 Caratteristiche dei pazienti trattati con natalizumab
Nella seconda parte dello studio, siamo andati ad analizzare l’effetto del trattamento con natalizumab sulla riattivazione di JCV. I pazienti trattati con natalizumab, le cui
principali caratteristiche sono riassunte nella tabella 4.3, sono stati divisi in due gruppi sulla base del numero di infusioni di mAb ricevute.
Il gruppo 4 comprende 26 pazienti affetti da sclerosi multipla recidivante remittente (RRSM), trattati con il mAb natalizumab, in cui è risultato fallimentare il trattamento di prima linea generalmente utilizzato in questa tipologia di pazienti, che prevede la somministrazione di IFNâ-1a, glatiramer acetato e aziatropina. I 26 pazienti arruolati hanno ricevuto un’infusione endovenosa mensile di 300 mg/kg del mAb, somministrato, a differenza di infliximab, come monoterapia. I pazienti hanno ricevuto un numero variabile di dosi che va da un minimo di 1 ad un massimo di 32 (media di 10 dosi), in base alle quali sono stati ulteriormente suddivisi in 3 sottogruppi. Il gruppo 5 rappresenta il gruppo controllo malattia: si tratta infatti di un gruppo di 13 pazienti per cosi dire naive, che non hanno ricevuto nemmeno una somministrazione mensile di mAb. Insieme al gruppo 4 e 5, in tabella è riportato lo stesso gruppo 3, dei 20 controlli sani, studiato come riferimento nella valutazione della riattivazione virale nel trattamento con infliximab. Anche in questo caso, l’età è distribuita equamente tra i tre
gruppi; si osserva invece, un maggior numero di pazienti donne: la SM è infatti una patologia che colpisce prevalentemente il sesso femminile.
4.7 Ricerca di JCV nel sangue e nell’urina dei pazienti trattati con
natalizumab
I valori di viremia e viruria di JCV nei pazienti trattati con natalizumab (gruppo 4), come riportato in tabella 4.4, in generale, non differiscono molto da quelli osservati nei pazienti trattati con infliximab (gruppo 1). Anche nei pazienti del gruppo 4, infatti, così come in quelli del gruppo 1, è stata rilevata una maggiore positività al virus nei PBMC piuttosto che nel plasma. Si osserva una maggiore prevalenza nei PBMC del gruppo 4 (35%) sia rispetto al gruppo 5 (15%) che rispetto ai controlli sani del gruppo 3 (5%).
a
Carica virale di JCV espressa come media del numero di copie ottenuta nei campioni positivi di ciascun gruppo. In parentesi, è riportato il range del numero di copie.
b
Nd, non disponibile.
Tra i pazienti trattati con natalizumab, suddividi in tre gruppi in base al numero di infusioni ricevute, il numero di positivi a JCV nel sangue (PBMC e plasma) sembra aumentare in relazione al numero di dosi di mAb somministrate; tuttavia, solo pochi pazienti risultano positivi contemporaneamente nei PBMC e nel plasma. La carica virale
invece, rimane moderatamente bassa tra i gruppi analizzati (102 copie/ml in media): non sono state osservate differenze significative nè tra i tre gruppi né all’interno dei sottogruppi del gruppo 4. La carica virale infatti non sembra aumentare in relazione al numero di infusioni ricevute. Il contrario si osserva invece, nella viruria: nonostante la carica virale anche in questo caso si mantenga relativamente bassa, rispetto a quella analizzata nei pazienti trattati con infliximab, si osserva una differenza significativa nella prevalenza di JCV nell’urina dei pazienti studiati. La positività al virus aumenta all’aumentare del numero di dosi di mAb: si passa da un 28% dei pazienti che hanno ricevuto da 1 a 20 dosi a un 60% dei pazienti che ne hanno ricevuto un massimo di 32. Tuttavia, pochi sono i pazienti che risultano positivi contemporaneamente in tutti e tre i distretti cellulari esaminati. Infine, anche per natalizumab, come precedentemente descritto per infliximab, una positività costante in differenti prelievi fatti da uno stesso paziente a tempi di infusione successive è stata osservata solo nei campioni di urina e non in quelli di PBMC e plasma (dati non mostrati).
4.8 Sequenziamento della regione di controllo trascrizionale NCCR
Il sequenziamento della regione NCCR dei pazienti del gruppo 4 risultati positivi al virus ha evidenziato, in tutte le sequenze analizzate, una struttura archetipo della NCCR (dati non mostrati).
4.9 Effetti del trattamento con il mAb sulla persistenza virale
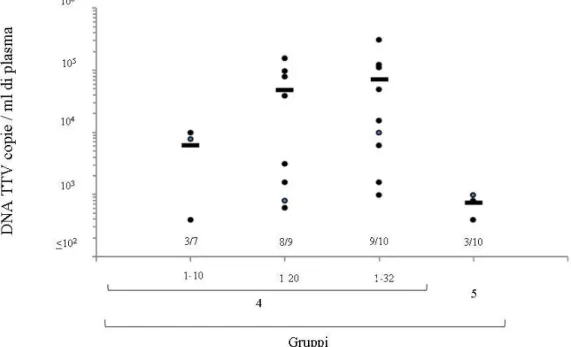
Gli effetti esercitati dal trattamento con natalizumab sulla persistenza di JCV sono stati valutati, così come per infliximab, esaminando la viremia plasmatica di TTV come indice di funzionalità immunitaria. Come riportato in figura 4.4, la prevalenza di TTV, in generale, non sembra variare tra il gruppo dei pazienti trattati con il mAb e quello dei pazienti non trattati, in linea con quanto osservato nei pazienti trattati con infliximab. Tuttavia esiste anche tra i pazienti trattati con natalizumab, così come in quelli trattati con infliximab, una correlazione positiva tra i livelli di viremia plasmatica di TTV e il numero di infusioni di mAb ricevute dai pazienti affetti da RRSM (Spearman’s Rho di 0,267, p < 0.05).
Figura 4.4 Ricerca di TTV nel plasma dei pazienti studiati. In figura è riportata la carica plasmatica di TTV dei due gruppi di pazienti analizzati. La barra orizzontale rappresenta la media dei valori della carica virale. Il numero di pazienti positivi a TTV è indicato in rapporto al numero totale di pazienti analizzati.
4.10 Effetti del trattamento con natalizumab sull’espressione di
miRNAs cellulari
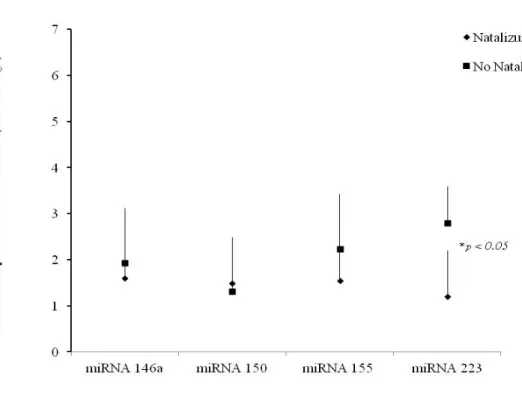
Il trattamento con natalizumab, a differenza di quanto osservato nei pazienti trattati con infliximab, sembra avere solo in parte un minimo effetto sui livelli d’espressione dei quattro miRNAs selezionati. Come infatti si evince dalla figura 4.5, i pazienti trattati con il mAb mostrano livelli d’espressione dei quattro miRNAs, espressi come fold change tra i livelli ottenuti nei pazienti affetti da RRSM e i controlli sani, solo di poco superiori rispetto a quelli osservati tra quest’ultimi. Valori statisticamente significativi (p<0.05) sono stati rilevati solo per il miR-223, confermando quanto osservato precedentemente osservato in altri studi.
Figura 4.5 Livelli d’espressione dei miRNAs cellulari. I valori riportati sono espressi come incremento del valore d’espressione dei relativi miRNAs osservato nei pazienti con sclerosi multipla recidivante remittente trattati o no con natalizumab rispetto a quelli ottenuti nei controlli sani. I valori mostrati in figura sono le medie + la deviazione standard di tre prove sperimentali indipendenti. L’asterisco indica i livelli d’espressione significativi ( test t di Student: p< 0.05 (*)) ottenuti per il miR-223 nei pazienti trattati con il mAb rispetto ai pazienti non trattati.