Introduzione e scopo della tesi
Introduzione e scopo della tesi
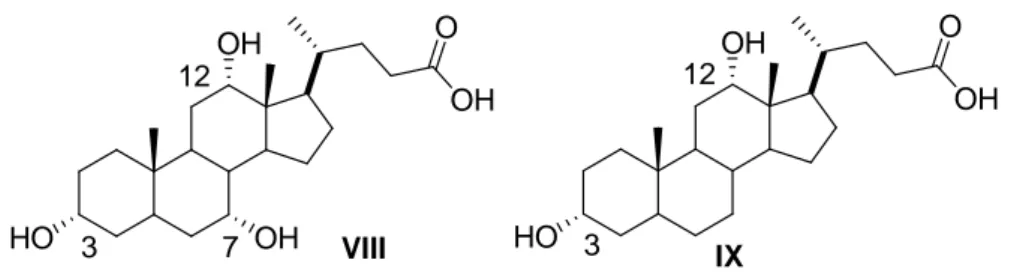
Il controllo diastereoisomerico di un legante tropoisomerico da parte di una subunità chirale, che dà luogo ad una conformazione preferenziale di un complesso diastereoisomerico, rappresenta un modo elegante per ottenere l’attivazione asimmetrica di catalizzatori tropoisomerici, cioè specie che esistono in conformazioni enantiomeriche tra loro velocemente interconvertibili.1 Sulla base di tale concetto sono stati sintetizzati leganti fosfito e fosforoammidito costituiti da una unità chirale configurazionalmente stabile, e da un sistema flessibile bifenolico, che sono stati impiegati in reazioni asimmetriche di idrogenazione,2 idroformilazione3 e di addizione coniugata di dietilzinco catalizzata da rame.4 Il loro successo risiede nella capacità dell’unità configurazionalmente stabile di indurre un senso di torsione prevalente sul frammento flessibile: questo fa sì che ci sia un’alta prevalenza di un’unica specie diastereoisomerica, cosa che permette di ottenere alti eccessi enantiomerici. Il vantaggio di un approccio di questo genere risiede nella possibilità di ottenere un legante chirale, dotato sia di chiralità centrale (uno o più atomi di carbonio stereogenici) che di chiralità assiale (un sistema biarilico) senza bisogno di risolvere la miscela degli enantiomeri del composto bifenilico. È ovvio che questa scelta risulta tanto più vincente quanto più l’unità chirale configurazionalmente stabile è prontamente reperibile o facilmente sintetizzabile. Nel laboratorio dove è stato svolto questo lavoro di tesi è già da tempo attiva una linea di ricerca che riguarda l’impiego di fosfiti tropos di acidi biliari in processi enantioselettivi.5 Gli acidi biliari, di cui l’acido colico e l’acido 7-deossicolico (Figura 1) sono i più noti rappresentanti, sono prodotti naturali di basso costo, caratterizzati dalla presenza, in una struttura chirale rigida, di vari centri stereogenici e di due o tre gruppi ossidrilici dotati di differente reattività in virtù del loro differente intorno stereochimico. Questo ne permette la loro diversa funzionalizzazione, consentendo così di introdurre unità molecolari differenti, per la preparazione di derivati le cui proprietà dipendono non solo dalle caratteristiche delle unità
colestanico. OH HO OH O OH HO OH O OH VIII IX 12 7 3 12 3
Figura 1 Acido colico VIII e deossicolico IX.
La derivatizzazione selettiva dei gruppi ossidrilici degli acidi colico e deossicolico mediante bifenilclorofosfito ha permesso di indagare la capacità del sistema colestanico di indurre un senso di torsione prevalente sull’unità tropoisomerica di bifenilfosfiti di acidi biliari da usare come leganti chirali in catalisi asimmetrica. Sono stati sintetizzati, infatti, i tre diversi fosfiti
X-XII (Figura 2) le cui caratteristiche stereochimiche sono state determinate mediante le
spettroscopie di dicroismo circolare ed NMR.6
O OMe O O O Me P O O O OMe O O O OMe O O O Me O Ph P O O O Me O PO O X XI XI
Figura 2 Struttura fosfiti X-XII.
L’analisi degli spettri CD ed NMR ha permesso di stabilire che il sistema colestanico è in grado di indurre un senso di torsione altamente prevalente all’unità bifenilfosfito, quando questa è legata alle posizioni 7 e 12 degli acidi biliari e che il senso di torsione è opposto nei due casi; M per X e P per XII. Il sistema biliare non è invece in grado di indurre un senso di torsione prevalente all’unità bifenilfosfito legata alla posizione 3 (Figura 2).
Grazie a misure 31P-NMR a temperatura variabile è stato possibile stabilire la natura tropos dei tre fosfiti. Questi sono stati impiegati come leganti chirali nell’addizione asimmetrica coniugata di dietilzinco a chetoni α,β-insaturi catalizzata da rame.
Introduzione e scopo della tesi
I migliori risultati sono stati ottenuti con il sistema in cui il gruppo bifenilfosfito è legato alla posizione 12 dell’acido deossicolico. Noto che la presenza di sostituenti sul sistema bifenilico porta ad un miglioramento della capacità di induzione asimmetrica dei sistemi tropos,4d sono stati in seguito sintetizzati fosfiti degli acidi biliari caratterizzati dalla presenza di sostituenti nelle posizioni 3,3’ o 5,5’ dell’unità bifenilica, che non ne alterano la natura flessibile, per indagare l’effetto che questa sostituzione ha sulla capacità enantioselettiva di questo tipo di leganti chirali.
Le caratteristiche stereochimiche dei nuovi fosfiti sono state studiate mediante le spettroscopie di dicroismo circolare e 31P-NMR.7 L’analisi degli spettri di dicroismo circolare ha messo in evidenza che il sistema colestanico è in grado di indurre un senso di torsione prevalente sulle unità tropoisomeriche di tutti i fosfiti sintetizzati. Pertanto, la presenza di sostituenti nelle posizioni 3,3’ o 5,5’ del sistema bifenilico non pregiudica la capacità di induzione asimmetrica da parte del sistema biliare quando le unità biarilfosfito sono legate alle posizioni 7 e 12; inoltre la presenza di sostituenti nelle posizioni 3,3’ dell’unità bifenilica rende possibile l’induzione di un senso di torsione prevalente anche quando il sistema biarilfosfito è legato alla posizione 3 dell’acido deossicolico.L’analisi degli spettri 31P-NMR a temperatura variabile ha permesso di determinare la natura tropos di tutti i fosfiti, l’entità della prevalenza del senso di torsione e, in alcuni casi, il senso di torsione.
Questi fosfiti sono stati poi impiegati in reazioni di idrogenazione asimmetrica di olefine prochirali catalizzata da Rh portando a buoni livelli di enantioselettività (e.e. fino al 90%).8 Tenendo conto di questi risultati e del fatto che catalizzatori di Rh(I) in presenza di sistemi di fosforo(III) hanno fornito ottimi risultati nella reazione di addizione asimmetrica coniugata di acidi arilboronici ad olefine elettrondeficienti (cfr. Capitolo 1) è sembrato logico impiegare i fosfiti tropos degli acidi biliari come leganti chirali in questa reazione.
La reazione di addizione coniugata asimmetrica di acidi boronici è piuttosto interessante, in quanto consente di ottenere la formazione di un legame C-C in modo enantioselettivo. Inoltre gli acidi boronici sono reattivi organometallici facili da preparare, stabili e che non richiedono condizioni di reazione particolarmente controllate, quali ad esempio ambiente anidro.
Sebbene siano noti vari esempi riguardo l’impiego di leganti bidentati nella reazione di addizione coniugata di acidi boronici a olefine elettrondeficienti (cfr. Capitolo 1), pochi sono gli esempi riguardo l’impiego di leganti al fosforo modentati e tra questi solo uno riguarda l’impiego di leganti tropos.9
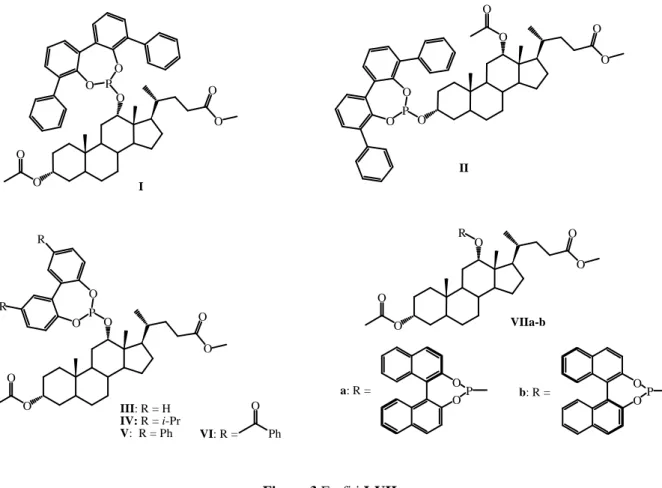
3,3’ difenilbifenilfosfito legato alle posizioni 3 e 12 dell’acido deossicolico, dei fosfiti
III-VI (Figura 3) che possiedono un gruppo bifenilfosfito 5,5’ disostituito legato alla
posizione 12 dello scheletro steroideo e dei fosfiti VIIa-b (Figura 3) rispettivamente con un gruppo (R) o (S)-binaftilfosfito legato alla posizione 12 del sistema colestanico, già messe a punto precedentemente all’interno del laboratorio dove è stato svolto questo lavoro di tesi.
O O O P O O O O P O O O O O O O O O O P O O O O R R O O O O O III: R = H IV: R = i-Pr V: R = Ph Ph O VI: R = R a: R = O b: R = OP O OP VIIa-b I II
Figura 3 Fosfiti I-VII.
2. L’impiego dei fosfiti I-VII come leganti chirali in reazioni di addizione coniugata asimmetrica catalizzate da Rh(I) di acidi arilboronici ad enoni ciclici. Questo permetterà di valutare l’attività catalitica e l’enantioselettività dei loro complessi e di confrontare le capacità enantioselettive dei vari fosfiti allo scopo di valutare l’influenza che i sostituenti presenti sulla porzione bifenilica hanno sull’induzione asimmetrica.
3. La caratterizzazione mediante spettroscopia 31P-NMR dei complessi Rh(I)-fosfito, allo scopo di studiare la complessazione di questi sistemi al Rh(I) e di avere informazioni
Introduzione e scopo della tesi
riguardo la loro natura tropos, il senso di torsione prevalente dell’unità bifenilica nei complessi e l’entità della prevalenza.
1
Mikami, K.; Yamanaka, M. Chem. Rev. 2003, 103, 3369-3400.
2 (a) Reetz, M.T.; Neugebeauer, T. Angew. Chem. Int. Ed. 1999, 38, 179-181. (b) Chen, W.; Xiao, J. Tetrahedron
Letters 2001, 42, 2897-2899. (c) Chen, W.; Xiao, J. Tetrahedron Letters 2001, 42, 8737-8740.
3
(a) Dièguez, M.; Pàmies, O.; Ruiz, A.; Castillòn, S.; Claver, C. Chem. Commun. 2000, 1607-1608. (b) Dièguez, M.; Pàmies, O.; Ruiz, A.; Castillòn, S.; Claver, C. Chem. Eur. J. 2001, 7, 3086-3094. (c) Pàmies, O.; Net, G.; Ruiz, A.; Claver, C. Tetrahedron: Asymmetry 2001, 12, 3441-3445.
4 (a) Alexakis, A.; Polet, D.; Benhaim, C.; Rosset, S. Tetrahedron: Asymmetry 2004, 15, 2199-2203. (b) Alexakis, A.; Benhaim, C.; Rosset, S.; Humam, M. J. Am. Chem. Soc. 2002, 124, 5262-5263. (c) Alexakis, A.; Rosset, S.; Allamand, J.; March, S.; Guillen, F.; Benhaim, C. Synlett 2001, 9, 1375-1378. (d) Alexakis, A.; Polet, D.; March, S.; Rosset, S. Org. Chem. 2004, 69, 5660-5667. (e) Scafato, P.; Cunsolo, G.; Labano, S.; Rosini,C.
Tetrahedron: Asymmetry 1999, 60, 8801-8806.
5
(a) Iuliano, A.; Salvadori, P.; Felix, G. Tetrahedron: Asymmetry 1999, 10, 3353-3364. (b) Iuliano, A.; Masini, G.; Felix, G.; Salvadori, P. Tetrahedron: Asymmetry 2001, 12, 2811. (c) Iuliano, A.; Pieraccini, I.; Felix, G.; Salvadori, P. Tetrahedron: Asymmetry 2002, 13, 1265-1275. (d) Iuliano, A.; Ruffini, A. Tetrahedron:
Asymmetry 2005, 16, 3820-3828.
6 Iuliano, A.; Facchetti, S.; Uccello-Barretta, G. J. Org. Chem. 2006, 71, 4943-4950. 7 Facchetti, S.; Losi, D.; Iuliano, A. Tetrahedron: Asymmetry 2006, 17, 2993-3003. 8 Iuliano, A.; Losi., D.; Facchetti, S. J. Org. Chem. 2007, 72, 8472-8477.
9