1
TITOLO
Controllo del dolore post-operatorio nel
paziente
pediatrico
sottoposto
ad
intervento
di
adeno-tonsillectomia:
2
RIASSUNTO ANALITICO
L’intervento di tonsillectomia con o senza adenoidectomia è uno
degli interventi più frequenti in età pediatrica. Presso l’ Unità Operativa di Otorinolaringoiatria dell’Azienda
Ospedaliero-Universitaria di Pisa si stima che vengano eseguiti
circa 440 interventi all’anno. Il dolore post-adenotonsillectomia in età pediatrica è un dolore
forte.
Rappresenta la principale causa di morbidità nel periodo post-
operatorio. Da tale consapevolezza è nato il nostro studio,con cui abbiamo
voluto verificare e valutare statisticamente l’efficacia e la
sicurezza di due differenti modalità antalgiche intraoperatorie e ottimizzare la gestione postoperatoria del dolore(pre-emptive
analgesia) al di là delle singole esperienze individuali. Le due modalità analgesiche utilizzate differiscono sia per quanto
riguarda il tipo di antidolorifico utilizzato sia per quanto concerne la via di somministrazione.Nello specifico un protocollo prevede
la somministrazione intraoperatoria di morfina endovena e l’altro la somministrazione intraoperatoria di un’associazione
3
INDICE
TITOLO pag. 1 RIASSUNTO ANALITICO pag. 2 SOMMARIO pag 3
INTRODUZIONE pag. 5
L’Adenotonsillectomia nei bambini pag. 5 Dolore post-Adenotonsillectomia pag. 6
Principali farmaci analgesici utilizzati pag. 7
per prevenire e trattare il dolore post adenotonsillectomia nei bambini
Valutazione del dolore in ambito pediatrico pag. 17
OBIETTIVO DELLO STUDIO pag. 22
METODI pag. 22
Modello di studio pag. 22 Popolazione studiata pag. 22 Procedure pag. 23 End Points pag. 25
RISULTATI pag. 28
4
CONCLUSIONI pag. 43
BIBLIOGRAFIA pag. 47
APPENDICE pag. 56 Allegato I :Esempio di Faces Pain Scale di Wong/Baker
Allegato II:Esempio di CHEOPS
Allegato III:-Livelli di evidenza clinica Allegato IV: -Gradi di raccomandazione
5
INTRODUZIONE
La tonsillectomia con o senza adenoidectomia é uno degli interventi chirurgici più frequenti nei pazienti pediatrici.
La più comune indicazione chirurgica é la tonsillite cronica o
ricorrente con iperplasia tonsillare che porta a ostruzione delle vie aeree superiori, tipo sindrome da apnea ostruttiva del sonno,otiti ed infezioni faringo-tonsillari ricorrenti.
Nel 2003 gli interventi di tonsillectomia in Italia ammontavano a 51.983 con un tasso(per 10.000) di 9,1, tasso che sale a 9,4 nel
20041 . Presso l’ Unità Operativa di Otorinolaringoiatria dell’Azienda
Ospedaliero-Universitaria di Pisa si stima che vengano eseguiti
circa 440 interventi all’anno. La possibilità di complicanze post-operatorie gravi come apnee,
sanguinamento post-operatorio e nausea e/o vomito post
operatorio(PONV) condizionano la scelta dei farmaci analgesici, del monitoraggio postoperatorio e della durata del ricovero
6 ospedaliero.
D’ altronde, la maggior parte delle meta-analisi sull’analgesia post tonsillectomia sono focalizzate sulla PONV e sul sanguinamento piuttosto che sull’efficacia analgesica,non considerando che il dolore post-operatorio è una complicanza dell’intervento
chirurgico e come tale va trattato e prevenuto (Pre-emptive Analgesia ossia precoce analgesia in sala operatoria).
L’ American Academy of Otolaryngology—Head and Neck Surgery Foundation, nelle Linee guida sulla tonsillectomia nei bambini, definisce il dolore oro-faringeo come la principale causa di morbidità post-tonsillectomia2
Tale dolore è descritto come dolore inteso a livello faringeo,dolore che aumenta alla fonazione e soprattutto alla deglutizione.
Ciò compromette spesso l’assunzione orale non solo di cibi solidi ma anche di liquidi, determinando in alcuni casi anche
disidratazione e perdita di peso del bambino3.
7 associata ad un incremento del dolore post-tonsillectomia.4
Oltre alla faringodinia, il dolore è spesso irradiato alle
orecchie(otalgia riflessa), per coinvolgimento delle vie sensitive dei nervi trigemino,glosso-faringeo e vago.
Il dolore chirurgico è, in genere, particolarmente intenso nelle
prime 24-72 ore ma può persistere diversi giorni dopo l’intervento. Infatti,nei 5-8 giorni successivi alla tonsillectomia possono
manifestarsi comparsa di dolore intenso,disturbi del
comportamento, interruzioni del sonno e alterata attività.5
Il Coordinamento della Rete Toscana HPH(Health Promoting Hospital) classifica il dolore post-tonsillectomia come Dolore Forte e in accordo con La S.A.R.N.e.P.I.(Società di Anestesia e Rianimazione Neonatale e Pediatrica Italiana) raccomanda,per questo tipo di intervento,la somministrazione di oppioidi intra- operatori dosati individualmente.
Quest’ultima,nelle sue Linee Guida sul dolore Post-operatorio, sostiene,inoltre, che la regolare somministrazione peri-operatoria
8 di analgesici quali FANS e/o paracetamolo sono necessari per il trattamento del dolore post-tonsillectomia (Grado A).6
Fino a qualche tempo fa,per un insieme di fattori(alcuni reali altri mistificati) l’uso degli oppioidi in ambito pediatrico era molto limitato.
La particolare sensibilità ai derivati dell’oppio del bambino,il timore dell’assuefazione,la paura della depressione respiratoria e una reale difficoltà nella valutazione e quantificazione del
dolore,supportavano un’istintiva riluttanza,confermata da una antica tradizione clinica,a non somministrare analgesici maggiori in età pediatrica.
Negli ultimi anni,fortunatamente,la situazione è cambiata:studi di farmacocinetica e farmacodinamica hanno puntualizzato
indicazioni e limiti all’uso dei farmaci oppioidi;l’OMS ha stabilito una scala graduata d’interventi in base alle caratteristiche e
all’entità del dolore;le paure legate alla dipendenza e alla tolleranza sono state ridimensionate.
9 Sono molte le modalità messe a disposizione per la
somministrazione e sono stati codificati parametri per un adeguato monitoraggio di efficacia e sicurezza d’uso.
Quindi, molti “miti” sono caduti ed attualmente nell’ambito del controllo del dolore nel bambino, gli oppioidi occupano un posto rilevante,sia per la loro efficacia che per l’ampia possibilità di uso clinico.
Infatti,la scelta oculata del farmaco in rapporto all’età e al tipo di dolore,una metodologia di somministrazione(timing e via) corretta ed un monitoraggio stretto sia dell’efficacia che degli eventuali effetti indesiderati,permettono di impostare delle terapie
farmacologiche efficaci e sicure.
Brevemente, l’attività farmacologica degli oppioidi deriva dal legame con siti recettoriali presenti in molte aree del SNC e a livello periferico(µ, δ, κ, N).
Le azioni principali sono:
· Inibizione diretta del sistema nocicettivo ascendente (k, µ)
10 · Inibizione della trasmissione algica a livello talamico(µ)
· Inibizione periferica della liberazione di mediatori infiammatori delle cellule del sistema immunitario (µ).
Sono effetti desiderati e terapeuticamente utili:
l’analgesia,l’euforia,la rimozione dell’ansia e l’attenuazione di tutte le risposte integrate all’attivazione del sistema nocicettivo. Diversi gli effetti collaterali: depressione
respiratoria,nausea,vomito, costipazione,ipotensione, prurito. Gli oppioidi più frequentemente usati in età pediatrica sono: codeina,morfina,tramadolo,fentanile,petidina e metadone. La morfina è l’oppioide di riferimento,quello più studiato ed usato in ambito pediatrico per la gestione sia del dolore acuto che cronico7.
La codeina e tramadolo sono oppioidi deboli,hanno una potenza pari al 10% della morfina e gli stessi effetti collaterali.
La codeina è un profarmaco che, per acquisire proprietà
11 dal citocromo CYP4502D6. L'effetto antalgico è legato alla sua metabolizzazione perché, la codeina in quanto tale, ha bassissima affinità per i recettori oppioidi.
Questo isoenzima è soggetto a polimorfismo genetico con ampie variazioni nei livelli di espressione o funzione individuale.8,9,10 Il polimorfismo genetico del citocromo CYP2D69 può spiegare la variabilità nella risposta clinica di soggetti diversi alla stessa dose di codeina. In particolare, i soggetti metabolizzatori poveri o lenti possono non convertire codeina in morfina e non beneficiare
dell’effetto analgesico ; i soggetti metabolizzatori ultra-rapidi convertono la codeina in morfina più rapidamente e possono
presentare un aumento delle concentrazioni di morfina nel sangue. Questi individui sono più a rischio di reazioni avverse a morfina pur ricevendo dosi terapeutiche di codeina*.
*La probabilità infatti di essere un metabolizzatore ultra-rapido varia tra i diversi gruppi etnici da meno di 1 su cento persone a circa 30 su 100 persone. Si stima che i metabolizzatori ultra-rapidi siano il 4-5% negli Stati Uniti ed il 20-30 % in Etiopia ed Arabia Saudita 11 .Sono,metabolizzatori ultra-rapidi circa l’1% delle persone di origine caucasica in Nord Europa12ed il 5,45% della popolazione in Europa occidentale . Analizzando la distribuzione dei metabolizzatori ultra-rapidi nei vari Paesi dell’Europa occidentale si osserva che in Italia la frequenza dei soggetti con un’aumentata espressione del geneCYP2D6 UM è del 10%, valore pari a quello del Portogallo, della Grecia e della Spagna e maggiore rispetto agli altri Paesi13
12 Il tramadolo è un analgesico centrale di sintesi.
La sua azione si esplica attraverso l’inibizione del reuptake delle amine biogene (noradrenalina e serotonina) e come debole
attivazione dei recettori µ per gli oppioidi (tramite il metabolita M1).
In alcuni studi sul dolore post-tonsillectomia, il tramadolo è
risultato meno efficace del ketoprofene ( più alto scores del dolore e maggiore richiesta di PCA con fentanyl nel postoperatorio) e non differiva dal placebo.14
Il Paracetamolo è di gran lunga l’analgesico più utilizzato nel bambino.
Molto spesso è il primo agente a cui si fa ricorso nel trattamento del dolore di media o moderata intensità.
Inoltre,viene usato anche come adiuvante ai morfinici nelle forme di dolore più severe.
Ha un elevato margine terapeutico ed è un farmaco “sicuro”,non ha alcun effetto indesiderato grave a carico del distretto gastro- enterico e renale,non altera la coagulazione né favorisce episodi di
13 sanguinamento.
Tale farmaco inibisce debolelmente la via di sintesi delle prostaglandine determinata in maggior parte dalla COX2.
Sembra,inoltre, che esista una terza isoforma di ciclo-ossigenasi espressa a livello cerebrale (COX3) che potrebbe essere il suo bersaglio preferenziale.
L'inibizione di questo enzima, potrebbe dar conto di una parte degli effetti analgesici ed antifebbrili centrali mediati dal
paracetamolo.15,16,17,18,19
Inoltre,si ritiene che il paracetamolo stimoli l’attività del Sistema serotoninergico discendente che inibisce la trasmissione di segnali nocicettivi a livello del midollo spinale20.
Da recenti studi, si è visto che il paracetamolo è più efficace se somministrato per os prima della tonsillectomia, piuttosto che per via rettale dopo l’induzione dell’anestesia e il suo utilizzo riduce la richiesta di oppioidi e l’incidenza di PONV.21,22
14
i parametri cinetici dei due farmaci sovrapponibili.23 Tuttavia,gli effetti collaterali associati alla codeina come la PONV e la
costipazione induce sempre più spesso ad utilizzare solo il paracetamolo,che tuttavia si rivela spesso inadeguato a controllare,da solo,il dolore post tonsillectomia.24
I FANS riducono il rilascio di mediatori dell’infiammazione e aumentano il tono serotoninergico.La somministrazione di FANS, così come la somministrazione di Desametasone per la
prevenzione della PONV, nel dolore post-tonsillectomia, rimane controversa.
Questi analgesici migliorano l’analgesia se confrontati con il
placebo (10/11 studi) e garantiscono un livello di analgesia simile agli oppioidi (7/8 studi) e al paracetamolo (3/3 studi).25
Tuttavia, una review sistematica di studi pediatrici ha stabilito che l’eterogeneità dei dati preclude una metanalisi.
Numerosi studi che confrontavano due trattamenti attivi non erano abbastanza significativi per mostrare una differenza.26
15 Studi successivi hanno riportato simile analgesia con ketorolac e fentanyl27, nessun miglioramento con l’aggiunta di rofecoxib agli oppioidi e paracetamolo28.
La PONV che segue la tonsillectomia sembra sia ridotta con l’utilizzo dei FANS, presumibilmente per la riduzione nella richiesta di oppioidi29
In conclusione, sebbene le metanalisi non offrano al momento dati certi, la somministrazione perioperatoria di FANS sembra essere associata ad un minimo rischio di sanguinamento post-
tonsillectomia,come risulta da alcuni importanti trials clinici.30,31,32 Suggestivi sono alcuni recenti studi sull’uso di infiltrazione con
anestetici locali delle fosse tonsillari post-tonsillectomia anche
se,una metanalisi condotta nel 2000 non ha confermato l’utilità di tale infiltrazione.
Soltanto 6 studi controllati randomizzati erano idonei per l’inclusione33.
16 Sia la Ropivacaina che la Bupivacaina iniettati nella fossa
tonsillare avevano ridotto gli scores del dolore,l’analgesia
supplementare nelle 24 ore postoperatorie e aumentato il tempo di somministrazione della analgesia rescue 34 , ma non sono state riportate differenze nelle prime registrazioni del VAS o nel tempo della prima assunzione orale.35
Allo stesso modo,sono stati evidenziati solo piccoli miglioramenti negli scores del dolore e nel tempo della prima assunzione orale dopo applicazione di garze impregnate di anestetico locale nella fossa tonsillare dopo rimozione della tonsilla36 . La somministrazione di ketamina intraoperatoria,in questo tipo di intervento, non garantisce vantaggi significativi nel postoperatorio rispetto ai farmaci oppioidi( Grado B). 37,38, 39
17 Infatti,la terapia del dolore non può prescindere dalla misura della stessa.
Studi dimostrano che il dolore è sottovalutato e poco documentato e ciò si traduce in bambini sotto-medicati il cui dolore è
scarsamente controllato40.
Una regolare valutazione del dolore può contribuire alla sicurezza ed all’efficacia del controllo del dolore acuto41. La misurazione del dolore deve produrre dei valori numerici confrontabili.
Tuttavia,il dolore è difficile da quantificare,in quanto non è una semplice risposta neurofisiologica ad uno stimolo,ma l’interazione di fattori psicologici,sociali,culturali,ambientali e di memoria,in grado di influenzare la sensazione algica,modificandola.
La difficoltà risulta maggiore nel bambino,soprattutto in età preverbale e prescolare: nessun bambino è uguale ad un altro(stessa età e livelli evolutivi diversi,influenze ambientali diverse).
18 Inoltre,per i più piccoli sono i genitori che interpretano gli
atteggiamenti dei bambini.
Al fine di valutare il dolore, è necessaria una fattiva
comunicazione, ove possibile, tra il bambino, la sua famiglia o chi si occupa di lui, e il personale sanitario del team multidisciplinare. Attualmente esistono diverse Scale algometriche.
Queste possono essere soggettive(self-report) e si basano sulla descrizione verbale o analogica che il paziente riesce a dare del proprio dolore o oggettive, e valutano specifici indici
comportamentali e fisiologici in risposta ad uno stimolo doloroso derivandone un punteggio secondo l’intensità del dolore.
Sono Scale soggettive:
• Wong and Baker FACES Pain Scale valido dai 3 -18 anni. (Wong and Baker 1988):
• Faces Pain Scale-Revised42,43, 44
• Scale di valutazione di visualizzazione analogica e numerica: valido dagli 8 anni in poi.
19 • Pieces of Hurt Tool 45,46 : valido dai 3 - 8 anni.
Invece tra quelle oggettive le più usate sono:
• FLACC (Face, Legs, Arms, Cry, Consolability)47,48,49,50,51:
valido da 1 - 18 anni.
• CHEOPS (Children’s Hospital of Eastern Ontario PainScale):52,53 valido da 1 - 18 anni.
L’ autovalutazione del dolore nei bambini è considerata spesso
come il “gold standard” e nella maggior parte dei casi è l'approccio preferito(GradoB)6.
Tuttavia bisogna riconoscere che l’autovalutazione negli adulti e nei bambini è complessa 54,55,56
Nessuna misura individuale di carattere osservazionale56 ,di
autovalutazione54 o misura fisiologica può essere raccomandata in linea generale per la valutazione del dolore di tutti i bambini o in tutti i contesti(GRADO B).
20 che utilizzino insieme con l’autovalutazione anche almeno uno degli altri metodi di misura54.
Riguardo alle misure dei parametri fisiologici(la pressione arteriosa, la frequenza cardiaca e la frequenza respiratoria), usate indirettamente per indicare la presenza di dolore,
si sono dimostrati indicatori inattendibili in neonati, infanti e bambini piccoli57 con ampie correlazioni interindividuali e fisiologico-comportamentali58.
22
OBIETTIVO DELLO STUDIO
Abbiamo deciso di confrontare l'efficacia di due protocolli analgesici:
-uno prevede la somministrazione di morfina per via endovenosa -l'altro prevede la somministrazione di Paracetamolo/Codeina per
via rettale
METODI Modello di studio:
Studio prospettico controllato randomizzato.
Popolazione studiata
Sono stati arruolati arruolati nello studio 30 bambini di età
compresa tra 3-7 anni sottoposti a adeno-tonsillectomia elettiva per tonsilliti croniche o sleep apnea nel periodo che va da Marzo a Maggio2011.
Sono stati esclusi dallo studio:bambini affetti da patologie cardiache e neurologiche.
23
Procedure
I 30 bambini sono stati divisi in 2 gruppi:
-un gruppo di 15 bambini ha ricevuto morfina per via endovenosa. Il dosaggio usualmente utilizzato è stato 0,1mg/kg.Veniva somministrata poco dopo l’inizio
dell’intervento(Gruppo A). -l’altro gruppo di 15 bambini ha ricevuto un’ associazione
farmacologica con paracetamolo-codeina per via rettale all’inizio dell’intervento.
La dose usualmente somministrata è stata 205mg
(200 mg di paracetamolo+ 5mg di codeina)(Gruppo B).
L'assegnazione ad uno dei due gruppi è avvenuta in modo casuale.
In modo standardizzato in entrambi i gruppi:
- i bambini non hanno ricevuto premedicazione. -l’induzione ed il mantenimento dell’anestesia era
inalatoria(Sevoflurano +/- Protossido d’azoto). - L’ accesso venoso veniva preso immediatamente dopo
24 l’induzione inalatoria,quando il bimbo dormiva in modo da ridurre
al minimo il grado di stress e il dolore legato alla procedura. - L’intubazione oro- tracheale veniva effettuata previa
somministrazione di mivacurio (0,2 mg/Kg).
Sono stati utilizzati tubi cuffiati.
-Liquidi di mantenimento(20-25 ml/KG di Soluzione Fisiologica)
-Non è stata usata decurarizzazione. -La tecnica chirurgica utilizzata è stata quella di dissezione delle
adenoidi/tonsille con Pinza bipolare. -La durata media dell’intervento è stato di 20-30 minuti.
- Dopo 15 minuti dalla fine dell’intervento sono stati rimandati nel
reparto di degenza e sono stati dimessi il giorno dopo. -Durante la degenza,potevano mangiare un gelato dopo quattro ore
dall’intervento e assumere liquidi chiari dopo due ore
dall’intervento.
-E’ stato utilizzato come analgesico rescue paracetamolo+codeina per via rettale.
25
END POINTS
Obiettivo primario
Valutazione dell' entità del dolore post-chirurgico tramite la
Faces Pain Scale (rFP) di Wong/Baker(allegato I) al risveglio,
a distanza di 3ore, 6 ore dall'intervento e alla dimissione dal reparto.
Un rFP score pari/inferiore a 4 viene considerato come un adeguato controllo del dolore.
Viene,inoltre,registrato il numero di bambini che necessitano nel
post-operatorio di somministrazione di analgesico rescue. Accanto a tale metodo di misura soggettivo(autovalutazione),in
accordo con la letteratura internazionale,abbiamo deciso di adottare anche un metodo di misura del dolore
oggettivo(eterovalutazione).
Questa valuta anche il grado di stress del bambino*.
*Si definisce stress: qualsiasi situazione di disagio fisico e/o psichico che generi sensazioni di ansia, angoscia, paura, accompagnate dalle reazioni fisiologiche di disagio dell’organismo
26 A tal fine,viene da noi utilizzata la CHEOPS(Children’s
Hospital of Eastern Ontario Pain Scale) adatta ai bambini di età
compresa tra i 1-18 anni(allegato II).
La CHEOPS valuta il dolore post-operatorio e l’atteggiamento del bambino sulla base di 6 ITEMS:
pianto,espressione facciale,verbalizzazione, atteggiamento del dorso,tendenza a toccare la parte dolente,posizione degli arti. Per ciascuna alternativa di descrizione dei 6 items c’è un punteggio distinto.
I 6 punteggi vengono alla fine sommati. Un punteggio finale pari o superiore a 7 indica un’analgesia
insufficiente.
Obiettivi secondari
1 ) Valutazione dell'incidenza degli effetti secondari associati
tradizionalmente all'uso di oppiacei.
In particolare:
• La PONV e l’eventuale ricorso a farmaci antiemetici.
• Depressione respiratoria con episodi di apnea
27
2)Concordanza tra le due modalità di valutazione del dolore,quella
soggettiva auto-valutativa (rFP Scale) e quella comportamentale etero-valutativa(CHEOPS).
Nel corso delle valutazioni sono registrati anche parametri fisiologici come la frequenza cardiaca e respiratoria.
28
Risultati
L’analisi statistica dei dati è stata effettuata mediante l’utilizzo di Excel.
In particolare,abbiamo calcolato parametri di statistica descrittiva(frequenza,percentuale;misure di tendenza
centrale:media. Misure di dispersione:errore standard della media) e test non parametrici:CHI-quadrato per il calcolo del p value. Lo studio è stato effettuato su 30 bambini, sottoposti ad intervento di adeno-tonsillectomia, di età compresa tra i 3 e 7 anni.
Sono stati formati 2 gruppi di 15 bambini selezionati in maniera random.
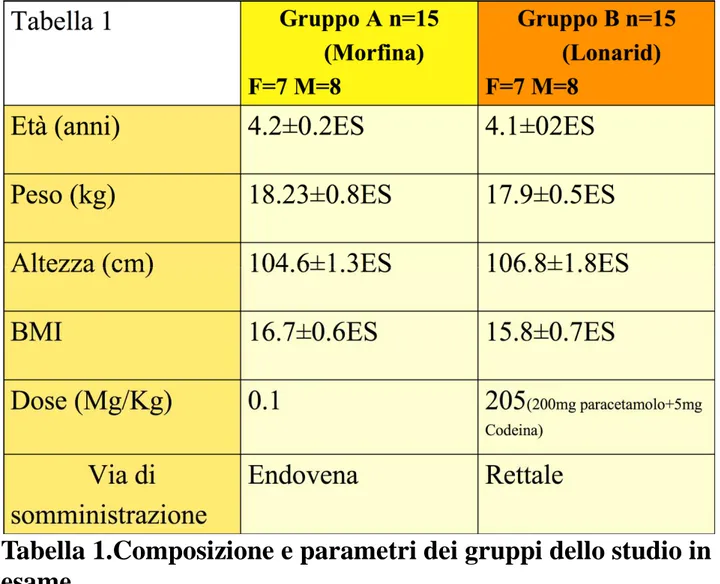
Il primo gruppo (gruppo A) ha ricevuto morfina(0.1 mg/kg) per via endovenosa nel periodo intraoperatorio (Tabella 1).
Il secondo gruppo(gruppo B) ha ricevuto, intraoperatoriamente, paracetamolo+codeina per via rettale(200mg paracetamolo+5mg codeina) (Tabella 1).
Le caratteristiche dei due gruppi sono riportate in Tabella 1, come appare chiaro le caratteristiche (età; peso; altezza;etc.) dei singoli gruppi non differiscono in maniera significativa, in questo modo si riduce ulteriormente l’eventuale variabilità dello studio dovuto a caratteri secondari.
29
Tabella 1.Composizione e parametri dei gruppi dello studio in esame.
Per ogni paziente, inserito nei due diversi gruppi sono stati annotati l’età, il peso, l’altezza, calcolato il BMI.
Si riporta il valore medio dei singoli gruppi per ogni parametro con il rispettivo Errore Standard.
La dose e la via di somministrazione sono state decise in base a parametri scelti e ai protocolli associati e sono riportati in alto.
Per paragonare i due diversi trattamenti analgesici abbiamo scelto,tra i numerosi strumenti di misurazione del dolore
30 tanti strumenti di misura del dolore in età pediatrica, questi due sono stati ben valutati e vengono comunemente utilizzati nella pratica corrente.
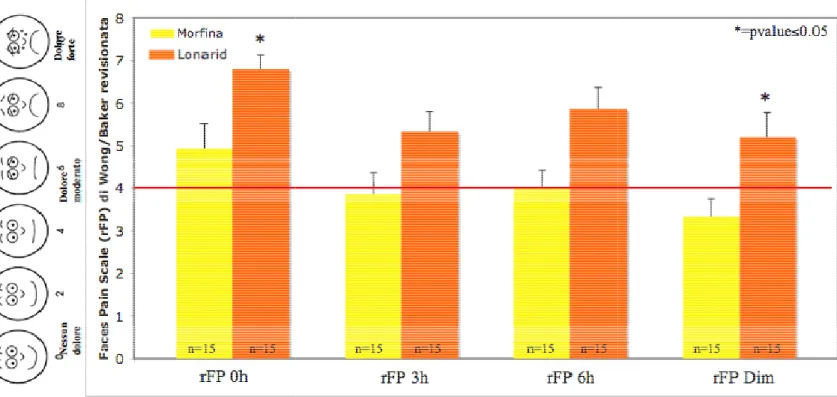
Nel gruppo A la valutazione del dolore con la Faces Pain Scale ha evidenziato un adeguato controllo del dolore nell’ immediato post-operatorio nel 40% dei casi(6 bambini),mentre ben il 60%(9 bambini) ha riportato un FP score superiore a 4(Media 4,9;E.S. 0,5).
A 3 e a 6 ore dall’intervento il 73,4%(11 bambini) ha riportato un FP score compreso tra 0 e 4 con un buon controllo del dolore (a 3ore Media 3,8; ES 0,49. A 6 ore Media 4 ES 0,58).
Alla dimissione il 93,3%(14 bambini) ha indicato un FPscore ≤ 4 (Media 3; ES 0,42) (Fig.1).
Solo un bambino ha evidenziato un’analgesia inadeguata con uno score di 6.
Per quanto riguarda la valutazione oggettiva mediante l’utilizzo della CHEOPS( valida per la fascia di età 1-18 anni) abbiamo rilevato uno score al risveglio ≥ 7 nell’80% dei casi (12 bambini) (Media 8,6;ES 0,6).
A 3 ore dall’intervento l’86,7%(13 bambini) ha avuto un CHEOPS score inferiore a 7(Media 5,6; ES 0,2).A 6 ore il
93,3%(14 bambini) ha riportato un valore CHEOPS inferiore a 7(Media 5,7; ES 0,3).
31 Alla dimissione tutti i bambini(100%) hanno indicato un valore inferiore a 7(dieci bambini hanno riportato uno score di 6;tre un valore di 5 e due bambini uno score di 4)(Media 5,5; ES 0,19) (Fig.2).
Per quanto concerne l’uso di analgesici rescue nel post-operatorio solo tre bambini(20%) hanno ricevuto paracetamolo+codeina per via rettale rescue (fig.3).
In particolare:
un bambino alla dimissione(rFP =6 e Cheops=6);
un bambino a sei ore dalla tonsillectomia(rFP=8;Cheops=10); un terzo bambino alla dimissione(rFP=4;Cheops=6).
Quest’ultimo rappresenta un outlier.
Per quanto riguarda la PONV il 26,7% dei bimbi(4 casi) ha
presentato nausea occasionale, 26,7% vomito e 46,7%(8 bambini) non ha avuto nessuna sintomatologia emetica( Es 0,3) (Fig.4). Nel gruppo B la valutazione del dolore con la Faces Pain Scale ha mostrato al risveglio che il 93,3% dei bambini ha avuto un
inadeguato controllo del dolore:otto bambini hanno indicato un FPs score di 6, sei bambini uno score di 8.
Un solo bambino ha riportato un adeguato controllo del dolore con un FPs score di 4(Media 6,8; ES 0,3) (Fig.1).
A 3 ore dall’intervento il 60 % dei casi(9 bambini) ha mostrato uno score superiore a 4( Media 5,3; ES 0,46).
32 Anche a 6 ore dall’intervento,il 60% dei bambini ha riportato uno score superiore a 4(Media 5,8; ES 0,6).
Alla dimissione il 60% dei bambini ha riportato un FP score superiore a 4:
sei bambini uno score di 6, tre bambini un valore di 8.(Media 5,2; ES 0,579) (Fig.1).
Utilizzando la CHEOPS in questo gruppo, abbiamo visto che al risveglio nessun bambino ha riportato uno score inferiore a 7 (Media di 10;ES 0,49).
A 3 ore dall’intervento,il 60%(9 bambini) ha indicato uno score CHEOPS≥7.
(Media 6,7;ES 0,26) (Fig.2).
A 6 ore dall’intervento il 66,7%(10 bambini) ha indicato un CHEOPS score ≥7;
(Media 7; ES 0,35).
Alla dimissione:CHEOPS≥ 7 nel 66,7% (Media di 6,8; ES 0,2). Nel dettaglio otto bambini uno score di 7; un bambino un valore di 8 ed un altro bambino un valore di 9 (Fig.2) .
Quattro bambini(26%) hanno ricevuto paracetamolo+codeina rescue nel postoperatorio.
Tre bambini a 6 ore dall’intervento(FP e CHEOPS= 10 in un caso;in altri due casi FP=8 e CHEOPS= 7;FP=8;CHEOPS 10) Un bambino alla dimissione(rFP=6 e CHEOPS=7).
33 Riguardo alla PONV,il 73,3% (11 bambini) non ha mai presentato episodi di nausea e/o vomito postoperatori.
Il 13,3%(2 bambini) hanno presentato nausea occasionale e l’altro 13,3% ha presentato vomito(ES 0,274) (Fig.4).
Figura 1. Media dei valori di Valutazione tramite Faces pain
Scale di Wong/Baker
In figura 1 si riportano i valori medi dei singoli gruppi alla valutazione del dolore postoperatorio,tramite Faces pain momento del trattamento,dopo 3h, 6h e al momento della dimissione. La linea rossa rappresenta il valore soglia. Le differenze tra i due gruppi a tempo 0h e al momento della dimissione sono altamente significative con un p
0.05.
Figura 1. Media dei valori di Valutazione tramite Faces pain
Scale di Wong/Baker In figura 1 si riportano i valori medi dei singoli gruppi alla
valutazione del dolore postoperatorio,tramite Faces pain momento del trattamento,dopo 3h, 6h e al momento della dimissione. La linea rossa rappresenta il valore soglia. Le differenze tra i due gruppi a tempo 0h e al momento della
dimissione sono altamente significative con un p-value inferiore a
34
Figura 1. Media dei valori di Valutazione tramite Faces pain
In figura 1 si riportano i valori medi dei singoli gruppi alla
valutazione del dolore postoperatorio,tramite Faces pain scale, al momento del trattamento,dopo 3h, 6h e al momento della
dimissione. La linea rossa rappresenta il valore soglia. Le differenze tra i due gruppi a tempo 0h e al momento della
35
Figura 2 Valutazione CHEOPS (Childrens’s of Eastern Ontario Pain Scale)
In figura 2 è riportato il grafico rappresentante la media dei
valori di misurazione del dolore con la CHEOPS. La linea rossa tratteggiata indica il valore soglia accettabile per
indicare un adeguato controllo del dolore. Anche,con tale metodo algometrico(oggettivo) si nota una
netta differenza nel controllo antalgico tra il gruppo A, a cui è stata somministrata morfina per via endovenosa ed il gruppo B,
che ha ricevuto paracetamolo+codeina per via rettale. Il gruppo A mostra un migliore livello di analgesia
36
Figura 3. Paracetamolo+codeina rescue nei gruppi A e B.
In figura 3 si rappresenta graficamente la percentuale dei bambini nei due gruppi che hanno ricevuto
paracetamolo+codeina per via rettale come analgesico
rescue.Si nota come tale percentuale in entrambi i gruppi è molto bassa Si 26% No 74% Si 20% No 80% Morfin Para+cod
Analgesia rescue:Gruppo A vs B
37
Fig.4.Percentuale di episodi PONV negli individui dei due gruppi (morfina vs paracetamolo+codeina).
In alto vediamo la rappresentazione grafica della percentuale dei bambini dei due gruppi che hanno manifestato episodi di PONV.
Si nota una tendenza maggiore a presentare PONV nel gruppo trattato intraoperatoriamente con la morfina rispetto al gruppo trattato con paracetamolo+codeina. 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% 1 2 % I n d iv id u i
PONV SCORE=0 PONV SCORE=1 PONV SCORE=3
38
Discussione
Attraverso l’analisi dei comportamenti post-operatori dei gruppi trattati con Morfina e Paracetamolo+Codeina(gruppo A e gruppo B) possiamo osservare un migliore controllo dell’analgesia post-operatoria nel gruppo che ha ricevuto morfina per via endovenosa rispetto al gruppo che ha ricevuto Paracetamolo+codeine per via rettale.
Inoltre nello stesso gruppo appare evidente un minore grado di stress.
Tali differenze sono osservabili con entrambi i metodi di valutazione del dolore adottati, il metodo soggettivo tramite la valutazione FPS di Wong/Baker ed il metodo oggettivo tramite la CHEOPS.
La valutazione algometrica con la FPS mostra come tale differenza sia altamente significativa nell’immediato post-operatorio e alla dimissione (p-value inferiore 0,05).
39 Tale tendenza è confermata anche nelle valutazioni a 3h e 6h dall’intervento, quando il 73,4% di bambini trattati con Morfina ha indicato un FP score≤4, contro il 40% dei bambini trattati con Paracetamolo+Codeina per via rettale.
Questa differenza non appare altamente significativa con un p-value=0.06, tuttavia tale valore non si discosta enormemente dalla significatività e potrebbe dunque derivare dall’intrinseca variabilità dei singoli individui.
Considerando l’intero periodo post-operatorio (dal risveglio alla dimissione) un grado di anelgesia migliore si osserva sempre nel gruppo che ha ricevuto Morfina, in tutti i tempi di osservazione ed analisi (0h, 3h, 6h, dimissione) anche attraverso l’analisi della CHEOPS, dove il p-value in tutti i tempi di analisi rimane inferiore a 0.05.
Abbiamo,inoltre, visto come la morfina ha ridotto non solo il grado di dolore ma anche lo stress del bambino.
40 Lo stress incide sia sulla componente fisica del bambino che su quella psicologica, determinando un aumento della percezione dolorosa ed un abbassamento della soglia del dolore, è dunque molto importante controllarne e monitorarne l’entità.
Un livello di stress più elevato, difatti, potrebbe anche spiegare la maggiore percentuale dei bambini (in entrambi i gruppi studiati) con un inadeguato grado di analgesia al risveglio, rispetto a quelle riscontrate nelle valutazioni successive, quando il bambino è in camera con i genitori, in un ambiente più confortevole, con i propri giochi.
Riguardo alla somministrazione di analgesico “rescue” nel postoperatorio, solo 4 bambini tra quelli trattati con Paracetamo+Codeina intra-operatoriamente e che hanno indicato un inadeguato controllo del dolore, ne hanno beneficiato.
Nel gruppo trattato con Morfina 3 bambini hanno ricevuto analgesico “rescue” e, singolarmente, osserviamo come uno di
41 questi, sia con la FPS che con la CHEOPS, ha riportato un adeguato controllo antalgico (“outlier”).
In entrambi i gruppi è importante sottolineare dunque che il ricorso alla somministrazione di analgesico “rescue” è avvenuto di rado
Relativamente alla PONV,abbiamo registrato una maggiore tendenza a manifestarsi nel gruppo trattato con Morfina(53,4%
dei casi) rispetto al gruppo trattato con l’associazione Paracetamolo+codeina, nei quali è stata riscontrata solo nel 26,7%
dei casi.
Questi dati concordano con quelli già riportati in letteratura riguardo all’effetto emetico della Morfina e comunque, in nessun caso, è stato necessario somministrare farmaci antiemetici ai bambini.
Infine, entrambi i farmaci, alle dosi somministrate, hanno dimostrato lo stesso grado di sicurezza.
42 Non ci sono stati casi di apnee o di altri disturbi respiratori né sono stati registrati episodi di sanguinamento post-operatorio tali da richiedere un re-intervento.
43
Conclusione
Con il nostro studio abbiamo constatato che,al di là delle singole esperienze individuali, la somministrazione di Morfina (dosata individualmente), è associata ad un migliore controllo del dolore nel post-operatorio, rispetto alla somministrazione per via rettale dell’associazione farmacologica Paracetamolo+Codeina.
Studi precedenti hanno inoltre dimostrato che la codeina risulta essere un farmaco poco maneggevole.
Le sue proprietà analgesiche sono dovute alla metabolizzazione in Morfina a livello del fegato dal citocromo CYP4502D6.
A causa di un ampio polimorfismo genetico nella popolazione, a parità di dose somministrata, potrebbe non provvedere ad una adeguata analgesia in alcuni individui (metabolizzatori lenti) o essere responsabile di un sovradosaggio di morfina con importanti effetti collaterali (metabolizzatori rapidi).
Per tale ragione sempre più spesso si tende ad usare solo il Paracetamolo che, tuttavia, senza la presenza degli oppioidi è
44 inadeguato a trattare un dolore forte come quello
post-adenotonsillectomia.
Altrettanto vero, è che, pur non essendo i dati relativi alla PONV statisticamente significativi (p-value=0,6), la somministrazione di Morfina è in genere associata ad una maggiore tendenza a
sviluppare nausea e vomito post-operatorio.
Al fine di minimizzare tale effetto collaterale, si potrebbe provare ad introdurre nella condotta anestesiologica intraoperatoria, l’uso di antiemetici a scopo profilattico.
Entrambi i trattamenti, comunque, sono risultati sicuri non avendo registrato fenomeni di apnee post-operatorie né di sanguinamenti importanti tali da richiedere un trattamento chirurgico (a
differenza di quanto si è osservato con i FANS).
Riguardo alla valutazione del dolore nel bambino, in accordo con quanto è raccomandato nelle principali Linee Guida, abbiamo potuto verificare come l’associazione di una scala soggettiva con
45 una oggettiva, ci consenta di avere una valutazione globale più completa del grado di dolore e stress del bambino.
Riteniamo inoltre importante sottolineare che in pochi casi si è ricorso a somministrazione di analgesico “rescue” nel
postoperatorio malgrado un non sempre adeguato controllo del dolore post-operatorio.A nostro avviso sarebbe auspicabile
ottimizzare la qualità del periodo postoperatorio con una regolare e adeguata misurazione del dolore associata ad una
47
A BIBLIOGRAFIA
1. G. Motta, D.Casolino, B.Cassiano, S.Conticello, et al. Epidemiology of
Adeno-Tonsillar Surgery in Italy. Acta Otorhinolaryngologica Italica. 2008; 28: 1-6
2. Clinical Practice Guideline : Tonsillectomy in Children R. Wald, Eric Wall, Gemma Sandberg and Milesh M. Patel Darrow, Terri Giordano, Ronald S. Litman, Kasey K. Li, Mary Ellen Mannix, Richard H. Schwartz, Gavin Setzen, Ellen Reginald F. Baugh, Sanford M. Archer, Ron B. Mitchell, Richard M. Rosenfeld, Raouf Amin, James J. Burns, David H. Otolaryngology -- Head and Neck Surgery 2011 144: S1
3.Tabaee A, Lin JW, Dupiton V, et al. The role of oral fluid intake following adeno-tonsillectomy. Int J Pediatr Otorhinolaryngol. 2006;70:1159-1164
4. Egeli E, Harputluoglu U, Ozturk O, et al. Can post-adenotonsillectomy
morbidity be reduced by intravenous 24 h hydration in pediatric patients following adenotonsillectomy Int J Pediatr Otorhinolaryngol. 2004;68:1047- 1051.
5. Warnock F, Lander J. Pain progression, intensity and outcomes following
Tonsillectomy Pain1998;75(1):37-45.; Giannoni et al.2001; Park et al. 2004;
Owczarzak and Haddad 2006.
6. Linee Guida sul dolore Post-operatorio S.A.R.N.e.P.I.(Società di Anestesia e Rianimazione Neonatale e Pediatrica Italiana).Testo adottato e tradotto dalle linee guida della Association of Pediatric Anesthesia (APA), Royal
College of Nursing (RCN) e Royal College of Paediatrics and Child Health
(RCPCH)
7. L’utilizzo degli oppioidi nell’ambito terapeutico del dolore pediatrico
F.Benini(Responsabile Servizio Terapia Antalgica e Cure Palliative dipartimento di Pediatria,Università degli Studi di Padova) Pathos(Rivista di
48
8. Williams DG, Patel A, Howard RF. Pharmacogenetics of codeine
metabolism in an urban population of children and its implications for analgesic reliability. Br J Anaesth.2002;89:839-845
9. Fagerlund TH, Braaten O. No pain relief from codeine...? An introduction to
pharmacogenomics. Acta Anaesthesiol Scand. 2001;45:140-149
10. Ciszkowski C, Madadi P, Phillips MS, et al. Codeine, ultrarapid-
metabolism genotype, and postoperative death. N Engl J Med. 2009;361:827-828
11. Ingelman-Sundberg M. Pharmacogenetics: an opportunity for a safer and
more efficient pharmacotherapy. J Intern Med 2001; 250: 186-200.
12. Dahl ML, Johansson I, Bertilsson L, et al. Ultrarapid hydroxylation of
debrisoquine in Swedish population. Analysis of the molecular genetic basis. J Pharmacol Exp Ther 1995;274: 516-20
13. Ingelman-Sundberg M. Genetic polymorphisms of cytochrome
P450 2D6 (CYP2D6):Clinical consequences, evolutionary aspects and functional diversity.Pharmacogenomics J 2005; 5: 6-13
14 Antila H, Manner T, Kuurila K, Salantera S, Kujala R, Aantaa R.
Ketoprofen and Tramadol for analgesia during early recovery
after tonsillectomy in children. Paediatr Anaesth 2006;16(5):548-553.
15 Botting R. Paracetamol-inhibitable COX-2. J Physiol Pharmacol. 2000
Dec;51(4 Pt 1):609-18
16. Graham GG, Scott KF. Mechanism of action of paracetamol. Am J Ther.
2005 Jan-Feb;12(1):46-55. Review. PMID: 15662292 [PubMed - indexed f or MEDLINE]
17. Chandrasekharan NV et al. COX-3, a cyclooxygenase-1 variant inhibited
by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression Proc Natl Acad Sci U S A. 2002 Oct 15; 99(21):13926-31. Epub 2002 Sep 19.
18. Schwab JM, Schluesener HJ, Laufer S. COX-3: just another COX or the
solitary elusive target of paracetamol? Lancet. 2003 Mar 22;361(9362): 981-82.
49
19. Botting R, Ayoub SS. COX-3 and the mechanism of action of
paracetamol/acetaminophen. Prostaglandins Leukot Essent Fatty Acids. 2005 Feb; 72(2):85-87.)
20. Bonnefont J. Alloui A E. et all.Orally administered paracetamol does not
act locally in the rat formalin test:evidence for a supraspinal,serotonin- dependent antinociceptive mechanism.Anesteshesiology 2003;99:976- 981
21. Anderson B, Kanagasundarum S, Woollard G. Analgesic efficacy of paracetamol in children using tonsillectomy as a pain model. Anaesth Intensive Care 1996;24(6):669-673.
22. Ander son BJ, Ralph CJ, Stewart AW, Barber C, Holford NH. The dose-
effect relationship for morphine and vomiting after day-stay tonsillectomy in children. Anaesth Intensive Care2000;28(2):155-160.
23. Bajorek P et al. Lack of inhibition of paracetamol absorption by codeine.
Br J Clin Pharmac 1987; 5:346
24. Anderson BJ, Holford NH, Woollard GA, et al. Perioperative
pharmacodynamics of acetaminophen analgesia in children. Anesthesiology. 1999;90:411-421
25. Keidan I, Zaslansky R, Eviatar E, Segal S, Sarfaty SM. Intraoperative
ketorolac is an effective substitute for fentanyl in children undergoing outpatient adenotonsillectomy.Paediatr Anaesth2004;14(4):318-323.
26 Sheeran PW, Rose JB, Fazi LM, Chiavacci R, McCormick L. Rofecoxib
50
Paediatr Anaesth 2004;14(7): 579- 583.
27. Hamunen K, Kontinen V. Systematic review on analgesics given for pain
following tonsillectomy in children. Pain 2005;117(1-2):40-50.
28. Keidan I, Zaslansky R, Eviatar E, Segal S, Sarfaty SM. Intraoperative
ketorolac is an effective substitute for fentanyl in children undergoing outpatient adenotonsillectomy. Paediatr Anaesth2004;14(4):318-323.
29. Moiniche S, Romsing J, Dahl J, Tramer M. Nonsteroidal
antiinflammatory drugs and the risk of operative site bleeding after tonsillectomy: a quantitative systematic review.
AnesthAnalg2003;96:68-77
30. Cardwell M, Siviter G, Smith A. Non-steroidal anti-inflammatory drugs
and perioperative bleeding in paediatric tonsillectomy. Cochrane
Database Syst Rev 2005(2):CD003591. Carre P, Joly A, Cluzel Field B, Wodey E, Lucas M, Ecoffey C. Axillary block in children:
single or multiple injection? Paediatr Anaesth 2000;10(1):35-39
31. Cardwell M, Siviter G, Smith A. Non-steroidal anti-inflammatory drugs
and perioperative bleeding in paediatric tonsillectomy. Cochrane Database Syst Rev 2005(2):CD003591
32. Marret E, Flahault A, Samama C, Bonnet F. Effects of postoperative,
nonsteroidal,antiinflammatory drugs on bleeding risk after tonsillectomy: meta-analysis of randomized,controlled trials. Anesthesiology
51
33. Hollis LJ, Burton MJ, Millar JM. Perioperative local anaesthesia for
reducing pain following tonsillectomy. Cochrane Database Syst Rev 2000(2):CD001874.
34. Akoglu E, Akkurt BC, Inanoglu K, Okuyucu S, Dagli S. Ropivacaine
compared to bupivacaine for post-tonsillectomy pain relief in children: a randomized controlled study. Int J Pediatr Otorhinolaryngol
2006;70(7):1169-1173.
35. Park AH, Pappas AL, Fluder E, Creech S, Lugo RA, Hotaling A. Effect
of perioperative administration of ropivacaine with epinephrine on postoperative pediatric adenotonsillectomy recovery.Arch Otolaryngol Head Neck Surg 2004;130(4):459-464
36. Hung T, Moore-Gillon V, Hern J, Hinton A, Patel N. Topical bupivacaine
in paediatric day-Case tonsillectomy: a prospective randomized controlled trial. J Laryngol Otol 2002;116:33-36.
37. Elhakim M, Khalafallah Z, El-Fattah H, Farouk S, Khattab A. Ketamine
reduces swallowingevoked pain after paediatric tonsillectomy. Acta Anaesthesiol Scand 2003;47(5):604-609.
52
38. O'Flaherty J, Lin C. Does ketamine or magnesium affect.
posttonsillectomy pain in children? Paediatr Anaesth 2003;13(5):413- 421.
39. Umuroglu T, Eti Z, Ciftci H, Yilmaz Gogus F. Analgesia for
adenotonsillectomy in children: a comparison of morphine, ketamine and tramadol. Paediatr Anaesth 2004;14(7):568-573
40. Kohler H, Schulz S, Wiebalck A. Pain management in children:
assessment and documentation in burn units. Eur J Pediatr Surg 2001;11(1):40-43.
41. Falanga IJ, Lafrenaye S, Mayer SK, trault JP. Management of acute pain
in children: Safety and efficacy of a nurse-controlled algorithm for pain relief. Acute Pain 2006;8:45-54.
42. Hicks C, von Baeyer C, Spafford P, van Korlaar I, Goodenough B.
The Faces Pain Scale- Revised:toward a common metric in pediatric pain measurement. Pain 2001;93:173-183.
43. Goodenough B, Addicoat L, Champion G, McInerney M, Young B,
Juniper K, Ziegler J. Pain in 4-to 6-year-old children receiving intramuscular injections: a comparison of the Faces Pain Scale with other self-report and behavioral measures. Clin J Pain 1997;13(1):60-73
53
44. Hunter M, McDowell L, Hennessy R, Cassey J. An evaluation of the Faces
Pain Scale with young children. J Pain Symptom Manage 2000;20:122- 129.
45. Hester N. The preoperational child's reaction to immunizations. Nurs Res
1979;28:250- 255.
46. Hester NO, Foster R, Kristensen K. Measurement of Pain in Children –
Generalizability and Validity of the Pain Ladder and the Poker Chip Tool. Advances in Pain Research and Therap1990;15:79-84
47 Merkel S, Voepel-Lewis T, Shayevitz J, Malviya S. The FLACC: a
behavioral scale for scoring postoperative pain in young children. Pediatr Nurs 1997;23(3):293-297.
48. Voepel-Lewis T, Malviya S, Merkel S, Tait AR. Behavioral pain assessment and the Face, Legs,Activity, Cry and Consolability instrument. Expert Review of Pharmacoeconomics and
Outcomes Research 2003;3(3):317-325.
49.Voepel-Lewis TMSN, Malviya SMD, Merkel SMSN, Tait ARP. Reliability
and Validity of the FLACC Behavioral Scale as a Measure of Pain in Cognitively Impaired Children. Anesthesiology2001;95(3A):A1229.
54
50. Malviya S, Voepel-Lewis T, Burke C, Merkel S, Tait AR. The revised
FLACC observational pain tool: Improved reliability and validity for pain assessment in children with cognitive . impairment. Paediatric Anaesthesia 2006;16:258-265.
51 Manworren RCB, Hynan LS. Clinical Validation of FLACC: Preverbal
Patient Pain Scale Pediatric Nursing 2003;29:140-146.
52. McGrath P, Johnson G, Goodman J, Schillinger j, Dunn J, Chapman J
CHEOPS: A behavioral scale for rating postoperative pain in children. In: H Fields, R Dubner, F Cervero, editors Advances in Pain Research and Therapy. 1985; 9: 395-402
53. Splinter WM, Semelhago LC, Chou S. The Reliability and Validity of a
Modified Cheops Pain Score. Anesthesia and Analgesia 1994;78(2): U220-U220.
54.Stinson J, Kavanagh T, Yamada J, Gill N, Stevens B. Systematic review of the psychometric properties,interpretability and feasibility of self-report pain intensity measures for use in clinical trials in children and adolescents. Pain 2006;125(1-2):143-157.
55. Von Baeyer C. Children's self-reports of pain intensity: scale selection, limitations and interpretation.Pain Res Manag 2006a;11(3):157-162.
55
56. Von Baeyer C, Spagrud L. Systematic review of observational (behavioral) measures of pain for children and adolescents aged 3 to 18 years. Pain 2007;127(1-2):140-150.
57.Buttner W, Fincke W. Analysis of behavioural and physiological parameters for the assessment of postoperative analgesic demand in newborns, infants and young children. Paediatri Anaesthesia 2000;10:303-318.
58. van Dijk M, de Boer J, Koot H, Tibboel D, Passchier J, Duivenvoorden H.
The reliability and validity of the COMFORT scale as a postoperative pain instrument in 0 to 3-year-old infants.Pain 2000;84(2-3):367-377.
56
ALLEGATI
ALLEGATO I
0 2 4 6 8 10
NIENTE UN PO’ UN PO’ PIU’ ANCORA PIU’ MOLTO MOLTISSIMO
57 ALLEGATO II SCALA CHEOPS GRIDA-PIANTO Assenti 1 Gemiti-pianti 2 Pianto vigoroso 3
ESPRESSIONE DEL VOLTO Sorride 0
Neutro 1
Smorfie 2
VERBALIZZAZIONE Parla di tutto 0
Non parla 1
Si lamenta di altro 1
Si lamenta di dolore 2
ATTEGGIAMENTO CORPOREO Corpo in riposo 1
Agitazione,rigidità,movimenti disordinati
2
In piedi sul letto 2
DESIDERIO DI TOCCARSI LA FERITA
nessuno 1
Molto forte 2
ARTI INFERIORI A riposo 1
movimenti incessanti,da colpi con piedi
2
Si accovaccia,si inginocchia,in piedi
58 ALLEGATO III
VALUTAZIONE DEGLI STUDI
Gli studi di efficacia o altri studi che riportano dati di efficacia sono stati valutati e classificati per qualità utilizzando il sistema di classificazione raccomandato dallo Scottish Intercolleageate Guideline Network (SIGN), qui di seguito riportato:
LIVELLI DI EVIDENZA
Level 1
1++
Metanalisi di alta qualita, revisioni sistematiche di RCT, o RCT con un rischio molto basso di bias
1+
Metanalisi ben condotte, revisioni sistematiche di RCT o RCT con un rischio basso di bias
1 -
Metanalisi, revisioni sistematiche di RCT o RCT con un alto rischio di bias
Level 2
2++
Revisioni sistematiche di alta qualita di studi di coorte o ”case-control”. Studi “case-control”o di
coorte di alta qualita con un rischio molto basso di: contenere errori, bias o possibilita o alta
probabilita che la relazione sia causale 2+
Studi caso-controllo o di coorte ben condotte con un rischio basso di: contenere errori, bias o
possibilita o moderata probabilita che la relazione sia causale 2 -
Studi caso-controllo o di coorte ben condotte con un alto rischio di: contenere errori, bias o
possibilita o rischio significativo che la relazione non sia causale
Level 3
Studi non analitici, ad esempio case report, case series Level 4 Opinione di un esperto
59
ALLEGATO IV
GRADO DELLE RACCOMANDAZIONI Grado A
Almeno una metanalisi, revisione sistematica o RCT valutata come 1++ e direttamente applicabile alla popolazione considerata; oppure
una revisione sistematica di RCT o un insieme di evidenze costituite soprattutto da studi valutati come 1+ , direttamente applicabili alla popolazione considerata e dimostranti una coerenza complessiva dei risultati.
Grado B
Evidenze comprendenti studi valutati come 2++ o meglio, direttamente applicabili alla popolazione considerata e dimostranti una coerenza complessiva dei risultati.
Evidenze estrapolate da studi valutati come 1++ o 1+
Grado C
Evidenze comprendenti studi valutati come 2+ o meglio, direttamente applicabili alla popolazione considerata e dimostranti una coerenza complessiva dei risultati.
Evidenze estrapolate da studi valutati come 2++
Grado D
Evidenze di livello 3 o 4
Evidenze estrapolate da studi valutati come 2+
60
RINGRAZIAMENTI
Si ringrazia il Professore Giunta E il Dottore De Masi