1 INDICE
1. Riassunto pag. 2 2. Introduzione pag. 6
2.1. Epidemiologia pag. 6 2.2. Anatomia patologica pag. 10 2.3. Vie di diffusione pag. 17 2.4. Diagnosi precoce pag. 18 2.5. Diagnosi clinica e sintomatologia pag. 20 2.6. Stadiazione e prognosi pag. 21 2.7. Terapia pag. 29 2.8. Follow-up pag. 44 2.9. Linee guida pag. 51 3. Obiettivo della tesi pag. 56 4. Materiali e metodi pag. 57 5. Risultati pag. 58 6. Discussione e conclusioni pag. 61 7. Bibliografia pag. 66 8. Appendice pag.96
2 1. Riassunto
Il carcinoma endometriale è il quarto tumore per incidenza nella popolazione femminile in Europa, dopo il carcinoma della mammella, del colon-retto e del polmone.
Il trattamento standard consiste nella chirurgia rappresentata dall’isterectomia totale con annessiectomia bilaterale +/- linfadenectomia, mentre la terapia adiuvante, è usualmente somministrata alle pazienti a medio e alto rischio. La più alta probabilità di recidiva per il carcinoma endometriale si ha entro i primi 36 mesi dalla diagnosi con percentuali variabili dall’11 al 19%.
Lo scopo di questa tesi è stato l’ analisi delle recidive in pazienti sottoposte a chirurgia primaria con o senza trattamento adiuvante per carcinoma endometriale.
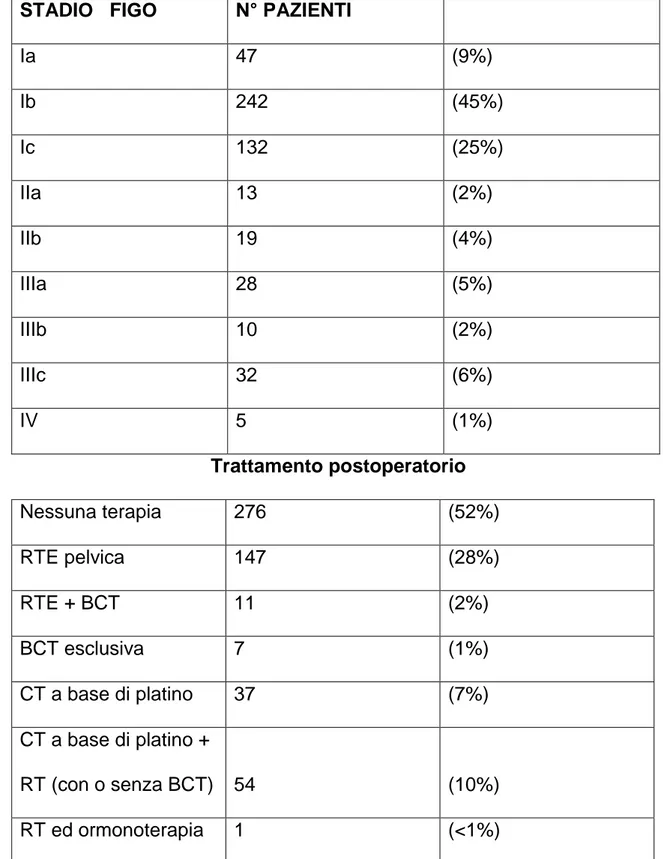
Tra il Maggio 1987 e il Dicembre 2009, 533 pazienti con carcinoma dell’endometrio sono state sottoposte a laparotomia, citologia peritoneale, isterectomia totale e salpingo-ovariectomia bilaterale con (n.295) o senza (n.238) linfadenectomia pelvica +/- lombo-aortica. L’ età media delle pazienti era 61 anni (range, 33-92 anni). Per quanto riguarda il trattamento adiuvante, 276 pazienti non hanno ricevuto alcun trattamento postoperatorio, 147 sono state sottoposte a radioterapia esterna pelvica adiuvante (seguita da brachiterapia in 11 casi), 7 sono state sottoposte a brachiterapia esclusiva, 37 a chemioterapia a base di platino, 54 hanno
3 eseguito un trattamento combinato di chemioterapia a base di platino e radioterapia esterna pelvica, 1 paziente ha ricevuto radioterapia ed ormonoterapia. Le pazienti sono state seguite fino a Luglio 2010 o fino ad un eventuale decesso.
Ottantasei pazienti (16.1%) hanno sviluppato recidiva di malattia dopo un tempo mediano di 18.5 mesi (range 2.3 – 129.1 mesi). La recidiva è stata loco-regionale in 14 casi (16.3%), a distanza in 38 casi (44.2%), sia loco- regionale che a distanza in 12 casi (13.9%); inoltre in 22 (25.2%) casi la recidiva è stata a livello dei linfonodi pelvici e lombo aortici.
All’ analisi univariata la sopravvivenza libera da progressione era significativamente correlata all’ età (≤ 61 anni versus >61 anni, p= 0.01), allo stadio ( I - II versus III - IV, p<0.0001), allo stato degli spazi linfovascolari (positivi versus negativi versus sconosciuto, p<0.0001), al grado di infiltrazione miometriale (<50% versus ≥ 50%, p<0.0001), al grado istologico (ben differenziato + moderatamente differenziato versus scarsamente differenziato, p<0.0001), allo stato linfonodale (linfonodi istologicamente negativi versus positivi versus linfonodi non esaminati, p<0.0001), al tipo istologico (endometrioide versus non endometrioide, p< 0,0001), all’ aver eseguito un trattamento adiuvante (effettuato versus non effettuato, p<0.0001).
La sopravvivenza globale era correlata allo stadio, allo stato degli spazi linfovascolari, al grado di infiltrazione miometriale, al grado istologico, allo stato linfonodale, al tipo istologico, al trattamento adiuvante.
4 All’ analisi multivariata l’ interessamento degli spazi vascolari (p=0.009) ed il grado istologico scarsamente differenziato (p<0.0001) sono fattori predittivi indipendenti per il rischio di recidiva.
Infatti le pazienti con interessamento degli spazi linfo-vascolari e tumori scarsamente differenziati hanno un rischio di sviluppare una recidiva rispettivamente di 2.512 volte e 2.774 volte superiore rispetto a quelle con spazi vascolari negativi e tumori ben o moderatamente differenziati. Per quanto riguarda la sopravivenza globale il grado istologico scarsamente differenziato (p= 0.001) e l’invasione miometriale profonda (p= 0.001) erano fattori prognostici indipendenti di sopravvivenza all’analisi multivariata. Infatti le pazienti che hanno un’ invasione miometriale > 50% e un tumore scarsamente differenziato hanno rispettivamente un rischio di morte di 3.813 volte e 3.169 volte superiore rispetto a quelle con invasione miometriale < 50% e un tumore ben o moderatamente differenziato.
Le pazienti con un tumore scarsamente differenziato, interessamento degli spazi linfovascolari, invasione miometriale profonda hanno la necessità di un trattamento adiuvante post-operatorio. In queste pazienti sono stati recentemente programmati studi che prevedono randomizzazione che confronta la radioterapia esterna versus la radioterapia associata a chemioterapia quale trattamento adiuvante. Tuttavia i risultati di recenti studi sembrano consigliare di classificare l’invasione miometriale come terzo interno, terzo medio e terzo esterno.
5 Le pazienti con tumore dell’endometrio di tipo endometrioide in fase iniziale con invasione del terzo esterno del miometrio e/o interessamento degli spazi linfo-vascolari dovrebbero essere incluse in studi randomizzati disegnati per valutare il ruolo della chemioterapia adiuvante sola o in combinazione con la radioterapia esterna pelvica sequenziale e/ o concomitante.
6 2. Introduzione
2.1. Epidemiologia
Il carcinoma dell’endometrio è la neoplasia ginecologica più comune nel mondo occidentale, essendo responsabile del 6% dei tumori nel sesso femminile. Ogni anno i casi di carcinoma endometriale ed i decessi per questa neoplasia sono, rispettivamente, 142˙000 e 42˙000 nel mondo e 5˙000 e 1˙700 in Italia. Secondo i dati dell’Annual Report n. 26 della Federazione Internazionale dei Ginecologi ed Ostetrici, la sopravvivenza globale a 5 anni è dell’80% (1).
Tuttavia è stata osservata una differenza di tipo razziale in sopravvivenza a 5 anni che è dell’80.8% per le donne over 65 di razza bianca e solo del 53.3% per le donne di razza nera appartenenti allo stesso gruppo d’età. Non è chiaro se l’alta mortalità nelle donne di razza nera sia legata ad un ritardo diagnostico, alla mancanza di accesso alle cure o alla presenza di una malattia biologicamente più aggressiva. Infatti solo il 52% delle donne di razza nera sopra i 50 anni presenta una malattia in I stadio rispetto al 73% di quelle di razza bianca della stessa età.
L’incidenza globale del carcinoma dell’endometrio è in aumento parallelamente all’ incremento dell’ aspettativa di vita del mondo femminile (2).
Attualmente nei quasi tre quarti dei casi la diagnosi viene fatta quando il tumore è limitato ancora al corpo uterino (139).
7 Nonostante questa favorevole distribuzione in stadi (stadio I: 72%, stadio II: 12%, stadio III: 13%, stadio IV: 3%) la neoplasia rappresenta l’ottava causa di morte tra le donne (140).
Sono state descritte due varianti anatomo-patologiche: il carcinoma endometrioide di tipo 1 è estrogeno dipendente, insorge frequentemente su un’iperplasia ed ha prognosi generalmente favorevole; il carcinoma non endometrioide di tipo 2, comprendente gli istotipi sieroso-papillifero e a cellule chiare, non è estrogeno dipendente, insorge su un endometrio atrofico, ha aggressività biologica molto elevata e prognosi sfavorevole. Nella tabella 1 sono riportate le principali caratteristiche cliniche ed istopatologiche delle due varianti del carcinoma dell’ endometrio.
L’ iperplasia endometriale costituisce il risultato di una crescita eccessiva dell’ endometrio in risposta a stimoli ormonali. Dal 1990 la Società Internazionale dei Patologi ginecologi ha proposto una classificazione che tiene conto sia degli aspetti architetturali (affollamento e complessità delle ghiandole) sia degli aspetti citologici (atipie cellulari).
Microscopicamente è l’ aumento del numero delle ghiandole che determina il quadro noto come iperplasia ghiandolare semplice. Le ghiandole assumono forma variabile, talora sono dilatate (iperplasia
ghiandolare cistica o semplice) per ostruzione dei dotti ghiandolari. In
qualche caso l’ iperplasia è caratterizzata da una pluristratificazione dell’ epitelio, aumento delle ghiandole rispetto allo stroma, gittate epiteliali verso lo stroma ancora contenuti dalla membrana basale, nuclei più scuri
8 (iperplasia adenomatosa o complessa); l’ iperplasia atipica ha delle atipie con ghiandole che mostrano aumento nucleolare, pleomorfismo, accumuli di cromatina, nucleolo prominente; l’ epitelio è stratificato con perdita di polarità ed una elevata attività mitotica.
L’ iperplasia atipica è il precursore morfologico del carcinoma endometrioide. (141).
Nella tabella 3 si riporta la classificazione della iperplasia endometriale secondo l’Organizzazione Mondiale della Sanità (8).
Frequentemente, in presenza di una iperplasia endometriale atipica, si trova un’area di adenocarcinoma non ancora diagnosticato (2).
ASPETTI MACROSCOPICI
Il carcinoma dell’ endometrio si presenta in due forme:
- la forma circoscritta appare come una formazione polipoide o una ulcerazione o un rilievo nodulare limitato ad una zona precisa dell’ endometrio. Frequenti necrosi ed emorragie.
- la forma diffusa occupa gran parte dell’ utero. È la conseguenza di un’ origine multicentrica del tumore oppure rappresenta l’ evoluzione di una forma nata come circoscritta. L’ infiltrazione del miometrio che è più frequente nelle forme ulcerate può esserci pure in quelle diffuse.
9 Tabella 1 : Caratteristiche cliniche ed istopatologiche principali dei due tipi di carcinoma endometrioide
Caratteristiche principali
Tipo I
(estrogeno correlato)
Tipo II
(da endometrio atrofico)
Anovulazione Presente Assente
Fertilità Ridotta Assente
Epoca alla diagnosi Perimenopausale Menopausa tardiva Endometrio peritumorale Iperplastico Atrofico
Obesità Spesso presente Assente
Diabete mellito Spesso presente Assente Tipo istologico Prevalentemente
endometrioide
Spesso sieroso, a cellule chiare, indifferenziato Grading > 80% G1-G2 > 60% G3
Invasione miometriale Superficiale Profonda Interessamento linfatico Raro Frequente
P 53 Iperespressa Rara Frequente
10
2.2 Anatomia patologica
L’adenocarcinoma endometrioide è il più comune tipo istologico di carcinoma dell’endometrio (75%). È alta la somiglianza con l’ epitelio ghiandolare dell’ endometrio. Si tratta per lo più di forme ben differenziate con ghiandole rivestite da cellule contenenti scarsa mucina. Man mano che la differenziazione diminuisce aumentano le aree solide nell’ epitelio.
Si parla di adenoacantoma (10% dei casi) quando la componente squamosa non presenta atipie mentre la componente ghiandolare ha caratteri di malignità.
Si definisce infine carcinoma squamoadenomatoso o adenosquamoso la lesione in cui sia la componente ghiandolare che quella squamosa mostrano segni di atipia; questo tumore sorge spesso su un terreno infiammatorio (piometra, endometrite) o di metaplasia squamosa endometriale con una prognosi sfavorevole.
Altre varietà:
- l’adenocarcinoma secernente mucina (simile all’adenocarcinoma cervicale)
- il carcinoma a cellule argirofile, rarissimo, formato da cellule contenenti dopamina.
11 Si distingue un grado architetturale ed uno nucleare:
- il grading architetturale si basa sulla proporzione di tumore che forma ghiandole e quella che invece forma nidi solidi: i tumori ben differenziati (G1) hanno una crescita prevalentemente ghiandolare, quelli scarsamente differenziati (G3) hanno una crescita prevalentemente come nidi solidi.
- Il grading nucleare: il tumore G1 ha nuclei ovali, poca cromatina , piccoli nucleoli; il tumore G3 ha pleomorfismo nucleare, accumuli di cromatina, nucleoli ben evidenti.
Secondo la classificazione FIGO i gradi sono tre (G1, G2, G3). I tumori G1 hanno prognosi migliore (3).
Grado1 (G1) :
ben differenziato con il 95% o più di struttura ghiandolare e/o papillare. (componente non squamosa o con aspettosolido non morulare della proliferazione inferiore al 5%).
Grado2 (G2)
: moderatamente differenziato. (dal 6% al 50% di aspettinon squamosi e/o solidi non morulari).
Grado3 (G3) :
oltre il 50% di aspetti non squamosi o solidi non morulari.12 Una importante atipia nucleare aumenta di un punto il grado istologico. Nel tumore sieroso-papillifero, carcinoma a cellule chiare e a cellule squamose, il grado nucleare è più importante di quello architetturale. Inoltre gli adenocarcinomi con differenziazione di tipo squamosa sono classificati secondo il grado nucleare della componente ghiandolare. Il carcinoma sieroso-papillifero è un tumore aggressivo, con una propensione per l’ invasione miometriale profonda e l’ interessamento linfonodale. Questo tumore ha la caratteristica architettura papillare ricoperta da cellule maligne che mostrano un considerevole pleomorfismo nucleare e anomala attività mitotica. Ha grado nucleare 2 o 3 e diffonde precocemente nella cavità peritoneale.
Nel carcinoma endometrioide sono state identificate anomalie genetiche quali instabilità dei microsatelliti, mutazioni dei geni PTEN, k-RAS e della β-catenina, mentre il carcinoma sieroso-papillifero presenta mutazioni a carico del gene p53 e perdita di eterozigosi di alcuni cromosomi. Inoltre il carcinoma non endometrioide può svilupparsi dalla dedifferenziazione di un precedente carcinoma endometrioide.
In alcuni casi il tumore presenta sovrapposizioni cliniche, morfologiche, immunoistochimiche e molecolari dei due tipi (5, 7).
Relativamente all’ espressione della β-catenina nel carcinoma endometrioide, la positività immunoistochimica è risultata essere nucleare
13 e citoplasmatica, mentre nell’ endometrio sano essa è risultata essere prevalentemente di membrana. L’ aumento dei livelli nucleari della β-catenina sarebbe responsabile dell’ attivazione di alcuni geni coinvolti nella proliferazione cellulare. Pertanto la mutazione della β-catenina rappresenterebbe un primo step della carcinogenesi endometriale; in analogia al carcinoma del colon, più geni potrebbero essere potenziati dalla disregolazione del pathway della β-catenina. (142, 143)
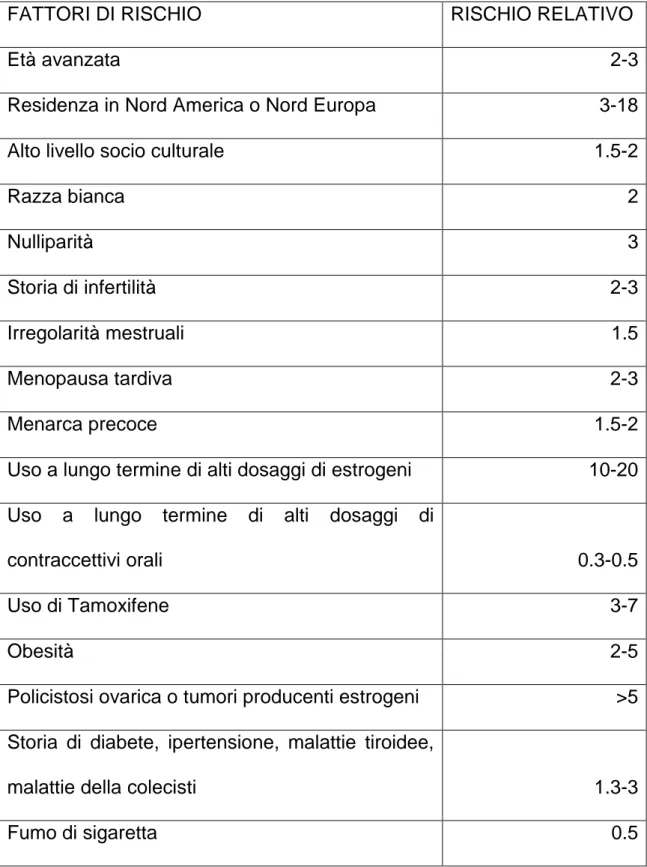
FATTORI DI RISCHIO
I fattori di rischio per il carcinoma endometroide comprendono: - menarca precoce
- menopausa tardiva - nulliparità e bassa parità
- iperestrogenismo abituale con cicli anovulatori (sindrome dell’ovaio policistico)
- diabete - ipertensione - obesità
14 - sindrome di Lynch II (sindrome cancerosa ereditaria a trasmissione autosomica dominante con maggior frequenza di neoplasie colon-rettali e dell’ endometrio)
- terapia estrogenica non associata alla somministrazione di progestinici (come succede nelle pazienti affette da disgenesia gonadica che vengono trattate dalla pubertà in poi)
- terapia con Tamoxifene nelle pazienti già trattate per cancro mammario
- tumori ovarici della granulosa e della teca estrogeno secernenti - immunodeficienza
Sono noti anche dei fattori protettivi: - multiparità
- menopausa precoce
- uso di terapia contraccettiva orale - fumo di sigaretta
- menarca precoce e menopausa tardiva: aumentano il rischio per l’aumentato periodo di esposizione agli estrogeni
- nulliparità (e bassa parità): aumentano il rischio perché queste pazienti sono esposte continuamente (o comunque per un lungo periodo) ad un tono estrogenico elevato e pertanto l’ endometrio è
15 sottoposto ad una stimolazione continuativa in conseguenza della fisiologica ciclicità ovarica.
- diabete: gli estrogeni modulano anche l’ attività di diversi fattori di crescita come le IGF; esse si legano a specifici recettori endometriali stimolandone la proliferazione. A contrastare questo meccanismo vi sono le IGF-BP, stimolate dal progesterone e inibite dall’ insulina. Quindi alti livelli di progesterone determinano aumento delle IGF-BP; queste legano le IGF ed impediscono pertanto il loro effetto mitogeno sull’ endometrio. L’insulina ha effetto opposto perché, come detto, inibisce e blocca le IGF-BP; perciò una donna con diabete di tipo II (e quindi iperinsulinemica) ha un rischio più alto di sviluppare il cancro.
- obesità: nelle pazienti obese si hanno livelli più alti di estrogeni rispetto ai controlli sani: questo perché una quota parte di androstenedione (ovarico e surrenalico) viene convertita a livello del tessuto adiposo in estrone (mediante una reazione di aromatizzazione). In condizioni normali la maggior parte dell’ estrone circola legato alla SHBG (una globulina sintetizzata dal fegato), pertanto la sua quota libera è ridotta cosi come la sua attività di stimolazione sull’ endometrio. Le donne obese hanno livelli più bassi di SHBG e in conseguenza hanno un aumento dell’ estrone libero circolante.
16 - terapia estrogenica non associata ad un progestinico: condizione in cui aumenta il rischio di sviluppare il carcinoma in relazione alla dose ed alla durata di assunzione. I progestinici hanno un effetto protettivo, riducendo il numero di recettori per estrogeni e promuovendo maturazione e differenziazione cellulare. Essi hanno un’azione antimitotica ed inibente la crescita.
- tamoxifene: è utilizzato nella ormonoterapia adiuvante del carcinoma mammario; il suo impiego aumenta il rischio di sviluppare un carcinoma dell’ endometrio: infatti la sua è un’ azione antiestrogena a livello della mammella ma ha un’ azione estrogeno-simile a livello dell’ endometrio.
- contraccettivi orali: gli estro-progestinici riducono il rischio di cancro perché la paziente assume per 21 giorni sia estrogeni che progesterone; invece fisiologicamente nel ciclo mestruale la copertura progestinica si ha solo per le due settimane post-ovulatorie.
17
2.3. Vie di diffusione
Il carcinoma dell’endometrio diffonde per continuità, contiguità (miometrio, cervice, annessi, vagina e, più raramente, vescica e retto), per via linfatica e per via ematogena (3, 7).
Il miometrio può essere eroso sino alla sierosa e ciò rende conto di uno sfaldamento di cellule neoplastiche in peritoneo.
La diffusione per via linfatica, più frequente di quella che si ha per via ematica, avviene lungo tre vie principali:
- la prima, attraverso i legamenti infundibulo-pelvici ed arriva ai linfonodi para-aortici;
- la seconda, attraverso i legamenti larghi ed i parametri e giunge ad i linfonodi otturatori ed ipogastrici, iliaci esterni, comuni e para- aortici;
- la terza, segue i legamenti rotondi ed arriva ai linfonodi inguinali superficiali. (3, 9-10,11).
La diffusione per via linfatica può inoltre arrivare a coinvolgere il fondo vaginale o il terzo inferiore della parete vaginale anteriore nella zona sottouretrale (1).
Le metastasi per via ematogena avvengono piuttosto tardivamente e coinvolgono il polmone (2-3% dei casi), il fegato, le ossa, la vagina per via venosa retrograda e altri organi e, assieme a quelle per via linfatica, sono tanto più frequenti quanto meno è differenziato il tumore e quanto
18 più invade in profondità il miometrio. Rare invece le metastasi cerebrali (3).
2.4. Diagnosi precoce
Attualmente non esistono metodi di screening efficaci per il carcinoma dell’ endometrio. La citologia cervico-vaginale secondo Papanicolau non ha alcun ruolo nella diagnosi di carcinoma endometriale. Questo, comunque, può essere sospettato quando si trovano cellule endometriali atipiche nella citologia di donne non gravide in qualsiasi età, e quando cellule endometriali sono rilevate in donne in postmenopausa che non assumono estrogeni (3).
La mucosa endometriale può essere prelevata per aspirazione con dispositivo tipo Vabra (cannula metallica o di plastica che abrade ed aspira con l’estremità distale aperta e ricurva mentre il materiale viene poi condotto in un contenitore attraverso un filtro in collegamento con l’estremità distale) o per abrasione (scraping) per mezzo di un apparecchio dotato di fibre di nylon o di alette di polietilene. Con queste tecniche si può fare il prelievo ambulatorialmente spesso evitando la presenza dell’ anestesista.
19 In presenza di aspetti citologici o di quadri istologici atipici dopo prelievo per scraping o per aspirazione, vi è indicazione all’isteroscopia.
Per quanto riguarda l’utilizzo dell’ecografia pelvica con sonda transvaginale questa può mettere in evidenza l’iperplasia indotta dagli estrogeni nelle donne in postmenopausa (spessore >4 mm) le quali dovrebbero invece avere un endometrio atrofico (spessore ≤4 mm) e l’utilizzo in associazione della flussimetria con il color Doppler potrebbe inoltre migliorare l’accuratezza dell’indagine e ridurre i falsi positivi. Inoltre l’ ecografia transvaginale valuta elementi prognostici quali infiltrazione miometriale, interessamento cervicale, e l’ eventuale presenza di metastasi annessiali. Attualmente si ritiene che, in alcuni casi, l’ accuratezza dell’ ecografia transvaginale è paragonabile a quella della risonanza magnetica.
20
2.5. Diagnosi clinica e sintomatologia
Il 90% delle pazienti con carcinoma dell’endometrio presenta un anomalo sanguinamento vaginale, ma in casi con stenosi cervicale la neoplasia può presentarsi con ematometra o piometra. Nelle donne in premenopausa un anomalo sanguinamento uterino spesso si associa a menorragia.
È importante che le pazienti sappiano che una perdita ematica, se compare al di fuori del periodo mestruale e ancor di più se compare in post-menopausa, può rappresentare il primo segno di un carcinoma endometriale.
Un’ altra manifestazione possibile della neoplasia è la leucoxantorrea dovuta a fenomeni di congestione che si associano al tumore e talora a fatti di necrosi e colliquativi che si verificano nelle vegetazioni neoplastiche. A volte si tratta di perdite bianco giallastre maleodoranti. Il dolore compare tardivamente e quando la neoplasia coinvolge organi pelvici addominali (sigma, intestino tenue, vescica e retto). In fase precoce il dolore può essere legato alla sovradistensione uterina da parte delle vegetazioni tumorali e alle contrazioni uterine che tale sovradistensione risveglia.
21
2.6. Stadiazione e prognosi
Nel 1988 la Federation International of Gynecology and Ostetrics [FIGO] Committee on Gynecologic Oncology ha cambiato la stadiazione del carcinoma dell’endometrio da una stadiazione clinica ad una chirurgica-patologica richiedente un accurato esame istopatologico del pezzo chirurgico per valutare la reale estensione della malattia e per definire una serie di variabili prognostiche (7).
Un’ accurata stadiazione chirurgica mostra che il 15-20% delle pazienti con tumore apparentemente confinato al corpo dell’utero ha in realtà un’estensione subclinica della malattia alla cervice, annessi, linfonodi o peritoneo (7, 12). Per quanto riguarda il work-up preoperatorio, la paziente deve eseguire:
• Rx torace
• Eco addome/pelvi per escludere i rari casi di pazienti con evidenza clinica di diffusione a distanza.
• TC e/o RM per poter valutare infiltrazione del miometrio, stato dei linfonodi, eventuale presenza di malattia peritoneale e/o epatica. Il ricorso a queste indagini è comunque opzionale.
Ulteriori indagini (cistoscopia, colonscopia, PET) possono essere eseguite su precisa indicazione clinica.
Il sistema di stadiazione FIGO (1988) prevede un’ accurata valutazione chirurgica, pertanto le pazienti con carcinoma endometriale devono
22 essere sottoposte a terapia chirurgica primaria ad eccezione dei rari casi che presentano, alla valutazione iniziale, una diffusione istologica confermata alla vescica e/o al retto o metastasi a distanza.
La chirurgia deve rappresentare il momento terapeutico principale in ogni paziente in cui la neoplasia sia aggredibile chirurgicamente.
Al momento dell’apertura dell’addome occorre praticare l’aspirazione del fluido peritoneale libero e/o, in sua assenza, fare il lavaggio peritoneale della pelvi su cui effettuare l’esame citologico; accurata esplorazione dell’omento e dei visceri addominali e la biopsia di ogni lesione sospetta a questo livello; la biopsia dei linfonodi pelvici e/o lombo-aortici se esiste alla diagnostica per immagini preoperatoria o alla palpazione intraoperatoria il sospetto di metastasi linfonodali (3).
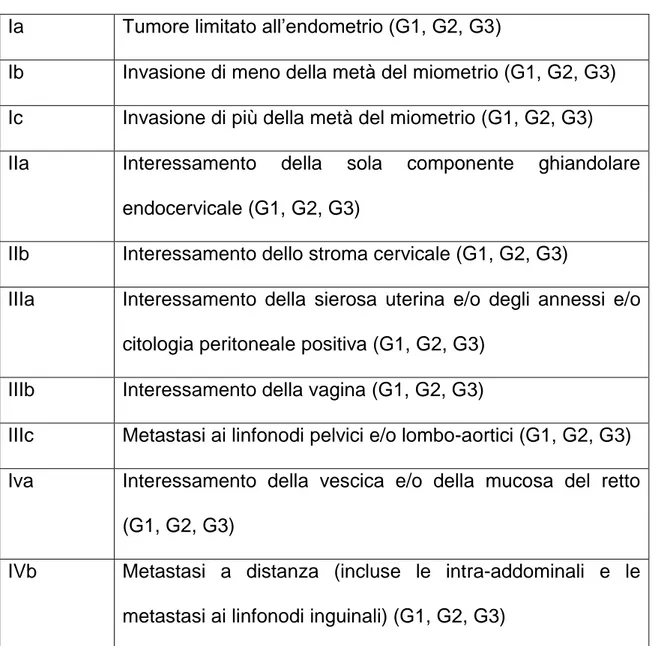
Nella tabella 4 si riporta la stadiazione chirurgica del carcinoma dell’endometrio secondo la FIGO.
La sopravvivenza a 5 anni secondo i dati dell’Annual Report n. 26, è del 90.8% per le pazienti in stadio Ia, 91.1% per lo stadio Ib, 85.4% nello stadio Ic, 83.3% per lo stadio IIa, 74.2% per lo stadio IIb, 66.2% per lo stadio IIIa, 49.9% per lo stadio IIIb, 57.2% per lo stadio IIIc, 25.5% per lo stadio IVa, e 20.1% per il IVb (1).
La sopravvivenza, per ogni stadio, correla col grado di differenziazione e con l’istotipo. Per esempio la sopravvivenza a 5 anni è del 92.9% per il G1, 89.9% per il G2 e 78.9% per il G3. Inoltre la sopravvivenza a 5 anni risultava essere dell’83.2% per il carcinoma endometrioide, 80.6% per
23 l’adenosquamoso, 52.6% per il carcinoma sieroso-papillifero e 62.5% per il carcinoma a cellule chiare. La prognosi sfavorevole di questi ultimi due tipi istologici dipende dal loro comportamento biologico aggressivo e, in particolare, dall’alta frequenza di diffusione extra-uterina (13, 14). Rispetto all’adenocarcinoma endometrioide, il carcinoma sieroso- papillifero è associato a più frequente invasione linfatica, invasione profonda del miometrio, metastasi ai linfonodi e peggiore sopravvivenza. La neoplasia è considerata avere una cattiva prognosi anche in assenza di invasione profonda del miometrio o di metastasi linfonodali (7).
Questi dati sono stati confermati da Cirisano e coll. (14) che hanno confrontato la sopravvivenza e le recidive nello stadio I-II dei carcinomi sieroso-papillifero, cellule chiare ed endometrioide.
Nel tumore endometrioide la sopravvivenza è risultata essere direttamente correlata all’invasione del miometrio mentre negli istotipi sieroso-papillifero e a cellule chiare può essere infausta indipendentemente dalla profondità di invasione. Una biologia più aggressiva nel sieroso-papillifero (36%) e nel tumore a cellule chiare (44%) rispetto al tumore endometrioide di alto grado (19%) sembra correlare con una più alta frequenza di diffusione intra-addominale disseminata. Tutte queste caratteristiche riflettono l’alto tasso di recidive nel tumore sieroso-papillifero (38%) e in quello a cellule chiare (22%) rispetto all’endometrioide (9%) con una sopravvivenza del 56% per i primi due istotipi allo stadio chirurgico I-II rispetto all’ 80% dell’endometrioide.
24 L’interessamento linfonodale è correlato ad alcune variabili patologiche quali il grado istologico, l’invasione miometriale, il tipo istologico, l’interessamento degli spazi linfo-vascolari, le dimensioni del tumore, l’estensione cervicale, la citologia peritoneale, le metastasi agli annessi (15-18).
In uno studio del Gynecologic Oncology Group [GOG] includente 621 pazienti con carcinoma dell’endometrio in stadio I la positività dei linfonodi pelvici e lombo-aortici decorreva tra il 3% e il 2% per il grado 1 e tra il 18% e l’11% per il grado 3 e tra l’1% e l’1% per i tumori confinati all’endometrio e tra il 25% e il 17% per quelli invadenti il miometrio in profondità (15).
La rilevanza prognostica della citologia peritoneale in pazienti con carcinoma dell’endometrio apparentemente confinato al corpo dell’utero ma classificato in stadio IIIa solo per la presenza di cellule neoplastiche nel fluido peritoneale o nel liquido ottenuto per washing peritoneale è ancora dibattuta (19-23). Al contrario la citologia peritoneale positiva è un fattore prognostico sfavorevole nelle pazienti con malattia extra-uterina (19-21, 24).
Ad esempio secondo Kadar e coll. (19) se il tumore ha disseminato agli annessi, linfonodi o peritoneo, la presenza di positività della citologia peritoneale fa scendere la sopravvivenza a 5 anni dal 73% al 13%. Analogamente Ebina e coll. (20) hanno riportato che negli stadi IIIc e IV la prognosi è significativamente peggiore per le pazienti con citologia
25 peritoneale positiva. Molti autori, comunque, sono concordi sul fatto che la positività della citologia peritoneale abbia un impatto prognostico significativo solo in presenza di altri fattori prognostici negativi (21, 25). Nella tabella 5 si riportano i fattori di rischio per la recidiva del carcinoma dell’endometrio (7).
Anche l’età è un fattore prognostico indipendente come provato da uno studio GOG nel quale la percentuale di sopravvivenza a 5 anni per le pazienti con meno di 40 anni era del 96.3%, comparato al 53.6% delle pazienti con più di 80 anni (26).
Si è dunque visto come l’invasione miometriale e il grado istologico abbiano un grande impatto sulla prognosi: una maggior invasione miometriale ed un più alto grado istologico correlano con un maggior rischio di diffusione linfonodale, annessiale, intra-peritoneale, nonché di recidive a livello della vagina e di metastasi ematogene (15).
Un altro fattore patologico di rischio che sembra influenzare le recidive e la mortalità è l’invasione degli spazi vascolari; Aalders e coll. (27) hanno descritto recidive e morti nel 26.7% dei pazienti con invasione degli spazi vascolari e nel 9.1% dei pazienti che non avevano questo reperto; l’incidenza complessiva di invasione degli spazi linfo-vascolari nello stadio I è del 15% ed è stato visto essere correlata con l’invasione miometriale e con la differenziazione tumorale.
Bell e coll. (18) hanno revisionato i dati di 31 casi di carcinoma dell’endometrio in stadio I per la determinazione di indicatori prognostici
26 indipendenti delle metastasi linfonodali e delle recidive dimostrando che l’unico fattore di rischio associato ad entrambi era proprio l’invasione degli spazi vascolari (p<0.05).
Watari e coll. (28) hanno comparato la sopravvivenza in 55 pazienti con linfonodi positivi, trattati con chirurgia e chemioterapia adiuvante, per determinare la variabile patologica determinante l’esito finale della malattia e la conclusione dello studio è stata che l’invasione degli spazi vascolari e il numero di linfonodi lombo-aortici positivi erano fattori prognostici indipendenti per la sopravvivenza. È stato stimato un tasso di sopravvivenza a 5 anni dell’86.4% per le pazienti senza linfonodi lombo- aortici positivi, 60.4% per quelle con un linfonodo positivo e 20% per le pazienti con più di due linfonodi positivi e la differenza era statisticamente significativa in casi con più di due linfonodi positivi. L’analisi univariata ha rivelato che l’invasione degli spazi vascolari (p=0.0173) e la positività dei linfonodi lombo-aortici (p=0.0016) erano correlati con una bassa sopravvivenza.
L’espressione dei recettori per estrogeni e progesterone nel tessuto maligno è inversamente proporzionale al grado istologico e correla con una migliore sopravvivenza rispetto ai casi in cui il tumore non esprime i medesimi (29).
Nello studio di Schink e coll. (30) la dimensione della neoplasia è stata determinata in 142 pazienti con carcinoma dell’endometrio in stadio clinico I, trattate primariamente con laparoisterectomia totale,
salpingo-27 ovariectomia bilaterale, e biopsie linfonodali per valutare se il rischio di interessamento linfonodale fosse correlato alla dimensione del tumore e se questa caratteristica influenzasse chiaramente la sopravvivenza. Gli autori hanno mostrato che le piccole neoplasie di diametro uguale o inferiore ai 2 cm, avevano solo un 4% di rischio di metastasi linfonodali e un 98% di sopravvivenza a 5 anni. Viceversa quando il carcinoma dell’endometrio in stadio clinico I interessa l’intera cavità uterina, il 35% delle pazienti presentano metastasi linfonodali con una sopravvivenza a 5 anni di solo il 64%.
Altri autori hanno tentato di identificare fattori prognostici per stratificare le donne con carcinoma dell’endometrio in gruppi di rischio così che il trattamento potesse essere adeguato al rischio di recidive. Secondo Mariani e coll. (31) l’analisi intra-operatoria del diametro del tumore dovrebbe permettere in precedenza la linfadenectomia in circa un quinto delle pazienti con carcinoma dell’endometrio. Egli ha arruolato 328 pazienti con carcinoma endometrioide del corpo dell’utero in stadio I, grado 1 o 2, confinato all’utero analizzando la sopravvivenza ed il rischio di metastasi linfonodali.
Gli autori hanno concluso che le pazienti affette da carcinoma del corpo dell’utero di dimensioni uguali a 2 cm potevano essere ottimamente trattate con la sola isterectomia.
I linfonodi rappresentano il più comune sito di malattia extra-uterina nel carcinoma dell’endometrio, perciò l’identificazione di pazienti con
28 metastasi linfonodali è importante per fornire una indicazione sulla prognosi e sulla terapia adiuvante.
Secondo i dati del GOG la sopravvivenza a 5 anni per le pazienti con malattia in stadio I e II decorre tra l’80% e il 91% e le pazienti con metastasi linfonodali hanno una sopravvivenza di solo il 44%-52% (1). Una revisione sul carcinoma dell’endometrio in stadio clinico I e II ha mostrato che le metastasi linfonodali erano presenti nell’11% delle pazienti mentre il coinvolgimento degli annessi e la diffusione al peritoneo veniva osservata solo nel 5% e nel 4% delle pazienti rispettivamente (11, 32, 33).
29
2.7. Terapia
2.7.1. Chirurgia
La terapia di scelta per il carcinoma dell’ endometrio è quella chirurgica. Essa ha una funzione terapeutica e stadiante. L’ intervento prevede citologia peritoneale, l’isterectomia totale extra fasciale, la salpingo-ovariectomia bilaterale.
La linfadenectomia pelvica e lomboaortica è prevista nelle procedure di stadiazione, raccomandata dalla FIGO, anche se vi sono controversie sulla necessità di effettuarla in tutti i casi e specialmente nei tumori ben differenziati (grado 1) con invasione miometriale inferiore al 50% (144, 145).
Diverse procedure chirurgiche possono essere utilizzate per valutare il retroperitoneo, andando da biopsie dei soli linfonodi aumentati di volume al campionamento linfonodale selettivo di siti multipli alla linfadenectomia sistematica pelvica e lombo-aortica (7, 34). Secondo l’esperienza di Kilgore e coll. (34) la possibilità di scoprire metastasi microscopiche dipendeva dal numero di siti pelvici campionati e dal quello dei linfonodi rimossi.
Nei casi avanzati è richiesta una chirurgia di debulking ovvero una massima citoriduzione chirurgica raccomandata in tutte quelle pazienti con carcinoma dell’endometrio in fase avanzata, poiché il conseguimento di una malattia residua < 1 cm sembra essere una variabile prognostica
30 indipendente per la sopravvivenza (7,10, 35, 36): le pazienti con residuo microscopico hanno una sopravvivenza significativamente migliore rispetto a quelle con residuo macroscopico.
Una stadiazione chirurgica intensiva (richiedente anche l’omentectomia e le biopsie peritoneali) similmente a quella richiesta per il carcinoma ovarico, è raccomandata nei tumori dell’endometrio sieroso-papillifero e a cellule chiare (14, 37, 38).
È stata pubblicata la comparazione tra l’ approccio laparoscopico e laparotomico e non sono state riscontrate differenze in termini di sopravvivenza tra i due gruppi. In particolare l’isterectomia vaginale laparo-assistita è stata recentemente considerata come una procedura chirurgica tecnicamente accettabile e sicura per il trattamento del carcinoma dell’endometrio nelle fasi iniziali di malattia e in centri specializzati per il trattamento delle neoplasie ginecologiche; essa è associata ad un più lungo tempo operatorio ma ad una minore perdita di sangue e ad una più breve degenza in ospedale a fronte di equivalenti risultati clinici quando comparata alla isterectomia per via addominale. Stesso discorso anche per la procedura totalmente laparoscopica. (39-44, 146, 147).
È ancora incerto se la dissezione linfonodale dia o meno un beneficio in termini di tasso di sopravvivenza (45-48).
Dati cumulativi dalla letteratura hanno mostrato lo sviluppo di malattia recidivante in 20 (6.6%) delle 305 pazienti sottoposte a linfadenectomia
31 sistematica per carcinoma dell’endometrio di rischio medio, con linfonodi istologicamente negativi e non sottoposte ad irradiazione pelvica postoperatoria (7). Solo cinque di queste recidive erano locoregionali. Seguenti studi hanno confermato questi risultati (7, 48).
Per quanto riguarda l’utilizzo della isterectomia radicale Piver III essa è a volte praticata nelle pazienti con carcinoma dell’endometrio e, in particolar modo, in coloro che hanno un macroscopico interessamento della cervice uterina (47, 49, 50). Il razionale di questo intervento è la rimozione dei parametri che fornisce margini chirurgici liberi più adeguati quando il carcinoma dell’endometrio si è già diffuso alla cervice (50). L’approccio chirurgico vaginale, in analgesia locoregionale, viene utilizzato quando le condizioni generali della paziente non permettono un intervento laparotomico. Ciò si verifica spesso per la coesistenza di più patologie sistemiche considerate, tra l’altro, fattori di rischio per la malattia (diabete, ipertensione, malattie cardiovascolari, ma anche l’ età avanzata), che rendono la paziente a rischio dal punto di vista anestesiologico e controindicano la narcosi. Anche l’obesità, caratteristica costituzionale spesso associata al tumore dell’endometrio, può rendere tecnicamente difficile l’approccio laparotomico, rendendo più semplice la rimozione di utero ed annessi per via vaginale.
È doveroso aggiungere che la via di approccio chirurgico vaginale nel trattamento del carcinoma endometrioide è stata sempre messa in discussione per la mancanza di un controllo della possibile diffusione
32 linfonodale. Grazie all’integrazione laparoscopica è oggi possibile ovviare a questo tipo di problema potendo cosi eseguire un intervento meno invasivo dell’approccio laparotomico tradizionale. Di non secondaria importanza inoltre la riduzione dei tempi chirurgici e della durata della degenza. (51-53, 148).
2.7.2 Radioterapia
La radioterapia esclusiva che consiste nell’irradiazione esterna e nella brachiterapia utero-vaginale si intraprende solo in casi selezionati (<3.5%) non suscettibili di trattamento chirurgico a causa delle controindicazioni mediche o dell’età avanzata (2, 7, 54, 55).
Nelle pazienti con neoplasia in fase precoce questa modalità di trattamento può ottenere un controllo locale in circa l’80%-90% dei casi (55).
Fishman e coll. (54) hanno svolto un confronto tra 54 pazienti con carcinoma endometrioide in stadio I e II giudicati intrattabili dal punto di vista chirurgico e sottoposti pertanto esclusivamente a terapia radiante, ed un gruppo di controllo rappresentato da una coorte di 108 pazienti operabili rese omogenee per età e stadio clinico. La sopravvivenza attuariale carcinoma-specifica a 5 anni per le pazienti in stadio II
33 inoperabile, stadio I inoperabile, stadio I operabile e stadio II operabile è risultata, rispettivamente, dell’80%, 85%, 98% e 100%.
L’irradiazione esterna pelvica è il più comune trattamento adiuvante nel carcinoma dell’endometrio, capace di ridurre le recidive loco-regionali senza aumentare però la sopravvivenza (27, 56-58). Nello studio randomizzato di Aalders e coll. (27) che arruolava 540 pazienti in stadio I, il tasso di recidive vaginali e pelviche era dell’1.9% nelle pazienti trattate con radioterapia esterna pelvica più brachiterapia rispetto al 6.9% (p< 0.1) in coloro che avevano ricevuto soltanto brachiterapia, mentre metastasi a distanza si erano sviluppate nel 9.9% delle prime e nel 5.4% delle seconde.
La sopravvivenza a 5 anni non era incrementata dalla radioterapia esterna. Un’ analisi più dettagliata ha portato alla conclusione che solo le pazienti con neoplasie scarsamente differenziate infiltranti più della metà del miometrio potevano trarre beneficio dalla radioterapia adiuvante esterna la quale non era invece indicata nelle pazienti con carcinoma dell’endometrio in stadio I e con meno di 60 anni e nelle pazienti con neoplasia di grado 2 e con invasione superficiale (56). Nello studio del GOG che comparava la chirurgia alla chirurgia più radioterapia esterna nelle pazienti con carcinoma dell’endometrio in stadio iniziale, il tasso di recidiva loco-regionale era dell’1.6% nelle pazienti sottoposte a radioterapia contro l’8.5% delle donne non sottoposte ad ulteriori
34 trattamenti, mentre la sopravvivenza non era significativamente diversa (59).
Nello studio randomizzato multicentrico PORTEC (Radioterapia Post Operatoria nel Carcinoma dell’Endometrio) che arruolava 715 pazienti con malattia in stadio I a rischio intermedio, la radioterapia esterna adiuvante riduceva il tasso di recidive loco-regionali (4% verso il 14%, p< 0.01) ma aumentava il tasso di complicanze legate al trattamento (25% verso il 6%, p<0.0001) rispetto alla chirurgia da sola mentre le morti per carcinoma (9% verso 6%), la sopravvivenza a 5 anni (81% verso 85%) e le sopravvivenze attuariali (71% verso 77%) non risultavano modificate (56, 57). Poiché la radioterapia pelvica sembra aumentare il controllo loco-regionale senza un beneficio in termini di sopravvivenza, il suo impiego dovrebbe essere limitato alle pazienti a rischio sufficientemente alto (15% o più) di recidive per aumentare il controllo locale e la sopravvivenza libera da ricaduta (57).
La recente meta-analisi del Cochrane di 4 studi randomizzati su questo argomento che hanno arruolato complessivamente 1770 pazienti ha dimostrato che l’aggiunta della radioterapia esterna pelvica alla chirurgia riduce del 72% il rischio di recidiva pelvica senza ridurre il rischio di recidiva a distanza o il rischio di morte (60). L’analisi dei sottogruppi ha evidenziato che questo trattamento si associa ad un trend per la riduzione del rischio di morte nelle pazienti con fattori di rischio multipli, quali il grado G3 e lo stadio Ic. I dati disponibili non consentono di trarre
35 conclusioni definitive per le pazienti con un singolo fattore di rischio (grado G3, e stadio Ic), mentre sconsigliano l’uso della radioterapia esterna nelle pazienti senza alcun fattore di rischio.
La sola brachiterapia è stata usata come trattamento post operatorio nelle pazienti a basso rischio (stadio Ib G1, G2) (61) o nelle pazienti con rischio intermedio (stadio I G3 o stadio Ic) con linfonodi istologicamente negativi (48) ma il beneficio clinico di tale terapia adiuvante rispetto alla sola chirurgia non è stato ancora ben definito. In più non c’è un definitivo convincimento che l’aggiunta di un boost di brachiterapia vaginale alla radioterapia esterna dia un beneficio nei termini di controllo pelvico della malattia o di sopravvivenza libera da malattia negli stadi I e II del carcinoma dell’endometrio e studi prospettici randomizzati atti a studiare l’irradiazione esterna da sola rispetto alla radioterapia più brachiterapia paiono mostrare risultati positivi (62).
Pochi dati sono attualmente disponibili circa la radioterapia a campi estesi (includente la regione pelvica e lombo-aortica) nelle pazienti con linfonodi lomboaortici positivi (12, 16, 63, 65).
Nello studio di Feuer e Calong (16) questo trattamento ha ottenuto una sopravvivenza a 5 anni del 66.7% nelle pazienti con microscopiche metastasi aortiche. Rose e coll. (64) hanno fornito una irradiazione a campo esteso a 17 delle 26 pazienti con interessamento dei linfonodi lombo-aortici ed hanno trovato che 9 (53%) di esse erano ancora vive senza evidenza di malattia con una sopravvivenza mediana di 27 mesi,
36 mentre l’87.5% delle 8 pazienti trattate con chemioterapia o progestinici erano decedute dopo un tempo medio di 13 mesi. Dalla valutazione di 19 pazienti con linfonodi lombo-aortici positivi, Hicks e coll. (65) hanno scoperto una sopravvivenza libera da malattia del 27% nelle pazienti trattate con irradiazione pelvica più lombo-aortica rispetto allo 0% in coloro che avevano ricevuto irradiazione pelvica più ormonoterapia.
L’irradiazione lombo-aortica potrebbe essere particolarmente efficace nel controllo della malattia microscopica anche dopo il debulking chirurgico; comunque questa procedura è usata sporadicamente nella pratica clinica per il rischio di severe complicanze intestinali e per la convinzione che l’interessamento dei linfonodi lombo-aortici sia associato alla diffusione sistemica della malattia (7, 63).
2.7.3. Chemioterapia
Nel carcinoma endometriale in stadio avanzato o recidivante sono impiegati sia ormoni che farmaci chemioterapici.
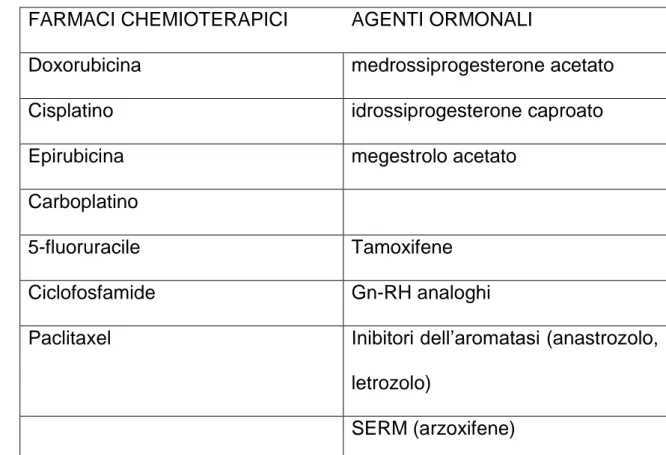
I farmaci chemioterapici più comunemente usati sono la doxorubicina [DOX] e il cisplatino [CDDP] (66, 67). Nella tabella 6 si riportano i principali farmaci in uso per il trattamento del carcinoma dell’endometrio.
37 I dati provenienti da serie cumulative mostrano una risposta obiettiva (RO) nel 26% delle 161 pazienti trattate con DOX e nel 24% delle 124 pazienti trattate con CDDP (7, 66, 67). L’ epirubicina [EPIDOX] è sembrata avere la stessa attività della DOX (7, 66, 67) ed il carboplatino [CBCDA] ha prodotto una percentuale di RO del 17 - 30% (7, 68). Per esempio, nello studio di van Wijk e coll. (68), il CBCDA ha ottenuto una RO nel 17% delle 47 pazienti valutabili e, nel dettaglio, nel 24% delle 33 pazienti che avevano ricevuto il CBCDA come prima linea di chemioterapia.
Altri farmaci con un tasso di RO > 20% sono il 5-fluoruracile (69), la ciclofosfamide [CTX] (70), l’ ifosfamide (71) e il taxolo [TAX] (72, 73). La maggior parte delle risposte ai singoli farmaci sono parziali e brevi, con una durata di risposta che decorre tra i 3 e i 6 mesi (7). Dati cumulativi da alcuni studi clinici hanno evidenziato un tasso di RO del 34% per la combinazione DOX + CTX (74, 75). Uno studio randomizzato del GOG ha mostrato che il tasso di RO era del 30% per DOX + CTX e del 22% per la singola DOX (p=0.06) (74). Trope e coll. (76) hanno scoperto che la chemioterapia con DOX 50 mg/m² + CDDP 50 mg/m² produceva un 60% di RO in 20 pazienti con carcinoma dell’endometrio recidivante. Un altro studio randomizzato del GOG su 297 pazienti ha rivelato che CDDP + DOX forniva un tasso di RO più elevato (45% verso 27%) ma una simile sopravvivenza (con una mediana di circa 9 mesi) (77). Uno studio dell’Organization for Research e and Treatment of Cancer [EORTC] su
38 154 pazienti ha evidenziato un incremento medio di sopravvivenza per il braccio CDDP + DOX (13 mesi verso 8 mesi, p=0.036) (78).
La combinazione di CDDP + DOX o di EPIDOX + CTX, con o senza progestinici, è stata largamente utilizzata nel carcinoma dell’endometrio recidivante o avanzato, con un tasso di RO compreso tra il 31% ed il 60%, una durata mediana di risposta di 4-10 mesi ed una sopravvivenza mediana di 7-15 mesi (7). L’analisi della relazione tra l’intensità di dose della chemioterapia e le risposte nel tumore dell’endometrio in fase avanzata ha mostrato che CTX è relativamente inattiva quando usata in regimi di combinazione (79). Quindi CTX potrebbe essere evitata nei regimi chemioterapici per il trattamento del carcinoma dell’endometrio e la combinazione CDDP + DOX potrebbe essere considerata lo standard nella cura dei tumori avanzati o recidivanti (66, 80).
In un recente studio randomizzato del GOG includente 342 pazienti con carcinoma dell’endometrio in stadio III, IV o recidivante non è stato osservato un beneficio significativo in termini di tasso di RO, sopravvivenza libera da progressione, sopravvivenza totale o profilo di tossicità dopo trattamento con chemioterapia circadiana consistente in DOX 60 mg/m² alle 6:00 am + CDDP 60 mg/m² alle 6:00 pm rispetto allo standard DOX 60 mg/m² + CDDP 60 mg/m² (81).
Per quanto riguarda il TAX nella fase II dello studio del GOG, questo agente alla dose di 250 mg/m² (infusione per 24 ore) ha ottenuto un tasso
39 di RO del 36% (con un tasso di risposte complete del 14%) in 28 pazienti con carcinoma dell’endometrio avanzato e recidivante (82).
Somministrando TAX a pazienti con carcinoma dell’endometrio persistente o recidivante dopo una prima linea di chemioterapia, Lincoln e coll. (73) hanno trovato che 3 (6.8%) delle 44 pazienti valutabili avevano ottenuto risposte complete e 9 (20.5%) una risposta parziale per un tasso complessivo di risposte del 27.3%. Il tempo mediano di sopravvivenza complessivo era di 10.3 mesi. La combinazione di TAX con un composto del platino sembra raggiungere risultati promettenti anche nell’istotipo sieroso-papillifero (83-86). Uno studio randomizzato di fase III del GOG includente 266 pazienti con carcinoma dell’endometrio avanzato o recidivante la combinazione di DOX 45 mg/m² + CDDP 50 mg/m² + TAX 160 mg/m² (infusione in 3 ore) otteneva un miglioramento delle percentuali di RO (57% verso il 33% p<0.001), un miglioramento della sopravvivenza libera da progressione (mediana, 8.3 vs 5.3 mesi; p> 0.01) e della sopravvivenza globale (mediana, 15.3 verso 12.3, p= 0.037) (83). Tuttavia la neurotossicità periferica di grado 2 e 3 era 12.3% rispettivamente verso 1.4% e cioè nettamente più frequente nelle pazienti trattate con questa combinazione di farmaci rispetto alla combinazione di DOX 60 mg/m² + CDDP 50 mg/m². Sulla base del profilo di tossicità favorevole molti autori hanno iniziato ad usare TAX + CBDCA nel carcinoma avanzato o recidivante ed il GOG sta attualmente conducendo
40 uno studio randomizzato di fase III che confronta questa combinazione con il regime DOX + CDDP + TAX.
L’inibitore della topoisomerasi I, il topotecan, è stato studiato per il trattamento del carcinoma dell’endometrio (87-89). Il topotecan in monochemioterapia ha ottenuto una risposta obiettiva nel 9% di 22 pazienti precedentemente trattate (89) e nel 20% di 40 pazienti nuove alla chemioterapia (5, 87).
2.7.4. Terapia ormonale
I progestinici sono stati usati a lungo nel trattamento del carcinoma dell’endometrio avanzato o recidivante. Kauppila (90) ha revisionato 1068 pazienti trattate con medrossiprogesterone acetato (MPA), megestrolo acetato, idrossiprogesterone caproato in diversi studi ed ha trovato una percentuale di risposta totale del 34%, con una durata media di risposta compresa tra i 16 ed i 28 mesi ed una sopravvivenza media tra i 18 e i 33 mesi. Seguenti studi clinici basati su criteri più restrittivi per la valutazione delle risposte, hanno riportato tassi di RO in realtà inferiori e compresi tra l’11.2% e il 15.8% senza differenza riguardo al tipo di progestinico (91,92). Nel trial randomizzato del GOG, 299 donne con carcinoma dell’endometrio avanzato o recidivante sono state trattate con MPA alla dose di 200 mg/die o di 1000 mg/die in maniera casuale (93). Nelle 145
41 donne che avevano ricevuto progestinici a basse dosi sono state contate 25 risposte complete e 11 parziali per un tasso di RO del 25% mentre tra le pazienti trattate con progestinici ad alte dosi le risposte complete sono state 14 e le parziali 10, con un tasso di risposta totale pari al 15%. La sopravvivenza libera da progressione mediana e la sopravvivenza mediana sono risultate, rispettivamente, di 3.2 e 11 mesi per il primo gruppo e 2.5 e 7 mesi per il secondo. In accordo con questo studio 200 mg/die di MPA è un ragionevole iniziale approccio terapeutico per il trattamento del carcinoma dell’endometrio avanzato o recidivante, particolarmente per quelle lesioni che sono ben differenziate e/o hanno un alto contenuto di recettori per il progesterone. (>50 fmol/mg di proteine del cytosol).
La maggior parte delle neoplasie sensibili ai progestinici sono carcinomi ben differenziati. Per esempio nelle serie di Podratz e coll. (91) una RO si è ottenuta nel 40% delle pazienti con tumore di grado 1 secondo Broders, rispetto al 17.5% delle pazienti con tumore di grado 2, 2.4% con grado 3 e 0% di quelle con grado 4.
Lo stato dei recettori ormonali (5, 90, 93), l’intervallo tra il trattamento primario e la terapia ormonale e la massa tumorale (91) sono predittivi della risposta ai progestinici. (12, 94).
Per quanto riguarda il tamoxifene in un recente studio del GOG in cui erano incluse 68 pazienti con malattia avanzata o recidivante questo farmaco ha ottenuto 3 risposte complete e 4 parziali, con una percentuale
42 di risposta complessiva del 10%, una sopravvivenza mediana libera da progressione di 1.9 mesi e una sopravvivenza mediana totale di 8.8 mesi (95). Il tamoxifene ha dunque una debole attività contro il carcinoma dell’endometrio tale da non autorizzare ulteriori indagini come agente singolo per il trattamento di tale patologia.
È ben noto che il tamoxifene possa aumentare i recettori per il progesterone contenuti nel carcinoma dell’endometrio (96) e studi sperimentali sul carcinoma dell’endometrio umano trasferito in topi nudi hanno rivelato che la somministrazione in sequenza di tamoxifene e MPA induce una maggiore regressione della neoplasia rispetto al tamoxifene da solo (97).
Studi clinici sul trattamento alternato con MPA e tamoxifene hanno dato tuttavia risultati insoddisfacenti nel carcinoma dell’endometrio avanzato e recidivante (98, 99).
Dopo la scoperta dei recettori dell’ormone rilasciante le gonadotropine (GnRh) nel carcinoma dell’endometrio, alcuni autori hanno cercato di capire se gli agonisti del GnRh fossero in grado di esercitare un’azione anti-tumorale nelle pazienti con tale neoplasia trovando tassi di RO comprese tra lo 0% ed il 28% (100). Per esempio uno studio del GOG che valutava il goserelin acetato su 40 pazienti valutabili con recidiva di malattia ha evidenziato due risposte complete e tre parziali per un tasso complessivo di risposta dell’11%, una sopravvivenza mediana libera da progressione di 1.9 mesi ed una sopravvivenza mediana totale di 7.3
43 mesi (100). L’attività del goserelin acetato nel carcinoma dell’endometrio è comunque insufficiente da giustificare ulteriori studi sul singolo farmaco. Pochi dati sono attualmente disponibili sugli inibitori dell’aromatasi e sui modulatori selettivi dei recettori per gli estrogeni (SERM)s nel carcinoma dell’endometrio (101-105). Nello studio di Rose e coll. (101) l’anastrozolo ha raggiunto una risposta obiettiva nel 9% delle 23 pazienti con malattia avanzata o recidivante che avevano ricevuto non più di un precedente regime di ormonoterapia. La sopravvivenza mediana libera da progressione e la sopravvivenza mediana totale sono state rispettivamente di 1 e 6 mesi. Il letrozolo è attualmente sotto valutazione (102, 103).
Il SERM di terza generazione arzoxifene, che si oppone all’azione degli estrogeni sulla mammella e sull’endometrio ma che ha un effetto estrogeno-agonista sull’osso e sul profilo lipidico, ha ottenuto, in 29 pazienti valutabili, una risposta completa e 8 risposte parziali con una percentuale complessiva di risposta del 31% ed una durata mediana della risposta di 13.9 mesi (104, 105). Tutte e 9 le risposte si sono realizzate in pazienti sensibili ai progestinici con una tossicità minima, senza raggiungere il grado 3-4. Proprio l’alto tasso di risposta e il profilo di tossicità estremamente favorevole rende questo farmaco suscettibile di ulteriori valutazioni.
44
2.8. Follow-up
Il razionale della necessità dei controlli di follow-up per un periodo più o meno lungo riguarda 4 aspetti:
- Una sorveglianza a lungo termine delle pazienti trattate con intento curativo si basa sulla premessa che una diagnosi precoce delle ricadute risulti in una riduzione della morbosità e della mortalità. - I controlli offrono alle pazienti rassicurazione e supporto
psicologico.
- Effettuare una diagnosi e controllo delle complicazioni e della morbosità della terapia chirurgica e della radioterapia eseguite come trattamento primario.
- Ultimo, ma non meno importante, monitorare i risultati delle terapie eseguite.
Attualmente i protocolli di follow-up sono molto variabili, utilizzando diversi test diagnostici e diversi intervalli. Non ci sono raccomandazioni formali su quello ottimale.
Nel 2006 è stata pubblicata la review “Follow-up after Primary Therapy for Endometrial Cancer: A Clinical Practice Guideline” di Fung-Kee-Fung
45 M. e altri, ricercatori di Gynecology Cancer Disease Site Group (149), con lo scopo di formulare dove possibile, un programma ottimale per il follow-up delle pazienti con carcinoma dell’ endometrio, basato sulla evidenza degli studi già pubblicati. I risultati analizzati riguardavano:
1 - Gli intervalli ottimali del follow-up
2 - La struttura clinica ottimale
3 - I test diagnostici che devono essere prescritti
4 - La modificazione della strategia di follow-up in base al rischio di
ricaduta. Di particolare interesse i risultati delle strategie di follow-up
per le pazienti a basso rischio (stadio I a-b, grado 1 o 2) e quelle ad
alto rischio di ricaduta (grado 3 di stadio I a-b, stadio Ic o stadi più
avanzati).
Sono stati analizzati 16 studi retrospettivi dei quali 12 (150, 151), riguardavano le strategie di follow-up e 4 (152, 153) il ruolo dell’utilizzo del CA 125 nella diagnosi precoce della ricaduta.
In 12 studi il tasso totale di recidive (locali ed a distanza) oscilla tra 8-19% con una media di 13%. In 4 studi che stratificano le pazienti in base al
46 rischio di ricadute è stato osservato un tasso di 1-3% per le pazienti a basso rischio e 5 -16% per la pazienti ad alto rischio.
I dati pool di questi studi dimostrano che il 61% delle ricadute sono a distanza (range 38-86%)
In 12 studi il 41-100% delle ricadute erano sintomatiche con una media di 77%.
In 9 studi il 68-100% delle ricadute si diagnosticavano nei primi 3 anni di follow - up.
Il numero delle pazienti asintomatiche nelle quali la diagnosi della ricaduta era risultato del follow-up di routine non è costantemente riportata. Tuttavia in base ai dati rapportati si osserva:
- 7 studi rapportano 5-33% di ricadute diagnosticate durante la visita. - 4 studi rapportano 0-4% di ricadute diagnosticate con il Pap-test. - 6 studi rapportano 0-14% di ricadute diagnosticate con un Rx
torace.
- 2 studi rapportano 4-13% di ricadute diagnosticate con una ecografia addominale.
- 2 studi rapportano 5-21% di ricadute diagnosticate da TAC. - 1 studio rapporta 15% di ricadute diagnosticate con il CA 125.
47 Non ci sono evidenze significative in studi clinici randomizzati sulla questione dei protocolli di follow-up delle pazienti trattate con intento curativo di carcinoma dell’ endometrio. Basato sulla interpretazione di studi retrospettivi od opinioni e consensi di esperti il “Gynecology Cancer Disease Site Group” raccomanda che tutte le pazienti debbano ricevere informazioni sui sintomi della potenziale ricaduta di carcinoma endometriale, perché la maggior parte delle ricadute, si evidenzia dagli studi, sono sintomatiche. I sintomi di una possibile ricaduta includono perdita ematica vaginale o leucorrea inspiegabile, palpazione di una neoformazione, distensione addominale, dolori persistenti, specialmente addominali e della regione pelvica, fatigue, diarrea, nausea e vomito, tosse persistente, perdita di peso.
La strategia di follow-up si basa sul rischio di ricorrenza e sulle preferenze della paziente:
- per le pazienti a basso rischio di ricaduta (quindi stadio Ia o Ib, G1 o 2): esame obiettivo generale con visita vagino-rettale ogni 6 - 12 mesi
per i primi 3 anni ed annualmente per i due anni successivi.
- per le pazienti ad alto rischio di ricaduta (quindi stadio Ia o Ib G3, Ic o stadi più avanzati): esame obiettivo generale con visita vagino-rettale ogni 3-6 mesi per i primi 3 anni ed ogni 6 mesi per i due anni successivi.
48 Dato che la maggior parte delle pazienti con ricaduta sono sintomatiche e quasi tutte le ricadute si osservano nei primi 5 anni, sembra ragionevole che le pazienti ritornino al controllo annuale della popolazione normale dopo 5 anni di follow-up libero dalla malattia. Si raccomanda che tutte le pazienti sintomatiche vengano ben stadiate, perché le ricadute locali sono potenzialmente curabili con terapia successiva.
In caso di trattamenti di radioterapia si raccomanda che la paziente sia
informata sugli effetti avversi della terapia che comprendono i disturbi rettali, urinari, vaginali , dei tessuti cutanei e sottocutanei, ossei ed altro. Lo scopo primario di una strategia di sorveglianza nelle pazienti trattate per carcinoma dell’endometrio è di facilitare la diagnosi precoce della malattia ricorrente. Questa diagnosi deve portare nella introduzione di terapie di salvataggio, con l’intenzione di migliorare la sopravvivenza e ridurre la morbosità correlata alla ricaduta. La letteratura suggerisce che non c’è una chiara evidenza che un follow-up intensivo con molti esami diagnostici porti in benefici sulla sopravvivenza.
Quando si valuta il ruolo dell’esame clinico o degli interventi diagnostici nelle pazienti asintomatiche, i risultati non sono consistenti. Solo l’esame clinico dimostra una certa utilità nel diagnosticare la ricaduta. Questo sottolinea che l’esame fisico che include anche un esame pelvico rettale è la parte più importante della strategia di follow-up.
49 Anche se i risultati degli studi retrospettivi siano modesti, ci sono delle riflessioni da fare sul più appropriato follow-up per la paziente. Uno di questi è il caso della paziente a basso rischio di recidive. Se la media di ricorrenze in tutte le pazienti trattate per il carcinoma dell’endometrio è di 13%, nelle pazienti a basso rischio l’incidenza è di <5%. Questo vuol dire che la maggioranza delle pazienti non avranno mai la ricaduta, indipendentemente dal follow-up. Quindi è ragionevole che le pazienti a basso rischio di ricaduta siano seguite in modo differente da quelle ad alto rischio.
Un altro punto di riflessione riguarda la storia naturale della malattia ricorrente. I dati dimostrano che circa il 70% delle recidive sono rilevate successivamente a qualche sintomo. Anche per queste la diagnosi della ricaduta sarebbe stata fatta indipendentemente dal follow-up. In aggiunta, nel 60% dei casi la ricaduta è a distanza e la prognosi per queste pazienti generalmente non è favorevole, indipendentemente dal momento della diagnosi. Per queste pazienti è improbabile che la diagnosi precoce della recidiva avrebbe portato in un certo beneficio sulla sopravvivenza.
L’ultimo punto riguarda il tempo della ricorrenza. Il 70-100% delle ricadute avvengono nei primi 3 anni di follow-up. Per la maggior parte delle pazienti, i controlli nel quarto, quinto e i successivi anni sarebbero di un beneficio discutibile.
50 programmi di follow-up non giustificherebbe il follow-up di routine per tutte le pazienti, ci sono argomenti altrettanto validi in sostegno delle strategie di sorveglianza. L’argomento principale è che i dati utilizzati provengono da studi retrospettivi e l’attuale tasso e tipo di ricorrenza possono variare in modo considerabile. Finché non ci saranno dati defi- nitivi, provenienti da trials clinici randomizzati e controllati o larghi studi prospettici, è prudente che le pazienti vengano sorvegliate nel modo più appropriato. Dall’altra parte le pazienti sembrano avere un beneficio psicologico dai programmi di follow-up, ma non c’è sufficiente evidenza a supportare o rifiutare questa ipotesi.
51
2.9. Linee guida
A. Pazienti suscettibili di trattamento chirurgico
Ogni qual volta possibile la chirurgia rappresenta il primo trattamento nel carcinoma dell’endometrio sia iniziale che avanzato. La chirurgia per le pazienti con la malattia clinicamente in fase precoce consiste nella laparotomia, citologia peritoneale, isterectomia totale extrafasciale e salpingo-ovariectomia bilaterale. La linfadenectomia pelvica e lombo-aortica è richiesta per le pazienti con linfonodi sospetti all’esplorazione chirurgica ed è raccomandata nei casi ad alto rischio di metastasi linfonodali, come quando si è in presenza di malattia macroscopica extrauterina o di malattia apparentemente confinata all’utero ma grado 3 (valutato su biopsia preoperatoria) o di profonda invasione del miometrio (valutata con ecografia preperatoria trans-vaginale e/o risonanza magnetica o esame estemporaneo intraoperatorio). Quando si è in presenza di un macroscopico interessamento cervicale si utilizza l’isterectomia radicale modificata, mentre l’isterectomia vaginale è presa in considerazione in specifiche condizioni cliniche (obesità, età avanzata, prolasso uterino importante, cattive condizioni generali ed alto rischio anestesiologico).
52
Trattamento postoperatorio dei tumori endometrioidi
Il piano di trattamento postoperatorio dovrebbe essere diverso per le pazienti con tumore endometrioide e non endometrioide. Nel primo caso le opzioni terapeutiche possono essere schematizzate come segue:
Nessun ulteriore trattamento è richiesto nelle pazienti con: - Malattia stadio Ia, ogni grado;
- Malattia stadio Ib, grado 1-2;
- Malattia stadio IIa, grado 1-2 con o senza invasione miometriale superficiale;
Al contrario la radioterapia adiuvante esterna pelvica è di solito raccomandata nelle pazienti:
- Malattia stadio Ib grado 3; - Malattia stadio Ic, ogni grado;
- Malattia stadio IIa, grado 3 o profonda invasione miometriale non sottoposta ad adeguata linfadenectomia;
- Malattia stadio IIb.
La radioterapia esterna pelvica è di incerta utilità nelle pazienti in stadio Ib G3 e Ic G1-G2.
Lo stadio III include pazienti con condizioni cliniche molto differenti. Le pazienti in stadio IIIa per interessamento della sierosa del corpo uterino o degli annessi dovrebbero essere trattate con radioterapia esterna pelvica