51
ALTRI AGENTI NEUROPROTETTIVI
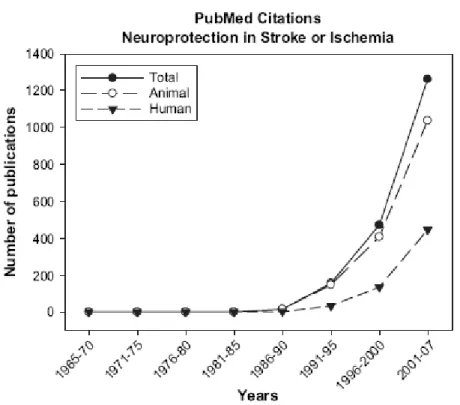
La neuroprotezione per il danno ischemico cerebrale è emersa solo recentemente come argomento di una seria inchiesta biomedica. Un sondaggio MEDLINE (PubMed, 2007) non ha rilevato sostanzialmente nessuna pubblicazione su questo argomento fino ai primi anni ’90, mentre ha rilevato un’ondata significativa di pubblicazioni nel corso degli ultimi 10 anni (Figura 18). Solo negli ultimi 6 anni sono apparsi su questa materia più di 1000 lavori sperimentali e oltre 400 articoli clinici. Dagli anni ’70 in poi, definita e caratterizzata la fisiopatologia del danno cerebrale ischemico, si è sviluppata la neuroprotezione nel settore produttivo; essa ha indicato la strada a potenziali strategie di intervento per prevenire e/o curare le patologie correlate all’ischemia cerebrale.
Figura 18 : Numero di pubblicazioni catalogate MEDLINE nella neuroprotezione nell’ictus/ischemia dal 1965 a oggi (PubMed, 2007).
52 Le finalità della neuroprotezione sono:
1) prevenire la morte cellulare;
2) riparare o rigenerare le cellule in via di degenerazione; 3) modificare il decorso della malattia.
Dopo l’ictus, il risultante danneggiamento delle funzioni essenziali per le attività di routine, quali la programmazione dei movimenti e la loro esecuzione, l’integrazione sensomotoria, il linguaggio e altre funzioni cognitive, hanno un profondo e permanente impatto sulla qualità di vita. Un punto interessante che può essere osservato nella pratica clinica è un lento, ma consistente, recupero in un periodo di settimane e mesi. Mentre il recupero nei primi giorni è probabilmente imputabile alla risoluzione dell’edema e/o alla riperfusione dell’area ischemica, gran parte del recupero è dovuto principalmente alla plasticità cerebrale, attraverso la quale alcune regioni del cervello assumono funzioni precedentemente svolte dalle aree danneggiate. La neurogenesi e l’angiogenesi sono altri possibili meccanismi di recupero dopo l’ictus.
Il coinvolgimento di vari neurotrasmettitori e neuromodulatori (quali recettori per gli amminoacidi eccitatori, le concentrazioni di calcio, l’ossido nitrico e lo stress ossidativo) nell’induzione del danno ischemico e nella morte neuronale associata all’ictus ha spinto numerosi ricercatori ad esplorare differenti strategie terapeutiche attraverso l’inibizione dell’attivazione dei recettori per gli amminoacidi eccitatori, il controllo della concentrazione di Calcio e dello stress ossidativo.
1) Bloccanti dei canali al Calcio: Nimodipina.
Il calcio gioca un ruolo centrale nella fisiopatologia del danno ischemico cerebrale, così come nei disordini cardiaci [77, 78, 79, 80]. Nel cervello, il blocco dei canali al calcio ad attivazione lenta (di tipo L) riduce l’ingresso di calcio nei neuroni e questo rappresenta un potenziale effetto benefico nell’ischemia e in altri disordini, dal momento che un aumento della concentrazione intracellulare di calcio può essere fatale nella cascata neurotossica che sfocia nell’ictus cerebrale.
53
La Nimodipina è una 1,4-diidropiridina (24) che ha la capacità di determinare un aumento selettivo del flusso sanguigno cerebrale senza influenzare i parametri circolatori sistemici. Viene impiegata per la prevenzione e la terapia dei disturbi neurologici dovuti ad un insufficiente afflusso di sangue arterioso a livello cerebrale. In pazienti con emorragia subaracnoidea, la nimodipina riduce gravi deficit neuronali dovuti al vasospasmo cerebrale [81].
(24)
2)Antagonismo dei recettori per il Glutammato
La eccitotossicità dovuta ad un elevato rilascio di glutammato può distruggere le funzioni mitocondriali. Abbiamo visto che il Glutammato è un essenziale neurotrasmettitore eccitatorio che agisce sui recettori AMPA e NMDA localizzati sulla membrana post-sinaptica dei neuroni. Dal legame e dalla attivazione di questi recettori, i canali ionici si aprono permettendo a vari cationi, come Na+, K+, e Ca2+ di entrare nelle cellule. I livelli sinaptici di glutammato sono regolati dai trasportatori del glutammato presenti negli astrociti, negli oligodendrociti, e microglia, i quali riprendono il glutammato rilasciato e lo convertono in glutamina. La glutamina è poi trasportata ai neuroni e riconvertita in glutammato dalla glutaminasi [82]. La eccitotossicità del glutammato si verifica quando c’è un elevato rilascio di glutammato nelle sinapsi, e un inadeguato reuptake da parte dei trasportatori nelle cellule di sostegno. Per esempio, durante un attacco infiammatorio nella sclerosi multipla, sono prodotte grandi quantità di glutammato dalle cellule immunitarie attivate quali macrofagi e microglia [82]. Si
54
può assistere anche ad una diminuizione nell’espressione dei trasportatori del glutammato negli astrociti e negli oligodendrociti circostanti, un ulteriore rafforzamento nella severità della eccitotossicità. La iperstimolazione dei recettori del glutammato porta a una disregolazione dei gradienti ionici, inclusa l’omeostasi del Ca2+.
2.a)Antagonisti dei recettori NMDA
I recettori NMDA sono recettori per il glutammato che rivestono un ruolo critico per la plasticità neuronale, per il normale sviluppo del SNC e per la sopravvivenza dell’organismo. Sono costituiti dalle subunità NR1/NR2, ma possono contenere anche una subunità modulatoria NR3 [83], la quale riduce l’ampiezza e la permeabilità del calcio associata ai canali NMDA, svolgendo quindi un ruolo neuroprotettivo. L’antagonista NMDA più ampiamente studiato è l’agente non competitivo MK-801 (dizocilpina) (25), il quale lega i recettori NMDA con alta affinità e produce un blocco di lunga durata.
Anche il Destrometorfano (26), un analogo destrorotatorio della codeina ad azione centrale, e un suo metabolita, il destrorfano, sono bloccanti non competitivi ad alta affinità del canale NMDA e sono neuroprotettivi nell’ischemia focale sperimentale [84].
55 2.b) Antagonisti del recettore AMPA
Il recettore AMPA è un recettore post-sinaptico non-NMDA ionotropico per il glutammato (e altri composti), importante per la trasmissione sinaptica eccitatoria rapida del SNC. L’AMPA (acido alfa-ammino-3-idrossi-5-metil-4-isoxazolone propionato) è una molecola agonista specifica per il recettore AMPA. Si tratta di un recettore ionotropico, in quanto il legame con i suoi agonisti provoca una modifica della sua conformazione facendolo diventare un canale aperto per il transito di specifici ioni (sodio, potassio e in alcuni casi calcio).
Il legame del glutammato con questi recettori provoca l’apertura dei canali ionici e conseguente sviluppo di un potenziale post-sinaptico eccitatorio.
L’iperattivazione del recettore AMPA si verifica sia nelle condizioni acute, come l’ictus, sia nelle condizioni croniche neurodegenerative, come nella sclerosi laterale amiotrofica [86].
Antagonisti non competitivi dei recettori AMPA che possono essere usati in terapia sono: la 2,3-benzodiazepina (27) e il nuovo neuroprotettore BIIR 561 (28).
27 28
3) Inibitori delle Specie Reattive dell’Ossigeno (ROS)
Le Specie Reattive dell’Ossigeno (ROS) sono importanti mediatori secondari coinvolti nel processo ischemico cerebrale, pertanto l’inibizione delle ROS è stata considerata come terapia neuroprotettiva.
56
L’NXY-059 (disodio 2,4-disolfofenil-terz-butilnitrone) (29) è un derivato N-ossido capace di intrappolare i radicali liberi (viene definito “spin-trap”) che ha dimostrato proprietà neuro protettive in vitro [87] .
Questi risultati interessanti devono ancora essere confermati dagli studi clinici in corso. L’NXY-059 è in corso di sviluppo dal laboratorio AstraZeneca sotto il nome di “Cerovive”.
29
Un altro antiossidante/scavenger di radicali è il Tirilazad mesilato (30), un potente inibitore della lipoperossidazione indotta dai radicali liberi. L’efficacia su modelli sperimentali di ischemia focale o globale nel ridurre l’infarto e migliorare l’outcome neurologico non è stata confermata in trial clinici di pazienti con ictus, emorragia subaracnoidea e trauma cranico [88]. E’ stata pubblicata, inoltre, un’ampia recensione sistematica preclinica, su modelli animali di ischemia focale che coinvolgono il tirilazad, nella quale il risultato è stato misurato come volume dell’infarto/valutazione neurologica [89]. Complessivamente il tirilazad ha ridotto il volume dell’infarto del 29% e ha migliorato la valutazione neuro comportamentale del 48%.
57
30
L’Ebselen (2-fenil-1,2-benzisoselenazol-3(2H)-one) (31) è un derivato organico del selenio che è stato ampliamente studiato durante l’ultima decade. Adesso è sotto un’attenta indagine come agente neuroprotettivo nei trial clinici [90]. Una parte sostanziale del profilo farmacologico dell’ebselen sembra essere dovuta alla sua azione come antiossidante, infatti è un composto che agisce come scavenger di idroperossidi organici, in particolare, di lipidi idroperossidi. L’interesse particolare su questo farmaco è dovuto al fatto che l’ebselen mima l’attività della glutatione perossidasi. Oltre a questo meccanismo, considerato il principale, l’ebselen inibisce a basse concentrazioni un vasto numero di enzimi coinvolti nell’infiammazione, come le lipoossigenasi, la ossido nitrico sintetasi, la NADPH ossidasi, la protein chinasi C, e la H+/K+-ATPasi [91].
31
L’Edaravone (3-metil-1-fenil-2-pirazolin-5-one) (32) è un nuovo scavenger dei radicali liberi, sviluppato dalla Mitsubishi-Tokyo Pharmaceuticals Inc (Tokyo,
58
Japan). Questo agente è stato utilizzato in pazienti con infarto cerebrale dall’aprile 2001 in Giappone [92, 93]. L’edaravone ha mostrato di prevenire l’edema cerebrale dopo l’ischemia, il danno da riperfusione in modelli animali [94, 95] e in pazienti affetti da ictus [96]. L’edaravone mostra la sua azione antiossidante attraverso il rafforzamento della produzione di prostacicline, l’inibizione del metabolismo della lipoossigenasi dell’acido arachidonico “intrappolando” i radicali idrossilici, inibendo la perossidazione lipidica e portando alla protezione di varie cellule, come le cellule endoteliali e le cellule del miocardio, contro il danno da ROS. Inoltre, l’edaravone, migliora la funzione endoteliale nei fumatori attraverso un aumento nella biodisponibilità dell’ossido nitrico [97]. Sebbene l’utilità dell’edaravone per il trattamento dell’ictus da lieve a moderato in fase acuta sia stato ben stabilito, non è chiaro se l’edaravone sia efficace contro il danno cerebrale in pazienti con ictus severo. Dati ottenuti con numerosi trial clinici devono ancora confermare la validità e la sicurezza di questo farmaco.