Com’è evidente dal titolo, l’obiettivo di questo capitolo è analizzare le categorie di sensori chimici CMOS-compatibili, facendo riferimento agli esempi attualmente presenti in letteratura. Lo spettro d’applicazione di tali sensori è molto ampio, e spazia dal campo industriale per, ad esempio, la rivelazione di gas dannosi, ma anche in campo ambientale, per il monitoraggio dell’inquinamento atmosferico [1], fino ad arrivare al campo medico/biologico, per analisi di vario genere. Il vantaggio dell’utilizzo di sensori chimici in tutti questi campi risiede principalmente nella comodità, nella velocità d’esecuzione, e nel basso costo rispetto alle tradizionali tecniche d’analisi basate su procedimenti chimici/biologici.
Di recente i sensori chimici hanno mostrato una grande versatilità nelle applicazioni mediche/biologiche, per la rivelazione di biomolecole. Stanno, infatti, nascendo numerose tipologie di sensori biochimici, detti anche biosensori, per i quali è possibile effettuare classificazioni in base al recettore dell’analita1 ed alla tecnica impiegata per la trasduzione da segnale chimico ad elettrico [2]. Fra tutte le possibili sotto-aree d’applicazione dei biosensori, occupano una posizione di rilievo le analisi sul DNA per la diagnosi di malattie genetiche. Per quanto affermato, il focus di questo capitolo sarà maggiormente puntato sui sensori di DNA, per i quali sono presenti numerosi esempi in letteratura.
Ovviamente, l’interesse è maggiore sui sensori CMOS-compatibili per i due vantaggi che sono enunciati qui di seguito. Il primo è che possono essere integrati in matrici, poiché sono scalabili in dimensioni, consentendo così la multianalisi, ossia la rivelazione contemporanea di diverse molecole. L’attuale ricerca sta concentrandosi, infatti, sullo
1 Per analita s’intende la molecola o lo ione di cui deve essere rivelata la presenza, mentre per recettore la
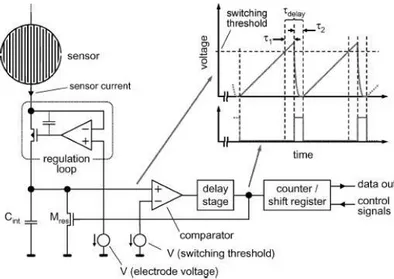
sviluppo di nuovi materiali caratterizzati da un’alta sensitività verso un solo tipo d’analita, oppure sullo sviluppo di tecnologie d’immobilizzazione dei recettori sul dispositivo. Facendo riferimento al caso dei sensori di DNA, il loro principio di funzionamento (quando sono organizzati in array) è sommariamente descritto in figura 1.1 [3].
Figura 1.1 – Principio di funzionamento delle matrici di sensori di DNA.
Il principio di rivelazione del sensore si basa sul fenomeno d’ibridazione del DNA, ossia sul legame che avviene fra due ssDNA complementari2. Non appena terminata la fabbricazione del sensore, segue, infatti, la fase d’immobilizzazione in posizioni predefinite delle molecole ricettrici di ssDNA, dette anche probes. Generalmente, tale fase si svolge mediante modifica delle molecole probes con un gruppo tiolo (SH-), il quale è in grado di legarsi in maniera covalente con un metallo deposto sull’area sensibile del rivelatore. In figura 1.1b e 1.1c sono mostrati due differenti
2
Con ssDNA (single stranded DNA) complementari s’intende due singole eliche di DNA in grado di legarsi selettivamente fra di loro (non con eliche diverse), poiché sono composte da sequenze complementari dei nucleotidi dell’acido desossiribonucleico (l’Adenina si lega con la Timida, la Citosina con la Guanina).
siti all’interno dell’array dopo la fase d’immobilizzazione, mentre in figura 1.1d e 1.1e è mostrata la fase successiva, in cui il chip viene a contatto con le molecole da rivelare. Possono, dunque, accadere due fenomeni: il matching (accoppiamento per complementarietà), oppure il mismatching fra gli ssDNA. Dopo la fase di lavaggio del sensore, solo nel caso di matching (figura 1.1f) si formano le doppie eliche di DNA (dsDNA – double stranded DNA), mentre nel caso di mismatching (figura 1.1g) il sensore ritorna nella situazione iniziale. A tale punto, la rivelazione della doppia catena può avvenire per metodi ottici [4] o magnetoresitivi [5], nel caso in cui le molecole target3 siano state etichettate con elementi fluorescenti o magnetici, oppure mediante FET sensibili alla carica contenuta nel DNA [6, 7, 8], ma anche mediante rivelazione gravimetrica a causa dell’aumento di massa (caso dei QCM –Quartz Crystal Microbalance– e dei MEMS). Esistono inoltre rivelazioni di tipo elettrochimico, chemiluminescente, ecc, che sono attualmente in uso per le analisi di DNA, ma sono svantaggiate dal fatto di non fornire un segnale d’uscita elettrico.
Il secondo vantaggio dei sensori CMOS-compatibili risiede, invece, nella possibilità di realizzare sullo stesso chip di semiconduttore anche l’elettronica d’acquisizione della misura [3].
Figura 1.2 – Esempio d’integrazione di sensore ed elettronica d’acquisizione.
3
La figura 1.2 mostra schematicamente il sensore e l’elettronica d’acquisizione del segnale da lui generato, entrambi direttamente integrati sullo stesso wafer di silicio. In tale maniera è possibile realizzare un dispositivo completo (Lab On a Chip), in grado di svolgere rapidamente e a basso costo analisi chimiche su varie entità.
Nonostante i MEMS siano attualmente la tipologia di sensore dominante per la realizzazione d’accelerometri, giroscopi, rivelatori di pressione, ed altri sensori di grandezze fisiche, negli ultimi anni stanno facendo il loro ingresso anche come sensori di specie chimiche. In generale, la misura è di tipo microgravimetrico, ossia il MEMS svolge la funzione di una microbilancia. Ciò significa che prima di tutto devono essere immobilizzate sul MEMS delle molecole ricettrici, selettive per la specie cercata, svolgere, quindi, una prima misura a vuoto ed una successiva all’introduzione del sensore nell’ambiente di misura. Nel caso di presenza delle molecole target, il MEMS si appesantisce, e con meccanismi di rivelazione che saranno illustrati di seguito, si può rivelare la presenza della sostanza che si cercava.
Nei paragrafi che seguono saranno quindi presentati vari sensori CMOS-compatibili, distinguendo i MEMS, che in generale sono delle strutture sospese tridimensionali, da i rivelatori di tipo “planare”, ossia sviluppati principalmente in due dimensioni, quali i sensori ad effetto di campo. Saranno inoltre trattate le microbilance al quarzo, poiché sono la tipologia di sensore microgravimetrico dominante del momento, sebbene non siano compatibili con la tecnologia CMOS.
Per tutte queste ragioni, a riguardo dei QCM sarà dedicata una maggiore attenzione alle loro prestazioni, che al momento sono le migliori in commercio, fatto per cui tali dispositivi sono anche utilizzati in microelettronica come misuratori di spessore dei film metallici deposti per evaporazione. D’altra parte, per i sensori CMOS-compatibili (siano essi MEMS o meno) sarà dedicata una maggiore attenzione al loro design, alle tipologie d’attuazione e rivelazione, e al processo di fabbricazione, poiché questi sono gl’argomenti su cui verte l’attuale ricerca.
1.1 Sensori planari di DNA
Con il termine planari s’intendono quei sensori (CMOS-compatibili) composti da strutture bidimensionali, sviluppati con sovrapposizione di strati diversi, in contrapposizione ai MEMS che, invece, sono strutture meccaniche tridimensionali, generalmente libere di oscillare. Una prima distinzione che è possibile praticare all’interno dei sensori planari si basa sulla necessità d’etichettare o meno le molecole target di DNA. L’etichettatura, o “labeling”, consiste nell’aggiunta agli ssDNA oggetto d’analisi di elementi reattivi, mediante particolari tecniche chimiche. Successivamente, se fra le molecole etichettate sono presenti quelle complementari ai probes, esse s’ibridano con quest’ultime ed il rivelatore è in grado di accorgersene proprio grazie alla presenza dei marker4. Sono questi, tuttavia, dei sensori realizzati con strutture complicate, o che necessitano di apparecchiature esterne per la rivelazione, che rendono costose e/o prolungate le operazioni di misura.
La possibilità di effettuare una rivelazione elettrica label-free, utilizzando sensori ad effetto di campo5 [9], offre un nuovo approccio per i chip d’analisi genetiche, permettendo letture veloci, semplici e meno costose [6]. In questa maniera, immobilizzando i filamenti di ssDNA sulla superficie dei transistori ad effetto di campo, sono stati realizzati i così detti DNA-FET che rivelano l’ibridazione del DNA mediante la variazione della tensione di bande piatte, o della tensione di soglia.
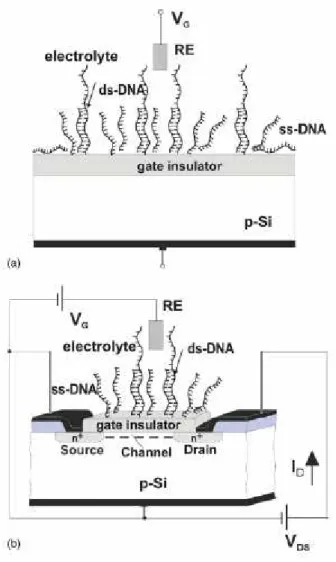
D’altra parte, all’interno di questa categoria di sensori di DNA possiamo distinguere due sottotipi: le strutture EIS (Elettrolita Isolante Semiconduttore) e le strutture EMIS ,provviste anche di metallizzazione di gate rispetto alle precedenti. La figura 1.3 mostra schematicamente le due strutture prima elencate (a – struttura EIS; b – struttura EMIS). In entrambi i casi, la tensione VG è applicata mediante un elettrodo che è anche
responsabile di fissare la tensione dell’elettrolita contenente le molecole target.
4
Elementi reattivi utilizzati per l’etichettatura.
5 L’esempio principe di sensori chimici CMOS-compatibili è l’ISFET di Bergveld per la rivelazione della
Figura 1.3 – Schemi delle strutture EIS (a) ed EMIS (b).
Generalmente esistono due modi per cui l’ibridazione del DNA può intervenire sulle proprietà elettriche dell’interfaccia fra elettrolita e sensore. Nel caso delle EMIS si considera l’effetto di modulazione del campo elettrico nell’isolante di gate, poiché le molecole di DNA sono portatrici di cariche negative6 [8]. Ogni variazione di carica superficiale (non appena le molecole target si legano alle probes) risulta in una variazione di segno opposto nella regione di carica spaziale del semiconduttore. In tale maniera si modula la popolazione d’inversione del canale, permettendo la rivelazione grazie ad un’effettiva variazione della corrente di drain. Nel caso, invece, delle strutture EIS, prevale l’effetto di diminuzione della
6
capacità di gate, dato che in seguito all’ibridazione aumenta lo spessore del dielettrico fra elettrolita e semiconduttore [7].
I DNA-FET riportati in letteratura impiegano varie configurazioni: capacitive del tipo EIS (ma anche ES – Elettrolita Semiconduttore), EMIS ad arricchimento o svuotamento, a gate flottante, con o senza elettrodo di riferimento, con differenti isolanti di gate (non solo SiO2, ma anche nitruro
di silicio – Si3N4) con vari spessori (da 2 fino a 1000 nm) [6]. Inoltre
esistono molteplici metodi d’immobilizzazione degli ssDNA (adsorbimento, legame covalente, mediante altre molecole leganti) e per tale motivo si possono ottenere diverse densità di probes, variabili da 2.4×108 a 5×1013 molecole/cm2. Esistono infine moltissime soluzioni tampone utilizzate per l’ibridazione, caratterizzate da differenti concentrazioni degli analiti (da 10 µM a 1M). Per quanto riguarda invece l’entità del segnale generato dall’ibridazione, facendo riferimento alla variazione della tensione di soglia o di bande piatte, può risultare in una differenza di pochi mV fino ad arrivare a 1.9 V, dopo vari tempi di attesa per l’ibridazione stessa. La diversità di tutti questi casi va ricercata nella molteplicità di strutture che possono essere realizzate. In aggiunta, l’assenza di un modello teorico unificante, che ne spieghi correttamente il principio di funzionamento, rende difficile un confronto tra le varie proposte. Per tale motivo, successivamente sono prese in considerazione una struttura EIS ed una di tipo EMIS, ritenute sufficientemente esemplificative per chiarire il funzionamento dei DNA-FET.
Struttura EIS – Il sensore presentato basa la propria sensitività sulla
diminuzione della capacità di gate in seguito all’ibridazione del DNA, aumenta lo spessore del dielettrico compreso fra il canale e l’elettrolita [7]. Tutto ciò in accordo alla ben nota espressione della capacità di un condensatore piano
d S
C=εrε0 , (1.1)
dove C è la capacità (F), ε0εr rispettivamente la costante dielettrica del
materiale (adimensionale), mentre S è la superficie attiva del dispositivo (m2), ed infine d è lo spessore del dielettrico (m).
Il condensatore realizzato consiste in una metallizzazione per il contatto di substrato (silicio drogato p, con impiantazione superficiale p+), un doppio strato d’isolante (30 nm di ossido e 26 nm di nitruro di silicio) con sopra immobilizzati gli ssDNA, ed infine la soluzione elettrolitica contenente il DNA da analizzare. La variazione della capacità di gate (rispetto a quella precedente all’ibridazione) risulta circa del 50% per ogni 1000 pmoli della concentrazione di DNA target in soluzione elettrolitica. Con tale dispositivo è pertanto possibile rivelare l’ibridazione a partire da 100 fino a 1800 pmol di DNA, che equivalgono a circa 1 e 180 µg di DNA. Dato che la tecnica PCR (Polymerase Chain Reaction7) tipicamente produce quantità di DNA da analizzare dell’ordine dei microgrammi, è evidente che il DNA-FET trattato è sufficientemente sensibile per le analisi genetiche.
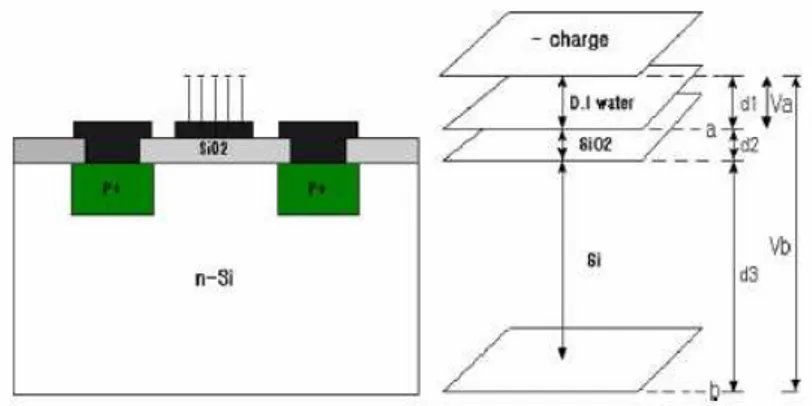
Struttura EMIS – Come precedentemente affermato, i sensori a struttura EMIS funzionano da rivelatori di carica sul gate, e del suo potenziale, indotti dalla presenza di cariche negative sul DNA [8]. La figura 1.4 qui di seguito mostra un possibile modello del sensore, considerando le cariche disposte su piani paralleli di spessore trascurabile rispetto alla loro larghezza e lunghezza.
Figura 1.4 – Modello di potenziale elettrico indotto da cariche disposte su piani paralleli.
7
Reazione a catena della polimerasi. Tecnica dominante per l’amplificazione di una sequenza di DNA, per cui, partendo da un certo gene, è possibile replicarlo fino ad ottenerne svariati milioni di copie identiche in poco tempo.
La differenza di potenziale fra due punti R1 ed R2 è data da: ) ( 2 2 2 1 1 2 1 2 R R dr r d E V R s R s R R ⋅ =− = − − =
∫
∫
ε ρ ε ρ . (1.2)Pertanto, considerando sempre le cariche distribuite su dei piani, si può ottenere una relazione fra le cariche stesse e il potenziale di gate:
1 1 0 2 d V s a
ε
ε
ρ
= , (1.3) + + = 3 0 3 2 0 2 1 0 1 2ε
ε
ε
ε
ε
ε
ρ
d d d V s b , (1.4) + = − 3 0 3 2 0 2 2ε
ε
ε
ε
ρ
d d V V s a b , (1.5)dove ρs è la densità di carica superficiale (C/m2), ε0, ε1, ε2, ε3 sono,
rispettivamente, la costante dielettrica del vuoto, dell’acqua deionizzata, dell’ossido di silicio, e del silicio. Si può pertanto concludere che la polarizzazione di gate indotta dal DNA è proporzionale alla densità di carica superficiale da lui posseduta. Le variazioni del potenziale elettrochimico dovute agli ssDNA ed ai dsDNA dopo l’ibridazione generano una variazione della tensione di gate e, conseguentemente, della conduttanza di canale. Quest’ultima è collegata alla variazione della corrente di drain, pertanto, misurando la variazione di corrente che attraversa il canale, si capisce se è avvenuta o meno la formazione delle doppie eliche di DNA.
A riguardo della fabbricazione del dispositivo, si nota che è stato necessario realizzare un FET a canale p poiché i gruppi fosfati presenti nell’acido desossiribonucleico hanno una carica negativa la quale garantisce così la corretta polarizzazione del transistore. Si tiene a precisare, anzi tutto, che l’intero dispositivo è stato realizzato con un processo CMOS standard a 0.5µm. Inizialmente è stato fatto crescere uno strato d’ossido sul substrato p di orientazione (100). Dopo le fasi standard di realizzazione di un MOSFET, sono stati deposti due strati d’isolante (SiO2 e Si3N4) per la passivazione del dispositivo, onde evitare danni
durante la sua immersione nelle soluzioni con analiti. A questo punto è stato possibile procedere con un fase di attacco verticale ad ioni per l’apertura dell’area di gate e dei contatti per i pad. Infine, è stato deposto uno strato di cromo e oro per permettere l’immobilizzazione degli ssDNA. La figura 1.5 riassume brevemente i passi di processo sopra descritti.
Figura 1.5 – Principali passi di processo per la realizzazione del dispositivo. Nella parte (a) è mostrato il
sensore completamente passivato, mentre nella parte (b) è stata aperta la finestra sul gate. Infine avviene la deposizione dell’oro necessario all’immobilizzazione degli ssDNA modificati con gruppi tiolo.
Per quanto riguarda invece i risultati ottenuti con tale sensore, la figura 1.6 mostra i diagrammi della corrente di source in funzione del tempo, durante la fase di immobilizzazione e quella d’ibridazione.
Dalla figura si nota che, non appena le molecole probes s’immobilizzano o quelle target si ibridano, l’intensità della corrente aumenta8 a causa della carica negativa portata dal DNA che tende a far aumentare la conducibilità di canale. Da una semplice misura di corrente si può pertanto risalire alla presenza della sequenza di DNA che si cercava.
1.2 Sensori al quarzo: i QCM (Quartz Crystal Microbalance)
Le microbilance al quarzo sono dei sensori microgravimetrici costituiti da sottili dischi di diossido di silicio cristallino (figura 1.7), in grado di rivelare variazioni di massa in tempo reale, fino a sensibilità dell’ordine dei nanogrammi [10].
Figura 1.7 – Immagine di un QCM (fonte tamadevice – www.tamadevice.co.jp).
Nel 1880 Jacques e Pierre Curie scoprirono che uno stress meccanico applicato a materiali cristallini come il quarzo produce in risposta un potenziale elettrico tra le superfici esterne del materiale, d’ampiezza proporzionale allo stress applicato. Questo comportamento è oggi noto come effetto piezoelettrico, termine che deriva dal greco πιέζω, che significa premere.
La piezoelettricità può essere diretta o inversa: la prima consiste nell’insorgere di una polarizzazione elettrica in seguito ad una deformazione o ad uno sforzo del materiale, la seconda prevede uno scambio tra causa ed effetto. Entrambi i risvolti della piezoelettricità sono
8
governati da una coppia d’equazioni che mettono in relazione grandezze come lo stress T, lo strain S, il campo elettrico E, e lo spostamento dielettrico D [11]. Per ottenere le equazioni costitutive del materiale piezoelettrico, è sufficiente unire una relazione della prima coppia ad una della seconda, ottenendo, ad esempio, il seguente sistema d’equazioni
T i ij j ijk jk E ij ijk k ijkl kl D E d T S d E s T
ε
= + = + % , (1.6)che caratterizza contemporaneamente il comportamento meccanico ed elettrico di un materiale piezoelettrico come il quarzo9. In tale sistema, con εT s’intende il tensore delle costanti dielettriche del materiale misurato in assenza di stress imposto dall’esterno, con d il tensore piezoelettrico di strain, con d~ il trasposto del precedente, e con sE il tensore delle compliances (inverso di rigidezze) misurato in assenza di campo elettrico imposto esternamente.
Queste caratteristiche del quarzo, fortemente dipendenti dalla sua orientazione cristallografica, permettono di mandarlo in risonanza meccanica, facendolo oscillare ad una frequenza ben definita e stabile nel tempo, poiché legata alle sue proprietà geometriche e fisiche [10]. Grazie alle loro perdite trascurabili, il fattore di qualità Q dei quarzi può raggiungere e superare il valore di 100'000, permettendo la realizzazione di oscillatori stabili in frequenza, fatto che giustifica il largo impiego di tali dispositivi in svariate applicazioni che richiedono rivelazioni gravimetriche di precisione.
Come dispositivo elettroacustico, il risonatore al quarzo può essere modellato, per la parte meccanica, come un sistema massa-molla-smorzatore (riportato in equivalente elettrico), in parallelo ad una capacità che ne rappresenta la parte puramente elettrica. Il circuito meccanico a parametri concentrati può, infatti, essere sostituito da uno equivalente, ma di tipo RLC serie (figura 1.8).
9
Combinando poi tale sistema d’equazioni con le equazioni del campo acustico e quelle di Maxwell si ottiene l’equazione di Christoffel per i materiali piezoelettrici, che ne descrive la propagazione di onde acustiche ed elettromagnetiche nel materiale.
Figura 1.8 – Circuito meccanico a parametri concentrati, e suo equivalente elettrico, per un risonatore al
quarzo.
Il circuito completo che si ottiene è mostrato in figura 1.9, ove con C0
s’intende la capacità del dispositivo a riposo.
Figura 1.9 – Circuito equivalente di un risonatore al quarzo.
I valori tipici di questi parametri sono dell’ordine di 10-12 F per C0, 10-14
F per C1, 10-2 H per L1, e 100Ω per R1. L’intervallo di frequenze di
risonanza dei QCM varia dalle decine di kHz alle centinaia di MHz, fino a raggiungere anche l’ordine dei GHz. Risolvendo, infatti, nel dominio di Laplace l’impedenza totale del bipolo rappresentato in figura 1.9 si giunge alla relazione (1.7)
( )
1 1 1 2 1 1 2 1 1 // + + + + ⋅ = Σ Σs RC s LC s C R s C L s C s Zq , (1.7)dove con C// s’intende il parallelo fra C0 e C1
(
C0 +C1)
, mentre con CΣla serie fra le stesse capacità
+ 1 0 1 0 C C C C
. A questo punto si possono
ricavare tre importanti parametri che caratterizzano il quarzo: la frequenza di risonanza serie, quella parallelo, e il fattore di merito Q:
1 1 2 1 C L fs
π
= , (1.8) Σ = C L fp 1 2 1π
, (1.9) Σ = C R f Q p 1 2 1π
. (1.10)La frequenza di risonanza serie è quell’oscillazione capace di annullare l’impedenza del QCM, mentre quella parallelo sarebbe tale da renderla infinita nel caso di perdite nulle. Tuttavia, ricordando che C0 >>C1, si
ottiene che 1 1 1 1 C R C L
Q ≅ , e, di conseguenza, fp ≅fs. Si può pertanto
assumere che la frequenza di risonanza del quarzo sia proprio pari a fs,
cui d’ora in avanti in avanti sarà assegnato il pedice q. Sostituendo i valori tipici di C0, C1, ed L1 la frequenza di risonanza ottenuta è dell’ordine delle
decine di MHz, mentre Q risulta dell’ordine di 100'000, come precedentemente annunciato. I QCM più diffusi sono i cosiddetti “AT-cut”, ottenuti tagliando il quarzo in fette sottili, con un angolo di 35°25’ rispetto all’asse z del cristallo, poiché mostrano ottima stabilità della frequenza di risonanza rispetto alla temperatura, oltre che nel tempo.
Si riportano qui di seguito i dati (misurati in aria [10]) caratterizzanti QCM di varie fasce di qualità (tabella 1.1).
Quarzo C0 (pf) R1 (Ω) C1 (fF) L1 (mH) fq (MHz) Q
NM25 12.93 6.89 53.68 4.73 9.984 43124
ICM 12.53 5.76 61.46 4.1 10.022 44742
COMM 4.58 7 13.83 11.31 9.972 123932
Tabella 1.1 – Esempi di caratteristiche di alcuni QCM.
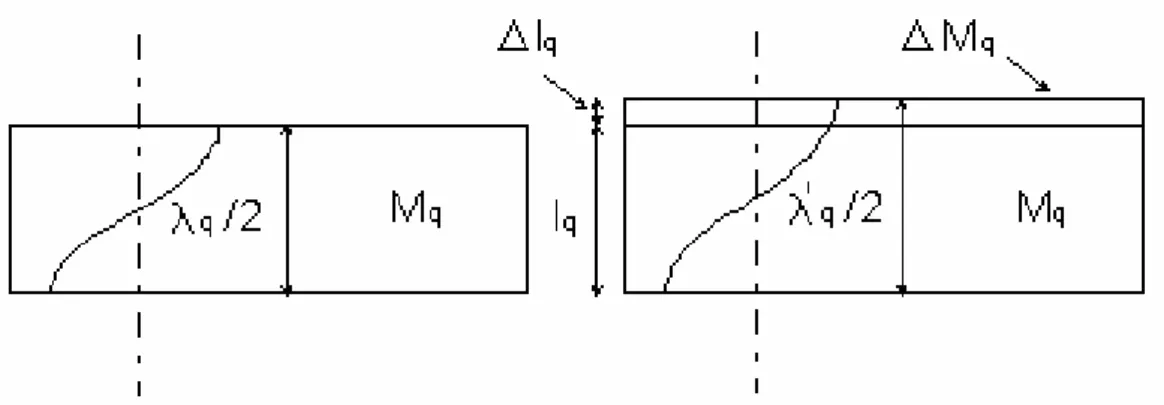
Nel 1959 Sauerbrey [12] ricavò per primo la relazione fra la frequenza di risonanza e la massa depositata su un disco di quarzo (tipica forma nella quale sono fabbricati i QCM). Nel suo modello si assume che, per
piccole variazioni, l’aumento di massa può essere considerato come uno strato sottile che si aggiunge al disco. La figura 1.10 mostra schematicamente (in sezione) il modello di Sauerbrey per un quarzo oscillante di massa Mq e spessore lq.
Figura 1.10 – Rappresentazione schematica del modello di Sauerbrey per piccole variazioni di massa su una
superficie del quarzo.
La frequenza di risonanza fq in tale modello è data da
q q q q q l v v f 2 = =
λ
, (1.11)dove λq è la lunghezza dell'onda acustica che si propaga nel quarzo,
pari al doppio del suo spessore, mentre vq è la velocità di fase di tale
onda.
Nel caso di deposizione di massa sulla superficie del quarzo si ha un aumento dello spessore ∆lq che determina una variazione negativa della
frequenza di risonanza. Pertanto, un aumento di spessore, ovvero di massa, genera una diminuzione della frequenza di risonanza in accordo alle (1.12) e (1.13) qui di seguito
q q q q l l f f ∆ − = ∆ , (1.12) q q q q M M f f ∆ − = ∆ . (1.13)
L’equazione fondamentale (1.14) per applicazioni microgravimetriche, derivata durante la deposizione di film sulla superficie del quarzo, è ottenuta dalla combinazione delle (1.11) e (1.13)
q q q q q q q q q q q M A v f M A l f f ∆ ⋅ − = ∆ ⋅ − = ∆
ρ
ρ
2 1 , (1.14)dove Aq è l’area del cristallo espressa in cm2, ρq la densità del quarzo in
g/cm3. E’ possibile quindi esprimere il ∆fq come
q q q q q A M f k f =− ⋅ ∆ ∆ 2 , (1.15)
dove Kq è una costante data da
6 10 26 . 2 2 = ⋅ − = q q q v k
ρ
cm 2 ·s·g-1, (1.16)dato che la densità del quarzo vale 2.648 g/cm3 mentre la velocità delle onde meccaniche è pari a 3.336×105 cm/s1. La (1.15) mette in evidenza il fatto che la variazione della frequenza di risonanza è indipendente dalla distanza dal centro del disco di quarzo ove si deposita il ∆Mq.
D’altra parte, alcuni studi hanno dimostrato che la sensibilità è massima al centro del disco e decresce con andamento pressoché gaussiano con la distanza radiale dal centro ,ossia uscendo dagli elettrodi che eccitano le onde acustiche nel materiale. Inoltre, per le applicazioni medico/biologiche, il risonatore deve lavorare a contatto dei fluidi contenenti gli analiti, e subisce pertanto un’ulteriore variazione della frequenza di risonanza, rispetto a quando si trova in aria10 [13, 14]. Considerando un fluido di densità ρl e viscosità ηl, il ∆fl da sommare a
quello dovuto alla deposizione di massa risulta
q q l l q l f f
µ
πρ
η
ρ
⋅ − = ∆ 32 , (1.17)dove ρq è la densità del quarzo, mentre µq è il suo modulo di taglio.
10
I parametri calcolati precedentemente per il risonatore presuppongono che lavori nel vuoto; tuttavia, anche nel caso di presenza di aria, si può considerare con buona approssimazione che il quarzo lavori senza essere caricato.
Per quanto precedentemente esposto, il QCM risulta un sensore microgravimetrico dalle prestazioni ottime, ed è pertanto impiegato anche in applicazioni che richiedono altissima sensibilità, come la deposizione di film sottili in microelettronica, per la determinazione dello spessore depositato. Per quanto riguarda invece il suo utilizzo per analisi su DNA si riportano qui di seguito due casi, a titolo d’esempio.
Nel primo caso [15] è stato utilizzato un quarzo AT-cut con fq=8 MHz
della ICM, per rivelare la presenza del batterio Escherichia coli O157:H7, causa di gravi patologie intestinali.
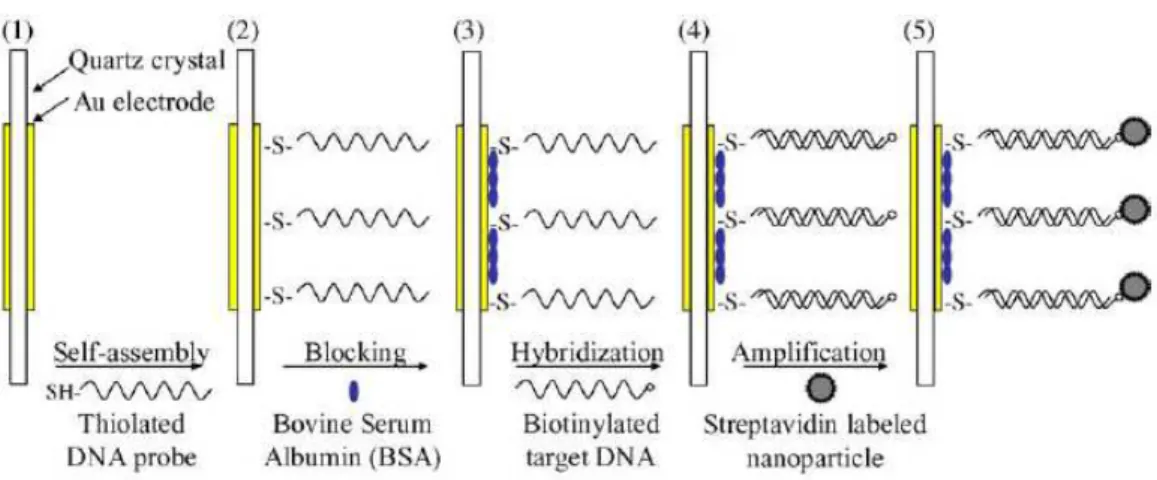
La figura 1.11 illustra la preparazione dei sensori (1) nella fase d’immobilizzazione (2), ibridazione (3), ed amplificazione del segnale d’uscita (4) (5) mediante appesantimento dei target con delle molecole contenenti un core di Fe3O4.
Figura 1.11 – Preparazione del QCM e procedura di rivelazione.
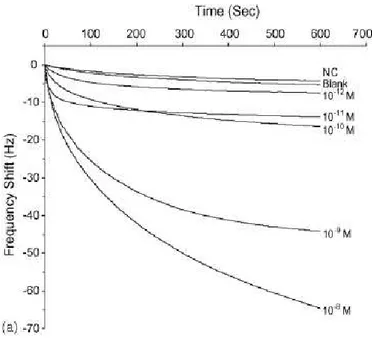
Nella pagina a seguire, il grafico in figura 1.12 mostra invece il decremento della frequenza di risonanza in funzione del tempo d’ibridazione, con parametro la concentrazione degli analiti in soluzione. Innanzi tutto si nota che non sono state rivelate sensibili variazioni della frequenza di risonanza nel caso di molecole target negative (ossia mismatching), ma anche nel caso di molecole positive ma non appesantite.
Figura 1.12 – Shift della frequenza di risonanza in funzione del tempo d’ibridazione, con parametro la
concentrazione di analita.
Per quanto riguarda invece gl’altri casi, sono state registrate variazioni di frequenza comprese fra 5 e 65 Hz circa, meglio illustrate nella figura 1.13, ossia il grafico dello spostamento del picco di risonanza in funzione della concentrazione di molecole target.
Figura 1.13 – Shift della frequenza di risonanza in funzione del tempo d’ibridazione, con parametro la
concentrazione di analita.
Anche il secondo caso presente in letteratura [16] utilizza un quarzo AT-cut, e i risultati sono riportati in figura 1.14, con (a) caso di matching e
(b) mismatching. Anche in questo esempio, lo shift della frequenza di risonanza è apprezzabile con certezza (circa 15 Hz).
Figura 1.14 – Shift della frequenza di risonanza in funzione del tempo d’ibridazione, (a) matching, (b)
mismatching.
Per le loro ottime prestazioni, i QCM risultano dunque dei buoni candidati per le rivelazioni gravimetriche d’ibridazione del DNA; tuttavia, non essendo realizzabili in tecnologia CMOS ne perdono i vantaggi, primo fra tutti la possibilità d’integrazione e la conseguente realizzazione di array di sensori per effettuare la multianalisi.
1.3 I MEMS come sensori chimici CMOS-compatibili
Come affermato in precedenza, i sistemi micro-elettro-meccanici possono essere impiegati non solo come sensori di grandezze fisiche, ma anche come rivelatori di specie chimiche. Sono essi generalmente costituiti da strutture sospese (cantilever – travi a mensola), attuate con vari sistemi (elettromagnetico, piezoelettrico, termico), sia in modo statico, sia dinamico. Il principio di funzionamento si basa sulla variazione delle loro caratteristiche meccaniche in seguito all’adsorbimento di molecole chimiche, sia a causa di stress indotti, sia a causa dell’aumento di massa della struttura stessa. In altre parole, si sta facendo riferimento alla flessione, oppure alla variazione della frequenza di risonanza nei risonatori, indotte dalle molecole adsorbite dalla struttura. Analogamente
alla varietà dei metodi d’attuazione, le tecniche di rivelazione del segnale d’uscita sono diverse, e variano dal sensing di tipo ottico, a quello di tipo piezoresistivo, capacitivo e magnetico.
Per quanto riguarda invece la tecnologia con cui tali dispositivi sono fabbricati, è particolarmente interessante la CMOS, poiché è la tecnologia attualmente dominante per i circuiti integrati, permettendo la produzione di massa, ossia a basso costo. D’altra parte, dato che essa è una tecnologia concepita per la produzione di soli circuiti integrati, non prevede di per sé la possibilità di creare le strutture sospese sopra menzionate, salvo che non si prevedano passi di processo aggiuntivi a quelli standard. Si parla, infatti, di tecnologie di micromachining, che possono essere di tipo bulk o surface. Con surface micromachining s’intende quella serie di processi per l’estrazione del MEMS, procedendo con passi litografici dalla superficie superiore del wafer di semiconduttore; mentre nel bulk micromachining tali procedure avvengono dal retro della fetta. Nel primo caso, pertanto, si tratta generalmente d’attacchi non profondi per la rimozione di strati sacrificali; al contrario, nel secondo caso sono richiesti attacchi profondi11 (centinaia di µm) per la rimozione del semiconduttore fino a liberare le strutture preformate sulla faccia superiore. Sono da considerare inclusi nelle tecniche di micromachining anche la deposizione di particolari film sottili, siano essi metallici o dielettrici, necessari alla fabbricazione del sistema. In ogni caso si parla di passi di post-processing, che devono essere aggiunti al regolare flusso di processo della tecnologia CMOS. Si può pertanto distinguere fra pre-CMOS MEMS, intermediate-CMOS MEMS, e CMOS MEMS, in base al punto d’inserimento del post-processing [17].
Nell’approccio pre-CMOS le strutture micro-eletrro-meccaniche sono formate prima dell’inizio della sequenza CMOS standard. Durante questi trattamenti le fette di semiconduttore devono rispettare i criteri di pulizia necessari per l’avvio dei passi microelettronici successivi. Nell’approccio
11
Si tratta d’attacchi in plasma, ossia scavi effettuati da ioni di un certo elemento accelerati verso il materiale da rimuovere. Se oltre all’azione fisica di scavo per impatto si utilizzano ioni in grado di attaccare anche chimicamente solo il materiale da rimuovere, allora si tratta di RIE (Reactive Ion Etching), che permette di raggiungere profondità d’attacco maggiori.
intermediate-CMOS la sequenza standard viene interrotta per l’inserimento di passi aggiuntivi, quali la deposizione di particolari film sottili. Generalmente, in questo tipo d’approccio sono realizzate delle strutture in surface micromachining aventi il polisilicio come materiale portante, e successivamente rilasciate mediante attacco di strati sacrificali. Infine, nell’approccio post-CMOS possono essere distinte due diverse strategie. La prima prevede che i MEMS siano completamente realizzati sulla faccia superiore di una fetta già finita di lavorare, senza intaccare gli strati della tecnologia CMOS. Le strutture vengono prima deposte, e poi definite mediante rimozione degli strati sacrificali. Alternativamente, nella seconda strategia è possibile liberare le strutture direttamente preformate negli strati CMOS superiori di lavorazione del wafer. Il post-processing della seconda strategia si basa soprattutto sull’attacco anisotropo12 del silicio di bulk, per il rilascio delle strutture su lui deposte. I reagenti generalmente utilizzati sono l’idrossido di potassio (KOH), l’etilendiammina pirocatecolo (EDP), oppure l’idrossido di tetrametilammonio (TMAH), tutti in grado di attaccare selettivamente i piani d’orientazione (100) e (110), ma non il piano (111). Se si considera, pertanto, di attaccare una comune superficie (100), si ottengono degli scavi degradanti a piramide (se la finestra da aprire è un quadrilatero – figura 1.15) con un angolo
73 . 54 3 1 arccos = =
ϕ °. In altre parole, vengono lasciate visibili le facce (111).
Figura 1.15 – Sezione di un attacco anisotropo del silicio (100) con apertura di una finestra quadrangolare.
12
Se tuttavia la finestra da aprire prevede degli angoli non soltanto concavi, ma anche convessi, come quelli dell’estremità di un cantilever, l’attacco precede ugualmente in quelle direzioni, rendendo possibile il rilascio completo della struttura, come mostrato in figura 1.16.
Figura 1.16 – Evoluzione del rilascio di una struttura sospesa mediante attacco anisotropo del substrato.
Le strutture così realizzate sono composte dagli strati dielettrici intermetallici della tecnologia CMOS, e dalle relative piste impacchettate all’interno di tali ossidi.
Entrambe le due strategie dell’approccio post-CMOS sono interessanti perché sono applicabili a qualsiasi tipo di processo, adottato da qualsiasi fonderia per la realizzazione di circuiti integrati. Inoltre, è possibile in tal maniera realizzare microsistemi dotati di multipli livelli di metallizzazione, come previsto per i circuiti integrati. D’altra parte, lo svantaggio dell’approccio post-CMOS risiede nel limitato intervallo di temperature operative impiegabili nel post-processing, per cui non si possono oltrepassare i 400 °C, onde evitare il deterioramen to di quanto prima realizzato.
I MEMS per applicazioni chimiche presenti in letteratura offrono una varietà di strutture, principi di funzionamento, e metodi d’attuazione e rivelazione, per cui è difficile metterli a confronto. Si possono, infatti, utilizzare strutture attuate in modalità statica, ossia dove il segnale d’uscita è legato alla flessione indotta in tali strutture a causa dell’adsorbimento di
massa, sia esso causa di carico aggiuntivo o di stress aggiuntivi nello strato superficiale. Per quanto riguarda invece l’attuazione dinamica, l’adsorbimento chimico è responsabile della variazione dei parametri dinamici della struttura, quale il suo momento d’inerzia, generando così uno spostamento della frequenza di risonanza come nel caso dei QCM.
Come preannunciato, i vari tipi d’attuazione comprendono quello elettromagnetico, piezoelettrico, termico; mentre i tipi di rivelazione comprendono quello ottico, piezoresistivo, capacitivo (ossia la misura d’impedenza), e magnetico. Tutte queste tecniche saranno trattate in dettaglio grazie agli esempi presenti in letteratura, dedicando sempre una maggiore attenzione ai sensori d’ibridazione del DNA.
La rivelazione ottica è forse la tecnica più largamente utilizzata per la misura della flessione di una struttura in grado di riflettere la luce generata da un laser. Il fascio di luce riflesso viene quindi raccolto da un fotodiodo segmentato, ossia un fotodiodo con l’area sensibile suddivisa in più zone. In base, dunque, alla zona colpita si riesce a risalire alla deflessione del fascio, e a sua volta allo spostamento della struttura riflettente (per questo motivo, tali dispositivi sono anche detti PSD – Position Sensitive optical Detector). Dato che per le analisi biologiche sono spesso richieste schiere di cantilever su cui verificare la deflessione del fascio riflesso, devono essere impiegati array di laser in numero pari a quello dei cantilever (figura 1.17)
Nonostante per tali applicazioni si utilizzino sorgenti laser a basso costo (VCSEL – Vertical Cavity Surface Emitting Laser), è stata sviluppata una tecnica di lettura che limita ad una sola la sorgente di luce richiesta [18]. Tale tecnica consiste, infatti, nella scansione sequenziale degli n cantilever mediante un solo laser e un solo fotodiodo, risparmiando così in costi d’attrezzatura.
D’altra parte, un sensing di tipo puramente elettronico è sempre preferibile, perché fornisce direttamente una grandezza di tipo tensione, corrente, o resistenza. Pertanto si preferisce utilizzare dei piezoresistori integrati nel semiconduttore per rivelare la variazione di stress interni ad una struttura. Facendo l’esempio di un cantilever, è possibile capire la sua flessione, sia statica, sia dinamica rivelando lo stress presente all’ancoraggio della struttura. Si sceglie proprio tale punto poiché è quello a massimo stress, visto che è a contatto con la zona del wafer considerata indeformabile, ossia a spostamento nullo.
Figura 1.18 – Posizione a massimo stress, ideale per l’integrazione dei piezoresistori su un cantilever.
In figura 1.18 si mostra schematicamente il posizionamento dei piezoresistori all’ancoraggio del cantilever. Supponendo una deformazione indotta flessionale, i soli resistori a risentire di una variazione di resistenza sono R2 ed R4, mentre R1 ed R3 mantengono il loro valore di riposo.
Montando questi quattro resistori a ponte di Wheatstone, è possibile ottenere una funzione di trasferimento del tipo
3 44T V V IN OUT =
π
, (1.18)dove con π44 (Pa-1)s’intende il coefficiente di piezoresistività, mentre
con T3 la componente longitudinale dello stress. Si tende quindi a
realizzare le strutture seguendo la direzione (110), ossia orientate a 45° rispetto alle orientazioni cristallografiche di riferimento, poiché in tale direzione compare il π44 (molto maggiore degli altri coefficienti), e pertanto
si massimizza la sensitività del rivelatore. E’ possibile realizzare tali resistori anche con dei transistori MOS polarizzati in zona triodo [19].
Si può menzionare quindi il sensing di tipo capacitivo, o più in generale mediante misura di un’impedenza. Tale metodo si basa sulla variazione dell’impedenza della struttura sotto misura, dovuto alla deformazione, in altre parole allo spostamento della stessa. Questa tipologia di rivelazione è utilizzata anche nei MEMS attuati piezoelettricamente, poiché si risale alla loro frequenza di risonanza grazie ad un’indagine della loro impedenza.
Infine, la rivelazione magnetica si basa sulla legge di Faraday-Lenz, secondo la quale s’induce una f.e.m. in una spira metallica attraversata da un flusso variabile nel tempo del campo d’induzione magnetica. Per maggiori chiarimenti su tale tipo di rivelazione, si rimanda al capitolo successivo di questa tesi, ove sarà trattato in dettaglio il MEMS realizzato.
Passando poi ad analizzare i metodi d’attuazione di tali strutture, si possono elencare quattro principali tecniche: elettrostatica, termica, piezoelettrica, e magnetica.
La tecnica elettrostatica è forse la più semplice da utilizzare, perché agisce sull’attrazione che subiscono due facce di un condensatore quando esso è polarizzato. Si possono così creare degli attuatori a facce piane parallele, oppure interdigitati per massimizzare la superficie d’attrazione. E’ questa, tuttavia, una tecnica d’attuazione comunemente utilizzata in modalità on/off, e non si presta bene per mandare in risonanza le strutture MEMS.
L’attuazione termica si basa, invece, sulle onde di deformazione indotte ad opera del surriscaldamento e raffreddamento periodico della struttura
mediante riscaldatori ad effetto Joule [19, 20, 21]. A titolo d’esempio, il caso riportato in [20, 21] tratta un cantilever lungo 160 µm, realizzato in polisilicio con surface micromachining, ed attuato mediante la periodica espansione e contrazione di due resistori montati nel punto d’ancoraggio della struttura (figura 1.19).
Figura 1.19 – Cantilever in polisilicio, definito con LPCVD (Low Pressure Chemical Vapour Deposition) e
rilasciato con attacco in HF dell’ossido sacrificale sottostante, attuato lateralmente.
I resistori laterali sono, infatti, attraversati da una corrente ad onda rettangolare (di frequenza pari alla risonanza meccanica), per cui si dilatano con il valore alto della corrente, e si rilassano nel semiperiodo in cui quest’ultima è nulla. Il problema che s’incontra nell’attuazione termica è la massima frequenza di pilotaggio, che è limitata dalle costanti di tempo di raffreddamento dei materiali che si devono prima espandere e poi contrarre. Per il caso in esame è stata calcolata una fmax = 600 kHz, che è
tuttavia ben oltre la risonanza meccanica (80 kHz).
Un’altra interessante tecnica d’attuazione è quella piezoelettrica, che porta alla fabbricazione di risonatori direttamente paragonabili ai QCM [22]. Il materiale piezoelettrico che più comunemente s’utilizza per la realizzazione di risonatori su silicio è l’ossido di zinco (ZnO) racchiuso fra due elettrodi metallici (figura 1.20).
Figura 1.20 – Struttura di un risonatore piezoelettrico integrato, completo di riflettore a reticolo di Bragg per
l’isolamento dal substrato.
In dettaglio, la struttura (150×150 µm) è stata realizzata a partire da una fetta di silicio su cui è stata deposta una pila di materiali ad alternata impedenza acustica, in modo da costituire uno specchio acustico tipo riflettore a reticolo di Bragg13. In tale modo, il risonatore, quando viene stimolato elettricamente, innesca delle onde acustiche verticali senza che la sua faccia inferiore risenta dell’effetto caricante del substrato. Il dispositivo, pertanto, risulta sensibile solo all’aumento di carico generato dalle molecole adsorbite sull’elettrodo superiore, e ciò si concretizza in una variazione della frequenza di risonanza. In figura 1.21 sono mostrati diagrammi d’ampiezza e fase dell’impedenza del risonatore, dai quali è stato estratto un fattore Q pari a 330.
Figura 1.21 – Ampiezza e fase dell’impedenza del risonatore piezoelettrico.
13 E’ sufficiente alternare tali strati con una periodicità spaziale tale che le varie onde riflesse alle interfacce fra
Nonostante i QCM siano caratterizzati da fattori molto maggiori anche a contatto con i fluidi (1÷5×103), grazie alla loro maggiore frequenza di risonanza, i risonatori piezoelettrici integrati riescono a raggiungere dei livelli di sensibilità e risoluzione comparabili a quelli delle microbilance al quarzo. Per il risonatore in esame sono state, infatti, registrate una sensibilità di 2.4 kHz cm2/ng e una risoluzione minima di circa 25 ng/cm2, che può essere ancora migliorata fino a raggiungere 1 ng/cm2.
Il risonatore piezoelettrico, oltre ad essere utilizzabile da solo, può essere anche impiegato come attuatore di un cantilever alla cui estremità si trova il film sensibile alle biomolecole [23]. Le dimensioni di tale struttura oscillante sono 100 µm in lunghezza, 30 µm in larghezza e 5 µm di spessore, mentre il film piezoelettrico, deposto con la tecnica del sol-gel14, è spesso 2.5 µm. In figura 1.22 è mostrata una sezione del dispositivo.
Figura 1.22 – Sezione trasversa del cantilever attuato piezoelettricamente.
Le strutture sulle faccia superiore del wafer sono state definite mediante attacchi in plasma, mentre per l’estrazione della struttura è stato necessario un procedimento di bulk micromachining con un RIE per il silicio. La frequenza di risonanza misurata per tale dispositivo è di circa 1.3 MHz, come mostrato in figura 1.23, riportante i diagrammi d’ampiezza e fase dell’impedenza del risonatore. Anche questo tipo di struttura si è dimostrato efficace nella rivelazione gravimetrica dell’ibridazione del DNA.
14 I materiali da deporre si trovano in ub gel a viscosità nota. Viene quindi deposto per spinning
Figura 1.23 – Grafici d’ampiezza (a) e fase (b) dell’impedenza misurata sul risonatore piezoelettrico.
L’ultimo mezzo d’attuazione dei MEMS preso in analisi è quello magnetico. Esso può essere realizzato in due diversi modi. Il primo prevede l’utilizzo di materiali magnetici depositati sulla struttura (figura 1.24), attuati poi mediante applicazione di un campo magnetico esterno, variabile nel tempo [24, 25].
Figura 1.24 – Immagini al SEM di un microcantilever attuato con dot magnetici.
Sono tuttavia questi dei dispositivi d’utilizzo poco funzionale, proprio per la necessità di generazione del campo esterno alternato, e oltretutto richiedono anche la deposizione dei film magnetici che generalmente sono
di composizione inusuale. Per questi motivi, generalmente si preferisce utilizzare la seconda opzione d’attuazione magnetica che tuttavia funziona solo grazie alla presenza di un campo magnetico esterno generato da uno o più magneti permanenti, meglio se integrati nel case di contenimento del sensore. Le strutture così realizzate possono essere mandate in risonanza semplicemente facendole attraversare da delle linee di corrente (alla frequenza opportuna), le quali interagiscono col campo magnetico esterno generando delle forze di Lorentz responsabili dell’attuazione.
Per maggiori chiarimenti su quest’ultimo metodo d’attuazione, si rimanda alla lettura del capitolo successivo, poiché è proprio il meccanismo utilizzato dal risonatore realizzato in questo lavoro di tesi.