Figura 1: rappresentazione schematica di sinapsi chimica ed elettrica. (A): nella sinapsi chimica, l’arrivo di un potenziale d’azione nel terminale presinaptico provoca il rilascio di vescicole contenenti neurotrasmettitore, che vengono rilasciate nello spazio sinaptico e che si legano in maniera specifica a recettori della membrana postsinaptica, influenzando l’apertura o la chiusura di canali ionici e modificando la conduttanza della membrana.
(B): nella sinapsi elettrica, le gap junctions mettono in diretta comunicazione il citoplasma delle due cellule adiacenti. La comunicazione, a differenza della sinapsi chimica, è bidirezionale.
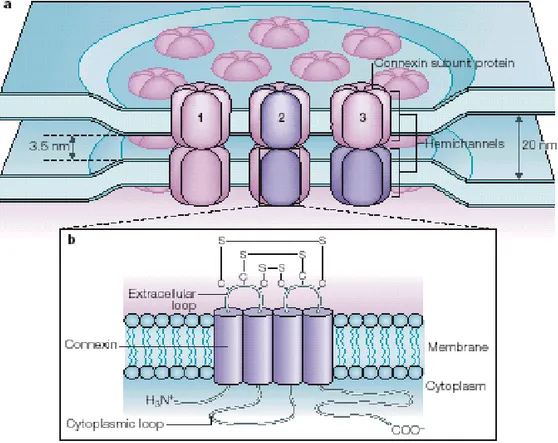
Figura 2: schema di organizzazione molecolare di una placca gap-giunzionale.
(a): tre tipi diversi di gap junctions: omomerico/ omotipico (1); eteromerico (2); ed eterotipico (3), dipendenti dalla composizione molecolare.
(b): subunità proteiche delle connessine (da Sohl et al., 2005)
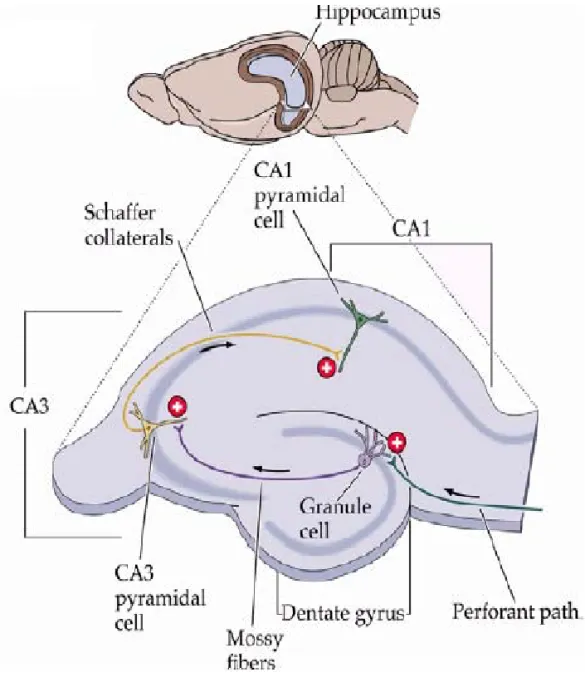
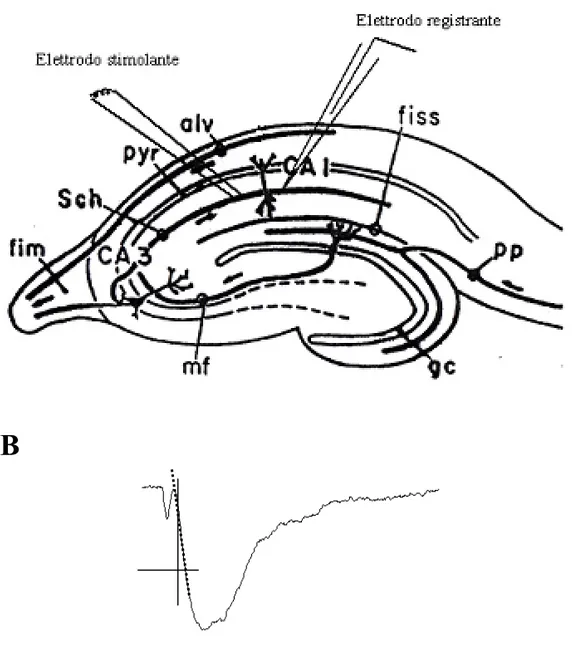
Figura 3: Veduta dell’ippocampo di ratto dopo rimozione di parte della sovrastante neocorteccia.
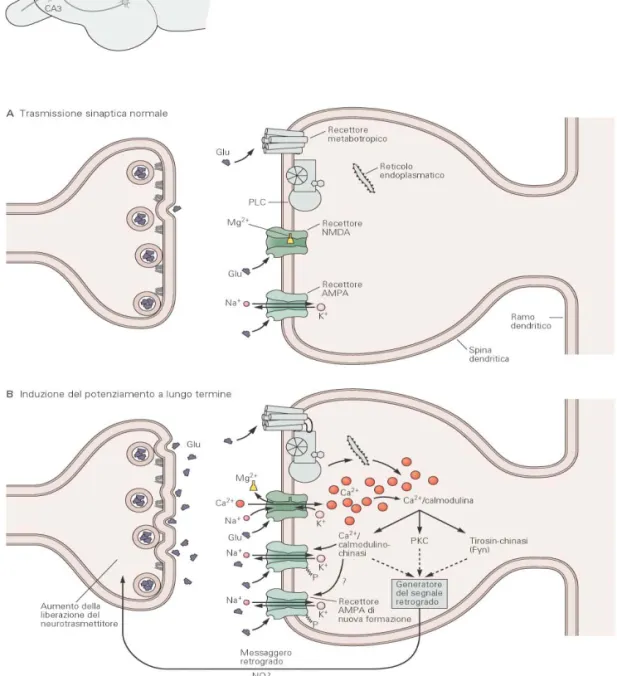
Figura 4: schema di induzione dell’LTP Vedi testo
*
*
Delay: 15 min
45 min
90 min
0
50
60
70
80
%
Cx36 (-/-)
Cx36 (
+/
+)
Percent
E
xploration
New Object
Figura 5. Effetto della delezione del gene per la Cx36 sul test di riconoscimento di un nuovo oggetto.
I topi Cx36 KO sono incapaci di riconoscere un oggetto dopo solo 15 minuti dalla prima presentazione.
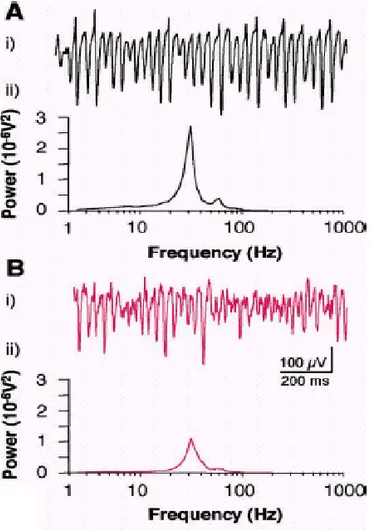
Figura 6: effetti della delezione della Cx36 sull’attività delle onde gamma indotte da kainato nell’area CA3 dell’ippocampo A) Oscillazioni gamma nei topi WT. Ai) registrazione extracellulare
dallo strato radiato del CA3 e corrispettivo spettro di frequenza(Aii). B) Oscillazioni gamma nei topi Cx36 KO. Bi) registrazione
extracellulare dallo strato radiato del CA3 e corrispettivo spettro di frequenza (Bii).
A
B
Figura 8. Slice di ippocampo con elettrodi
A) posizionamento degli elettrodi stimolante e registrante nello strato sinaptico dell’area CA1 dell’ippocampo.
B) Potenziale eccitatorio di campo registrato extracellularmente dallo strato radiato.
0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 1.1 -0.2 0.0 0.2 0.4 0.6 0.8 1.0 fEPSP slope (mV/msec)
Intensità di stimolazione (mA)
2.0 1.8 1.6 1.4 1.2
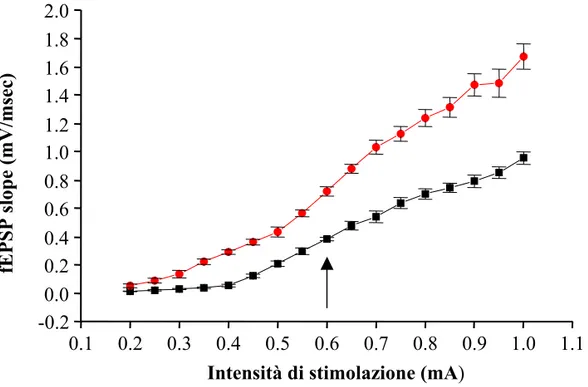
Figura 9: Curve stimolo/risposta.
Le due curve sigmoidi rappresentano l’interpolazione tra i valori della slope iniziale del fEPSP evocati a diverse intensità di stimolazione nelle slices di controllo (n=5, ) e nelle slices dei topi Cx36 KO (n=5, ).
La freccia indica l’intensità di stimolazione utilizzata sia per lo stimolo test sia per lo stimolo tetanico per gli esperimenti successivi.
A
-20 80 100 120 140 160 180 200 220 240 fEPSP slope (% del controllo) -10 0 10 20 30 40 50 60 70 Tempo (min) a b c a b c -20 80 100 120 140 160 180 200 220 240 fEPSP slope (% del controllo) -10 0 10 20 30 40 50 60 70 Tempo (min)B
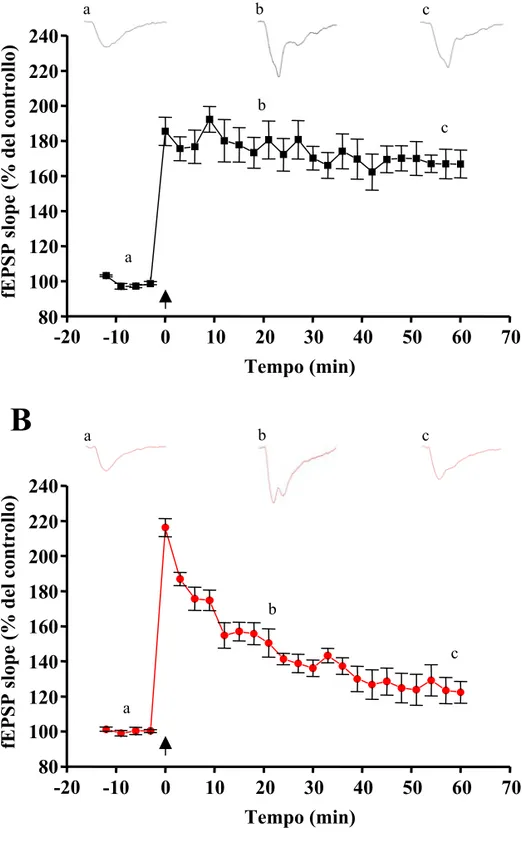
c b a a b cFigura 10: mancata espressione dell’LTP nei topi Cx36 KO A: La stimolazione ad alta frequenza delle collaterali di Schaffer induce un LTP nelle slice di controllo nel campo CA1 di ippocampo (n=5).
B: Nei topi Cx36 KO la stimolazione ad alta frequenza delle collaterali di Schaffer induce un STP ma non un LTP (n=5).
Il valore di ogni punto esprime la media del valore della slope iniziale di 5 fEPSP alla stimolazione test. Le tacce sopra ogni grafico rappresentano la media di 5 fEPSP evocati prima (a), 20 (b) e 60 (c) minuti dopo stimolazione tetanica.
A
aCSF normaleB
1 mV 20 sec aCSF MG2+-free/4 AP (50 µM)Figura 11: ridotta attività epilettica nei topi Cx36 KO
A) Registrazione extracellulare condotta nella regione CA3 con aCSF normale nei topi WT (nero) e nei topi Cx36 KO (rosso)
B) Registrazione extracellulare dell’attività epilettiforme nella regione CA3 indotta in aCSF MG2+-free/4 AP (50 µM).
RECETTORI NMDA Non- NMDA METABOTROPICI Risposta Cellulare Apertura canale per Ca2+, Na+, K+ Apertura canale per Na+e K+ Attivazione PKC e formazione di IP3 per scissione dei fosfolipidi di membrana
Agonisti N-metil-D-Acido aspartico Acido cainico, acido quisqualico, AMPA ACPD Antagonisti APV, MK801 CNQX, DNQX MCGP
Subunità NR1, NR2A-NR2D GluR1-GluR4