CAPITOLO IV
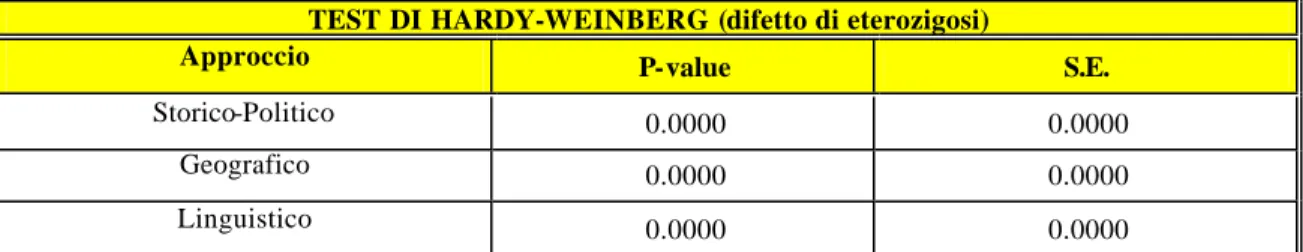
Come già detto in precedenza l’intero campione è stato tipizzato per 5 loci VNTR e STR, ma dal momento che per il marcatore D17S5 è stato riscontrato un forte difetto di eterozigosi, i dati relativi a tale locus sono stati esclusi dalle analisi comparative. Il fenomeno è stato rilevato dalle analisi con tutti i differenti tipi di approccio. Il calcolo della deviazione dall’equilibrio di Hardy-Weinberg per difetto di eterozigosi, calcolati per il complesso del campione analizzato in ognuno degli approcci analitici, mostra valori molto significativi (P=0,000), in tutti i casi senza eccezione alcuna (tabella 4.1).
Si pone dunque il problema di capire la ragione di tale situazione di forte omozigosi nel campione oggetto di questa tesi. Fenomeni di deriva genetica per effetto del fondatore o bottleneck (collo di bottiglia) causano all’interno delle popolazioni che ne sono oggetto una riduzione della diversità genetica e dunque un aumento dell’omozigosi. Dobbiamo però escludere che la popolazione in esame sia andata incontro ad uno qualsiasi di questi fenomeni. Il campione studiato è composto di individui che popolano una regione molto vasta e non isolata dal resto del continente europeo per cui si considera altamente improbabile la presenza di un fenomeno di drift o effetto del fondatore tale da generare la mancata variazione osservata rispetto all’attesa. La possibilità che una forte riduzione nelle dimensioni della popolazione, quali le pesti del 1348 e del 1353, abbia causato una forte riduzione di variabilità unicamente per gli alleli pesanti di questo locus o, per essere più precisi, per i genotipi combinazioni degli alleli più corti con quelli più lunghi appare, quantomeno, inverosimile. Si potrebbe obiettare che il sistema in esame è legato alla malattia di Miller-Dieker ed è dunque sottoposto a selezione, ma questa sindrome è molto rara e non interessa il sistema D17S5 in sé, ma la delezione dell’intera regione cromosomica (Tunien et al.1988; Batatian et al. 1990).
L’analisi dei dati ottenuti con il marcatore D17S5, riportati per ciascuno degli approcci sui quali è stata condotta l’analisi, suggerisce invece la presenza di un problema metodologico legato alla propria natura del locus ed al tipo di tecniche adoperate. L’allontanamento significativo dall’equilibrio per tale locus era già stato osservato nell’analisi di una popolazione greca (Kondopoulou et al. 1999), e valori molto vicini alla significatività sono descritti anche in un lavoro su una popolazione italiana (Buscemi et al.1994; Drmic e coll. 1998). Questi ricercatori hanno, anch’essi, individuato delle difficoltà
TEST DI HARDY-WEINBERG (difetto di eterozigosi)
Approccio P-value S.E.
Storico-Politico 0.0000 0.0000
Geografico 0.0000 0.0000
Linguistico 0.0000 0.0000
Tabella 4.1 : Valori di P e relativi errori standard nel test di Hardy-Weingerg in difetto di
eterozigosi calcolato per il locus D17S5 nel complesso della popolazione in ogni tipo di approccio analitico seguito.
tecniche di studio con questo sistema (Buscemi et al.1994; Drmic e coll. 1998). È stato possibile rilevare il problema, purtroppo, solo al momento dell’analisi statistica dei dati, per cui la correzione dello stesso è da rimandarsi a lavori succ essivi.
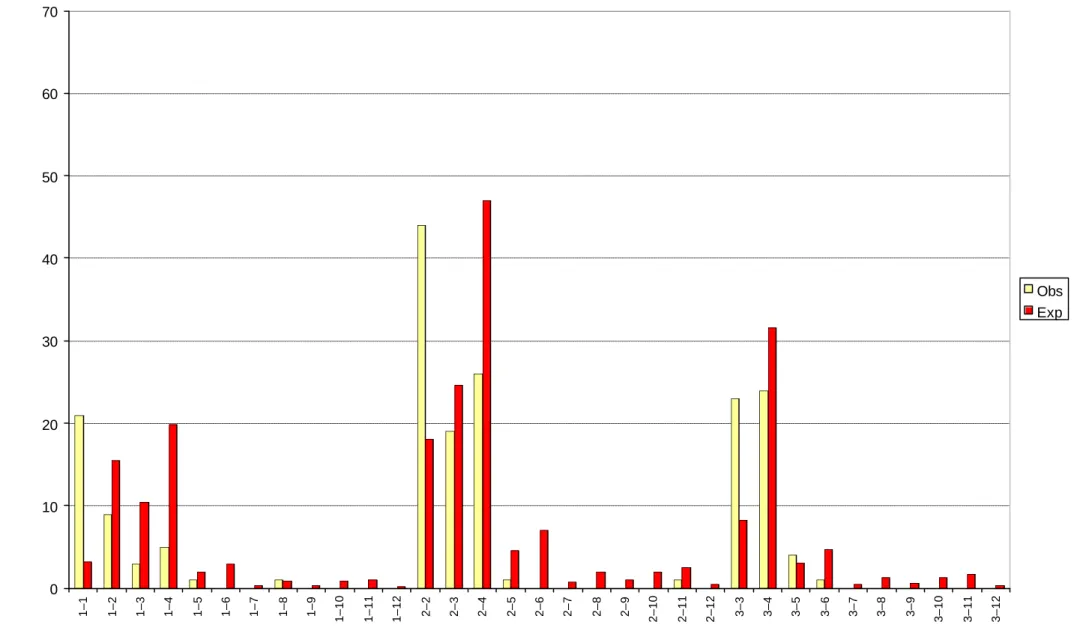
Lo studio delle frequenze alleliche del D17S5 mostra una netta prevalenza degli alleli con poche ripetizioni (tabella 4.2), ed un bassissimo numero di alleli con 7 o più ripetizioni. Come si può osservare dai grafici della distribuzione dei genotip i attesi ed osservati (figura 4.1), sono pressoché assenti i genotipi eterozigoti formati da alleli medio corti (da 1 a 7 ripetizioni) e alleli lunghi.
Il D17S5 è un sistema minisatellite con una sequenza ripetuta di 70pb (Wolff et al. 1988). Tale sequenza di ripetizione è molto lunga e, attraverso la PCR, per la propria natura del sistema di amplificazione, è possibile che venga favorita la moltiplicazione dei frammenti con un minor numero di sequenze ripetute in tandem. Alla fine del processo gli alleli più corti si troverebbero in concentrazione notevolmente maggiore nella soluzione amplificata e un metodo non sufficientemente risolutivo dei frammenti amplificati non consentirebbe la visualizzazione degli amplificati a concentrazione più bassa cioè quelli con un maggior numero di ripetizioni. La colorazione con bromuro d’etidio su gel di agarosio probabilmente non permette di visualizzare i frammenti più pesanti, le bande più sottili. Questo giustificherebbe l’elevato numero di omozigoti osservato rispetto all’atteso.
Allele 1 2 3 4 5 6 7 8 9 10 11 12 Frequenza 0,112 0,253 0,165 0,320 0,039 0,044 0,005 0,014 0,011 0,014 0,018 0,004
Tabella 4.2 : Frequenze alleliche del sistema D17S5 calcolate sulla totalità del campione della
Figura 4.1 : Rappresentazione grafica della distribuzione dei genotipi osservati ed attesi del sistema D17S5 0 10 20 30 40 50 60 70 1–1 1–2 1–3 1–4 1–5 1–6 1–7 1–8 1–9 1–10 1–11 1–12 2–2 2–3 2–4 2–5 2–6 2–7 2–8 2–9 2–10 2–11 2–12 3–3 3–4 3–5 3–6 3–7 3–8 3–9 3–10 3–11 3–12 Obs Exp
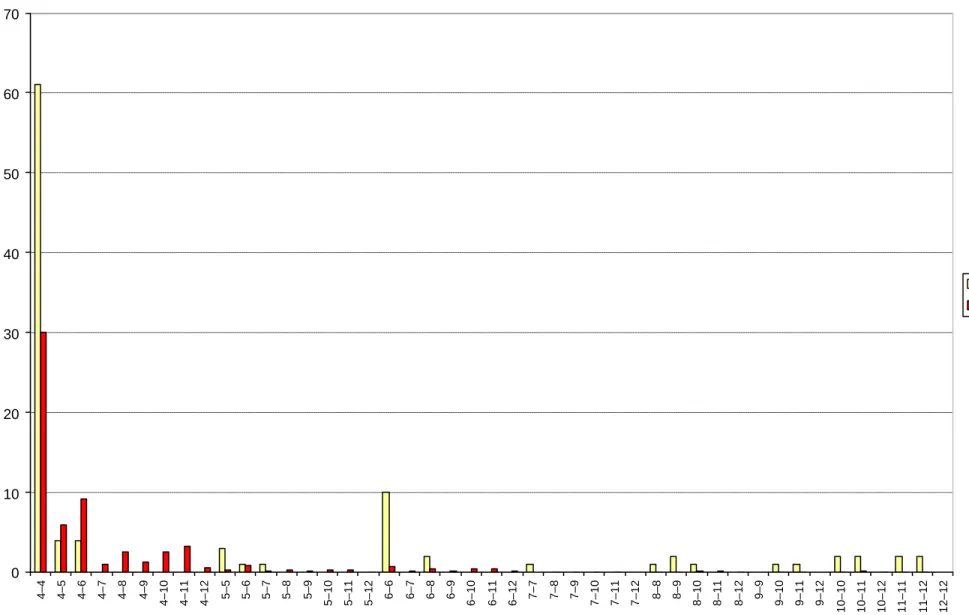
0 10 20 30 40 50 60 70 4–4 4–5 4–6 4–7 4–8 4–9 4–10 4–11 4–12 5–5 5–6 5–7 5–8 5–9 5–10 5–11 5–12 6–6 6–7 6–8 6–9 6–10 6–11 6–12 7–7 7–8 7–9 7–10 7–11 7–12 8–8 8–9 8–10 8–11 8–12 9–9 9–10 9–11 9–12 10–10 10–11 10–12 11–11 11–12 12–12 Obs Exp
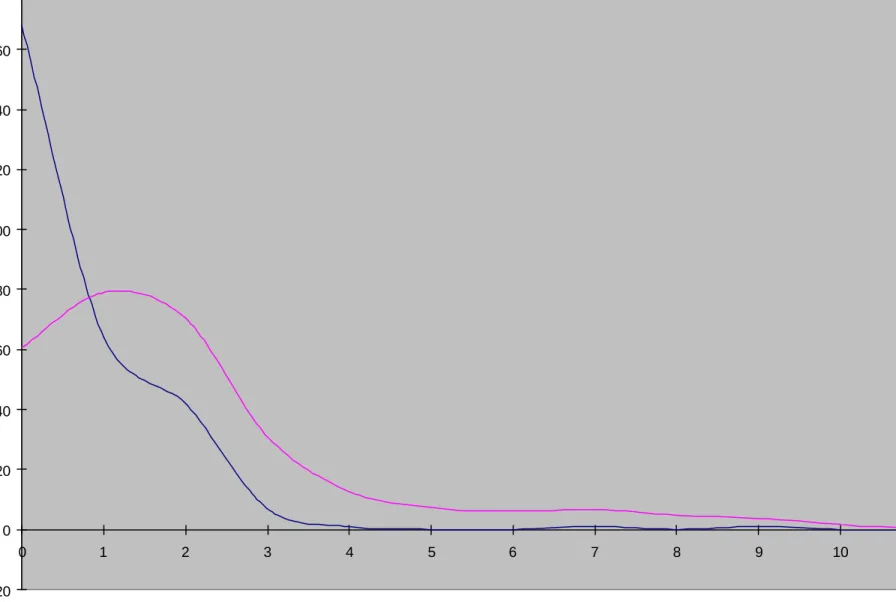
Un grafico sulle differenze alleliche osservate ed attese, ossia delle differenze in numero di ripetizioni fra gli alleli di un genotipo, ci permette di visualizzare la differenza fra le due situazioni (Figura 4.2). I valori sui dati osservati mostrano un andamento iperbolico con un leggerissimo picco secondario in corrispondenza di combinazioni alleliche con 2 sequenze ripetute di differenza. La curva dei valori attesi, al contrario, mostra un andamento unimodale con il picco a livello di una differenza di ripetizioni fra i due alleli e con valori asintotici, ma sempre diversi da zero, per differenze di addirittura 10 ripetizioni fra i due alleli. Questa situazione concorda perfettamente con quanto da noi ipotizzato per spiegare la forte omozigosi con combinazione degli alleli più corti osservata. Sarebbe necessario prendere alcuni accorgimenti nel momento in cui si effettua l’amplificazione per PCR. Si potrebbe ad esempio aumentare leggermente la concentrazione dei primers al fine di favorire l’accoppiamento fra tutti i filamenti con l’allele di maggiori dimensioni anche quando la macchina di replicazione lavora principalmente sugli alleli più corti. Si potrebbe anche diminuire la temperatura di annealing in modo tale da favorire l’appaiamento di tutto il DNA a singolo filamento con gli inneschi (primers). L’aspetto principale sul quale correggere la tecnica rimane comunque la visualizzazione dei frammenti amplificati, perché, ad ogni modo, l’amplificazione di alleli con molte pb di differenza continuerà a generare un maggior numero di frammenti più corti. L’uso di primers marcati con un fluorocromo e successiva analisi automatizzata, nella migliore delle ipotesi addirittura con una PCR quantitativa (Alonso, 2004).
Figura 4.2 : Rappresentazione grafica delle differenze alleliche attese (rosa) ed osservate (blu) per il sistema D17S5. -20 0 20 40 60 80 100 120 140 160 180 0 1 2 3 4 5 6 7 8 9 10 11 Obs Exp