2. Richiami teorici sulla convezione naturale in monofase e
bifase
2.1. Generalità
Lo scambio termico può esser definito come la trasmissione di energia da una regione ad un’altra dovuta ad una differenza di temperatura. La letteratura distingue in genere tre differenti modalità di trasmissione del calore: conduzione, irraggiamento e convezione. A rigore, solo la conduzione e l’irraggiamento dovrebbero essere classificati come processo di scambio termico perché solo questi due meccanismi dipendono dalla semplice esistenza di una differenza di temperatura. L’ultimo dei tre, la convezione, non è rigorosamente conforme alla definizione di scambio di calore dipendendo anche dal trasporto di materia; ma, poiché la convezione comporta anche la trasmissione di energia da regioni a temperatura superiore verso regioni a temperatura inferiore, è invalsa l’espressione “scambio di calore per convezione”. In questa tesi si è focalizzata l’attenzione proprio su quest’ultima modalità. In realtà, la convezione è un processo di trasporto di energia mediante l’azione combinata della conduzione, dell’accumulo di energia e del mescolamento; essa rappresenta il più importante meccanismo di scambio di energia tra una superficie solida ed fluido. La trasmissione di energia per convezione da una superficie, la cui temperatura sia superiore a quella del fluido circostante, avviene in diversi stadi. Dapprima il calore si trasmette per conduzione dalla superficie alle particelle di fluido adiacenti; l’energia così trasmessa fa aumentare l’energia interna e la temperatura delle particelle. Queste si muovono poi verso una regione del fluido a temperatura minore e si mescolano con esso cedendo parte della loro energia ad altre particelle: si ha quindi flusso tanto di materia quanto di energia, l’energia è cioè effettivamente immagazzinata nelle particelle ed è asportata dal loro moto. Questo meccanismo non dipende solamente da una differenza di temperatura e quindi non è strettamente conforme alla definizione di trasmissione del calore. L’effettiva conseguenza, comunque, è un trasporto di energia, che, avvenendo secondo la direzione del gradiente di temperatura, è anche classificato come un meccanismo di scambio termico ed è chiamato trasmissione del calore per convezione. Tale fenomeno si può distinguere in convezione naturale, o libera, e forzata, secondo la causa che determina il moto. Quando il moto dipende unicamente da differenze di densità dovute a gradiente di temperatura, in presenza di un campo gravitazionale, si parla di convezione naturale o libera; quando il moto è indotto da qualche agente esterno, una pompa od un ventilatore, il processo è chiamato convezione forzata. Poiché l’efficacia
dello scambio termico convettivo dipende in gran misura dal moto del fluido, lo studio della convezione è basato sulla conoscenza delle caratteristiche fluidodinamiche. Nella soluzione di problemi di trasmissione del calore occorre non solo individuare i meccanismi di scambio in gioco, ma anche stabilire se il processo è o non è a regime stazionario, detto anche regime permanente. Quando la potenza termica in un sistema non varia nel tempo, cioè è costante, la temperatura e tutte le altre variabili di stato, in ciascun punto non cambiano e si hanno condizioni stazionarie: in qualsiasi punto del sistema la potenza termica entrante deve essere esattamente uguale alla potenza termica uscente e non si ha alcuna variazione dell’energia interna. La maggior parte dei problemi ingegneristici riguarda sistemi a regime stazionario, come il flusso di calore dai prodotti della combustione all’acqua nei tubi di una caldaia e la trasmissione del calore da un fluido caldo ad un fluido freddo in uno scambiatore di calore. La trasmissione di calore in un sistema avviene in condizioni di regime non stazionario o transitorio quando la temperatura, e le altre grandezze di stato, in qualche punto variano nel tempo. Poiché una variazione di temperatura sta ad indicare una variazione di energia interna, si può concludere che l’accumulo e la diminuzione di energia è peculiare del flusso non a regime. I problemi di flusso termico transitorio sono più complicati di quelli relativi a flusso stazionario e spesso possono essere risolti soltanto con metodi approssimati. Si incontrano problemi di flusso termico transitorio nell’avviamento e nell’arresto di forni, caldaie, turbine e nei trattamenti termici dei pezzi fusi. Un caso particolare di flusso termico transitorio si ha quando un sistema è sottoposto a variazioni cicliche della temperatura dell’ambiente che lo circonda: in questi problemi la temperatura di ciascun punto del sistema assume periodicamente lo stesso valore ed anche la potenza termica e l’energia accumulata subiscono variazioni periodiche. Problemi di questo tipo rientrano nella trasmissione del calore in regime periodico o quasi stazionario. Esempi tipici sono la variazione giornaliera della temperatura di un edificio ed il flusso di calore attraverso le pareti del cilindro di un motore alternativo quando la temperatura dei gas nel cilindro cambia periodicamente [4].
La potenza termica specifica, q”, scambiata per convezione tra un fluido a velocità V e temperatura T∞ ed una superficie di forma arbitraria di sezione As ed a temperatura Ts≠ T∞,
si può esprimere con la relazione universalmente attribuita a Newton:
q” = h (Ts - T∞) [W/m2] (2.1) dove h è il coefficiente di scambio convettivo.
Poiché le condizioni di flusso variano punto per punto sulla superficie in questione, anche q” ed h varieranno lungo la superficie stessa. Il flusso totale scambiato si può allora ottenere integrando lungo As:
∫
= s A s dA q q " (2.2) o, nel caso di uniformità di temperatura sulla superficie,(
− ∞)
∫
= s A s s T hdA T q (2.3)Definendo un coefficiente di convezione medio, h, per l’intera superficie, il flusso totale scambiato sarà:
) ( − ∞
=hA T T
q s s (2.4)
Dividendo tra loro le equazioni 2.3 e 2.4, si ricava che il coefficiente convettivo medio e locale sono correlate in base all’equazione 2.5:
∫
= s A s s hdA A h 1 (2.5) Si può dunque evincere come i problemi di trasmissione del calore per convezione vertano sulla determinazione proprio del coefficiente di scambio convettivo h. Quest’ultimo dipende non solo dalle proprietà del fluido, quali densità, viscosità, conducibilità termica e calore specifico, ma anche dalla geometria della superficie e dalle condizioni dinamiche di flusso. Questa molteplicità di variabili indipendenti fa sì che h sia determinato dalle condizioni al contorno che si sviluppano sulla superficie coinvolta nello scambio [5].2.2. Le equazioni della convezione naturale
Andiamo ora a focalizzare la nostra attenzione sul meccanismo di scambio in convezione naturale, in quanto sarà il fenomeno di interesse della presente tesi.
La trasmissione del calore per convezione naturale ha luogo ogni qualvolta un corpo viene posto in un fluido che si trovi ad una temperatura maggiore o minore di quella del corpo stesso. A causa di suddetta differenza di temperatura, si origina un flusso di calore tra il corpo ed il fluido, che provoca variazioni nella densità degli strati fluidi prossimi alla superficie del corpo. Le differenze di densità determinano, in presenza di un campo di forza gravitazionale, il moto del fluido più pesante verso il basso e del più leggero verso l’alto; se il moto del fluido è dovuto unicamente a tali differenze si può parlare di convezione naturale o libera. Nella convezione naturale ed in quella forzata i moti
convettivi trasferiscono l’energia interna del fluido in modo essenzialmente analogo; tuttavia, nella libera l’intensità dei moti di mescolamento è generalmente minore e perciò i coefficienti di scambio sono inferiori rispetto a quelli che si riscontrano nella forzata. Tuttavia, il raffreddamento di molte apparecchiature avviene per convezione naturale, quali ad esempio, in campo elettronico, linee di trasmissione, trasformatori, raddrizzatori e fili riscaldati elettricamente, o gli elementi scaldanti di un forno elettrico. Per la generazione interna di calore, la temperatura di questi sistemi supera quella dell’ambiente circostante; al crescere della differenza di temperatura cresce anche la potenza termica scambiata finché si raggiunge una condizione di equilibrio in cui la potenza generata uguaglia quella dissipata. La convezione libera è il meccanismo di scambio termico predominante nel caso di radiatori, di pareti di edifici, del corpo umano quando è fermo in atmosfera calma. La determinazione dei carichi temici negli impianti di condizionamento o negli impianti frigoriferi richiede, quindi, la conoscenza dei coefficienti di scambio termico in convezione naturale. Sono dovute a questa anche le dispersioni termiche di condotte che trasportano vapor d’acqua od altri fluidi caldi. Negli ultimi anni è stato adottato questo meccanismo di scambio anche negli impianti nucleari per il raffreddamento degli elementi nei quali si genera calore per fissione. In tutti gli esempi visti fin ora, la forza di massa che dà luogo ai moti convettivi è la forza di gravità, ma potrebbe essere anche la forza centrifuga nel caso di macchine centrifughe a fluido, come nelle turbine a gas, oppure la forza di Coriolis nei moti rotazionali atmosferici od oceanici. Esistono inoltre differenti meccanismi per cui in un fluido si può sviluppare un gradiente di densità, ma nella maggior parte delle applicazioni dipende dalla presenza di un gradiente di temperatura. In generale, è noto come la densità di un fluido, liquido e/o gassoso, dipenda dalla temperatura, in particolare decresca (a causa dell’espansione del fluido stesso) con l’aumento della temperatura (∂ρ/∂T <0).
Dunque riassumendo, in convezione libera il moto del fluido è dovuto alle forze di galleggiamento che agiscono nel fluido stesso. Il galleggiamento a sua volta deriva dall’azione combinata tra la presenza di un gradiente di densità nel fluido e da una forza che agisce sul corpo proporzionale alla densità. In questa tesi focalizzeremo l’attenzione sul caso in cui il gradiente di densità dipende da un gradiente di temperatura e la forza coinvolta è quella gravitazionale.
Le equazioni che governano il fenomeno della convezione naturale prendono origine da bilanci di massa, quantità di moto ed energia, così come accade in convezione forzata. La differenza principale è proprio il ruolo delle forze di galleggiamento. Partendo dalle ipotesi
di regime stazionario, bidimensionale, proprietà termofisiche del fluido costanti e forza di gravità agente nel verso negativo dell’asse x, si assume anche, con un’eccezione, che il fluido sia incomprimibile. L’eccezione riguarda il considerare la densità del mezzo variabile solo nel termine di galleggiamento, in quanto questo induce il movimento del fluido. Questa assunzione è nota come approssimazione di Boussinesq. In base a questa nell’equazione del momento lungo la direzione verticale identificata con l’asse x, il termine della forza di massa per unità di volume agente sul fluido è dato da –ρg, dove ρ è la densità del fluido e g è l’accelerazione di gravità; dunque l’equazione diventa:
2 2 1 y u g x p y u v x u u ∂ ∂ + − ∂ ∂ − = ∂ ∂ + ∂ ∂
ν
ρ
(2.6)con il termine ∂p/∂y=0nell’equazione del momento lungo la direzione y. Dunque il gradiente di pressione lungo x nello strato limite deve essere uguale al gradiente di pressione nella regione al di fuori dello strato limite. D’altro canto, in questa regione u=v=0 e l’equazione 2.6 può esser semplificata nella 2.7:
g x p ∞ − = ∂ ∂ ρ (2.7) Sostituendo la 2.7 nella 2.6, si ottiene
(
)
2 2 y u g y u v x u u ∂ ∂ + − = ∂ ∂ + ∂ ∂ ∞ ρ ν ρ ρ (2.8)valida in ogni punto dello strato limite. Il primo termino alla destra dell’uguale rappresenta la forza i galleggiamento e le condizioni di moto si sviluppano proprio perché la densità ρ è variabile. Introducendo il coefficiente di espansione termica volumetrica, β, dato dall’Eq. 2.9: p T ∂ ∂ − = ρ ρ β 1 (2.9) Questo parametro è una proprietà del fluido che fornisce una misura di quanto la densità del fluido cambia in risposta ad una variazione di temperatura, a pressione costante. Esprimendo β come: T T − − − ≈ ∞ ∞
ρ
ρ
ρ
β
1 , (2.10) e dunque:(
∞)
∞ −ρ
≈ρβ
T −Tρ
) ( (2.11)Andando ora a sostituire l’equazione 2.11 nella 2.8, si ottiene l’equazione della conservazione della quantità di moto lungo la direzione x del moto:
2 2 ) ( y u T T g y u v x u u ∂ ∂ + − = ∂ ∂ + ∂ ∂ ∞
ν
β
(2.12) dove compare direttamente come la forza di galleggiamento, che governa il moto, sia correlata alla differenza di temperatura.Dal momento che gli effetti di galleggiamento sono presenti solo nell’equazione della quantità di moto, le equazioni di conservazione della massa e dell’energia sono le medesime della convezione forzata, e dunque:
0 = ∂ ∂ + ∂ ∂ y v x u (2.13) 2 2 ) ( y u T T g y u v x u u ∂ ∂ + − = ∂ ∂ + ∂ ∂ ∞
ν
β
(2.14) 2 2 y T y T v x T u ∂ ∂ = ∂ ∂ + ∂ ∂α
(2.15) La grossa differenza rispetto alle analoghe equazioni del caso forzato è che in naturale la soluzione dell’equazione di conservazione della quantità di moto non può prescindere dalla conoscenza della T, dunque le due equazioni 2.14 e 2.15 non sono più indipendenti tra loro. Il parametro β dipende chiaramente dal tipo di fluido coinvolto nello scambio. Per un gas limite, per il quale è valida la legge di stato dei gas, si ha ρ=p/RT e dunque:T RT p T p 1 1 1 2 = = ∂ ∂ − =
ρ
ρ
ρ
β
(2.16) dove T è la temperatura termodinamica assoluta. Per liquidi e gas reali, β è ricavabile da apposite tabelle, in funzione della temperatura.I parametri che caratterizzano il moto possono essere adimensionalizzati e si ottiene:
L x x∗ = L y y∗ = 0 u u u∗ = 0 u v v∗ = ∞ ∞ ∗ − − = T T T T T s
dove L è una lunghezza caratteristica e u0 una velocità di riferimento arbitraria.
Le equazioni 2.14 e 2.15 diventano:
(
)
2 2 2 0 Re 1 ∗ ∗ ∗ ∞ ∗ ∗ ∗ ∗ ∗ ∗ ∂ ∂ + − = ∂ ∂ + ∂ ∂ y u T u L T T g y u v x u u L sβ
(2.17)2 2 Pr Re 1 ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∂ ∂ = ∂ ∂ + ∂ ∂ y T y T v x T u L (2.18) In queste equazioni compaiono due numeri adimensionali molto usati nello studio dei fenomeni convettivi in genere: il numero di Reynolds ed il numero di Prandtl.
Partendo dal secondo, esso è funzione solo delle proprietà termofisiche del fluido ed è dato da:
α
v =
Pr (2.19) dove ν è la viscosità cinematica del fluido, espressa in m2/s ed α la diffusività termica, sempre in m2/s. Le proprietà del fluido vengono calcolate alla temperatura di film, che corrisponde alla media aritmetica tra la temperatura del fluido e quella di parete.
Il numero di Reynolds è un parametro convenzionalmente usato in convezione forzata, dato da:
ν
VL =
Re (2.20) Dove V è la velocità del fluido ed L una grandezza geometrica caratteristica del problema. Nel caso dell’equazione 2.17 e 2.18 il Reynolds è dato da:
ν
L u0
Re= (2.21) Essendo u0 una velocità di riferimento arbitraria, che non è nota però in regime di
convezione naturale (al contrario di V imposta dall’esterno, nel caso forzato), conviene moltiplicare il termine legato alle forze di galleggiamento che compare nel primo termine a destra dell’uguale in Equazione 2.17 per ReL2; da qui si ottiene:
(
)
(
)
2 3 2 0 2 0ν
β
ν
β
u L g T T L u L T T g GrL s s ∞ ∞ = − − = (2.22) Il numero di Grashof, GrL, ha lo stesso ruolo nella convezione libera del Re nella forzata.Mentre il Reynolds esprime il rapporto tra le forze di inerzia e quelle viscose agenti sul fluido, il Grashof rappresenta il rapporto tra le forze di galleggiamento e quelle viscose che agiscono sull’elemento di fluido. Infine introduciamo il numero di Nusselt:
f k hL
Nu = (2.23) che rappresenta in termini adimensionali il coefficiente di scambio convettivo h. Al denominatore compare la conducibilità termica del fluido, espressa in W/mK.
In generale NuL=f(ReL, GrL, Pr); in realtà ciò è vero solo nel caso di convezione mista, in
cui si ha cioè la co-presenza di forzata e naturale, in altre parole quando il rapporto (GrL/ReL2) ≈ 1. Se invece tale rapporto è molto minore di 1, gli effetti della convezione
naturale sono trascurabili rispetto a quelli della forzata, nel caso sia molto maggiore dell’unità accade esattamente il contrario.
Nella presente tesi lo studio riguarda lo scambio termico tra una superficie cilindrica ed acqua distillata in convezione naturale. Dunque si parla di moto convettivo esterno, per distinguerlo da quello detto interno nei condotti, in condizioni laminari. La differenza tra moto laminare e turbolento è che il primo è un moto ordinato e si possono distinguere delle linee di flusso lungo cui la particella fluida si muove; nel secondo invece si ha una situazione di moto caotica caratterizzata da fluttuazioni di velocità. Queste fluttuazioni incrementano il trasporto di quantità di moto, energia e massa. La transizione dal regime di moto laminare a quello turbolento dipende dagli ordini di grandezza che raggiungono le forze di galleggiamento e quelle viscose nel fluido. Per convezione si è adottato un nuovo parametro adimensionale, il numero di Rayleigh, Ra, che rappresenta il prodotto di Gr per Pr. Per una piastra verticale il limite che segna la transizione da laminare a turbolento è:
(
)
9 3 , , Pr ≈10 − = = ∞να
β
T T x g Gr Ra s c x c x (2.24)Una trattazione dettagliata sulla stabilità e sulla fenomenologia della transizione tra i due regimi di moto è fornita da Gebhart [6-7]. Come nel caso di convezione forzata, anche per la naturale, la turbolenza ha una notevole influenza sullo scambio termico: il problema si complica ulteriormente anche dal punto di vista matematico ed infatti ci si affida per lo più a correlazioni di tipo empirico.
2.3 Convezione naturale esterna su superfici cilindriche
Dalle precedenti considerazioni si evince che il numero di Nusselt è funzione dei numeri di Grashof e Prandtl, cioè Nu=f(Gr, Pr).
Servendosi di un’equazione di questo, sono stati correlati nella Fig.2.1 i dati sperimentali di vari autori relativi a convezione libera da tubi e fili orizzontali, riportando il valor medio del numero di Nussselt, h /D kf , in funzione del prodotto dei numeri di Gr e Pr, nella
forma Cp
ρ
gβ
T/µ
kf 2 ∆. Le proprietà fisiche sono calcolate alla temperatura di film. Si nota che i dati per fluidi molto diversi tra loro, quali aria, glicerina ed acqua, sono ben
correlati per valori del prodotto GrPr compresi nell’intervallo 105÷107 per cilindri che vanno da piccoli fili a grandi condotte [8].
Fig.2.1: Correlazione di dati relativi alla trasmissione del calore per convezione libera da cilindri orizzontali a gas e liquidi [8]
Lo studio della convezione naturale esterna su superfici cilindriche si basa per lo più su correlazioni di tipo empirico, valide in certi campi del numero di Rayleigh. Ne riportiamo alcune qui di seguito, più comunemente usate, valide per cilindri orizzontali, come nel nostro caso di studio, catalogate in un lavoro di review di Morgan [9].
La formulazione di riferimento per tutte tali correlazioni è:
n D f D D CRa k h Nu = = (2.25) C e n sono ricavate dalla tabella 2.1:
Tabella 2.1
Costanti dell’equazione 2.25 per convezione naturale esterna su cilindri circolari orizzontali RaD C n 10-10÷10-2 0,675 0,058 10-2÷102 1,02 0,148 102÷104 0,850 0,188 104÷107 0,480 0,250 107÷1012 0,125 0,333
Churchill and Chu [10] hanno proposto una singola correlazione valida in un ampio range di Ra:
(
)
[
]
2 27 / 8 16 / 9 6 / 1 Pr / 559 , 0 1 387 , 0 60 , 0 + + = D D Ra Nu per 10-5<RaD<1012 (2.26)Mentre per cilindri di diametro molto piccolo, dunque fili, la correlazione di Elenbaas [11] sembra fornire un miglior accordo con i dati sperimentali:
235 Pr / 6 3 Gr e Nu − Nu = GrPr < 104 (2.27) Il campo termico che circonda un cilindro orizzontale riscaldato in aria è mostrato nella Figura 2.2, che riporta le frange di interferenza fotografate da Eckert e Soehnghen [12]. Il moto è laminare lungo tutta la superficie. La minore distanza tra le frange di interferenza sulla parte inferiore del cilindro indica un maggior gradiente di temperatura e quindi una conduttanza per unità di superficie maggiore che sulla parte posteriore.
In figura 2.3 è riportata la variazione della conduttanza superficiale con l’angolo α, per due numeri di Grashof. I risultati sperimentali non differiscono in modo apprezzabile dai valori teorici di Herman [13], che, per l’aria ovvero per Pr=0,74, ricavò l’equazione:
) ( 604 , 0 1/4 ,α D
ϕ
α
D Gr Nu = (2.28)Fig.2.2: Campo termico attorno ad un cilindro orizzontale, per moto laminare [12]
Fig.2.3: Conduttanza locale adimensionale per unità di superficie lungo la circonferenza di un cilindro orizzontale in convezione libera laminare [12]
L’angolo α è misurato dalla posizione orizzontale e di valori numerici della funzione φ(α) sono i seguenti: Tabella 2.2 Valori di α e φ(α) α φ(α) -90 0,76 -60 0,75 -30 0,72 0 0,66 30 0,58 60 0,46 75 0,36 90 0
metà inferiore metà superiore
Un’equazione per il coefficiente medio di scambio termico da un filo od un tubo isolati in convezione libera, suggerita da Mc Adams [8], sulla base dei dati sperimentali riportati in Fig.2.1, è la seguente:
(
)
1/4 Pr 53 , 0 Gr NuD = (2.29) L’equazione è valida per Pr maggiore di 0,5 e per Gr tra 103 e 109. Per diametri molto piccoli, è stato dimostrato come la potenza termica dissipata per unità di lunghezza sia quasi indipendente dal diametro del filo. La conduttanza media per unità di superficie, quando GrD è minore di 103, è determinata mediante la curva A-A di Fig.2.1, ottenuta dapunti sperimentali nel campo dei bassi numeri di Grashof. L’inizio della turbolenza nella convezione libera su cilindri orizzontali per fluidi diversi dai metalli liquidi si ha per un valore di GrDPr/D3 (con D espresso in metri) di circa 3,5·1013 m-3 [14]. Sulla base di tale
valore, possiamo affermare che nelle condizioni e nei regimi di scambio da noi indagati, non si verifica mai la transizione dal regime laminare a quello turbolento. Si è osservato che nel moto turbolento il flusso termico può essere notevolmente incrementato senza un corrispondente aumento della temperatura della superficie, in quanto aumenta il coefficiente di scambio convettivo.
2.4 Principi dello scambio termico in ebollizione
La trasmissione del calore in ebollizione è un processo convettivo comprendente un cambiamento di fase. I fenomeni di scambio termico per ebollizione sono notevolmente più complessi di quelli per convezione senza cambiamento di fase, poiché, oltre a tutte le variabili associate alla convezione, assumono importanza anche quelle associate al cambiamento di fase. Mentre nella sola fase liquida, la geometria del sistema, la viscosità, la densità, la conducibilità termica, il coefficiente di dilatazione ed il calore specifico del
fluido sono sufficienti a descrivere il processo, nello scambio termico per ebollizione giocano un ruolo importante le caratteristiche superficiali, la tensione superficiale, il calore latente di evaporazione, la pressione, la differenza di densità delle due fasi ed eventualmente altre proprietà del vapore. In conseguenza di un così gran numero di variabili in gioco, tutt’oggi non sono disponibili né equazioni generali che descrivano il processo di ebollizione, né correlazioni generali tra i dati relativi allo scambio termico per ebollizione. Negli ultimi cinquanta anni, grazie alla fotografia veloce ad elevata risoluzione, si è rilevato la presenza di diversi regimi di ebollizione nei quali i meccanismi di trasmissione del calore differiscono radicalmente [15-18]. Per correlare i dati sperimentali è perciò necessario descrivere ed analizzare separatamente ciascun regime di ebollizione. Per una miglior comprensione fisica dei fenomeni caratteristici dei vari regimi di ebollizione, si considererà dapprima un sistema semplice costituito da una superficie riscaldante, quale una piastra piana od un filo, immersa in una massa di acqua alla temperatura di saturazione senza agitazione indotta dall’esterno: questo fenomeno è noto come ebollizione di massa. Finché la temperatura della superficie supera la temperatura di ebollizione del liquido solo di alcuni gradi, il calore viene trasmesso per convezione libera al liquido vicino alla superficie riscaldante; i moti convettivi determinano il movimento del liquido surriscaldato e sulla superficie libera del liquido avviene l’evaporazione. Ciononostante, lo scambio termico avviene unicamente per convezione naturale, poiché soltanto parte del liquido è a contatto con la superficie riscaldante. Se la temperatura della superficie riscaldante aumenta, accade che in alcune zone il contenuto energetico del liquido adiacente alla superficie diventa talmente alto che alcune molecole riescono a staccarsi dalle molecole circostanti, vengono trasformate da liquido in nuclei di vapore, formando infine una bolla. Questo processo avviene contemporaneamente in certi punti particolari della superficie riscaldante. Le bolle di vapore sono inizialmente piccole e condensano prima di raggiungere la superficie libera ma, quando la temperatura viene ulteriormente innalzata, diventano più numerose e più grandi finché riescono a raggiungere la superficie libera del liquido. L’appropriata forma dell’equazione di Newton nel caso di scambio termico in presenza di ebollizione é:
q”= h (Ts-Tsat) =h ∆Tsat (2.30)
dove ∆Tsat= Ts-Tsat è chiamata grado di surriscaldamento e rappresenta la differenza di
temperatura tra la superficie riscaldata e quella di saturazione del liquido. Abbiamo già accennato a come il processo sia caratterizzato dalla formazione di bolle di vapore, che crescono e successivamente si distaccano dalla superficie. La crescita di tali bolle dipende
dal parametro ∆Tsat, dalla natura della superficie, dalle proprietà termodinamiche del fluido
e dalla tensione superficiale. In pratica la dinamica di crescita delle bolle influenza il moto del fluido in prossimità della superficie e dunque il coefficiente di scambio convettivo. L’ebollizione può avvenire in diverse condizioni: il pool boiling, come nel nostro caso, si verifica quando il liquido è stagnante ed il suo moto attorno alla superficie riscaldata è dovuto unicamente alla convezione libera ed al miscelamento indotto dalla crescita delle bolle e dal loro distacco. Al contrario, nella convezione forzata in presenza di ebollizione, il moto del fluido è indotto da cause esterne, a cui poi si vanno a sommare anche gli effetti della convezione libera e del miscelamento delle bolle. Un caso molto studiato è quello del flow boiling, per le sue notevoli applicazioni in campo tecnico: esso riguarda la convezione forzata di un liquido in cambiamento di fase all’interno di tubi e condotti. Inoltre l’ebollizione può essere sottoraffreddata o satura. Nel primo caso la temperatura del liquido è al di sotto della sua temperatura di saturazione e le bolle formatesi sulla superficie condensano nel liquido. In ebollizione satura, invece, la temperatura del liquido eccede leggermente la temperatura di saturazione e le bolle formatesi sulla superficie sono spinte verso il liquido più freddo da forze di galleggiamento.
Andiamo ad esaminare il fenomeno da noi indagato in questa tesi, cioè il pool boling, sia in condizioni sottoraffreddate, sia sature.
2.5 Pool boiling in condizioni sature
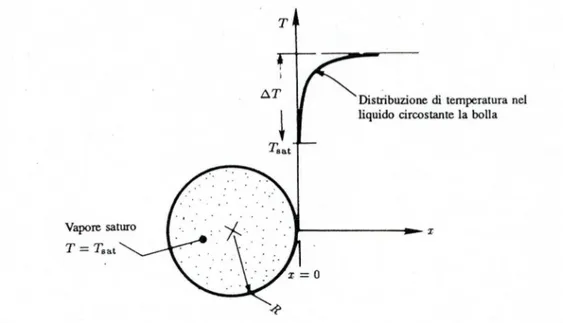
La Fig. 2.4 mostra la distribuzione di temperatura nel caso di pool boiling in condizioni sature.
Fig.2.4: Andamento della temperatura all’interfaccia liquido-vapore, in condizioni di pool boiling saturo
Sebbene sia visibile una forte diminuzione della temperatura del liquido vicino alla superficie solida, la temperatura della maggior parte di volume di liquido rimane al di sopra della saturazione, anche se di poco. Le bolle formatesi nell’interfaccia liquido-solido aumentano e vengono trasportate via da questa regione di interfaccia. Nukiyama [19] fu il
primo ad identificare diversi regimi di pool boiling usando l’apparato di Fig.2.5: il flusso termico trasmesso da un filo di nichrome ad acqua satura è stato calcolato misurando la corrente che passava nel filo stesso e la caduta di potenziale ai suoi capi. La temperatura del filo è stata determinata misurando la sua resistenza elettrica, al variare della temperatura. Questo sistema è stato denominato a flusso termico imposto, dove la temperatura del filo Ts è la variabile dipendente ed il flusso appunto, q”, quella
indipendente.
Fig.2.5: Apparato a flusso termico controllato usato da Nukiyama per costruire la curva di ebollizione
Fig.2.6: Curva di ebollizione di Nukiyama per acqua satura
Seguendo la curva di Fig.2.6, si nota come il flusso q” aumenti con il grado di surriscaldamento, prima lentamente e poi rapidamente. Nukiyama osservò che l’ebollizione, identificabile con la presenza di bolle, non aveva inizio fino a ∆Tsat circa pari
∆Tsat[°C]
q” [W/m2]
a 5°C. Da questo punto in poi, l’aumento di q” determinava un rapido incremento di ∆Tsat,
fino ad un punto in cui istantaneamente la temperatura del filo arrivava al suo punto di fusione ed avveniva il burnout, o bruciamento, del filo stesso. Tuttavia, ripetendo l’esperimento con un filo di platino con più alto punto di fusione (2045K contro i 1500K del nichrome), Nukiyama riuscì a mantenere alti flussi al di sopra del flusso massimo q”max, senza che si verificasse il burnout. Quando egli andò a diminuire progressivamente
la potenza fornita al filo, la variazione di ∆Tsat seguì la curva di raffreddamento indicata
dalle frecce in Fig. 2.6. Quando la potenza arrivò al punto q”min, un’ulteriore diminuzione
della stessa causò la caduta del ∆Tsat ed il raffreddamento riprese a seguire la curva
originale del riscaldamento fino al punto di inizio saturazione. Nukiyama attribuì questa sorta di effetti di isteresi alla metodologia da lui utilizzata, cioè a flusso termico imposto, ed era convinto che con un sistema a temperatura imposta la parte mancante della curva (tratteggiata in Fig.2.6) potesse essere ricavata sperimentalmente. Queste sue ipotesi furono più tardi confermate da Drew e Mueller [20]. Infatti, essi, condensando vapore dentro un tubo a differenti pressioni, riuscirono a rendere variabile indipendente il ∆Tsat
relativo all’ebollizione sulla superficie esterna del tubo ed ottennero la porzione mancante della curva. Grazie a questi risultati sopra descritti è stato possibile costruire la curva di ebollizione di Fig. 2.7:
Fig.2.7: Curva di ebollizione per un liquido in quiete (acqua satura pressione atmosferica)
Tale curva si riferisce ad acqua alla pressione di un’atmosfera, anche se è stato scoperto che comportamenti analoghi si riscontrano per fluidi diversi, e può esser esaminata dividendola in differenti regioni:
1. Ebollizione in convezione naturale
Il regime di convezione naturale permane fino a ∆Tsat< ∆Tsat,A dove ∆Tsat,A è all’incirca
pari a 5°C. In questa fase la quantità di vapore in contatto con la fase liquida è insufficiente a causare l’ebollizione alla temperatura di saturazione. Man mano che ∆Tsat aumenta,
iniziano a formarsi bolle, ma al di sotto del punto (denominato in letteratura, ONB, onset of nucleate boiling), il moto del fluido dipende principalmente dalla convezione libera. In base al tipo di moto, cioè se laminare o turbolento, h varia con ∆Tsat elevato a 1/3
(laminare) od a ¼ (turbolento) e q” varia con ∆Tsat elevato a 5/4 (laminare) o 4/3
(turbolento).
2. Ebollizione nucleata
Tale regime sussiste per ∆Tsat,A ≤∆Tsat ≤∆Tsat,C, dove ∆Tsat,C è pari a circa 30°C. In questa
fase si possono distinguere due differenti regimi. Nella regione da A a B, si formano delle bolle isolate nei siti di nucleazione che, separandosi dalla superficie, incrementano h e q”. La maggior aliquota dello scambio termico dipende dal trasferimento diretto di calore dalla superficie riscaldata al liquido in movimento in prossimità della stessa, e non dal vapore che cresce sulla superficie. Quando ∆Tsat aumenta, più siti di nucleazione diventano attivi,
le bolle crescono in numero ed iniziano a interferire tra loro ed anche a coalescere. Il liquido caldo viene continuamente spinto lontano dalla superficie scaldante verso la massa di liquido più fredda ed inoltre nascono delle intense correnti microconvettive quando le bolle di vapore si allontanano ed il liquido più freddo fluisce verso la superficie a riempire i vuoti. Nella regione B-C, la quantità di vapore è talmente accresciuta che si vedono getti o colonne di vapore, che poi fondono tra loro fino a diventare un’unica colonna di vapore. Questa condizione è visibile in Fig.2.8. L’elevata densità ed interferenza delle bolle inibisce il moto del liquido vicino alla superficie. Il punto P della curva di Fig. 2.7 corrisponde ad un punto di flesso della curva stessa, dove il coefficiente h è massimo. A questo punto h incomincia a decrescere con l’aumento di ∆Tsat, sebbene q”, dato dal
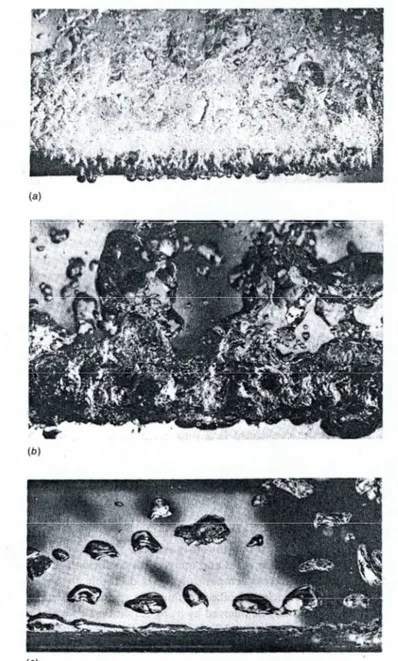
Fig. 2.8: Visualizzazioni dell’ebollizione del metanolo su un tubo orizzontale; (a)
ebollizione nucleata con getti e/o colonne di vapore, (b) fase di transizione , (c) ebollizione a film.
Questo trend si verifica perché, per ∆Tsat >∆Tsat,P, l’incremento relativo di ∆Tsat supera il
decremento relativo di h. Nel punto C, invece l’ulteriore incremento di ∆Tsat è esattamente
uguale alla riduzione di h. In prossimità del punto C il numero delle colonne di vapore cresce, ma, poiché ogni nuova colonna occupa lo spazio precedentemente occupato dal liquido, c’è un limite al numero massimo di colonne di vapore che può essere emesso dalla superficie. Tale limite viene raggiunto quando lo spazio tra queste colonne non è più sufficiente a contenere le correnti di liquido che devono muoversi verso la superficie calda per sostituire il liquido evaporato per formare le colonne di vapore. Il massimo flusso, q” è usualmente denominato punto critico (in letteratura anglosassone, CHF, critical
heat flux) e generalmente è superiore a 1MW/m2. Arrivati a q”max, la quantità di vapore è
così elevata, che il liquido non riesce più a bagnare e, dunque, a raffreddare, la superficie. Dal momento che i flussi smaltiti ed i coefficienti h più elevati sono associati con modesti valori di ∆Tsat, nella pratica è auspicabile operare nel regime di ebollizione nucleata: in
questa zona h raggiunge ordini di grandezza di 104W/Km2, valori di gran lunga superiori a quelli ottenibili in condizioni di convezione monofase.
1. Zona di transizione
La regione tra il punto C ed L, è denominata di transizione, od anche regione a film instabile o a film parziale. Il grado di surriscaldamento in L ha raggiunto circa 120°C. Il processo di formazione delle bolle è divenuto ormai molto rapido, tanto che una pellicola di vapore, denominata film, inizia a ricoprire la superficie. In ogni punto della stessa, si oscilla tra le condizioni di ebollizione nucleata ed a film, ma la frazione di superficie coperta di vapore aumenta con l’aumento di ∆Tsat. Poiché la conducibilità termica del
vapore è molto minore di quella del liquido, h (e q”) devono necessariamente decrescere con l’aumento di ∆Tsat.
2. Ebollizione a film
La regione di ebollizione a film esiste per ∆Tsat> ∆Tsat,L. Il punto L è noto come punto di
Leidenfrost ed il flusso corrispondente come punto di minimo flusso termico, q”min. La
superficie è ormai ricoperta da un film di vapore e lo scambio termico dalla superficie al liquido avviene solo per conduzione attraverso il vapore. Fu proprio Leidenfrost nel 1756 ad osservare per primo che goccioline di liquido posatesi sul film di vapore, formatosi sopra una superficie metallica incandescente, non bollivano immediatamente, ma scorrevano quasi sul metallo, perché il film stesso isolava la goccia.
All’aumentare della temperatura della superficie, inizia a divenire influente anche lo scambio radiativo attraverso il film di vapore ed il flusso aumenta con ∆Tsat.
La Fig.2.8 illustra le fasi di formazione di vapore e la dinamica delle bolle in ebollizione nucleata, nella fase di transizione e nella regione a film. Tali fotografie, fatte da J.W. Westwater, dell’Università dell’Illinois a Champaign-Urbana, sono state eseguite su un tubo orizzontale immerso in metanolo. Ritornando ai risultati trovati da Nukiyama, va precisato che se il flusso termico è la variabile indipendente non sarà possibile raggiungere il punto L, ma si passerà direttamente dal punto C a C’. Se il solido ha un punto di fusione elevato allora si avrà la transizione dall’ebollizione nucleata a quella a film; se, invece, come per la maggior parte dei solidi, la temperatura del punto C’supera il punto di fusione, il riscaldatore può fondere ed infatti il punto C’ è noto come punto di burnout o di crisi
termica, la cui conoscenza è determinante nelle applicazioni pratiche. Nel caso invece in cui il ∆Tsat sia la variabile indipendente si avrà ebollizione in regime di transizione ed il
flusso termico diminuirà. Un'altra visualizzazione delle fasi di ebollizione nucleata ed a film è riportata in Fig.2.9 (a) e (b) rispettivamente:
(a) (b)
Fig.2.9: Visualizzazioni delle fasi di ebollizione su un filo riscaldato elettricamente in acqua a pressione atmosferica; (a) ebollizione nucleata, (b) ebollizione a film.
2.6 Pool boiling in condizioni sottoraffreddate
Quando la temperatura della superficie è maggiore della temperatura di saturazione può aversi ebollizione localizzata in prossimità della superficie anche se la temperatura di tutto il liquido è inferiore alla temperatura di ebollizione. Il processo di ebollizione in un liquido la cui temperatura sia inferiore alla temperatura di saturazione, ma il cui strato limite sia sufficientemente surriscaldato da consentire la formazione di bolle vicino alla superficie scaldante è di solito chiamato trasmissione di calore ad un liquido in ebollizione sottoraffreddata od ebollizione superficiale. I meccanismi di formazione delle bolle e di trasmissione del calore sono simili a quelli descritti per i liquidi alla temperatura di saturazione, tuttavia le bolle sono più numerose, mentre le loro dimensioni e la loro vita media diminuiscono al diminuire della temperatura del liquido, per un certo flusso termico. A causa del maggior numero di bolle, l’agitazione del liquido determinata dal loro movimento è più intensa in un liquido sottoraffreddato che in un liquido saturo e si possono ottenere flussi termici molto maggiori prima che avvenga la bruciatura.
Fig.2.10: Movimento del liquido determinato da una bolla in ebollizione sotto raffreddata
Il meccanismo mediante il quale una bolla trasmette calore in acqua sottoraffreddata e degasata è illustrato in Fig.2.10, e può esser schematizzato in una serie di stadi successivi:
a) il liquido vicino alla parete si surriscalda;
b) un nucleo di vapore, di grandezza sufficiente a permettere la nascita di una bolla, si è formato in corrispondenza di una cavità o di una screpolatura della superficie; c) la bolla cresce ed il sovrastante strato di liquido surriscaldato viene spinto lontano
dalla parete verso il liquido più freddo: il conseguente movimento del liquido è indicato dalle frecce;
d) la sommità della superficie della bolla si estende all’interno del fluido più freddo. La sua temperatura diminuisce; la bolla continua a crescere in virtù dell’inerzia del liquido, ma ad una velocità minore che durante lo stadio c, poiché riceve meno calore per unità di volume;
e) l’inerzia del liquido ha determinato una crescita tale della bolla che la sua superficie superiore si estende all’interno del liquido più freddo; la bolla perde più calore per evaporazione e convezione di quanto ne riceva per conduzione dalla superficie scaldante;
f) le forze di inerzia sono state dissipate e la bolla comincia ad afflosciarsi; il liquido freddo occupa lo spazio resosi libero;
g) la fase vapore si è condensata, la bolla è scomparsa e la parete calda è investita da una corrente di liquido freddo;
h) il film liquido si è ristabilito ed il ciclo si ripete.
La descrizione della vita di una bolla vale qualitativamente fino allo stadio (e) anche per i liquidi che contengono gas disciolti, per le soluzioni di più di un liquido e per i liquidi saturi. In questi casi, tuttavia, la bolla non si affloscia, ma viene strappata alla superficie
dai moti convettivi o dalle forze ascensionali e si determina ugualmente un vuoto occupato dal fluido più freddo che affluisce dall’alto. Ciò che in ogni caso accade alle bolle, sia che si collassino sulla superficie, sia che vengano spazzate via, ha una piccola influenza sul meccanismo di scambio termico, che dipende principalmente dall’azione di pompaggio e dall’agitazione del liquido. La principale variabile che controlla il meccanismo di formazione della bolla è il surriscaldamento. Va osservato, tuttavia, che nel regime di ebollizione a nuclei la variazione del surriscaldamento, indipendentemente dalla temperatura della massa del fluido, è relativamente piccola in un grande intervallo del flusso termico. Ai fini progettuali, il coefficiente di scambio termico convenzionale, che è basato sulla differenza di temperatura tra la massa del fluido e la superficie, è perciò soltanto di secondario interesse, se paragonato al massimo flusso termico che può essere ottenuto nell’ebollizione nucleata ed alla temperatura della parete alla quale comincia l’ebollizione.
Il parametro di interesse in pool boiling in condizioni sottoraffreddate, senza effetti di convezione forzata, è il grado di sottoraffreddamento, ∆TSUB, cioè la differenza tra la
temperatura di saturazione del liquido e la sua temperatura effettiva, dunque ∆TSUB=Tsat-Tl.
Nella zona della curva di Fig.2.7, dove si ha regime di convezione naturale, il flusso termico è stato dimostrato incrementare con (Ts-Tl)5/4 o (∆Tsat +∆TSUB)5/4. In regime di
ebollizione nucleata l’influenza del sottoraffreddamento è considerata nulla sebbene sia stato dimostrato che il massimo ed il minimo flusso termico, q”max e q”min, incrementano
leggermente con ∆TSUB. In ebollizione a film, l’influenza del ∆TSUB sullo scambio termico
è invece significativa, anche se in letteratura sono presenti scarsi riferimenti.
2.7 Influenza della superficie sull’ebollizione
L’influenza della rugosità superficiale sul massimo ed il minimo flusso termico ed in regime di ebollizione a film è considerato trascurabile. Nelle condizioni nucleate invece, è stato dimostrato da Berensen [21] come l’incremento della rugosità superficiale possa portare all’incremento di un ordine di grandezza del flusso termico dissipato. Questa influenza è riscontrabile anche nelle relazioni proposte da Yamagata [22]. S. Faggiani et al. [23-25] hanno proposto delle correlazioni che legassero tra loro numero di germi, flusso termico, differenza di temperatura, frequenza delle bolle e loro diametro, con i principali parametri caratteristici della morfologia e dello stato chimico - fisico superficiale della superficie riscaldata.
Fig.2.11: Formazione dei siti di nucleazione; (a) cavità bagnata senza vapore dentro, (b) cavità rientrante con vapore intrappolato, (c) profilo esteso di un superficie rugosa.
Come illustrato in Fig. 2.11, una superficie più rugosa ha numerose cavità che servono ad intrappolare il vapore, fornendo un maggior numero di siti per la formazione e la crescita di bolle. Dunque i siti di nucleazione delle bolle di vapore sono maggiori su una superficie rugosa rispetto ad una liscia, anche se sperimentalmente è stato osservato come, rimanendo in condizioni di ebollizione, gli effetti della rugosità superficiale vadano a diminuire: ciò
sta ad indicare come i siti sempre più grandi di nucleazione non siano punti stabili per l’ “intrappolamento” del vapore. Una serie di interventi sulla superficie, tali da
incrementare il flusso dissipato in ebollizione nucleata sono stati classificati da Webb [26-27]. Essi sono fondamentalmente di due tipi (Fig.2.12):
- rivestimento della superficie con materiale poroso ottenuto per sinterizzazione, abrasione, spray di fiamme, deposizione elettrolitica o tramite l’uso di schiume; - interventi meccanici.
Queste tecniche passive per l’incremento dello scambio termico sono affiancate anche da tecniche di tipo attivo come la rotazione della superficie, la vibrazione della superficie e/o del fluido e campi elettrostatici. Esse sono state classificate da Bergles [28-29].
Fig.2.12. Tipiche strutture di superfici per aumentare il flusso dissipato in ebollizione nucleata; (a) rivestimento con particelle metalliche sinterizzate, (b) formazione di cavità a
2.8Correlazioni di scambio termico in pool boilng
1. Ebollizione in convezione naturale
In questa regione, che permane fino al punto A della curva in Fig.2.7, si fa generalmente uso delle equazioni della convezione naturale viste nei paragrafi precedenti, per il calcolo di q” e di h.
2. Ebollizione nucleata
Il regime di ebollizione a nuclei presenta il maggior interesse dal punto di vista applicativo e per tale ragione è stato maggiormente studiato rispetto agli altri regimi di ebollizione; in questo regime infatti si possono ottenere elevate efficienze di scambio termico con associate caratteristiche di stabilità. Numerose indagini teoriche e sperimentali sono state sviluppate sull’ebollizione a nuclei al fine di approfondire la conoscenza di base del fenomeno termico e di ottenere quindi indicazioni su possibili correlazioni tra le grandezze indipendenti influenzanti il processo. Due principali meccanismi sono stati individuati per la spiegazione degli elevati flussi termici che si ottengono:
i. micro convezione connessa con l’agitazione indotta dalla crescita e distacco delle bolle dalla superficie;
ii. evaporazione di un micro strato di liquido sottostante le bolle (teoria del micro strato evaporante).
Il primo meccanismo prevede che la crescita ed il distacco delle bolle di vapore dalla superficie riscaldata provochi nello strato limite surriscaldato un’azione di “pompaggio” che intensifica lo scambio termico. Infatti, in seguito al distacco della bolla dalla parete, una porzione di liquido surriscaldato è trascinata via e del liquido freddo la sostituisce dando origine ad una conduzione termica in transitorio sulla parete per ripristinare lo strato liquido surriscaldato. La teoria del micro strato evaporante assume che le bolle crescano su di un micro strato di liquido surriscaldato al di sotto di esse. Durante la crescita della bolla, dato che il film liquido cede energia, la temperatura di parete diminuisce. Dopo la fase di crescita lo strato liquido non cede più energia e la temperatura di parete aumenta nuovamente per riprendere il ciclo di nucleazione successivo. Da entrambi i modelli descritti sono state ricavate equazioni per la valutazione dei coefficienti di scambio termico; queste equazioni contengono tuttavia parametri di difficile determinazione quali ad esempio la distribuzione dei centri attivi di nucleazione, la frequenza di formazione delle bolle da ognuno di essi, ecc.. La fenomenologia di base della nucleazione è stata ampiamente studiata, tuttavia per la valutazione del flusso termico trasmesso nell’ebollizione ci si riferisce a correlazioni semiempiriche.
Yamagata et al. [22] furono i primi a correlare il flusso termico q” con il ∆Tsat ed il numero
di siti di nucleazione tramite l’equazione 2.30:
b a satn T C q"= ∆ (2.30) dove n rappresenta la densità di sito (cioè i siti attivi di nucleazione per unità di area) e gli esponenti valgono approssimativamente a = 1,2 e b=1/3. Sebbene C e n varino notevolmente in base alla combinazione liquido-superficie di contatto, è stato ricavato sperimentalmente che n∝∆Tsat5 o
6 sat
T
∆ . Dunque, in base alla 2.30, ne segue che q” è proporzionale a ∆Tsat3.
Nel 1952, Rohsenow [30] partì dall’ipotesi che il surriscaldamento di parete ∆Tsat
dipendesse da Pr e da un numero di Reynolds “bolle”, definito Reb=GbDb/µl, dove Gb
rappresenta la portata in massa di vapore per unità di superficie trasmettente, Db il
diametro della bolla e µl la viscosità dinamica del liquido. La portata Gb viene inoltre
assunta proporzionale al rapporto tra il flusso termico specifico, q”, e l’entalpia di vaporizzazione hfg, ed il diametro Db viene espresso mediante la relazione: Db
(
)
2 / 1 − ∝ g v lρ
ρ
σ
e dunque(
)
g h q v l l fg bρ
ρ
σ
µ
− = " Re .La formulazione finale della correlazione sviluppata da Rohsenow fu:
(
)
3 , , 2 / 1 Pr " ∆ − = n l fg f s sat l p v l fg l h C T C g h qσ
ρ
ρ
µ
(2.31) dove i pedici l e v si riferiscono rispettivamente alla fase liquido e vapore. La tensione superficiale σ[N/m] racchiude gli effetti delle proprietà del fluido sulla nascita delle bolle e sul loro sviluppo, Cp,l è il calore specifico a pressione costante del liquido [J/kgK], hfgrappresenta l’entalpia di vaporizzazione [J/kg], Prl il numero di Prandtl del liquido saturo,
ρla densità del fluido [kg/m3
], g l’accelerazione di gravità [m/s2] e µl la viscosità dinamica
del liquido saturo [Ns/m2]. Tutte le proprietà del liquido sono valutate alla temperatura di saturazione. I coefficienti Cs,f e l’esponente n dipendono dalla combinazione
superficie-fluido ed i loro valori sono riassunti in Tabella 2.3 [31], mentre i valori di Cs,f ed n per altre
Tabella 2.3
Valori di Cs,f ed n per varie combinazioni liquido-superficie
Combinazione liquido-superficie Cs,f n
Acqua -rame 0,013 1,0
Acqua- acciaio inossidabile
pulito meccanicamente 0,013 1,7 levigato e pulito 0,008 1,7 Acqua- ottone 0,006 1,0 Acqua- nichel 0,006 1,0 Acqua- platino 0,013 1,0 n-pentano- cromo 0,015 1,7 Isopropanolo-rame 0,0025 1,7 Benzene- cromo 0,101 1,7
Alcool etilico- cromo 0,0027 1,7
n-butanolo-rame 0,003 1,7
CCl4 - rame 0,013 1,7
I valori di Cs,f sono influenzati anche dall’angolo di contatto tra la bolla e la superficie
scaldante, che è una misura della bagnabilità della superficie da parte del fluido. La Fig. 2.13 mostra che l’angolo di contatto diminuisce al crescere della bagnabilità: una superficie completamente bagnata ha la minima area ricoperta di vapore, per un certo surriscaldamento, e quindi rappresenta la condizione più favorevole ad un’efficiente trasmissione del calore.
Fig.2.13: Influenza della bagnabilità di una superficie sull’angolo di contatto della bolla. In assenza di informazioni quantitative sull’influenza della bagnabilità e delle condizioni superficiali sulla costante Cs,f, il suo valore deve essere determinato empiricamente per
Raggruppando i termini ∆ fg sat l p h T C ,
in un nuovo numero adimensionale, il numero di
Jacob (Ja), si ricava che: q"∝Ja3Pr−3n. Dal punto di vista fisico il numero di Jacob rappresenta il rapporto tra i calori latenti assorbiti durante il cambiamento di fase liquido-vapore.
Riportando la 2.31 in termini di numeri adimensionali dunque si ha : Ja=Csf Re1b/3Prln. La correlazione di Rohsenow si applica solo per superficie pulite. L’errore che si commette usandola per stimare il flusso, può essere anche del ±100%. Tuttavia, essendo ∆Tsat ∝q"1/3
, l’errore si riduce ad un fattore 3 quando l’espressione si usa per la stima di ∆Tsat a partire
da q”. Inoltre, essendo q"∝h−fg2e considerando che hfg decresce notevolmente con
l’incremento della pressione di saturazione, il flusso termico in ebollizione nucleata incrementerà considerevolmente quando il liquido è pressurizzato.
3. Flusso critico in ebollizione nucleata
Esso è un punto di importanza cruciale nelle applicazioni ingegneristiche in quanto che lo scopo sarebbe quello di poter operare in prossimità di tale punto, per garantire i più alti h, senza però mai raggiungere il punto di burnout. Come già detto precedentemente lo studio dell’ebollizione a nuclei consente, in realtà, di individuare per lo meno due sottoregimi: nel primo, al quale corrispondono basse densità di flusso termico, le bolle si comportano come entità isolate e non interferiscono tra loro; al crescere del flusso termico, però, il processo di asportazione del vapore dalla superficie scaldante da intermittente diventa continuo finché, aumentando la frequenza di emissione delle bolle dalla superficie, le bolle isolate si riuniscono in colonne continue di vapore. Gli stadi della transizione da bolle isolate a colonne continue di vapore sono mostrati schematicamente in Fig.2.14 (a) e fotografati in Fig.2.14 (b) e (c). Durante la transizione dal regime delle bolle isolate a quello delle colonne di vapore, soltanto una piccola parte della superficie riscaldante è ricoperta di vapore, ma, al crescere del flusso termico, cresce il diametro della colonna e si formano ulteriori colonne. Aumentando la parte dell’area della sezione parallela alla superficie riscaldante occupata dal vapore, le colonne di vapore adiacenti ed il liquido in esse incluso cominciano ad interagire; infine si giunge ad un produzione di vapore tale che la minima distanza tra le colonne adiacenti di vapore determina elevate velocità relative tra il vapore che si allontana dalla superficie ed il liquido che scorre verso la stessa. La condizione di flusso termico massimo si realizza quando la velocità del liquido è tanto
grande rispetto a quella del vapore, che un suo ulteriore aumento determina l’allontanamento del liquido dalla superficie scaldante da parte delle colonne di vapore od il trascinamento del vapore verso la superficie scaldante da parte del liquido. E’ ovviamente impossibile che ciascuno dei due casi avvenga senza una diminuzione del flusso termico. Kutateladze [32], facendo uso dell’analisi dimensionale, e Zuber [33], attraverso un’analisi di stabilità idrodinamica, ottennero l’equazione 2.32:
Fig.2.14: Transizione dal regime delle bolle isolate a l regime delle colonne nell’ebollizione a nuclei; (a) Descrizione schematica della transizione, (b) Fotografia del
regime delle bolle isolate per acqua alla pressione atmosferica con flusso termico di
1,16·105 W/m2, (c) Fotografia del regime delle colonne per acqua alla pressione
atmosferica con un flusso termico di 3,6·105 W/m2.
(
)
1/4 1/2 2 " max 24 + − = l v l v v l v fg g h qρ
ρ
ρ
ρ
ρ
ρ
σ
ρ
π
(2.32)che, in prima approssimazione, è indipendente dalla superficie del materiale ed è solo debolmente dipendente dalla geometria. Sostituendo alla costante di Zuber π/24 (pari a 0,131) il valore ottenuto sperimentalmente di 0,149 [34] ed approssimando l’ultimo termine all’unità, l’equazione 2.32 diviene:
(
)
1/4 2 " max 0,149 − = v v l v fg g h qρ
ρ
ρ
σ
ρ
(2.33) In teoria, dal momento che questa espressione si applica per superfici riscaldate di dimensioni infinite, non compare nell’espressione 2.33 una lunghezza caratteristica; in pratica, tuttavia, l’espressione è applicabile se la lunghezza caratteristica del problema in esame è comparabile con il parametro del diametro medio di bolla, Db. Se il rapporto tra lalunghezza caratteristica e Db, denominato numero di Bond, è minore di 3, deve essere
applicato all’equazione 2.33, un fattore correttivo (Il numero di Bond rappresenta il rapporto tra le forze gravitazionali e la tensione superficiale ed è pari a
(
)
σ
ρ
ρ
2 L g Bo= l − v). Lienhard e Dhir [35] hanno ricavato tali fattori per differenti geometrie, quali lastre, cilindri, sfere e nastri orientati orizzontalmente e verticalmente. In generale la costante può variare tra 0,13 e 0,18. E’ importante notare come il flusso critico dipenda fortemente dalla pressione, specie perché da essa dipendono le variazioni della densità di vapore ed anche della temperatura di ebollizione, dalla quale a sua volta dipendono il calore latente di vaporizzazione e la tensione superficiale. Cichelli e Bonila [36] hanno dimostrato sperimentalmente come il picco del flusso termico incrementi con la pressione fino ad un terzo della pressione critica e come, dopo tale punto, il flusso tenda a zero alla pressione critica (Fig.2.15).
Fig.2.15: Massimo flusso termico nell’ebollizione a nuclei per alcune pressioni
(ps/pc è il rapporto tra la pressione del sistema e la pressione critica) [36]
Per ciascun liquido è stato ricavato un valore della pressione che determina il flusso termico massimo, in particolare per l’acqua, la pressione ottimale è risultata di 101,3 bar ed il massimo flusso termico pari a 3,72·106 W/m2.
Anche il campo gravitazionale può influenzare il flusso termico massimo. In particolare una diminuzione dello stesso determina una diminuzione del flusso massimo. La diminuzione di q”max è provocata anche dall’aggiunta in soluzione all’acqua di un
tensioattivo, così come i gas non condensabili e le superfici non bagnabili riducono il massimo flusso termico per una certa temperatura della massa fluida. D’altra parte, la presenza di certi additivi, così come un campo ultrasonico o elettrostatico, può accrescere il massimo flusso termico ottenibile nell’ebollizione a nuclei.
4. Minimo flusso termico
La zona di transizione dalla regione di ebollizione nucleata a film a dire il vero è di scarso interesse nella pratica, in quanto che si ottiene solo controllando la temperatura del riscaldatore, come detto più volte. Le condizioni di questa zona sono caratterizzate da un periodico ed instabile contatto tra il liquido e la superficie riscaldata. Il limite superiore di questa zona riveste invece un certo interesse in quanto corrisponde alla formazione del film stabile di vapore, a cui corrisponde un certo valore di flusso minimo, q”min. Se il flusso
termico va al di sotto di tale punto, il film collassa, causando il raffreddamento della superficie e la ristabilizzazione del regime nucleato. Zuber [33] usò la teoria della stabilità per derivare la seguente espressione per il punto di minimo flusso termico, per una piastra orizzontale larga:
(
)
(
)
4 / 1 2 " min + − = v l v l fg v g h C qρ
ρ
ρ
ρ
σ
ρ
(2.34) La costante C è stata ricavata sperimentale da Berenson [37]. Questo risultato è accurato circa al 50% per la maggior parte di fluidi a basse pressioni, ma fornisce stime poco accurate ad alte pressioni [38]. Un risultato simile è stato ottenuto per cilindri orizzontali [39].5. Ebollizione a film
Aumentando la temperatura oltre il punto di Leidenfrost, il film di vapore stabile ricopre la superficie e non si ha più il contatto tra la fase liquida e la superficie. Essendo tali condizioni molto simili dal punto di vista fenomenologico a quelle della condensazione laminare a film, è ormai consuetudine fare uso dei risultati ottenuti dalla teoria della condensazione. Uno di questi è rappresentato dall’equazione 2.35, che per cilindri o sfere di diametro D, è:
(
)
(
)
4 / 1 3 ' − − = = sat s v v fg v l v conv D T T k D h g C k D h Nuν
ρ
ρ
(2.35)Il valore della costante C è pari a 0,62 per cilindri orizzontali [40] e 0,67 per sfere [34] ed il calore latente hfg =hfg + cp,v
(
Ts −Tsat)
'
4 ,
0 . Le proprietà del vapore sono valutate alla temperatura di film pari a: Tf =
(
Ts +Tsat)
/2.Ad elevate temperature della superficie (Ts > 300°C), lo scambio termico per
irraggiamento attraverso il film di vapore diventa significativo. Dal momento che questo tende ad incrementare lo spessore del film, si può assumere che gli effetti dovuti alla convezione e quelli dovuti all’irraggiamento si possono sommare. Bromley [40] investigò il regime di ebollizione a film tra la superficie esterna di tubi orizzontali e suggerì di calcolare il coefficiente di scambio globale da un’equazione in forma trascendente:
3 / 1 3 / 4 3 / 4 h h h h = conv + rad (2.36) Se hrad <hconv, si può ricondurre la 2.36 ad una formulazione più semplice:
rad conv h h h 4 3 + = (2.37) Il coefficiente hrad si può approssimare come:
(
)
sat s sat s rad T T T T h − − =εσ
4 4 (2.38)dove ε è l’emissività del solido e σ la costante di Stefan- Boltzmann.
E’ da notare che l’analogia tra l’ebollizione a film e la condensazione a film non funziona per piccole superfici con grande curvatura, a causa della disparità tra gli spessori di vapore e liquido nei due processi. Quest’analogia perde anche validità per superfici verticali, sebbene siano stati ottenuti predizioni soddisfacenti in alcune limitate condizioni.
2.9Considerazioni generali sull’equilibrio di una bolla
Le condizioni per attivare la nucleazione sono chiaramente di non equilibrio, tuttavia è possibile ottenere utili informazioni sul fenomeno in base a considerazioni di equilibrio termodinamico riguardanti un nucleo di vapore immerso in un liquido a temperatura uniforme [31]. Le condizioni di equilibrio termodinamico comportano, come è noto, l’equilibrio meccanico, termico e chimico all’interfaccia vapore – liquido. Un’interfaccia può in generale essere considerata come una membrana uniformemente tesa di spessore nullo: la tensione superficiale σ tra le due fasi è la forza per unità di lunghezza che tende tale membrana. Nel caso in cui la superficie di separazione tra le fasi sia sferica, come si può ritenere per bolle di vapore sufficientemente piccole, le due fasi a causa della tensione superficiale sono a pressioni diverse, legate dalla relazione:
r p
pv − l = 2σ (2.39) Se infatti si considera una bolla di vapore di raggio r, in una fase liquida continua, le forze agenti all’interfaccia vapore-liquido sono costituite dalla pressione di vapore pv all’interno
della bolla, dalla pressione del liquido agente all’esterno pl e dalla tensione superficiale σ.
L’equilibrio meccanico tra le suddette forze conduce alla seguente relazione: r p p r v l πσ π 2( − )=2 (2.40) da cui si ottiene la 2.39.
L’equilibrio termodinamico comporta inoltre che la temperatura delle due fasi sia la stessa: Tl=Tv=T.
Per esprimere infine l’equilibrio tra le fasi, è necessario ricordare che, secondo la termodinamica classica, devono essere uguali i relativi potenziali di Gibbs. Tale potenziale è definito da: µ =i –Ts, essendo i ed s l’entalpia e l’entropia specifiche e T la temperatura assoluta. In forma differenziale, introducendo il volume specifico v si ricava dµ =vdp – sdT, ed a temperatura costante diviene dµ =vdp. Tenendo presente che il differenziale dµ esprime una piccola perturbazione attorno al punto di equilibrio, integrando la precedente si possono ottenere gli scostamenti rispetto alle condizioni di saturazione delle due fasi.